–Э–∞ —Б–µ–≥–Њ–і–љ—П –љ–∞–Ї–Њ–њ–ї–µ–љ –±–Њ–≥–∞—В—Л–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ —Г –і–µ—В–µ–є –≤—Б–µ—Е –≤–Њ–Ј—А–∞—Б—В–Њ–≤, –і–Њ–Ї–∞–Ј–∞–љ–∞ –Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –ї–µ—З–µ–љ–Є–Є —Б–ї–µ–і—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є: –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –ї–∞–Ї—В–Њ–Ј—Л [11], –∞–љ—В–Є–±–Є–Њ—В–Є–Ї––∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П –і–Є–∞—А–µ—П [12,13,14], –∞—В–Њ–њ–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [15,16], —А–Њ—В–∞–≤–Є—А—Г—Б–љ—Л–є –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Є—В —Г –і–µ—В–µ–є [17], –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є —П–Ј–≤–µ–љ–љ—Л–є –Ї–Њ–ї–Є—В –Є –±–Њ–ї–µ–Ј–љ—М –Ъ—А–Њ–љ–∞. –°–Њ–≤—Б–µ–Љ –љ–µ–і–∞–≤–љ–Њ —Б—В–∞–ї–Є –њ–Њ—П–≤–ї—П—В—М—Б—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Л–µ —А–∞–±–Њ—В—Л –Њ–± –Є—Е –±–ї–∞–≥–Њ—В–≤–Њ—А–љ–Њ–Љ –≤–ї–Є—П–љ–Є–Є –љ–∞ –і–µ—В–µ–є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ–µ—А–≤–Њ–≥–Њ –њ–Њ–ї—Г–≥–Њ–і–Є—П –ґ–Є–Ј–љ–Є. –Ю—Б—В–∞–љ–Њ–≤–Є–Љ—Б—П –љ–∞ –љ–Є—Е –њ–Њ–і—А–Њ–±–љ–µ–µ.
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Ї–Є—И–µ—З–љ–Є–Ї —З–µ–ї–Њ–≤–µ–Ї–∞ – —Н—В–Њ —Б–≤–Њ–µ–Њ–±—А–∞–Ј–љ–Њ–µ –≤–Љ–µ—Б—В–Є–ї–Є—Й–µ –Њ–≥—А–Њ–Љ–љ–Њ–≥–Њ —З–Є—Б–ї–∞ –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Є –њ—А–Њ—Б–≤–µ—В–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л, —З—В–Њ —Б–Њ–Ј–і–∞–µ—В –њ—А–µ–і–њ–Њ—Б—Л–ї–Ї–Є –і–ї—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –Є–Љ–Љ—Г–љ–Є—В–µ—В —А–µ–±–µ–љ–Ї–∞. –Я–Њ—Б—В–љ–∞—В–∞–ї—М–љ–∞—П –Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є—П –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Г—Б–ї–Њ–≤–Є–є –њ—А–Њ—В–µ–Ї–∞–љ–Є—П —А–Њ–і–Њ–≤, —Г—А–Њ–≤–љ—П –≥–Є–≥–Є–µ–љ—Л, –Љ–∞—В–µ—А–Є–љ—Б–Ї–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Є —В–Є–њ–∞ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є—П: –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–µ, —Б–Љ–µ—И–∞–љ–љ–Њ–µ –Є–ї–Є –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–µ. –Э–∞–Є–±–Њ–ї—М—И–µ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –њ–Њ —Б–≤–Њ–µ–Љ—Г —Б–Њ—Б—В–∞–≤—Г –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–∞ —А–µ–±–µ–љ–Ї–∞ –њ—А–µ—В–µ—А–њ–µ–≤–∞–µ—В –≤ —А–∞–љ–љ–µ–Љ –≤–Њ–Ј—А–∞—Б—В–µ —Б 2 –Ї—А–Є—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ–µ—А–Є–Њ–і–∞–Љ–Є: –њ—А–Є —А–Њ–ґ–і–µ–љ–Є–Є –Є –≤ –њ–µ—А–Є–Њ–і –≤–≤–µ–і–µ–љ–Є—П –њ—А–Є–Ї–Њ—А–Љ–∞, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ—Л–Љ–Є –Є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є [18]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є –љ–∞ –≥–љ–Њ—В–Њ–±–Є–Њ–љ—В–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–µ–µ –≤–ї–Є—П–љ–Є–µ –Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –Љ–µ—Б—В–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є —Г—А–Њ–≤–µ–љ—М —Б–Є—Б—В–µ–Љ–љ—Л—Е –∞–љ—В–Є—В–µ–ї, —З—В–Њ –Є –њ–Њ–і–≤–µ–ї–Њ –Ї –Є–і–µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е —И—В–∞–Љ–Љ–Њ–≤ –±–∞–Ї—В–µ—А–Є–є –і–ї—П –ї–µ—З–µ–љ–Є—П –Є–Љ–Љ—Г–љ–Њ––Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –њ—Г—В–µ–Љ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –±–∞–ї–∞–љ—Б–∞ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л. –Ґ–∞–Ї, –љ–∞–њ—А–Є–Љ–µ—А, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є M. Rinne et al. (2005, –§–Є–љ–ї—П–љ–і–Є—П) –ґ–µ–љ—Й–Є–љ—Л –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ 4 –љ–µ–і. –њ–µ—А–µ–і —А–Њ–і–∞–Љ–Є –Є –Ј–∞—В–µ–Љ 96 –Ј–і–Њ—А–Њ–≤—Л—Е –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. (–љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –≤–Є–і–∞ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є—П) –њ–Њ–ї—Г—З–∞–ї–Є –њ—А–Њ–±–Є–Њ—В–Є–Ї –љ–∞ –Њ—Б–љ–Њ–≤–µ Lactobacillus rhamnosus –≤ –і–Њ–Ј–µ 1•106 –Ъ–Ю–Х –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ––њ—А–µ–њ–∞—А–∞—В [19]. –Т 3, 6 –Є 12 –Љ–µ—Б. —Г –љ–Є—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Љ–Є–Ї—А–Њ–±–Є–Њ—Ж–µ–љ–Њ–Ј –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞. –Ф–µ—В–Є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –±—Л–ї–Є —Б—А–∞–≤–љ–Є–Љ—Л –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ —Б—А–Њ–Ї–∞ —А–Њ–ґ–і–µ–љ–Є—П (39 –љ–µ–і. –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –Є 40 –љ–µ–і. – –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П) –Є –≤–µ—Б—Г —В–µ–ї–∞ –њ—А–Є —А–Њ–ґ–і–µ–љ–Є–Є (3577 –≥ –Є 3666 –≥ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –°—А–µ–і–љ—П—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –≥—А—Г–і–љ–Њ–≥–Њ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є—П –±—Л–ї–∞ 2,6 –Љ–µ—Б., —Б–Љ–µ—И–∞–љ–љ–Њ–≥–Њ – 6,9 –Љ–µ—Б. –Т 6 –Љ–µ—Б. —Г 46 –Є–Ј 96 –і–µ—В–µ–є (48%) –≤ –њ–Є—В–∞–љ–Є–Є –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Њ –ґ–µ–љ—Б–Ї–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ, —Г 43 –і–µ—В–µ–є (45%) – –∞–і–∞–њ—В–Є—А–Њ–≤–∞–љ–љ–∞—П —Б–Љ–µ—Б—М –љ–∞ –Њ—Б–љ–Њ–≤–µ –Ї–Њ—А–Њ–≤—М–µ–≥–Њ –Љ–Њ–ї–Њ–Ї–∞, 4 (4%) –Љ–ї–∞–і–µ–љ—Ж–∞ —Г–њ–Њ—В—А–µ–±–ї—П–ї–Є —З–∞—Б—В–Є—З–љ—Л–є –±–µ–ї–Ї–Њ–≤—Л–є –≥–Є–і—А–Њ–ї–Є–Ј–∞—В, 3 (3%) – –њ–Њ–ї–љ—Л–є –±–µ–ї–Ї–Њ–≤—Л–є –≥–Є–і—А–Њ–ї–Є–Ј–∞—В. –Я—А–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–Њ—Б—В–∞–≤–∞ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –Њ–±—Й–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Д–µ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї–Њ—Б—М —Г –і–µ—В–µ–є —Б 3 –і–Њ 12 –Љ–µ—Б. (—А<0,001) –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е. –Т –≤–Њ–Ј—А–∞—Б—В–µ –і–Њ 3 –Љ–µ—Б. –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ –≤ –≥—А—Г–њ–њ–µ –і–µ—В–µ–є, –Ї–Њ—А–Љ–Є–≤—И–Є—Е—Б—П –≥—А—Г–і—М—О, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–µ–Љ–Є, –Ї—В–Њ –љ–µ –њ–Њ–ї—Г—З–∞–ї –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ – 1,8•109 vs 4,4•108 –Ъ–Ю–Х/–≥ (—А<0,001). –Ґ–∞–Ї–Њ–µ –ґ–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є (—А=0,1) –Є –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є (—А<0,001) –Є–Љ–µ–ї–Є –і–µ—В–Є –љ–∞ –≥—А—Г–і–љ–Њ–Љ –Є–ї–Є —Б–Љ–µ—И–∞–љ–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є –≤–њ–ї–Њ—В—М –і–Њ 6 –Љ–µ—Б. –Т 12 –Љ–µ—Б. —А–∞–Ј–ї–Є—З–Є–є —Г–ґ–µ –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М. –Р–≤—В–Њ—А–∞–Љ–Є –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ —Б—Г–Љ–Љ–∞—А–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –і–≤—Г—Е —Д–∞–Ї—В–Њ—А–Њ–≤ (–њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–∞ –Є –≥—А—Г–і–љ–Њ–≥–Њ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є—П) –љ–∞ —Г—А–Њ–≤–µ–љ—М –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–Њ–≤ (Ig) –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є. –Т –≤–Њ–Ј—А–∞—Б—В–µ 3 –Љ–µ—Б. –Њ–±—Й–µ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ IgG –±—Л–ї–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ —Г –Љ–ї–∞–і–µ–љ—Ж–µ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ –Є –њ—А–Њ–±–Є–Њ—В–Є–Ї, –Є —Б–Њ—Б—В–∞–≤–Є–ї–Њ 1210 –Љ–Ї–≥/–Љ–ї (942–1553 –Љ–Ї–≥/–Љ–ї) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і–µ—В—М–Љ–Є –љ–∞ –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є –њ–ї–∞—Ж–µ–±–Њ – 1196 –Љ–Ї–≥/–Љ–ї (871–1643 –Љ–Ї–≥/–Љ–ї) (—А=0,05). –Т 12 –Љ–µ—Б. –Њ–±—Й–Є–µ —Г—А–Њ–≤–љ–Є IgM, IgA, IgG –±—Л–ї–Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ–Є —Г —В–µ—Е –Љ–ї–∞–і–µ–љ—Ж–µ–≤, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –љ–∞ –≥—А—Г–і–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є –±–Њ–ї–µ–µ 3 –Љ–µ—Б. –Є –њ–Њ–ї—Г—З–∞–ї–Є –њ—А–Њ–±–Є–Њ—В–Є–Ї, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–µ–Љ–Є, –Ї—В–Њ –Ї–Њ—А–Љ–Є–ї—Б—П –≥—А—Г–і—М—О –Є –њ–Њ–ї—Г—З–∞–ї –њ–ї–∞—Ж–µ–±–Њ (—А=0,005, —А=0,03, —А=0,04 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –∞–≤—В–Њ—А—Л —Б–і–µ–ї–∞–ї–Є –≤—Л–≤–Њ–і, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ –і–Є–µ—В–µ –Љ–∞—В–µ—А–Є –њ–µ—А–µ–і —А–Њ–і–Њ—А–∞–Ј—А–µ—И–µ–љ–Є–µ–Љ –Є —Г –Љ–ї–∞–і–µ–љ—Ж–µ–≤ –љ–∞ –≥—А—Г–і–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ –њ—А–Њ—Ж–µ—Б—Б —Б–Њ–Ј—А–µ–≤–∞–љ–Є—П –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞.
–Ю–±—Й–µ–Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–µ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і–µ—В—М–Љ–Є, –њ–Њ–ї—Г—З–∞—О—Й–Є–Љ–Є –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ—Л–µ —Б–Љ–µ—Б–Є. –≠—В–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –Ј–∞—Й–Є—В—Л –Њ—В –Є–љ—Д–µ–Ї—Ж–Є–Є. –Т –Ї–∞—З–µ—Б—В–≤–µ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ —Н—В–Њ–≥–Њ –Љ–Њ–ґ–љ–Њ –њ—А–Є–≤–µ—Б—В–Є –і–∞–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –≤ 2005 –≥. –≤ –Ш–Ј—А–∞–Є–ї–µ [20]. 201 –Ј–і–Њ—А–Њ–≤—Л–є —А–µ–±–µ–љ–Њ–Ї –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 4 –і–Њ 10 –Љ–µ—Б. –њ–Њ–ї—Г—З–∞–ї–Є —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л: –≥—А—Г–њ–њ–∞ 1–—П – –Љ–Њ–ї–Њ—З–љ—Г—О —Б–Љ–µ—Б—М —Б Bifidobacterium lactis (73 —А–µ–±–µ–љ–Ї–∞), 2–—П –≥—А—Г–њ–њ–∞ – –Љ–Њ–ї–Њ—З–љ—Г—О —Б–Љ–µ—Б—М —Б Lactobacillus reuteri (68 —З–µ–ї.), 3–—П –≥—А—Г–њ–њ–∞ (–≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П) – –Љ–Њ–ї–Њ—З–љ—Г—О —Б–Љ–µ—Б—М –±–µ–Ј –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ (60 —З–µ–ї.). –Ъ–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ —Б–Љ–µ—Б—П—Е —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 1•107 –Ъ–Ю–Х/–Љ–ї. –£ –і–µ—В–µ–є —Д–Є–Ї—Б–Є—А–Њ–≤–∞–ї–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б–ї—Г—З–∞–µ–≤ –Є —З–Є—Б–ї–Њ –і–љ–µ–є —Б —В–µ–Љ–њ–µ—А–∞—В—Г—А–Њ–є —В–µ–ї–∞ –≤—Л—И–µ 38°–°, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–Є–∞—А–µ–Є –Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Г –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Љ–Њ–ї–Њ—З–љ—Г—О —Б–Љ–µ—Б—М –±–µ–Ј –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤, —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Њ—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї—М—И–µ–µ —З–Є—Б–ї–Њ —Н–њ–Є–Ј–Њ–і–Њ–≤ –ї–Є—Е–Њ—А–∞–і–Ї–Є –љ–∞ –Њ–і–љ–Њ–≥–Њ —Г—З–∞—Б—В–љ–Є–Ї–∞ (–≤ —Б—А–µ–і–љ–µ–Љ 0,41 [95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї 0,28–0,54]) –Є –і–Є–∞—А–µ–Є (0,31 [0,22–0,40]) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–∞–Љ–Є, –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–µ–Љ—Л–Љ–Є —Б–Љ–µ—Б—П–Љ–Є —Б –њ—А–Њ–±–Є–Њ—В–Є–Ї–∞–Љ–Є: B. Lactis (0,27 [0,17–0,37] –Є 0,13 [0,05–0,21]) –Є L. reuteri (0,11 [0,04–0,18] –Є 0,02 [0,01–0,05]). –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–Є–∞—А–µ–Є —В–∞–Ї–ґ–µ –±—Л–ї–∞ –±–Њ–ї—М—И–µ –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П – 0,59, 0,37 –Є 0,15 –і–љ—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –≥—А—Г–њ–њ —Б –њ—А–Њ–±–Є–Њ—В–Є–Ї–∞–Љ–Є –Љ–µ–ґ–і—Г —Б–Њ–±–Њ–є –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ —Г –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б–Љ–µ—Б—М —Б L. reuteri, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–Є—Е–Њ—А–∞–і–Ї–Є (0,17), —З–Є—Б–ї–Њ –Њ–±—А–∞—Й–µ–љ–Є–є –Ї –≤—А–∞—З—Г (0,23), –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Њ—В—Б—Г—В—Б—В–≤–Є—П –≤ —П—Б–ї—П—Е (0,14) –Є —З–∞—Б—В–Њ—В–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є (0,06) –±—Л–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ B. Lactis (0,86, 0,51, 0,41, 0,21, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) –Є –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П (0,83, 0,55, 0,43, 0,19). –Ф–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —П–≤–Є–ї–Њ—Б—М –њ–µ—А–≤—Л–Љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ–і—Г–Ї—В–Њ–≤ —Б —А–∞–Ј–љ—Л–Љ–Є –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–Љ —И—В–∞–Љ–Љ–∞–Љ–Є –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б—А–µ–і–Є –і–µ—В–µ–є 1––≥–Њ –≥–Њ–і–∞ –ґ–Є–Ј–љ–Є. –Я—А–Є —Н—В–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ L. reuteri, –њ–Њ –і–∞–љ–љ—Л–Љ –∞–≤—В–Њ—А–Њ–≤, –±—Л–ї–Њ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ.
–Т –µ—Й–µ –Њ–і–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г—З–µ–љ—Л–µ –Є–Ј –Ґ—Г—А–Є–љ—Б–Ї–Њ–≥–Њ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–∞ –њ—Л—В–∞–ї–Є—Б—М —Б–≤—П–Ј–∞—В—М —З–∞—Б—В–Њ—В—Г –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ї–Є—И–µ—З–љ—Л—Е –Ї–Њ–ї–Є–Ї —Г –Љ–ї–∞–і–µ–љ—Ж–µ–≤ —Б —Б–Њ—Б—В–∞–≤–Њ–Љ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Є –Є–Ј—Г—З–Є—В—М —А–Њ–ї—М Lactobacillus reuteri –≤ —В–µ—А–∞–њ–Є–Є –і–∞–љ–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —Г –љ–Њ–≤–Њ—А–Њ–ґ–і–µ–љ–љ—Л—Е [21]. –Ф–Њ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П —Н—В–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ—А–Є–љ–∞–і–ї–µ–ґ–∞–ї –і–Є—Ж–Є–Ї–ї–Њ–≤–µ—А–Є–љ—Г, –∞ —В–∞–Ї–ґ–µ —Б–Є–Љ–µ—В–Є–Ї–Њ–љ—Г. F. Savino —Б –Ї–Њ–ї–ї–µ–≥–∞–Љ–Є —Г—Б—В–∞–љ–Њ–≤–Є–ї–Є, —З—В–Њ –≤ –Ї–Є—И–µ—З–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–µ —Г 83 –і–µ—В–µ–є –љ–∞ –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є, —Б—В—А–∞–і–∞—О—Й–Є—Е –Ї–Њ–ї–Є–Ї–∞–Љ–Є, –≤ –≥–Њ—А–∞–Ј–і–Њ –Љ–µ–љ—М—И–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ —Б–Њ–і–µ—А–ґ–∞—В—Б—П –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–Є –Є –±–Њ–ї–µ–µ —З–∞—Б—В–Њ – –∞–љ–∞—Н—А–Њ–±–љ—Л–µ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ—Л. –Т —В–µ—З–µ–љ–Є–µ 28 –і–љ–µ–є 41 —А–µ–±–µ–љ–Њ–Ї –њ–Њ–ї—Г—З–∞–ї –њ—А–Њ–±–Є–Њ—В–Є–Ї L. reuteri –≤ –і–Њ–Ј–µ 108 –Ъ–Ю–Х (5 –Ї–∞–њ–µ–ї—М –Љ–∞—Б–ї—П–љ–Њ–є —Б—Г—Б–њ–µ–љ–Ј–Є–Є 1 —А–∞–Ј/—Б—Г—В.). –Ф–µ—В–Є –Є–Ј –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П (42 —А–µ–±–µ–љ–Ї–∞) –њ–Њ–ї—Г—З–∞–ї–Є —Б—Г—Б–њ–µ–љ–Ј–Є—О —Б–Є–Љ–µ—В–Є–Ї–Њ–љ–∞ –њ–Њ 60 –Љ–≥/—Б—Г—В. –І–µ—А–µ–Ј –Љ–µ—Б—П—Ж —Б–Є–Љ–њ—В–Њ–Љ—Л –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ї–Њ–ї–Є–Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–Ј–Є–ї–Є—Б—М —Г 95% –Љ–ї–∞–і–µ–љ—Ж–µ–≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ—Л –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є —Б—А–∞–≤–љ–µ–љ–Є—П, –≥–і–µ —В–Њ–ї—М–Ї–Њ 7% –і–µ—В–µ–є –Њ—В–≤–µ—В–Є–ї–Є –љ–∞ —В–µ—А–∞–њ–Є—О —Б–Є–Љ–µ—В–Є–Ї–Њ–љ–Њ–Љ (p<0,001). –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ—В—Б–Ї–Њ–≥–Њ –њ–ї–∞—З–∞ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –Є—Б—Е–Њ–і–љ–Њ –±—Л–ї–∞ 197 –Љ–Є–љ./—Б—Г—В., –∞ —Г–ґ–µ —З–µ—А–µ–Ј 7 –і–љ–µ–є –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –і–Њ 159 –Љ–Є–љ./—Б—Г—В., –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П – —В–Њ–ї—М–Ї–Њ –і–Њ 177 –Љ–Є–љ./—Б—Г—В. (—А<0,005). –С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О L. reuteri –і–µ–ї–∞–µ—В —Н—В–Њ—В —Б–њ–Њ—Б–Њ–± –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –≤—Б–µ–Љ –і—А—Г–≥–Є–Љ –Љ–µ—В–Њ–і–∞–Љ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Ї–Њ–ї–Є–Ї —Г –Љ–ї–∞–і–µ–љ—Ж–µ–≤ –љ–∞ –≥—А—Г–і–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —И–Є—А–Њ–Ї–Њ –њ—А–Њ–≤–Њ–і—П—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –≤–ї–Є—П–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е –±–∞–Ї—В–µ—А–Є–є –љ–∞ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –њ—А–Є –Њ–ґ–Є—А–µ–љ–Є–Є. –Т—Б–µ —З–∞—Й–µ –њ—А–Њ–±–Є–Њ—В–Є–Ї–Є –њ—А–Є–Љ–µ–љ—П—О—В –і–ї—П –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–∞ –њ—А–Њ–і—Г–Ї—В–Њ–≤ –њ–Є—В–∞–љ–Є—П, –њ–∞—А–∞—Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ —Б —Ж–µ–ї—М—О –Ї–Њ–љ—В—А–Њ–ї—П –њ—А–Є–±–∞–≤–Ї–Є –≤–µ—Б–∞, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ–ґ–Є—А–µ–љ–Є—П, —Г–Љ–µ–љ—М—И–µ–љ–Є—П –њ–Є—Й–µ–≤–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є, —Б–≤—П–Ј—Л–≤–∞–љ–Є—П –Є –≤—Л–≤–µ–і–µ–љ–Є—П –Є–Ј–±—Л—В–Ї–Њ–≤ –ґ–Є—А–Њ–≤, —Г–ї—Г—З—И–µ–љ–Є—П —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞, —Б–љ–Є–ґ–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –Ю–ґ–Є—А–µ–љ–Є–µ – –Њ–і–љ–Њ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є, –Ї–Њ—В–Њ—А–Њ–≥–Њ –Љ–Њ–ґ–љ–Њ –Є–Ј–±–µ–ґ–∞—В—М –њ—Г—В–µ–Љ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –љ–∞–≤—Л–Ї–Њ–≤ –њ—А–∞–≤–Є–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П. –Э–µ–Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–µ —И—В–∞–Љ–Љ—Л —Б–њ–Њ—Б–Њ–±–љ—Л –Њ–Ї–∞–Ј—Л–≤–∞—В—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–∞ —Г—А–Њ–≤–µ–љ—М —Е–Њ–ї–µ—Б—В–µ—А–Њ–ї–∞ –Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Н—В–Њ–≥–Њ –њ—А–Є —А–µ–≥—Г–ї—П—А–љ–Њ–Љ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–Є –≤ –њ–Є—Й—Г –Љ–Њ–ї–Њ—З–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤, —Д–µ—А–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е, –љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Њ—В–µ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–є –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–µ–є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Б–љ–Є–ґ–µ–љ–Є—О –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П. –®–Є—А–Њ–Ї–Њ –Є–Ј–≤–µ—Б—В–љ—Л–є —И—В–∞–Љ–Љ Lactobacillus rhamnosus GG –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞ –Є–Љ–Љ—Г–љ–љ—Г—О —Б–Є—Б—В–µ–Љ—Г, –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –∞–њ–Њ–њ—В–Њ–Ј, –Ї–ї–µ—В–Њ—З–љ—Л–є —А–Њ—Б—В –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї—Г, –Ї–ї–µ—В–Њ—З–љ—Г—О –∞–і–≥–µ–Ј–Є—О –Є —В—А–∞–љ—Б–Ї—А–Є–њ—Ж–Є—О –Ј–∞ —Б—З–µ—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є –≥–µ–љ–Њ–≤ –≤ —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–µ. –Ю–і–љ–∞–Ї–Њ –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Г—А–Њ–≤–µ–љ—М —Н–љ–µ—А–≥–Є–Є, –ґ–Є—А–Њ–≤, –≥–ї—О–Ї–Њ–Ј—Л –Є–ї–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Є–љ—Б—Г–ї–Є–љ–∞ –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ [22]. –Ш, –љ–∞–њ—А–Њ—В–Є–≤, –њ–Њ–і–Њ–±–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±—Л–ї–∞ –Њ—В–Љ–µ—З–µ–љ–∞ —Г –і—А—Г–≥–Њ–є –≥—А—Г–њ–њ—Л —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ –≤—Л–і–µ–ї–µ–љ–љ—Л—Е –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е —И—В–∞–Љ–Љ–Њ–≤ –Є–Ј –≥—А—Г–њ–њ—Л –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є – Lactobacillus acidophilus, Lactobacillus casei –Є Bifidobacterium lactis, –љ–Њ —Б–∞–Љ—Л–Љ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П —И—В–∞–Љ–Љ Lactobacillus casei F19 (LMG P–17806), –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤ –њ—А–Њ–і—Г–Ї—В–∞—Е –њ–Є—В–∞–љ–Є—П –Њ—Д–Є—Ж–Є–∞–ї—М–љ–Њ –Ј–∞–њ–∞—В–µ–љ—В–Њ–≤–∞–љ–Њ (WO 99/29833). –Т—Б–µ 3 —И—В–∞–Љ–Љ–∞ —Г—Б–њ–µ—И–љ–Њ –њ—А–Є–ґ–Є–≤–∞—О—В—Б—П –≤ –њ—А–Њ–і—Г–Ї—В–∞—Е –Є —Г–ґ–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є —Е–Њ—А–Њ—И–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є—О –Ї–Є—Б–ї–Њ—В–љ–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –≤ –ґ–µ–ї—Г–і–Ї–µ –Є –њ–∞—Б—Б–∞–ґ—Г –њ–Њ –Ї–Є—И–µ—З–љ–Є–Ї—Г. –Ю–і–љ–∞–Ї–Њ –Є–Љ–µ–љ–љ–Њ –µ–ґ–µ–і–љ–µ–≤–љ–Њ–µ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—В–Њ–≤, –Њ–±–Њ–≥–∞—Й–µ–љ–љ—Л—Е –і–∞–љ–љ—Л–Љ–Є —И—В–∞–Љ–Љ–∞–Љ–Є, –њ–Њ–Љ–Њ–≥–∞–µ—В –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –≤–µ—Б, –±–Њ—А–Њ—В—М—Б—П —Б –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Є –Њ–ґ–Є—А–µ–љ–Є–µ–Љ, –њ–Њ–≤—Л—И–∞–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –Є–љ—Б—Г–ї–Є–љ—Г. –Ф–∞–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –±—Л–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ—Л –≤ —Ж–µ–ї–Њ–Љ —А—П–і–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є [23–25]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, in vitro –±—Л–ї –і–Њ–Ї–∞–Ј–∞–љ –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В —И—В–∞–Љ–Љ–∞ Lactobacillus casei F 19 [26].
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ –≤–ї–Є—П–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–∞ –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ –њ–Њ–ї—Г—З–Є–ї–Є —Б–≤–Њ–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –і–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤–∞–Ї—Ж–Є–љ–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є GG –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Њ –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В—М –Њ—А–∞–ї—М–љ–Њ–є —А–Њ—В–∞–≤–Є—А—Г—Б–љ–Њ–є –≤–∞–Ї—Ж–Є–љ—Л [27]. –°–Њ–≤–Љ–µ—Б—В–љ—Л–є –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ –і–∞–љ–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є –Є —Б–∞–ї—М–Љ–Њ–љ–µ–ї–ї–µ–Ј–љ–Њ–є –≤–∞–Ї—Ж–Є–љ—Л —Б–Њ–Ј–і–∞–≤–∞–ї–Є —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Г—А–Њ–≤–љ—П —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–≥–Њ IgA –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ [28]. –Я–Њ–і–Њ–±–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –љ–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є—Е —А–µ–∞–Ї—Ж–Є—О –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –±—Л–ї–Њ –Њ–њ–Є—Б–∞–љ–Њ –Є –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л—Е –≤–∞–Ї—Ж–Є–љ [29,30].
–Т 2007 –≥. –≤ –®–≤–µ—Ж–Є–Є –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Ї–∞—И, –Њ–±–Њ–≥–∞—Й–µ–љ–љ—Л—Е –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–Љ —И—В–∞–Љ–Љ–Њ–Љ Lactobacillus casei F19 (LMG P–17806) (–і–∞–ї–µ–µ – LF19), —Г –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –≤ –њ–µ—А–Є–Њ–і –≤–≤–µ–і–µ–љ–Є—П –њ—А–Є–Ї–Њ—А–Љ–∞ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–Љ–Љ—Г–љ–Њ–Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Ю–†–Ч –Є –Ю–Ъ–Ш [31]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Њ—И–ї–Є 179 –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–љ–Њ—И–µ–љ–љ—Л—Е –і–µ—В–µ–є –Њ—В 4 –і–Њ 13 –Љ–µ—Б. –ґ–Є–Ј–љ–Є, —А–Њ–ґ–і–µ–љ–љ—Л—Е –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ—Г—В–µ–Љ, –±–µ–Ј –њ—А–Њ—П–≤–ї–µ–љ–Є–є –∞—В–Њ–њ–Є–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Є –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –і–Њ —Н—В–Њ–≥–Њ –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤–ї–Є—П—О—Й–Є—Е –љ–∞ —Б–Њ—Б—В–∞–≤ –Ї–Є—И–µ—З–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л. –Ф–µ—В–Є –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л–µ –≥—А—Г–њ–њ—Л: –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –Ї–∞—И–Є —Б –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–Љ LF19 —Б 4 –Љ–µ—Б. –Є –Є–і–µ–љ—В–Є—З–љ—Л–µ –Ї–∞—И–Є –±–µ–Ј –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П. –° 4 –і–Њ 6 –Љ–µ—Б. –њ—А–Є–Љ–µ–љ—П–ї–∞—Б—М —А–Є—Б–Њ–≤–∞—П –Ї–∞—И–∞, —Б 6 –і–Њ 13 –Љ–µ—Б. – –њ—И–µ–љ–Є—З–љ–∞—П, –Љ–Є–љ–Є–Љ—Г–Љ 1 –њ–Њ—А—Ж–Є—П –≤ –і–µ–љ—М (108 –Ъ–Ю–Х –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є). –Ш–Љ–Љ—Г–љ–Є–Ј–∞—Ж–Є—П –і–µ—В–µ–є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–∞—Б—М –≤ –і–µ–Ї—А–µ—В–Є—А–Њ–≤–∞–љ–љ—Л–µ —Б—А–Њ–Ї–Є (3, 5,5 –Є 12 –Љ–µ—Б. –ґ–Є–Ј–љ–Є) –≤–∞–Ї—Ж–Є–љ–∞–Љ–Є DTaP (diphtheria and tetanus toxoid and acellular pertussis), –†olio and Hib–conjugate vaccines (Infanrix Polio + Hib, GlaxoSmith Kline). –†–Њ–і–Є—В–µ–ї–Є –≤–µ–ї–Є –µ–ґ–µ–і–љ–µ–≤–љ—Л–µ –Ј–∞–њ–Є—Б–Є –≤ –і–љ–µ–≤–љ–Є–Ї–∞—Е, –≥–і–µ –Њ—В–Љ–µ—З–∞–ї–Є —З–Є—Б–ї–Њ –Ї–Њ—А–Љ–ї–µ–љ–Є–є –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–Љ –њ—А–Њ–і—Г–Ї—В–Њ–Љ, –Ї–Њ–љ—Б–Є—Б—В–µ–љ—Ж–Є—О –Є —З–∞—Б—В–Њ—В—Г —Б—В—Г–ї–∞, –∞ —В–∞–Ї–ґ–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –µ—Б–ї–Є –Њ–љ–Є –≤–Њ–Ј–љ–Є–Ї–∞–ї–Є (–Ї–∞—И–µ–ї—М, –љ–∞—Б–Љ–Њ—А–Ї, –њ–Њ–і—К–µ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –ґ–Є–і–Ї–Є–є —Б—В—Г–ї –Є –і—А.). –Ф–µ—В—П–Љ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є –Ј–∞–±–Њ—А –≤–µ–љ–Њ–Ј–љ–Њ–є –Ї—А–Њ–≤–Є –≤ 5,5, 6,5, 12 –Є 13 –Љ–µ—Б. –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –љ–∞–њ—А—П–ґ–µ–љ–љ–Њ—Б—В–Є –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –њ—А–Њ—В–Є–≤ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є–≥–µ–љ–Њ–≤ – –≤–∞–Ї—Ж–Є–љ. –Р–љ–∞–ї–Є–Ј –Ї–∞–ї–∞ –љ–∞ —Б–Њ—Б—В–∞–≤ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї—Б—П –≤ –љ–∞—З–∞–ї–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ 6,5, 9 –Є 13 –Љ–µ—Б.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–µ –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ —А–∞–Ј–љ–Є—Ж—Л –њ–Њ —З–∞—Б—В–Њ—В–µ –Є –Ї–Њ–љ—Б–Є—Б—В–µ–љ—Ж–Є–Є —Б—В—Г–ї–∞ (–≤ —Б—Г—В–Ї–Є) —Г –і–µ—В–µ–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є. –Я—А–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –Ї–∞–ї–∞ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –±–∞–Ї—В–µ—А–Є–Є LF19 –±—Л–ї–Є –≤—Л–і–µ–ї–µ–љ—Л —Г 1 —А–µ–±–µ–љ–Ї–∞ –Є–Ј –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ—Л –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є —Г 4 –і–µ—В–µ–є –Є–Ј –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –њ—А–Є–µ–Љ–∞ –њ—А–Њ–і—Г–Ї—В–∞. –Т –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –і–∞–љ–љ—Л–є —И—В–∞–Љ–Љ –≤—Л–і–µ–ї—П–ї—Б—П —Г 90% –і–µ—В–µ–є –≤ 6,5 –Љ–µ—Б., —Г 85% – –≤ 9 –Љ–µ—Б. –Є —Г 71% – –≤ 13 –Љ–µ—Б. –£ 64% –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Њ–±–Њ–≥–∞—Й–µ–љ–љ—Л–є –њ—А–Њ–і—Г–Ї—В, –±–∞–Ї—В–µ—А–Є–Є –≥—А—Г–њ–њ—Л LF19 –≤—Л–і–µ–ї—П–ї–Є—Б—М –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –љ–Њ —Г 2 –і–µ—В–µ–є –±—Л–ї–Є —Б–ї—Г—З–∞–Є, –Ї–Њ–≥–і–∞ –±–∞–Ї—В–µ—А–Є–Є –љ–µ –≤—Л—П–≤–ї—П–ї–Є—Б—М.
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —А–∞–Ј–љ–Є—Ж—Л —Г –Љ–ї–∞–і–µ–љ—Ж–µ–≤ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –њ–Њ —З–Є—Б–ї—Г –і–љ–µ–є —Б –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–Њ–є —В–µ–ї–∞, —Б –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Є–ї–Є –і–Є–∞—А–µ–µ–є, –љ–Њ –њ–Њ —З–Є—Б–ї—Г –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Р–С) —Г –і–µ—В–µ–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П —А–∞–Ј–љ–Є—Ж–∞.
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є –≤–ї–Є—П–љ–Є—П –њ–Є—В–∞–љ–Є—П –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–Њ—Б—В–≤–∞–Ї—Ж–Є–љ–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ —Г –і–µ—В–µ–є –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є—Б—М —Г—А–Њ–≤–љ–Є IgG –Ї –і–≤—Г–Љ –±–µ–ї–Ї–Њ–≤—Л–Љ –∞–љ—В–Є–≥–µ–љ–∞–Љ (–і–Є—Д—В–µ—А–Є–є–љ–Њ–Љ—Г –Є —Б—В–Њ–ї–±–љ—П—З–љ–Њ–Љ—Г —В–Њ–Ї—Б–Є–љ–∞–Љ) –Є –Њ–і–љ–Њ–Љ—Г –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–љ–Њ–Љ—Г (Hib). –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –љ–∞–Є–±–Њ–ї–µ–µ —Б–Є–ї—М–љ–Њ —Г—А–Њ–≤–љ–Є IgG –Ї –і–∞–љ–љ—Л–Љ –∞–љ—В–Є–≥–µ–љ–∞–Љ –њ–Њ–≤—Л—И–∞–ї–Є—Б—М –њ–Њ—Б–ї–µ 3––є –≤–∞–Ї—Ж–Є–љ–∞—Ж–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ 2––є. –Ю–і–љ–∞–Ї–Њ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –і–µ—В–µ–є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –∞–≤—В–Њ—А—Л –љ–µ –≤—Л—П–≤–Є–ї–Є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –≥—А—Г–і–љ–Њ–µ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–µ, —А–∞–≤–љ–Њ –Ї–∞–Ї –Є –µ–≥–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –≥—Г–Љ–Њ—А–∞–ї—М–љ—Л–є –Є–Љ–Љ—Г–љ–Є—В–µ—В, –і–µ—В–µ–є —А–∞–Ј–і–µ–ї–Є–ї–Є –љ–∞ –≥—А—Г–њ–њ—Л –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–Њ–≥–Њ, –Ї–∞–Ї –і–Њ–ї–≥–Њ –Њ–љ–Є –њ–Њ–ї—Г—З–∞–ї–Є –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ: –±–Њ–ї–µ–µ 6 –Љ–µ—Б. –Є–ї–Є –Љ–µ–љ–µ–µ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤–ї–Є—П–љ–Є–µ –Є–Љ–µ–љ–љ–Њ –≤–Ї–ї—О—З–µ–љ–Є—П LF19 –≤ –њ–Є—В–∞–љ–Є–µ –і–µ—В–µ–є, —В.–µ. –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Ј–∞—Б–µ–ї–µ–љ–Є–µ (–Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є—О) –Ї–Є—И–µ—З–љ–Є–Ї–∞ –і–µ—В–µ–є –і–∞–љ–љ—Л–Љ —И—В–∞–Љ–Љ–Њ–Љ: –і–µ—В–Є, –Ї–Њ—В–Њ—А—Л–µ —В—А–Є–ґ–і—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ –і–µ–Ї—А–µ—В–Є—А–Њ–≤–∞–љ–љ—Л–µ —Б—А–Њ–Ї–Є –≤—Л–і–µ–ї—П–ї–Є —Н—В–Є –±–∞–Ї—В–µ—А–Є–Є («–Ї–Њ–ї–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–∞—П –≥—А—Г–њ–њ–∞»), –Є «–љ–µ–Ї–Њ–ї–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ» –і–µ—В–Є, —Г –Ї–Њ—В–Њ—А—Л—Е –Є—Е –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є –Љ–µ–љ–µ–µ —З–µ–Љ –≤ —В—А–µ—Е –∞–љ–∞–ї–Є–Ј–∞—Е –Ї–∞–ї–∞. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ —Г—А–Њ–≤–µ–љ—М –∞–љ—В–Є–і–Є—Д—В–µ—А–Є–є–љ—Л—Е –∞–љ—В–Є—В–µ–ї –±—Л–ї –≤—Л—И–µ –≤ –≥—А—Г–њ–њ–µ «–Ї–Њ–ї–Њ–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е» –і–µ—В–µ–є (p=0,024).
–Я–Њ—Б–ї–µ–і—Г—О—Й–Є–µ –∞–љ–∞–ї–Є–Ј—Л –і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–љ—В–Є–і–Є—Д—В–µ—А–Є–є–љ—Л—Е –∞–љ—В–Є—В–µ–ї —З–µ—А–µ–Ј 4 –љ–µ–і. –њ–Њ—Б–ї–µ 2––є –і–Њ–Ј—Л (p=0,044) –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –і–µ—В–µ–є. –Я—А–Є—З–µ–Љ –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –±—Л–ї —Г –Љ–ї–∞–і–µ–љ—Ж–µ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є –њ—А–Њ–±–Є–Њ—В–Є–Ї–Є –Є –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–ї–Є—Б—М –≥—А—Г–і–љ—Л–Љ –Љ–Њ–ї–Њ–Ї–Њ–Љ –Љ–µ–љ–µ–µ 6 –Љ–µ—Б.: —Г –љ–Є—Е –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ —В–Є—В—А—Л –∞–љ—В–Є—В–µ–ї –њ–Њ—Б–ї–µ 2––є (p=0,018) –Є –њ–µ—А–µ–і 3––є –≤–∞–Ї—Ж–Є–љ–∞—Ж–Є–µ–є (p=0,048). –Ф—А—Г–≥–Є–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, —Н—Д—Д–µ–Ї—В –±—Л–ї –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Г –і–µ—В–µ–є, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ –њ–Њ—Б–ї–µ 6 –Љ–µ—Б., –њ—А–Є—З–µ–Љ –Њ–љ –љ–µ –Ј–∞–≤–Є—Б–µ–ї –љ–Є –Њ—В –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞, –љ–Є –Њ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є «–Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є–Є» —А–µ–±–µ–љ–Ї–∞ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –љ–Є –Њ—В –Љ–∞—Б—Б–Њ–—А–Њ—Б—В–Њ–≤—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є.
–С–Њ–ї—М—И–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —И—В–∞–Љ–Љ–∞ –љ–∞ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О anti––Ґ –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ. –Я—А–Є –Њ—Ж–µ–љ–Ї–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є anti–Hib IgG –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –≥—А—Г–і–љ–Њ–≥–Њ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є—П, –њ—А–Є—З–µ–Љ –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В «–Ї–Њ–ї–Њ–љ–Є–Ј–∞—Ж–Є–Є» –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–Љ: —Г–ґ–µ –њ–µ—А–µ–і 2––є –і–Њ–Ј–Њ–є –≤ –≥—А—Г–њ–њ–µ –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ –Љ–µ–љ–µ–µ 6 –Љ–µ—Б., –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П anti–Hib IgG –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П (–±–Њ–ї–µ–µ 6 –Љ–µ—Б.). –Ю—В—З–∞—Б—В–Є —Н—В–Њ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М —В–µ–Љ, —З—В–Њ —Н—В–Є –і–µ—В–Є —А–∞–љ—М—И–µ —Б—В–∞–ї–Є –њ–Њ–ї—Г—З–∞—В—М –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –Є –±–Њ–ї—М—И–µ–µ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–њ–∞–і–∞–ї–Њ –≤–Љ–µ—Б—В–µ —Б –љ–Є–Љ, –љ–∞ –Ї–Њ—В–Њ—А—Г—О –Њ—А–≥–∞–љ–Є–Ј–Љ—Г –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М –≤—Л—А–∞–±–∞—В—Л–≤–∞—В—М –Є–Љ–Љ—Г–љ–Є—В–µ—В, –∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —А–∞–љ—М—И–µ –њ—А–Њ—Е–Њ–і–Є–ї–∞ —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Т –њ—А–Њ—В–Є–≤–Њ–≤–µ—Б —Н—В–Њ–Љ—Г –і–µ—В–Є –љ–∞ –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є –њ–Њ–ї—Г—З–∞—О—В –Љ–∞—Б—Б—Г —Г–ґ–µ –≥–Њ—В–Њ–≤—Л—Е –Љ–∞—В–µ—А–Є–љ—Б–Ї–Є—Е –∞–љ—В–Є—В–µ–ї –Є –і—А—Г–≥–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Ј–∞—Й–Є—В—Л, –њ–Њ—Н—В–Њ–Љ—Г –Є—Е –Є–Љ–Љ—Г–љ–Є—В–µ—В —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Є —Б–Њ–Ј—А–µ–≤–∞–µ—В –њ–Њ–Ј–ґ–µ [32].
–Я–Њ –Њ–Ї–Њ–љ—З–∞–љ–Є–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –∞–≤—В–Њ—А–∞–Љ–Є –±—Л–ї–Є —Б–і–µ–ї–∞–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –≤–∞–ґ–љ—Л–µ –Ј–∞–Ї–ї—О—З–µ–љ–Є—П.
• –Я—А–Њ–±–Є–Њ—В–Є–Ї LF19 –≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ –љ–µ –Ј–∞—Й–Є—Й–∞–ї –Њ—В –Є–љ—Д–µ–Ї—Ж–Є–Є, –љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–љ–Є–ґ–∞–ї –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –≤ —Б–ї—Г—З–∞–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –і–∞–љ–љ—Л–µ, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–∞–љ–µ–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤–ї–Є—П–љ–Є—П –Ј–∞–Љ–µ–љ–Є—В–µ–ї—П –≥—А—Г–і–љ–Њ–≥–Њ –Љ–Њ–ї–Њ–Ї–∞, –Њ–±–Њ–≥–∞—Й–µ–љ–љ–Њ–≥–Њ Bb 12 –Є Streptococcus thermophilus, —Г –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ [33].
• –Э–µ —Г–і–∞–ї–Њ—Б—М –≤—Л—П–≤–Є—В—М –Ї–∞–Ї–Њ–≥–Њ––ї–Є–±–Њ —Б–µ—А—М–µ–Ј–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є–Ї–∞ –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–љ–Њ–≥–Њ –∞–љ—В–Є–≥–µ–љ–∞, –Њ–і–љ–∞–Ї–Њ –≤—Л—П–≤–ї–µ–љ–∞ —З–µ—В–Ї–∞—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –њ–Њ—Б—В–≤–∞–Ї—Ж–Є–љ–∞–ї—М–љ–Њ–≥–Њ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ—В–Є–≥–µ–Љ–Њ—Д–Є–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –Њ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≥—А—Г–і–љ–Њ–≥–Њ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є—П.
• –†–µ–≥—Г–ї—П—А–љ—Л–є –њ—А–Є–µ–Љ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —И—В–∞–Љ–Љ–∞ LF19 –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–≤—Л—Б–Є—В—М —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤—Л—А–∞–±–∞—В—Л–≤–∞—В—М —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –њ–Њ—Б—В–≤–∞–Ї—Ж–Є–љ–∞–ї—М–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–і–Є—Д—В–µ—А–Є–є–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –≥—А—Г–њ–њ–µ –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ –Љ–µ–љ–µ–µ 6 –Љ–µ—Б.
• –Ы–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–Є LF19 –≤—Л—П–≤–ї—П–ї–Є—Б—М —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –і–µ—В–µ–є –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ: –≤ 6,5 –Љ–µ—Б. – —Г 90% –Є 13 –Љ–µ—Б. – —Г 71%, —В–Њ–≥–і–∞ –Ї–∞–Ї, –њ–Њ –ї–Є—В–µ—А–∞—В—Г—А–љ—Л–Љ –і–∞–љ–љ—Л–Љ, –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є –Ј–і–Њ—А–Њ–≤—Л—Е —И–≤–µ–і—Б–Ї–Є—Е –і–µ—В–µ–є —Г–ґ–µ –≤ 6 –Љ–µ—Б. –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–Є –≤—Л—П–≤–ї—П–ї–Є—Б—М –≤ –∞–љ–∞–ї–Є–Ј–∞—Е –Ї–∞–ї–∞ —В–Њ–ї—М–Ї–Њ —Г 45% (–њ—А–Є —Н—В–Њ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –±–∞–Ї—В–µ—А–Є–є –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –±—Л–ї–Њ –≤—Л—И–µ —Г –і–µ—В–µ–є –љ–∞ –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–Љ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є–Є), –∞ –≤ 12 –Љ–µ—Б. – —В–Њ–ї—М–Ї–Њ —Г 17% –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –≤–Є–і–∞ –≤—Б–Ї–∞—А–Љ–ї–Є–≤–∞–љ–Є—П [34]. –Ф–∞–љ–љ–∞—П —А–µ–≥—А–µ—Б—Б–Є—П –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —А–Њ—Б—В—Г –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ–є –і–ї—П –Љ–∞–ї–µ–љ—М–Ї–Њ–≥–Њ —А–µ–±–µ–љ–Ї–∞ —Д–ї–Њ—А—Л, —Б–љ–Є–ґ–∞—В—М —Б–Њ–њ—А–Њ—В–Є–≤–ї—П–µ–Љ–Њ—Б—В—М —З—Г–ґ–µ—А–Њ–і–љ–Њ–є –њ–∞—В–Њ–≥–µ–љ–љ–Њ–є —Д–ї–Њ—А–µ.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –≤–Њ –≤—Б–µ–Љ –Љ–Є—А–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –≥–Њ–і –Њ—В –≥–Њ–і–∞. –Ю–і–љ–∞–Ї–Њ –Њ–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –Є–Ј—Г—З–µ–љ–љ—Л—Е –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤, –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—Й–Є—Е —Б 2001 –≥. –љ–∞ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ, —П–≤–ї—П–µ—В—Б—П Actimel, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ—Л–є –Є –њ—А–Њ–Є–Ј–≤–Њ–і–Є–Љ—Л–є –Ї–Њ–Љ–њ–∞–љ–Є–µ–є «–Ф–∞–љ–Њ–љ». –Ф–∞–љ–љ—Л–є –њ—А–Њ–і—Г–Ї—В —Б–Њ–Ј–і–∞–љ –љ–∞ –Њ—Б–љ–Њ–≤–µ –Љ–Њ–ї–Њ–Ї–∞, —Д–µ—А–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ Lactobacillus bulgaricus –Є Streptococcus thermophilus, –Є –Њ–±–Њ–≥–∞—Й–µ–љ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–Љ —И—В–∞–Љ–Љ–Њ–Љ Lactobacillus casei DN–114001 (–Ї–Њ–Љ–Љ–µ—А—З–µ—Б–Ї–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ L. casei Imunitass). –Ф–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –≤–Њ –≤—Б–µ–Љ –Љ–Є—А–µ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ, –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ–Ї–Њ–ї–Њ 30 –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –љ–∞—Г—З–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –Є–Ј—Г—З–µ–љ–Є–µ –њ–Њ–ї–µ–Ј–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ –і–∞–љ–љ–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞, –Є –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Г–Ї—А–µ–њ–ї—П—В—М –Ј–∞—Й–Є—В–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Ї–∞–Ї —Г –≤–Ј—А–Њ—Б–ї—Л—Е, —В–∞–Ї –Є —Г –і–µ—В–µ–є —А–∞–Ј–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞.
–Я–µ—А–≤–Њ–µ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–µ–і–µ–љ–Њ –≤ –і–µ—В—Б–Ї–Є—Е –і–Њ—И–Ї–Њ–ї—М–љ—Л—Е —Г—З—А–µ–ґ–і–µ–љ–Є—П—Е –≤–Њ –§—А–∞–љ—Ж–Є–Є (1999), –Њ–љ–Њ –і–ї–Є–ї–Њ—Б—М 6 –Љ–µ—Б. –Є –≤–Ї–ї—О—З–∞–ї–Њ 287 –і–µ—В–µ–є –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 3 –і–Њ 36 –Љ–µ—Б. [35]. –Ф–µ—В–Є –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 3 –≥—А—Г–њ–њ—Л: 1–—П –≥—А—Г–њ–њ–∞ –њ–Њ–ї—Г—З–∞–ї–∞ –є–Њ–≥—Г—А—В (–Щ), 2–—П –≥—А—Г–њ–њ–∞ – –ґ–µ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ (–Ц–Ь), 3–—П –≥—А—Г–њ–њ–∞ – –Ї–Є—Б–ї–Њ–Љ–Њ–ї–Њ—З–љ—Л–є –њ—А–Њ–і—Г–Ї—В, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є L. bulgaricus, Str. thermophilus –Є –Њ–±–Њ–≥–∞—Й–µ–љ–љ—Л–є –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–Љ —И—В–∞–Љ–Љ–Њ–Љ L. casei Imunitass. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ—Е–Њ–і–Є–ї–Њ –≤ –Ј–Є–Љ–љ–Є–µ –Љ–µ—Б—П—Ж—Л. –Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –і–Є–Ј–∞–є–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–Ј—Г—З–∞–µ–Љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л –≤–Ї–ї—О—З–∞–ї–Є—Б—М –≤ —А–∞—Ж–Є–Њ–љ –њ–Є—В–∞–љ–Є—П –і–µ—В–µ–є –≤ —В–µ—З–µ–љ–Є–µ 1 –Љ–µ—Б., –Ј–∞—В–µ–Љ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 30 –і–љ–µ–є –і–µ—В–Є –љ–µ —Г–њ–Њ—В—А–µ–±–ї—П–ї–Є –і–∞–љ–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л. –Ґ–∞–Ї–Њ–µ —З–µ—А–µ–і–Њ–≤–∞–љ–Є–µ –њ–µ—А–Є–Њ–і–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Њ –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б.
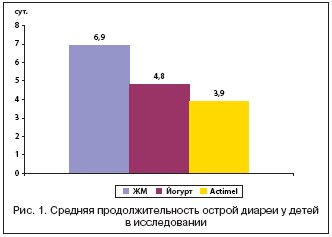
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 3 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П 69 (26%) –і–µ—В–µ–є –њ–µ—А–µ–љ–µ—Б–ї–Є –Ю–Ъ–Ш. –£ 84% –і–µ—В–µ–є –±—Л–ї –Њ—В–Љ–µ—З–µ–љ —В–Њ–ї—М–Ї–Њ –Њ–і–Є–љ —Н–њ–Є–Ј–Њ–і –і–Є–∞—А–µ–Є. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–µ—В–µ–є, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Ю–Ъ–Ш, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Њ—Б—М –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є: 26 (28,3%) –і–µ—В–µ–є –≤ 1––є –≥—А—Г–њ–њ–µ, 23 (26,4%) – –≤–Њ 2––є –Є 20 (23,3%) – –≤ 3––є –≥—А—Г–њ–њ–µ. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —Н–њ–Є–Ј–Њ–і–Њ–≤ –і–Є–∞—А–µ–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —Г 62 –Є–Ј 69 –і–µ—В–µ–є, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –і–Є–∞—А–µ—О. –Т–Њ 2––є –Є 3––є –≥—А—Г–њ–њ–∞—Е —Н–њ–Є–Ј–Њ–і—Л –і–Є–∞—А–µ–є –±—Л–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Ї–Њ—А–Њ—З–µ (4,8±2,3 –Є 3,9±2,4 –і–љ—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ), —З–µ–Љ –≤ 1––є –≥—А—Г–њ–њ–µ (6,9±3,0 –і–љ—П, —А<0,01) (—А–Є—Б. 1). –°–Њ–Ї—А–∞—Й–µ–љ–Є–µ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–Є–∞—А–µ–Є, –љ–∞–±–ї—О–і–∞–≤—И–µ–µ—Б—П –≤ –≥—А—Г–њ–њ–µ –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ—А–Њ–і—Г–Ї—В, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є L. casei DN–114001, –±—Л–ї–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–Љ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –є–Њ–≥—Г—А—В (—А<0,05).
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–і–µ–ї–∞–љ –≤—Л–≤–Њ–і, —З—В–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ –≤ –њ–Є—В–∞–љ–Є–µ –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –Ї–Є—Б–ї–Њ–Љ–Њ–ї–Њ—З–љ–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞, —Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ —И—В–∞–Љ–Љ –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є L. casei DN–114001, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–ї–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Њ—Б—В—А–Њ–є –і–Є–∞—А–µ–Є.
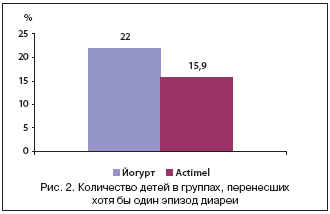
–Ф–∞–ї–µ–µ –∞–≤—В–Њ—А –њ—А–Њ–і–Њ–ї–ґ–Є–ї —Б–≤–Њ–Є –љ–∞–±–ї—О–і–µ–љ–Є—П –≤ –і—А—Г–≥–Њ–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (2000, –§—А–∞–љ—Ж–Є—П), –≤ –Ї–Њ—В–Њ—А–Њ–µ –≤–Њ—И–ї–Є —Г–ґ–µ 928 –і–µ—В–µ–є –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 6 –і–Њ 24 –Љ–µ—Б., —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –љ–∞ 2 –≥—А—Г–њ–њ—Л: –≤ –Њ—Б–љ–Њ–≤–љ—Г—О –≤–Њ—И–ї–Є 463 —А–µ–±–µ–љ–Ї–∞, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤ —В–µ—З–µ–љ–Є–µ 12 –љ–µ–і–µ–ї—М Actimel; –≤ –≥—А—Г–њ–њ—Г —Б—А–∞–≤–љ–µ–љ–Є—П –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 465 –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≤ —В–µ—З–µ–љ–Є–µ —В–Њ–≥–Њ –ґ–µ –≤—А–µ–Љ–µ–љ–Є –є–Њ–≥—Г—А—В, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є L. bulgaricus –Є Str. thermophilus. –¶–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –≤–ї–Є—П–љ–Є—П —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П Actimel –љ–∞ —З–∞—Б—В–Њ—В—Г –Ю–Ъ–Ш —Г –і–µ—В–µ–є —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ [17]. –Т —В–µ—З–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П 148 –і–µ—В–µ–є –њ–µ—А–µ–љ–µ—Б–ї–Є –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ –Њ–і–Є–љ —Н–њ–Є–Ј–Њ–і –і–Є–∞—А–µ–Є. –Ю–і–љ–∞–Ї–Њ —З–Є—Б–ї–Њ –і–µ—В–µ–є, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Ю–Ъ–Ш, –±—Л–ї–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И–µ –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є Actimel (15,9%), —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є –є–Њ–≥—Г—А—В (22%; —А=0,029) (—А–Є—Б. 2). –°—А–µ–і–Є –і—А—Г–≥–Є—Е –Є–Ј—Г—З–∞–≤—И–Є—Е—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ —А–Њ—В–∞–≤–Є—А—Г—Б–Њ–≤ –Є —Г—А–Њ–≤–µ–љ—М –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є –≤ –Ї–∞–ї–µ. –Я–Њ—Б–ї–µ 12 –љ–µ–і. –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–µ—В–µ–є, —Г –Ї–Њ—В–Њ—А—Л—Е –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є –∞–љ—В–Є–≥–µ–љ —А–Њ—В–∞–≤–Є—А—Г—Б–∞ –≤ –Ї–∞–ї–µ, —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М —Б 5,21 –і–Њ 0,29% –≤ 1––є –≥—А—Г–њ–њ–µ –Є —Б 4,81 –і–Њ 2,2% –≤–Њ 2––є –≥—А—Г–њ–њ–µ (—А–∞–Ј–ї–Є—З–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Ј–љ–∞—З–Є–Љ—Л). –£ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –і–µ—В–µ–є –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —В–∞–Ї–ґ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є –≤ —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–µ; –Њ–і–љ–∞–Ї–Њ —Г –і–µ—В–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е Actimel, –Њ–љ–Њ –±—Л–ї–Њ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–Њ, —З–µ–Љ —Г –і–µ—В–µ–є, —Г–њ–Њ—В—А–µ–±–ї—П–≤—И–Є—Е –є–Њ–≥—Г—А—В (–Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є –≤—Л—И–µ 106 –Ъ–Ю–Х/–≥ —Г 48,44 –Є 28,47% –і–µ—В–µ–є –≤ 1––є –Є –≤–Њ 2––є –≥—А—Г–њ–њ–∞—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ).
–Ф–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —А–µ–≥—Г–ї—П—А–љ–Њ–µ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ Actimel –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–Є—И–µ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –і–µ—В–µ–є –Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Г —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є.
–Э–µ –Љ–µ–љ–µ–µ –Є–љ—В–µ—А–µ—Б–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Є–Ј—Г—З–µ–љ–Є–µ –≤–ї–Є—П–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –љ–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ –і–µ—В–µ–є —Б—В–∞—А—И–µ 3 –ї–µ—В. –Ґ–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –њ—А–Њ—Д. –Р.–Т. –У–Њ—А–µ–ї–Њ–≤—Л–Љ –Є —Б–Њ–∞–≤—В. [36], –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П Actimel –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ю–Ъ–Ш —Г –і–µ—В–µ–є. –Ш–Ј 85 –±–Њ–ї—М–љ—Л—Е –Ю–Ъ–Ш –і–µ—В–µ–є –≤ –≤–Њ–Ј—А–∞—Б—В–µ 3–8 –ї–µ—В 55 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ї—Г—З–∞–ї–Є –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є «Actimel» (–Њ—Б–љ–Њ–≤–љ–∞—П –≥—А—Г–њ–њ–∞), –Є 30 –і–µ—В–µ–є (–≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П) – «—В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–є» –є–Њ–≥—Г—А—В. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –≤—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞–ї–Є —Б—В–∞–љ–і–∞—А—В–љ—Г—О —В–µ—А–∞–њ–Є—О –Ю–Ъ–Ш: —Н–љ—В–µ—А–Њ—Б–Њ—А–±–µ–љ—В—Л, –њ–µ—А–Њ—А–∞–ї—М–љ—Г—О —А–µ–≥–Є–і—А–∞—В–∞—Ж–Є—О, —Д–µ—А–Љ–µ–љ—В–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л.
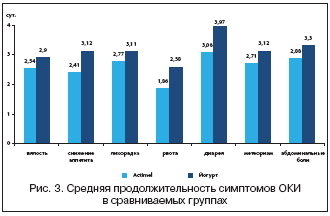
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –і–Є–љ–∞–Љ–Є–Ї–Є –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є –њ—А–Њ–і—Г–Ї—В —Б L. casei DN–114001, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —В–Њ–Ї—Б–Є–Ї–Њ–Ј–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –≤—П–ї–Њ—Б—В–Є –Є –∞–љ–Њ—А–µ–Ї—Б–Є–Є, –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П (—А–Є—Б. 3). –Ґ–∞–Ї, —Г–ґ–µ –љ–∞ 3––Є —Б—Г—В–Ї–Є –ї–µ—З–µ–љ–Є—П —Г –≤—Б–µ—Е –і–µ—В–µ–є –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –Є—Б—З–µ–Ј–∞–ї–∞ –≤—П–ї–Њ—Б—В—М, —Г 96,1% –љ–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–ї—Б—П –∞–њ–њ–µ—В–Є—В, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П –і–∞–љ–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –Є—Б—З–µ–Ј–∞–ї–Є –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ —Б—Г—В–Ї–Є –њ–Њ–Ј–ґ–µ. –Ґ–∞–Ї–ґ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –і–Є–∞—А–µ–є–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (3,31±0,37 –Є 4,33±0,39 —Б—Г—В. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —А=0,048). –Я—А–Є —Н—В–Њ–Љ –Ї –Ї–Њ–љ—Ж—Г 3–—Е —Б—Г—В–Њ–Ї –ї–µ—З–µ–љ–Є—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —Б—В—Г–ї–∞ –±—Л–ї–∞ –Њ—В–Љ–µ—З–µ–љ–∞ —Г 90,3% –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е Actimel, –Є —В–Њ–ї—М–Ї–Њ —Г 51,7% –≥—А—Г–њ–њ—Л —Б—А–∞–≤–љ–µ–љ–Є—П.
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ —А–µ–≥—Г–ї—П—А–љ–Њ–≥–Њ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П Actimel –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —Г—А–Њ–≤–љ—П –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є —Г 30,9% –±–Њ–ї—М–љ—Л—Е, –∞ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ–µ–є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ —Г 25,4%, —Б—Г–ї—М—Д–Є—В—А–µ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –Ї–ї–Њ—Б—В—А–Є–і–Є–є – —Г 20% –Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ – —Г 30,9%. –Т –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П, –њ–Њ–ї—Г—З–∞–≤—И–µ–є —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–є –є–Њ–≥—Г—А—В, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —Б–і–≤–Є–≥–Њ–≤ –≤ —Б–Њ—Б—В–∞–≤–µ –Ї–Є—И–µ—З–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ.
–Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤—Л—И–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞–≥–ї—П–і–љ–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞ Actimel –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є–Є –Ю–Ъ–Ш —Г –і–µ—В–µ–є.
–Т –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е —А–∞–љ–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Ю–Ъ–Ш —Г –і–µ—В–µ–є —Б –∞—В–Њ–њ–Є—З–µ—Б–Ї–Є–Љ –і–µ—А–Љ–∞—В–Є—В–Њ–Љ (–Р—В–Ф) —Б–Є–љ–і—А–Њ–Љ –і–Є–∞—А–µ–Є –Є–Љ–µ–µ—В –±–Њ–ї—М—И—Г—О –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М, —З–µ–Љ —Г –і–µ—В–µ–є –±–µ–Ј –∞–ї–ї–µ—А–≥–Є–Є, –Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Г—Б–Є–ї–µ–љ–Є–µ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –∞—В–Њ–њ–Є–Є [37]. –Ф–ї—П –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Є –Є–љ—В–µ—А–µ—Б–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–ї–Є–љ–Є–Ї–Њ––ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ –Ї–Њ—В–Њ—А–Њ–Љ —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є 45 –±–Њ–ї—М–љ—Л—Е –Ю–Ъ–Ш –≤ –≤–Њ–Ј—А–∞—Б—В–µ 3–8 –ї–µ—В —Б –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –Р—В–Ф, –њ–Њ–ї—Г—З–∞–≤—И–Є–Љ–Є –Ї–Є—Б–ї–Њ–Љ–Њ–ї–Њ—З–љ—Л–є –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–є –њ—А–Њ–і—Г–Ї—В Actimel (–Њ—Б–љ–Њ–≤–љ–∞—П –≥—А—Г–њ–њ–∞) –Є–ї–Є –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–є –њ—А–Њ–і—Г–Ї—В –±–µ–Ј –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ (–≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П) [38]. –С—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ –≤ —В–µ—А–∞–њ–Є—О –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –њ—А–Њ–і—Г–Ї—В–∞, —Б–Њ–і–µ—А–ґ–∞—Й–µ–≥–Њ L. —Бasei, —Б –њ–µ—А–≤—Л—Е –і–љ–µ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–Љ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –і–Є–∞—А–µ–Є, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П (4,8±0,42 —Б—Г—В. –Є 6,2±0,42 —Б—Г—В. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —А<0,05). –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —А–∞–Ј–ї–Є—З–Є—П –≤ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є, –±–Њ–ї–µ–є –≤ –ґ–Є–≤–Њ—В–µ, –∞–љ–Њ—А–µ–Ї—Б–Є–Є –≤ –Є–Ј—Г—З–∞–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е –±—Л–ї–Є –љ–µ—Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞ –≤ —В–µ—А–∞–њ–Є–Є –і–µ—В–µ–є –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –Њ–Ї–∞–Ј–∞–ї–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ –Є –љ–∞ —В–µ—З–µ–љ–Є–µ –Р—В–Ф: —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–µ–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–∞–њ—Г–ї–µ–Ј–љ—Л—Е –≤—Л—Б—Л–њ–∞–љ–Є–є, –Њ—Б–ї–∞–±–ї–µ–љ–Є–µ –Ї–Њ–ґ–љ–Њ–≥–Њ –Ј—Г–і–∞. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї—Б—П –Є–љ–і–µ–Ї—Б SCORAD (—В–∞–±–ї. 1).
–Я—А–Є –Њ—Ж–µ–љ–Ї–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –Ї–Є—И–µ—З–љ–Є–Ї–∞ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Г 100% –і–µ—В–µ–є —Б –Р—В–Ф –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Ю–Ъ–Ш –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –і–Є—Б–±–Є–Њ—В–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П (1––є —Б—В–µ–њ–µ–љ–Є – —Г 31,1% –і–µ—В–µ–є, 2––є —Б—В–µ–њ–µ–љ–Є – —Г 40%, 3––є —Б—В–µ–њ–µ–љ–Є – —Г 28,9%), —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–≤—И–Є–µ—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є (<106) – —Г 19 (42,2%) –±–Њ–ї—М–љ—Л—Е, –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є – —Г 14 (31,1%). –£ 37,8% –і–µ—В–µ–є —Б –Р—В–Ф –Њ—В–Љ–µ—З–µ–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ Staphilococcus; —Г 33,3% – –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –°lostridium –Є —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л (Proteus, Citroba—Бter, Enteroba—Бter –Є –і—А.); —Г 20% –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є—Б—М –≤ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –≥—А–Є–±—Л —А–Њ–і–∞ Candida –Є –Ї–Є—И–µ—З–љ–∞—П –њ–∞–ї–Њ—З–Ї–∞ —Б –Є–Ј–Љ–µ–љ–µ–љ–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є. –Т–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Н—Г–±–Є–Њ–Ј–∞ —З–∞—Й–µ (—Г 40% –і–µ—В–µ–є) –љ–∞—Б—В—Г–њ–∞–ї–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є –Ї–Є—Б–ї–Њ–Љ–Њ–ї–Њ—З–љ—Л–є –њ—А–Њ–і—Г–Ї—В —Б L. casei DN–114001, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ —Б—А–∞–≤–љ–µ–љ–Є—П (–≤ 15% —Б–ї—Г—З–∞–µ–≤). –Т–Ї–ї—О—З–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—В–∞ Actimel –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Г—О —В–µ—А–∞–њ–Є—О –Ю–Ъ–Ш —Г –і–µ—В–µ–є –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Г—А–Њ–≤–љ—П –ї–∞–Ї—В–Њ–±–∞–Ї—В–µ—А–Є–є —Г 7 (28%) –±–Њ–ї—М–љ—Л—Е, –±–Є—Д–Є–і–Њ–±–∞–Ї—В–µ—А–Є–є –Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ – —Г 4 (16%), –љ–∞ —Д–Њ–љ–µ —З–µ–≥–Њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ–µ–є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ <104 —Г 7 (28%), –≥—А–Є–±–Њ–≤ —А–Њ–і–∞ Candida – —Г 3 (12%), –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ —А–Њ–і–∞ Clostridium – —Г 5 (20%), —Г—Б–ї–Њ–≤–љ–Њ––њ–∞—В–Њ–≥–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ – —Г 4 (16%). –Ф–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–∞–≥–ї—П–і–љ–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Њ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —В–µ—З–µ–љ–Є–µ –Ї–∞–Ї –Ю–Ъ–Ш (—Б–Њ–Ї—А–∞—Й–∞–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї–Є—И–µ—З–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є, –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В—Б—П –Љ–Є–Ї—А–Њ–±–љ—Л–є –њ–µ–є–Ј–∞–ґ –Ц–Ъ–Ґ –Є –±–∞—А—М–µ—А–љ–∞—П —Д—Г–љ–Ї—Ж–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є), —В–∞–Ї –Є –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –Њ —З–µ–Љ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Є–љ–і–µ–Ї—Б–∞ SCORAD.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ј–≤–Њ–ї—П—О—В —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і –Њ —В–Њ–Љ, —З—В–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е —И—В–∞–Љ–Љ–Њ–≤ –≤ –њ–Є—В–∞–љ–Є–µ –і–µ—В–µ–є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –љ–∞–Є–±–Њ–ї–µ–µ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–µ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ –Ї–Є—И–µ—З–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –њ–Њ—Б—В–≤–∞–Ї—Ж–Є–љ–∞–ї—М–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–є –Є –ї–µ—З–µ–±–љ—Л–є —Н—Д—Д–µ–Ї—В—Л –њ—А–Є –Ю–Ъ–Ш, —Г–Љ–µ–љ—М—И–∞–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Я—А–Њ–і—Г–Ї—В—Л –њ–Є—Й–µ–≤—Л–µ. –Я—А–Њ–і—Г–Ї—В—Л –њ–Є—Й–µ–≤—Л–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ. –Ґ–µ—А–Љ–Є–љ—Л –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ. –У–Ю–°–Ґ 52349–2005.
2. Mercenier A, Pavan S, Pot B. Probiotics as biotherapeutic agents: present knowledge and future prospects. Current Pharmaceutical Design. 2002; 8: 99–110.
3. FAO/WHO Guidelines for the evaluation of probiotics in food, 2002. Working Group on Drafting Guidelines for the Evaluation of Probiotics in Food. (section 5.3, Expert report). ftp://ftp.fao.org/es/esn/food/Reid.pdf
4. Olivares M, Diaz–Romero MP, Martin R, et al. Antimicrobial potential of four Lactobacillus strains isolated from breast milk. J Appl Microbiol. 2006; 101 (1): 72–79.
5. Martin R, Olivares M, Marin ML, et al. Probiotic potential of 3 Lactobacilli strains isolated from breast milk. J Hum Lact. 2005; 21 (1): 8–17.
6. Lara–Villoslada F. Beneficial effects of probiotic bacteria isolated from breast milk. Br J Nutr. 2007; 98 (Suppl. 1): S96–S100.
7. Isolourie E., Sutas Y, Kankaanpaa P, et al. Am J Clin Nutr. 2001;73(Suppl 2):S444–S450.
8. Kukkonen K., Savilahti E, Haahtela T., et al. Probiotics and prebiotic galacto–oligosaccharides in the prevention of allergic disease. J Allergy Clin Immunol. 2007; 119(4): 1019–21.
9. Kalliomaki M. Collado M, Salminen S and Isolauri E. Functional foods forum and program on health biosciences Univ. of Turku. Am J Clin Nutr. 2008; 88(6):1643–47.
10. Ohlson K, Mahlapuu M, Svensson U. Probiotics to influence fat metabolism and obesity. 2007–04–19: (WO2007043933).
11. Pettoello M.M., Guandalini S. Ecuba P., et al. Lactose malabsorption in children with symptomatic giardia Lamblia infection: feasibility of yoghurt supplementation. J Pediat Gastroenterol. 1989; 9 (3): 295–230.
12. Johnston BC. Probiotics for pediatric antibiotic–associated diarrhea: a meta–analysis of randomized placebo–controlled trials. CMAJ. 2006; 175 (4): 377–383.
13. Rolf RD. The role of probiotic cultures in the control of gastro intestinal Health. J Nutr. 2000: 30 (Suppl. 1): S396– S402.
14. Gotz V, Romankiewicz JA, Moss J and HW Murray. Prophylaxis against Ampicillin associated diarrhea with a Lactobacillus preparation. Am J Hosp Pharm. 1979; 36(6): 754–757.
15. Kalliomaki M. Probiotics and prevention of atopic disease: 4–year follow–up of a randomised placebo–controlled trial. Lancet. 2003; 361 (9372): 1869–1871.
16. Taylor AL. Probiotic supplementation for the first 6 months of life fails to reduce the risk of atopic dermatitis and increases the risk of allergen sensitization in high–risk children: a randomized controlled trial. J Allergy Clin Immunol. 2007; 119 (1): 184–191.
17. Pedone CA, Arnaud CC, Postaire ER, et al. Multicentric study of the effect of milk fermented by Lactobacillus casei on the incidence of diarrhea. Int J Clin Prac. 2000; 54 (9): 568–571.
18. Ljungh A, Lan J, Yanagisawa N. Isolation, selection and characteristics of Lactobacillus paracasei subsp. Paracasei F19. Microb Ecol Health Dis. 2002; 14 (Suppl. 3): S4–S6.
19. Rinne M, Kalliomaki M, Arvilommi H, et al. Effect of probiotics and breastfeeding on the Bifidobacterium and Lactobacillus/ Enterococcus microbiota and humoral immune responses. J Pediatr. 2005; 147(2): 186–191.
20. Weizman Z, Asli G, Alsheikh A. Effect of a probiotic infant formula on infections in child care centers: comparison of two probiotic agents. Pediatrics. 2005; 115(1): 5–9.
21. Savino F, Pelle E, Palumeri E, et al. Lactobacillus reuteri (american type culture collection strain 55730) versus simethicone in the treatment of infantile colic: a prospective randomized study. Pediatrics. 2007; 119e:124–e–130.
22. Di Caro S, Tao H, Grillo A, et al. Effects of Lactobacillus GG on genes expression pattern in small bowel mucosa. Digestive and Liver Disease. 2005; 37:320–329.
23. Park HO, Bang YB, Joung HJ, et al. Lactobacillus KTCK 0774BP and acetobacter KCTC 0773 BP for treatment or prevention of obesity and diabetes mellitus. 2004; US patent N 6 808 703.
24. Pereira DI, Gibson GR. Effects of consumption of probiotics and prebiotics on serum lipid levels in humans. Crit Rev Biochem Mol Biol. 2002; 37(4): 259–281.
25. Steppan CM, Bailey ST, Bath S, et al. The hormone resistine links obesity to diabetes. Nature. 2001; 409(6818):307–12
26. Orrhage K, Nord CE. Factors controlling the bacterial colonization in the intestine in breastfed infants. Acta Paediatr. 1999; 430 (Suppl. 1): S47–S57.
27. Isolauri E, Joensuu J, Soumalainen H, et al. Improved immunogenicity of oral DxRRV reassortant rotavirus vaccine by Lactobacillus casei GG. Vaccine. 1995; 13(3): 310–312.
28. He F, Elina T, Heikki A, et al. Modulation of humoral immune response through probiotics intake. FEMS Immunol Med Microbiol. 2000; 29: 47–52.
29 .Mullie C, Yazourh A, Thibault H, et al. Increased poliovirus–specific intestinal antibody response coincides with promotion of Bifidobacterium Longum–infantis and Bifidobacterium breve in infants: a randomized, double–blind, placebo–controlled trial. Pediatr Res. 2004; 56 (5): 791–795.
30. Kukkonen K, Nieminen T, Poussa T, et al. Effect of probiotics on vaccine antibody responses in infancy – a randomized, double–blind, placebo–controlled trial. Pediatr Allergy Immunol. 2006; 17 (6): 416–421.
31. West CE, Gothefors L, Granstrom M, et al. Effects of feeding probiotics during weaning on infections and antibody responses to diphtheria, tetanus and Hib vaccines. Pediatr Allergy and Immunol. 2008; 19 (1): 53–60.
32. Wold AE, Adlerberth I. Does brestfeeding affect the infants immune responsiveness? Acta Paediatr. 1998; 87 (1): 19–22.
33. Saavedra J., Abi–Hanna A., Moore N., Yolken R. Long–term consumption on infant formulas containing live probiotic bacteria: tolerance and safety. Am J Nutr. 2004;79:261–7.
34. Ahrne S, Lonnermark E, Wold AE, et al. Lactobacilli in the interstinal microbiota of Swedish infants. Microbes Infect. 2005; 7 (11–12): 1256–1262.
35. Pedone CA, Bernabeu AO, Postaire ER, et al. The effect of supplementation with milk fermented by Lactobacillus casei (strain DN–114 001) on acute diarrhoea in children attending day care centres. Int J Clin Prac. 1999; 53 (3): 179–184.
36. –У–Њ—А–µ–ї–Њ–≤ –Р.–Т., –£—Б–µ–љ–Ї–Њ –Ф.–Т., –Х–ї–µ–Ј–Њ–≤–∞ –Ы.–Ш. –Є –і—А. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –≤ –ї–µ—З–µ–љ–Є–Є –Ї–Є—И–µ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –і–µ—В–µ–є // –Т–Њ–њ—А. —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –њ–µ–і–Є–∞—В—А–Є–Є. 2005; 2 (4): 47–52.
37. –£—Б–µ–љ–Ї–Њ –Ф.–Т. –Ю—Б—В—А—Л–µ –Ї–Є—И–µ—З–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є —Г –і–µ—В–µ–є —Б –∞—В–Њ–њ–Є–µ–є. –Ь–∞—В–µ—А–Є–∞–ї—Л XI –Ъ–Њ–љ–≥—А–µ—Б—Б–∞ –і–µ—В—Б–Ї–Є—Е –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Њ–≤ –†–Њ—Б—Б–Є–Є «–Р–Ї—В—Г–∞–ї—М–љ—Л–µ –њ—А–Њ–±–ї–µ–Љ—Л –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Г –і–µ—В–µ–є». –Ь., 2004: 325–326.
38. –£—Б–µ–љ–Ї–Њ –Ф.–Т., –У–Њ—А–µ–ї–Њ–≤ –Р.–Т., –®–∞–±–∞–ї–Є–љ–∞ –°.–Т. –Ю–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Є—Б–ї–Њ–Љ–Њ–ї–Њ—З–љ–Њ–≥–Њ –њ—А–Њ–±–Є–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ–і—Г–Ї—В–∞ –≤ –ї–µ—З–µ–љ–Є–Є –Њ—Б—В—А—Л—Е –Ї–Є—И–µ—З–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є —Г –і–µ—В–µ–є —Б –∞—В–Њ–њ–Є—З–µ—Б–Ї–Є–Љ –і–µ—А–Љ–∞—В–Є—В–Њ–Љ // –Я–µ–і–Є–∞—В—А–Є—П. 2008; 87 (4): 82–87.











