–Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –њ–Њ—А–∞–ґ–µ–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є—П —Г –і–µ—В–µ–є —П–≤–ї—П–µ—В—Б—П —Б—В–µ—А–µ–Њ—В–Є–њ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –љ–Њ–Ј–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ–∞—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–Т–Ю–Я–Ґ), –≥–µ–њ–∞—В–Њ–±–Є–ї–Є–∞—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є, –Њ—З–µ–љ—М —З–∞—Б—В–Њ, –Ї–Є—И–µ—З–љ–Є–Ї–∞. –І–µ–Љ –Љ–ї–∞–і—И–µ —А–µ–±–µ–љ–Њ–Ї, —В–µ–Љ –Љ–µ–љ–µ–µ —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ–є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Ї–∞—А—В–Є–љ–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, —А–∞–Ј–Љ—Л–≤–∞—О—В—Б—П —З–µ—В–Ї–Є–µ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ––і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є –≥–∞—Б—В—А–Є—В–∞ –Є –і—Г–Њ–і–µ–љ–Є—В–∞, —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є (–ѓ–С), –њ–Њ—А–∞–ґ–µ–љ–Є–є –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –і–µ—В–µ–є —Б —Б–Є–Љ–њ—В–Њ–Љ–Њ–Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–Љ –і–Є—Б–њ–µ–њ—Б–Є–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –љ–µ –љ–Њ–Ј–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П, –∞ —Б–Є–љ–і—А–Њ–Љ–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ [2].
–Э–Є –Њ–і–Є–љ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–є –Љ–µ—В–Њ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї –Є—Б—З–µ—А–њ—Л–≤–∞—О—Й–µ –Њ–±—К—П—Б–љ–Є—В—М –њ—А–Є—З–Є–љ—Л –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л—Е –±–Њ–ї–µ–є –Є –і–Є—Б–њ–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Э–∞–≤—П–Ј—Л–≤–∞–љ–Є–µ —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–њ–∞—Б–љ–Њ –љ–µ —Б—В–Њ–ї—М–Ї–Њ –≥–Є–њ–µ—А–і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Њ–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≥–∞—Б—В—А–Є—В–∞, —Б–Ї–Њ–ї—М–Ї–Њ –Є–≥–љ–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Є—Б—В–Є–љ–љ—Л—Е –њ—А–Є—З–Є–љ –°–Ф, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В —В–Њ—А–њ–Є–і–љ–Њ—Б—В—М –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є, —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є. –Я–Њ—Н—В–Њ–Љ—Г —Б–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–∞—П —В–µ—А–Љ–Є–љ–Њ–ї–Њ–≥–Є—П –њ—А–µ–і–ї–∞–≥–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –і–ї—П –Њ–њ–Є—Б–∞–љ–Є—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л —В–µ—А–Љ–Є–љ «–≥–∞—Б—В—А–Њ–њ–∞—В–Є—П» (—Н—А–Њ–Ј–Є–≤–љ–∞—П, —Н—А–Є—В–µ–Љ–∞—В–Њ–Ј–љ–∞—П, –≥–Є–њ–µ—А—В—А–Њ—Д–Є—З–µ—Б–Ї–∞—П, –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–∞—П) –≤–Љ–µ—Б—В–Њ —В–µ—А–Љ–Є–љ–∞ «–≥–∞—Б—В—А–Є—В» [3]. –Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –љ–µ –і–Њ–ї–ґ–љ–Њ –њ–µ—А–µ–Њ—Ж–µ–љ–Є–≤–∞—В—М—Б—П, –∞ —Н—В–Њ –Ј–∞—Б—В–∞–≤–ї—П–µ—В –љ–∞—Б –±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ –≤–Ј–≥–ї—П–љ—Г—В—М –љ–∞ –њ—А–Є—А–Њ–і—Г –°–Ф, –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –≤ –µ–≥–Њ —А–∞–Ј–≤–Є—В–Є–Є –њ—А–Є–љ–Є–Љ–∞—О—В —Г—З–∞—Б—В–Є–µ –Є –љ–µ–≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л.
–°–Ф –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–Ц–Ъ–Ґ), —В–∞–Ї–Є–Љ–Є –Ї–∞–Ї –ѓ–С, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В –Є –ґ–µ–ї—З–љ–Њ––Ї–∞–Љ–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –њ–∞–љ–Ї—А–µ–∞—В–Є—В, –љ–µ–Ї–Њ—В–Њ—А—Л–Љ–Є –і—А—Г–≥–Є–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ—Б—В–∞–≤–ї—П—О—В –≥—А—Г–њ–њ—Г –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –і–Є—Б–њ–µ–њ—Б–Є–Є. –Х—Б–ї–Є –≤ —Е–Њ–і–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ, —В–Њ –≥–Њ–≤–Њ—А—П—В –Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–Љ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–µ –Ц–Ъ–Ґ [4].
–Т 1999 –≥. –њ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Ї–Њ–Љ–Є—В–µ—В–∞ –њ–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ –Є–Ј –°–Ф –±—Л–ї–Є –≤—Л–і–µ–ї–µ–љ—Л –≤ –Њ—Б–Њ–±—Г—О —Д–Њ—А–Љ—Г —Б–ї—Г—З–∞–Є, –Ї–Њ–≥–і–∞ –±–Њ–ї—М –Є–ї–Є –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –≤ –ґ–Є–≤–Њ—В–µ –∞—Б—Б–Њ—Ж–Є–Є—А—Г—О—В—Б—П —Б –і–µ—Д–µ–Ї–∞—Ж–Є—П–Љ–Є – –Њ–љ–Є –Њ—В–љ–µ—Б–µ–љ—Л –Ї —Б–Є–љ–і—А–Њ–Љ—Г —А–∞–Ј–і—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Є–Ї–∞ (–°–†–Ъ). –Я—А–Є –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –і–Є—Б–њ–µ–њ—Б–Є–Є —В–∞–Ї–Њ–≥–Њ —Б–Є–Љ–њ—В–Њ–Љ–∞, –Ї–∞–Ї –Є–Ј–ґ–Њ–≥–∞ —Б–ї—Г—З–∞–є —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —А–∞—Б—Ж–µ–љ–Є–≤–∞—В—М –Ї–∞–Ї –≥–∞—Б—В—А–Њ—Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ—Г—О —А–µ—Д–ї—О–Ї—Б–љ—Г—О –±–Њ–ї–µ–Ј–љ—М (–У–≠–†–С). –≠—В–Є–Љ —Б–Њ–≥–ї–∞—И–µ–љ–Є–µ–Љ, –њ–Њ–ї—Г—З–Є–≤—И–Є–Љ –љ–∞–Ј–≤–∞–љ–Є–µ –†–Є–Љ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є II, –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –±–Њ–ї–Є, –ї–Њ–Ї–∞–ї–Є–Ј—Г—О—Й–Є–µ—Б—П –≤ –њ—А–∞–≤–Њ–Љ –≤–µ—А—Е–љ–µ–Љ –Ї–≤–∞–і—А–∞–љ—В–µ –Є —Б–Њ—З–µ—В–∞—О—Й–Є–µ—Б—П —Б –≥–Њ—А–µ—З—М—О –≤–Њ —А—В—Г, –≤–Ј–і—Г—В–Є–µ–Љ –ґ–Є–≤–Њ—В–∞ –Є–ї–Є –љ–µ—Г—Б—В–Њ–є—З–Є–≤—Л–Љ —Б—В—Г–ї–Њ–Љ, –±—Л–ї–Є –Њ–њ—А–µ–і–µ–ї–µ–љ—Л –Ї–∞–Ї –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ [5]. –Т–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е —А–∞–Ј–ї–Є—З–љ—Л–µ —Д–Њ—А–Љ—Л —Б–Њ—З–µ—В–∞—О—В—Б—П, —В.–Ї. —Г 50–70% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–†–Ъ –Є–Љ–µ—О—В—Б—П –ґ–∞–ї–Њ–±—Л, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –і–Є—Б–њ–µ–њ—Б–Є–Є (–§–Ф).
–Ґ–∞–Ї–ґ–µ –†–Є–Љ—Б–Ї–Є–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є II –≤–≤–µ–і–µ–љ–Њ —В–∞–Ї–Њ–µ –њ–Њ–љ—П—В–Є–µ, –Ї–∞–Ї «—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –і–Є—Б–њ–µ–њ—Б–Є—П» – –Њ—Й—Г—Й–µ–љ–Є–µ –±–Њ–ї–Є –Є–ї–Є –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В–∞ (—В—П–ґ–µ—Б—В—М, –њ–µ—А–µ–њ–Њ–ї–љ–µ–љ–Є–µ, —А–∞–љ–љ–µ–µ –љ–∞—Б—Л—Й–µ–љ–Є–µ), –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–Њ–µ –≤ —Н–њ–Є–≥–∞—Б—В—А–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –±–ї–Є–ґ–µ –Ї —Б—А–µ–і–Є–љ–љ–Њ–є –ї–Є–љ–Є–Є, –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є, —З—В–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ц–Ъ–Ґ –љ–µ –≤—Л—П–≤–Є–ї–Њ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Т —Б–ї–µ–і—Г—О—Й–µ–є —А–µ–і–∞–Ї—Ж–Є–Є –†–Є–Љ—Б–Ї–Є—Е –Ъ—А–Є—В–µ—А–Є–µ–≤ III (2006 –≥.) –≤—Л–і–µ–ї–µ–љ—Л —В–∞–Ї–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –≤–∞—А–Є–∞–љ—В—Л –§–Ф, –Ї–∞–Ї –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ—Л–є –Є –±–Њ–ї–µ–≤–Њ–є. –Т –њ–µ—А–≤–Њ–Љ —Б–ї—Г—З–∞–µ –њ—А–µ–Њ–±–ї–∞–і–∞—О—В –ґ–∞–ї–Њ–±—Л –љ–∞ —В—П–ґ–µ—Б—В—М, –≤–Ј–і—Г—В–Є–µ –Є —А–∞–љ–љ–Є–µ –±–Њ–ї–Є –≤ –ґ–Є–≤–Њ—В–µ, —В–Њ—И–љ–Њ—В—Г, –Њ—В—А—Л–ґ–Ї—Г. –Т—В–Њ—А–Њ–є –≤–∞—А–Є–∞–љ—В —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ–Є –≥–Њ–ї–Њ–і–љ—Л–Љ–Є –Є–ї–Є –љ–Њ—З–љ—Л–Љ–Є –±–Њ–ї—П–Љ–Є, –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є – —В–Њ—И–љ–Њ—В–Њ–є –Є —А–≤–Њ—В–Њ–є, –Є–Ј–ґ–Њ–≥–Њ–є. –Ю–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ –і–ї—П –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і–Є–∞–≥–љ–Њ–Ј–∞ –§–Ф —П–≤–ї—П–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є–є –љ–µ –Љ–µ–љ–µ–µ 12 –љ–µ–і. –Ј–∞ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є–є –≥–Њ–і [6].
–†–µ–≥–Є—Б—В—А–Є—А—Г–µ–Љ–∞—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –њ—А–Њ—П–≤–ї—П—О—Й–Є—Е—Б—П –°–Ф, —Б–Њ—Б—В–∞–≤–ї—П–µ—В —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ 5–7%, –Њ–і–љ–∞–Ї–Њ, –њ–Њ –і–∞–љ–љ—Л–Љ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Њ–љ–∞ –і–Њ—Б—В–Є–≥–∞–µ—В 25–40%. –Т —Б—В—А—Г–Ї—В—Г—А–µ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–Њ –Њ–±—А–∞—Й–∞–µ–Љ–Њ—Б—В–Є –°–Ф –Ј–∞–љ–Є–Љ–∞–µ—В –і–Њ 95%, –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –і–µ—В—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —П–≤–ї—П–µ—В—Б—П –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є —Г–і–µ–ї—М–љ—Л–є –≤–µ—Б –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –і–Є—Б–њ–µ–њ—Б–Є–Є, –Ї–Њ—В–Њ—А—Л–є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 1–5%, —Г–≤–µ–ї–Є—З–Є–≤–∞—П—Б—М –≤ —Б—В–∞—А—И–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ–∞—Е.
–Т —Б—В—А—Г–Ї—В—Г—А–µ –§–† –Ц–Ъ–Ґ, –њ—А–Њ—П–≤–ї—П—О—Й–Є—Е—Б—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–Љ –і–Є—Б–њ–µ–њ—Б–Є–Є, –њ–Њ –љ–∞—И–Є–Љ –і–∞–љ–љ—Л–Љ, –њ—А–µ–Њ–±–ї–∞–і–∞–µ—В –§–Ф, –і–Њ–ї—П –Ї–Њ—В–Њ—А–Њ–є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 64,6%, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –±–Њ–ї–Є (–§–Р–С) –≤—Б—В—А–µ—З–∞—О—В—Б—П —Г –Ї–∞–ґ–і–Њ–≥–Њ –њ—П—В–Њ–≥–Њ —А–µ–±–µ–љ–Ї–∞ (20,1%), –°–†–Ъ – —Г –Ї–∞–ґ–і–Њ–≥–Њ –і–µ—Б—П—В–Њ–≥–Њ (10,4%), –∞ –±–Є–ї–Є–∞—А–љ–∞—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П – —Г –Ї–∞–ґ–і–Њ–≥–Њ –і–≤–∞–і—Ж–∞—В–Њ–≥–Њ (4,9%) [7].
–Ю–±—Й–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –°–Ф –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –і–Њ–≤–Њ–ї—М–љ–Њ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ—Л –Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л. –Ш–Љ–Є —П–≤–ї—П—О—В—Б—П –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Љ–Њ—В–Њ—А–Є–Ї–Є –Є –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М, –љ–∞ –≤—В–Њ—А–Њ–Љ –њ–ї–∞–љ–µ –љ–∞—Е–Њ–і—П—В—Б—П –љ–∞—А—Г—И–µ–љ–Є—П —Б–µ–Ї—А–µ—Ж–Є–Є –Є –±–Є–Њ—Ж–µ–љ–Њ–Ј–∞, –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—П –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Д–Њ—А–Љ—Г —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞. –Э–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –§–Ф –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–≥—Г—В –њ—А–Њ—П–≤–ї—П—В—М—Б—П –≤ –∞–љ—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є –і–Є—Б–Ї–Њ–Њ—А–і–Є–љ–∞—Ж–Є–Є, –≥–∞—Б—В—А–Њ–њ–∞—А–µ–Ј–∞—Е, –Њ—Б–ї–∞–±–ї–µ–љ–Є–Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–є –Љ–Њ—В–Њ—А–Є–Ї–Є –∞–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞, —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е —А–µ–ї–∞–Ї—Б–∞—Ж–Є–Є, –∞–Ї–Ї–Њ–Љ–Њ–і–∞—Ж–Є–Є, –љ–∞—А—Г—И–µ–љ–Є–Є —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –ґ–µ–ї—Г–і–Ї–∞ –≤ –Љ–µ–ґ–њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ, –ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –і–Є—Б—А–Є—В–Љ–Є–Є, –і—Г–Њ–і–µ–љ–Њ–≥–∞—Б—В—А–∞–ї—М–љ–Њ–Љ —А–µ—Д–ї—О–Ї—Б–µ.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ —В–Њ–ї—М–Ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ —А–Њ–ї—М –љ–∞—А—Г—И–µ–љ–Є–є –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є –Љ–Њ—В–Њ—А–Є–Ї–Є –≤ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є –ґ–∞–ї–Њ–±, –љ–Њ –Є –≤—Л—П–≤–ї–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –Ї–Њ—А—А–µ–ї—П—Ж–Є—П –Љ–µ–ґ–і—Г —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –ґ–µ–ї—Г–і–Ї–∞. –Ґ–∞–Ї, –≥–∞—Б—В—А–Њ–њ–∞—А–µ–Ј –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б —В–∞–Ї–Є–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є, –Ї–∞–Ї —З—Г–≤—Б—В–≤–Њ –њ–µ—А–µ–њ–Њ–ї–љ–µ–љ–Є—П –њ–Њ—Б–ї–µ –µ–і—Л, —В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞; –љ–∞—А—Г—И–µ–љ–Є—П –∞–Ї–Ї–Њ–Љ–Њ–і–∞—Ж–Є–Є – —Б —А–∞–љ–љ–Є–Љ –љ–∞—Б—Л—Й–µ–љ–Є–µ–Љ, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —Б—В–µ–љ–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Ї —А–∞—Б—В—П–ґ–µ–љ–Є—О – —Б —З—Г–≤—Б—В–≤–Њ–Љ –њ–µ—А–µ–њ–Њ–ї–љ–µ–љ–Є—П –Є –±–Њ–ї—П–Љ–Є –≤ —Н–њ–Є–≥–∞—Б—В—А–Є–Є –љ–∞—В–Њ—Й–∞–Ї [8]. –Я—А–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —Н–≤–∞–Ї—Г–∞—В–Њ—А–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –ґ–µ–ї—Г–і–Ї–∞ –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –і–Є—Б–њ–µ–њ—В–Є—З–µ—Б–Ї–Є—Е –ґ–∞–ї–Њ–± –Љ–Њ–ґ–µ—В –±—Л—В—М –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М – –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б—В–µ–љ–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –Ї —А–∞—Б—В—П–ґ–µ–љ–Є—О, –Ї–Њ—В–Њ—А–∞—П —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –Є—Б—В–Є–љ–љ—Л–Љ –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Љ–µ—Е–∞–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б—В–µ–љ–Ї–Є –Є–ї–Є —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —В–Њ–љ—Г—Б–Њ–Љ —Д—Г–љ–і–∞–ї—М–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –ґ–µ–ї—Г–і–Ї–∞.
–Т—Б–µ —Д–Њ—А–Љ—Л —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Ц–Ъ–Ґ –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –њ—Б–Є—Е–Њ—Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ –Є–ї–Є –±–Є–Њ—Б–Њ—Ж–Є–∞–ї—М–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ. –Я—Б–Є—Е–Њ—В—А–∞–≤–Љ–Є—А—Г—О—Й–Є–µ –Є —Б—В—А–µ—Б—Б–Њ–≤—Л–µ —Б–Є—В—Г–∞—Ж–Є–Є —З–∞—Й–µ —А–µ–∞–ї–Є–Ј—Г—О—В—Б—П –≤ –≤–Є–і–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Г –і–µ—В–µ–є, –Є–Љ–µ—О—Й–Є—Е –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –њ–µ—А–Є–љ–∞—В–∞–ї—М–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј, —А–µ–Ј–Є–і—Г–∞–ї—М–љ–Њ––Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –¶–Э–°, –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є, –∞–ї–ї–µ—А–≥–Є—О [10]. –Ю–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–µ —Н—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –і–ї—П —А–∞–Ј–≤–Є—В–Є—П –°–Ф, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –і–µ—В—Б–Ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ, –Є–Љ–µ—О—В –њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л–µ –Є–љ–≤–∞–Ј–Є–Є (–Ї–Є—И–µ—З–љ—Л–µ –≥–µ–ї—М–Љ–Є–љ—В–Њ–Ј—Л –Є –ї—П–Љ–±–ї–Є–Њ–Ј).
–Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Є—З–Є–љ—Л –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ—В–Њ—А–Є–Ї–Є –Є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Ї–Њ—В–Њ—А—Л–µ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—В—Б—П –њ—А–Є –§–Ф. –Т–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—В —Б–Њ—З–µ—В–∞–љ–љ—Л–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Њ—В–і–µ–ї–Њ–≤ –Ц–Ъ–Ґ, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ—О—В –Љ–µ—Б—В–Њ –≤ 2/3 —Б–ї—Г—З–∞–µ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Я–Њ–њ—Л—В–Ї–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М —Н—В–Є –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Ї–∞–Ї —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є–ї–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –њ—А–Є–≤–Њ–і—П—В –Ї –њ–Њ–ї–Є–њ—А–∞–≥–Љ–∞–Ј–Є–Є –Є –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ–µ –ї–µ—З–µ–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –ґ–∞–ї–Њ–± – –і–Њ 1 –≥–Њ–і–∞ —Н—В–Њ —З–∞—Й–µ –≤—Б–µ–≥–Њ —Б—А—Л–≥–Є–≤–∞–љ–Є—П, –Њ—В 3 –і–Њ 8 –ї–µ—В – —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–∞—П —А–≤–Њ—В–∞, –∞ –≤ 8–12 –ї–µ—В – –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–µ –±–Њ–ї–Є –Є –і–Є—Б–њ–µ–њ—В–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ [31].
–£ –і–µ—В–µ–є –Њ–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —П–≤–ї—П–µ—В—Б—П –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Ц–Ъ–Ґ —Б –≤–∞–≥–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В—М—О. –Ъ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є—П–Љ, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В —Б—Г–і–Є—В—М –Њ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–Є –њ–∞—А–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є –Ц–Ъ–Ґ, –Њ—В–љ–Њ—Б—П—В—Б—П —Г—Б–Є–ї–µ–љ–љ–Њ–µ —Б–ї—О–љ–Њ–Њ—В–і–µ–ї–µ–љ–Є–µ, —Б–Є–Љ–њ—В–Њ–Љ—Л –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –Ї–Є—Б–ї–Њ—В–љ–Њ—Б—В–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–Ї–∞, –Є–Ј–±—Л—В–Њ—З–љ–∞—П –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї–∞ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –Є —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї –њ–Њ–љ–Њ—Б–∞–Љ, —В–Њ—И–љ–Њ—В–∞, –њ—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –±–Њ–ї–Є –≤ –ґ–Є–≤–Њ—В–µ. –Я—А–Є–Ј–љ–∞–Ї–∞–Љ–Є —Б–Є–Љ–њ–∞—В–Є–Ї–Њ—В–Њ–љ–Є–Є —Б—З–Є—В–∞—О—В—Б—П —Б—Г—Е–Њ—Б—В—М –≤–Њ —А—В—Г, –љ–Њ—О—Й–Є–µ –±–Њ–ї–Є –≤ –ґ–Є–≤–Њ—В–µ –Є –∞—В–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Ј–∞–њ–Њ—А—Л. –Ш–љ—В–µ–≥—А–Є—А–Њ–≤–∞–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–Є—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–µ –Њ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П—Е –≤ —Б–Є—Б—В–µ–Љ–µ –Ц–Ъ–Ґ [11]. –°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ—Г –љ–∞–Љ–Є –∞–љ–∞–ї–Є–Ј—Г, –њ–∞—А–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–∞—П —А–µ–∞–Ї—Ж–Є—П –њ—А–Є –°–Ф –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г –і–µ—В–µ–є –≤ 2 —А–∞–Ј–∞ —З–∞—Й–µ, —З–µ–Љ —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–∞—П [2].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е –ї–Є—В–µ—А–∞—В—Г—А—Л –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ —Н—В–Є–Њ–ї–Њ–≥–Є—П –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј –Њ–і–љ–Њ–≥–Њ –Є–Ј —Б–∞–Љ—Л—Е —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є, –Ї–∞–Ї–Є–Љ —П–≤–ї—П–µ—В—Б—П –§–Ф, –і–Њ –Ї–Њ–љ—Ж–∞ –љ–µ —П—Б–љ—Л, –≤–µ—А–Њ—П—В–љ–Њ, —Н—В–Њ –≥–µ—В–µ—А–Њ–≥–µ–љ–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Є —Г –Ї–∞–ґ–і–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –Љ–Њ–ґ–µ—В –њ—А–µ–Њ–±–ї–∞–і–∞—В—М —В–Њ—В –Є–ї–Є –Є–љ–Њ–є —Н—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є —Д–∞–Ї—В–Њ—А.
–Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–Є –љ–∞–ї–Є—З–Є–Є –°–Ф –≤—А–∞—З –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –Ї–Њ–љ—В–∞–Ї—В–∞ —А–∞—Б–њ–Њ–ї–∞–≥–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ –Є –≤ –њ–ї–∞–љ–Њ–≤–Њ–Љ –њ–Њ—А—П–і–Ї–µ. –Ю–і–љ–∞–Ї–Њ –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –°–Ф –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–Ј–≤–∞–љ —Б–Њ—Б—В–Њ—П–љ–Є—П–Љ–Є, —В—А–µ–±—Г—О—Й–Є–Љ–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–µ–Њ—В–ї–Њ–ґ–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є. –Ф–ї—П —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –љ–∞–ї–Є—З–Є–µ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е «—Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —В—А–µ–≤–Њ–≥–Є», –Ї –Ї–Њ—В–Њ—А—Л–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –Є–љ—В–µ–љ—Б–Є–≤–љ–∞—П –Є –љ–µ–Ї—Г–њ–Є—А—Г—О—Й–∞—П—Б—П –±–Њ–ї—М, –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є—П, –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –њ–Њ—В–µ—А—П –≤–µ—Б–∞, –њ—А–Є–Ј–љ–∞–Ї–Є –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П. –Ф–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Є–Ј —Н—В–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –∞ —З—В–Њ–±—Л –Њ—Ж–µ–љ–Є—В—М –љ–∞–ї–Є—З–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е –і–≤—Г—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –∞–љ–∞–ї–Є–Ј–∞ –Ї—А–Њ–≤–Є –љ–∞ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ, —Н—А–Є—В—А–Њ—Ж–Є—В—Л –Є –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–Ј [8].
–Э–µ —Г–Љ–∞–ї—П—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤—Л—П–≤–ї–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —В—А–µ–≤–Њ–≥–Є –њ—А–Є –Ї–∞–ґ–і–Њ–Љ –Њ—Б–Љ–Њ—В—А–µ, –љ—Г–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Њ–љ–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Б–Ї—А–Є–љ–Є–љ–≥—Г –љ–µ —Б–∞–Љ–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –∞ –Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Ф—А—Г–≥–Њ–є –Ї—А–∞–є–љ–Њ—Б—В—М—О —П–≤–ї—П–µ—В—Б—П –њ–Њ–і—Е–Њ–і, –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞—О—Й–Є–є —Б–њ–ї–Њ—И–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–∞—Б–µ–ї–µ–љ–Є—П —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Є–љ–≤–∞–Ј–Є–≤–љ—Л—Е –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –і–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П «–љ–µ–Љ—Л—Е» —Б–ї—Г—З–∞–µ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –≠–У–Ф–° –≤ –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –≥—А—Г–њ–њ–∞—Е —Б –љ–Є–Ј–Ї–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О –ѓ–С –≤–µ–і–µ—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–Ї–ї—О—З–µ–љ–Є–є. –§–∞–Ї—В–Њ—А–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —Б–љ–Є–Ј–Є—В—М —В–Њ—З–љ–Њ—Б—В—М —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —П–≤–ї—П—О—В—Б—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–є –Њ–њ—Л—В –Є –љ–∞–≤—Л–Ї–Є –≤—А–∞—З–∞, –Ј–∞–≥—А—Г–ґ–µ–љ–љ–Њ—Б—В—М —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–∞–±–Є–љ–µ—В–∞, –љ–µ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ–∞—П –њ–Њ–і–≥–Њ—В–Њ–≤–Ї–∞ –±–Њ–ї—М–љ–Њ–≥–Њ –Ї –њ—А–Њ—Ж–µ–і—Г—А–µ, –љ–µ—Б–Њ–≤–µ—А—И–µ–љ–љ–Њ–µ –Њ–±–Њ—А—Г–і–Њ–≤–∞–љ–Є–µ. –Х—Й–µ –Њ–і–љ–Є–Љ –∞—Б–њ–µ–Ї—В–Њ–Љ, –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—Й–Є–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≠–У–Ф–° –≤ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–∞—Е —Б –љ–Є–Ј–Ї–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О –њ–∞—В–Њ–ї–Њ–≥–Є–Є, —П–≤–ї—П–µ—В—Б—П —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–∞—П –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–∞–Ї–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞. –°–њ–ї–Њ—И–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤ –љ–µ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –≥—А—Г–њ–њ–∞—Е –і–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –ѓ–С —А–µ–Ј–Ї–Њ –њ–Њ–≤—Л—И–∞–µ—В –Ј–∞—В—А–∞—В—Л –љ–∞ –≤—Л—П–≤–ї–µ–љ–Є–µ –Њ–і–љ–Њ–≥–Њ —Б–ї—Г—З–∞—П.
–Т—Л—Е–Њ–і –Є–Ј —Б–ї–Њ–ґ–Є–≤—И–µ–є—Б—П —Б–Є—В—Г–∞—Ж–Є–Є —Б–Њ—Б—В–Њ–Є—В –≤ –њ–Њ–≤—Л—И–µ–љ–Є–Є –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–≥–Њ –≤—Л—П–≤–ї–µ–љ–Є—П —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л—Е –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–≤—Л—И–∞—О—В –∞–њ—А–Є–Њ—А–љ—Г—О (–њ—А–µ—В–µ—Б—В–Њ–≤—Г—О) –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Њ—В–љ–Њ—Б—П—Й–Є—Е—Б—П –Ї –≥—А—Г–њ–њ–µ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –і–Є—Б–њ–µ–њ—Б–Є–Є, –Є —Б–ї—Г–ґ–∞—В —Ж–µ–ї—П–Љ –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–±–Њ—А–∞ –њ–µ—А–µ–і –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–Љ–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—А–Њ–њ—А–Є—П—В–Є—П –њ—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Њ–±—А–∞—Й–µ–љ–Є–Є –і–µ—В–µ–є —Б –°–Ф —А–∞–Ј–і–µ–ї—П—О—В—Б—П –љ–∞ –і–≤–∞ —Н—В–∞–њ–∞: –њ–µ—А–≤—Л–є —Б–Њ—Б—В–Њ–Є—В –≤ –≤—Л—П–≤–ї–µ–љ–Є–Є –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –і–Є—Б–њ–µ–њ—Б–Є–Є, –Є—Б—Е–Њ–і—П –Є–Ј —Б–Ї—А–Є–љ–Є—А—Г—О—Й–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —В–µ—Б—В–Њ–≤ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –µ–µ –љ–∞–ї–Є—З–Є—П, –Є –≤ –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Є–Љ –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ –≠–У–Ф–°, –£–Ч–Ш, —А–µ–љ—В–≥–µ–љ–Њ–Ї–Њ–љ—В—А–∞—Б—В–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤, –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —В–µ—Б—В–Њ–≤. –Э–∞ –≤—В–Њ—А–Њ–Љ —Н—В–∞–њ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–µ –≤—Л—П–≤–ї–µ–љ–∞ –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–∞—П –і–Є—Б–њ–µ–њ—Б–Є—П, —Г—В–Њ—З–љ—П–µ—В—Б—П —Д–Њ—А–Љ–∞ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –†–Є–Љ—Б–Ї–Є–Љ–Є –Ъ—А–Є—В–µ—А–Є—П–Љ–Є III –Є, –≤ –љ—Г–ґ–љ—Л—Е —Б–ї—Г—З–∞—П—Е, —Б –њ–Њ–Љ–Њ—Й—М—О –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Є–Ј—Г—З–∞—О—В—Б—П –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–µ –Є —Б–µ–Ї—А–µ—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П, –Є—Б—Б–ї–µ–і—Г—О—В—Б—П –љ–µ–≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ—Л–µ –њ—А–Є—З–Є–љ—Л –і–Є—Б–њ–µ–њ—Б–Є–Є. –° —Г—З–µ—В–Њ–Љ –≤—Л—Б–Њ–Ї–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –°–Ф –≤–µ–і–µ–љ–Є–µ —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –і–Њ–ї–ґ–љ–Њ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—В—М—Б—П –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ.
–Э–∞–њ—А–Є–Љ–µ—А, –і–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П –∞–њ—А–Є–Њ—А–љ–Њ–є (–њ—А–µ—В–µ—Б—В–Њ–≤–Њ–є) –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –ѓ–С –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Њ—В–±–Њ—А–∞ –і–ї—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –і–ї—П —З–µ–≥–Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ (–њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤—Л–є –≤–Њ–Ј—А–∞—Б—В, –Љ—Г–ґ—Б–Ї–Њ–є –њ–Њ–ї, –Њ—В—П–≥–Њ—Й–µ–љ–љ–∞—П –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В—М) –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є. –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –ѓ–С –Љ–Њ–ґ–љ–Њ –њ—А–µ–і—Б—В–∞–≤–Є—В—М –Ї–∞–Ї –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —В–µ—Б—В–Њ–≤ (—Б–Ї—А–Є–љ–Є–љ–≥) –Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Т—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —В–µ—Б—В–∞–Љ–Є —П–≤–ї—П—О—В—Б—П –≥–Њ–ї–Њ–і–љ—Л–µ, –љ–Њ—З–љ—Л–µ –±–Њ–ї–Є, —Б–Є–ї—М–љ—Л–µ —А–µ–і–Ї–Є–µ –±–Њ–ї–Є, –Є–Ј–ґ–Њ–≥–∞ –Є –Њ—В—А—Л–ґ–Ї–∞ –Ї–Є—Б–ї—Л–Љ. –Э–∞–ї–Є—З–Є–µ —Е–Њ—В—П –±—Л –Њ–і–љ–Њ–≥–Њ –Є–Ј —Н—В–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –≠–У–Ф–°, –≤ —Б–ї—Г—З–∞–µ –Њ—В—Б—Г—В—Б—В–≤–Є—П –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–Њ–њ—А–Њ—Б –Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є–Є —Б–ї–µ–і—Г–µ—В —А–µ—И–Є—В—М –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П —Б —Г—З–µ—В–Њ–Љ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ H. pylori —Г –і–µ—В–µ–є —Б –°–Ф —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–∞ –≤ —В–µ—Е —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ –µ–≥–Њ —Н—А–∞–і–Є–Ї–∞—Ж–Є—П —А–µ–≥–ї–∞–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–∞ –і–µ–є—Б—В–≤—Г—О—Й–Є–Љ–Є —Б—В–∞–љ–і–∞—А—В–∞–Љ–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –Ь–∞–∞—Б—В—А–Є—Е—В—Б–Ї–Є–Љ –Ї–Њ–љ—Б–µ–љ—Б—Г—Б–Њ–Љ. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї –≠–У–Ф–° –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –і–Њ–ї–ґ–љ–∞ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—М—Б—П –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –љ–∞–Є–±–Њ–ї–µ–µ –і–Њ—Б—В—Г–њ–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –Я–¶–† –≤ –Ї—А–Њ–≤–Є, —Б–ї—О–љ–µ –Є –Ї–∞–ї–µ, –∞ —В–∞–Ї–ґ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Ш–§–Р –Ї H. pylori, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ–Њ–і–≤–µ—А–≥–∞–µ—В—Б—П —Б–Њ–Љ–љ–µ–љ–Є—О. –Я–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є H. pylori —Б—З–Є—В–∞—О—В—Б—П –≤–њ–µ—А–≤—Л–µ –≤—Л—П–≤–ї–µ–љ–љ–∞—П –ѓ–С –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –Є–ї–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–µ —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ –њ—А–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–Љ —В–µ—Б—В–µ –љ–∞ H. pylori – –Њ—В—П–≥–Њ—Й–µ–љ–љ–∞—П –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В—М –њ–Њ —А–∞–Ї—Г –ґ–µ–ї—Г–і–Ї–∞ –Є–ї–Є –ї–Є–Љ—Д–Њ–Љ–µ –ґ–µ–ї—Г–і–Ї–∞, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [12].
–¶–µ–ї—П–Љ–Є —Г—В–Њ—З–љ–µ–љ–Є—П —Д–Њ—А–Љ—Л —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —П–≤–ї—П—О—В—Б—П –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –њ–µ—А–µ—З–љ—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –Я—А–Є –љ–∞–ї–Є—З–Є–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –±–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –£–Ч–Ш –њ—А–Њ–≤–Њ–і–Є—В—Б—П —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –ґ–µ–ї—З–љ–Њ–≥–Њ –њ—Г–Ј—Л—А—П, –∞ –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–∞ –ґ–µ–ї—З–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Њ –і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–µ –Ј–Њ–љ–і–Є—А–Њ–≤–∞–љ–Є–µ. –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–Ї–ї—О—З–∞–µ—В—Б—П –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є (–Њ–±—Й–Є–є –±–µ–ї–Њ–Ї, –∞–ї–∞–љ–Є–љ–Њ–≤–∞—П –∞–Љ–Є–љ–Њ—В—А–∞–љ—Б—Д–µ—А–∞–Ј–∞, –±–Є–ї–Є—А—Г–±–Є–љ).
–Э–∞–Є–±–Њ–ї—М—И—Г—О —Б–ї–Њ–ґ–љ–Њ—Б—В—М –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–Љ –њ–ї–∞–љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –§–Р–С, —В.–Ї. –Ї—А–Њ–Љ–µ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ–љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –њ–Њ—З–µ–Ї, —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤, –Ї–Њ—Б—В–љ–Њ––Љ—Л—И–µ—З–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞. –Я–Њ—Н—В–Њ–Љ—Г –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —В–∞–Ї–Є—Е –і–µ—В–µ–є –≤–Ї–ї—О—З–∞—О—В—Б—П –∞–љ–∞–ї–Є–Ј –Љ–Њ—З–Є, –£–Ч–Ш –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є—П –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–∞ –Є–ї–Є —Г—А–Њ–ї–Њ–≥–∞.
–Х—Б–ї–Є –°–Ф —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –і–Є–∞—А–µ–µ–є –Є–ї–Є –Љ–µ—В–µ–Њ—А–Є–Ј–Љ–Њ–Љ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ—А–Є –°–†–Ъ, –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є, —Н–Њ–Ј–Є–љ–Њ—Д–Є–ї–Є–µ–є –Є–ї–Є –∞–љ–µ–Љ–Є–µ–є, –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –∞—Б—В–µ–љ–Є–Ј–∞—Ж–Є–µ–є, –Ї —Н—В–Њ–Љ—Г –њ–µ—А–µ—З–љ—О –і–Њ–±–∞–≤–ї—П–µ—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ї–∞–ї–∞ –љ–∞ —П–є—Ж–∞ –≥–µ–ї—М–Љ–Є–љ—В–Њ–≤ –Є —Ж–Є—Б—В—Л –ї—П–Љ–±–ї–Є–є. –Ф–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –µ–≥–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М —В–Њ–ї—М–Ї–Њ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Љ–µ—В–Њ–і–Њ–≤ –Њ–±–Њ–≥–∞—Й–µ–љ–Є—П –Є–ї–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Ї–∞–ї–Њ–≤–Њ–≥–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞, –љ–∞–њ—А–Є–Љ–µ—А, –њ–Њ –§—О–ї–ї–µ–±–Њ—А–љ—Г, –®—Г–ї—М–Љ–∞–љ—Г –Є–ї–Є —Д–Њ—А–Љ–∞–ї–Є–љ–—Н—Д–Є—А–љ–Њ–µ –Њ–±–Њ–≥–∞—Й–µ–љ–Є–µ. –°–њ–ї–Њ—И–љ—Л–µ –љ–µ–≤—Л–±–Њ—А–Њ—З–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–µ—В–Њ–і–Њ–Љ –љ–∞—В–Є–≤–љ–Њ–≥–Њ –Љ–∞–Ј–Ї–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –љ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В, –љ–Њ –Є —Б–љ–Є–ґ–∞—О—В –≤—Л—П–≤–ї—П–µ–Љ–Њ—Б—В—М –≥–µ–ї—М–Љ–Є–љ—В–Њ–Ј–Њ–≤ –Є –ї—П–Љ–±–ї–Є–Њ–Ј–∞. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–є –Ї–Є—И–µ—З–љ–Є–Ї–∞ –≤—А–∞—З —В–∞–Ї–ґ–µ –Њ–±—П–Ј–∞–љ –Є—Б–Ї–ї—О—З–Є—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є–µ —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Љ–∞–ї—М–∞–±—Б–Њ—А–±—Ж–Є–Є, –љ–∞–њ—А–Є–Љ–µ—А –ї–∞–Ї—В–∞–Ј–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Є–ї–Є —Ж–µ–ї–Є–∞–Ї–Є—О, —З—В–Њ —В—А–µ–±—Г–µ—В –њ—А–Њ–≤–µ–і–µ–љ–Є—П –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б–Ї—А–Є–љ–Є—А—Г—О—Й–µ–≥–Њ –Љ–µ—В–Њ–і–∞ –Ї–Њ–њ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–±—Л –љ–∞ —А–µ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ —Г–≥–ї–µ–≤–Њ–і—Л.
–Ф—А—Г–≥–Є–Љ –∞—Б–њ–µ–Ї—В–Њ–Љ –≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –њ—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Њ–±—А–∞—Й–µ–љ–Є–Є —П–≤–ї—П–µ—В—Б—П –∞–і–µ–Ї–≤–∞—В–љ–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П –Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П, –Ї–Њ—В–Њ—А–∞—П –і–Њ–ї–ґ–љ–∞ –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П —Б —Г—З–µ—В–Њ–Љ —Д–Њ—А–Љ—Л —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞. –Я—А–Є –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–Њ–Љ –≤–∞—А–Є–∞–љ—В–µ –§–Ф –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–Њ–Ї–Є–љ–µ—В–Є–Ї–Њ–≤ – –±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –і–Њ–њ–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–і–Њ–Љ–њ–µ—А–Є–і–Њ–љ) –Є –Љ–∞–≥–љ–Є–є—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –∞–љ—В–∞—Ж–Є–і–Њ–≤. –Ъ—Г—А—Б –ї–µ—З–µ–љ–Є—П –Њ–±—Л—З–љ–Њ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 2 –љ–µ–і., –і–Њ–Ј–∞ –і–Њ–Љ–њ–µ—А–Є–і–Њ–љ–∞ – 5–10 –Љ–≥ 3–4 —А./ —Б—Г—В. –Ј–∞ 20 –Љ–Є–љ. –і–Њ –µ–і—Л, –∞–љ—В–∞—Ж–Є–і—Л –і–∞—О—В—Б—П —З–µ—А–µ–Ј —З–∞—Б –њ–Њ—Б–ї–µ –µ–і—Л –њ–Њ 10–15 –Љ–ї. –Я—А–Є —Б–Є–љ–і—А–Њ–Љ–µ —Н–њ–Є–≥–∞—Б—В—А–∞–ї—М–љ–Њ–є –±–Њ–ї–Є —Г –Э–†––љ–µ–≥–∞—В–Є–≤–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ —Н–љ–Ї–µ—Д–∞–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–є –њ—А–µ–њ–∞—А–∞—В —В—А–Є–Љ–µ–±—Г—В–Є–љ, –∞–љ—В–Є—Б–µ–Ї—А–µ—В–Њ—А–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Є Al–—Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –∞–љ—В–∞—Ж–Є–і—Л, –∞ –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є H. pylori –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—Б—П –∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–∞—П —В–µ—А–∞–њ–Є—П. –£ –і–µ—В–µ–є –і–Њ 12 –ї–µ—В –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –∞–љ—В–Є—Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П–µ—В—Б—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –Ь1–—Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Ї –њ–Є—А–µ–љ–Ј–µ–њ–Є–љ, –Ї–Њ—В–Њ—А—Л–є –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –≤ –і–Њ–Ј–µ –і–Њ 1–1,5 –Љ–≥/–Ї–≥/—Б—Г—В., —Г –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Е–Њ—А–Њ—И–Є–є —Н—Д—Д–µ–Ї—В –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —А–∞–±–µ–њ—А–∞–Ј–Њ–ї–∞ –≤ –і–Њ–Ј–µ 10 –Љ–≥/—Б—Г—В. –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ.
–Т –Ї–Њ–Љ–њ–ї–µ–Ї—Б —В–µ—А–∞–њ–Є–Є –њ—А–Є —Б–Є–љ–і—А–Њ–Љ–µ –±–Є–ї–Є–∞—А–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –і–Њ–ї–ґ–љ—Л –≤—Е–Њ–і–Є—В—М —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –і–µ–є—Б—В–≤—Г—О—Й–Є–µ –љ–∞ –≥–ї–∞–і–Ї—Г—О –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Г –ґ–µ–ї—З–µ–≤—Л–і–µ–ї–Є—В–µ–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л (–≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і, –≥–Є–Љ–µ–Ї—А–Њ–Љ–Њ–љ, –Љ–µ–±–µ–≤–µ—А–Є–љ), –Є–ї–Є –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є (–і—А–Њ—В–∞–≤–µ—А–Є–љ, –њ–∞–њ–∞–≤–µ—А–Є–љ), –ґ–µ–ї—З–µ–≥–Њ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞.
–Ы–µ—З–µ–љ–Є–µ –°–†–Ъ –≤–Ї–ї—О—З–∞–µ—В –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Ї–Є—И–µ—З–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–Љ–µ–±–µ–≤–µ—А–Є–љ, –њ–Є–љ–∞–≤–µ—А–Є–љ–∞ –±—А–Њ–Љ–Є–і), –њ—А–Њ–±–Є–Њ—В–Є–Ї–Њ–≤, –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ —Б–ї–∞–±–Є—В–µ–ї—М–љ—Л—Е –Є–ї–Є –∞–љ—В–Є–і–Є–∞—А–µ–є–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л—Е —Б —Г—З–µ—В–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–∞—А–Є–∞–љ—В–∞. –Ь–µ–±–µ–≤–µ—А–Є–љ —П–≤–ї—П–µ—В—Б—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –Љ–Є–Њ—В—А–Њ–њ–љ—Л–Љ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–Љ. –Ю–љ –њ–Њ–љ–Є–ґ–∞–µ—В —В–Њ–љ—Г—Б –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –±–Є–ї–Є–∞—А–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Є –Ї–Є—И–µ—З–љ–Є–Ї–∞, –љ–µ –≤–ї–Є—П—П –љ–∞ –Є—Е –љ–Њ—А–Љ–∞–ї—М–љ—Г—О –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї—Г. –Я–Њ—Н—В–Њ–Љ—Г –µ–≥–Њ –Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М –њ—А–Є –Ј–∞–њ–Њ—А–∞—Е, –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П—Е. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –њ–µ–і–Є–∞—В—А–Є–Є –Њ–≥—А–∞–љ–Є—З–µ–љ–Њ —В–µ–Љ, —З—В–Њ –Є–Љ–µ—О—Й–∞—П—Б—П –≤ –њ—А–Њ–і–∞–ґ–µ –Ї–∞–њ—Б—Г–ї—М–љ–∞—П —Д–Њ—А–Љ–∞ (200 –Љ–≥) –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Ї –њ—А–Є–µ–Љ—Г —Г –і–µ—В–µ–є. –Ф–Њ–Ј–∞ –і–ї—П –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –њ–Њ 1 –Ї–∞–њ—Б—Г–ї–µ 1–2 —А./—Б—Г—В. –Ї—Г—А—Б–Њ–Љ –і–Њ 4 –љ–µ–і. –Я—А–Њ–±–Є–Њ—В–Є–Ї–Є –Є –њ—А–µ–њ–∞—А–∞—В—Л –њ–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ—Л –њ—А–Є –≤—Б–µ—Е –≤–∞—А–Є–∞–љ—В–∞—Е –°–†–Ъ, —В.–Ї. –љ–∞—А—Г—И–µ–љ–Є–µ –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ –њ–µ—А–µ–≤–∞—А–Є–≤–∞—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Є —Е–Є–Љ–Є–Ј–Љ–∞ –Ї–Є—И–µ—З–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ.
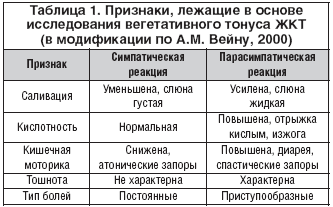
–Я—А–Є –ї—О–±—Л—Е —Д–Њ—А–Љ–∞—Е –§–† –Ц–Ъ–Ґ —Е–Њ—А–Њ—И–Є–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –≤ –њ–ї–∞–љ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –і–∞–µ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ь–—Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Ї–Њ–≤. –Ґ.–Ї. –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Њ–њ–Њ—Б—А–µ–і—Г–µ—В—Б—П —З–µ—А–µ–Ј –љ–µ—А–≤–љ—Л–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П –≤–∞–≥—Г—Б–∞, —В–Њ –Є —Н—Д—Д–µ–Ї—В –Ј–∞–≤–Є—Б–Є—В –≤ –±–Њ–ї—М—И–µ–є –Љ–µ—А–µ –Њ—В –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–Њ—В–љ–Њ—И–µ–љ–Є–є –≤ –Ц–Ъ–Ґ. –Я—А–Є—З–µ–Љ –і–µ–є—Б—В–≤–Є–µ –•–Ы —В–µ–Љ —Б–Є–ї—М–љ–µ–µ, —З–µ–Љ –≤—Л—И–µ —В–Њ–љ—Г—Б –±–ї—Г–ґ–і–∞—О—Й–µ–≥–Њ –љ–µ—А–≤–∞. –Ф–ї—П —В–Њ–≥–Њ —З—В–Њ–±—Л –Њ–±–ї–µ–≥—З–Є—В—М –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ—Г –≤—А–∞—З—Г –≤—Л—П–≤–ї–µ–љ–Є–µ –Є —Г—В–Њ—З–љ–µ–љ–Є–µ —Д–Њ—А–Љ—Л –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–≥–Њ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Ц–Ъ–Ґ, –Љ—Л –њ—А–µ–і–ї–∞–≥–∞–µ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —В–∞–±–ї–Є—Ж—Г –Р.–Ь. –Т–µ–є–љ–∞ –≤ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є (—В–∞–±–ї. 1).
–Я–Њ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є—О —Г –њ–∞—Ж–Є–µ–љ—В–∞ —В–µ—Е –Є–ї–Є –Є–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Љ–Њ–ґ–љ–Њ —Б—Г–і–Є—В—М –Њ –љ–∞–ї–Є—З–Є–Є –Є —В–Є–њ–µ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –і–Є—Б—В–Њ–љ–Є–Є, –љ–∞–Ј–љ–∞—З–∞—В—М —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –≤–µ–≥–µ—В–Њ—В—А–Њ–њ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –≤–µ–≥–µ—В–Њ—В—А–Њ–њ–љ—Л–Љ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–Љ, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–Љ –≤ –њ–µ–і–Є–∞—В—А–Є–Є, —П–≤–ї—П–µ—В—Б—П –≥–Є–Њ—Б—Ж–Є–љ–∞ –±—Г—В–Є–ї–±—А–Њ–Љ–Є–і (–С—Г—Б–Ї–Њ–њ–∞–љ®). –≠—В–Њ –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї, –Њ–±–ї–∞–і–∞—О—Й–Є–є –і–≤–Њ–є–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, –∞ –Є–Љ–µ–љ–љ–Њ: –њ—А—П–Љ—Л–Љ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Ј–∞ —Б—З–µ—В –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є—П –Ь3–—Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –Њ—А–≥–∞–љ–Њ–≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Є –∞–љ—В–Є—Б–µ–Ї—А–µ—В–Њ—А–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, —Б–љ–Є–ґ–∞—П (–љ–µ –њ–Њ–і–∞–≤–ї—П—П) —Б–µ–Ї—А–µ—Ж–Є—О –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј –Ј–∞ —Б—З–µ—В –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є—П –Э–—Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –≥–∞–љ–≥–ї–Є–µ–≤. –С–ї–Њ–Ї–∞–і–∞ –Ь–—Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Њ–±—К—П—Б–љ—П–µ—В—Б—П —В–µ–Љ, —З—В–Њ –С—Г—Б–Ї–Њ–њ–∞–љ –Є–љ–≥–Є–±–Є—А—Г–µ—В –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –Љ–µ–і–Є–∞—В–Њ—А–∞ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞ (Ach) —Б –Ь–—Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є, —В.–µ –і–µ–є—Б—В–≤—Г–µ—В –љ–∞ –њ–µ—А–≤–Њ–Љ —Н—В–∞–њ–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Б–њ–∞–Ј–Љ–∞, —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В –µ–≥–Њ –±—Л—Б—В—А—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В: —Г–ґ–µ —З–µ—А–µ–Ј 15 –Љ–Є–љ. –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ —В–∞–±–ї–µ—В–Ї–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–є [Mueller–Lissner S., Schaefer E. Symptoms and their interpretation in patients self–treating abdominal cramping and pain with a spasmolytic // Pharmacol. Pharm 2011. Vol. 2. P. 82–87]. –С—Г–і—Г—З–Є —З–µ—В–≤–µ—А—В–Є—З–љ—Л–Љ –∞–Љ–Љ–Њ–љ–Є–µ–≤—Л–Љ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ, –С—Г—Б–Ї–Њ–њ–∞–љ –љ–µ –њ—А–Њ–љ–Є–Ї–∞–µ—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А, –њ–Њ—Н—В–Њ–Љ—Г –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–љ—В–Є—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–∞ –¶–Э–°, –∞ –Ј–љ–∞—З–Є—В, —П–≤–ї—П–µ—В—Б—П –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, —З—В–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ –≤ –њ–µ–і–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –С—Г—Б–Ї–Њ–њ–∞–љ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Г—Б—В—А–∞–љ—П–µ—В —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Є–µ –±–Њ–ї–Є –≤–Њ –≤—Б–µ—Е –Њ—В–і–µ–ї–∞—Е –Ц–Ъ–Ґ, –њ–Њ—Н—В–Њ–Љ—Г —Б–њ–µ–Ї—В—А –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ—З–µ–љ—М –≤–µ–ї–Є–Ї – –Ї–Є—И–µ—З–љ–∞—П, –њ–Њ—З–µ—З–љ–∞—П –Є –ґ–µ–ї—З–љ–∞—П –Ї–Њ–ї–Є–Ї–Є, —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–∞—П –і–Є—Б–Ї–Є–љ–µ–Ј–Є—П –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В, –њ–Є–ї–Њ—А–Њ—Б–њ–∞–Ј–Љ, —П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –≤ —Д–∞–Ј–µ –Њ–±–Њ—Б—В—А–µ–љ–Є—П (–≤ —Б–Њ—Б—В–∞–≤–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є). –С—Г—Б–Ї–Њ–њ–∞–љ –≤—Л–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ –≤–Є–і–µ —В–∞–±–ї–µ—В–Њ–Ї –Є —Б—Г–њ–њ–Њ–Ј–Є—В–Њ—А–Є–µ–≤ –њ–Њ 10 –Љ–≥, –Љ–Њ–ґ–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П –і–µ—В—П–Љ —Б 6 –ї–µ—В.
–Ф–ї—П —Г—Б–њ–µ—И–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –љ—Г–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –љ–∞–ї–Є—З–Є–µ –љ–µ–≤—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–µ–Њ–±–ї–∞–і–∞—О—Й–µ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (—В—А–µ–≤–Њ–ґ–љ–Њ–≥–Њ, –∞—Б—В–µ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ) –≤—А–∞—З –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ –Љ–Њ–ґ–µ—В –љ–∞–Ј–љ–∞—З–Є—В—М —Б–µ–і–∞—В–Є–≤–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Є–ї–Є –∞–і–∞–њ—В–Њ–≥–µ–љ—Л –ї–Є–±–Њ –љ–∞–њ—А–∞–≤–Є—В—М –њ–∞—Ж–Є–µ–љ—В–∞ –љ–∞ –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є—О –Ї –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–µ–≤—В—Г –Є–ї–Є –љ–µ–≤—А–Њ–ї–Њ–≥—Г. –Т –њ–µ–і–Є–∞—В—А–Є–Є –Њ—В–і–∞–µ—В—Б—П –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ —Б—А–µ–і—Б—В–≤–∞–Љ —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П, —В–∞–Ї–Є–Љ –Ї–∞–Ї –Љ—П—В–∞ –њ–µ—А–µ—З–љ–∞—П, –Љ—П—В–∞ –ї–Є–Љ–Њ–љ–љ–∞—П, –≤–∞–ї–µ—А–Є–∞–љ–∞, –Њ–±–ї–∞–і–∞—О—Й–Є–Љ —Г—Б–њ–Њ–Ї–∞–Є–≤–∞—О—Й–Є–Љ –Є —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ.
–Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –њ—А–Є –°–Ф —Б–Њ—Б—В–∞–≤–ї—П–µ—В 2 –љ–µ–і., –Њ–і–љ–∞–Ї–Њ –µ—Й–µ –і–Њ –µ–≥–Њ –љ–∞—З–∞–ї–∞, —Б–і–µ–ї–∞–≤ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П, –≤—А–∞—З –і–Њ–ї–ґ–µ–љ –њ—А–µ–і—Г–њ—А–µ–і–Є—В—М —А–µ–±–µ–љ–Ї–∞ –Є —А–Њ–і–Є—В–µ–ї–µ–є, –≤ –Ї–∞–Ї–Є—Е —Б–ї—Г—З–∞—П—Е –Њ–љ–Є –і–Њ–ї–ґ–љ—Л –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ –Њ–±—А–∞—В–Є—В—М—Б—П –Ј–∞ –њ–Њ–Љ–Њ—Й—М—О. –Я–Њ –Ј–∞–≤–µ—А—И–µ–љ–Є–Є –ї–µ—З–µ–љ–Є—П –≤—А–∞—З –Њ—Ж–µ–љ–Є–≤–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –њ—А–Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–≤–µ–і–µ–љ–Є—П. –°–Њ—Е—А–∞–љ–µ–љ–Є–µ –Є–ї–Є —Г—Б—Г–≥—Г–±–ї–µ–љ–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є —А–∞—Б—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –Є–Љ –Ї–∞–Ї —Б–Є–Љ–њ—В–Њ–Љ —В—А–µ–≤–Њ–≥–Є, –Є —В–∞–Ї–Њ–є –њ–∞—Ж–Є–µ–љ—В –і–Њ–ї–ґ–µ–љ –±—Л—В—М –љ–∞–њ—А–∞–≤–ї–µ–љ –љ–∞ —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–є —Н—В–∞–њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є.
–Я—А–Њ–≥–љ–Њ–Ј –њ—А–Є –°–Ф —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –њ—А–Є—А–Њ–і—Л –≤ –њ–ї–∞–љ–µ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є. –Ю–і–љ–∞–Ї–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ –ї—О–±–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є —Б–≤–Њ–є—Б—В–≤–µ–љ–љ–Њ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–µ —В–µ—З–µ–љ–Є–µ, —Б–Њ—З–µ—В–∞–љ–љ–Њ—Б—В—М –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б –і—А—Г–≥–Є–Љ–Є –Њ—А–≥–∞–љ–∞–Љ–Є –Є —Б–Є—Б—В–µ–Љ–∞–Љ–Є. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –њ–∞—Ж–Є–µ–љ—В—Л –Є –њ–Њ –Њ–Ї–Њ–љ—З–∞–љ–Є–Є –њ–µ—А–Є–Њ–і–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є—П –љ—Г–ґ–і–∞—О—В—Б—П –≤ –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ–±—Й–µ—Г–Ї—А–µ–њ–ї—П—О—Й–Є—Е –Є –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–∞ –Њ—В–Ї–∞–Ј –Њ—В –≤—А–µ–і–љ—Л—Е –њ—А–Є–≤—Л—З–µ–Ї, —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –њ–Њ–Ј–Є—В–Є–≤–љ–Њ–≥–Њ –Љ—Л—И–ї–µ–љ–Є—П, —Г–ї—Г—З—И–µ–љ–Є–µ –њ—Б–Є—Е–Њ—Б–Њ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Talley N.J. –Рnd the working team for functional gastroduodenal disorders. Functional gastroduodenal disorders // The functional gastrointestinal disorders. – Boston–New York–Toronto–London, 1994. – P.71–113.
2. –Я–µ—З–Ї—Г—А–Њ–≤ –Ф.–Т. –°–Є–љ–і—А–Њ–Љ –і–Є—Б–њ–µ–њ—Б–Є–Є —Г –і–µ—В–µ–є: –і–Є—Б. –і–Њ–Ї—В. –Љ–µ–і. –љ–∞—Г–Ї. – –Ь., 2005. – 259 —Б.
3. –Ф–µ–ї—М–≤–Њ –Ь. –≠–љ–і–Њ—Б–Ї–Њ–њ–Є—П –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Ь–Є–љ–Є–Љ–∞–ї—М–љ–∞—П —Б—В–∞–љ–і–∞—А—В–љ–∞—П —В–µ—А–Љ–Є–љ–Њ–ї–Њ–≥–Є—П (–Ї–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–∞). –Т–µ—А—Б–Є—П 2.0h. –§–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–∞—П. – 1999 / –Ь.–Ф–µ–ї—М–≤–Њ, –Ы.–Ъ–Њ—А–Љ–∞–љ, –Ѓ.–Ф.–§–µ–і–Њ—А–Њ–≤ // endoscopy.ru/doctor/mst.html. http://endos.ru/default.asp?section_id=146.
4. Holtmann G., Talley N. Clinician’s manual on managing dyspepsia. – London : Life Science Communications, 2000. – 88 p.
5. Talley N.J., Heading R.C., Koch K.L. et al. Functional gastroduodenal disorders – Rome II: A multinational consensus Document on functional gastrointestinal disorders //Gut. – 1999. Vol. 45 (Suppl. 11). P. 1137–1142.
6. Drossman D.A. (ed), Corrazziari E., Delvaux M. et al. RomeIII: The Functional Gastrointestinal Disorders / 3rd ed. McLean. – VA: Degnon Associates, 2006. P. 374–381.
7. –Я–µ—З–Ї—Г—А–Њ–≤ –Ф.–Т., –©–µ—А–±–∞–Ї–Њ–≤ –Я.–Ы., –Ъ–∞–≥–∞–љ–Њ–≤–∞ –Ґ.–Ш. –°–Є–љ–і—А–Њ–Љ –і–Є—Б–њ–µ–њ—Б–Є–Є —Г –і–µ—В–µ–є. – –Ь.: –Ь–µ–і–њ—А–∞–Ї—В–Є–Ї–∞, 2007.
8. –Ш–≤–∞—И–Ї–Є–љ –Т.–Ґ., –®–µ–њ—В—Г–ї–Є–љ –Р.–Р., –С–∞—А–∞–љ—Б–Ї–∞—П –Х.–Ъ. –Є –і—А. –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –Є –ї–µ—З–µ–љ–Є—О –±–Њ–ї—М–љ—Л—Е —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –і–Є—Б–њ–µ–њ—Б–Є–Є – –Ь., 2001. – 30 —Б.
9. Quigley E.M.M. Functional dyspepsia – the 21st century disorder? // Innovation towards better GI care. 1. Janssen–Cilag congress. Abstracts. – Madrid, 1999. P.18–19.
10. –†—Л–Ї–Њ–≤–∞ –°.–Ь., –Я–Њ–≥—А–Њ–Љ–Њ–≤ –Р.–Я., –Ф—О–Ї–Њ–≤–∞ –У.–Ь., –Т–µ–є–љ –Р. –Ь. –Я—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Є –У–≠–†–С // –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–∞—П –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—П. — 2003.– вДЦ 4.
11. –Т–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞: r–ї–Є–љ–Є–Ї–∞, –ї–µ—З–µ–љ–Є–µ, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞/ –Я–Њ–і —А–µ–і. –Р.–Ь. –Т–µ–є–љ–∞. – –Ь.: –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–µ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ–Њ–µ –∞–≥–µ–љ—Б—В–≤–Њ, 2000.
12. –®–µ–њ—В—Г–ї–Є–љ –Р.–Р., –Ъ–Є–њ—А–Є–∞–љ–Є—Б –Т.–Р. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –Є–љ—Д–µ–Ї—Ж–Є–Є Helicobacter pylori: –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–ї–Њ–ґ–µ–љ–Є—П —Б–Њ–≥–ї–∞—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б–Њ–≤–µ—Й–∞–љ–Є—П «–Ь–∞–∞—Б—В—А–Є—Е—В–3» // –†–Њ—Б. –ґ—Г—А–љ–∞–ї –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є–Є, –≥–µ–њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї–Њ–ї–Њ–њ—А–Њ–Ї—В–Њ–ї–Њ–≥–Є–Є. – 2006. – –Ґ.16, вДЦ 2. – –°. 88–91.











