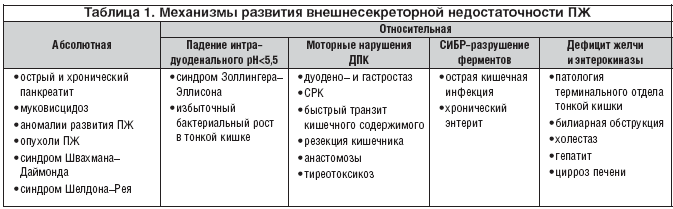
Панкреатическая недостаточность может протекать как с общим снижением выработки всех ферментов ПЖ, так и с изолированным снижением выработки одного из них. Клинически внешнесекреторная недостаточность ПЖ может проявляться диареей, метеоризмом, болями в животе, тошнотой, повторными рвотами, снижением аппетита, а также такими неспецифическими симптомами, как общая слабость, снижение физической активности, похудание, отставание в росте (при тяжелых формах мальдигестии). Важным диагностическим признаком экзокринной недостаточности ПЖ является изменение характера стула, т.к. проявления липазной недостаточности развиваются раньше снижения амилазной и протеазной активности. Стул становится объемным, отмечается полифекалия, каловые массы – сероватого цвета, имеют «сальный» вид, появляется стеаторея.
Диагностика патологии ПЖ является одной из наиболее сложных проблем детской гастроэнтерологии и основывается на анализе результатов как лабораторных, так и инструментальных методов исследования.
Определение содержания панкреатических ферментов в крови (a–амилазы, липазы, трипсина и его ингибитора) позволяет судить об органическом поражении органа, наличии повреждения ацинарных клеток, однако внешнесекреторную функцию ПЖ отражает в меньшей степени. В норме 60% амилазы сыворотки составляет амилаза слюнных желез, остальные 40% – ПЖ [1]. Нарастание содержания фермента в сыворотке крови является довольно ранним маркером острого панкреатита: повышение активности амилазы отмечается в течение 2–12 ч от начала заболевания. Следует отметить, что чувствительность и специфичность данного маркера при панкреатитах у детей несколько ниже, чем у взрослых и составляет не более 80–90% [1], при этом до 40% панкреатитов в детском возрасте могут протекать с нормальной активностью амилазы в сыворотке [2]. При оценке результатов лабораторного исследования следует помнить, что гиперамилаземия является неспецифическим симптомом и может быть вызвана другой патологией: аппендицитом, острым холециститом, заболеваниями слюнных желез, почечной недостаточностью (вследствие снижения клиренса амилазы) (табл. 2).
Для дифференциальной диагностики гиперамилаземии можно использовать определение уровня изоферментов амилазы (табл. 3).
Уровень липазы в сыворотке крови также обычно повышается при остром панкреатите и остается повышенным дольше, чем уровень амилазы. Повышение активности данного фермента в крови является более чувствительным и специфичным маркером поражения ПЖ, и при одновременном определении уровня обоих ферментов чувствительность метода достигает 94% [3,4].
Важное значение для диагностики острого панкреатита имеет определение активности других ферментов ПЖ в сыворотке крови, в частности эластазы–1, трипсина и его ингибитора с определением отношения ингибитор/трипсин, которое уменьшается при патологии органа. Значимым в диагностике панкреатита является определение концентрации в крови и моче фосфолипазы А2 – маркера деструктивного процесса в ПЖ.
По данным Н.Б. Губергриц (2001), чувствительность различных панкреатических ферментов крови зависит от длительности заболевания (табл. 4) [5].
Для диагностики острого и обострения хронического панкреатита большое значение имеет определение уровня панкреатических ферментов в моче. При остром панкреатите уровень амилазы мочи (диастаза) может быть повышен в 5–10 раз.
Следует признать, что копрологическое исследование до настоящего времени не потеряло своей актуальности и является самым доступным методом, способным подтвердить наличие внешнесекреторной недостаточности ПЖ, однако, в отличие от определения уровня ферментов ПЖ в крови, указывающих на непосредственное поражение органа, на основании результатов копрологии провести дифференциальную диагностику абсолютной и относительной недостаточности ПЖ достоверно невозможно. Исследование кала следует проводить до назначения панкреатических ферментов. На точность данного метода также влияют: состояние моторики кишечника, объем выделяемой желчи в просвет кишечника, ее качественный состав, наличие воспалительных процессов в кишечнике и др.
Анализ результатов копрологического исследования позволяет выделить следующие симптомы:
• стеаторея – повышение содержания в кале нейтрального жира (стеаторея 1–го типа), жирных кислот/мыл (стеаторея 2–го типа) или их сочетания (стеаторея 3–го типа);
• креаторея – повышение содержания в кале содержания мышечных волокон (++ или +++);
• амилорея – наличие в кале крахмальных зерен.
Стойкое сохранение стеатореи и креатореи может с большой вероятностью свидетельствовать о наличии у пациента внешнесекреторной недостаточности ПЖ, в то время как амилорея выявляется у больных с панкреатической недостаточностью довольно редко, поскольку гидролиз крахмала часто не нарушается ввиду высокой активности кишечной амилазы.
Липидограмма кала позволяет уточнить характер стеатореи и имеет определенное значение при оценке эффективности ферментотерапии. Содержание жиров в стуле оценивается качественным (добавление к калу суданового красителя) либо количественным методом. Последний является наиболее информативным [6], позволяя суммарно определить общее количество жира в фекалиях с учетом жира экзогенного (пищевого) происхождения. В норме количество жира, выделяющегося с калом, не должно превышать 10% жира, введенного с пищей. При заболеваниях ПЖ количество выделенного с калом жира иногда увеличивается до 60% [7].
Определение эластазы–1 в кале позволяет оценить степень экзокринной недостаточности ПЖ и провести дифференциальный диагноз между абсолютной внешнесекреторной недостаточностью и относительной. Эластаза–1 – протеолитический фермент ПЖ с молекулярным весом около 28 мДа. Известно, что фермент не меняет своей структуры по мере прохождения через желудочно–кишечный тракт, что позволяет считать его чувствительным маркером экзокринной недостаточности ПЖ. Данная методика имеет качественные преимущества перед используемыми сегодня методами определения экзокринной недостаточности ПЖ (липидограмма кала, копрограмма) ввиду большей специфичности метода и отсутствия влияния ферментативной терапии на результаты эластазного теста. Содержание эластазы в кале должно быть выше 200 мкг/г. Уровень фекальной эластазы от 200 до 100 мкг/л свидетельствует об умеренной экзокринной недостаточности ПЖ, снижение уровня фермента в кале менее 100 мкг/л – о наличии выраженной панкреатической недостаточности. Данный тест нашел широкое применение у пациентов, страдающих муковисцидозом, синдромом Швахмана, поскольку определение у них уровня фекальной эластазы дает возможность, не отменяя ферментотерапии, контролировать состояние ПЖ.
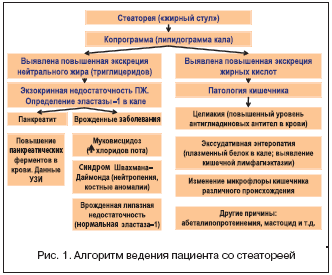
В таблице 5 и на рисунке 1 представлен алгоритм диагностики экзокринной недостаточности ПЖ по результатам исследования уровня эластазы–1 в кале [8].
Имевший ранее довольно широкое применение секретин–панкреозиминовый тест (SPT) – зондовый метод изучения экзокринной функции ПЖ основан на определении содержания бикарбонатов и ферментов в дуоденальном содержимом с помощью зонда после прямой стимуляции ацинарных и протоковых клеток ПЖ. При проведении исследования вначале определяют базальную секрецию при введении секретина (1 Ед/кг), который стимулирует увеличение объема секрета ПЖ и продукцию бикарбонатов. Затем вводят холецистокинин–панкреозимин (1 Ед/кг), стимулирующий выработку ферментов и вызывающий сокращение желчного пузыря (стимулированная секреция).
Нормальные показатели секретин–панкреозиминового теста: бикарбонаты – не менее 70 ммоль/л, амилаза – не менее 12000 Ед/30 мин., трипсин – не менее 3 Ед/30 мин., липаза – не менее 65000 Ед/30 мин., стеаторея – не более 7 г/сут.
На основании полученных результатов можно определить типы панкреатической секреции на раздражители:
• нормосекреторный ответ – повышение активности ферментов, объема секрета и уровня бикарбонатов;
• гиперсекреторный тип секреции – избыточное повышение концентрации ферментов при нормальном или повышенном объеме секрета и уровня бикарбонатов, характерно для нетяжелых воспалительно–дистрофических изменений ПЖ, связанных с гиперфункцией ацинарной ткани;
• гипосекреторный тип секреции – нормальный или сниженный объем сока и уровня бикарбонатов при сниженной активности ферментов, свидетельствует о качественной недостаточности панкреатической секреции, характерен при развитии фиброза ПЖ;
• обтурационный тип секреции – снижение объема сока при нормальном содержании ферментов и бикарбонатов, характерен для обтурации протока (папиллит, дуоденит, спазм сфинктера Одди, холедохолитиаз).
Следует отметить, что у детей чаще нарушается ферментосинтезирующая функция ПЖ, только при выраженной панкреатической недостаточности снижается уровень бикарбонатов и секреции. Данный тест в настоящее время не находит широкого применения ввиду наличия современных чувствительных и малоинвазивных методик оценки структурного и функционального состояния ПЖ.
Инструментальные методы исследования при диагностике внешнесекреторной недостаточности ПЖ имеют вспомогательное значение, позволяя оценить анатомическую структуру органа.
Ультразвуковое исследование ПЖ является одним из ведущих методов лучевой диагностики, который позволяет быстро, достаточно информативно, независимо от тяжести состояния больного оценить состояние ПЖ: увеличение ее размеров, изменение эхоплотности (отек, уплотнение), наличие эхоплотных включений, состояние Вирсунгова протока.
Акустическая характеристика неизмененной ПЖ включает определение формы, контура, размеров, эхогенности внутренней структуры и состояния главного панкреатического протока. Традиционно в клинической практике применяются возрастные нормативы ультразвуковых размеров ПЖ (табл. 6).
Одним из основных критериев повреждения ПЖ является изменение размеров органа. На основании анализа более чем 3000 обследованных детей М.И. Пыков (1997) показал, что увеличение размеров ПЖ, особенно хвостовой ее части, и визуализация расширенного протока у детей являются свидетельством повышенного давления в просвете 12–перстной кишки. Ряд авторов рассматривают умеренное увеличение размеров ПЖ (или ее частей) при неизмененной эхогенности и гомогенной эхоструктуре как проявление функциональных изменений органа компенсированного характера. В то же время для органического поражения ПЖ характерны изменения размеров, контуров, формы, эхоструктуры и расширение главного панкреатического протока [9].
К признакам хронического панкреатита при УЗИ относят: расширение протока ПЖ, обнаружение камней в протоке ПЖ, неравномерность краев железы/изменения эхоструктуры, наличие псевдокист [10,11].
С помощью ультразвуковых сканеров, использующих эффект Допплера, можно получить данные о кровотоке в артериальных и венозных сосудах. Принимая во внимание, что наиболее ранние изменения в ПЖ происходят на уровне микроваскулярного русла, значение визуализации паренхиматозного кровотока в ПЖ для оценки ее состояния трудно переоценить. Поражение данного органа нередко сопровождается изменениями гемодинамики и в крупных сосудах, кровоснабжающих верхние отделы пищеварительной системы.
В отечественной литературе имеются лишь единичные сообщения о допплерографических показателях в норме и при патологии. По данным В.В. Митькова (1998), частота визуализации мелких сосудов ПЖ с помощью цветового допплеровского сканирования (ЦДК) и энергетического допплера (ЭД) составляет от 60 до 90%, при этом наибольшее количество сосудов определяется в области головки ПЖ [12]. По данным импульсно–волновой допплерометрии максимальная систолическая скорость в мелких артериях ПЖ составляет 30±1 см/с, в венах – 15 см/с, индекс резистентности в мелких артериях ПЖ – 0,61±0,05. При остром панкреатите наблюдается усиление внутриорганного кровотока, по мере увеличения отека паренхимы по данным импульсного допплера (ИД) может отмечаться повышение индексов периферического сопротивления в мелких артериях. По мере развития деструктивных процессов в паренхиме ПЖ фиксируется деформация сосудистого рисунка в зоне деструкции, а при ИД – снижение показателей периферического сопротивления и выявление признаков артерио–венозного шунтирования. При хроническом панкреатите при проведении ЦДК наблюдается ослабление кровотока, а при ИД – снижение скоростных показателей кровотока в мелких сосудах ПЖ.
Эндоскопическая ретроградная панкреатохолангиография (ЭРПХГ) – «золотой стандарт» диагностики патологии ПЖ. С помощью этой методики возможно выявление расширения и деформации главного панкреатического протока, обнаружение стриктур протоков, отложения кальция на стенках протока, обызвествление паренхимы ПЖ. При исследовании также выявляются изменения желчевыводящей системы: стенозирующий папиллит, холедохолитиаз, аномалии развития желчных протоков и желчного пузыря и т.д.
Показаниями к проведению ЭРПХГ являются:
• рецидивирующий хронический панкреатит;
• тупая травма живота с выраженным болевым синдромом;
• дуоденостаз;
• желтуха неясной этиологии;
• хронический калькулезный холецистит;
• предоперационное обследование больных.
Основные показания к проведению компьютерной томографии и магнитно–резонансной холангиопанкреатографии у детей:
• осложненное течение острого и хронического панкреатита;
• подозрение на объемный процесс в ПЖ и смежных органах.
Коррекция панкреатической недостаточности направлена на ликвидацию нарушений расщепления жиров, белков и углеводов и предусматривает назначение специальной высококалорийной диеты и заместительную терапию ферментами, что может уменьшить проявления мальдигестии и мальабсорбции. Многие традиционно используемые педиатрами ферментные препараты обладают значительными технологическими и фармакологическими недостатками, а также низкой активностью в 12–перстной кишке. Назначая тот или иной препарат, врач прежде всего должен знать его состав и иметь сведения об активности его компонентов.
Препараты для заместительной терапии внешнесекреторной недостаточности ПЖ у детей должны [13,14]:
• содержать в своем составе липазу и быть устойчивыми к соляной кислоте;
• обладать максимумом действия при рН 5–7;
• быстро и гомогенно смешиваться с химусом и транспортироваться в 12–перстную кишку;
• иметь микротаблетированную (микросферическую) форму диаметром не более 2 мм, обеспечивающую большую поверхность соприкосновения с химусом. Это способствует одновременному поступлению препарата в 12–перстную кишку и быстрому высвобождению липазы в кишечнике;
• иметь хорошую переносимость;
• не обладать токсичностью.
Для обеспечения быстрого и гомогенного смешивания ферментов с пищевым химусом, предотвращения внутрижелудочной инактивации и адекватного пассажа из желудка в 12–перстную кишку были созданы ферментные препараты панкреатина нового поколения – Креон 10000, Креон 25000 и Креон 40000 в виде мини–микросфер, диаметр которых не превышает 1,4 мм.
Мини–микросферы Креон 40000 покрыты энтеросолюбильной оболочкой и заключены в желатиновую капсулу. При попадании в желудок капсула быстро растворяется, мини–микросферы смешиваются с пищей и постепенно поступают в 12–перстную кишку. При pH дуоденального содержимого выше 5,5 оболочки растворяются, и ферменты начинают действовать на большой поверхности. Механизм действия Креона 40000 позволяет воспроизвести физиологический процесс пищеварения, при котором панкреатический сок выделяется порциями в ответ на периодическое поступление пищи из желудка. Препарат характеризуется оптимальным соотношением активности липазы и протеазы, а также высоким содержанием карбоксилэстеролипазы и фосфолипазы А2 для наиболее эффективного расщепления жиров.
Успех терапии внешнесекреторной недостаточности ПЖ зависит от многих причин. Наиболее удобным и физиологичным для пациента является прием ферментных препаратов во время еды. В случае адекватно подобранной дозы и формы ферментного препарата наступает значительное улучшение состояния пациента. Критериями эффективности лечения являются исчезновение полифекалии, уменьшение или ликвидация диареи, нарастание массы тела, исчезновение стеатореи, амилореи и креатореи.
Доза ферментного препарата подбирается индивидуально в течение 1–й нед. лечения в зависимости от выраженности экзокринной недостаточности ПЖ. Дозу ферментного препарата целесообразно рассчитывать по липазе и начинать с небольшой (1000 ЕД липазы на кг массы). В случае отсутствия эффекта доза препарата постепенно увеличивается под контролем копрологических исследований. При тяжелой экзокринной недостаточности ПЖ мы используем 4000–5000 ЕД липазы на кг массы. Длительность терапии определяется индивидуально. Прием ферментов прекращают в случае исчезновения клинических и копрологических признаков мальдигестии и мальабсорбции.




![Таблица 6. Размеры ПЖ в зависимости от возраста [9] (мм)](/data/articles/Image/t20/n33/1604-7.gif)
Литература
1. Lerner A., Branski D., Lebenthal E. Pancreatic diseases in children // Pediatr. Clin. North Am. 1996. Vol. 43. Р. 125–156.
2. Cox K.L., Ament M.E., Sample W.F., Sarti D.A., O’Donnell M., Byrne W.J. The ultrasonic and biochemical diagnosis of pancreatitis in children // J. Pediatr. 1980. Vol. 96 (3 Part 1). Р. 407–411.
3. Frank B., Gottlieb K. Amylase normal, lipase elevated: is it pancreatitis? A case series and review of the literature // Am. J. Gastroenterol. 1999. Vol. 94. Р. 463–469.
4. Russell M.K. Acute pancreatitis: a review of pathophysiology and nutrition management // Nutr. Clin. Pract. 2004. Vol. 19. Р. 16–24.
5. Губергриц Н.Б., Голубова О.А. Лабораторная диагностика заболеваний поджелудочной железы / Медицинская лабораторная диагностика (программы и алгоритмы) / под ред. А.И. Карпищенко. СПб., 2001.
6. Хендерсон Д.М. Патофизиология органов пищеварения. М.: Бином, 1997. С. 288.
7. Коровина Н.А., Левицкая С.В., Будакова Л.В., Каменева О.П. Диагностика панкреатитов у детей. М., 1989. 24 с.
8. Бельмер С.В., Гасилина Т.В. Пищеварительная недостаточность поджелудочной железы у детей. Дифференцированный подход // Русский медицинский журнал. 2007. № 1. С. 57–60.
9. Пыков М.И. Допплерографическое исследование сосудов поджелудочной железы у детей // Ультразвуковая и функцион. диагностика. 2001. № 2. C. 53–57.
10. Загоренко Ю.А. Клинико–патогенетическая оценка информативности и современные возможности оптимизации ультразвуковой диагностики хронического рецидивирующего панкреатита // Мед. визуал. 2002. № 1. C. 48–58.
11. Зубарев А.В. Ультразвуковой мониторинг лечения острого панкреатита // Мед. визуал. 2000. № 4. C. 21–24.
12. Митьков В.В., Брюховецкий Ю.А., Кондратова Г.М. Цветовая допплерография и энеогетический допплер при ультразвуковых исследованиях поджелудочной железы. Клиническая физиология. Диагностика – новые методы. М., 1998. С. 177–180.
13. Яковенко Э.П. Ферментные препараты в клинической практике // Клиническая фармакология и терапия. 1998. № 7. С.17–20.
14. Graham D.Y. Treatment of exocrine pancreatic insufficiency // Pract.Gastroenterol. 1980. Vol. 4. Р. 18–23.











