В докладе ВОЗ от 30 апреля 2014 г., посвященном проблеме устойчивости к противомикробным препаратам на глобальном уровне, было отмечено, что эта серьезная опасность уже не является лишь прогнозом на будущее, поскольку она проявляется сейчас в каждом регионе мира и представляет собой серьезную угрозу для здоровья людей [3].
Противоинфекционная терапия и прежде всего АБТ имеет принципиальное отличие от остальных направлений фармакотерапии в связи с тем, что ее последствия выходят далеко за рамки воздействия на человека, получающего лекарственный препарат. В последние годы все чаще выявляются штаммы бактерий, которые устойчивы к действию всех известных антибиотиков, увеличивается необходимость использования более дорогостоящих препаратов, отмечаются более тяжелое течение заболеваний и более высокая летальность среди пациентов с инфекциями, вызванными резистентными штаммами бактерий.
Основная причина роста резистентности бактерий – это широкое применение антибиотиков, прежде всего в медицинской практике, а также в ветеринарии и сельском хозяйстве. В этой связи во многих странах в настоящее время разрабатываются и внедряются национальные стратегии противодействия росту резистентности. Ключевыми в данных стратегиях являются мероприятия, направленные на рациональное применение антибактериальных препаратов: разработка и внедрение стандартных рекомендаций по лечению инфекционных заболеваний, надзор за назначением антибиотиков в лечебных учреждениях и продажей их в аптеках, контроль за лекарственной резистентностью возбудителей, оптимизация и внедрение образовательных программ для медицинских работников и населения [4].
В процессе принятия решения о назначении АБТ врач сталкивается с решением 3-х принципиальных вопросов:
1. Определение показаний к назначению АБТ.
2. Выбор оптимального препарата для АБТ (в случае положительного решения первого вопроса).
3. Определение режима применения выбранного препарата.
Каждый из этих вопросов сопряжен с целым рядом сложных проблем, оптимальное решение которых требует от практического врача не только глубоких знаний по основной специальности, но и понимания ключевых аспектов клинической микробиологии и фармакологии.
Весной 2014 г. в рамках работы Межрегионального педиатрического респираторного общества авторами начато тестирование участковых педиатров по вопросам АБТ при респираторных инфекциях. Тестирование проводится анонимно в рамках образовательных мероприятий для врачей в различных регионах Российской Федерации. Разработанные тестовые задания построены на основании современных российских и международных клинических рекомендаций. Тест включает 20 вопросов, касающихся этиологии и АБТ острого тонзиллофарингита (ОТФ), острого среднего отита (ОСО), острого риносинусита (ОРС) и внебольничной пневмонии (ВП) у детей. На каждый вопрос предлагается 5 вариантов ответов, при этом можно выбрать один или несколько ответов. В данной статье будут использованы полученные предварительные результаты тестирования – ответы 48 участковых педиатров из г. Москвы и Новосибирской области.
Определение показаний к назначению АБТ
В реальной клинической практике этиотропная терапия инфекционных заболеваний в амбулаторных условиях, как правило, проводится эмпирическим путем, т. е. без верификации возбудителя. Фармакоэпидемиологические исследования отчетливо показывают, что антибиотики назначаются существенно чаще (иногда в несколько раз), чем это требуется. Данное обстоятельство создает целый ряд существенных проблем, таких как стимуляция роста лекарственной резистентности бактерий, безосновательное увеличение стоимости лечения, развитие нежелательных лекарственных реакций. С другой стороны, отказ от применения антибиотика в ряде клинических ситуаций чреват развитием опасных осложнений или неблагоприятным исходом заболевания, что, безусловно, также определяет существенную проблему.
Острый тонзиллофарингит
ОТФ – одна из наиболее значимых причин обращения к педиатру и один из частых поводов для назначения антибиотиков у детей. Чаще всего это заболевание – проявление ОРВИ. Среди бактериальных возбудителей ОТФ доминирующее значение имеет β-гемолитический стрептококк группы А (БГСА, Streptococcus pyogenes), на долю которого приходится от 15 до 36% случаев заболевания [5–7]. При стрептококковой этиологии ОТФ необходимо обязательное назначение АБТ в связи с опасностью развития серьезных осложнений: ранних гнойных (средний отит, синусит, перитонзиллярный абсцесс и др.) и поздних негнойных (острая ревматическая лихорадка, гломерулонефрит и др.), что подтверждается данными Кокрановского систематического обзора [8].
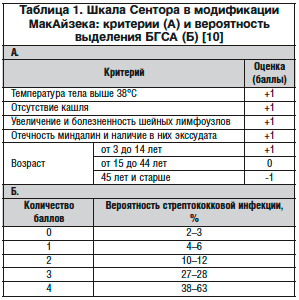
В подавляющем большинстве случаев АБТ при нестрептококковом ОТФ не обоснованна. Однако данные фармакоэпидемиологических исследований в разных странах показывают, что АБТ назначается большинству пациентов с клинической картиной ОТФ. По данным российского масштабного исследования, антибиотики назначаются 95% пациентов с ОТФ. Для определения показаний к назначению антибиотика при ОТФ необходимо верифицировать случаи заболевания, вызванные БГСА. Для выявления случаев стрептококкового ОТФ по клиническим данным имеется несколько балльных шкал, из которых наибольшее распространение получила шкала Сентора в модификации МакАйзека (табл. 1) [9].
Как видно из таблицы 1, при повышении суммарной оценки вероятность стрептококковой инфекции увеличивается, но даже при максимальном значении она выявляется примерно у половины больных. У пациентов с баллом 0–1 лабораторное обследование и назначение антибиотика не рекомендуются. У пациентов с 2 баллами и выше рекомендуется лабораторное обследование для выявления БГСА, а в случае его невозможности – назначение антибиотика.
Исследования показали, что применение шкалы Сентора в модификации МакАйзека позволяет примерно в 2 раза сократить частоту назначения антибиотиков у пациентов с ОТФ [10]. В нашем исследовании, проведенном в подмосковной поликлинике и включавшем 119 детей с ОТФ, у детей со стрептококковой и нестрептококковой этиологией заболевания медиана суммы баллов по шкале Сентора в модификации МакАйзека была одинаковой (3 балла), а среднее значение не имело достоверных различий. При этом у 94% детей оценка была 2 балла и выше. Таким образом, результаты нашего исследования ставят под сомнение диагностическую ценность данной шкалы [7]. В целом на сегодняшний день можно говорить о том, что клинические данные не позволяют верифицировать стрептококковую этиологию ОТФ, а следовательно, не дают возможности принять обоснованное решение о назначении АБТ.
Многие годы ведущим методом верификации стрептококкового ОТФ является бактериологическое исследование, которое позволяет выявить различные возбудители и определить их чувствительность к антибиотикам. Исследование проводится в специализированной лаборатории (куда необходимо доставить материал в течение 2-х ч), а результат анализа может быть получен только через несколько суток [9]. Указанных недостатков лишены экспресс-тесты для выявления БГСА, которые позволяют в течение нескольких минут провести анализ непосредственно при осмотре больного. Данные тесты обладают чувствительностью и специфичностью в отношении БГСА более 95% и на этапе скрининга способны заменить бактериологическое исследование. Применение высокоточных тестов способствует раннему назначению АБТ при стрептококковом ОТФ и в то же время позволяет отказаться от необоснованного назначения антибиотиков при заболевании иной этиологии. Проведенное фармакоэкономическое исследование показало, что использование экспресс-тестов на БГСА – это наиболее выгодная стратегия диагностики при ОТФ как у детей, так и у взрослых [11]. Внедрение экспресс-диагностики БГСА при ОТФ во Франции привело к уменьшению применения антибиотиков на 41%, в нашем исследовании удалось снизить частоту назначения антибиотиков на 57% [7, 12].
Одно из тестовых заданий, которые были предложены участковым педиатрам, содержало вопрос: «Какие бактерии являются ключевыми возбудителями ОТФ?». Примерно 2/3 врачей указали единственный верный ответ – Streptococcus pyogenes. При этом в 40 и 38% тестов в качестве правильных ответов неверно были указаны Staphylococcus aureus и Streptococcus pneumoniae.
Таким образом, имеются объективные проблемы в определении показаний к назначению АБТ при ОТФ у детей, связанные со сложностью этиологической диагностики заболевания. Очевидное решение данных проблем – широкое внедрение диагностики стрептококкового тонзиллофарингита с помощью современных экспресс-тестов. Кроме того, у врачей нередко имеются неверные представления относительно этиологии ОТФ: во многих случаях этиологическая роль приписывается бактериям, которые часто выделяются из ротоглотки у детей, но не являются возбудителями заболевания.
Острый средний отит
ОСО встречается у детей преимущественно в первые 3 года жизни. Обычно заболевание развивается у пациентов с ОРВИ и может быть вызвано различными вирусами. Однако чаще причиной ОСО являются бактерии: прежде всего Haemophilus influenzae и Streptococcus pneumonae, а также Moraxella catarrhalis, существенно меньшее место в этиологической структуре занимают Streptococcus pyogenes и Staphylococcus aureus [2]. В США на долю заболевания приходилось до 46% случаев всех назначений антибиотиков у детей (до внедрения универсальной вакцинации против пневмококковой и гемофильной инфекций) [13].
Диагностика ОСО основывается на клинических данных и результатах отоскопии. Поскольку заболевание чаще встречается у детей раннего возраста, имеются очевидные проблемы с выявлением ключевой жалобы – боли в ухе. В этой связи в нашей стране ОСО констатируется у детей значительно реже, чем в странах, где педиатры рутинно используют отоскопию. По данным российского исследования, при внедрении в практику педиатра пневматической отоскопии выявление ОСО у детей с респираторными инфекциями увеличивалось более чем в 2 раза [14].
Во многих случаях ОСО купируется без применения антибиотиков, однако необходимо учитывать возможность развития опасных системных осложнений этого заболевания: мастоидита, гнойного менингита, абсцесса головного мозга и др. (чаще осложнения развиваются при пневмококковой этиологии заболевания). В качестве абсолютных показаний к назначению антибиотиков при ОСО рассматриваются возраст до 2 лет и тяжелое течение заболевания [2]. Результаты доказательных клинических исследований показывают, что во многих случаях выжидательная тактика в отношении АБТ не ухудшает прогноз заболевания, что позволило Американской академии педиатров рекомендовать отсрочку решения о назначении антибиотиков у детей старше 2 лет с нетяжелым ОСО в случае активного наблюдения в последующие дни. Соответственно, при положительной динамике через 2–3 сут целесообразно воздержаться от назначения антибиотиков [15]. Аналогичная тактика рекомендуется и в российских руководствах [2].
Таким образом, ключевой проблемой при ОСО является его верификация у детей раннего возраста. Решение данной проблемы заключается в применении отоскопии у пациентов с респираторными инфекциями. Считаем целесообразным внедрение наблюдательной тактики в отношении применения антибиотиков при диагностированном ОСО в тех клинических ситуациях, когда это возможно.
Острый риносинусит
ОРС имеет высокую распространенность: по данным эпидемиологических исследований, за 1 год его переносят от 6 до 15% людей. Заболевание вызывают различные вирусы, в небольшом количестве случаев (менее 2%) на фоне ОРВИ развивается бактериальный синусит, который в детской популяции чаще наблюдается у подростков [16]. Так же как при ОСО, основными бактериальными возбудителями при ОРС являются Streptococcus pneumoniaе, Haemophilus influenzae и Moraxella catarrhalis. При рецидивирующем течении заболевания отмечается роль и других возбудителей, прежде всего анаэробов [1–2, 16].
В подавляющем большинстве случаев при ОРС назначение антибиотиков не показано. В то же время отказ от АБТ при бактериальном процессе чреват развитием редких, но очень опасных осложнений: флегмоны орбиты, внутричерепных абсцессов, менингита, тромбоза венозных синусов, остеомиелита костей лицевого скелета и др. Основаниями для диагностики бактериального процесса и, соответственно, показаниями для назначения АБТ при ОРС считаются:
– сохранение симптомов более 10 дней;
– выраженное ухудшение состояния пациента после первоначального улучшения;
– тяжелое течение заболевания: высокая температура тела, обильные гнойные выделения из носа, выраженный болевой синдром, периорбитальный отек.
О бактериальном процессе может свидетельствовать повышение показателей СОЭ и/или С-реактивного белка. При подозрении на бактериальный ОРС целесообразны консультация оториноларинголога и проведение риноскопии. Рентгенологическое обследование (рентгенография или компьютерная томография) не рекомендуются для рутинного исследования и должны применяться у пациентов с тяжелым течением заболевания или подозрением на развитие осложнений [16].
Таким образом, ключевыми проблемами при ОРС являются отказ от назначения антибиотиков у детей с вирусной инфекцией и своевременное выявление пациентов с бактериальными осложнениями. Поскольку определяющее значение имеют клинические данные, для решения указанной проблемы необходимо ознакомление врачей с современными рекомендациями по ведению пациентов с ОРС и, при необходимости, совместное ведение этих пациентов с оториноларингологами.
Внебольничная пневмония
Основные возбудители ВП – бактерии, при этом имеются возрастные особенности этиологической структуры заболевания. Все новорожденные и дети первого полугодия жизни с ВП подлежат госпитализации. В возрасте от 6 мес. до 5 лет основным возбудителем заболевания является Streptococcus pneumoniae, на долю которого приходится 70–88% случаев, определенную роль в этом возрасте играют также Haemophilus influenzae, Mycoplasma pneumoniae и Chlamydia pneumoniae. У детей старше 5 лет увеличивается значение атипичных возбудителей (Mycoplasma pneumoniae, Chlamydia pneumoniae), но при этом остается важная роль Streptococcus pneumoniae. Заболевание может иметь вирусную этиологию (особенно в первые годы жизни), однако быстро дифференцировать такие случаи сложно, к тому же в таких ситуациях имеется высокая вероятность развития вирусно-бактериальной ассоциации. Поэтому при выявлении ВП у ребенка требуется обязательное и незамедлительное назначение АБТ [2, 17].
Согласно российским рекомендациям диагноз пневмонии может быть достоверным только в случае рентгенологического подтверждения [17]. В то же время ВОЗ предлагает для диагностики ВП у детей использовать клинические критерии, такие как лихорадка, кашель, тахипноэ. В одном из исследований, включавшем анализ рентгенограмм 1848 детей до 5 лет с установленным по критериям ВОЗ диагнозом «пневмония», показано, что у 82% пациентов не было изменений на рентгенограмме, у 4% имелись признаки бронхиолита и только у 14% были выявлены рентгенологические изменения, характерные для пневмонии [18]. Вероятнее всего, в подавляющем большинстве случаев имел место острый бронхит, который обычно является проявлением ОРВИ и, соответственно, не требует назначения АБТ, за исключением отдельных клинических ситуаций [2]. Очевидно, что критерии ВОЗ имеют значение для ситуаций, когда недоступно проведение рентгенологического исследования и анализа крови. В остальных случаях их использование приводит к значительному увеличению объема неоправданной АБТ. В то же время диагноз ВП при обращении к педиатру в амбулаторной практике своевременно (в первые 3 сут) верифицируется не более чем у 30% пациентов [19].
Таким образом, ВП рассматривается как абсолютное показание к назначению АБТ, в связи с чем не возникает вопросов о необходимости применения антибиотиков при установленном в соответствии со стандартом РФ диагнозе. Однако существуют проблемы, которые могут быть обусловлены как гипер-, так и гиподиагностикой заболевания. Внедрение алгоритма диагностики при подозрении на ВП и расширение возможностей для проведения быстрого обследования помогают нивелировать эти недостатки.
Выбор оптимального препарата для АБТ
Для оптимального выбора антибиотика в конкретной клинической ситуации необходимо учитывать целый ряд факторов: наличие у пациента аллергии, концентрацию лекарственного препарата в очаге инфекции, чувствительность возбудителя инфекции к антибиотикам. Поскольку в реальной клинической практике в амбулаторных условиях АБТ чаще всего проводится эмпирически (т. е. без выявления возбудителя и определения его чувствительности к антибиотикам), то необходимо рассматривать спектр возможных возбудителей и оценивать их возможную резистентность.
Острый тонзиллофарингит
Назначение антибиотиков при ОТФ (за исключением редких случаев) направлено против БГСА. Данный возбудитель не только не обладает способностью продуцировать β-лактамазы (как и другие стрептококки), но и не имеет других механизмов резистентности к β-лактамным антибиотикам – пенициллинам и цефалоспоринам. Однако БГСА может быть резистентен к антибактериальным препаратам других групп. В ходе динамического российского многоцентрового исследования, проходившего в 1999–2009 гг., были получены данные о резистентности 860 штаммов БГСА, большинство из которых были выделены из ротоглотки. По результатам данного исследования отмечаются высокий уровень резистентности штаммов БГСА к тетрациклинам, небольшой уровень резистентности к 14- и 15-членным макролидам (до 13%) и хлорамфениколу (до 10%), минимальная резистентность к 16-членным макролидам и линкозамидам (менее 4%), а также фторхинолонам (менее 5%) и ко-тримоксазолу (менее 1%) [20].
Как в отечественных, так и в зарубежных руководствах в качестве препаратов выбора для лечения стрептококкового тонзиллофарингита рассматриваются пенициллины – феноксиметилпенициллин и амоксициллин [2, 21]. Однако нередко может наблюдаться клиническая и микробиологическая неэффективность пенициллинов при стрептококковом ОТФ. Установлено, что ведущей причиной этого является продукция β-лактамаз копатогенной флорой ротоглотки (Bacteroides spp., Staphylococcus aureus и др.) [22]. В связи с этим у пациентов с рецидивирующим ОТФ и/или получавших недавно антибиотики рекомендуется применение ингибиторозащищенных аминопенициллинов или цефалоспоринов, а в случае аллергии на β-лактамные антибиотики – линкозамидов [2, 21]. Также в качестве возможных причин неэффективности пенициллинов при ОТФ рассматриваются подавление в результате АБТ α-гемолитических (зеленящих) стрептококков, которые являются представителями нормальной микрофлоры ротоглотки и препятствуют колонизации БГСА [22], и низкая приверженность пациентов к лечению [23]. В целом возможная неэффективность пенициллинов, которая может быть связана с разными причинами, ведет к снижению значимости этих антибиотиков в лечении ОТФ. В то же время в подавляющем большинстве случаев необоснованный отказ от использования пенициллинов является ошибочным.
Еще одна проблема при выборе антибиотика для лечения ОТФ – нередкое развитие аллергических реакций на пенициллины [24]. Если у пациентов есть указания на аллергию на β-лактамные антибиотики в анамнезе, то для лечения ОТФ рекомендуется использование макролидов [1–2, 21]. Однако в этом случае существует риск неудачи терапии из-за резистентности БГСА. Как было сказано выше, резистентность возбудителя в разной степени проявляется в отношении различных макролидов. Это подтверждает еще одно многоцентровое российское исследование, проведенное в 2004–2007 гг., в котором также были отмечены принципиальные региональные особенности резистентности БГСА к макролидам [25]. В целом с учетом имеющихся в настоящее время данных предпочтение в лечении ОТФ отдается 16-членным макролидам: джозамицину, мидекамицину, спирамицину.
Также фактором, влияющим на выбор АБТ, является трудность дифференциальной диагностики по клиническим признакам между стрептококковым ОТФ и инфекционным мононуклеозом. Использование аминопенициллинов (ампициллина, амоксициллина, в т. ч. в составе ингибиторозащищенных препаратов) при инфекционном мононуклеозе приводит к развитию пятнисто-папулезной сыпи практически у всех пациентов [24]. Необходимо отметить, что накоплены обширные данные по использованию цефалоспоринов при ОТФ у детей, которые были представлены в метаанализе, включавшем 35 исследований с участием более 7000 пациентов. Во всех исследованиях сравнивалась эффективность 10-дневных курсов перорального приема цефалоспорина (I–III поколения) и пенициллина. Установлено, что, несмотря на абсолютную активность против БГСА, клиническая и микробиологическая эффективность цефалоспоринов была существенно выше, чем у пенициллина. Более высокая эффективность цефалоспоринов может объясняться их устойчивостью ко многим β-лактамазам, слабой активностью в отношении α-гемолитических стрептококков, а также более значимыми концентрациями препаратов в небных миндалинах [26].
В ходе тестового контроля знаний участковым педиатрам был задан вопрос: «К каким антибактериальным препаратам всегда чувствителен Streptococcus pyogenes?». Только 54% и 40% врачей указали в качестве ответа пенициллины и цефалоспорины соответственно. При этом в 25% случаев неверно были указаны макролиды. Еще одно тестовое задание содержало вопрос: «Какие антибиотики считаются препаратами выбора для ребенка 3 лет со стрептококковым тонзиллофарингитом?». Только 17% и 48% врачей выбрали правильные ответы: пенициллин и амоксициллин соответственно. При этом 71% врачей указали в ответах амоксициллин/клавуланат, а 23% – азитромицин. В ответе на вопрос: «Какие макролиды обладают наибольшей активностью в отношении Streptococcus pyogenes?» только 27% участковых педиатров назвали джозамицин и лишь 8% – спирамицин. При этом 60 и 79% врачей неверно отметили азитромицин и кларитромицин соответственно.
Таким образом, имеется целый ряд проблем в выборе оптимального антибиотика при ОТФ у детей, связанных как с эффективностью, так и с безопасностью препаратов. Решение данных проблем заключается в учете всех актуальных факторов для выбора АБТ у конкретного пациента в конкретной клинической ситуации. К сожалению, участковые педиатры часто имеют неверные представления об эффективности антибиотиков при инфекциях, вызванных БГСА, что может быть причиной неправильного выбора препарата для АБТ.
Острый средний отит и риносинусит
В этиологической структуре ОСО и ОРС ключевую роль играют одни и те же бактериальные возбудители: Streptococcus pneumoniaе и Haemophilus influenzae, в меньшей степени – Moraxella catarrhalis, поэтому принципы выбора АБТ при данных заболеваниях во многом совпадают. Препаратом выбора при ОСО и ОРС является амоксициллин, который в подавляющем большинстве случаев высокоэффективен в отношении возбудителей заболеваний. По данным динамического российского многоцентрового исследования, проходившего в 1999–2009 гг., резистентность к амоксициллину у пневмококка составляет менее 0,5% (анализ почти 2,5 тыс. штаммов) [27], а у гемофильной палочки – менее 6% (анализ почти 700 штаммов) [28].
У детей при наличии риска того, что заболевание вызвано штаммом Haemophilus influenzae, продуцирующим β-лактамазы (при недавнем приеме антибиотиков), и в случае неэффективности стартовой терапии амоксициллином в течение 3-х дней рекомендуется применение ингибиторозащищенного аминопенициллина или цефуроксима аксетила. При рецидивирующем ОРС применение ингибиторозащищенного аминопенициллина целесообразно также в связи с увеличением роли анаэробных бактерий. У пациентов с аллергией на β-лактамные антибиотики при ОСО и ОРС рекомендуется применение макролидов: азитромицина или кларитромицина (другие препараты этой группы не имеют значимой активности против Haemophilus influenzae) [2]. Трудность составляет выбор антибиотика у детей с аллергией на β-лактамные антибиотики, в случае недавнего приема антибиотиков или при неэффективности макролидов. Необходимо учитывать, что даже азитромицин, имеющий в отношении Haemophilus influenzae высокую активность in vitro (резистентность в России – ниже 2% [28]), обеспечивает эрадикацию возбудителя менее чем в половине случаев, что, возможно, связано с недостаточной концентрацией антибиотика в жидкости среднего уха [29].
Использование препаратов других групп (линкозамиды, тетрациклины, хлорамфеникол, ко-тримоксазол, аминогликозиды, фторхинолоны) при ОСО и ОРС у детей не показано из-за низкой активности в отношении ключевых возбудителей, неудовлетворительного профиля безопасности и/или возрастных ограничений к применению [2]. В данном случае целесообразно проанализировать аллергоанамнез пациента: если реакция была зафиксирована на пенициллины, то можно рассмотреть вопрос о применении цефалоспоринов. Данные обзоров многочисленных исследований показали, что у пациентов с аллергией на пенициллины существенная частота перекрестной реакции наблюдается только на цефалоспорины I поколения (примерно в 11% случаев), тогда как на цефалоспорины III поколения она незначительна (менее 1%). Это дает основание для назначения цефалоспоринов III–IV поколения пациентам с аллергией на пенициллины [24, 30]. Соответственно, у детей с аллергией на пенициллины в случае недавнего приема антибиотиков в качестве альтернативных препаратов для лечения ОСО и ОРС можно рассматривать цефалоспорины III поколения. В инструкциях к ряду препаратов (цефтибутен, цефотаксим, цефтриаксон) такая возможность допускается. Однако необходимо учитывать, что пероральные цефалоспорины III поколения, как правило, обладают невысокой активностью в отношении Streptococcus pneumoniae (резистентные к пенициллину штаммы устойчивы к цефиксиму, цефтибутену) [27]. В то же время парентеральный цефалоспорин III поколения цефтриаксон не только высокоактивен в отношении возбудителей ОСО и ОРС, но и создает высокие концентрации в жидкости среднего уха. Это дает возможность использовать данный антибиотик при ОСО в виде короткого курса – 1–3 дня [2].
Одно из тестовых заданий, которые были предложены участковым педиатрам, содержало вопрос: «Какие бактерии являются основными возбудителями ОСО у детей?». Менее половины врачей указали 2 верных ответа: Haemophilus influenzae (48%) и Streptococcus pneumoniaе (40%). При этом в 40 и 38% тестов в качестве правильных ответов ошибочно были названы Streptococcus pyogenes и Staphylococcus aureus. Также был задан вопрос: «Какие бактерии являются основными возбудителями острого бактериального риносинусита у детей младше 5 лет?». Большинство врачей верно указало в ответах Streptococcus pneumoniaе и Haemophilus influenzae – в 63 и 54% случаев соответственно. Но в то же время только 8% участковых педиатров назвали среди основных возбудителей Moraxella catarrhalis, а 52% ошибочно указали Staphylococcus aureus. Еще один вопрос звучал следующим образом: «Какие антибиотики считаются препаратами выбора для лечения нетяжелого ОСО у ребенка 10 мес., который ранее не получал АБТ?». Только 40% участковых педиатров дали верный ответ – амоксициллин. При этом 52% неверно назвали амоксициллин/клавуланат, а 21% – азитромицин.
Таким образом, определенной сложностью в лечении ОСО и ОРС является выбор препарата для АБТ у детей с аллергией на пенициллины при неэффективности макролидов. Эта проблема во многом может быть решена путем применения цефалоспоринов III поколения. Частое неверное представление участковых педиатров об этиологии ОСО и ОРС может приводить к ошибкам в выборе антибиотика.
Внебольничная пневмония
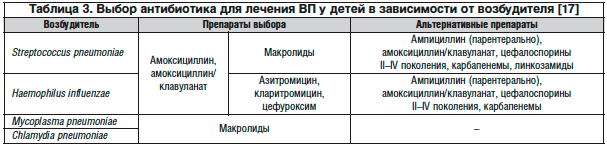
Как уже упоминалось, ВП у детей могут вызывать различные бактерии, при этом имеются принципиальные возрастные особенности этиологии (табл. 2). Безусловно, основным критерием выбора антибиотика для лечения ВП у детей является этиологическая структура заболевания. При выборе препарата для АБТ также нужно учитывать возраст ребенка, тяжесть заболевания и наличие осложнений, преморбидный фон и ряд других факторов.
В качестве основного препарата для лечения ВП у детей от 3 мес. до 5 лет как российские, так и зарубежные руководства указывают амоксициллин, который сохраняет высокую активность в отношении пневмококка – основного и наиболее опасного возбудителя ВП в этом возрасте. Эффективность амоксициллина при ВП (в т. ч. при тяжелой) у детей показана в ряде современных систематических обзоров [19]. В руководстве Американского общества по инфекционным заболеваниям в качестве одного из препаратов для лечения ВП у детей назван левофлоксацин [31]. В этой связи необходимо отметить, что все зарегистрированные в настоящее время в России фторхинолоны противопоказаны для применения у детей до 18 лет (исключение – ципрофлоксацин, который разрешен по отдельным показаниям), а на отечественном фармацевтическом рынке нет пероральной формы левофлоксацина для детей. Поэтому в нашей стране основными препаратами для АБТ при ВП у детей остаются пенициллины, макролиды и цефалоспорины, в отдельных случаях – антибиотики из других групп (табл. 3).
В российских рекомендациях ингибиторозащищенные аминопенициллины рассматриваются в качестве препаратов выбора для лечения ВП у детей в определенных случаях – в частности, при наличии фоновых заболеваний или у детей, которые получали антибиотики в последние 3 мес. [17]. В случае если ВП вызвана атипичными бактериями, а также у пациентов с аллергией на пенициллины рекомендуется использовать макролиды. При этом нужно учитывать, что у детей первых лет жизни в этиологической структуре заболевания определенную роль играет Haemophilus influenzae, в отношении которой из макролидов активность могут проявлять только азитромицин и кларитромицин [28]. В то же время в отношении Streptococcus pneumoniae большую активность проявляют 16-членные макролиды [25].
Необходимо отметить, что в подавляющем большинстве случаев при ВП назначается эмпирическая АБТ, т. е. без верификации возбудителя, что может быть сопряжено с ошибочным выбором антибиотика. Наибольшее значение данная проблема имеет при ВП у детей школьного возраста, когда в этиологической структуре важную роль играют и типичные, и атипичные бактерии [17].
При ответе на заданный в ходе тестирования вопрос: «Какие возбудители чаще вызывают ВП в возрасте от 3 мес. до 5 лет?» большинство педиатров (81%) отметили единственный верный ответ – Streptococcus pneumoniae. Нередко отмечались и неверные ответы, в частности, 1/4 врачей выбрали Mycoplasma pneumoniae, которая в этом возрасте не играет большой роли в этиологии ВП. Также был задан вопрос: «Какие антибиотики считаются препаратами выбора для лечения ВП, вызванной типичными возбудителями, у ребенка 4 лет?». Только 31% участковых педиатров назвали амоксициллин, тогда как амоксициллин/клавуланат (второй правильный ответ) – 79%. При этом 21 и 38% врачей ошибочно назвали азитромицин и кларитромицин соответственно.
Таким образом, при выборе антибиотика для лечения ВП имеет место проблема, связанная с разнообразием этиологии заболевания. Определенной проблемой является неверное представление части педиатров относительно этиологии ВП у детей разного возраста и эффективности антибиотиков при ВП. В частности, отмечается недооценка роли амоксициллина в качестве эффективного антипневмококкового препарата.
Определение режима применения выбранного препарата
Для достижения целей АБТ (которые могут иметь некоторые отличия в зависимости от заболевания) большое значение имеет не только правильный выбор антибиотика, но и определение оптимального режима его применения: дозировки, длительности, а в ряде случаев – и других критериев.
Острый тонзиллофарингит
Целью АБТ при стрептококковом ОТФ является не только излечение пациента, но и эрадикация БГСА, которая предотвращает развитие осложнений (в т. ч. поздних) и распространение инфекции. В связи с этим при ОТФ рекомендуется 10-дневный курс АБТ, за исключением 2-х антибиотиков:
• бензатинпенициллина – пенициллина пролонгированного действия (эффект длится несколько недель), который вводится однократно в/м;
• азитромицина – макролида, имеющего специфическую фармакокинетику (концентрация длительно сохраняется в тканях после отмены), который назначается на 5 дней. При этом курсовая доза данного препарата при ОТФ должна быть в 2 раза выше обычной (60 мг/кг, а не 30 мг/кг) [1–2].
Ряд исследований показал, что назначенный 10-дневный курс лечения пенициллином большинство больных не проходит, что ведет к снижению эффективности терапии. В связи с этим начали проводиться клинические испытания коротких курсов антибиотиков [32]. В Кокрановском систематическом обзоре, включавшем 20 доказательных исследований (более 13 тыс. пациентов), сравнивалась эффективность коротких курсов АБТ и стандартного 10-дневного курса лечения пенициллином при ОТФ у детей. Установлено, что микробиологическая эффективность и частота рецидивов не имели достоверных различий при короткой и стандартной длительности курса АБТ [33].
В ходе тестирования участковым педиатрам был задан вопрос: «Какой курс лечения может быть рекомендован ребенку 5 лет при остром стрептококковом тонзиллофарингите?». Лишь 29% врачей отметили правильный ответ – 10-дневный курс лечения пенициллином, еще 52% отметили второй верный ответ – 5-дневный курс лечения азитромицинами. При этом по 33% врачей неверно указали 7-дневный курс лечения пенициллином и 3-дневный курс лечения азитромицином.
Таким образом, основная проблема в определении режима АБТ у детей с ОТФ – это низкая комплаентность пациентов. В случае низкой приверженности к лечению целесообразно применение антибиотиков, которые обеспечивают высокую эффективность и при коротких курсах применения. Также проблему составляет то, что врачи недостаточно осведомлены о необходимой длительности АБТ при стрептококковом ОТФ.
Острый средний отит
Определенной проблемой в лечении пневмококковых инфекций, в частности ОСО, ВП, является выбор дозы амоксициллина (в т. ч. в составе ингибиторозащищенных пенициллинов). В российских рекомендациях для лечения ОСО (а также ОРС и ВП) у детей указана доза 40–45 мг/кг/сут [2].
Так же как и другие стрептококки, Streptococcus pneumoniae не продуцирует β-лактамазы, его резистентность к β-лактамным антибиотикам обусловлена модификацией пенициллиносвязывающего белка. Преодоление резистентности в данном случае возможно путем повышения дозы амоксициллина до 80–90 мг/кг/сут. Использование указанных доз амоксициллина рекомендуется для лечения инфекций у детей (вызванных Streptococcus pneumoniae) в регионах с высоким уровнем резистентности пневмококка к пенициллину; пациентам с риском того, что заболевание вызвано резистентным штаммом пневмококка [17].
В течение последних десятилетий отмечается глобальный рост уровня резистентности пневмококка к пенициллину. По данным динамического российского многоцентрового исследования, проходившего в 1999–2009 гг., доля штаммов пневмококка с высокой резистентностью к пенициллину составила 2,1%, с промежуточной резистентностью – 9,1%. Однако, как уже было сказано выше, уровень резистентности Streptococcus pneumoniae к амоксициллину составил всего 0,4% [27]. Аналогичная картина, когда резистентность Streptococcus pneumoniae к амоксициллину была существенно меньше, чем к пенициллину, наблюдалась во время исследований, выполненных в других странах [19]. Полученные данные свидетельствуют о том, что на сегодняшний день в России нет оснований для широкого применения высоких доз амоксициллина.
Определенной проблемой является выбор кратности применения амоксициллина, в т. ч. в комбинации с ингибитором β-лактамаз. Согласно рекомендациям и инструкциям по применению эти препараты можно использовать как 3, так и 2 р./сут [2]. По данным Кокрановского систематического обзора, при ОСО у детей эффективность амоксициллина не имеет отличий в случаях приема суточной дозы препарата за 2 или 3 раза [34]. В то же время необходимо учитывать, что предиктором эффективности амоксициллина, как и других β-лактамных антибиотиков, является показатель Т>МПК, т. е. время (Т), в течение которого концентрация антибиотика в крови превышает минимальную подавляющую концентрацию (МПК) для возбудителя. Считается, что для достижения надежного эффекта показатель Т>МПК должен составлять не менее 40% от времени между приемами препарата, а максимальный эффект должен наблюдаться при значении более 50% [35]. В ряде исследований было показано, что показатель Т>МПК для Streptococcus pneumoniae достоверно выше в случае разделения суточной дозы амоксициллина или амоксициллина/клавуланата на 3 приема по сравнению с 2-кратным приемом [36–37]. В связи с этим при лечении среднетяжелых и тяжелых форм ОСО дозу амоксициллина или амоксициллина/клавуланата (при пероральном приеме) целесообразно назначать 3 р./сут.
Рекомендуемая длительность АБТ при ОСО составляет от 5 до 10 дней в зависимости от тяжести заболевания. Исключение составляют азитромицин, который допустимо применять 3–5 дней, а также цефтриаксон, длительность курса которого составляет 1–3 дня [1–2].
Участковым педиатрам был задан вопрос: «Какая тактика лечения целесообразна в случае выделения у ребенка 1 года со средним отитом штамма Streptococcus pneumoniae, резистентного к пенициллину?». Только 19% врачей выбрали верный ответ – назначение амоксициллина в высокой дозе. При этом 60% неверно указали амоксициллин/клавуланат, а 56% – азитромицин.
Таким образом, при выборе режима АБТ при ОСО существует проблема, связанная с выбором режима применения амоксициллина и ингибиторозащищенных аминопенициллинов. Решение проблемы заключается в определении на основании современных научных данных контингента пациентов, требующих повышения дозы амоксициллина и разделения суточной дозы амоксициллина на 3 приема. Также проблемой является низкий уровень осведомленности врачей о возможности преодоления резистентности Streptococcus pneumoniae к пенициллинам.
Острый риносинусит
Вследствие схожей этиологической структуры бактериального ОРС и ОСО при выборе режима применения АБТ имеют место проблемы, описанные выше. Рекомендуемая длительность АБТ при бактериальном ОРС составляет от 7 до 14 дней в зависимости от тяжести заболевания. Исключение составляет азитромицин, который допустимо применять 3–5 дней [2]. Дополнительно следует отметить, что, согласно современным рекомендациям, детям с бактериальным ОРС целесообразно назначение антибиотиков в комбинации с назальными кортикостероидами [16].
Внебольничная пневмония
В связи с тем, что Streptococcus pneumoniae занимает важное место в этиологической структуре ВП, при выборе режима применения АБТ в лечении данного заболевания имеются те же проблемы, что при ОСО и бактериальном ОРС. Очевидную проблему составляет выбор оптимальной продолжительности АБТ при ВП у детей. Российские и зарубежные руководства рекомендуют проводить АБТ от 7 до 14 дней (для азитромицина – 3–5 дней) в зависимости от этиологии, тяжести и течения заболевания [2, 19]. При этом в последнее время появляются рекомендации по использованию более коротких курсов АБТ при ВП. В Кокрановском систематическом обзоре, включавшем 3 крупных рандомизированных исследования (почти 6 тыс. пациентов), было показано, что у детей в возрасте от 2 мес. до 5 лет с нетяжелой пневмонией 3-дневный курс АБТ эффективен так же, как 10-дневный курс [38]. Однако в ряде публикаций результаты данного обзора были подвергнуты серьезной критике [19]. Это связано с тем, что диагноз ставился в соответствии с критериями ВОЗ, о которых было сказано выше; имеется высокая вероятность того, что у большинства детей, включенных в эти исследования, была вирусная инфекция, и применение АБТ у них не требовалось в принципе. В то же время недавнее доказательное исследование, включавшее детей с рентгенологически подтвержденной нетяжелой ВП в возрасте от 6 мес. до 5 лет, показало, что эффективность 3-дневного курса АБТ составляет только 60%. При этом 5- и 10-дневный курсы показали эффективность во всех случаях [39].
Таким образом, имеет место проблема выбора продолжительности проведения АБТ у детей с ВП. Детальный анализ имеющихся в настоящее время научных данных показывает, что длительность АБТ при подтвержденной ВП у детей должна составлять не менее 5 дней.
Заключение
В настоящее время АБТ у детей с респираторными инфекциями в амбулаторной практике сопряжена с целым рядом серьезных проблем, которые связаны как с правильным определением показаний к назначению антибиотиков, так и с оптимальным выбором антибактериального препарата и режима его применения. Решение этих проблем требует проведения организационных мероприятий, направленных на выполнение современных клинических рекомендаций и усиление контроля за фармакотерапией при респираторных инфекциях (прежде всего за счет вневедомственной экспертизы).
На наш взгляд, необходимо принципиальное изменение подхода к повышению уровня знаний врачей относительно применения антибиотиков. Первые результаты проведенного нами тестирования участковых педиатров демонстрируют низкий уровень их осведомленности о современных аспектах АБТ. Это требует внедрения образовательных технологий, которые направлены на формирование умений и навыков, связанных с применением антибиотиков в педиатрической практике: интерактивных семинаров и практикумов с решением ситуационных задач, исходным и итоговым контролем знаний. С целью оценки эффективности системы образования врачей необходимо проведение динамических фармакоэпидемиологических исследований применения антибиотиков в детских амбулаторных учреждениях.

Литература
1. Острые респираторные инфекции у детей: лечение и профилактика. Научно-практическая программа. М.: Международный фонд охраны здоровья матери и ребенка, 2002. 72 с.
2. Современные клинические рекомендации по антимикробной терапии. Вып. 2. Смоленск: МАКМАХ, 2007. 608 с.
3. Устойчивость к антибиотикам — серьезная угроза общественному здравоохранению.URL: http://www.who.int/mediacentre/news/releases/2014/amr-report/ru.
4. Laxminarayan R., Duse A., Wattal C. et al. Antibiotic resistance-the need for global solutions / /Lancet Infect. Dis. 2013. Vol. 13. N 12. P. 1057–1098.
5. Linder J.A., Bates D.W., Lee G.M., Finkelstein J.A. Antibiotic treatment of children with sore throat // JAMA. 2005. Vol. 294. N 18. P. 2315–2322.
6. Bisno A.L. Acute pharyngitis // N. Engl. J. Med. 2001. Vol. 344. N 3. P. 205–211.
7. Dronov I.A., Botneva A.V., Neskorodova K.A., Malakhova-Kapanadze M.A. The experience of rapid diagnosis of streptococcal tonsillopharyngitis in children in outpatient care // 4th European Congress of Clinical Microbiology and Infectious Diseases, Barcelona, Spain, 10-13 May 2014. Poster R342.
8. Spinks A., Glasziou P.P., Del Mar C.B. Antibiotics for sore throat // Cochrane Database Syst. Rev. 2013. Vol. 5. N 11. CD000023.
9. Шпынев К.В., Кречиков В.А. Современные подходы к диагностике стрептококкового фарингита // КМАХ, 2007. Т. 9. № 1. C. 20–33.
10. McIsaac W.J., White D., Tannenbaum D., Low D.E. A clinical score to reduce unnecessary antibiotic use in patients with sore throat // CMAJ. 1998. Vol. 158. N 1. P. 75–83.
11. Maizia A., Letrilliart L., Colin C. Diagnostic strategies for acute tonsillitis in France: a cost-effectiveness study // Presse Med. 2012. Vol. 41. N 4. Р. 195–203.
12. Portier H., Grappin M., Chavanet P. New strategies for angina case management in France // Bull. Acad. Natl. Med. 2003. Vol. 187. N 6. P. 1107–1116.
13. Jacobs M.R. Emergence of antibiotic resistance in upper and lower respiratory tract infections // Am. J. Manag. Care. 1999. Vol. 5. Suppl. 11. Р. 651–661.
14. Тарасова Г.Д. Эпидемиология острого среднего отита в детской практике: Мат-лы Межд. конф. «Антибактериальная терапия в педиатрии». 25-26 мая 1999. С. 26–29.
15. American Academy of Pediatrics Subcommittee on Management of Acute Otitis Media. Diagnosis and management of acute otitis media // Pediatrics. 2004. Vol. 113. N 5. P. 1451–1465.
16. Fokkens W.J., Lund V.J., Mullol J. et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2012 // Rhinol. Suppl. 2012. Vol. 23. P. 1–298.
17. Внебольничная пневмония у детей: распространенность, диагностика, лечение, профилактика. Научно-практическая программа. М., 2010. 64 с.
18. Hazir T., Nisar Y.B., Qazi S.A. et al. Chest radiography in children aged 2-59 months diagnosed with non-severe pneumonia as defined by World Health Organization: descriptive multicentre study in Pakistan // BMJ. 2006. Vol. 333. P. 629.
19. Геппе Н.А., Малахов А.Б., Волков И.К. и др. К вопросу о дальнейшем развитии научно-практической программы по внебольничной пневмонии у детей // РМЖ. Педиатрия. 2014. № 3. С. 188–193.
20. Азовскова О.В., Иванчик Н.В., Дехнич А.В. и др. Динамика антибиотикорезистентности респираторных штаммов Streptococcus pyogenes в России за период 1999–2009 гг. // КМАХ. 2012. Т. 14. № 4. С. 309–321.
21. Gerber M.A., Baltimore R.S., Eaton C.B. et al. Prevention of Rheumatic Fever and Diagnosis and Treatment of Acute Streptococcal Pharyngitis // Circulation. 2009. Vol. 119. P. 1541–1551.
22. Brook I., Gober A.E. Role of bacterial interference and beta-lactamase-producing bacteria in the failure of penicillin to eradicate group A streptococcal pharyngotonsillitis // Arch. Otolaryngol. Head Neck Surg. 1995. Vol. 121. N 12. Р. 1405–1409.
23. Pichichero M.E. The Importance of Bacteriologic Eradication in the Treatment of Group A Streptococcal Tonsillopharyngitis // Clin. Pediatr. 2007. Vol. 46. P. 3–16.
24. Pichichero M.E. A review of evidence supporting the American Academy of Pediatrics recommendation for prescribing cephalosporin antibiotics for penicillin-allergic patients // Pediatrics. 2005. Vol. 115. N 4. P. 1048–1057.
25. Сидоренко С.В., Грудинина С.А., Филимонова О.Ю. и др. Резистентность к макролидам и линкозамидам среди Streptococcus pneumoniae и Streptococcus pyogenes в Российской Федерации // Клин. фармакол. и терапия. 2008. Т. 17. № 2. С. 1–4.
26. Casey J.R., Pichichero M.E. Metaanalysis of cephalosporin versus penicillin treatment of group A streptococcal tonsillopharyngitis in children // Pediatrics. 2004. Vol. 113. N 4. P. 866–882.
27. Козлов Р.С., Сивая О.В., Кречикова О.И. и др. Динамика резистентности Streptococcus pneumoniae к антибиотикам в России за период 1999–2009 гг. // КМАХ. 2010. Т. 12. N 4. С. 329–341.
28. Сивая О.В., Козлов Р.С., Кречикова О.И. и др. Антибиотикорезистентность Haemophilus influenzae в России: результаты многоцентрового проспективного исследования ПеГАС // КМАХ. 2014. Т. 16. № 1. С. 57–69.
29. Leibovitz E., Jacobs M.R., Dagan R. Haemophilus influenzae: a significant pathogen in acute otitis media / /Pediatr. Infect. Dis. J. 2004. Vol. 23. N 12. P. 1142–1152.
30. Campagna J.D., Bond M.C., Schabelman E., Hayes B.D. The Use of Cephalosporins in Penicillin-allergic Patients: A Literature Review // J. Emerg. Med. 2012. Vol. 42. N 5. P. 612– 620.
31. Bradley J.S., Byington C.L., Shah S.S. et al. The management of community-acquired pneumonia in infants and children older than 3 months of age: clinical practice guidelines by the Pediatric Infectious Diseases Society and the Infectious Diseases Society of America // Clin. Infect. Dis. 2011. Vol. 53. N 7. P. 25–76.
32. Pichichero M.E. Streptococcal Tonsillopharyngitis: Advantages of Shorter Antibiotic Courses. 2001. URL: http://www.medscape.com/viewarticle/418264.
33. Altamimi S., Khalil A., Khalaiwi K.A. et al. Short versus standard duration antibiotic therapy for acute streptococcal pharyngitis in children // Cochrane Database Syst. Rev. 2009. Vol. 21. N 1. CD004872.
34. Thanaviratananich S., Laopaiboon M., Vatanasapt P. Once or twice daily versus three times daily amoxicillin with or without clavulanate for the treatment of acute otitis media // Cochrane Database Syst. Rev. 2013. Vol. 12. CD004975.
35. Craig W.A. Antimicrobial resistance issues of the future // Diagn. Microbiol. Infect. Dis. 1996. Vol. 25. N 4. P. 213–217.
36. Jacobs M.R. Building in efficacy: developing solutions to combat drug-resistant S. pneumonia // Clin. Microbiol. Infect. 2004. Vol. 10. Suppl. 2. P. 18–27.
37. Fonseca W., Hoppu K., Rey L.C. et al. Comparing pharmacokinetics of amoxicillin given twice or three times per day to children older than 3 months with pneumonia // Antimicrob. Agents Chemother. 2003. Vol. 47. N 3. P. 997–1001.
38. Haider B.A., Saeed M.A., Bhutta Z.A. Short-course versus long-course antibiotic therapy for non-severe community-acquired pneumonia in children aged 2 months to 59 months // Cochrane Database Syst. Rev. 2008. Vol. 16. N 2. CD005976.
39. Greenberg D., Givon-Lavi N., Sadaka Y. et al. Short-course Antibiotic Treatment for Community-acquired Alveolar Pneumonia in Ambulatory Children: A Double-blind, Randomized, Placebo-controlled Trial // Pediatr. Infect. Dis. J. 2014. Vol. 33. N 2. P. 136–142.











