–Ф.–Љ.–љ. –Х.–Ѓ. –Ь–∞–є—З—Г–Ї
–Ь–Ь–°–£ –Є–Љ–µ–љ–Є –Э.–Р. –°–µ–Љ–∞—И–Ї–Њ–С–Њ–ї—М –≤ –Њ–±–ї–∞—Б—В–Є —Б–µ—А–і—Ж–∞ – –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–∞—П –Є —В—А–µ–≤–Њ–ґ–љ–∞—П –њ—А–Є—З–Є–љ–∞ –Ј–∞—Б—В–∞–≤–ї—П—О—Й–∞—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±—А–∞—Й–∞—В—М—Б—П –Ї –≤—А–∞—З–∞–Љ–—В–µ—А–∞–њ–µ–≤—В–∞–Љ. –°–ї–Њ–ґ–љ–Њ—Б—В—М, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –µ–і–Є–љ–Њ–≥–Њ –≤–Ј–≥–ї—П–і–∞ –љ–∞ –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П —Н—В–Њ–≥–Њ —Д–µ–љ–Њ–Љ–µ–љ–∞ –Њ–±—К—П—Б–љ—П—О—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–µ—Б –Ї –љ–µ–Љ—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є. –≠—В–Њ –љ–∞—И–ї–Њ –Њ—В—А–∞–ґ–µ–љ–Є–µ –≤ –±–Њ–ї—М—И–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –≥–Є–њ–Њ—В–µ–Ј –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ї–∞—А–і–Є–∞–ї–≥–Є–є (–Т.–Ш. –Ь–∞–Ї–Њ–ї–Ї–Є–љ, 1989, R. Melzak, 1987). –£–љ–Є–≤–µ—А—Б–∞–ї—М–љ–Њ–є, –љ–∞–Є–±–Њ–ї–µ–µ –њ–Њ–ї–љ–Њ –Њ—В—А–∞–ґ–∞—О—Й–µ–є –Љ–љ–Њ–≥–Њ–Љ–µ—А–љ–Њ—Б—В—М —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–Є, —П–≤–ї—П–µ—В—Б—П –Ї–Њ–љ—Ж–µ–њ—Ж–Є—П Karoly (1985), —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—Й–∞—П —И–µ—Б—В—М —Б–Њ—Б—В–∞–≤–ї—П—О—Й–Є—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –±–Њ–ї–Є, –Њ—В—А–∞–ґ–∞—О—Й–Є—Е —А–∞–Ј–ї–Є—З–љ—Л–µ —Г—А–Њ–≤–љ–Є –µ–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П: 1––є – —З—Г–≤—Б—В–≤–µ–љ–љ—Л–є (–≤–Њ—Б–њ—А–Є—П—В–Є–µ, —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П –њ–µ—А—Ж–µ–њ—Ж–Є—П), 2––є – –љ–µ–є—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є (–∞–≤—В–Њ–љ–Њ–Љ–љ–Њ––±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є), 3––є – –∞—Д—Д–µ–Ї—В–Є–≤–љ–Њ––Љ–Њ—В–Є–≤–∞—Ж–Є–Њ–љ–љ—Л–є, 4 – –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є–є (–≤–µ—А–±–∞–ї—М–љ–Њ––Љ–Њ—В–Њ—А–љ—Л–є), 5 – –Є–љ—В–µ—А–њ–µ—А—Б–Њ–љ–∞–ї—М–љ—Л–є, 6 – –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ–Њ––њ—А–Њ—Ж–µ—Б—Б—Г–∞–ї—М–љ—Л–є (—Ж–µ–љ—В—А–∞–ї—М–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М).
–Ь–Њ–і–µ–ї—М Levental (1984) –Њ—Б–љ–Њ–≤–Њ–њ–Њ–ї–∞–≥–∞—О—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ—А–Є–і–∞–µ—В —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–Љ—Г –Љ–µ—Е–∞–љ–Є–Ј–Љ—Г, –∞ –љ–µ —З—Г–≤—Б—В–≤–µ–љ–љ–Њ–Љ—Г –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Г. –°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є—О —Н—В–Њ–≥–Њ –∞–≤—В–Њ—А–∞, –±–Њ–ї—М –Љ–Њ–ґ–µ—В –≤–Њ–Ј–љ–Є–Ї–∞—В—М –Є –±–µ–Ј —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–Є (–љ–∞–њ—А–Є–Љ–µ—А, –±–Њ–ї—М –њ—А–Є —Д–∞–љ—В–Њ–Љ–љ–Њ––±–Њ–ї–µ–≤–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ, –±–Њ–ї—М –њ—А–Є —Б–Њ–Љ–∞—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ (—Б–Њ–Љ–∞—В–Њ—Д–Њ—А–Љ–љ–Њ–Љ) —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–µ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П —В–µ–Њ—А–Є–Є –Љ–љ–Њ–≥–Њ—Д–∞–Ї—В–Њ—А–љ–Њ–≥–Њ –Є –Љ–љ–Њ–≥–Њ—Г—А–Њ–≤–љ–µ–≤–Њ–≥–Њ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є –≤–Њ—Б–њ—А–Є—П—В–Є—П –±–Њ–ї–Є, —Б–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ—В–Њ—А—Л–Љ –≤–Њ—Б–њ—А–Є—П—В–Є–µ –Є –њ–µ—А–µ–і–∞—З–∞ –±–Њ–ї–µ–≤—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є –Ј–∞–≤–Є—Б—П—В –љ–µ —В–Њ–ї—М–Ї–Њ –Њ—В —Б—В–Є–Љ—Г–ї–∞ —А–µ—Ж–µ–њ—В–Њ—А–∞, –љ–Њ –Є –Њ—В —Б–Њ—Б—В–Њ—П–љ–Є—П –≤–Њ—Б–њ—А–Є–љ–Є–Љ–∞—О—Й–µ–≥–Њ —Ж–µ–љ—В—А–∞, –љ–µ–є—А–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є, –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є (–Љ—Л—Б–ї–Є—В–µ–ї—М–љ–Њ–є) —Б—Д–µ—А—Л.
–Ъ–ї–Є–љ–Є—Ж–Є—Б—В–∞–Љ —Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–∞ –≤—Л—А–∞–ґ–µ–љ–љ–∞—П —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —А–µ–∞–Ї—Ж–Є—П —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–µ–љ–Є–µ–Љ, —Б–≤–Њ–є—Б—В–≤–µ–љ–љ–∞—П —Б–µ—А–і–µ—З–љ–Њ–є –±–Њ–ї–Є. –Э–∞ —П–Ј—Л–Ї–∞—Е —А–∞–Ј–љ—Л—Е –љ–∞—А–Њ–і–Њ–≤ –Љ–Є—А–∞ —Б–µ—А–і—Ж–µ –Є–Љ–µ–µ—В —Б–Є–Љ–≤–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П –Љ–µ—В–∞—Д–Њ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –≤—Л—А–∞–ґ–µ–љ–Є—П —Н–Љ–Њ—Ж–Є–є. –°–ї–Њ–≤–∞ «–і—Г—И–µ–≤–љ—Л–є» –Є «—Б–µ—А–і–µ—З–љ—Л–є» —П–≤–ї—П—О—В—Б—П —Б–Є–љ–Њ–љ–Є–Љ–∞–Љ–Є. –°–µ—А–і—Ж–µ —А–µ–∞–≥–Є—А—Г–µ—В –љ–∞ —А–∞–і–Њ—Б—В—М –Є –≥–Њ—А–µ, –Њ–љ–Њ «—З—Г–≤—Б—В–≤—Г–µ—В, –њ–Њ–µ—В, —А–∞–Ј—А—Л–≤–∞–µ—В—Б—П, —Б—В–Њ–љ–µ—В, –њ–ї–∞—З–µ—В, —В–Њ—Б–Ї—Г–µ—В, –ї–Є–Ї—Г–µ—В». –≠–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–Љ–Є—Б—П –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є, —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П –≤—А–∞—З–∞–Љ–Є –Њ–±—Й–µ—Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Є, –Ї–∞–Ї –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ—Л–µ –Є –љ–µ–Є–Ј–±–µ–ґ–љ—Л–µ —Б–њ—Г—В–љ–Є–Ї–Є —Б–µ—А–і–µ—З–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є–ї–Є –ґ–µ –Ї–∞–Ї –µ–≥–Њ —Б–Є–Љ–њ—В–Њ–Љ—Л. –Я—А–Є —Н—В–Њ–Љ –љ–µ–і–Њ–Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –Є—Е —В—П–ґ–µ—Б—В—М –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ, –љ–µ —Г—З–Є—В—Л–≤–∞–µ—В—Б—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–°–≤—П–Ј—М –Љ–µ–ґ–і—Г —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞
–Т –ї–Є—В–µ—А–∞—В—Г—А–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е –ї–µ—В –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –љ–∞—Б—В—А–Њ–µ–љ–Є—П (–і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є –Є —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є) –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–c–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞. –Я–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В—М (—Б–Њ—Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є–µ) —Н—В–Є—Е —Д–Њ—А–Љ –њ–∞—В–Њ–ї–Њ–≥–Є–Є, —З—В–Њ –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –Њ—Б–Њ–±–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ —Б–≤—П–Ј–Є c —И–Є—А–Њ–Ї–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О —В—А–µ–≤–Њ–ґ–љ—Л—Е –Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Ї–∞–Ї –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є (2,5–11,3%) , —В–∞–Ї –Є, –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±—Й–µ—Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–ї–Є–Ї–ї–Є–љ–Є–Ї, —Б—В–∞—Ж–Є–Њ–љ–∞—А–Њ–≤ –Є —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Њ—В–і–µ–ї–µ–љ–Є–є (22–47%).
–°–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —П–≤–ї—П—О—В—Б—П –Њ–і–љ–Є–Љ–Є –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б–љ–Є–ґ–∞—О—Й–Є—Е —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°—Г—Й–µ—Б—В–≤—Г—О—В —А–∞–Ј–ї–Є—З–љ—Л–µ –≥–Є–њ–Њ—В–µ–Ј—Л –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Т–Њ–Ј–Љ–Њ–ґ–љ—Л –≤–∞—А–Є–∞–љ—В—Л —Б–Њ—З–µ—В–∞–љ–Є—П —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ф–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ, —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Љ–Њ–≥—Г—В –±—Л—В—М –њ–µ—А–≤–Є—З–љ—Л–Љ–Є, —В.–µ. –њ—А–µ–і—И–µ—Б—В–≤–Њ–≤–∞—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—О —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Љ–Њ–≥—Г—В —Б–Њ–њ—Г—В—Б—В–≤–Њ–≤–∞—В—М –µ–Љ—Г –Є–ї–Є –ґ–µ —А–∞–Ј–≤–Є–≤–∞—В—М—Б—П –≤—В–Њ—А–Є—З–љ–Њ –љ–∞ –µ–≥–Њ —Д–Њ–љ–µ. –§–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ –Ї–∞–Ї —Б –Њ—Б–Њ–Ј–љ–∞–љ–Є–µ–Љ —Д–∞–Ї—В–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —В–∞–Ї –Є —Б –µ–≥–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є, –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—П–Љ–Є –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–Я—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Л—П–≤–Є–ї–Є, —З—В–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –љ–µ–є—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ, –љ–µ–є—А–Њ—Н–љ–і–Њ–Ї—А–Є–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е –Љ–Њ–≥—Г—В —П–≤–ї—П—В—М—Б—П –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ, –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—Й–Є–Љ –њ–Њ–≤—Л—И–µ–љ–љ—Г—О —Г—П–Ј–≤–Є–Љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е –і–µ–њ—А–µ—Б—Б–Є–µ–є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –≠—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤–Ї–ї—О—З–∞—О—В –≥–Є–њ–µ—А–∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є–Љ–њ–∞—В–Њ–∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л, —Б–љ–Є–ґ–µ–љ–љ—Г—О –≤–∞—А–Є–∞—В–Є–≤–љ–Њ—Б—В—М —З–∞—Б—В–Њ—В—Л —Б–µ—А–і–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–є —Б–µ—А–Њ—В–Њ–љ–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л (—Г—Б–Є–ї–µ–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤), –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤—Г—О –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ—Б—В—М –≤ –Њ—В–≤–µ—В –љ–∞ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —Б—В—А–µ—Б—Б –Є –Є—И–µ–Љ–Є—О –Љ–Є–Њ–Ї–∞—А–і–∞. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –і–∞–ї–Є –Њ–±—К—П—Б–љ–µ–љ–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В–Є –і–µ–њ—А–µ—Б—Б–Є–Є –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, —Б—В–∞–ї–Є –Љ–Њ—Б—В–Њ–Љ –Љ–µ–ґ–і—Г –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є –њ—Б–Є—Е–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–∞–Љ–Є, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є – —Б –і—А—Г–≥–Њ–є, –Є–≥—А–∞—О—Й–Є–Љ–Є –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є —Н—В–Є—Е —Д–Њ—А–Љ –њ–∞—В–Њ–ї–Њ–≥–Є–Є.
–Я—А–Њ–±–ї–µ–Љ—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є —В–µ—А–∞–њ–Є–Є
–С–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –Є –≤ —В–Њ –ґ–µ –≤—А–µ–Љ—П –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ —В—А—Г–і–љ–Њ—Б—В–Є –≤—Л–Ј—Л–≤–∞—О—В –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ї–Њ—В–Њ—А—Л—Е —Б—Е–Њ–і–љ—Л —Б —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є – —Б–Њ–Љ–∞—В–Њ—Д–Њ—А–Љ–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, —Б–Њ–Љ–∞—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ, –Љ–∞—Б–Ї–Є—А–Њ–≤–∞–љ–љ—Л–µ –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П. –Т –Њ–±—Й–µ—Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Г —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ—А–µ–і–Ї–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—А—Г–µ—В—Б—П —Б–Є–љ–і—А–Њ–Љ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–Є—Б—В–Њ–љ–Є–Є, –∞ —В–µ –Є–ї–Є –Є–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –і–µ–њ—А–µ—Б—Б–Є–Є –Є —В—А–µ–≤–Њ–≥–Є –Њ—Б—В–∞—О—В—Б—П –љ–µ–≤—Л—П–≤–ї–µ–љ–љ—Л–Љ–Є. –Я–∞—Ж–Є–µ–љ—В—Л –љ–µ –њ–Њ–ї—Г—З–∞—О—В –∞–і–µ–Ї–≤–∞—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —Б—В–∞–љ–Њ–≤—П—В—Б—П –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ–Є –њ–Њ—Б–µ—В–Є—В–µ–ї—П–Љ–Є —А–∞–є–Њ–љ–љ—Л—Е –њ–Њ–ї–Є–Ї–ї–Є–љ–Є–Ї, –Ї–Њ–љ—Б—Г–ї—М—В–∞—В–Є–≤–љ–Њ––і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є—Е —Ж–µ–љ—В—А–Њ–≤.
–Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –Є –Ј–љ–∞—З–Є–Љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —П–≤–ї—П–µ—В—Б—П –±–Њ–ї—М –≤ –Њ–±–ї–∞—Б—В–Є —Б–µ—А–і—Ж–∞. –Ф–ї—П –Ї–∞—А–і–Є–∞–ї–≥–Є–є —Б–≤–Њ–є—Б—В–≤–µ–љ–љ–Њ –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Њ–≤ –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є, –Є—Е –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є. –Я—А–Њ—П–≤–ї–µ–љ–Є—П –Ї–∞—А–і–Є–∞–ї–≥–Є–є —З–∞—Б—В–Њ –љ–µ—В–Є–њ–Є—З–љ—Л –і–ї—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Ї–∞–Ї–Њ–≥–Њ––ї–Є–±–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Н—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –Ї–∞—А–і–Є–∞–ї–≥–Є–є —Г –ґ–µ–љ—Й–Є–љ –≤ –њ–µ—А–Є–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ. –С–Њ–ї–Є –≤ –Њ–±–ї–∞—Б—В–Є —Б–µ—А–і—Ж–∞ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –і–ї—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б–µ—А–і—Ж–∞ (–Ш–С–°, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П, –Ї–ї–Є–Љ–∞–Ї—В–µ—А–Є—З–µ—Б–Ї–∞—П –Љ–Є–Њ–Ї–∞—А–і–Є–Њ–і–Є—Б—В—А–Њ—Д–Є—П –Є –і—А.), —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л (—Б–Є–љ–і—А–Њ–Љ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–Є—Б—В–Њ–љ–Є–Є), –∞ —В–∞–Ї–ґ–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–Њ—А–Љ —Н–Ї—Б—В—А–∞–Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є (–љ–∞–њ—А–Є–Љ–µ—А, —А–µ—Д–ї–µ–Ї—В–Њ—А–љ—Л–µ –±–Њ–ї–Є –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Њ–њ–Њ—А–љ–Њ––і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є, –Љ—Л—И–µ—З–љ–Њ–є —Б–Є—Б—В–µ–Љ, –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Є –і—А.) –Э–∞–Є–±–Њ–ї—М—И–µ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –њ—А–Є–≤–ї–µ–Ї–∞—О—В –Ї —Б–µ–±–µ –Ї–∞—А–і–Є–∞–ї–≥–Є–Є –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Є—Е —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О, –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М—О.
–Ь–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–µ —Д–Њ—А–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ї–∞—А–і–Є–∞–ї–≥–Є–є, —Б–ї–Њ–ґ–љ–Њ—Б—В—М, –њ–Њ–ї–Є–Љ–Њ—А—Д–љ–Њ—Б—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л —Г—З–∞—Б—В–Є–µ–Љ –≤ –Є—Е —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–∞–љ–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤: —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –Ї–∞—А–і–Є–∞–ї—М–љ—Л—Е, –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е, –љ–µ–є—А–Њ—Н–љ–і–Њ–Ї—А–Є–љ–љ—Л—Е, –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е (–і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е, —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е), –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е.
–Я–Њ –і–∞–љ–љ—Л–Љ —А—П–і–∞ –∞–≤—В–Њ—А–Њ–≤, –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ –Є —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Њ—В–Љ–µ—З–∞—О—В—Б—П —Г 20–70% –±–Њ–ї—М–љ—Л—Е —Б –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ш–С–°, –њ—А–Є –Ї–ї–Є–Љ–∞–Ї—В–µ—А–Є—З–µ—Б–Ї–Њ–є –Љ–Є–Њ–Ї–∞—А–і–Є–Њ–і–Є—Б—В—А–Њ—Д–Є–Є –≤ 40–80%, –њ—А–Є —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є —Н–Ї—Б—В—А–∞–Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є (—В–Њ—А–∞–Ї–∞–ї–≥–Є–Є) – –≤ 60–80% –љ–∞–±–ї—О–і–µ–љ–Є–є. –Я—А–Є —Н—В–Њ–Љ 50–90% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Г–Ї–∞–Ј–∞–љ–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –љ–µ –њ–Њ–ї—Г—З–∞—О—В –∞–і–µ–Ї–≤–∞—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–∞–ґ–µ –њ—А–Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є –і–Є–∞–≥–љ–Њ–Ј–∞. –Э–∞–ї–Є—З–Є–µ –і–µ–њ—А–µ—Б—Б–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л —Г—В—П–ґ–µ–ї—П–µ—В –Ї–∞—А—В–Є–љ—Г –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Є –Ш–С–° —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і–Є–Ї—В–Њ—А–Њ–Љ –њ–Њ–≤—В–Њ—А–љ—Л—Е –Є–љ—Д–∞—А–Ї—В–Њ–≤ –Љ–Є–Њ–Ї–∞—А–і–∞, –≤–љ–µ–Ј–∞–њ–љ–Њ–є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є —Б–Љ–µ—А—В–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є —Д–Є–±—А–Є–ї–ї—П—Ж–Є–µ–є –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤, –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е, —Б–љ–Є–ґ–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–±–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є.
–Э–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–Њ–є —П–≤–ї—П–µ—В—Б—П —В–∞–Ї–ґ–µ –њ—А–Њ–±–ї–µ–Љ–∞ —В–µ—А–∞–њ–Є–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е –Є —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞, –њ—А–Њ—П–≤–ї—П—О—Й–Є—Е—Б—П –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є. –°–ї–Њ–ґ–љ–Њ—Б—В—М –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –љ–∞–ї–Є—З–Є–Є —Г –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –≥—А—Г–њ–њ, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —В—А–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є—Е, –њ–Њ–±–Њ—З–љ—Л—Е –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ (–Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є—П, –љ–∞—А—Г—И–µ–љ–Є–µ –≤–љ—Г—В—А–Є—Б–µ—А–і–µ—З–љ–Њ–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є). –Ґ—А–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В —А–Є—Б–Ї –∞—А–Є—В–Љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–С–°. –Т–љ–µ–і—А–µ–љ–Є–µ –≤ –њ—А–∞–Ї—В–Є–Ї—Г —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ (—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Њ–±—А–∞—В–љ–Њ–≥–Њ –Ј–∞—Е–≤–∞—В–∞ —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞, —Б—В–Є–Љ—Г–ї—П—В–Њ—А –Њ–±—А–∞—В–љ–Њ–≥–Њ –Ј–∞—Е–≤–∞—В–∞ —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞ –Є –і—А.), –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Є—Б—В–µ–Љ—Г (—Б–µ—А—В—А–∞–ї–Є–љ, —В–Є–∞–љ–µ–њ—В–Є–љ) –Є–ї–Є –≤–ї–Є—П—О—Й–Є—Е –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ (—Д–ї—Г–Њ–Ї—Б–µ—В–Є–љ) –Њ–њ—А–µ–і–µ–ї—П–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —А–∞–Ј—А–∞–±–Њ—В–Ї–Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –Є—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П. –£ –≤—А–∞—З–µ–є –Њ–±—Й–µ—Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Є –љ–µ –≤—Б–µ–≥–і–∞ –Є–Љ–µ–µ—В—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –њ–Њ–ї–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Њ –њ—А–∞–≤–Є–ї–∞—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є—П, –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –Є –і–Њ–ї–≥–Њ—Б—А–Њ—З–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–∞—Е –∞–љ–Ї—Б–Є–Њ–ї–Є—В–Є–Ї–Њ–≤ —В–Є–њ–∞ –∞–ї–њ—А–∞–Ј–Њ–ї–∞–Љ–∞, –і—А—Г–≥–Є—Е —В—А–∞–љ–Ї–≤–Є–ї–Є–Ј–∞—В–Њ—А–Њ–≤ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞.
–†–µ–Ј—Г–ї—М—В–∞—В—Л —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–°–ї–Њ–ґ–љ—Л–є, –Љ–љ–Њ–≥–Њ—Г—А–Њ–≤–љ–µ–≤—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –±–Њ–ї–Є, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л–є –љ–∞ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–Є —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е (–Ї–∞—А–і–Є–∞–ї—М–љ—Л—Е) –Є –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Њ–њ—А–µ–і–µ–ї—П–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –Љ–µ–ґ–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї —А–µ—И–µ–љ–Є—О –њ—А–Њ–±–ї–µ–Љ—Л –Ї–ї–Є–љ–Є–Ї–Є –Є —В–µ—А–∞–њ–Є–Є –Ї–∞—А–і–Є–∞–ї–≥–Є–Є —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П.
–¶–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–Є–ї–Њ—Б—М –Є–Ј—Г—З–µ–љ–Є–µ –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е, –Ї–ї–Є–љ–Є–Ї–Њ––њ—Б–Є—Е–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –±–Њ–ї—М–љ—Л—Е —Б –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞, —Г—В–Њ—З–љ–µ–љ–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ––±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є –Є –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л–Љ–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ –Є —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞. –Я—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –≤–ї–Є—П–љ–Є—П –њ—Б–Є—Е–Њ—Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –љ–∞ –Ї–ї–Є–љ–Є–Ї–Њ–—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б–Њ–≤–Љ–µ—Б—В–љ–Њ —Б–Њ—В—А—Г–і–љ–Є–Ї–∞–Љ–Є –Э–Ш–Ш –њ—Б–Є—Е–Є–∞—В—А–Є–Є –Ь–Ч –†–§ –Є –Ї–∞—Д–µ–і—А—Л –≤–љ—Г—В—А–µ–љ–љ–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є N1 –Ь–Ь–°–£ –Є–Љ. –Э.–Р. –°–µ–Љ–∞—И–Ї–Њ.
–° —Г—З–µ—В–Њ–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –Њ —А–Њ–ї–Є –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –њ—Б–Є—Е–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е (–≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е, —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е) —Д–∞–Ї—В–Њ—А–Њ–≤ –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –Ї–∞—А–і–Є–∞–ї–≥–Є–є –і–ї—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М —Б–њ–µ—Ж–Є–∞–ї—М–љ–∞—П –Ї–∞—А—В–∞, –≤–Ї–ї—О—З–∞—О—Й–∞—П 50 –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е –Є 146 —А–∞–љ–ґ–Є—А–Њ–≤–∞–љ–љ—Л—Е —Д–µ–љ–Њ–Љ–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ (—А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–∞—П –њ—А–Њ—Д–µ—Б—Б–Њ—А–Њ–Љ –Т.–Э. –Ъ—А–∞—Б–љ–Њ–≤—Л–Љ –Є –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–∞—П —Б —Г—З–µ—В–Њ–Љ —Ж–µ–ї–µ–є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П), –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —И–Ї–∞–ї–∞ —Б–∞–Љ–Њ–Њ—В—З–µ—В–∞ SCL–90, —И–Ї–∞–ї–∞ —В—А–µ–≤–Њ–≥–Є –У–∞–Љ–Є–ї—М—В–Њ–љ–∞ (HARS), –Ь–∞–Ї––У–Є–ї–ї–Њ–≤—Б–Ї–Є–є –±–Њ–ї–µ–≤–Њ–є –Њ–њ—А–Њ—Б–љ–Є–Ї (MPQ), –Ґ–Њ—А–Њ–љ—В—Б–Ї–∞—П —И–Ї–∞–ї–∞ –∞–ї–µ–Ї—Б–Є—В–Є–Љ–Є–Є (TAS).
–Ф–ї—П –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є–Є —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Ї–∞—А–і–Є–∞–ї–≥–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Њ–њ—А–Њ—Б–љ–Є–Ї, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ—Л–є –Т.–Ш. –Ь–∞–Ї–Њ–ї–Ї–Є–љ—Л–Љ. –° —Ж–µ–ї—М—О –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Ї–ї–Є–љ–Є–Ї–Њ–—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤–Ї–ї—О—З–∞–≤—И–µ–µ —Б—Г—В–Њ—З–љ–Њ–µ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ –≠–Ъ–У –Є –Р–Ф, —В–µ—Б—В —Б –і–Њ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Њ–є –љ–∞ —В—А–µ–і–Љ–Є–ї–µ.
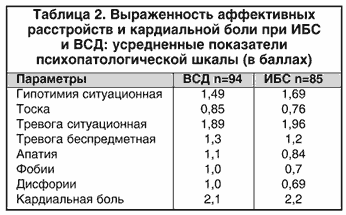
–С—Л–ї–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ—Л 85 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞ (–Ш–С–° – 1 –≥—А—Г–њ–њ–∞) –Є 94 –њ–∞—Ж–Є–µ–љ—В–∞ —Б –≤–µ–≥–µ—В–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–Є—Б—В–Њ–љ–Є–µ–є (–Т–°–Ф – 2 –≥—А—Г–њ–њ–∞). –Т –≥—А—Г–њ–њ—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–Њ—И–ї–Є —В–Њ–ї—М–Ї–Њ –ґ–µ–љ—Й–Є–љ—Л. –Т—Л–±–Њ—А –≥—А—Г–њ–њ—Л –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –∞–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М—О –і–ї—П —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є –Є–Ј—Г—З–µ–љ–Є—П –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Б–µ—А–і–µ—З–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Г –ґ–µ–љ—Й–Є–љ. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —В–µ–Љ, —З—В–Њ —Г –ґ–µ–љ—Й–Є–љ —З–∞—Й–µ, —З–µ–Љ —Г –Љ—Г–ґ—З–Є–љ –љ–∞–±–ї—О–і–∞—О—В—Б—П –∞—В–Є–њ–Є—З–љ—Л–µ (–і–ї—П —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є) –Ї–∞—А–і–Є–∞–ї—М–љ—Л–µ –±–Њ–ї–Є –њ—А–Є –Ш–С–°. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—В–Є–њ–Є—З–љ—Л–Љ–Є –±–Њ–ї—П–Љ–Є –≤ —Б–µ—А–і—Ж–µ –Њ–Ї–Њ–ї–Њ 90% —Б–Њ—Б—В–∞–≤–ї—П—О—В –ґ–µ–љ—Й–Є–љ—Л. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї 50 –≥–Њ–і–∞–Љ –ґ–µ–љ—Й–Є–љ—Л —Б—А–∞–≤–љ–Є–≤–∞—О—В—Б—П —Б –Љ—Г–ґ—З–Є–љ–∞–Љ–Є –њ–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Ш–С–°, –∞ –≤ –њ–µ—А–Є–Њ–і –Љ–µ–љ–Њ–њ–∞—Г–Ј—Л –Њ–њ–µ—А–µ–ґ–∞—О—В –Љ—Г–ґ—З–Є–љ –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –Њ—Б—В—А—Л—Е –Є–љ—Д–∞—А–Ї—В–Њ–≤ –Љ–Є–Њ–Ї–∞—А–і–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —В—П–ґ–µ–ї–Њ –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е (—В–∞–±–ї. 1).

–Т—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–Љ–Є –і–ї—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ш–С–° —П–≤–ї—П—О—В—Б—П —В–∞–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –±–Њ–ї–Є, –Ї–∞–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –µ–µ –њ—А–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–µ, –њ—А–µ–Ї—А–∞—Й–µ–љ–Є–µ –≤ –њ–Њ–Ї–Њ–µ –Є –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –љ–Є—В—А–Њ–≥–ї–Є—Ж–µ—А–Є–љ–∞, –∞ —В–∞–Ї–ґ–µ –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є—П –Ј–∞ –≥—А—Г–і–Є–љ–Њ–є. –£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –≥—А—Г–њ–њ—Л –Ш–С–° –≤—Б—В—А–µ—З–∞–ї–Њ—Б—М —Б–Њ—З–µ—В–∞–љ–Є–µ —В—А–µ—Е –Є –±–Њ–ї–µ–µ –Є–Ј –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤. –Э–∞—А—П–і—Г —Б –≤—Л—И–µ–Њ–њ–Є—Б–∞–љ–љ—Л–Љ–Є –±–Њ–ї—П–Љ–Є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ–Є –і–ї—П —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є, —Г —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е –Ш–С–° –≤ 45% –љ–∞–±–ї—О–і–µ–љ–Є–є –Њ—В–Љ–µ—З–µ–љ—Л —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –Ї–∞—А–і–Є–∞–ї–≥–Є–Є.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –Т–°–Ф –Ї–∞—А–і–Є–∞–ї–≥–Є–Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Є—Б—М –њ–Њ–ї–Є–Љ–Њ—А—Д–љ–Њ—Б—В—М—О, –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —Б–≤—П–Ј–Є —Б —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Њ–є –Є —З–µ—В–Ї–Њ–є, –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–µ–є. –С–Њ–ї–µ–µ 75% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –Њ–±–µ–Є—Е –≥—А—Г–њ–њ —Б–≤—П–Ј—Л–≤–∞–ї–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –±–Њ–ї–Є —Б –њ—Б–Є—Е–Њ–≥–µ–љ–љ—Л–Љ –њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞–љ–Є–µ–Љ.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –∞–љ–∞–ї–Є–Ј–∞ –≥–Є—Б—В–Њ–≥—А–∞–Љ–Љ –Є–љ—В–µ—А–≤–∞–ї–Њ–≤ R–R –Є –Є—Е –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е, –∞–љ–∞–ї–Є–Ј–∞ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П —Н–њ–Є–Ј–Њ–і–Њ–≤ —В–∞—Е–Є–Ї–∞—А–і–Є–Є –Є –±—А–∞–і–Є–Ї–∞—А–і–Є–Є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –≠–Ъ–У, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–≥–Њ –Є–љ–і–µ–Ї—Б–∞ –Ъ–µ—А–і–Њ –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є –љ–∞–ї–Є—З–Є–µ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —З–∞—Б—В–Њ—В—Л –љ–∞—А—Г—И–µ–љ–Є–є –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є —Б–µ—А–і—Ж–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –Њ–±–µ–Є—Е –≥—А—Г–њ–њ, –њ—А–Є —Н—В–Њ–Љ –≥–∞—А–Љ–Њ–љ–Є—З–љ–Њ–µ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–µ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ (—Н–є—В–Њ–љ–Є—П) –≤—Л—П–≤–ї—П–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–µ–ґ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–Њ—А–Љ–Њ–є.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –±–Њ–ї—М—О –≤ —Б–µ—А–і—Ж–µ –≤—Л—П–≤–ї—П–ї–Є—Б—М —А–∞–Ј–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –≤–ї–Є—П–љ–Є—П –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ–ї–Є –Њ—В—З–µ—В–ї–Є–≤—Г—О —Б–≤—П–Ј—М —Б —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, –∞ —В–∞–Ї–ґ–µ —Б —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–є –Ї–∞—А—В–Є–љ–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –Є–љ—В–µ—А–µ—Б –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ –њ—А–Њ–≥–љ–Њ–Ј–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т –≥—А—Г–њ–њ–µ –Ш–С–° –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–Ї–∞–Љ–Є —Б –Т–°–Ф –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –њ–Њ–љ–Є–ґ–µ–љ–Є–µ —В–Њ–љ—Г—Б–∞ –њ–∞—А–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–≤–µ–љ–∞ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л (—В–∞–Ї –ґ–µ, –Ї–∞–Ї –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є), —З—В–Њ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А—М–µ–Ј–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Я—А–Є –Ї–ї–Є–љ–Є–Ї–Њ––њ—Б–Є—Е–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ –Є —В—А–µ–≤–Њ–ґ–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Ї–∞–Ї —Б–Є—В—Г–∞—Ж–Є–Њ–љ–љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ, —В–∞–Ї –Є –љ–µ –Є–Љ–µ–≤—И–Є–µ –≤–Є–і–Є–Љ–Њ–є —Б–≤—П–Ј–Є —Б –њ—Б–Є—Е–Њ–≥–µ–љ–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –∞–њ–∞—В–Є—П, –і–Є—Б—Д–Њ—А–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М, —Б–µ–љ—Б–Њ—А–љ–∞—П –≥–Є–њ–µ—А–µ—Б—В–µ–Ј–Є—П, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, —Б–љ–Є–ґ–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –њ–Њ–±—Г–ґ–і–µ–љ–Є–є, –∞–љ–≥–µ–і–Њ–љ–Є—П, —Д–Њ–±–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П.
–Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤ —В–∞–±–ї–Є—Ж–µ 2 –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В, —З—В–Њ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –љ–∞–Є–±–Њ–ї—М—И–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–ї–Є —Б–Є—В—Г–∞—Ж–Є–Њ–љ–љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ —В—А–µ–≤–Њ–≥–∞ –Є –≥–Є–њ–Њ—В–Є–Љ–Є—П, –±–µ—Б–њ—А–µ–і–Љ–µ—В–љ–∞—П —В—А–µ–≤–Њ–≥–∞. –Т—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —В–Њ—Б–Ї–Є, –∞–њ–∞—В–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Т–°–Ф –±—Л–ї–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –≤—Л—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –Ш–С–°.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ SCL–90 –њ–Њ–Ј–≤–Њ–ї–Є–ї–Є –≤—Л—П–≤–Є—В—М –њ—А–µ–≤—Л—И–µ–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ —И–Ї–∞–ї–∞–Љ —Г 87% –±–Њ–ї—М–љ—Л—Е –Ш–С–° –≥—А—Г–њ–њ—Л –Є —Г 80% – –≥—А—Г–њ–њ—Л –Т–°–Ф. –Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ –Ј–љ–∞—З–µ–љ–Є—П, —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–∞–Ј–ї–Є—З–∞—О—Й–Є–µ—Б—П —Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є —Г—Б–ї–Њ–≤–љ–Њ–є –љ–Њ—А–Љ—Л, –≤—Л—П–≤–ї–µ–љ—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –њ–Њ —И–Ї–∞–ї–∞–Љ —Б–Њ–Љ–∞—В–Є–Ј–∞—Ж–Є–Є, –і–µ–њ—А–µ—Б—Б–Є–Є, —В—А–µ–≤–Њ–≥–Є, –Њ–±—Б–µ—Б—Б–Є–≤–љ–Њ––Ї–Њ–Љ–њ—Г–ї—М—Б–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –≤—А–∞–ґ–і–µ–±–љ–Њ—Б—В–Є. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –Ј–љ–∞—З–Є–Љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –Њ—В—Б—Г—В—Б—В–≤—Г—О—В.
–° —Ж–µ–ї—М—О –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Е–∞—А–∞–Ї—В–µ—А–∞ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –Ь–∞–Ї––У–Є–ї–ї–Њ–≤—Б–Ї–Є–є –±–Њ–ї–µ–≤–Њ–є –Њ–њ—А–Њ—Б–љ–Є–Ї (MPQ). –†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П —Б—Г–Љ–Љ–∞—А–љ—Л—Е –Є–љ–і–µ–Ї—Б–Њ–≤ –±–Њ–ї–Є (—В.–µ. –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–Є) –≤ –≥—А—Г–њ–њ–µ —Б –Ш–С–° –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—И–µ, —З–µ–Љ –њ—А–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Ї–∞—А–і–Є–∞–ї–≥–Є—П—Е. –Т—Л—П–≤–ї–µ–љ–Њ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ —Б–µ–љ—Б–Њ—А–љ–Њ–≥–Њ (—З—Г–≤—Б—В–≤–µ–љ–љ–Њ–≥–Њ, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ) –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –љ–∞–і –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ (—Ж–µ–љ—В—А–∞–ї—М–љ—Л–Љ) —Г –±–Њ–ї—М–љ—Л—Е —Б –Ш–С–°, –∞ —В–∞–Ї–ґ–µ –µ–≥–Њ –±–Њ–ї—М—И–∞—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Б–µ–љ—Б–Њ—А–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –≤ –≥—А—Г–њ–њ–µ –Т–°–Ф. –Я—А–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Ї–∞—А–і–Є–∞–ї–≥–Є—П—Е –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М —Б–µ—А–і–µ—З–љ–Њ–є –±–Њ–ї–Є –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –∞—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ (—Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ) –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞.
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ґ–Њ—А–Њ–љ—В—Б–Ї–Њ–є —И–Ї–∞–ї—Л –∞–ї–µ–Ї—Б–Є—В–Є–Љ–Є–Є (TAS) –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Ш–С–°, –Њ—В—А–∞–ґ–∞—О—Й–Є–µ –Є—Е –±–Њ–ї—М—И—Г—О —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є, –Ї —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ—Г —В–Є–њ—Г —А–µ–∞–≥–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Є —Б—В—А–µ—Б—Б–∞—Е, —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ –њ—А–Є —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –±–Њ–ї—М–љ—Л—Е –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Ь–Ъ–С–10 –≤—Л—П–≤–Є–ї–∞, —З—В–Њ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –љ–∞–Є–±–Њ–ї—М—И—Г—О —З–∞—Б—В—М —Б–Њ—Б—В–∞–≤–Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –љ–∞—Б—В—А–Њ–µ–љ–Є—П (–і–Є—Б—В–Є–Љ–Є—П, —Ж–Є–Ї–ї–Њ—В–Є–Љ–Є—П). –Ф–Њ—Б—В–∞—В–Њ—З–љ–Њ —З–∞—Б—В–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–ї–Є—Б—М –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ —Н–њ–Є–Ј–Њ–і—Л, –Ї–∞–Ї –≤–Њ–Ј–љ–Є–Ї—И–Є–µ –≤–њ–µ—А–≤—Л–µ, —В–∞–Ї –Є –њ–Њ–≤—В–Њ—А–љ—Л–µ, —Б–Љ–µ—И–∞–љ–љ—Л–µ —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ —Б–Њ—Б—В–Њ—П–љ–Є—П.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є –±–Њ–ї—М—И—Г—О —А–Њ–ї—М –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е, —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –Є –љ–µ–Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–Є—А–Њ–і—Л, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≤ —А–∞–Ј–≤–Є—В–Є–Є –Ї–∞—А–і–Є–∞–ї–≥–Є–є. –≠—В–Њ —П–≤–Є–ї–Њ—Б—М –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л–Љ –њ–∞—Ж–Є–µ–љ—В–Ї–∞–Љ —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Є –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—Г—А—Б–∞ —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ –Є –∞–љ–Ї—Б–Є–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ.
–Я—А–Є –≤—Л–±–Њ—А–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г—З–Є—В—Л–≤–∞–ї—Б—П —Б–њ–µ–Ї—В—А –њ—Б–Є—Е–Њ—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –≤–ї–Є—П–љ–Є–µ –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Э–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ —П–≤–ї—П–ї–Њ—Б—М –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ, —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–Њ–≤, –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ, —З–∞—Б—В–Њ—В—Г –Є —А–Є—В–Љ —Б–µ—А–і–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є, –≤–љ—Г—В—А–Є—Б–µ—А–і–µ—З–љ—Г—О –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В—М, —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В—М –Љ–Є–Њ–Ї–∞—А–і–∞. –≠—В–Є–Љ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В—Л –Љ–Є–∞–љ—Б–µ—А–Є–љ, —В–Є–∞–љ–µ–њ—В–Є–љ, —Б–µ—А—В—А–∞–ї–Є–љ, –∞–ї–њ—А–∞–Ј–Њ–ї–∞–Љ. 46 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –њ—А–Њ—И–ї–Є –Ї—Г—А—Б —В–µ—А–∞–њ–Є–Є –Љ–Є–∞–љ—Б–µ—А–Є–љ–Њ–Љ, 49 – —В–Є–∞–љ–µ–њ—В–Є–љ–Њ–Љ, 34 – —Б–µ—А—В—А–∞–ї–Є–љ–Њ–Љ, 50 – –∞–ї–њ—А–∞–Ј–Њ–ї–∞–Љ–Њ–Љ.
–Я—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —В–µ—А–∞–њ–Є–Є –±—Л–ї–Є —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ—Л –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –њ–Њ—Б—В–µ–њ–µ–љ–љ—Л–Љ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Є—Е –і–Њ —Г—А–Њ–≤–љ—П —В–µ—А–∞–њ–µ–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є (—В–∞–±–ї. 3).

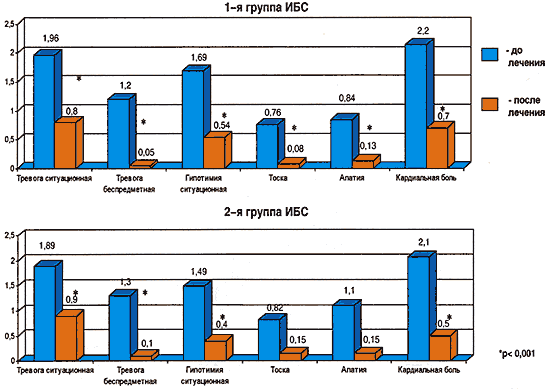
–†–Є—Б. 1. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Є –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –±–Њ–ї–Є –љ–∞ —Д–Њ–љ–µ –њ—Б–Є—Е–Њ—Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є
–Э–µ –Њ—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—П—Б—М –љ–∞ –њ–Њ–і—А–Њ–±–љ–Њ—Б—В—П—Е –і–Є–љ–∞–Љ–Є–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є —В–µ—А–∞–њ–Є–Є –Ї–∞–ґ–і—Л–Љ –Є–Ј –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ SCL–90 –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –≤—Л—П–≤–Є—В—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ (—Б–Њ–Љ–∞—В–Є–Ј–∞—Ж–Є–Є, –і–µ–њ—А–µ—Б—Б–Є–Є, —В—А–µ–≤–Њ–≥–Є, –Њ–±—Б–µ—Б—Б–Є–≤–љ–Њ––Ї–Њ–Љ–њ—Г–ї—М—Б–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –≤—А–∞–ґ–і–µ–±–љ–Њ—Б—В–Є, –Є–љ—В–µ–≥—А–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П) –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —В–µ—А–∞–њ–Є–Є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е (—А–Є—Б. 2).
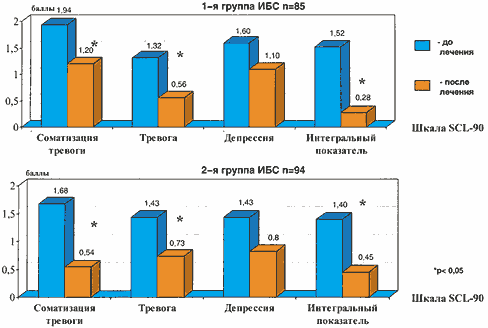
–†–Є—Б. 2. –Ф–Є–љ–∞–Љ–Є–Ї–∞ —Б—А–µ–і–љ–Є—Е –Ј–љ–∞—З–µ–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —И–Ї–∞–ї SCL-90 –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —В–µ—А–∞–њ–Є–Є
–Ш–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —И–Ї–∞–ї—Л —В—А–µ–≤–Њ–≥–Є –У–∞–Љ–Є–ї—М—В–Њ–љ–∞ (HARS) –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —В–µ—А–∞–њ–Є–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–є —В—А–µ–≤–Њ–≥–Є –њ—А–Є –Ї–∞—А–і–Є–∞–ї–≥–Є—П—Е –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ –≤ –≥—А—Г–њ–њ–µ –Ш–С–° –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —В—А–µ–≤–Њ–≥–Є —Б–Њ—Е—А–∞–љ—П–ї—Б—П –љ–∞ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Ї–∞—А–і–Є–∞–ї–≥–Є–є. –Т–µ—А–Њ—П—В–љ–Њ, —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–Є—А–Њ–і–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ–Љ –ґ–∞–ї–Њ–± –Є—Б—В–Є–љ–љ–Њ–є –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –њ—А–Є—А–Њ–і—Л (—В–∞–±–ї. 4).

–Э–∞ —Д–Њ–љ–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є 69,2% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –Ш–С–° –Є 87,3% –±–Њ–ї—М–љ—Л—Е —Б –Т–°–Ф –Њ—В–Љ–µ—З–∞–ї–Є –ї—Г—З—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е –љ–∞–≥—А—Г–Ј–Њ–Ї, —Г—А–µ–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –±–Њ–ї–µ–є –≤ –Њ–±–ї–∞—Б—В–Є —Б–µ—А–і—Ж–∞, –Ї–∞–Ї –њ—А–Є—З–Є–љ—Л –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П —В–µ—Б—В–∞, –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–є —А–Њ—Б—В –Њ–±—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є —В–µ—Б—В–∞. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Р–Ф, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—Й–µ–µ –Њ–± —Н–Ї–Њ–љ–Њ–Љ–Є—З–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—А–µ—Б—Б–—В–µ—Б—В–∞, —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П, –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ —Б–Њ—Б—Г–і–Њ–і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–є —Ж–µ–љ—В—А –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е—Б—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є –Є–Љ–µ—О—Й–Є–µ—Б—П –≤ –ї–Є—В–µ—А–∞—В—Г—А–µ –і–∞–љ–љ—Л–µ –Њ —А–Њ–ї–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –і–µ–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –Ї–∞—А–і–Є–∞–ї–≥–Є–є, –Є—Е –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г, –і–Є–љ–∞–Љ–Є–Ї—Г —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –≠—В–Њ —П–≤–Є–ї–Њ—Б—М –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ, –∞–љ–Ї—Б–Є–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П –Є –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л–Љ–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є. –Р–љ–∞–ї–Є–Ј –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е, —В—А–µ–≤–Њ–ґ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, —Б–Њ–Љ–∞—В–Њ––≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є, –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –±–Њ–ї–Є, —Г–ї—Г—З—И–µ–љ–Є—П –Њ–±—Й–µ–≥–Њ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є–Є –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П, –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ —Б–Њ—Б—Г–і–Њ–і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–є —Ж–µ–љ—В—А.
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ, –∞–љ–Ї—Б–Є–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ –±–Њ–ї—М–љ—Л–Љ —Б –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л–Љ–Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є.
–°–њ–Є—Б–Њ–Ї –ї–Є—В–µ—А–∞—В—Г—А—Л –Т—Л –Љ–Њ–ґ–µ—В–µ –љ–∞–є—В–Є –љ–∞ —Б–∞–є—В–µ http://www.rmj.ru
1. –Т–µ–є–љ –Р.–Ь. (—А–µ–і.) –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л (—А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є). – –Ь. – 1991. – 623 c.
2. –Ь–∞–Ї–Њ–ї–Ї–Є–љ –Т.–Ш., –Р–±–±–∞–Ї—Г–Љ–Њ–≤ –°.–Р., –°–∞–њ–Њ–ґ–љ–Є–Ї–Њ–≤–∞ –Р. –Р., –Э–µ–є—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–∞—П –і–Є—Б—В–Њ–љ–Є—П. – –І–µ–±–Њ–Ї—Б–∞—А—Л. – 1995. – 248 –°
3. Beitman B. D., Mukerji V., Flaker G. Panic disorder in cardiology patients with atypical chest pain in clinical aspects of panic disorders. // Edited by Ballenger J. C. – вДЦew–York. – Wiley–Liss. – 1990. – P. 111 – 137
4. Benjamin S. Psychological trearment of chronic pain: a selective review. // J. of Psychosomatic. Res. – 1989. – V.33. – P. 121 –131.
5. Carter C.S., Servan–Schreiber D., Perlstain W. M. Anxiety disorders and the syndrome of chest pain with normal coronary arteries: prevalence and pathophysiology // J. Clin. Psych. – 1997. – V. 58 (suppl 3). – P. 70–73.
6. Fava G.A., Magelli C., Savron G., Conti S. et al. Neurocirculatory asthenia: a reassessment using modern psychosomatic criteria //Acta–Psych.–Scand. – 1994. – V.89(5). – P.314–319.
7. Katon W., Lin E., Korff M., Russo J. et al. Somatization: a spectrum of severity. // Am. J. Psychiatry. – 1991. – V.148. – P.34–40.
8. Mayou R. Atypical chest pain. // J. Psychosom Res. – 1989. – V.33. – P.393–406.
9. Nutzinger D.O. The heart and anxiety. Cardiac anxiety and risk of cardiovascular morbidity in patients with an anxiety disorder //Nervenarzt. – 1992. – V.62 (2). – P. – 187–189.












