Однако не более 10% больных требуют парентерального введения лекарства в связи с отказом от таблетированных форм. Ряд больных воспринимает инъекции как репрессивную меру, свидетельство особой опасности своего состояния. Кроме того, инъекции болезненны (особенно для пациентов со сниженным болевым порогом), дорогостоящи и чреваты осложнениями (угнетение дыхания, инфильтраты).
Сероквель в связи с его безопасностью может быть назначен до получения результатов лабораторных анализов; в неотложных случаях, когда больной сопротивляется осмотру (но не приему лекарства) – до полного медицинского обследования. Возможно пробное 48–часовое лечение «пробными» дозами Сероквеля (50–100 мг) для выявления индивидуальной чувствительности пациента с оценкой его субъективной реакции [16]. Сероквель реже, чем ТН, вызывает дисфорию, эмоциональное безразличие. Такая неприятная и памятная больному ранняя симптоматика, опережающая терапевтический эффект, нередко приводит к отказу от дальнейшего лечения. Гипотензия (важно предупредить больного резко не вставать, избегать обезвоживания, особенно летом и пожилым) и сухость во рту (хороши полоскание рта, жевательная резинка без сахара) обычно редуцируются по мере адаптации к Сероквелю, как большинство ранних «общетоксических» действий нейролептиков [1].
В психогеронтологической практике актуален риск ортостатической гипотонии (предупредить резкие вставания с постели) и головокружения (с возможными падениями), тахикардии в начальной стадии лечения (начальная доза Сероквеля не должна быть более 25 мг; чем медленнее наращивание дозы, тем лучше переносится препарат). Риск желудочковой тахиаритмии при лечении Сероквелем (10%) соответствует таковому при лечении таблетированным галоперидолом и в 1,5 раза меньше, чем при лечении рисперидоном [22]. При остром лечении важна быстрота действия лекарства. Оланзапин внутрь (включая форму для рассасывания) требует 5–8 часов для того, чтобы его концентрация в плазме крови достигла максимума, пероральный галоперидол – 4 часа, рисперидон и Сероквель – 2 часа. Возможно наращивание дозы кветиапина до 800–1000 мг за 3–5 дней (по 200 мг в сутки) при асимметричном двухразовом назначении большей части препарата на ночь, по необходимости в сочетании с высокопотентными транквилизаторами (лоразепамом, феназепамом). Неспецифический успокаивающий эффект Сероквеля без гиперседации (потребность в транквилизаторах снижается) полезен для скорейшего, в течение 5–7 дней, купирования возбуждения и враждебности больных [8], положительно воспринимается больными, не препятствует детальной сомато–неврологической оценке и ранним психосоциальным мероприятиям. Пока соотношение риск/польза назначения кветиапина выше рекомендованного порога малоизучено, но и в рамках терапевтического диапазона при выборе Сероквеля (до 750 мг/сут.) происходит уменьшение психотической тревоги в течение недели [12].
Постепенное наращивание дозировок (до 400 мг/сут. за пять дней) показано пожилым и при заболеваниях печени. Дозировка Сероквеля 450 мг в сутки, примерно соответствующая 8 мг галоперидола, обычно достаточна пациентам в первом эпизоде шизофрении. Действенность (в РКИ) острого лечения Сероквелем (400–800 мг/сут.), оланзапином (10–20 мг/сут.) и рисперидоном (4–8 мг/сут.) сходна [3]. Антипсихотический эффект Сероквеля наиболее выражен к 8–12–й неделям у 50–85% пациентов [15]. Монотерапия Сероквелем позволяет избежать риска фармакокинетических взаимодействий и сложной для больного и медицинского персонала схемы лечения. Меньшая потребность в антихолинергических корректорах (циклодоле), обостряющих и затягивающих психоз, имеющих потенциал зависимости и усугубляющих когнитивные расстройства шизофрении, способствует оптимизации терапии при выборе Сероквеля.
Распространенное в повседневной практике (до 40%) сочетание Сероквеля с ТН и иными АА связано с нетерпением врача, не учитывающего риск лечения при его удорожании, затуманивание клинической картины [2]. При остром лечении пациенты предпочитают Сероквель ряду прочих АА и ТН [7], особенно те, кто избегает принимать лекарства из–за повышенной чувствительности к неврологическим и метаболическим (ожирение, гиперпролактинемия) побочным эффектам, как, например, в первом эпизоде шизофрении [3]. Так, повышение веса вызывает не меньший дистресс, чем острые неврологические расстройства, особенно у молодых девушек (группа риска), что важно при выборе антипсихотика во избежание позднейшего обрыва даже успешной клинически терапии. Риск повышения веса (у 25% больных, обычно не более 4 кг за первые 12 недель с последующим выходом на плато при годичном лечении) у Сероквеля ниже, чем у ряда АА [3].
На фоне Сероквеля изначально повышенный вес может даже снизиться. В повседневной практике, однако, большинство пациентов лечится сочетанием препаратов, в том числе и с высоким риском повышения веса (например, «классическими» трициклическими антидепрессантами, литием), а благотворный эффект Сероквеля на фоне полифармации может теряться. Поэтому актуально привитие больному навыков здорового образа жизни (физические упражнения, низкокалорийное питание). Неэффективность лечения отмечают при отсутствии положительной динамики в клинической и функциональной областях оценки, включая субъективную – самого пациента, в течение 3–8 недель после достижения терапевтической дозы Сероквеля; при частичном ответе курс лечения стоит продолжить еще на 4–10 недель.
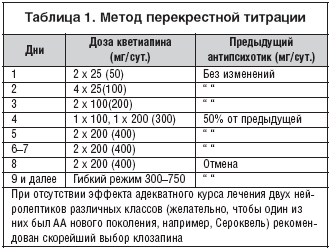
При малоэффективном лечении необходима переоценка психического и соматического состояния пациента (выявление скрытой органической неполноценности, злоупотребления психоактивными веществами, аффективных расстройств, проблем комплайнса, хронического психосоциального дистресса, повышенного уровня эмоциональных переживаний в семье). Возможно повышение дозы Сероквеля спустя 6–8 недель лечения, но следует избегать сверхвысоких доз. Практика преждевременной замены Сероквеля на другой препарат или полинейролепсия приводят к тому, что для врача остается неясной причина улучшения состояния пациента и нежелательных действий. Переход на Сероквель логичен при неконтролируемых нежелательных явлениях ТН (например, острых экстрапирамидных расстройствах) или иных АА за исключеним клозапина (например, ожирение). Желателен метод перекрестной титрации, минимизирующий риск симптомов «рикошета», порой интерпретируемых врачом, как нежелательные действия нового лечения (табл. 1)
Упорядочивающий поведение эффект Сероквеля с «дистанцированием» личности от сохраняющихся психотических переживаний позволяет на ранних этапах больничного лечения начать индивидуальные, а затем групповые психосоциальные вмешательства (обучение управлению болезнью и ее лечением), продолжаемые по выписке. Терапия включает ряд компонентов: 1) выявление и профилактика факторов рецидива, активный контроль «ранних» симптомов ухудшения; 2) неотложное лечение при их выявлении по выработанному совместно с врачом и близким кризисному плану (управление дистрессом, интенсификация наблюдения и лечения, усиление неформальной поддержки); 3) тренинг навыков эффективного совладания с симптомами и средовым (семейным) дистрессом с привлечением позитивного опыта участников группы и поведенческой техники, обучение решению типовых проблем и социальным навыкам организации лечении (поиск помощи, союз с близкими и профессионалами); 4) индивидуальная или групповая семейная терапия для эмоциональной поддержки, обучения совладанию с болезнью близкого через понимание активной роли в лечении, снижение чрезмерных эмоций как триггеров рецидива, профилактики дистресса.
По мере стабилизации состояния пациента следует переходить к долечивающей терапии эффективным при остром лечении препаратом (Сероквелем) для предупреждения ранних рецидивов и обострений, усиления и консолидации успеха терапии. По мере углубления ремиссии пациент все более выступает субъектом лечения на принципах партнерства. Психиатр (социальный работник, клинический психолог) сосредоточен на проблемах пациента за пределами защищенной среды больницы (дневного стационара): ограничивает нереалистичные ожидания и требования к функционированию пациента в его семье. Следует соблюсти баланс между стимуляцией ответственности пациента за результат лечения и предоставлением эмоциональной и социальной защиты. Важно избавить пациента и его близких от фаталистического ожидания возврата психоза, ориентировать их на здороровый образ жизни. Ведение больного фокусировано на оценке, поддержке, объяснении, укреплении чувства реальности, изменениях его поведения. Облегчение психотической симптоматики при лечении Сероквелем позволяет опосредованно освоить (восстановить) социальные навыки. Проводится групповая психосоциальная терапия для выработки навыков управления болезнью и лечением, полезно участие больного и его близких в мероприятиях общества самопомощи по месту жительства (важная часть плана лечения). Улучшение симптомов опережает улучшение социально–трудового функционирования. Характер и степень нетрудоспособности – более уместный и реальный показатель оценки результата лечения шизофрении, нежели изменение клинической картины («синдрома–мишени»). Явный признак социального восстановления больного – возвращение к занятиям, соответствующим возрасту. При персистирующих симптомах нужно усилить психосоциальное лечение (когнитиво–поведенческая терапия).
Фармакозависимые ремиссии с «зашторенной» симптоматикой, актуализирующейся при отмене или снижении доз ТН или АА у более 60% больных шизофренией, определяют продолжение лечения полными (неизменными) дозами Сероквеля большинством внебольничных больных. Схема лечения должна соответствовать ежедневному функционированию пациента, и ее следует упростить, что улучшит комплайнс и облегчит его контроль обученными близкими. Целесообразен «асимметричный» прием большей части Сероквеля в вечернее время, так как препарат в средних дозах назначают дважды в сутки, но клинический эффект у больных, получавших препарат 1 раз в сутки, сходен [13]. При выявлении ранних симптомов рецидива (тема психообразования) возможно повышение дозы Сероквеля на 100–200 мг с временным присоединением транквилизаторов.
Клинические проблемы при становлении ремиссии. Переживающие состояние «пробуждения», то есть выраженное и быстрое клиническое улучшение при лечении Сероквелем, пациенты выявляют широкий круг реакций (отчуждение заболевания, реактивная депрессия), нарушают режим терапии и потому требуют интенсивной эмоциональной поддержки, так как их «Я» не успело приспособиться к новым социальным проблемам, а семья больного не всегда способна воспринять с пониманием новую роль пациента, более привычного в заторможенном состоянии. Состояние преходяще, возможно назначение транквилизаторов на срок до недели. Негативные расстройства, их выраженность (нарастание) сложно выявить в острый период. Следует отличать вызванную, например, ТН акинезию, а также депрессивную ангедонию, параноидную асоциальность, обеднение речи при расстройствах мышления от первичных негативных симптомов. Следует объяснить близким природу изменений больного (не «леность»), осторожно подготовить их к мысли, что пациенты, возможно, не вернутся к доболезненному состоянию, а для улучшения требуются не только медикаментозные, но психосоциальные воздействия. Выступающие на передний план негативные расстройства – основание выбора Сероквеля, если он уже не назначен ранее, памятуя о его возможном антидефицитарном и улучшающем когнитивные расстройства действии (по крайней мере, он не усугубляет их нежелательными действиями), но стоит настроить семью не уповать на скорое «чудо» (для определения эффективности лечения требуется не менее полугода) и призвать к активному сотрудничеству в деле ресоциализации больного. Ведь «дефект» больного во многом – его личностная компенсаторная реакция на пренебрежение окружающих, а «выученная беспомощность» – следствие заниженных требований в больничной и внебольничной среде. Поэтому наиболее тяжелые больные должны как можно скорее направляться в реабилитационное отделение для освоения (восстановления) социальных навыков, в более легких случаях – в дневной стационар для продолжения реабилитационной программы или домой на попечение близких с обязательной связью с социальными службами. Неподготовленная выписка из больницы чревата усилением бремени шизофрении для семьи и скорым ухудшением состояния больного. Постшизофреническая депрессия возможна у 50% больных, хотя в большинстве (до 60–80%) случаев активное лечение ТН или АА (Сероквелем) и интенсивная психологическая поддержка в остром периоде способствуют разрешению депрессии в рамках психоза. При депрессии врачу предстоит исключить не выявленное ранее органическое заболевание и шизоаффективное расстройство, дистресс после перенесенного психоза, продром нового эпизода, лечить любые сопутствующие медицинские заболевания, исключить злоупотребление психоактивными веществами и неврологические нежелательные действия (акинезию, акатизию нельзя исключить при лечении любыми ТН или АА), выявить сохраняющуюся или привнесенную болезнью психотравмирующую ситуацию в семье или на работе. Необходимым условием лечения является информация родственников о риске суицидальных тенденций у пациента, создание атмосферы разумно взвешенного оптимизма. Можно предполагать, что гармоничное воздействие Сероквеля на все компоненты острого приступа позволит достичь более глубокой ремиссии (в том числе уменьшить частоту постшизофренической депрессии). При депрессии на фоне Сероквеля показано лечение антидепрессантами нового поколения не менее 6 месяцев [9,26]. При сложности отграничения депрессивной симптоматики от негативной показан пробный курс антидепрессивной терапии. Назначение антидепрессантов без Сероквеля может обострить психоз.
Несоблюдение режима лечения. Хорошая переносимость Сероквеля не служит залогом продолжения лечения без систематической психосоциальной работы с больным и его близкими, так как основные причины проблем долговременного комплайнса – внутренняя картина болезни (у больного нет потребности в лечении, он активно настроен против лекарств), неудовлетворительный терапевтический союз с врачом, незаинтересованность семьи в результатах лечения. Не менее 50% больных теряют связь с ПНД в первые месяцы после выписки из больницы. Ряд больных, прекращая лечение самовольно, отмечают, что чувствуют себя хорошо спустя 3–4 недели. Следует учесть неокончательно сформированную реакцию на острый период, уязвимость пациента к психосоциальным стрессам, возможные нежелательные действия терапии, объяснить больному и его семье, что риск ухудшения высок и он отставлен по времени, а путь к выздоровлению долог, но путь осилит идущий.
Противорецидивная (поддерживающая) терапия снижает риск рецидивов (обострений) шизофрении и, видимо, замедляет темп ее прогредиентности. Лечение необходимо до тех пор, пока сохраняется основная патология, и не подразумевает, что риск рецидива снижен после прекращения приема лекарств и что в дальнейшем не понадобится его возобновление. Вторичная профилактика важнее риска нежелательных эффектов лекарств, так как большинство из них обратимо, а последствия рецидива могут быть фатальными. Адекватная фармакотерапия («правильное лекарство для правильного пациента») позволяет улучшить, закрепить достигнутые терапевтические результаты с наименьшим риском нежелательных действий. В связи с неясным прогнозом прекращения активности болезненного процесса поддерживающее лечение показано всем больным. Для пациентов, перенесших первый эпизод и полностью ремитированных в течение года, возможна постепенная отмена лечения Сероквелем в течение 1–2–х лет [6,9,26]. Не менее 5 лет предстоит лечиться при отсутствии психотических симптомов больным с повторными приступами. Профилактическое лечение в течение жизни показано трети хронических больных, особенно опасных для себя и окружающих в остром периоде (или если повторные психозы отличались длительностью и плохо поддавались терапии). Для многих пациентов психиатр становится врачом общей практики. Ему следует уделять больше внимания состоянию физического здоровья и благополучия больных, динамически контролируя возможные нежелательные эффекты длительной терапии. В этой связи важен низкий риск нежелательных действий Сероквеля при длительном применении [3], например, поздней дискинезии, бича поддерживающей терапии ТН или ожирения при лечении рядом АА. Выбор Сероквеля показан стабилизированным симптоматически больным, но испытывающим указанные не корригируемые иными способами побочные действия. Снижение дозы Сероквеля в связи с хорошей переносимостью и малым риском дозозависимых нежелательных действий нецелесообразно у больных в фармакозависимой ремиссии, у остальных возможно (при переоценке соотношения риск / польза терапии) не ранее, чем через 6–12 месяцев устойчивого послабления симптомов приступообразной шизофрении при усилении динамического контроля. Минимальная терапевтическая доза Сероквеля определяется врачами после проб и ошибок. При недостаточных дозах Сероквеля рецидивы (обострения) могут быть отставлены на несколько месяцев, поэтому служат ненадежным показателем. Хорошая переносимость Сероквеля в сочетании с его высокой антирецидивной эффективностью способствует удовлетворенности пациентов длительным лечением [11,14,17,21,24]. Однако обрыв терапии АА (зипрасидоном, кветиапином, оланзапином, рисперидоном) хроническими больными достигает 75% в течение 18 месяцев, и он лишь в малой степени определен непереносимостью лекарств [18]. Отсев при лечении Сероквелем составляет 80% в течение трех лет [22], что подчеркивает опасность пренебрежения психосоциальной работой по укреплению и контролю долговременного комплайнса пациентов.
Итак, в первые месяцы лечения Сероквелем основные усилия направлены на уменьшение психотических симптомов при минимальном риске нежелательных эффектов терапии. Через 3–12 месяцев акцент сдвинут на предупреждение рецидивов (обострений), поддержание и контроль комплайнса пациентом, снижение риска медицинских осложнений терапии, социально–трудовое вовлечение и удовлетворение изменчивых потребностей больного и его семьи. Спустя год терапия фокусирована на обеспечение независимой благополучной жизни для большинства больных, независимо от «стажа» их расстройства.
Симптоматический эффект, социальное функционирование и качество жизни больного шизофренией при лечении Сероквелем будут выше при координированном межпрофессиональном и межведомственном вмешательстве (табл. 2).
Сероквель открывает шлюзы ранней реабилитации (за счет упорядочивающего действия); способствует установлению стойкой полноценной ремиссии (антипсихотический и антирецидивный эффекты), как основы социального выздоровления [4]. «Дружественный» пациенту Сероквель с близким к оптимальному соотношением риск/польза терапии выступает лекарством первого выбора на последовательных этапах систематического биопсихосоциального лечения шизофрении.

Литература
1. Гурович И.Я. Побочные эффекты и осложнения при нейролептической терапии. / Дисс. докт. мед. наук. – М., 1971. – 443 с.
2. Гурович И.Я., Любов Е.Б. Фармакоэпидемиология и фармакоэкономика в психиатрии. – М.: Медпрактика, 2003. – 264 с.
3. Гурович И.Я., Любов Е.Б. Сероквель в ряду других антипсихотиков при лечении больных шизофренией. // Русский медицинский журнал, 2008. – Т.16, №12. – С. 1705–1710.
4. Гурович И.Я., Любов Е.Б., Сторожакова Я.А Выздоровление при шизофрении: Концепция «recovery». // Социальная и клиническая психиатрия . – 2008. – Т. 18. – Вып. 2. – С. 7 –14.
5. Гурович И.Я., Шмуклер А.Б., Сторожакова Я.А. Психосоциальная терапия и психосоциальная реабилитация в психиатрии. – М.: Медпрактика–М., 2004. – 492 с.
6. Психиатрическая помощь больным шизофренией: Клиническое руководство. / Ред. Краснов В.Н., Гурович И.Я., Мосолов С.Н. и соавт. – М.: ИД Медпрактика–М., 2007 – 260 с.
7. Allen M.H., Carpenter D., Sheets J.L. et al. What do consumers say they want and need during a psychiatric emergency? // J. Psychiatr. Prac, 2003. – V. 9. 39–58.
8. Allen M.H., Currier G.W., Hughes D.H. et al. The expert consensus guideline series: treatment of behavioral emergencies. // Postgrad Med., 2001. – P. 1–88.
9. American Psychiatric Association: Practice Guidelines for the treatment of patients with schizophrenia. – Washington, DC: APA, 2004.
10. Bagnall A.–M., Jones L., Ginnelly L. et al. A systematic review of atypical antipsychotic drugs in schizophrenia. // Health Technol Assess., 2003. – V. 7, N. 13. – Р. 1–193.
11. Bartko G, Varadi H, Simon L et al. Patient satisfaction after switching from conventional to new atypical antipsychotics in schizophrenia. // Int J Psychiatry Clin Pract., 2002, V. 6. – Р. 9–14.
12. Chengappa K.N., Goldstein JM, Greenwood M et al. A post hoc analysis of the impact on hostility and agitation of quetiapine and haloperidol among patients with schizophrenia. // Clin Ther , 2003. 25: – Р. 530–541.
13. Chengappa K.N., Parepally H., Brar J.S. et al. A random– assignment, double–blind, clinical trial of once– vs twice–daily administration of quetiapine fumarate in patients with schizophrenia or schizoaffective disorder: a pilot study. // Can. J. Psychiatry, 2003; 48. – Р. 187–194.
14. Chue P., Abouelnasr W., Escobedo S. et al. A Canadian multicentre patient satisfaction study with oral long–term quetiapine treatment. Canadian Psychiatric Association, Banff, Alberta, Canada, 31 October – 3 November 2002.
15. Dossenbach M.., Erol A.., Kessaci M.. et al.. Effectiveness of antipsychoic treatments for schizophrenia: interim 6–month analysis from a prospective observational study (IC–SOHO) comparing olanzapine, quetiapine, risperidone, and haloperidol. // J. Clin. Psychiatry,. 2004. – V. 65. – P. 312–321.
16. Еxpert consensus guideline series. Optimizing pharmacologic treatment of psychotic disorders. / Kane J.M., Leucht S., Carpenter D. et al. // J. Clin. Psychiatry, 2003. – V. 64, Suppl. 12. – P. 21–51.
17. Hellewell J.S., Kalali A.H., Langham S.J. et al.. Patient satisfaction and acceptability of long–term treatment with quetiapine. // Int. J. Psychiatry Clin. Pract .,1999. – V. 3: – P. 105–113.
18. Lieberman J.A., Stroup T.S., McEvoy J.P. et al. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. // N. Engl. J. Med., 2005. – V. 353. – P. 1209–1223.
19. National Institute for clinical Excellence (NICE): Guidance on the use of newer (atypical) antipsychotic drugs for the treatment of schizophrenia. Technology Appraisal Guidance, 2002, № 43. – P. 1–21.
20. Peuskens J., Kasper S. Arango C. et al. The usefulness and use of second–generation anyipsychotic medication – an update. // Curr. Opin. Psychiatry, 2003. – V. 16, Suppl.1. – P. S.1–S.23.
21. Simons W.R., Bassi R., White R. Antipsychotic compliance evaluation: a population–based managed care study of persistence with initially prescribed antipsychotic medication. International Society for Pharmacoeconomics and Outcomes Research 4th Annual European Congress, Cannes, France, 11–13 November 2001.
22. Srisurapanont M., Disayavanish C., Taimkaew K. Quetiapine for schizophrenia (Cochrane Review). // Cochrane Library, Issue 2, Oxford: Update Software, 2003.
23. The usefulness and use of second–generation anyipsychotic medication – an update. // Curr. Opin.. Psychiatry, 2003. – V.16, Suppl.1. – P. S.1–S.23.
24. Voruganti L., Cortese L., Owyeumi L. et al. Switching from conventional to novel antipsychotic drugs: results of a prospective naturalistic study. // Schizophr. Res., 2002. – V. 57, № 2–3. – P. 201–208.
25. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of schizophrenia, part 1: acute treatment of schizophrenia. / Falkai P., Wobrock T., Lieberman J. et al. // World J. Biol. Psychiatry, 2005. – V.6. – P. 132–191.
26. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of schizophrenia, part 2: long–term treatment of schizophrenia. / Falkai P., Wobrock T., Lieberman J. et al. // World J. Biol. Psychiatry, 2006. – V. 7. – P. 1–40.












