–ü–Β―Ä–Ψ―Ä–Α–Μ―¨–Ϋ–Α―è ―³–Ψ―Ä–Φ–Α –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α ―É–Ε–Β –±–Ψ–Μ–Β–Β 20 –Μ–Β―² –Η―¹–Ω–Ψ–Μ―¨–Ζ―É–Β―²―¹―è –¥–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η. –ù–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ –Ω–Ψ–Κ–Α–Ζ–Α–Μ ―¹–≤–Ψ―é ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –≤–Ψ –Φ–Ϋ–Ψ–≥–Η―Ö ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ―΄―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è―Ö [9–11]. –ë–Ψ–Μ―¨―à–Η–Ϋ―¹―²–≤–Ψ ―ç―²–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –Ω–Ψ–Κ–Α–Ζ―΄–≤–Α–Β―², ―΅―²–Ψ –±–Μ–Ψ–Κ–Α―²–Ψ―Ä―΄ ―¹–Ϋ–Η–Ε–Α―é―² ―ç–Ι―³–Ψ―Ä–Η–Ζ–Η―Ä―É―é―â–Η–Ι ―ç―³―³–Β–Κ―² –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Η –Η–Ζ–±–Η―Ä–Α―²–Β–Μ―¨–Ϋ–Ψ –≤–Μ–Η―è―é―² –Ϋ–Α –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Β –≤–Μ–Β―΅–Β–Ϋ–Η–Β –Κ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―é [10]. –û―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ –≤―΄―¹–Ψ–Κ–Α ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ ―²–Β―Ä–Α–Ω–Η–Η –±–Μ–Ψ–Κ–Α―²–Ψ―Ä–Α–Φ–Η –Ω―Ä–Η –Η―Ö –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ–Ψ–Φ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Η ―¹ –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η–Β–Ι [12].
–ü―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Β–≤―²–Η―΅–Β―¹–Κ–Ψ–Β –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η–Β, –Κ–Α–Κ –Η –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β –Ω―¹–Η―Ö–Ψ―³–Α―Ä–Φ–Α–Κ–Ψ―²–Β―Ä–Α–Ω–Η–Η, ―è–≤–Μ―è–Β―²―¹―è –Ω–Α―²–Ψ–≥–Β–Ϋ–Β―²–Η―΅–Β―¹–Κ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Β–Ι, –Ω–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –≤–Μ–Η―è–Β―² –Ϋ–Α –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Β –≤–Μ–Β―΅–Β–Ϋ–Η–Β –Κ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―é – ―¹―²–Β―Ä–Ε–Ϋ–Β–≤–Ψ–Β –Ζ–≤–Β–Ϋ–Ψ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η [2,8]. –ü–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ ―Ä―è–¥–Α –Α–≤―²–Ψ―Ä–Ψ–≤, –Ϋ–Α–Η–±–Ψ–Μ–Β–Β ―ç―³―³–Β–Κ―²–Η–≤–Ϋ―΄–Φ–Η –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Β–≤―²–Η―΅–Β―¹–Κ–Η–Φ–Η –Φ–Β―²–Ψ–¥–Η–Κ–Α–Φ–Η, –Η―¹–Ω–Ψ–Μ―¨–Ζ―É–Β–Φ―΄–Φ–Η –≤ ―¹–Ψ―΅–Β―²–Α–Ϋ–Η–Η ―¹ –Ω―Ä–Η–Β–Φ–Ψ–Φ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α, ―è–≤–Μ―è―é―²―¹―è –Κ–Μ–Η–Β–Ϋ―²―Ü–Β–Ϋ―²―Ä–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Α―è –Η –Ω–Ψ–≤–Β–¥–Β–Ϋ―΅–Β―¹–Κ–Α―è –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η―è [14].
–û–¥–Ϋ–Α–Κ–Ψ –Ϋ–Α–Η–±–Ψ–Μ–Β–Β ―¹–Μ–Ψ–Ε–Ϋ–Ψ–Ι –Ω―Ä–Ψ–±–Μ–Β–Φ–Ψ–Ι ―è–≤–Μ―è–Β―²―¹―è –Ω–Ψ–¥–¥–Β―Ä–Ε–Α–Ϋ–Η–Β –Κ–Ψ–Φ–Ω–Μ–Α–Ι–Ϋ―¹–Α –±–Ψ–Μ―¨–Ϋ―΄–Φ –Ω―Ä–Η –Μ–Β―΅–Β–Ϋ–Η–Η –±–Μ–Ψ–Κ–Α―²–Ψ―Ä–Α–Φ–Η –Ψ–Ω–Η–Α―²–Ϋ―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤. –Δ–Α–Κ–Η–Β –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Ω―Ä–Ψ―³–Η–Μ―è, –Κ–Α–Κ –Ϋ–Β―¹―²–Ψ–Ι–Κ–Α―è –Φ–Ψ―²–Η–≤–Α―Ü–Η―è –Ϋ–Α –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–Β –Μ–Β―΅–Β–Ϋ–Η–Β, –Α―É―²–Ψ―Ö―²–Ψ–Ϋ–Ϋ―΄–Β –Ψ–±–Ψ―¹―²―Ä–Β–Ϋ–Η―è ―¹–Η–Ϋ–¥―Ä–Ψ–Φ–Α –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –≤–Μ–Β―΅–Β–Ϋ–Η―è, ―¹–≤―è–Ζ–Α–Ϋ–Ϋ―΄–Β –Κ–Α–Κ ―¹ ―²―è–Ε–Β―¹―²―¨―é –Ω―Ä–Ψ―è–≤–Μ–Β–Ϋ–Η–Ι –±–Ψ–Μ–Β–Ζ–Ϋ–Η, ―²–Α–Κ –Η ―¹ –Β–Β –Ω–Ψ―¹–Μ–Β–¥―¹―²–≤–Η―è–Φ–Η (–Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ–Ψ–Ι –Ϋ–Β―Ä–≤–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄, –Ϋ–Α―Ä–Α―¹―²–Α–Ϋ–Η–Β –Ω―¹–Η―Ö–Ψ–Ψ―Ä–≥–Α–Ϋ–Η―΅–Β―¹–Κ–Η―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤, ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Κ―Ä–Η―²–Η―΅–Β―¹–Κ–Η―Ö ―¹–Ω–Ψ―¹–Ψ–±–Ϋ–Ψ―¹―²–Β–Ι, –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―è –Α–¥–Α–Ω―²–Α―Ü–Η–Ψ–Ϋ–Ϋ―΄―Ö –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²–Β–Ι) –¥–Η–Κ―²―É―é―² –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²―¨ ―É―¹–Ψ–≤–Β―Ä―à–Β–Ϋ―¹―²–≤–Ψ–≤–Α–Ϋ–Η―è –Η–Φ–Β―é―â–Η―Ö―¹―è –Ω–Ψ–¥―Ö–Ψ–¥–Ψ–≤ –Κ ―²–Β―Ä–Α–Ω–Η–Η ―ç―²–Ψ–≥–Ψ –Κ–Ψ–Ϋ―²–Η–Ϋ–≥–Β–Ϋ―²–Α –±–Ψ–Μ―¨–Ϋ―΄―Ö.
–†–Β―²―Ä–Ψ―¹–Ω–Β–Κ―²–Η–≤–Ϋ―΄–Ι –Α–Ϋ–Α–Μ–Η–Ζ ―²–Β―Ä–Α–Ω–Η–Η –Ω–Β―Ä–Ψ―Ä–Α–Μ―¨–Ϋ–Ψ–Ι ―³–Ψ―Ä–Φ–Ψ–Ι –Ϋ–Α–Μ―²―Ä–Β–Ϋ–Κ―¹–Ψ–Ϋ–Α –Ω–Ψ–Κ–Α–Ζ–Α–Μ, ―΅―²–Ψ –±–Ψ–Μ―¨―à–Η–Ϋ―¹―²–≤–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ϋ–Β –Ζ–Α–≤–Β―Ä―à–Η–Μ–Ψ –Κ―É―Ä―¹ –Μ–Β―΅–Β–Ϋ–Η―è [15]. –≠―²–Ψ, –Ω–Ψ ―¹―É―²–Η, –Φ–Β―à–Α–Β―² ―É―¹―²–Α–Ϋ–Ψ–≤–Η―²―¨ ―Ä–Β–Α–Μ―¨–Ϋ―É―é ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –¥–Α–Ϋ–Ϋ–Ψ–≥–Ψ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α. –ù–Β―¹–Ψ–±–Μ―é–¥–Β–Ϋ–Η–Β ―Ä–Β–Ε–Η–Φ–Α –Μ–Β―΅–Β–Ϋ–Η―è –≤―΄–Ζ―΄–≤–Α–Β―² –Ω–Ψ–≤―΄―à–Β–Ϋ–Η–Β ―Ä–Η―¹–Κ–Α ―Ä–Β―Ü–Η–¥–Η–≤–Α –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –±–Ψ–Μ–Β–Β ―΅–Β–Φ –≤ 4 ―Ä–Α–Ζ–Α [16]. –Δ–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, –≤―¹–Β –≤―΄―à–Β–Ω–Β―Ä–Β―΅–Η―¹–Μ–Β–Ϋ–Ϋ―΄–Β –Ω―Ä–Ψ–±–Μ–Β–Φ―΄ –≤ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Ι ―¹―²–Β–Ω–Β–Ϋ–Η –Ψ–≥―Ä–Α–Ϋ–Η―΅–Η–≤–Α―é―² –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Β –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α [17,18].
–ù–Α–±–Μ―é–¥–Β–Ϋ–Η―è, ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤―É―é―â–Η–Β –Ψ ―²–Ψ–Φ, ―΅―²–Ψ ―É –Ε–Η–≤–Ψ―²–Ϋ―΄―Ö m––Ψ–Ω–Η–Ψ–Η–¥–Ϋ―΄–Β (–Φ–Ψ―Ä―³–Η–Ϋ–Ψ–Ω–Ψ–¥–Ψ–±–Ϋ―΄–Β) –Α–≥–Ψ–Ϋ–Η―¹―²―΄ –≤―΄–Ζ―΄–≤–Α―é―² ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è, –Α m––Ψ–Ω–Η–Ψ–Η–¥–Ϋ―΄–Β –Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η―¹―²―΄ – ―¹–Ψ–Κ―Ä–Α―â–Β–Ϋ–Η–Β [19,20], –Ω–Ψ―¹–Μ―É–Ε–Η–Μ–Ψ –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Β–Φ –¥–Μ―è –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Η―è –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Η―¹–Ω―΄―²–Α–Ϋ–Η–Ι –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –Ω―Ä–Η –Μ–Β―΅–Β–Ϋ–Η–Η –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é. –ë―΄–Μ–Ψ ―¹―³–Ψ―Ä–Φ―É–Μ–Η―Ä–Ψ–≤–Α–Ϋ–Ψ –Ω―Ä–Β–¥–Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β –Ψ ―²–Ψ–Φ, ―΅―²–Ψ ―ç―²–Ψ―² –Ω―Ä–Β–Ω–Α―Ä–Α―² –Ψ–≥―Ä–Α–Ϋ–Η―΅–Η–≤–Α–Β―² ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Η ―É–≤–Β–Μ–Η―΅–Η–≤–Α–Β―² –Ω–Β―Ä–Η–Ψ–¥ –≤–Ψ–Ζ–¥–Β―Ä–Ε–Α–Ϋ–Η―è –Ψ―² –Ϋ–Β–≥–Ψ, ―É–Φ–Β–Ϋ―¨―à–Α―è ―¹―²–Β–Ω–Β–Ϋ―¨ –Ω–Ψ–Ζ–Η―²–Η–≤–Ϋ–Ψ–≥–Ψ –Ω–Ψ–¥–Κ―Ä–Β–Ω–Μ–Β–Ϋ–Η―è, –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ―¹―²―¨ ―ç―³―³–Β–Κ―²–Α ―É–¥–Ψ–≤–Ψ–Μ―¨―¹―²–≤–Η―è –Η –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –≤–Μ–Β―΅–Β–Ϋ–Η―è –Κ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―é. –ù–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ –Η –¥―Ä―É–≥–Η–Β m––Ψ–Ω–Η–Ψ–Η–¥–Ϋ―΄–Β –Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η―¹―²―΄ –±–Μ–Ψ–Κ–Η―Ä―É―é―² –≤―΄–Ζ―΄–≤–Α–Β–Φ–Ψ–Β –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Β–Ϋ–Η–Β –¥–Ψ―³–Α–Φ–Η–Ϋ–Α –≤ –≤–Ψ―¹―Ö–Ψ–¥―è―â–Β–Φ ―è–¥―Ä–Β (nucleus accumbens) [21,22]. –¦–Η―Ü–Α, ―É –Κ–Ψ―²–Ψ―Ä―΄―Ö ―¹―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Μ–Ψ―¹―¨ –±―΄―²–Ψ–≤–Ψ–Β –Ω―¨―è–Ϋ―¹―²–≤–Ψ, –Ω―Ä–Η–Ϋ–Η–Φ–Α―è –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ, ―¹–Ψ–Ψ–±―â–Α―é―² –Ψ –Φ–Β–Ϋ–Β–Β –Ω―Ä–Η―è―²–Ϋ–Ψ–Φ –Η –±–Ψ–Μ–Β–Β –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ–Φ ―¹–Β–¥–Α―²–Η–≤–Ϋ–Ψ–Φ –¥–Β–Ι―¹―²–≤–Η–Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è, –Α ―²–Α–Κ–Ε–Β –Ψ ―²―è–≥–Ψ―¹―²–Ϋ―΄―Ö –Ψ―â―É―â–Β–Ϋ–Η―è―Ö –Ω–Ψ―¹–Μ–Β –Β–≥–Ψ –Ω―Ä–Η–Β–Φ–Α [23]. –ë–Ψ–Μ―¨–Ϋ―΄–Β –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é, –Κ–Ψ―²–Ψ―Ä―΄–Β –≤ –Ω―Ä–Ψ―Ü–Β―¹―¹–Β –Μ–Β―΅–Β–Ϋ–Η―è –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Ψ–Φ –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α–Μ–Η –≤―΄–Ω–Η–≤–Α―²―¨, –Ψ―²–Φ–Β―΅–Α–Μ–Η –±–Ψ–Μ–Β–Β ―¹–Μ–Α–±―É―é ―¹―²–Β–Ω–Β–Ϋ―¨ –Ψ–Ω―¨―è–Ϋ–Β–Ϋ–Η―è –Η –Ψ–±–Ϋ–Α―Ä―É–Ε–Η–≤–Α–Μ–Η –Φ–Β–Ϋ―¨―à―É―é –≤–Β―Ä–Ψ―è―²–Ϋ–Ψ―¹―²―¨ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α –Κ «―²―è–Ε–Β–Μ–Ψ–Φ―É» –Ω―¨―è–Ϋ―¹―²–≤―É [11]. –ù–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ –≤ –Ψ–¥–Η–Ϋ–Α–Κ–Ψ–≤–Ψ–Ι ―¹―²–Β–Ω–Β–Ϋ–Η ―¹–Ϋ–Η–Ε–Α–Β―² ―²―è–≥―É –Κ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―é –Κ–Α–Κ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Η–Ζ–Φ–Ψ–Φ [23], ―²–Α–Κ –Η –Ω―Ä–Η «―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ–Ψ–Φ» ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è.
–£ –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Η―Ö –¥–≤–Ψ–Ι–Ϋ―΄―Ö ―¹–Μ–Β–Ω―΄―Ö –Ω–Μ–Α―Ü–Β–±–Ψ––Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ―΄―Ö –Η―¹–Ω―΄―²–Α–Ϋ–Η―è―Ö –±―΄–Μ–Ψ ―É―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Ψ, ―΅―²–Ψ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ ―ç―³―³–Β–Κ―²–Η–≤–Β–Ϋ –≤ –Κ–Ψ–Φ–±–Η–Ϋ–Α―Ü–Η–Η ―¹ ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ–Ψ––Ω―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Φ–Η –Φ–Β―²–Ψ–¥–Α–Φ–Η –Μ–Β―΅–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η. –£ 12––Ϋ–Β–¥–Β–Μ―¨–Ϋ–Ψ–Φ –Ω–Μ–Α―Ü–Β–±–Ψ––Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ–Ψ–Φ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Φ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Φ –Η―¹–Ω―΄―²–Α–Ϋ–Η–Η –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ –±―΄–Μ –Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ –≤ –¥–Ψ–Ζ–Β 50 –Φ–≥/―¹―É―². 70 –Φ―É–Ε―΅–Η–Ϋ–Α–Φ ―¹ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é, –Ω―Ä–Ψ―Ö–Ψ–¥–Η–≤―à–Η–Φ –Α–Φ–±―É–Μ–Α―²–Ψ―Ä–Ϋ―΄–Ι –Κ―É―Ä―¹ –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η–Η. –£ –≥―Ä―É–Ω–Ω–Β –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ω―Ä–Η–Ϋ–Η–Φ–Α–≤―à–Η―Ö –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ, –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –≥―Ä―É–Ω–Ω–Ψ–Ι, –Ω–Ψ–Μ―É―΅–Α–≤―à–Β–Ι –Ω–Μ–Α―Ü–Β–±–Ψ, ―Ä–Β–Ε–Β ―³–Η–Κ―¹–Η―Ä–Ψ–≤–Α–Μ–Η―¹―¨ ―¹–Μ―É―΅–Α–Η –Ω―Ä–Η–Β–Φ–Α –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è (4 –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ 14% –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α –¥–Ϋ–Β–Ι –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è) –Η –≤ –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Β–Φ ―Ä–Β–Ε–Β (―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ 23 –Η 54%) –≤–Ψ–Ζ–Ψ–±–Ϋ–Ψ–≤–Μ―è–Μ–Ψ―¹―¨ «―²―è–Ε–Β–Μ–Ψ–Β» ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è (–Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β–Φ–Ψ–Β –Κ–Α–Κ –Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β –≤ ―²–Β―΅–Β–Ϋ–Η–Β –¥–Ϋ―è –Ϋ–Β –Φ–Β–Ϋ–Β–Β –Ω―è―²–Η ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ―΄―Ö –¥–Ψ–Ζ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è) [11]. –£ –¥–≤–Ψ–Ι–Ϋ–Ψ–Φ ―¹–Μ–Β–Ω–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –≤ –≥―Ä―É–Ω–Ω–Β –±–Ψ–Μ―¨–Ϋ―΄―Ö –Η–Ζ 97 –Φ―É–Ε―΅–Η–Ϋ –Η –Ε–Β–Ϋ―â–Η–Ϋ ―¹ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é [12], –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω―Ä–Ψ―Ö–Ψ–¥–Η–Μ–Η 12––Ϋ–Β–¥–Β–Μ―¨–Ϋ―΄–Ι –Κ―É―Ä―¹ –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η–Η (–Ω―Ä–Η ―ç―²–Ψ–Φ –¥–Μ―è ―΅–Α―¹―²–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η―è –±―΄–Μ–Α –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Α –Ϋ–Α ―É–Κ―Ä–Β–Ω–Μ–Β–Ϋ–Η–Β –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ―΄―Ö –Ϋ–Α–≤―΄–Κ–Ψ–≤ –Ω―Ä–Η―¹–Ω–Ψ―¹–Ψ–±–Μ–Β–Ϋ–Η―è –Η –Ω―Ä–Β–¥–Ψ―²–≤―Ä–Α―â–Β–Ϋ–Η–Β ―¹―Ä―΄–≤–Α, –Α –¥―Ä―É–≥–Α―è ―΅–Α―¹―²―¨ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω―Ä–Ψ―Ö–Ψ–¥–Η–Μ–Α –Ω–Ψ–¥–¥–Β―Ä–Ε–Η–≤–Α―é―â―É―é –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η―é), –Ϋ–Α–Ζ–Ϋ–Α―΅–Α–Μ―¹―è –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ (50 –Φ–≥/―¹―É―².) –Η–Μ–Η –Ω–Μ–Α―Ü–Β–±–Ψ. –£ –≥―Ä―É–Ω–Ω–Β –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ω―Ä–Η–Ϋ–Η–Φ–Α–≤―à–Η―Ö –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ, ―É―Ä–Ψ–≤–Β–Ϋ―¨ ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –±―΄–Μ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –Ϋ–Η–Ε–Β, –Α –Ω―Ä–Ψ―Ü–Β–Ϋ―² –±–Ψ–Μ―¨–Ϋ―΄―Ö, –≤–Ψ–Ζ–¥–Β―Ä–Ε–Η–≤–Α–≤―à–Η―Ö―¹―è –Ψ―² –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è, –±―΄–Μ –≤―΄―à–Β, ―΅–Β–Φ –≤ –≥―Ä―É–Ω–Ω–Β, –Ω–Ψ–Μ―É―΅–Α–≤―à–Β–Ι –Ω–Μ–Α―Ü–Β–±–Ψ. «–Δ―è–Ε–Β–Μ–Ψ–Β» ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –≤–Ψ–Ζ–Ψ–±–Ϋ–Ψ–≤–Η–Μ–Ψ―¹―¨ –Φ–Β–Ϋ–Β–Β ―΅–Β–Φ ―É –Ω–Ψ–Μ–Ψ–≤–Η–Ϋ―΄ –±–Ψ–Μ―¨–Ϋ―΄―Ö –≤ –≥―Ä―É–Ω–Ω–Β, –Ω―Ä–Η–Ϋ–Η–Φ–Α–≤―à–Β–Ι –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ, –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ 80% –±–Ψ–Μ―¨–Ϋ―΄―Ö –≤ –≥―Ä―É–Ω–Ω–Β, –Ω–Ψ–Μ―É―΅–Α–≤―à–Β–Ι –Ω–Μ–Α―Ü–Β–±–Ψ. –ü―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –±―΄–Μ–Ψ –Ϋ–Α–Η–±–Ψ–Μ–Β–Β ―ç―³―³–Β–Κ―²–Η–≤–Ϋ―΄–Φ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω―Ä–Η –≤–Κ–Μ―é―΅–Β–Ϋ–Η–Η –≤ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β ―¹–Ψ–Ψ–±―â–Η–Μ–Η –Ψ –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ–Φ –≤–Μ–Β―΅–Β–Ϋ–Η–Η –Κ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―é («―²―è–≥–Β») [24]. –ë―΄–Μ–Ψ –Ψ–±–Ϋ–Α―Ä―É–Ε–Β–Ϋ–Ψ –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η–Β –Φ–Β–¥–Η–Κ–Α–Φ–Β–Ϋ―²–Ψ–Ζ–Ϋ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –Η –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η–Η. –û–Ϋ–Ψ –Ω―Ä–Ψ―è–≤–Μ―è–Μ–Ψ―¹―¨ –≤ ―²–Ψ–Φ, ―΅―²–Ψ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤–Ψ–≤–Α–Μ ―²―Ä–Β–Ζ–≤–Ψ―¹―²–Η ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö, –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Ϋ―΄―Ö –≤ –Ω–Ψ–¥–¥–Β―Ä–Ε–Η–≤–Α―é―â―É―é ―²–Β―Ä–Α–Ω–Η―é, –Ϋ–Ψ –Ϋ–Β ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö, ―É―΅–Α―¹―²–≤―É―é―â–Η―Ö –≤ –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η–Η, –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Ϋ–Ψ–Ι –≤ –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–Φ –Ϋ–Α ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –Ϋ–Α–≤―΄–Κ–Ψ–≤ –Ω―Ä–Η―¹–Ω–Ψ―¹–Ψ–±–Μ–Β–Ϋ–Η―è. –Γ –¥―Ä―É–≥–Ψ–Ι ―¹―²–Ψ―Ä–Ψ–Ϋ―΄, –≤ ―¹–Μ―É―΅–Α―è―Ö –Ω―Ä–Η–Β–Φ–Α –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –Η ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Μ–Η―Ü–Α, –Ω―Ä–Ψ―Ö–Ψ–¥–Η–≤―à–Η–Β –Κ―É―Ä―¹ –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η–Η, –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Ϋ–Ψ–Ι –≤ –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–Φ –Ϋ–Α ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –Ϋ–Α–≤―΄–Κ–Ψ–≤ –Ω―Ä–Β–Ψ–¥–Ψ–Μ–Β–Ϋ–Η―è ―¹―Ä―΄–≤–Α, –±―΄–Μ–Η –≤ –Φ–Β–Ϋ―¨―à–Β–Ι ―¹―²–Β–Ω–Β–Ϋ–Η ―¹–Κ–Μ–Ψ–Ϋ–Ϋ―΄ –Κ «―²―è–Ε–Β–Μ–Ψ–Φ―É» ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―é –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –±–Ψ–Μ―¨–Ϋ―΄–Φ–Η, –Κ–Ψ―²–Ψ―Ä―΄–Φ –±―΄–Μ–Α –Ω―Ä–Β–¥–Ω–Η―¹–Α–Ϋ–Α –Ω–Ψ–¥–¥–Β―Ä–Ε–Η–≤–Α―é―â–Α―è ―²–Β―Ä–Α–Ω–Η―è.
–£ –¥―Ä―É–≥–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è―Ö –Ϋ–Β –≤―΄―è–≤–Μ–Β–Ϋ–Ψ –¥–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨―¹―²–≤ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α. –£ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η 108 –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é –Η –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β–Φ –Κ–Ψ–Κ–Α–Η–Ϋ–Ψ–Φ –Η –Ψ–Ω–Η–Α―²–Α–Φ–Η, –Κ–Ψ―²–Ψ―Ä―΄–Φ –Ϋ–Α ―³–Ψ–Ϋ–Β ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ–Ψ––Ω―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η―Ö –Φ–Β―Ä–Ψ–Ω―Ä–Η―è―²–Η–Ι –Ϋ–Α–Ζ–Ϋ–Α―΅–Α–Μ–Η―¹―¨ –Ω–Μ–Α―Ü–Β–±–Ψ –Η–Μ–Η –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ –≤ –¥–Ψ–Ζ–Β 50 –Η–Μ–Η 100 –Φ–≥/―¹―É―². (–Ω–Ψ―¹–Μ–Β–¥–Ϋ–Η–Ι –Ϋ–Β –≤–Μ–Η―è–Μ –Ϋ–Α ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è) [25]. –ê–Ϋ–Α–Μ–Ψ–≥–Η―΅–Ϋ–Ψ, –≤ 12––Ϋ–Β–¥–Β–Μ―¨–Ϋ–Ψ–Φ –¥–≤–Ψ–Ι–Ϋ–Ψ–Φ ―¹–Μ–Β–Ω–Ψ–Φ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Φ –Η―¹–Ω―΄―²–Α–Ϋ–Η–Η, –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–Φ –≤ –£–Β–Μ–Η–Κ–Ψ–±―Ä–Η―²–Α–Ϋ–Η–Η, ―É 175 –±–Ψ–Μ―¨–Ϋ―΄―Ö –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Η–Ζ–Φ–Ψ–Φ, ―É―΅–Α―¹―²–≤―É―é―â–Η―Ö –≤ –Φ–Η–Ϋ–Η–Φ–Α–Μ―¨–Ϋ―΄―Ö ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η–Ψ–Ϋ–Ϋ―΄―Ö –Φ–Β―Ä–Ψ–Ω―Ä–Η―è―²–Η―è―Ö, –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η, ―¹–≤―è–Ζ–Α–Ϋ―΄–Β ―¹–Ψ –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β–Φ –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ, –Ϋ–Β –Η–Ζ–Φ–Β–Ϋ–Η–Μ–Η―¹―¨ –Ϋ–Η –≤ –≥―Ä―É–Ω–Ω–Β, –Κ–Ψ―²–Ψ―Ä–Ψ–Ι –Ϋ–Α–Ζ–Ϋ–Α―΅–Α–Μ–Ψ―¹―¨ –Ω–Μ–Α―Ü–Β–±–Ψ, –Ϋ–Η –≤ –≥―Ä―É–Ω–Ω–Β, –Ω―Ä–Η–Ϋ–Η–Φ–Α–≤―à–Β–Ι –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ (50 –Φ–≥/―¹―É―².) [26]. –£ –¥–≤–Ψ–Ι–Ϋ–Ψ–Φ ―¹–Μ–Β–Ω–Ψ–Φ –Ω–Μ–Α―Ü–Β–±–Ψ––Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ–Ψ–Φ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Φ –Η―¹–Ω―΄―²–Α–Ϋ–Η–Η 64 –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ ―¹–Ψ―΅–Β―²–Α–Ϋ–Ϋ–Ψ–Ι –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Η –Κ–Ψ–Κ–Α–Η–Ϋ–Ψ–≤–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α (50 –Φ–≥/―¹―É―².) –Ϋ–Β –Ψ―²–Μ–Η―΅–Α–Μ–Α―¹―¨ –Ψ―² ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ω–Μ–Α―Ü–Β–±–Ψ [27].
–Γ―É―â–Β―¹―²–≤―É–Β―² –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Ψ –Ψ–±―ä―è―¹–Ϋ–Β–Ϋ–Η–Ι –Ω–Ψ–Μ–Ψ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –Ϋ–Α ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η–Β –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –≤ –Ψ–¥–Ϋ–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è―Ö –Η –Ψ―²―¹―É―²―¹―²–≤–Η―è ―²–Α–Κ–Ψ–≤–Ψ–≥–Ψ –≤ –¥―Ä―É–≥–Η―Ö. –£ –Ψ–¥–Ϋ–Ψ–Φ –Η–Ζ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α ―¹ –Ψ―²―Ä–Η―Ü–Α―²–Β–Μ―¨–Ϋ―΄–Φ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–Φ [26] ―¹ ―É―΅–Β―²–Ψ–Φ ―É–Φ–Β―Ä–Β–Ϋ–Ϋ–Ψ―¹―²–Η –¥–Β–Ι―¹―²–≤–Η―è –Η–Ζ―É―΅–Α–Β–Φ–Ψ–≥–Ψ –≤–Β―â–Β―¹―²–≤–Α ―Ä–Α–Ζ–Φ–Β―Ä –≤―΄–±–Ψ―Ä–Κ–Η –±―΄–Μ –Ϋ–Β–¥–Ψ―¹―²–Α―²–Ψ―΅–Β–Ϋ –¥–Μ―è ―³–Η–Κ―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η―è ―Ä–Α–Ζ–Μ–Η―΅–Η–Ι –Φ–Β–Ε–¥―É –≥―Ä―É–Ω–Ω–Α–Φ–Η, –≤ –Κ–Ψ―²–Ψ―Ä―΄―Ö –Ϋ–Α–Ζ–Ϋ–Α―΅–Α–Μ–Η―¹―¨ –Μ–Η–±–Ψ –Ω–Μ–Α―Ü–Β–±–Ψ, –Μ–Η–±–Ψ –Α–Κ―²–Η–≤–Ϋ–Ψ–Β –≤–Β―â–Β―¹―²–≤–Ψ. –£ –¥―Ä―É–≥–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η ―¹ –Ψ―²―Ä–Η―Ü–Α―²–Β–Μ―¨–Ϋ―΄–Φ ―Ä–Β-–Ζ―É–Μ―¨―²–Α―²–Ψ–Φ [27] –±–Ψ–Μ―¨–Ϋ―΄–Β –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ―è–Μ–Η –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Η–Φ–Η –Ω―¹–Η―Ö–Ψ–Α–Κ―²–Η–≤–Ϋ―΄–Φ–Η –≤–Β―â–Β―¹―²–≤–Α–Φ–Η, ―΅―²–Ψ –Φ–Ψ–≥–Μ–Ψ –Ψ–≥―Ä–Α–Ϋ–Η―΅–Η–≤–Α―²―¨ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α. –£–Α–Ε–Ϋ–Ψ ―²–Α–Κ–Ε–Β –Ψ―²–Φ–Β―²–Η―²―¨ –Ω―Ä–Ψ–±–Μ–Β–Φ―É ―¹–Ψ–±–Μ―é–¥–Β–Ϋ–Η―è –±–Ψ–Μ―¨–Ϋ―΄–Φ–Η ―²–Β―Ä–Α–Ω–Β–≤―²–Η―΅–Β―¹–Κ–Ψ–≥–Ψ ―Ä–Β–Ε–Η–Φ–Α. –£ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η, –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–Φ –≤ –£–Β–Μ–Η–Κ–Ψ–±―Ä–Η―²–Α–Ϋ–Η–Η, –≤ –Κ–Ψ―²–Ψ―Ä–Ψ–Φ –±―΄–Μ –Ω–Ψ–Μ―É―΅–Β–Ϋ –Ψ―²―Ä–Η―Ü–Α―²–Β–Μ―¨–Ϋ―΄–Ι ―Ä–Β–Ζ―É–Μ―¨―²–Α―², –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –Ω–Ψ–Ζ–≤–Ψ–Μ–Η–Μ–Ψ ―¹–Ψ–Κ―Ä–Α―²–Η―²―¨ –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ ―É–Ω–Ψ―²―Ä–Β–±–Μ―è–Β–Φ–Ψ–≥–Ψ –±–Ψ–Μ―¨–Ϋ―΄–Φ–Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Η –Κ―Ä–Α―²–Ϋ–Ψ―¹―²―¨ –≤―΄–Ω–Η–≤–Ψ–Κ –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Ψ–¥–Ϋ–Ψ–≥–Ψ –¥–Ϋ―è –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –≥―Ä―É–Ω–Ω–Ψ–Ι, –Ω–Ψ–Μ―É―΅–Α–≤―à–Β–Ι –Ω–Μ–Α―Ü–Β–±–Ψ, –Ϋ–Ψ ―²–Ψ–Μ―¨–Κ–Ψ ―É ―²–Β―Ö, –Κ―²–Ψ –≤ –Ω―Ä–Ψ―Ü–Β―¹―¹–Β –Μ–Β―΅–Β–Ϋ–Η―è –Ω―Ä–Η–Ϋ―è–Μ –Ϋ–Β –Φ–Β–Ϋ–Β–Β 80% –Ω―Ä–Β–¥–Ω–Η―¹–Α–Ϋ–Ϋ–Ψ–≥–Ψ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α [26]. –£–Α–Ε–Ϋ–Ψ―¹―²―¨ –Ω―Ä–Ψ–±–Μ–Β–Φ―΄ ―¹–Ψ–±–Μ―é–¥–Β–Ϋ–Η―è ―²–Β―Ä–Α–Ω–Β–≤―²–Η―΅–Β―¹–Κ–Η―Ö –Φ–Β―Ä–Ψ–Ω―Ä–Η―è―²–Η–Ι –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Α–Β―²―¹―è –¥–Α–Ϋ–Ϋ―΄–Φ–Η –Α–Φ–Β―Ä–Η–Κ–Α–Ϋ―¹–Κ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è, –≤ –Κ–Ψ―²–Ψ―Ä–Ψ–Φ ―¹―Ä–Α–≤–Ϋ–Η–≤–Α–Μ–Α―¹―¨ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –¥–Β–Ι―¹―²–≤–Η―è –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –Η –Ω–Μ–Α―Ü–Β–±–Ψ –≤ ―²–Β―Ä–Α–Ω–Η–Η 97 –±–Ψ–Μ―¨–Ϋ―΄―Ö –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Η–Ζ–Φ–Ψ–Φ, –Β–Ε–Β–Ϋ–Β–¥–Β–Μ―¨–Ϋ–Ψ –Ω–Ψ―¹–Β―â–Α–≤―à–Η―Ö –≤―Ä–Α―΅–Α. –Θ –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Κ–Ψ―²–Ψ―Ä―΄–Β –Μ―É―΅―à–Β ―¹–Ψ–±–Μ―é–¥–Α–Μ–Η –≥―Ä–Α―³–Η–Κ –Ω―Ä–Η–Β–Φ–Α –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α, –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ ―Ä–Β–Ε–Β –Ψ―²–Φ–Β―΅–Α–Μ–Η―¹―¨ ―ç–Ω–Η–Ζ–Ψ–¥―΄ «―²―è–Ε–Β–Μ–Ψ–≥–Ψ» ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Η –±―΄–Μ–Ψ –Φ–Β–Ϋ―¨―à–Β–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –¥–Ϋ–Β–Ι, –Κ–Ψ–≥–¥–Α –Ψ–Ϋ–Η ―É–Ω–Ψ―²―Ä–Β–±–Μ―è–Μ–Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨, –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –±–Ψ–Μ―¨–Ϋ―΄–Φ–Η –≤ –≥―Ä―É–Ω–Ω–Β, –≤ –Κ–Ψ―²–Ψ―Ä–Ψ–Ι –Ϋ–Α–Ζ–Ϋ–Α―΅–Α–Μ–Ψ―¹―¨ –Ω–Μ–Α―Ü–Β–±–Ψ (―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ 14 –Η 52%; 2,8 –Η 11%), ―²–Ψ–≥–¥–Α –Κ–Α–Κ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ϋ–Β –Ω―Ä–Η–¥–Β―Ä–Ε–Η–≤–Α–≤―à–Η―Ö―¹―è ―¹―Ö–Β–Φ―΄ –Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α, ―ç―²–Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Η –Ϋ–Β ―Ä–Α–Ζ–Μ–Η―΅–Α–Μ–Η―¹―¨ [13]. –£ ―²–Β―΅–Β–Ϋ–Η–Β –Ω–Β―Ä–≤―΄―Ö 90 –¥–Ϋ–Β–Ι –Ψ―²–Κ–Α–Ζ–Α –Ψ―² –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è, –Κ–Ψ–≥–¥–Α –≤–Β―Ä–Ψ―è―²–Ϋ–Ψ―¹―²―¨ ―¹―Ä―΄–≤–Α –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ –≤–Β–Μ–Η–Κ–Α, ―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥―É–Β―²―¹―è –Ϋ–Α–Ζ–Ϋ–Α―΅–Α―²―¨ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ –≤ –¥–Ψ–Ζ–Η―Ä–Ψ–≤–Κ–Β 50 –Φ–≥/―¹―É―²., –Ψ–¥–Ϋ–Α–Κ–Ψ –≤ –Ϋ–Β–Κ–Ψ―²–Ψ―Ä―΄―Ö ―¹–Μ―É―΅–Α―è―Ö –Η―¹–Ω–Ψ–Μ―¨–Ζ―É―é―² –¥–Ψ–Ζ–Η―Ä–Ψ–≤–Κ–Η –Ψ―² 25 –¥–Ψ 100 –Φ–≥/―¹―É―². –Γ―Ä–Β–¥–Η –Ω–Ψ–±–Ψ―΅–Ϋ―΄―Ö ―ç―³―³–Β–Κ―²–Ψ–≤ ―΅–Α―â–Β –≤―¹–Β–≥–Ψ –Ϋ–Α–±–Μ―é–¥–Α―é―²―¹―è ―²–Ψ―à–Ϋ–Ψ―²–Α (10%), –≥–Ψ–Μ–Ψ–≤–Ϋ–Α―è –±–Ψ–Μ―¨ (7%), ―²―Ä–Β–≤–Ψ–≥–Α (2%) –Η ―¹–Β–¥–Α―Ü–Η―è (2%) [28]. –ù–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ ―É―¹―²―Ä–Α–Ϋ―è–Β―² ―΅―É–≤―¹―²–≤–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Κ –Ψ–Ω–Η–Ψ–Η–¥–Ϋ―΄–Φ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α–Φ –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Ω–Ψ―¹–Μ–Β–¥―É―é―â–Η―Ö 72 ―΅–Α―¹–Ψ–≤. –ï―¹–Μ–Η –¥–Μ―è –Ψ–Κ–Α–Ζ–Α–Ϋ–Η―è –Ϋ–Β–Ψ―²–Μ–Ψ–Ε–Ϋ–Ψ–Ι –Ω–Ψ–Φ–Ψ―â–Η –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ –Ϋ–Α–Ζ–Ϋ–Α―΅–Η―²―¨ –Ψ–Ω–Η–Ψ–Η–Ψ–¥–Ϋ―΄–Ι –Α–Ϋ–Α–Μ―¨–≥–Β―²–Η–Κ, –≤–≤–Β–¥–Β–Ϋ–Η–Β –±–Ψ–Μ–Β–Β –≤―΄―¹–Ψ–Κ–Ψ–Ι –¥–Ψ–Ζ―΄ –Ψ–Ω–Η–Α―²–Ψ–≤ –Φ–Ψ–Ε–Β―² –Ω―Ä–Β–Ψ–¥–Ψ–Μ–Β―²―¨ ―ç―²―É –Ϋ–Β―΅―É–≤―¹―²–≤–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨, –Ϋ–Ψ –Ω―Ä–Η ―ç―²–Ψ–Φ ―¹–Μ–Β–¥―É–Β―² –Ψ–±―è–Ζ–Α―²–Β–Μ―¨–Ϋ–Ψ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä–Ψ–≤–Α―²―¨ ―³―É–Ϋ–Κ―Ü–Η―é –¥―΄―Ö–Α–Ϋ–Η―è. –î–Ψ–Ζ–Η―Ä–Ψ–≤–Κ–Α 300 –Φ–≥/―¹―É―². –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –Φ–Ψ–Ε–Β―² –Ψ–Κ–Α–Ζ―΄–≤–Α―²―¨ –≥–Β–Ω–Α―²–Ψ―²–Ψ–Κ―¹–Η―΅–Β―¹–Κ–Ψ–Β –¥–Β–Ι―¹―²–≤–Η–Β, ―΅―²–Ψ ―Ä–Β–¥–Κ–Ψ –±―΄–≤–Α–Β―² –Ω―Ä–Η –¥–Ψ–Ζ–Β 50 –Φ–≥/―¹―É―². [29]. –ö–Ψ–Ϋ―Ü–Β–Ϋ―²―Ä–Α―Ü–Η–Η –Α–Φ–Η–Ϋ–Ψ―²―Ä–Α–Ϋ―¹―³–Β―Ä–Α–Ζ –≤ ―¹―΄–≤–Ψ―Ä–Ψ―²–Κ–Β –Κ―Ä–Ψ–≤–Η ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ω―Ä–Η–Ϋ–Η–Φ–Α―é―â–Η―Ö –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ, ―΅–Α―¹―²–Ψ –Ϋ–Η–Ε–Β, ―΅–Β–Φ ―É –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ω–Ψ–Μ―É―΅–Α―é―â–Η―Ö –Ω–Μ–Α―Ü–Β–±–Ψ (–≤–Β―Ä–Ψ―è―²–Ϋ–Ψ, –≤―¹–Μ–Β–¥―¹―²–≤–Η–Β ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η―è –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α ―É–Ω–Ψ―²―Ä–Β–±–Μ―è–Β–Φ–Ψ–≥–Ψ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è). –Δ–Β–Φ –Ϋ–Β –Φ–Β–Ϋ–Β–Β –±–Ψ–Μ―¨–Ϋ―΄–Φ ―¹ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è–Φ–Η –Ω–Β―΅–Β–Ϋ–Η –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ ―¹–Μ–Β–¥―É–Β―² –Ϋ–Α–Ζ–Ϋ–Α―΅–Α―²―¨ ―¹ –Ψ―¹―²–Ψ―Ä–Ψ–Ε–Ϋ–Ψ―¹―²―¨―é, –Ω–Β―Ä–Η–Ψ–¥–Η―΅–Β―¹–Κ–Η –Ω―Ä–Ψ–≤–Β―Ä―è―è ―³―É–Ϋ–Κ―Ü–Η–Η –Ω–Β―΅–Β–Ϋ–Η [30].
–û–¥–Ϋ–Α–Κ–Ψ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η―è –±–Μ–Ψ–Κ–Α―²–Ψ―Ä–Ψ–≤ –Ψ–Ω–Η–Α―²–Ϋ―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –Ω―Ä–Η –Μ–Β―΅–Β–Ϋ–Η–Η –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è ―É–Ε–Β –Ϋ–Β –Ψ―¹–Ω–Α―Ä–Η–≤–Α–Β―²―¹―è –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―è–Φ–Η –Η –Ω―Ä–Α–Κ―²–Η–Κ–Α–Φ–Η. –û―²–Β―΅–Β―¹―²–≤–Β–Ϋ–Ϋ―΄–Ι –Ψ–Ω―΄―² –Ω–Ψ–Κ–Α–Ζ–Α–Μ, ―΅―²–Ψ –Ω–Ψ–≤―΄―¹–Η―²―¨ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Μ–Β―΅–Β–±–Ϋ―΄―Ö –Ω―Ä–Ψ–≥―Ä–Α–Φ–Φ –Ω–Ψ–Φ–Ψ–≥–Α–Β―² –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ―΄–Ι –Ω–Ψ–¥―Ö–Ψ–¥ –Κ ―²–Β―Ä–Α–Ω–Η–Η –Η –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β –≤ –Ω–Β―Ä–≤―É―é –Ψ―΅–Β―Ä–Β–¥―¨ ―²–Β―Ö –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö ―¹―Ä–Β–¥―¹―²–≤, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ―΄ –Ϋ–Α ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –≤–Μ–Β―΅–Β–Ϋ–Η―è –Κ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―é, ―΅―²–Ψ, –≤ ―¹–≤–Ψ―é –Ψ―΅–Β―Ä–Β–¥―¨, –Ω–Ψ–≤―΄―à–Α–Β―² –Φ–Ψ―²–Η–≤–Α―Ü–Η―é –Ϋ–Α –Ω–Ψ–¥–¥–Β―Ä–Ε–Α–Ϋ–Η–Β ―²―Ä–Β–Ζ–≤–Ψ–≥–Ψ –Ψ–±―Ä–Α–Ζ–Α –Ε–Η–Ζ–Ϋ–Η, –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–Β –Μ–Β―΅–Β–Ϋ–Η–Β –Η –¥–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Ι –Ω―Ä–Η–Β–Φ –Ω–Ψ–¥–¥–Β―Ä–Ε–Η–≤–Α―é―â–Β–Ι ―²–Β―Ä–Α–Ω–Η–Η [31].
–Γ ―Ü–Β–Μ―¨―é ―Ä–Β―à–Β–Ϋ–Η―è –≤―΄―à–Β―É–Κ–Α–Ζ–Α–Ϋ–Ϋ―΄―Ö –Ω―Ä–Ψ–±–Μ–Β–Φ –±―΄–Μ ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Α–Ϋ –Ϋ–Ψ–≤―΄–Ι –Ω―Ä–Β–Ω–Α―Ä–Α―² –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Φ –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Β–Ϋ–Η–Β–Φ –¥–Β–Ι―¹―²–≤―É―é―â–Β–≥–Ψ –≤–Β―â–Β―¹―²–≤–Α. –ù–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ ―¹ –¥–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Φ –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Β–Ϋ–Η–Β–Φ (extended–release naltrexone, Vivitrex, Vivitrol) – –Ϋ–Ψ–≤–Α―è ―³–Ψ―Ä–Φ–Α –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α, –Κ–Ψ―²–Ψ―Ä–Α―è –Ω―Ä–Β–¥–Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Α –¥–Μ―è –≤–Ϋ―É―²―Ä–Η–Φ―΄―à–Β―΅–Ϋ–Ψ–≥–Ψ –≤–≤–Β–¥–Β–Ϋ–Η―è. –≠―²–Ψ―² –Ω―Ä–Β–Ω–Α―Ä–Α―² –≤–≤–Ψ–¥–Η―²―¹―è ―Ä–Α–Ζ –≤ –Φ–Β―¹―è―Ü, ―²–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Β–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 4 –Ϋ–Β–¥–Β–Μ–Η. –£–Η–≤–Η―²―Ä–Ψ–Μ –Η–Φ–Β–Β―² –Ψ―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ –Ω–Μ–Α–≤–Ϋ―΄–Ι ―³–Α―Ä–Φ–Α–Κ–Ψ–Κ–Η–Ϋ–Β―²–Η―΅–Β―¹–Κ–Η–Ι –Ω―Ä–Ψ―³–Η–Μ―¨ ―¹ –Ϋ–Β–±–Ψ–Μ―¨―à–Η–Φ–Η ―³–Μ―é–Κ―²―É–Α―Ü–Η―è–Φ–Η –≤ ―²–Β―΅–Β–Ϋ–Η–Β –¥–Ϋ―è –Η–Μ–Η –±–Β–Ζ –Ϋ–Η―Ö [32]. –£–Η–≤–Η―²―Ä–Ψ–Μ –±―΄–Μ –Ψ–¥–Ψ–±―Ä–Β–Ϋ –¥–Μ―è –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η―è –Η ―É―²–≤–Β―Ä–Ε–¥–Β–Ϋ –≤ –Α–Ω―Ä–Β–Μ–Β 2006 –≥–Ψ–¥–Α –ê–¥–Φ–Η–Ϋ–Η―¹―²―Ä–Α―Ü–Η–Β–Ι –Γ–®–ê –Ω–Ψ –Ω―Ä–Ψ–¥―É–Κ―²–Α–Φ –Ω–Η―²–Α–Ϋ–Η―è –Η –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄–Φ ―¹―Ä–Β–¥―¹―²–≤–Α–Φ (FDA) –¥–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η [33].
–î–Ψ –Ϋ–Α―¹―²–Ψ―è―â–Β–≥–Ψ –≤―Ä–Β–Φ–Β–Ϋ–Η –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ψ ―É–Ε–Β ―¹―Ä–Α–≤–Ϋ–Η―²–Β–Μ―¨–Ϋ–Ψ –Φ–Ϋ–Ψ–≥–Ψ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ―΄―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –£–Η–≤–Η―²―Ä–Ψ–Μ–Α. –†–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Ψ―¹–Ϋ–Ψ–≤–Ϋ―΄―Ö –Η–Ζ –Ϋ–Η―Ö –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ―΄ –Ϋ–Η–Ε–Β.
–ü–Β―Ä–≤–Ψ–Β –±–Α–Ζ–Ψ–≤–Ψ–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ–Α –±―΄–Μ–Ψ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ψ –≤ –Ω–Β―Ä–Η–Ψ–¥ 2002–2003 –≥–Ψ–¥―΄ [34], –≤ –Γ–®–ê. –î–Α–Ϋ–Ϋ–Ψ–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β ―è–≤–Μ―è–Μ–Ψ―¹―¨ –¥–≤–Ψ–Ι–Ϋ―΄–Φ ―¹–Μ–Β–Ω―΄–Φ –Ω–Μ–Α―Ü–Β–±–Ψ––Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ―΄–Φ –Η –≤–Κ–Μ―é―΅–Α–Μ–Ψ –Ψ–¥–Ϋ―É –Η–Ζ ―¹–Α–Φ―΄―Ö –±–Ψ–Μ―¨―à–Η―Ö –≥―Ä―É–Ω–Ω –±–Ψ–Μ―¨–Ϋ―΄―Ö –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é, –Κ–Ψ–≥–¥–Α––Μ–Η–±–Ψ –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –Ω–Ψ–¥–Ψ–±–Ϋ–Ψ–Β –Μ–Β―΅–Β–Ϋ–Η–Β –≤ ―Ä–Α–Φ–Κ–Α―Ö –Ψ–¥–Ϋ–Ψ–Ι –Ϋ–Α―É―΅–Ϋ–Ψ–Ι ―Ä–Α–±–Ψ―²―΄ – 627 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤. –£ –Ψ–±―â–Β–Ι ―¹–Μ–Ψ–Ε–Ϋ–Ψ―¹―²–Η 401 –Ω–Α―Ü–Η–Β–Ϋ―² (64%) –Ω–Ψ–Μ―É―΅–Η–Μ 6 –Η–Ϋ―ä–Β–Κ―Ü–Η–Ι –Η 463 (74%) –Ϋ–Β –Φ–Β–Ϋ–Β–Β 4 –Η–Ϋ―ä–Β–Κ―Ü–Η–Ι
–ü–Α―Ü–Η–Β–Ϋ―²―΄, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η–Β –Μ–Β―΅–Β–Ϋ–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ–Ψ–Φ 380 –Φ–≥, –Ψ―²–Φ–Β―΅–Α–Μ–Η –Ω―Ä–Η–Φ–Β―Ä–Ϋ–Ψ –Ϋ–Α 25% –±–Ψ–Μ–Β–Β –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ–Β ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α ―ç–Ω–Η–Ζ–Ψ–¥–Ψ–≤ –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Ω–Ψ–Μ―É―΅–Α–≤―à–Η–Φ–Η –Ω–Μ–Α―Ü–Β–±–Ψ (―Ä–Η―¹. 1). –ü–Α―Ü–Η–Β–Ϋ―²―΄, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 190 –Φ–≥, –Ψ―²–Φ–Β―΅–Α–Μ–Η ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Ω–Ψ–¥–Ψ–±–Ϋ―΄―Ö ―ç–Ω–Η–Ζ–Ψ–¥–Ψ–≤ –Ϋ–Α 17% –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –≥―Ä―É–Ω–Ω–Ψ–Ι, –Ω–Ψ–Μ―É―΅–Α–≤―à–Β–Ι –Ω–Μ–Α―Ü–Β–±–Ψ (―Ä=0,07). –ù–Η –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ «–Ψ–Ω–Α―¹–Ϋ―΄―Ö» –¥–Ϋ–Β–Ι, –Ϋ–Η ―΅–Α―¹―²–Ψ―²–Α –¥–Ϋ–Β–Ι ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Ϋ–Β ―¹–Ϋ–Η–Ε–Α–Μ–Η―¹―¨ –Ϋ–Α ―³–Ψ–Ϋ–Β –Μ–Β―΅–Β–Ϋ–Η―è. –£ ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Η–Η ―¹ –Ψ―²–Φ–Β―΅–Β–Ϋ–Ϋ―΄–Φ ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β–Φ –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α ―ç–Ω–Η–Ζ–Ψ–¥–Ψ–≤ –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ –±―΄–Μ–Ψ –≤―΄―è–≤–Μ–Β–Ϋ–Ψ ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β ―É―Ä–Ψ–≤–Ϋ–Β–Ι –≥–Α–Φ–Φ–Α––≥–Μ―É―²–Α–Φ–Η–Μ–―²―Ä–Α–Ϋ―¹―³–Β―Ä―Ä–Α–Ζ―΄ (–™–™–Δ) –Ϋ–Α 15%. –ß–Α―¹―²–Ψ―²–Α –≤―¹―²―Ä–Β―΅–Α–Β–Φ–Ψ―¹―²–Η ―²–Ψ―à–Ϋ–Ψ―²―΄ –Ϋ–Β –±―΄–Μ–Α ―¹–≤―è–Ζ–Α–Ϋ–Α ―¹ –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ–Φ ―ç–Ω–Η–Ζ–Ψ–¥–Ψ–≤ –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ. –≠―²–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Ψ, ―΅―²–Ψ –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ ―¹–Ψ―΅–Β―²–Α–Ϋ–Η–Η ―¹ ―¹–Β–Α–Ϋ―¹–Α–Φ–Η ―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ–Ψ–Ι –Ω―¹–Η―Ö–Ψ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ–Ψ–Ι –Ω–Ψ–¥–¥–Β―Ä–Ε–Κ–Η –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ ―¹–Ϋ–Η–Ε–Α–Β―² ―΅–Α―¹―²–Ψ―²―É –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ –≤ –±–Ψ–Μ―¨―à–Ψ–Ι –≥―Ä―É–Ω–Ω–Β –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Φ–Η –Κ–Μ–Η–Ϋ–Η–Κ–Ψ––¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Η–Φ–Η –Η ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ–Ψ––¥–Β–Φ–Ψ–≥―Ä–Α―³–Η―΅–Β―¹–Κ–Η–Φ–Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―è–Φ–Η. –≠―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Μ–Β―΅–Β–Ϋ–Η―è –Ζ–Α–≤–Η―¹–Β–Μ–Α –Ψ―² –Ω–Ψ–Μ–Α –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Α ―²–Α–Κ–Ε–Β –Ψ―² –≤–Ψ–Ζ–¥–Β―Ä–Ε–Α–Ϋ–Η―è –Ψ―² –Ω―Ä–Η–Β–Φ–Α –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –¥–Ψ –Ϋ–Α―΅–Α–Μ–Α –Μ–Β―΅–Β–Ϋ–Η―è. –≠―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –¥–Ψ–Ζ―΄ –£–Η–≤–Η―²―Ä–Ψ–Μ–Α 380 –Φ–≥ –Ω―Ä–Ψ―è–≤–Μ―è–Μ–Α―¹―¨ ―É–Ε–Β –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Ω–Β―Ä–≤–Ψ–≥–Ψ –Φ–Β―¹―è―Ü–Α –Μ–Β―΅–Β–Ϋ–Η―è –Η ―¹–Ψ―Ö―Ä–Α–Ϋ―è–Μ–Α―¹―¨ –≤ ―²–Β―΅–Β–Ϋ–Η–Β –≤―¹–Β―Ö 24 –Ϋ–Β–¥–Β–Μ―¨.
–ü–Ψ–±–Ψ―΅–Ϋ―΄–Β ―ç―³―³–Β–Κ―²―΄ –Η–Φ–Β–Μ–Η –Φ–Β―¹―²–Ψ, –Κ–Α–Κ –Φ–Η–Ϋ–Η–Φ―É–Φ, ―É 10% –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ –¥–Β–Ι―¹―²–≤―É―é―â–Η–Ι –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ. –ù–Α–Η–±–Ψ–Μ–Β–Β ―΅–Α―¹―²―΄–Φ–Η ―¹―Ä–Β–¥–Η –Ϋ–Η―Ö –±―΄–Μ–Η ―²–Ψ―à–Ϋ–Ψ―²–Α, –≥–Ψ–Μ–Ψ–≤–Ϋ–Α―è –±–Ψ–Μ―¨ –Η ―¹–Μ–Α–±–Ψ―¹―²―¨. –ü―Ä–Η–Φ–Β―Ä–Ϋ–Ψ –≤ 95% ―¹–Μ―É―΅–Α–Β–≤ ―²–Ψ―à–Ϋ–Ψ―²–Α –±―΄–Μ–Α ―¹–Μ–Α–±–Ψ–Ι, –Κ―Ä–Ψ–Φ–Β ―²–Ψ–≥–Ψ, –Ω–Ψ–¥–Α–≤–Μ―è―é―â–Β–Β –±–Ψ–Μ―¨―à–Η–Ϋ―¹―²–≤–Ψ –Ω–Ψ–¥–Ψ–±–Ϋ―΄―Ö ―ç–Ω–Η–Ζ–Ψ–¥–Ψ–≤ –±―΄–Μ–Η –Ψ―²–Φ–Β―΅–Β–Ϋ―΄ –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Ω–Β―Ä–≤–Ψ–≥–Ψ –Φ–Β―¹―è―Ü–Α –Μ–Β―΅–Β–Ϋ–Η―è. –Δ–Ψ―à–Ϋ–Ψ―²–Α –Η ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Α–Ω–Ω–Β―²–Η―²–Α ―΅–Α―â–Β –≤―¹―²―Ä–Β―΅–Α–Μ–Η―¹―¨ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω–Ψ–Μ―É―΅–Α–Μ–Η –Μ–Β―΅–Β–Ϋ–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ–Ψ–Φ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥. –£ –Φ–Β―¹―²–Β –Η–Ϋ―ä–Β–Κ―Ü–Η–Η ―΅–Α―¹―²―¨ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ψ―²–Φ–Β―΅–Α–Μ–Α –±–Ψ–Μ–Β–Ζ–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨. C―Ä–Β–¥–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥, ―ç―²–Ψ –Η–Φ–Β–Μ–Ψ –Φ–Β―¹―²–Ψ –≤ 15,9% ―¹–Μ―É―΅–Α–Β–≤, –Α –≤ –¥–Ψ–Ζ–Β 190 –Φ–≥ – –≤ 13,6% ―¹–Μ―É―΅–Α–Β–≤. –Γ―Ä–Β–¥–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –Ω–Μ–Α―Ü–Β–±–Ψ –≤ –Ψ–±―ä–Β–Φ–Β 4 –Φ–Μ – –≤ 17,6%, –Α 2 –Φ–Μ – –≤ 9,2% ―¹–Μ―É―΅–Α–Β–≤. 7 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (–Ψ–Κ–Ψ–Μ–Ψ 1%) –Ψ―²–Κ–Α–Ζ–Α–Μ–Η―¹―¨ –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α―²―¨ –Μ–Β―΅–Β–Ϋ–Η–Β –≤―¹–Μ–Β–¥―¹―²–≤–Η–Β –Φ–Β―¹―²–Ϋ―΄―Ö ―Ä–Β–Α–Κ―Ü–Η–Ι, –Η–Ζ –Ϋ–Η―Ö 4 –Ω–Α―Ü–Η–Β–Ϋ―²–Α, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥, 2 –Ω–Α―Ü–Η–Β–Ϋ―²–Α, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –¥–Α–Ϋ–Ϋ―΄–Ι –Ω―Ä–Β–Ω–Α―Ä–Α―² –≤ –¥–Ψ–Ζ–Β 190 –Φ–≥, –Η 1 –Ω–Α―Ü–Η–Β–Ϋ―², –Ω–Ψ–Μ―É―΅–Α–≤―à–Η–Ι –Ω–Μ–Α―Ü–Β–±–Ψ –≤ –Ψ–±―ä–Β–Φ–Β 4 –Φ–Μ.
–‰–Ϋ―ä–Β–Κ―Ü–Η–Η –£–Η–≤–Η―²―Ä–Ψ–Μ–Α ―Ö–Ψ―Ä–Ψ―à–Ψ –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Μ–Η―¹―¨, –±―΄–Μ–Ψ –Ψ―²–Φ–Β―΅–Β–Ϋ–Ψ –≤―¹–Β–≥–Ψ –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Ψ ―¹–Β―Ä―¨–Β–Ζ–Ϋ―΄―Ö –Ϋ–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η–Ι, –Ω―Ä–Η ―ç―²–Ψ–Φ –Ϋ–Β –Ϋ–Α–±–Μ―é–¥–Α–Μ–Ψ―¹―¨ –Ω―Ä–Η–Ζ–Ϋ–Α–Κ–Ψ–≤ –≥–Β–Ω–Α―²–Ψ―²–Ψ–Κ―¹–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è.
–ü―Ä–Β–Κ―Ä–Α―²–Η–Μ–Η ―É―΅–Α―¹―²–Η–Β –≤ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –≤―¹–Μ–Β–¥―¹―²–≤–Η–Β ―Ä–Α–Ζ–≤–Η―²–Η―è –Ω–Ψ–±–Ψ―΅–Ϋ―΄―Ö ―ç―³―³–Β–Κ―²–Ψ–≤ 29 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (14,1%), –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥, 14 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (6,7%), –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 190 –Φ–≥ –Η 14 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (6,7%), –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –Ω–Μ–Α―Ü–Β–±–Ψ (―Ä=0,01)
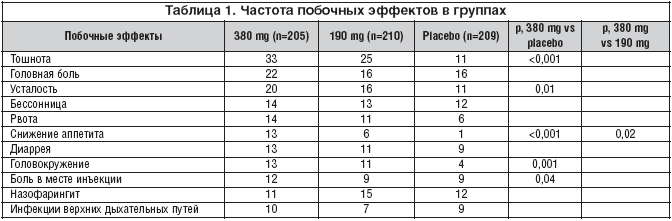
–ü―Ä–Η ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α 380 –Φ–≥ ―¹ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Ψ–Φ 190 –Φ–≥ –Η –Ω–Μ–Α―Ü–Β–±–Ψ ―Ä–Α–Ζ–Μ–Η―΅–Η―è –Ω―Ä–Β–Ε–¥–Β –≤―¹–Β–≥–Ψ –Ψ–±―ä―è―¹–Ϋ―è–Μ–Η―¹―¨ –±–Ψ–Μ―¨―à–Β–Ι ―΅–Α―¹―²–Ψ―²–Ψ–Ι ―²–Ψ―à–Ϋ–Ψ―²―΄, –Φ–Β―¹―²–Ϋ―΄―Ö ―Ä–Β–Α–Κ―Ü–Η–Ι –Η –≥–Ψ–Μ–Ψ–≤–Ϋ―΄―Ö –±–Ψ–Μ–Β–Ι ―¹―Ä–Β–¥–Η –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ 380 –Φ–≥ (―²–Α–±–Μ. 1). –ß–Η―¹–Μ–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Η–Φ–Β–≤―à–Η―Ö ―¹–Β―Ä―¨–Β–Ζ–Ϋ―΄–Β –Ϋ–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄–Β ―è–≤–Μ–Β–Ϋ–Η―è, –±―΄–Μ–Ψ ―¹―Ö–Ψ–¥–Ϋ―΄–Φ –≤ ―Ä–Α–Ζ–Ϋ―΄―Ö –≥―Ä―É–Ω–Ω–Α―Ö: 11 (5,4%) ―¹―Ä–Β–¥–Η –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥, 10 (4,8%) ―¹―Ä–Β–¥–Η –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ 190 –Φ–≥ –Η 15 (7,2%) ―¹―Ä–Β–¥–Η –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –Ω–Μ–Α―Ü–Β–±–Ψ. –ù–Α–Η–±–Ψ–Μ–Β–Β ―΅–Α―¹―²―΄–Φ ―¹–Β―Ä―¨–Β–Ζ–Ϋ―΄–Φ –Ϋ–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄–Φ ―è–≤–Μ–Β–Ϋ–Η–Β–Φ –±―΄–Μ–Α –≥–Ψ―¹–Ω–Η―²–Α–Μ–Η–Ζ–Α―Ü–Η―è ―¹ ―Ü–Β–Μ―¨―é –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –¥–Β―²–Ψ–Κ―¹–Η–Κ–Α―Ü–Η–Η. –î–≤–Α ―¹–Β―Ä―¨–Β–Ζ–Ϋ―΄―Ö –Ϋ–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η―è (―ç–Ψ–Ζ–Η–Ϋ–Ψ―³–Η–Μ―¨–Ϋ–Α―è –Ω–Ϋ–Β–≤–Φ–Ψ–Ϋ–Η―è –Η –Η–Ϋ―²–Β―Ä―¹―²–Η―Ü–Η–Α–Μ―¨–Ϋ–Α―è –Ω–Ϋ–Β–≤–Φ–Ψ–Ϋ–Η―è) –±―΄–Μ–Η ―Ä–Α―¹―Ü–Β–Ϋ–Β–Ϋ―΄ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―è–Φ–Η, –Κ–Α–Κ «–≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ ―¹–≤―è–Ζ–Α–Ϋ–Ϋ―΄–Β ―¹ –Η―¹―¹–Μ–Β–¥―É–Β–Φ―΄–Φ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–Φ». –û–±–Α ―ç―²–Η―Ö ―¹–Β―Ä―¨–Β–Ζ–Ϋ―΄―Ö –Ϋ–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η―è –Η–Φ–Β–Μ–Η –Φ–Β―¹―²–Ψ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥, –Η –±–Μ–Α–≥–Ψ–Ω–Ψ–Μ―É―΅–Ϋ–Ψ ―Ä–Α–Ζ―Ä–Β―à–Η–Μ–Η―¹―¨ –Ω–Ψ―¹–Μ–Β –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η. –≠―²–Η –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η―è ―Ä–Α–Ϋ–Β–Β –Ϋ–Β –Ψ―²–Φ–Β―΅–Α–Μ–Η―¹―¨ –Ω―Ä–Η –Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Η –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α –Η–Μ–Η –ü–¦–™ (–Ω–Ψ–Μ–Η–Μ–Α–Κ―²–Η–¥–Β–Κ–Ψ–≥–Μ–Η–Κ–Ψ–Μ–Η–¥–Ϋ―΄―Ö) –Φ–Η–Κ―Ä–Ψ―¹―³–Β―Ä. –ù–Α ―³–Ψ–Ϋ–Β –Μ–Β―΅–Β–Ϋ–Η―è ―É―Ä–Ψ–≤–Ϋ–Η –ê–Γ–Δ –Η –ê–¦–Δ –Ϋ–Β –Ω―Ä–Β―²–Β―Ä–Ω–Β–≤–Α–Μ–Η ―¹―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η–Ι. –ë–Ψ–Μ–Β–Β ―²–Ψ–≥–Ψ, –Ϋ–Β –Ψ–±–Ϋ–Α―Ä―É–Ε–Β–Ϋ–Ψ –≤–Μ–Η―è–Ϋ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α –Ϋ–Α ―¹–Ψ–Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ω–Ψ–≤―΄―à–Β–Ϋ–Η–Β–Φ ―É―Ä–Ψ–≤–Ϋ―è –ê–Γ–Δ –Η–Μ–Η –ê–¦–Δ –±–Ψ–Μ–Β–Β 3–―Ö –Ϋ–Ψ―Ä–Φ–Α–Μ―¨–Ϋ―΄―Ö –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Ι –≤ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –≥―Ä―É–Ω–Ω–Α―Ö –Μ–Β―΅–Β–Ϋ–Η―è.
–û―¹–Ϋ–Ψ–≤–Ϋ–Ψ–Ι –Ψ―Ü–Β–Ϋ–Η–≤–Α–≤―à–Η–Ι―¹―è –≤ –¥–Α–Ϋ–Ϋ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨ – –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –¥–Ϋ–Β–Ι –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ, ―è–≤–Μ―è–Β―²―¹―è –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –≤–Α–Ε–Ϋ―΄–Φ –Κ―Ä–Η―²–Β―Ä–Η–Β–Φ –¥–Μ―è –Ψ―Ü–Β–Ϋ–Κ–Η ―²―è–Ε–Β―¹―²–Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Η –Η–Φ–Β–Β―² –Κ–Α–Κ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Β, ―²–Α–Κ –Η ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ–Ψ–Β –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β. –Γ―Ä–Β–¥–Η –≤―¹–Β―Ö –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ–Β–Ι –Ψ–Ϋ –Ϋ–Α–Η–±–Ψ–Μ–Β–Β ―¹–Η–Μ―¨–Ϋ–Ψ –Κ–Ψ―Ä―Ä–Β–Μ–Η―Ä―É–Β―² ―¹ –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄–Φ–Η –Ω–Ψ―¹–Μ–Β–¥―¹―²–≤–Η―è–Φ–Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η, ―²–Α–Κ–Η–Φ–Η –Κ–Α–Κ –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―è –Ω―Ä–Α–≤–Η–Μ –¥–Ψ―Ä–Ψ–Ε–Ϋ–Ψ–≥–Ψ –¥–≤–Η–Ε–Β–Ϋ–Η―è, –Φ–Β–Ε–Μ–Η―΅–Ϋ–Ψ―¹―²–Ϋ―΄–Φ–Η –Κ–Ψ–Ϋ―³–Μ–Η–Κ―²–Α–Φ–Η –Η ―²―Ä–Α–≤–Φ–Α―²–Η–Ζ–Φ–Ψ–Φ.
–Γ–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ ―É–Μ―É―΅―à–Β–Ϋ–Η―é ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –Α―¹–Ω–Β–Κ―²–Ψ–≤ –Ζ–¥–Ψ―Ä–Ψ–≤―¨―è –Η –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η –±–Ψ–Μ―¨–Ϋ―΄―Ö, ―΅―²–Ψ –±―΄–Μ–Ψ –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Β–Ϋ–Ψ –≤ –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è―Ö. –ù–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ ―É―΅–Η―²―΄–≤–Α―²―¨ –Η ―²–Ψ –Ψ–±―¹―²–Ψ―è―²–Β–Μ―¨―¹―²–≤–Ψ, ―΅―²–Ψ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Α―è –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨ ―è–≤–Μ―è–Β―²―¹―è ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η–Φ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β–Φ, –≤ ―¹–≤―è–Ζ–Η ―¹ ―΅–Β–Φ –Ϋ–Η –Ψ–¥–Η–Ϋ –≤–Η–¥ –Μ–Β―΅–Β–Ϋ–Η―è –Ϋ–Β –Ω–Ψ–Ζ–≤–Ψ–Μ―è–Β―² –Ω–Ψ–Μ–Ϋ–Ψ―¹―²―¨―é –Η―¹–Κ–Μ―é―΅–Η―²―¨ ―Ä–Η―¹–Κ –Ζ–Μ–Ψ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ–Β–Φ –Η ―Ä–Β―Ü–Η–¥–Η–≤–Α. –£ ―¹–≤―è–Ζ–Η ―¹ ―ç―²–Η–Φ ―¹–Μ–Β–¥―É–Β―² –Ψ―²–Φ–Β―²–Η―²―¨ –≤–Α–Ε–Ϋ–Ψ–Β –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Β –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Ψ –£–Η–≤–Η―²―Ä–Ψ–Μ–Α: –Ω―Ä–Β–Ω–Α―Ä–Α―² –Φ–Ψ–Ε–Β―² ―É―¹–Ω–Β―à–Ϋ–Ψ –Ω―Ä–Η–Φ–Β–Ϋ―è―²―¨―¹―è –≤ –Κ–Ψ–Φ–±–Η–Ϋ–Α―Ü–Η–Η ―¹ –¥―Ä―É–≥–Η–Φ–Η –≤–Η–¥–Α–Φ–Η –Μ–Β―΅–Β–Ϋ–Η―è, –≤–Κ–Μ―é―΅–Α―è ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄–Β ―¹―Ä–Β–¥―¹―²–≤–Α –Η/–Η–Μ–Η –Ω―¹–Η―Ö–Ψ―²–Β―Ä–Α–Ω–Η―é.
–£ –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Β–Φ –±―΄–Μ–Ψ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ψ ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ–Α –Ϋ–Α ―²–Ψ–Ι –Ε–Β –≤―΄–±–Ψ―Ä–Κ–Β –±–Ψ–Μ―¨–Ϋ―΄―Ö [35,36], –Κ–Ψ―²–Ψ―Ä–Ψ–Β –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α–Μ–Ψ―¹―¨ –±–Ψ–Μ–Β–Β 12 –Φ–Β―¹―è―Ü–Β–≤. –ê–≤―²–Ψ―Ä―΄ –Ω―Ä–Η―à–Μ–Η –Κ –Ζ–Α–Κ–Μ―é―΅–Β–Ϋ–Η―é, ―΅―²–Ψ –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ ―ç―³―³–Β–Κ―²–Α –Μ–Β―΅–Β–Ϋ–Η―è ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α–Μ–Η –Ω―Ä–Η–Ϋ–Η–Φ–Α―²―¨ –£–Η–≤–Η―²―Ä–Ψ–Μ, –Ω―Ä–Β–≤―΄―à–Α–Β―² ―ç―²–Ψ―² –Ω–Β―Ä–Η–Ψ–¥. –£–Α–Ε–Ϋ–Ψ –Ψ―²–Φ–Β―²–Η―²―¨, ―΅―²–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²―΄, –Κ–Ψ―²–Ψ―Ä―΄–Β –≤ –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–Φ (–Ω–Β―Ä–≤–Ψ–Φ) –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Ω–Ψ–Μ―É―΅–Α–Μ–Η –Ω―¹–Η―Ö–Ψ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ―É―é –Ω–Ψ–¥–¥–Β―Ä–Ε–Κ―É –Η –Ω–Μ–Α―Ü–Β–±–Ψ, –≤ –¥–Α–Ϋ–Ϋ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Ϋ–Α―΅–Η–Ϋ–Α–Μ–Η –Ω–Ψ–Μ―É―΅–Α―²―¨ –Ω―¹–Η―Ö–Ψ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ―É―é –Ω–Ψ–¥–¥–Β―Ä–Ε–Κ―É –Η –£–Η–≤–Η―²―Ä–Ψ–Μ, –Ω―Ä–Η ―ç―²–Ψ–Φ ―É –Ϋ–Η―Ö –Ψ―²–Φ–Β―΅–Α–Μ–Ψ―¹―¨ ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α ―Ä–Β―Ü–Η–¥–Η–≤–Ψ–≤ –Η –Ζ–Α–Ω–Ψ–Β–≤. –¦–Β―΅–Β–Ϋ–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ–Ψ–Φ –≤ –¥–Ψ–Ζ–Α―Ö 190 –Φ–≥ –Η 380 –Φ–≥ –Ψ–±―΄―΅–Ϋ–Ψ ―Ö–Ψ―Ä–Ψ―à–Ψ –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Μ–Ψ―¹―¨ –Ϋ–Α –Ω―Ä–Ψ―²―è–Ε–Β–Ϋ–Η–Η 1,5 –Μ–Β―² –±–Β–Ζ –Ω―Ä–Η–Ζ–Ϋ–Α–Κ–Ψ–≤ ―²–Ψ–Κ―¹–Η―΅–Ϋ–Ψ―¹―²–Η –¥–Μ―è –Ω–Β―΅–Β–Ϋ–Η –Η ―¹ –Ϋ–Η–Ζ–Κ–Ψ–Ι –≤–Β―Ä–Ψ―è―²–Ϋ–Ψ―¹―²―¨―é –Ω―Ä–Β–Κ―Ä–Α―â–Β–Ϋ–Η―è –Μ–Β―΅–Β–Ϋ–Η―è –≤―¹–Μ–Β–¥―¹―²–≤–Η–Β –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄―Ö ―ç―³―³–Β–Κ―²–Ψ–≤. –†–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Κ–Α–Κ –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–≥–Ψ, ―²–Α–Κ –Η ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –Ω―Ä–Ψ–¥–Β–Φ–Ψ–Ϋ―¹―²―Ä–Η―Ä–Ψ–≤–Α–Μ–Η –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ―É―é ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –£–Η–≤–Η―²―Ä–Ψ–Μ–Α –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η.
–ü―Ä–Η –Η–Ζ―É―΅–Β–Ϋ–Η–Η ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α –≤ –≥―Ä―É–Ω–Ω–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (–≤―΄–±–Ψ―Ä–Κ–Α ―¹–Ψ―¹―²–Α–≤–Μ―è–Μ–Α 82 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤), –Κ–Ψ―²–Ψ―Ä―΄–Β –¥–Ψ–±―Ä–Ψ–≤–Ψ–Μ―¨–Ϋ–Ψ –≤–Ψ–Ζ–¥–Β―Ä–Ε–Η–≤–Α–Μ–Η―¹―¨ –Ψ―² –Ω―Ä–Η–Β–Φ–Α –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –≤ ―²–Β―΅–Β–Ϋ–Η–Β 4–―Ö –Η–Μ–Η –±–Ψ–Μ–Β–Β –¥–Ϋ–Β–Ι –¥–Ψ –Ϋ–Α―΅–Α–Μ–Α –Μ–Β―΅–Β–Ϋ–Η―è, –±―΄–Μ–Η –Ω–Ψ–Μ―É―΅–Β–Ϋ―΄ ―¹–Μ–Β–¥―É―é―â–Η–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ [37]. –Γ―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –≤―Ä–Β–Φ–Β–Ϋ–Η –¥–Ψ –Μ―é–±–Ψ–≥–Ψ ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è ―¹–Ψ―¹―²–Α–≤–Μ―è–Μ–Α 41 –¥–Β–Ϋ―¨ –¥–Μ―è –≥―Ä―É–Ω–Ω―΄ –£–Η–≤–Η―²―Ä–Ψ–Μ 380 –Φ–≥ –Ω―Ä–Ψ―²–Η–≤ 12 –¥–Ϋ–Β–Ι –¥–Μ―è –Ω–Μ–Α―Ü–Β–±–Ψ. –Γ―²–Β–Ω–Β–Ϋ―¨ –Ω–Ψ–Μ–Ϋ–Ψ–≥–Ψ –≤–Ψ–Ζ–¥–Β―Ä–Ε–Α–Ϋ–Η―è –≤ –Κ–Ψ–Ϋ―Ü–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è (24 –Ϋ–Β–¥–Β–Μ–Η) ―¹–Ψ―¹―²–Α–≤–Μ―è–Μ–Α 32% –¥–Μ―è –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Η–Ζ –≥―Ä―É–Ω–Ω―΄ –£–Η–≤–Η―²―Ä–Ψ–Μ 380 –Φ–≥ –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ 11% –¥–Μ―è –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Η–Ζ –≥―Ä―É–Ω–Ω―΄ –Ω–Μ–Α―Ü–Β–±–Ψ (p=0,02) (―Ä–Η―¹. 2).
–ê–≤―²–Ψ―Ä―΄ –Ψ―²–Φ–Β―²–Η–Μ–Η, ―΅―²–Ψ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö 380 –Φ–≥ –£–Η–≤–Η―²―Ä–Ψ–Μ–Α, –Ψ―²–Φ–Β―΅–Α–Μ–Ψ―¹―¨ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –Φ–Β–Ϋ―¨―à–Β –¥–Ϋ–Β–Ι ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –≤ –Φ–Β―¹―è―Ü, ―΅–Β–Φ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –Ω–Μ–Α―Ü–Β–±–Ψ (―¹―Ä–Β–¥–Ϋ–Β–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –¥–Ϋ–Β–Ι – 0,7 –Ω―Ä–Ψ―²–Η–≤ 7,2 ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ; ―Ä=0,005). –ü―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –≤―Ä–Β–Φ–Β–Ϋ–Η –¥–Ψ ―Ä–Α–Ζ–≤–Η―²–Η―è ―Ä–Β―Ü–Η–¥–Η–≤–Α –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –±―΄–Μ–Α –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –±–Ψ–Μ―¨―à–Β –¥–Μ―è –≥―Ä―É–Ω–Ω―΄ –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ 380 –Φ–≥ –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Ω–Μ–Α―Ü–Β–±–Ψ (>180 –¥–Ϋ–Β–Ι –Ω―Ä–Ψ―²–Η–≤ 20 –¥–Ϋ–Β–Ι, ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ; ―Ä=0,04). –£ ―²–Ψ –Ε–Β –≤―Ä–Β–Φ―è, –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –¥–Ϋ–Β–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ–≥–Ψ ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –≤ –Φ–Β―¹―è―Ü ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ 380 –Φ–≥ ―²–Α–Κ–Ε–Β –±―΄–Μ–Ψ –≥–Ψ―Ä–Α–Ζ–¥–Ψ –Φ–Β–Ϋ―¨―à–Β, ―΅–Β–Φ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –Ω–Μ–Α―Ü–Β–±–Ψ (―¹―Ä–Β–¥–Ϋ–Β–Β ―΅–Η―¹–Μ–Ψ –¥–Ϋ–Β–Ι, 0,2 –Ω―Ä–Ψ―²–Η–≤ 2,9, ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ; ―Ä=0,007). –ö―Ä–Ψ–Φ–Β ―²–Ψ–≥–Ψ, –Α–≤―²–Ψ―Ä―΄ –Ψ―²–Φ–Β―²–Η–Μ–Η –Η –±–Ψ–Μ―¨―à―É―é –Κ–Ψ–Φ–Ω–Μ–Α–Β–Ϋ―²–Ϋ–Ψ―¹―²―¨ –±–Ψ–Μ―¨–Ϋ―΄―Ö –≤ –≥―Ä―É–Ω–Ω–Β, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö 380 –Φ–≥ –£–Η–≤–Η―²―Ä–Ψ–Μ–Α –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Ω–Μ–Α―Ü–Β–±–Ψ (70% –≤ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹ 30%, ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Β–Ϋ–Ϋ–Ψ ―Ä=0,006). –û―²–≤–Β―² –Ϋ–Α –Μ–Β―΅–Β–Ϋ–Η–Β –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Μ―¹―è –Κ–Α–Κ –Ϋ–Β –±–Ψ–Μ–Β–Β ―΅–Β–Φ 2 –¥–Ϋ―è –Α–Κ―²–Η–≤–Ϋ–Ψ–≥–Ψ ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –≤ –Μ―é–±–Ψ–Ι –Ω–Ψ―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―¨–Ϋ―΄–Ι 28 –¥–Ϋ–Β–≤–Ϋ―΄–Ι –Ω–Β―Ä–Η–Ψ–¥.
–Θ―΅–Η―²―΄–≤–Α―è, ―΅―²–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²―΄ –≤ –≥―Ä―É–Ω–Ω–Β, –Ω–Ψ–Μ―É―΅–Α–≤―à–Β–Ι –£–Η–≤–Η―²―Ä–Ψ–Μ 380 –Φ–≥ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –≤ –Φ–Β–Ϋ―¨―à–Β–Ι ―¹―²–Β–Ω–Β–Ϋ–Η –Ω–Ψ–¥–≤–Β―Ä–≥–Α–Μ–Η―¹―¨ –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η―é –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Η–Ϋ―²–Ψ–Κ―¹–Η–Κ–Α―Ü–Η–Η, ―²–Ψ –Η ―É―Ä–Ψ–≤–Β–Ϋ―¨ –™–™–Δ ―¹–Ϋ–Η–Ε–Α–Μ―¹―è –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –±―΄―¹―²―Ä–Β–Β ―É ―ç―²–Ψ–Ι –≥―Ä―É–Ω–Ω―΄ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –≥―Ä―É–Ω–Ω–Ψ–Ι –Ω–Μ–Α―Ü–Β–±–Ψ (–Ψ–±–Ψ–±―â–Β–Ϋ–Ϋ―΄–Ι –Α–Ϋ–Α–Μ–Η–Ζ –Ψ―Ü–Β–Ϋ–Ψ―΅–Ϋ―΄―Ö ―É―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Ι, ―Ä=0,03).
–£ ―Ö–Ψ–¥–Β 6––Φ–Β―¹―è―΅–Ϋ–Ψ–≥–Ψ, –Φ–Ϋ–Ψ–≥–Ψ―Ü–Β–Ϋ―²―Ä–Ψ–≤–Ψ–≥–Ψ, –Ω–Μ–Α―Ü–Β–±–Ψ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è, –≤–Κ–Μ―é―΅–Α–≤―à–Β–≥–Ψ –Η –Ω–Ψ–¥–≥―Ä―É–Ω–Ω―΄ ―¹–Η–Μ―¨–Ϋ–Ψ –Ω―¨―é―â–Η―Ö, ―¹―²―Ä–Α–¥–Α―é―â–Η―Ö –Ψ–Ε–Η―Ä–Β–Ϋ–Η–Β–Φ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Η–Μ–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω―Ä–Η–Φ–Β–Ϋ―è―é―â–Η―Ö –≤–Ψ –≤―Ä–Β–Φ―è –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è NSAID (–Ϋ–Β―¹―²–Β―Ä–Ψ–Η–¥–Ϋ―΄–Β –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Β –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄–Β ―¹―Ä–Β–¥―¹―²–≤–Α) –±―΄–Μ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ –≤―¹–Β―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Η–Ι –Α–Ϋ–Α–Μ–Η–Ζ –≤–Μ–Η―è–Ϋ–Η―è –£–Η–≤–Η―²―Ä–Ψ–Μ–Α –Ϋ–Α ―³―É–Ϋ–Κ―Ü–Η–Η –Ω–Β―΅–Β–Ϋ–Η [38].
–û―² –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ϋ–Β ―²―Ä–Β–±–Ψ–≤–Α–Μ–Ψ―¹―¨ –≤–Ψ–Ζ–¥–Β―Ä–Ε–Η–≤–Α―²―¨―¹―è –Ψ―² –Ω―Ä–Η–Β–Φ–Α –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Κ –Φ–Ψ–Φ–Β–Ϋ―²―É –Ω–Β―Ä–≤–Ψ–Ι –Η–Ϋ―ä–Β–Κ―Ü–Η–Η, –Η –Ψ–Ϋ–Η –Ϋ–Β –Η―¹–Κ–Μ―é―΅–Α–Μ–Η―¹―¨ –Η–Ζ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è, –Β―¹–Μ–Η –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α–Μ–Η ―É–Ω–Ψ―²―Ä–Β–±–Μ―è―²―¨ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨. –£ –¥–Ψ–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Β –Κ –Μ–Β―΅–Β–Ϋ–Η―é –Η―¹―¹–Μ–Β–¥―É–Β–Φ―΄–Φ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–Φ –Ω–Α―Ü–Η–Β–Ϋ―²–Α–Φ –≤–Ψ –≤―Ä–Β–Φ―è –≤–Η–Ζ–Η―²–Ψ–≤ –≤ –Κ–Μ–Η–Ϋ–Η–Κ―É –Ψ–Κ–Α–Ζ―΄–≤–Α–Μ–Α―¹―¨ ―²–Α–Κ–Ε–Β –Ω―¹–Η―Ö–Ψ―¹–Ψ―Ü–Η–Α–Μ―¨–Ϋ–Α―è –Ω–Ψ–¥–¥–Β―Ä–Ε–Κ–Α. –¦–Α–±–Ψ―Ä–Α―²–Ψ―Ä–Ϋ–Α―è –Ψ―Ü–Β–Ϋ–Κ–Α ―³―É–Ϋ–Κ―Ü–Η–Η –Ω–Β―΅–Β–Ϋ–Η –±―΄–Μ–Α –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Α ―É 193 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω―Ä–Η–Ϋ–Η–Φ–Α―é―â–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥, 193 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω―Ä–Η–Ϋ–Η–Φ–Α―é―â–Η―Ö –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 190 –Φ–≥ –Η 198 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α―é―â–Η―Ö –Ω–Μ–Α―Ü–Β–±–Ψ. –‰–Ζ ―ç―²–Ψ–Ι –±–Ψ–Μ―¨―à–Ψ–Ι –≤―΄–±–Ψ―Ä–Κ–Η –Μ–Η―à―¨ 2 –Ω–Α―Ü–Η–Β–Ϋ―²–Α –±―΄–Μ–Η –Η―¹–Κ–Μ―é―΅–Β–Ϋ―΄ –Η–Ζ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –Η–Ζ––Ζ–Α ―¹–≤―è–Ζ–Α–Ϋ–Ϋ―΄―Ö ―¹ –Ω–Β―΅–Β–Ϋ―¨―é –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η–Ι. –†–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –Ω–Ψ–Ζ–≤–Ψ–Μ–Η–Μ–Η ―¹–¥–Β–Μ–Α―²―¨ –≤―΄–≤–Ψ–¥ –Ψ ―²–Ψ–Φ, ―΅―²–Ψ –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Α―Ö 380 –Φ–≥, 190 –Φ–≥ ―è–≤–Μ―è–Β―²―¹―è –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ –±–Β–Ζ–Ψ–Ω–Α―¹–Ϋ―΄–Φ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–Φ. –ù–Β –±―΄–Μ–Ψ –Ω–Ψ–Μ―É―΅–Β–Ϋ–Ψ ―¹–≤–Η–¥–Β―²–Β–Μ―¨―¹―²–≤ –Ψ –Β―â–Β –±–Ψ–Μ―¨―à–Β–Φ –Ω–Ψ–≤―΄―à–Β–Ϋ–Η–Η –≤―΄―¹–Ψ–Κ–Η―Ö (>3–―Ö –Ϋ–Ψ―Ä–Φ) –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Ι –Α–Φ–Η–Ϋ–Ψ―²―Ä–Α–Ϋ―¹―³–Β―Ä–Α–Ζ –Ζ–Α –Ω–Β―Ä–≤―΄–Β –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Ψ –Ϋ–Β–¥–Β–Μ―¨ –Μ–Β―΅–Β–Ϋ–Η―è –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–Φ –£–Η–≤–Η―²―Ä–Ψ–Μ. –Γ―²–Β–Ω–Β–Ϋ―¨ ―¹–≤―è–Ζ–Α–Ϋ–Ϋ―΄―Ö ―¹ ―³―É–Ϋ–Κ―Ü–Η–Β–Ι –Ω–Β―΅–Β–Ϋ–Η –Ϋ–Β–±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η–Ι –±―΄–Μ–Α –Ϋ–Η–Ζ–Κ–Ψ–Ι, –Η ―Ä–Α–Ζ–Μ–Η―΅–Η–Β –Φ–Β–Ε–¥―É –≥―Ä―É–Ω–Ω–Α–Φ–Η, –Ω―Ä–Η–Φ–Β–Ϋ―è―é―â–Η–Φ–Η –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –Μ―é–±–Ψ–Ι –¥–Ψ–Ζ–Β –Η –Ω–Μ–Α―Ü–Β–±–Ψ, –±―΄–Μ–Ψ –Ϋ–Β–Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ―΄–Φ. –½–Ϋ–Α―΅–Β–Ϋ–Η―è –™–™–Δ –±―΄–Μ–Η –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –Ϋ–Η–Ε–Β –≤ –≥―Ä―É–Ω–Ω–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α―é―â–Η―Ö –≤–Ψ –≤―Ä–Β–Φ―è –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –£–Η–≤–Η―²―Ä–Ψ–Μ –≤ –¥–Ψ–Ζ–Β 380 –Φ–≥, ―΅–Β–Φ –≤ –≥―Ä―É–Ω–Ω–Β, –Ω–Ψ–Μ―É―΅–Α―é―â–Β–Ι –Ω–Μ–Α―Ü–Β–±–Ψ. –≠―²–Ψ –±–Μ–Α–≥–Ψ–Ω―Ä–Η―è―²–Ϋ–Ψ–Β –≤–Μ–Η―è–Ϋ–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ–Α 380 –Φ–≥, –Κ–Α–Κ ―É–Ε–Β ―É–Ω–Ψ–Φ–Η–Ϋ–Α–Μ–Ψ―¹―¨ –≤―΄―à–Β, –≤―΄–Ζ–≤–Α–Ϋ–Ψ –Η–Φ–Β–Ϋ–Ϋ–Ψ –≤–Ψ–Ζ–¥–Β―Ä–Ε–Α–Ϋ–Η–Β–Φ –Ψ―² ―É–Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –Η –≥–Μ–Α–≤–Ϋ―΄–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ – ―¹–Ϋ–Η–Ε–Β–Ϋ–Η―è –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α –Ζ–Α–Ω–Ψ–Β–≤.
–ù–Β―¹–Φ–Ψ―²―Ä―è –Ϋ–Α ―²–Ψ, ―΅―²–Ψ –£–Η–≤–Η―²―Ä–Ψ–Μ –Ω―Ä–Ψ―è–≤–Η–Μ ―¹–Β–±―è, –Κ–Α–Κ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ―΄–Ι –Φ–Ψ–¥–Η―³–Η–Κ–Α―²–Ψ―Ä –≤―Ä–Β–¥–Ϋ–Ψ–≥–Ψ –Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è, –Ϋ–Β–Κ–Ψ―²–Ψ―Ä―΄–Β –Ω–Α―Ü–Η–Β–Ϋ―²―΄ –≤–Ψ –≤―Ä–Β–Φ―è –Μ–Β―΅–Β–Ϋ–Η―è –±―É–¥―É―² –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α―²―¨ –Ω–Η―²―¨, –≤―Ä–Β–Φ–Β–Ϋ–Α–Φ–Η –Α–Κ―²–Η–≤–Ϋ–Ψ. –ö–Μ―é―΅–Β–≤―΄–Φ –≤―΄–≤–Ψ–¥–Ψ–Φ –¥–Α–Ϋ–Ϋ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è ―è–≤–Η–Μ–Ψ―¹―¨ ―²–Ψ, ―΅―²–Ψ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –£–Η–≤–Η―²―Ä–Ψ–Μ–Α –≤ –Ω–Ψ–¥–≥―Ä―É–Ω–Ω–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Α―é―â–Η―Ö –Α–Κ―²–Η–≤–Ϋ–Ψ –Ω―Ä–Η–Ϋ–Η–Φ–Α―²―¨ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨ –≤–Ψ –≤―Ä–Β–Φ―è –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è, –Ϋ–Β –≤―΄–Ζ―΄–≤–Α–Μ–Ψ –Ω–Ψ–≤―΄―à–Β–Ϋ–Η―è ―É―Ä–Ψ–≤–Ϋ―è ―¹―΄–≤–Ψ―Ä–Ψ―²–Ψ―΅–Ϋ―΄―Ö ―²―Ä–Α–Ϋ―¹–Α–Φ–Η–Ϋ–Α–Ζ. –≠―²–Η –¥–Α–Ϋ–Ϋ―΄–Β –≥–Ψ–≤–Ψ―Ä―è―² –Ψ ―²–Ψ–Φ, ―΅―²–Ψ –£–Η–≤–Η―²―Ä–Ψ–Μ –Ϋ–Β –Ψ–±–Μ–Α–¥–Α–Β―² –≥–Β–Ω–Α―²–Ψ―²–Ψ–Κ―¹–Η―΅–Ϋ–Ψ―¹―²―¨―é. –ï–≥–Ψ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β (–≤ –Μ―é–±–Ψ–Ι –¥–Ψ–Ζ–Β) ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹―²―Ä–Α–¥–Α―é―â–Η―Ö –Ψ–Ε–Η―Ä–Β–Ϋ–Η–Β–Φ, –Α ―²–Α–Κ–Ε–Β ―¹–Ψ–≤–Φ–Β―¹―²–Ϋ–Ψ–Β –Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β NSAID (–Ϋ–Β―¹―²–Β―Ä–Ψ–Η–¥–Ϋ―΄―Ö –Ω―Ä–Ψ―²–Η–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄―Ö ―¹―Ä–Β–¥―¹―²–≤) –Ϋ–Β –≤―΄–Ζ―΄–≤–Α–Μ–Ψ –Ω–Ψ–≤―΄―à–Β–Ϋ–Η―è ―É―Ä–Ψ–≤–Ϋ–Β–Ι –Α–Φ–Η–Ϋ–Ψ―²―Ä–Α–Ϋ―¹―³–Β―Ä–Α–Ζ –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Ω–Μ–Α―Ü–Β–±–Ψ. –ü―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ϋ―΄–Ι –Α–Ϋ–Α–Μ–Η–Ζ –Ϋ–Α―É―΅–Ϋ―΄―Ö ―Ä–Α–±–Ψ―² –Ω–Ψ–Κ–Α–Ζ―΄–≤–Α–Β―² –Ω–Β―Ä―¹–Ω–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η―è –Η–Ϋ―ä–Β–Κ―Ü–Η–Ψ–Ϋ–Ϋ–Ψ–Ι –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ –¥–Β–Ι―¹―²–≤―É―é―â–Β–Ι ―³–Ψ―Ä–Φ―΄ –Ϋ–Α–Μ―²―Ä–Β–Κ―¹–Ψ–Ϋ–Α (–£–Η–≤–Η―²―Ä–Ψ–Μ–Α) –≤ –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Ι –Ω―Ä–Α–Κ―²–Η–Κ–Β. –£ –Ψ―¹–Ϋ–Ψ–≤–Ϋ–Ψ–Φ ―ç―²–Ψ –Κ–Α―¹–Α–Β―²―¹―è –±–Ψ–Μ―¨–Ϋ―΄―Ö ―¹ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²―¨―é –Ψ―² –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è. –ù–Β―¹–Ψ–Φ–Ϋ–Β–Ϋ–Ϋ–Ψ, –±–Ψ–Μ–Β–Β –±―΄―¹―²―Ä–Ψ–Β –≤–Ϋ–Β–¥―Ä–Β–Ϋ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α –Κ–Α–Κ –≤ ―¹―²–Α―Ü–Η–Ψ–Ϋ–Α―Ä–Ϋ―É―é, ―²–Α–Κ –Η –≤ –Α–Φ–±―É–Μ–Α―²–Ψ―Ä–Ϋ―É―é –Ω―Ä–Α–Κ―²–Η–Κ―É ―Ä–Α―¹―à–Η―Ä–Η―² –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²–Η ―²–Β―Ä–Α–Ω–Η–Η –Η –¥–Μ―è –≤―Ä–Α―΅–Α, –Η –¥–Μ―è –Ω–Α―Ü–Η–Β–Ϋ―²–Α.
–£ –Ζ–Α–Κ–Μ―é―΅–Β–Ϋ–Η–Β ―Ö–Ψ―²–Β–Μ–Ψ―¹―¨ –±―΄ –Β―â–Β ―Ä–Α–Ζ –Ω–Ψ–¥―΅–Β―Ä–Κ–Ϋ―É―²―¨, ―΅―²–Ψ –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ―΄ ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –¥–Ψ―¹―²–Α―²–Ψ―΅–Ϋ–Ψ ―¹–Μ–Ψ–Ε–Ϋ―΄, –≤ –Ϋ–Η―Ö –Ζ–Α–¥–Β–Ι―¹―²–≤–Ψ–≤–Α–Ϋ―΄ –Φ–Ϋ–Ψ–≥–Η–Β –Ϋ–Β–Ι―Ä–Ψ–Φ–Β–¥–Η–Α―²–Ψ―Ä–Ϋ―΄–Β ―¹–Η―¹―²–Β–Φ―΄: –¥–Ψ―³–Α–Φ–Η–Ϋ–Ψ–≤–Α―è, –™–ê–€–ö––Β―Ä–≥–Η―΅–Β―¹–Κ–Α―è, ―¹–Β―Ä–Ψ―²–Ψ–Ϋ–Η–Ϋ–Β―Ä–≥–Η―΅–Β―¹–Κ–Α―è, ―¹–Η―¹―²–Β–Φ–Α –Ψ–Ω–Η–Α―²–Ϋ―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –Η –¥―Ä. –£ ―¹–≤―è–Ζ–Η ―¹ ―ç―²–Η–Φ ―²–Β―Ä–Α–Ω–Β–≤―²–Η―΅–Β―¹–Κ–Η–Β –Ω―Ä–Ψ–≥―Ä–Α–Φ–Φ―΄ –¥–Ψ–Μ–Ε–Ϋ―΄ –±―΄―²―¨ –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ―΄–Φ–Η –Η ―¹–Ψ―΅–Β―²–Α―²―¨ –≤ ―¹–Β–±–Β –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η–Β –Ϋ–Α ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –Ζ–≤–Β–Ϋ―¨―è –Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ–Α. –Δ–Ψ–Μ―¨–Κ–Ψ –Ω―Ä–Η ―¹–Ψ–±–Μ―é–¥–Β–Ϋ–Η–Η ―ç―²–Ψ–≥–Ψ ―É―¹–Μ–Ψ–≤–Η―è –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ –¥–Ψ―¹―²–Η–Ε–Β–Ϋ–Η–Β –Ω–Ψ–Μ–Ψ–Ε–Η―²–Β–Μ―¨–Ϋ―΄―Ö ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è, –Ζ–Α–Κ–Μ―é―΅–Α―é―â–Β–Β―¹―è –≤ ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η–Η –¥–Μ–Η―²–Β–Μ―¨–Ϋ―΄―Ö, ―¹―²–Α–±–Η–Μ―¨–Ϋ―΄―Ö ―Ä–Β–Φ–Η―¹―¹–Η–Ι.


–¦–Η―²–Β―Ä–Α―²―É―Ä–Α
1. –ê–Ϋ–Ψ―Ö–Η–Ϋ–Α –‰.–ü. –ë–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Β –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ―΄ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –Ω―¹–Η―Ö–Ψ–Α–Κ―²–Η–≤–Ϋ―΄―Ö –≤–Β―â–Β―¹―²–≤ (–Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ). –£ –Κ–Ϋ. –¦–Β–Κ―Ü–Η–Η –Ω–Ψ –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η–Η. –‰–Ζ–¥. ―²―Ä–Β―²―¨–Β, –Ω–Β―Ä–Β―Ä–Α–±–Ψ―²–Α–Ϋ–Ϋ–Ψ–Β –Η ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–Β /–ü–Ψ–¥ ―Ä–Β–¥. –Ω―Ä–Ψ―³. –‰–≤–Α–Ϋ―Ü–Α –ù.–ù. – –€.: –€–Β–¥–Ω―Ä–Α–Κ―²–Η–Κ–Α, 2001. –Γ. 13–33.
2. –‰–≤–Α–Ϋ–Β―Ü –ù.–ù. –Γ–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Α―è –Κ–Ψ–Ϋ―Ü–Β–Ω―Ü–Η―è ―²–Β―Ä–Α–Ω–Η–Η –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η―Ö –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Ι. –£ –Κ–Ϋ.: –¦–Β–Κ―Ü–Η–Η –Ω–Ψ –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η–Η. –‰–Ζ–¥. ―²―Ä–Β―²―¨–Β, –Ω–Β―Ä–Β―Ä–Α–±–Ψ―²–Α–Ϋ–Ϋ–Ψ–Β –Η ―Ä–Α―¹―à–Η―Ä–Β–Ϋ–Ϋ–Ψ–Β /–ü–Ψ–¥ ―Ä–Β–¥. –Ω―Ä–Ψ―³. –‰–≤–Α–Ϋ―Ü–Α –ù.–ù. – –€.: –€–Β–¥–Ω―Ä–Α–Κ―²–Η–Κ–Α, 2001. –Γ. 105–117.
3. Block B. A., Holland R.T. Recidivist Alcoholies: A doubl–blind, placeco–controlled study of Fluvoxamin // Alcohol and Alcoholism. – 1993. – V. 38. – ⳕ 2. – P. 253.
4. Erickson C.K. The neurochemistry of craving // Treatment today. – 1995. – Vol. 7. – ⳕ 2. – P. 8–9.
5. Erickson C.K. Review of neurotransmitters and their role in alcoholism treatment // Alcohol & Alcoholism. – 1996. – Vol. 13. – Suppl. 1. – P. 5–11.
6. Ludwig A.M. Biology of alcohol psychosocial factors / Eds. B. Kissin, H. Begleiter. – New York, 1983. – –†. 197–214.
7. –ê–Ϋ–Ψ―Ö–Η–Ϋ–Α –‰.–ü. –ë–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Β –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ―΄ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –Ω―¹–Η―Ö–Ψ―²―Ä–Ψ–Ω–Ϋ―΄―Ö –≤–Β―â–Β―¹―²–≤ //–£–Ψ–Ω―Ä–Ψ―¹―΄ –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η–Η. 1995. ⳕ. 2. –Γ. 27–31.
8. –ê–Ϋ–Ψ―Ö–Η–Ϋ–Α –‰.–ü., –ë–Α–Μ–Α―à–Ψ–≤ –ê.–€., –ö–Ψ–≥–Α–Ϋ –ë.–€., –ü–Α–Ϋ―΅–Β–Ϋ–Κ–Ψ –¦.–Λ. –†–Ψ–Μ―¨ –Ψ–Ω–Η–Α―²–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄ –≤ –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Α―Ö ―³–Ψ―Ä–Φ–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –Α–Μ–Κ–Ψ–≥–Ψ–Μ―¨–Ϋ–Ψ–Ι –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η // –£–Ψ–Ω―Ä–Ψ―¹―΄ –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η–Η. 1989. ⳕ. 3. –Γ. 3–11.
9. Srisurapanont M, Jarusuraisin N. Opioid antagonists for alcohol dependence. Cochrane Database Syst Rev. 2005;1: CD001867.
10. Volpicelli JR, Watson NT, King AC, Sherman Ce, O’Brien CP. Effect of naltrexon on alcohol «high» in alcoholics. //Am J Psychiatry. – 1995. – V. 152. – P. 613–615.
11. Volpicelli JR, Alterman AI, Hayashida M, O’Brien CP. Naltrexone in the treatment of alcohol dependence. //Arch Gen Psychiatry. – 1992. – V. 49. – P. 876–880.
12. O’ Malley S. S., Jaffe A. J., Chang G et al. Naltrexone and coping skills therapy for alcohol dependence: a controlled study // Archives of General Psychiatry. – 1992. – Nov. Vol. 49. – P. 881–887.
13. Volpicelli J. R., Rhines K. S., Rhines J. S. et al. Naltrexone and alcohol dependence: role of subject compliance. // J. Arch. Gen. Psychiatry. – 1997. Aug. – Vol. 54. – ⳕ 8. – P. 737–742.
14. Soyka M. Klinicshe Erfahrungen mit Naltrexon in der alkoholabhaengigkeit. //Psycho. – 22. – 1996. – ⳕ. 6. – s. 429–433.
15. Harris KM, DeVries A, Dimidjian K. Trends in naltrexonenuse among members of a large private health plan. Psychiatr Serv. 2004;55(3):221.
16. Pettinati HM, Volpicelli JR, Pierce JD Jr, et al. Improving naltrexone response: an intervention for medical practitioners to enhance medication compliance in alcohol dependent patients. J Addict Dis. 2000; 19(1): 71–83.
17. Bouza C, Angeles M, Munoz A, et al. Efficacy and safety of naltrexone and acamprosate in the treatment of alcohol dependence: a systematic review. Addiction. 2004; 99: 811–828.
18. Mark TL, Kranzler HR, Song X. Understanding US addiction physicians’ low rate of naltrexone prescription. Drug alcohol Depend. 2003; 71: 219–228.
19. Hubbell CL, Czirr SA, Hunter GA, Beaman CM, LeCann NC, Reid LD. Consumption of ethanol solution is potentiated by morphine and attenuated by naloxone persistently across repeated daily administrations. //Alcohol. – 1986. – V.3. – P. 39–54.
20. Froechlich JC, Harts J, Lumeng L, Li TK. Naloxone attenuates voluntary ethanol intake in rats selectively bred for the high ethanol preference. //Pharmacol biochem Behav. – 1990. – V. 35. – P. 385–390.
21. Gessa GL, Muntoni F, Collu M, Vargiu L, Mereu G. Low doses of ethanol activate dopaminergic neurons in the ventral tegmental area.//Brain Res. – 1985. – V. 348. – P. 201–203.
22. Benjamin D, Grant E, Pohorecky LA. Naltrexone reverses ethanol–induced dopamine release in the nucleus accumbens in awake, freely moving rats.// Brain Res. – 1993. – V. 621. – P. 137–140.
23. Swift RM, Whelihan W, Kuznetsov O, Buongiorno G, Hsuing H. Naltrexone–induced alterations in human ethanol intoxication. //Am J Psychiatry. – 1994. – V. 151. – P. 1463–1467.
24. Jaffe AJ, Rounsaville B, Chang G., Schottenfeld RS, Meyer RE, O’Malley SS. Naltrexone, relapse prevention, and supportive therapy with alcoholics: an analysis of patient treatment matching. //J. Consult Clin Psychol. – 1996. – V. 64. – P. 1044–1053.
25. Robert M. Swift. Drug Therapy for Alcohol Dependence //NEJM. – Vol. 340. – N. 19. – P. 1482–1490.
26. Chick J. UK multicentre study of naltrexone as adjunctive therapy in the treatment of alcoholism: efficacy results.//Presented at the 10th World Psychiatry Conference, Madrid, Spain, August 24, 1996.
27. Hersh D, Van Kirk JR, Kranzler HR. Naltrexone treatment of comorbide alcohol and cocaine use disorders. //Psychopharmacology (Berl). – 1998. – V. 139. – P. 44–52.
28. Croop RS, Faulkner EB, Labriola DF. The safety profile of naltrexone in the treatment of alcoholism: results from a multicentre usage study. //Arch Gen Psychiatry. – 1997. – V. 54. – P. 1130–1135.
29. Berg BJ, Pettinati HM, Volpicelli JR. A risk–benefit assessment of naltrexone in the treatment of alcohol dependence. //Drug Saf. – 1997. – V. 15. – P. 274–282.
30. Naltrexone and alcoholism treatment. Treatment improvement protocol (TIP) series 28. Rockville. Md.: Center for Substance Abuse Treatment, 1998. (DHHS publication no. (SMA) 98–3206.) www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=hstat5.chapter.51510.
31. –£–Η–Ϋ–Ϋ–Η–Κ–Ψ–≤–Α –€.–ê. –¦–Ψ–±–Α―΅–Β–≤–Α –ê.–Γ., –ë–Α―¹–Φ–Α–Ϋ–Ψ–≤–Α –Δ.–£., –ë–Ψ–Ι–Κ–Ψ –ï.–û., –™―É―Ä–Β–≤–Η―΅ –™.–ü.–ê–Ϋ―²–Α–Κ―¹–Ψ–Ϋ –≤ ―²–Β―Ä–Α–Ω–Η–Η –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –≤–Μ–Β―΅–Β–Ϋ–Η―è –Κ –Α–Μ–Κ–Ψ–≥–Ψ–Μ―é: ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ ―¹―Ä–Α–≤–Ϋ–Η―²–Β–Μ―¨–Ϋ―΄―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι //–•. «–£–Ψ–Ω―Ä–Ψ―¹―΄ –Ϋ–Α―Ä–Κ–Ψ–Μ–Ψ–≥–Η–Η» – –€. – 2007. – ⳕ1. – –Γ.5–11.
32. Dunbar JD, Turncliff RZ, Dong Q, et al. Single and multiple dose pharmacokinetics of long–acting naltrexone. Alcohol Clin Exp.Res. 2006; 30: 480–490.
33. –‰–Ϋ―²–Β―Ä–Ϋ–Β―²–―Ä–Β―¹―É―Ä―¹: www.bio–medicine.org/medicine–news/Alcoholism–Drug–Vivitrol–Approved–By–FDA–9455–1.
34. Garbutt JC, Kranzler HR, O’Malley SS, et al. Efficacy and tolerability of long–acting injectable naltrexone for alcohol dependence: a randomized controlled trial.// JAMA. 2005. V. 293. – P. 1617–1625.
35. Gastfriend D.R., Dong Q., Loewy J. et al. Durability of Effect of Long–Acting Injectable Naltrexone The Journal of Family Practice Vol. 5, No. 3 / March 2006.
36. Gastfriend DR, Dong Q, Loewy J, et al. Durability of effect of long–acting injectable naltrexone. Presented at Annual Meeting of the American Psychiatric Association; 2005; Atlanta, GA.
37. O’Malley SS, Garbutt JC, Gastfriend DR, et al. Efficacy of Extended–Release Naltrexone in Alcohol–Dependent Who are Abstinent Before Treatment //J Clin Psychopharm. 2007. – V. 27. – No.5. – P. 507–512.
38. Lucey M.R., Silverman B.H., Illeperuma A., O’Brien C.P. Hepatic Safety of Once–Monthly Injectable Extended–Release Naltrexone Administered to Actively Drinking Alcoholics //Alc. Clin Exp. Research . – V. 32. – No. 3. – 2008. – P. 498–504.












