Материалы и методы
При выборе методики настоящего исследования учитывали следующее обстоятельство. Одним из важнейших вопросов, зачастую встающим перед практикующим психиатром в современных условиях, является возможность адекватной замены брендового препарата на его дженерик. Такое изменение назначений часто требуется при выписке больного из стационара или при его длительном наблюдении в психоневрологическом диспансере. Соответственно, было решено, что программа ТЭССА будет фактически воспроизводить рассмотренные ситуации. В частности, предполагалось вести наблюдение за двумя естественным образом сформировавшимися группами пациентов, наблюдавшихся в психиатрическом стационаре Санкт–Петербургского психоневрологического диспансера № 7 и Военно–медицинской академии. Первую из них составляют больные, страдающие шизофренией, шизотипическим или бредовым расстройствами, в возрасте старше 18 лет, получавшие лечение Спериданом (в т.ч. и в составе комбинированной терапии). Причем для включения в исследование необходимо, чтобы у указанных пациентов было достигнуто стойкое улучшение состояния, а также не наблюдались побочные эффекты, мешающие дальнейшему осуществлению терапии. Вторую группу составляют больные, получавшие Рисполепт (в т.ч. и в составе комбинированной терапии). Причем результаты такого лечения должны быть столь же благоприятны, как и у больных, принимавших Сперидан.
После включения в исследование больные обеих групп наблюдаются в течение 14 дней (подготовительная стадия) для того, чтобы убедиться в стойкости достигнутого улучшения. В дальнейшем осуществляется перекрестный перевод пациентов, получавших Сперидан, на Рисполепт, а лечившихся Рисполептом – на Сперидан. Результаты перевода отслеживаются в течение месяца (основная стадия исследования). В частности, оценивали долю пациентов, успешно переведенных с одного препарата на другой. Успешность перехода будет определяться стойким сохранением суммы баллов PANSS–EC [3] в течение 4 недель, отсутствием вновь зарегистрированных побочных эффектов по шкале UKU [6] мнением врача, участвующего в программе, верифицированного с помощью шкалы общего клинического впечатления – тяжесть (CGI–S – Clinical Global Impression Severity) и улучшение (CGI–I – Clinical Global Impression Improvement) [5]. Кроме того, учитывали долю больных, решивших продолжать терапию препаратом Сперидан или Рисполепт на момент окончания основной стадии исследования.
Важным условием проведения исследования является тот факт, что любые изменения схемы лечения являются прерогативой врача. За исключением перевода больного с одного антипсихотика на другой терапия назначается по обычным терапевтическим стандартам.
Результаты
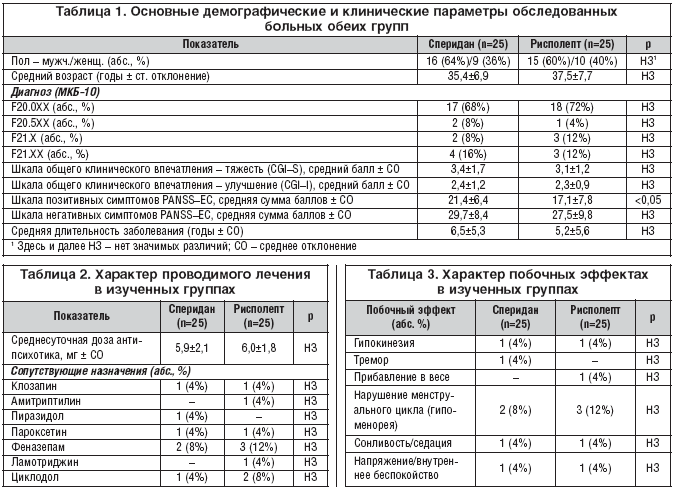
В обе группы включено по 25 пациентов. Больные, получавшие Сперидан и Рисполепт, оказались вполне сопоставимы по основным демографическим и клиническим параметрам (табл. 1).
Среди этих показателей: пол, средний возраст, диагноз, выраженность заболевания и общего улучшения по шкале общего клинического впечатления, средняя сумма баллов шкалы негативных симптомов (PANSS–EC) [3], средняя длительность заболевания. Единственное отличие между группами связано с более выраженными позитивными расстройствами, оцениваемыми по соответствующей шкале PANSS–EC [3], у больных, получавших Сперидан.
Следует также отметить, что рассматриваемые показатели вне зависимости от того, какой антипсихотик принимали пациенты, вполне соотносятся с критериями включения в исследование. Так, средний балл, отражающий выраженность заболевания и общего улучшения по шкале общего клинического впечатления соответствуют градациям «легко болен» и «большое улучшение» [5]. Аналогичным образом, средняя сумма баллов по шкалам позитивных и негативных симптомов PANSS–EC [3] свидетельствует о слабой или умеренной выраженности симптоматики.
В плане дальнейшего анализа результатов исследования важно, что при включении в исследование среднесуточные дозы Сперидана и Рисполепта были одинаковыми, а их величина свидетельствует о том, что сами антипсихотики используются для проведения купирующей терапии (табл. 2).
Важно также, что Сперидан и Рисполепт являются основой проводимого лечения, приближающегося по своему характеру к монотерапии. Во всяком случае, число больных, получавших сопутствующую терапию, не велико. Более того, препараты, использующиеся вместе со Спериданом и Рисполептом, как правило, назначаются в низких или очень низких суточных дозировках (клозапин – 125 мг, амитриптилин – 50 мг, пиразидол – 150 мг, феназепам – 1 мг, ламотриджин – 400 мг, циклодол – 2 мг).
Наконец, вполне соответствует критериям включения характер наблюдаемых побочных эффектов (табл. 3).
Все они (гипокинезия, тремор, прибавление в весе, нарушение менструального цикла – гипоменорея, сонливость/седация, напряжение/внутренние беспокойство) не только наблюдались с одинаковой частотой в обследованных группах, но и их степень выраженности (судя по шкале UKU [6]) во всех случаях расценивалась как «легкая».
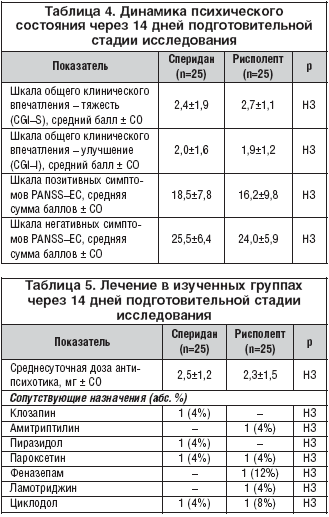
Результаты повторного осмотра больных через 14 дней свидетельствуют, с одной стороны, о незначительной положительной динамике состояния, а с другой – о практически полной нивелировке различий между группами по шкалам CGI–S, CGI–I [6], а также позитивных и негативных симптомов PANSS–EC (3) (табл. 4).
Так, при некотором (большем или меньшем) снижении всех анализируемых показателей исчезает даже отмеченное выше отличие в средней сумме баллов Шкалы позитивных симптомов PANSS–EC [3].
Что же касается проводимой терапии, то отмечается отчетливое снижение среднесуточных доз Сперидана и Рисполепта до уровня, используемого при поддерживающей терапии (табл. 5).
Сопутствующие назначения также уменьшились по объему. Соответственно, характер лечения еще более приближается к монотерапии Спериданом и Рисполептом.
Через три дня после перевода больных с одного препарата на другой, показатели, отражающие клинические особенности состояния, практически не изменились. Более того, они остаются неизменными вплоть до окончания исследования и потому не приводятся. Практически не претерпевает модификации и проводимая терапия. Так, в ходе дальнейшего исследования среднесуточные дозы Сперидана и Рисполепта и характер сопутствующих назначений остаются неизменными.
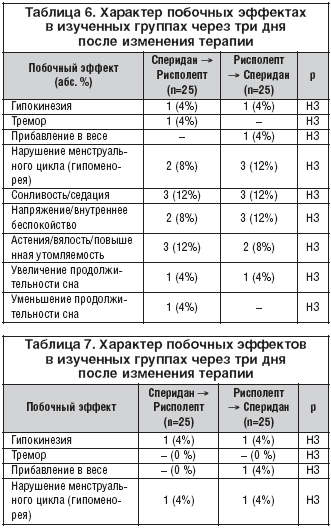
В то же время несколько расширился круг т.н. психологических побочных эффектов, причем как количественно (сонливость/седация, напряжение/внутреннее беспокойство), так и качественно (астения/вялость/повышенная утомляемость, увеличение или уменьшение продолжительности сна) (табл. 6).
Следует, однако, иметь в виду, что выраженность этих побочных эффектов во всех случаях оценивалась (согласно шкале UKU [6] как «легкая». Важно, также, что рассматриваемые явления возникают в обеих группах больных (перешедших со Сперидана на Рисполепт и с Рисполепта на Сперидан).
Указанная ситуация полностью разрешилась уже на седьмой день после изменения терапии. В этот момент набор побочных эффектов сузился, даже в сравнении с ситуацией, наблюдающейся до перехода с одного антипсихотика на другой (табл. 7).
В частности, исчезли психологические побочные эффекты, а доля больных с остальными рассматриваемыми неблагоприятными явления снизилась. В дальнейшем рассмотренный набор побочных эффектов оставался стабильным вплоть до момента окончания исследования.
Через 28 дней после перевода подавляющее большинство больных (23 в группе перешедших со Сперидана на Рисполепт и 24 переведенных с Рисполепта на Сперидан) сообщили о своем желании продолжить лечение тем антипсихотиком, который они принимали на момент окончания исследования.
Обсуждение
Результаты проведенного исследования в целом совпадают с данными ряда публикаций, подтверждающих терапевтическую эквивалентность оригинальных и воспроизведенных ЛС [1,8]. При этом тождество Сперидана и Рисполепта показано в достаточно часто встречающейся ситуации, когда требуется замена брендового препарата на его дженерик в условиях перехода на поддерживающую терапию и ее осуществления.
Косвенным образом результаты проведенного исследования свидетельствуют и о сопоставимости рассматриваемых антипсихотиков по эффективности купирующего лечения. Об этом, в частности, корреспондируют сопоставимые данные обследования больных на момент включения в исследование. Таким образом, результаты работы позволяют заключить, что Сперидан вполне может заменить таблетированную форму Рисполета при лечении больных как в стационаре, так и в амбулаторной практике, причем на любом этапе осуществления терапии.
Следует, однако, иметь в виду, что эта замена на этапе перехода к поддерживающей терапии может быть сопряжена с определенными сложностями. Последние связаны с возможностью манифестации у некоторых больных т.н. психологических побочных эффектов. Они, по всей видимости, вызваны переходом на «новый» антипсихотик на фоне очевидного улучшения их состояния. Важно, что психологические побочные эффекты возникли, несмотря на то, что программой ТЭССА предусматривались специальные разъяснения, направленные на купирование возможных опасений. В частности, больным объясняли, что Сперидан и Рисполепт представляют собой одно и то же лекарственное средство – рисперидон. Внимание пациента обращали на то, что упаковки антипсихотиков содержат один и тот же лист вкладыш и т.д. Тем не менее для некоторых больных этих разъяснений оказалось недостаточно.
Все же значение этих психологических побочных эффектов не стоит переоценивать. Данные проведенного исследования свидетельствуют о транзиторном характере рассматриваемых явлений и их «легкой» степени выраженности. Очевидно, что для предотвращения возникновения психологических побочных эффектов в ранние сроки после замены антипсихотиков, следует более подробно обсудить с больным проблему эквивалентности брендовых и дженериковых препаратов.
Наконец, результаты проведенного исследования в значительной мере выходят за рамки проблемы сопоставимости оригинальных и воспроизведенных средств. Действительно, замена одного препарата на другой достаточно часто имеет место на этапе перехода от купирующей к поддерживающей терапии широкого круга психических расстройств. В этой ситуации следует обратить самое тщательное внимание на возможность развития психологических побочных эффектов, связанных с изменением характера лечения.
Литература
1. Белоусов Ю.Б. Дженерики – мифы и реалии Remedium. www.pliva.ru/content/files/ library/170.doc 26.07.2004.
2. Вольская Е., Коковин Л. Сила и слабость генериков: российский рынок воспроизведенных препаратов. www.health–ua.com/articles/444.html 28.01.2004.
3. Мосолов С.Н. Шкалы психометрической оценки симптоматики шизофрении и концепции позитивных и негативных расстройств. ООО «РИСТАР КОМ» М., 2000. – 238 С.
4. Guberman A, Corman C. Generic substitution for brand name antiepileptic drugs: a survey. Can J Neurol Sci. 2000 Feb;27(1):37–43.
5. Guy W: Clinical Global Impression. ECDEU Assessment Manual for Psychopharmacology, revised National Institute of Mental Health, Rockville, MD 1976.
6. Lingjaerde O, Ahlfors I, Bech P, Dencker SJ, Elgen К The UKU Side Effect Rating Scale. Acta Psychiatr Scand 19S7;76[suppl 334]:85–100.
7. Stahl S.M. Essential psychopharmacology. Neuroscientific basis and practical applications. 2nd ed. Cambridge University Press. New York. 2000. – 601 P.
8. Verster GC, Joubert G, Stevens M, van der Merwe H.Generic substitution—comparing the clinical efficacy of a generic substitute for fluphenazine decanoate with the original product. S Afr Med J. 1998 Mar;88(3):260–2.












