Вопрос о необходимости антибактериальной терапии больным с обострением хронического бронхита (ХБ) требует обоснования назначения антибиотика с учетом вероятности этиологической роли инфекционного фактора, возможности спонтанных ремиссий, а также риска негативных последствий при необоснованном назначении (развитие резистентности микроорганизмов, нежелательные побочные эффекты, неоправданные затраты и др.). Кроме того, большой арсенал современных антибиотиков ставит перед врачом проблему выбора оптимального препарата.
Польза антибактериальной терапии при верифицированной инфекционной природе обострения ХБ имеет достаточно высокий уровень доказательности, базирующейся на контролированных рандомизированных исследованиях, хотя и с недостаточным количеством наблюдений (уровень доказательности В). Мета–анализ рандомизированных исследований эффективности антибиотиков при обострениях ХБ показал незначительный, но статистически достоверный эффект антибактериальной терапии [1]. У больных, получавших антибиотики, отмечены достоверно лучшие показатели пиковой скорости выдоха. Таким образом, с позиций доказательной медицины антибактериальная терапия инфекционных обострений ХБ является обоснованной и клинически оправданной.
Принятие решения о назначении антибактериального препарата больному обострением ХБ должно базироваться на этиологической роли инфекции, определении типа и тяжести обострения. Тактические вопросы антибактериальной терапии обострения ХБ сводятся к выбору оптимального антибактериального препарата, пути введения, длительности терапии, оценки ее эффективности.
Роль инфекции при обострении ХБ
Инфекция является причиной обострения ХБ в 50–60% случаев [2] и во многом определяет дальнейшее течение и прогрессирование заболевания. Инфекционное обострение ХБ может быть определено, как эпизод респираторной декомпенсации, не связанной с объективно документированными другими причинами и, прежде всего, с пневмонией.
Роль инфекции при обострениях ХБ подтверждается обнаружением большого количества бактерий и нейтрофилов в мокроте больных, повышением титров антител к этим микроорганизмам и содержания воспалительных медиаторов в гнойной мокроте. Однако связь между бактериальной инфекцией и наличием симптоматики не всегда может быть однозначной с учетом высокой частоты спонтанных ремиссий, которые наблюдаются в случаях, если процесс ограничивается только слизистой бронхов.
Спектр основных этиологически значимых инфекционных возбудителей обострения ХБ включает следующие микроорганизмы: H. influenzae, H. parainfluenzae, S. pneumoniae, M. cattarhalis, Enterobacteriacea, Pseudomonas spp, St. aureus, вирусы гриппа А и В, риновирусы.
За последнее время произошли определенные изменения в динамике этиологического спектра возбудителей обострений ХБ, в частности, значительно уменьшился удельный вес пневмококка и преобладание грамотрицательной флоры. По данным мета–анализа 9256 случаев обострения ХБ, наиболее частым возбудителем являлась H. influenzae, в то время как частота выделения S. pneumoniae и M. catarrhalis не превышала 10% и 20% соответственно [3]. Причины подобного изменения спектра микроорганизмов при обострениях ХБ пока не ясны.
H. influenzae, являющаяся наиболее типичным патогеном, выделяемым у больных с обострением ХБ, продуцирует различные субстанции, оказывающие повреждающее действие на некоторые звенья местной защиты легких. К таким эффектам относятся:
- снижение мукоцилиарного клиренса
- повышенная продукция слизи
- локальное разрушение иммуноглобулинов
- угнетение фагоцитарной активности нейтрофилов и альвеолярных макрофагов
- повреждение трахеобронхиального эпителия
- синтез гистамина и других провоспалительных медиаторов.
H. parainfluenzae является составной частью нормальной микрофлоры ротоглотки, в связи с чем потенциальное значение его, как патогена, до настоящего времени игнорировалось. Однако выделение большого количества H. parainfluenzae у больных с клинической симптоматикой обострения ХБ, лейкоцитозом и наличием в мокроте различных цитокинов позволяет говорить об этиологической роли данного микроорганизма.
Среди других микроорганизмов, выявляемых у больных, главным образом с тяжелыми обострениями ХБ указывается на St. aureus и грамотрицательные микроорганизмы (Enterobactericae, P. аeruginosa)
Роль других микроорганизмов в развитии инфекционного обострения ХБ, в частности, атипичных возбудителей (Mycoplasma pneumoniae, Chlamidia pneumoniae) не столь значительна, однако некоторые исследователи [4–8] выявили C. pneumoniae у 22% больных с обострением ХБ, причем в большинстве случаев данный возбудитель был расценен, как единственная причина инфекции.
Особое место в возникновении инфекционных обострений ХБ занимает вирусная инфекция, которая, по некоторым данным, [5–9] выявлялась в качестве причин обострения ХБ в 30% случаев, причем у большинства обнаруживались риновирусы и значительно реже – вирусы гриппа А и В. В других исследованиях вирусная инфекция явилась причиной обострения ХБ у 28% больных, преобладали вирусы гриппа группы А [6–10].
Вирусная инфекция у больных ХБ может приобретать патогенетическое значение в развитии бактериальных инфекций. Имеются данные о том, что вирусы оказывают повреждающее действие на различные звенья системы местной защиты легких, в частности, на мукоцилиарный клиренс, клеточное звено (макрофаги, лимфоциты, нейтрофилы) и гуморальное звено (иммуноглобулины, лизоцим, лактоферрин). Возникающие дефекты в системе местной защиты способствуют колонизации бактерий на слизистой, что является одним из факторов развития бронхолегочной бактериальной инфекции. Так, у больных с документированной инфекцией вирусом гриппа А спустя 7 дней в мокроте обнаруживалась H. influenzae, персистирующая в течение 30 дней. Наличие H. influenzae в мокроте было отмечено также у больных на фоне других вирусных инфекций (аденовирусы, риновирусы, вирусы простого герпеса), хотя такая тенденция была не столь выражена [7–11]. Кроме того, при инфекции вирусом герпеса наблюдается более выраженная колонизация бронхиального секрета S. pneumoniae. Таким образом, вирусная инфекция может предрасполагать к развитию бактериальной бронхолегочной инфекции у больных ХБ.
Клиника и диагностика инфекционных обострений ХБ
Основными клиническими проявлениями обострения ХБ являются следующие признаки:
- усиление кашля
- увеличение количества отделяемой мокроты
- изменение характера мокроты (увеличение гнойности мокроты)
- усиление одышки
- усиление клинических признаков бронхиальной обструкции
- декомпенсация сопутствующей патологии
- лихорадка.
Нарастание дыхательной недостаточности обусловлено главным образом усилением бронхиальной обструкции за счет воспалительного набухания слизистой бронхов, скопления густого и вязкого секрета, бронхоспазма, утраты эластической тяги легочной ткани. Если клинические признаки бронхиальной обструкции могут быть не всегда убедительными, то с помощью исследования функции внешнего дыхания, в частности, показателя ОФВ1 (объем форсированного выдоха за 1 с) можно не только верифицировать нарушение бронхиальной проходимости, но и оценить выраженность бронхиальной обструкции и величину ее динамического ухудшения по сравнению со стабильным состоянием. Выраженность бронхиальной обструкции считается одним из немногих, пожалуй, едва ли не единственным объективным признаком тяжести обострения ХБ.
Полученные в последнее время данные свидетельствуют о взаимосвязи между тяжестью обострения ХБ (по данным ОФВ1) и характером выделенной микробной флоры. Так, среди больных с обострением хронического обструктивного бронхита (ХОБ) с показателями ОФВ1 более 50% от должных основным этиологическим фактором инфекционного обострения оказались S. pneumoniae и S. aureus (46,7%). По мере ухудшения бронхиальной проходимости (ОФВ1 от 35 до 50% от должного) удельный вес S. pneumoniae и S. aureus составлял 26,7%, а при ОФВ1 ниже 35% от должного уменьшался до 23,1%. Частота выделения из мокроты H. influenzae и M. catarrhalis была приблизительно одинаковой среди больных с различной выраженностью бронхиальной обструкции (23,3%, 33,3% и 13,5% соответственно). В то же время с увеличением тяжести обострения по данным ОФВ1 возрастала этиологическая роль грамотрицательных микроорганизмов (Enterobacteriacea, P. aeruginosa) – 30,5%, 40% и 63,5% соответственно [8].
В другом исследовании [9] также было показано преобладание P. aeruginosa и H. influenzae у больных c обострением ХОБ, при ОФВ1 ниже 50% от должного. Авторы предлагают рассматривать снижение ОФВ1 менее 50% в качестве прогностического показателя и фактора высокого риска инфекции P. aeruginosa и H. influenzae. Приведенные данные могут иметь важное значение при выборе эмпирической антибактериальной терапии у больных с различной тяжестью обострения ХБ.
В некоторых ситуациях одним из клинических проявлений обострения ХБ является декомпенсация сопутствующей патологии, в том числе усугубление признаков сердечной недостаточности (у больных ИБС), гипоксии головного мозга при дисциркуляторной энцефалопатии, декомпенсация сахарного диабета и др.
Лихорадка не является типичным клиническим проявлением обострения, однако повышение температуры (обычно до субфебрильных цифр), не связанное с другими причинами и в сочетании с отдельными респираторными симптомами, может свидетельствовать об обострении ХБ.
У каждого больного обострение может проявляться разнообразным сочетанием вышеуказанных симптомов, а также другими признаками, имеющими диагностическое значение и определяющими тяжесть обострения. В связи с этим выделяют различные типы обострения ХБ в зависимости от клинической симптоматики [10] (табл. 1).

- исследование бронхиальной проходимости (ОФВ1)
- рентгенологическое исследование грудной клетки (исключить пневмонию)
- цитологическое исследование мокроты (подсчет количества нейтрофилов, эпителиальных клеток, макрофагов)
- окраска мокроты по Граму
- клинический анализ крови (лейкоцитоз, нейтрофильный сдвиг, увеличение СОЭ)
- бактериологическое исследование мокроты.
На выбор антибиотика при обострении ХБ влияют:
– клиническая ситуация
– клиническая ситуация– активность препарата против основных (наиболее вероятных в данной ситуации) возбудителей инфекционного обострения ХБ
– вероятность антибиотикорезистентности в данной ситуации
– фармакокинетика препарата (проникновение в мокроту и бронхиальный секрет, время полувыведения и т.д.), взаимодействие с другими медикаментами
– режим дозирования
– побочные эффекты
– стоимостные показатели.
Клиническая ситуация
Определение клинического варианта обострения ХБ на основании клинической симптоматики, степени бронхиальной обструкции и некоторых других признаков позволяет ориентировочно предположить этиологическую роль различных микроорганизмов в развитии обострения. Это, в свою очередь, может служить обоснованием для выбора антибактериального препарата. Принято выделять следующие основные клинические варианты обострения ХБ [11]:
1. Острый трахеобронхит
2. Простой хронический бронхит
3. Осложненный хронический бронхит
4. Хроническая бронхиальная инфекция.
Острый трахеобронхит (1 группа больных)
- Остро возникшая респираторная симптоматика (кашель, трудноотделяемая мокрота)
- Отсутствие легочного анамнеза
- Отсутствие фоновой патологии
- Отсутствие нарушений бронхиальной проходимости
- Основные этиологически значимые микроорганизмы: вирусы
Простой хронический бронхит (2 группа)
- Возраст больных менее 65 лет
- Частота обострений менее 4 в год
- Увеличение объема и гнойности мокроты при обострениях
- ОФВ1 более 50% от должного
- Основные этиологически значимые микроорганизмы: S. pneumoniae, H. influenzae, M. catarrhalis (возможна резистентность к b–лактамам).
– защищенные пенициллины (амоксициллин/клавулановая кислота 625 мг каждые 8 часов внутрь, ампициллин/сульбактам 3 г 4 раза в сутки),
– респираторные фторхинолоны (левофлоксацин 0,5 один раз в сутки, моксифлоксацин 0,4 один раз в сутки, спарфлоксацин 0,4 один раз в сутки).
Эффективными антибиотиками при данном варианте обострения ХБ могут быть также аминопенициллины (амоксициллин 0,375 х 3 раза внутрь, ампициллин 1,0 х 4 раза в сутки внутрь); макролиды (азитромицин 0,5 в сутки в первый день, затем 0,25 в сутки в течение 5 дней, кларитромицин 0,5 г 2 раза в сутки внутрь), обладающие, однако, низкой активностью по отношению к H. influenzae; тетрациклины (доксициклин 0,1 г 2 раза в сутки), которые могут использоваться в регионах с невысокой резистентностью пневмококка.
Осложненный хронический бронхит (3 группа больных)
- Возраст старше 65 лет
- Частота обострений более 4 раз в год
- Увеличение объема и гнойности мокроты при обострениях
- ОФВ1 менее 50% от должного
- Частая сопутствующая патология
- Более выраженные симптомы обострения
- Основные этиологически значимые микроорганизмы: те же, что и во 2 группе + S. aureus + грамотрицательная флора (K. pneumoniae), частая резистентность к b–лактамам.
– защищенные пенициллины (амоксициллин/клавулановая кислота 0,625 каждые 8 часов внутрь, ампициллин/сульбактам 3 г 4 раза в сутки в/в),
– защищенные пенициллины (амоксициллин/клавулановая кислота 0,625 каждые 8 часов внутрь, ампициллин/сульбактам 3 г 4 раза в сутки в/в),– цефалоспорины 1–2 поколения (цефазолин 2 г 3 раза в сутки в/в, цефуроксим 0,75 3 раза в сутки в/в, цефуроксим–аксетил 0,75 каждые 12 часов внутрь),
– респираторные фторхинолоны (моксифлоксацин 0,4 в сутки внутрь, левофлоксацин 0,5 в сутки внутрь).
При неэффективности могут использоваться цефалоспорины 3 поколения (цефотаксим 2 г 3 раза в сутки в/в, цефтриаксон 2 г один раз в сутки в/в),
Хроническая бронхиальная инфекция (4 группа больных)
- Возраст любой
- Постоянное выделение гнойной мокроты
- Частая сопутствующая патология
- Частое наличие бронхоэктазов
- ОФВ1 менее 50%
- Тяжелая симптоматика обострения, нередко с развитием острой дыхательной недостаточности
- Основные этиологически значимые микроорганизмы: те же, что и в 3 группе + Enterobacteriacea, P. aeruginosa.
– цефалоспорины 3 поколения (цефотаксим 2 г 3 раза в сутки в/в, цефтазидим 2 г 2–3 раза в сутки в/в, цефтриаксон 2 г один раз в сутки в/в),
– цефалоспорины 3 поколения (цефотаксим 2 г 3 раза в сутки в/в, цефтазидим 2 г 2–3 раза в сутки в/в, цефтриаксон 2 г один раз в сутки в/в),– респираторные фторхинолоны (левофлоксацин 0,5 один раз в сутки, моксифлоксацин 0,4 один раз в сутки).
При высокой вероятности синегнойной инфекции показаны:
– «грамотрицательные» фторхинолоны (ципрофлоксацин 0,5 2 раза внутрь или 0,4 г в/в 2 раза в сутки),
– цефалоспорины 4 поколения (цефепим 2 г 2 раза в сутки в/в),
– антисинегнойные пенициллины (пиперациллин/тазобактам 2,5 г 3 раза в сутки в/в, тикарциллин/клавуланат 3,2 г 3 раза в сутки в/в),
– меропенем 0,5 3 раза в сутки в/в.

Наряду с учетом вероятных возбудителей обострения ХБ в различных клинических ситуациях важным ориентиром при выборе антибиотика являются фармакокинетические свойства препарата. Среди них наибольшее значение могут иметь:
Наряду с учетом вероятных возбудителей обострения ХБ в различных клинических ситуациях важным ориентиром при выборе антибиотика являются фармакокинетические свойства препарата. Среди них наибольшее значение могут иметь:– проникновение в бронхиальный секрет,
– биодоступность препарата при приеме внутрь,
– период полувыведения препарата,
– отсутствие взаимодействия с другими медикаментами.
Хорошее проникновение респираторных фторхинолонов в мокроту, их высокая концентрация в бронхиальной слизистой и в альвеолярных макрофагах (особенно моксифлоксацина и левофлоксацина) являются одним из факторов высокой эффективности данной группы антимикробных препаратов при бронхолегочных инфекциях.
Большая биодоступность амоксициллина по сравнению с ампициллином делает его выбор предпочтительным. У некоторых антибиотиков, например, цефуроксима, антимикробная активность, в том числе и против b–лактамазопродуцирующей H. influenzae, может нивелироваться низкой биодоступностью препарата. Высокой биодоступностью при приеме внутрь характеризуются новые поколения макролидов (кларитромицин, рокситромицин, азитромицин), респираторные фторхинолоны (левофлоксацин, моксифлоксацин).
Антимикробные препараты с большим периодом полужизни антибиотика позволяют обеспечить удобный режим дозирования, что в свою очередь способствует лучшему комплайенсу больных. С учетом этого очевидное преимущество имеют препараты, которые могут назначаться 1–2 раза в сутки (левофлоксацин, моксифлоксацин, ципрофлоксацин, азитромицин).
Поскольку многие больные ХБ получают различную медикаментозную терапию по поводу основного или сопутствующего заболевания, необходимо учитывать возможность взаимодействия выбранного антибиотика с другим медикаментом (повышение концентрации теофиллина в крови при приеме некоторых фторхинолонов и макролидов, нарушение всасывания препаратов железа при лечении тетрациклинами и т.д.). Минимальное клинически значимое взаимодействие с другими лекарственными препаратами наблюдается у респираторных фторхинолонов.
Антибиотикорезистентность
До 1980 г. большинство микроорганизмов, выделенных у больных обострениями ХБ, были чувствительными к ампициллину, эритромицину, тетрациклину и триметоприм/сульфаметоксазолу, которые использовались в качестве препаратов первого ряда. Однако с 1990 г. стали появляться данные о нарастающей резистентности бактериальной флоры больных ХБ к этим препаратам. За период 1994–1995 г.г. было выделено 36,4% штаммов H. influenzae, продуцирующих b–лактамазу, а 2,5% лактамазо–негативных штаммов были устойчивы к ампициллину [12]. В другом исследовании было показано, что 35–40% выделенных штаммов H. influenzae продуцируют b–лактамазу, вызывающую устойчивость данного микроорганизма к пенициллинам и цефалоспоринам. Более того, некоторые штаммы, продуцирующие b–лактамазу, были резистентными и к так называемым «защищенным пенициллинам» (амоксициллин/клавулановая кислота), предназначенным именно для преодоления устойчивости, индуцированной b-лактамазами [7].
Впечатляет частота антибиотикорезистентности M. catarrhalis, значительно превышающая таковую у S. pneumoniae и H. influenzae. Имеются данные, что около 95% штаммов M. catarrhalis продуцируют b-лактамазу, а половина из них резистентны к тетрациклинам и триметоприм/сульфаметоксазолу [7].
В последние годы накоплены данные о быстрорастущей резистентности пневмококка к пенициллину. Если до 1992 г. менее 1% пнемококков в США имели высокий уровень резистентности, то в 1994–1995 гг. уже 24% пневмококков были пенициллинорезистентными, причем у 10% отмечалась высокая степень резистентности. За 1996–1997 гг. уже 33,5% пневмококков оказались резистентными к пенициллину, причем у 13% отмечалась высокая степень резистентности. Это исследование, проведенное в течение «респираторного сезона» в 45 штатах, включало 9190 штаммов пневмококка, выделенного у взрослых [13]. Примечательно, что пенициллинорезистентность сочеталась со снижением чувствительности к другим антибиотикам (макролидам, цефалоспоринам, тетрациклинам и триметоприм/сульфометоксазолу).
Основными факторами риска развития пенициллинорезистентности пневмококка являются следующие:
– возраст до 7 лет и свыше 60 лет,
– клинически значимая сопутствующая патология (сердечная недостаточность, сахарный диабет, хронический алкоголизм, заболевания печени и почек),
– частая и длительная предшествующая антибиотикотерапия,
– частые госпитализации и пребывание в местах призрения (интернаты).
При изучении резистентности к макролидам установлено, что в зимний период 1993–1994 гг. резистентность к данной группе антибиотиков составляла 20%, а в 1997 г. возросла до 39% [14]. В более поздних исследованиях было показано, что пенициллинорезистентные пневмококки оказались резистентными к цефуроксим аксетилу (100%), цефотаксиму (73%) и амоксициллин/клавуланату (94%). В то же время резистентность к пенициллину не сочеталась со снижением чувствительности к фторхинолонам [7].
Наряду с ростом пенициллинорезистентных штаммов пневмококка значительно возросла частота выделения H. influenzae, продуцирующей b-лактамазы. С учетом этой тенденции оправдано назначение защищенных пенициллинов (амоксициллин/клавуланат). Вместе с тем необходимо иметь в виду, что защищенные пенициллины остаются неактивными по отношению к пенициллинорезистентным пневмококкам, поскольку механизмы развития резистентности S. pneumoniae и H. influenzae различны. В настоящее время активными против пенициллинорезистентных пневмококков остаются респираторные фторхинолоны (левофлоксацин, моксифлоксацин). Кроме того, указанные препараты сохраняют активность и против пневмококков, резистентных к макролидам.
С учетом быстрых темпов развития антибиотикорезистентности эмпирическая антибактериальная терапия обострений ХБ должна базироваться на данных о факторах риска развития резистентности и чувствительности к антибиотикам в различных регионах.
Нежелательные эффекты антибиотиков
Современные антибактериальные препараты обладают низкой частотой побочных эффектов. В то же время такие препараты, как тетрациклины, триметоприм/сульфаметоксазол, которым присущи нежелательные эффекты, в настоящее время занимают незначительное место в лечении инфекционных обострений ХБ. Некоторые фторхинолоны нового поколения ассоциировались с опасными осложнениями (например, укорочение интервала QT на ЭКГ с высоким риском развития фатальных нарушений ритма). Именно в связи с этим некоторые из них были сняты с производства и исключены из клинической практики (грепафлоксацин). Респираторные фторхинолоны (левофлоксацин, моксифлоксацин) занимают важное место в лечении обострений ХБ с учетом не только их противомикробной активности (в частности, в отношении S. рnemoniae), оптимальной фармакокинетики, отсутствия взаимодействия с другими медикаментами (теофиллин, варфарин), но также низкой частоты побочных эффектов и отсутствия риска тяжелых осложнений. Опыт клинического применения левофлоксацина более чем у 150 млн. пациентов свидетельствует об отсутствии у препарата значимых нежелательных эффектов, в том числе со стороны печени (повышение активности печеночных ферментов), сердечно–сосудистой системы (жизненно опасные нарушения ритма), центральной нервной системы.
Стоимостные показатели
Поскольку при антибактериальной терапии важны не только стоимость препарата, но и его эффективность, то при выборе антибиотика для лечения обострения ХБ следует ориентироваться не только на стоимость, но и на адекватность его назначения в конкретной ситуации. Выбор препарата, приемлемого по своей стоимости, но не отвечающего другим требованиям, чреват отсутствием эффекта, затяжным течением обострения, возможным развитием осложнений и утяжелением состояния больного, что в конечном счете удорожает стоимость лечения. Важное значение при экономической оценке лечения имеет также дальнейшее течение заболевания и качество жизни пациента. Более продолжительные ремиссии и увеличение длительности безрецидивного периода на фоне применения более дорогого антибиотика, оказывающего не только клинический, но и бактериологический эффект, могут оказаться более экономичными, нежели назначение дешевого, но не адекватного ситуации препарата. Поэтому не следует забывать, что самым дорогим антибиотиком оказывается тот, который не обеспечивает необходимого эффекта.
В этом отношении заслуживает внимания исследование сравнительной стоимости и эффективности лечения обострений ХБ ципрофлоксацином и т.н. стандартной антибактериальной терапией (амоксициллин, эритромицин, тетрациклин, доксициклин). У больных, леченных ципрофлоксацином, отмечена более низкая частота обострений в последующий год, более быстрое стихание обострений, а также улучшение показателей качества жизни (по данным опросника госпиталя св. Георгия) при более низкой конечной стоимости лечения по сравнению с группой пациентов, леченных более дешевыми антибиотиками [15].
В большинстве случаев обострений хронического бронхита антибиотики следует назначать внутрь. Показаниями для парентерального применения антибиотиков являются:
- отсутствие оральной формы препарата
- нарушения со стороны желудочно–кишечного тракта
- тяжелое обострение заболевания
- ИВЛ
- плохой комплайенс больных.
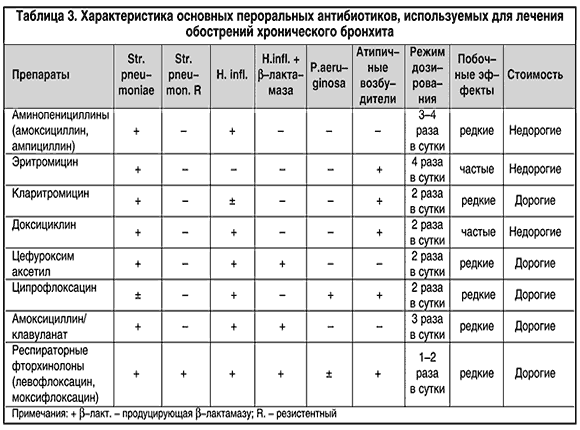
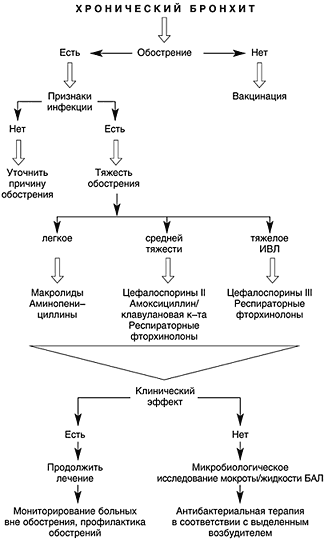
Рис. 1. Алгоритм ведения больных хроническим бронхитом
1. Saint S, Bent S, Vittinghof E, Grady D. Antibiotics in chronic obstructive pulmonary disease exacerbations. A meta–analisis. JAMA. 1995; 273; 957–960
2. Авдеев С.Н., Чучалин А.Г. Роль бактериальной инфекции и выбор антибиотиков при обострении хронического бронхита. Consilium, 2000, 2, 418–426
3. Leeper KV, Jones АМ, Tillotson G The changing bacterial etiology of chronic obstructive pulmonary disease (COPD) Chest 1997, 112, 21S
4. Mogulkoc N Karakurt S Isalska B Bayindir U Gelikel t Korten V Colpan N. Acute purulent exacerbation of chronic obstructive pulmonary disease and Chlamydia pneumoniae infection. Amer. J. Resrir. Crit.Care Med.1999; 160; 349–353
5. Seemungal T, Donaldson G C, Breuer J, Jhonston I S, Jeffries DJ, Wedzicha JA. Rinoviruses are associated with exacerbations of COPD. Eur. Resp. J. 1998; 12 (Suppl. 28); 298S.
6. Goh SK, Joban A, Cheong TH, Wang YT. A prospective study of infections with atipical pneumonia organisms in acute exacerbations of chronic bronchitis. Ann. Acad. Med. Singapore 1999; 28; 476–78
7. Anzueto A. Contemporary Diagnosis and Management of Bronchitis. 1998, 23
8. Eller J Ede A Schaberg T Niedermann MS Mauch H Lode H/ Infective exacerbations of chronic bronchitis relations bettween bacteriologic etiology and lung function Chest 1998 113 6 1542–1548
9. Miravilles M Espinosa C Fernandes – Laso E Martos J A Maldonaldo J A Galego M Relationship between bacterial flora in sputum and functional imhairtment in patients with acute exacerbations of COPD. Study Group of Bacterial Infection in COPD. Chest 1999; 116; 40–46
10. Anthonisen NR, Manfreda J, Warren CP, Hershfield ES, Harding GK, Nelson NA. Antibiotic therapy in exacerbations of chronic obstructive pulmonary disease. Ann. Intern. Med. 1987; 106; 196–204
11. Grossman RF. Guidelines for the treatment of acute exacerbations of chronic bronchitis JAMA, 1997;278; 901–904
12. Doern GV, Brueggemann A, Holley HP, Rauch AM. Antimicrobial resistance of Streptococcus pneumoniae recovered from outpatients in the United States during the winter month of 1994 to 1995: results of a 30–center national surveillance study. Antimicrob. Agents Chemother. 1996; 40; 1208–1213
13. Doern G V Trends in antimicrobial susceptibility of bacterial patogens of the respiratory tract. Am. J. Med. 1995;99; 3S – 7S
14. Thornsberry C, Ogilvie P,Kahn J. Surveillance of antimicrobial resistance in Streptococcus pneumoniae, Haemophilus influenzae and Moraxella catarrhalis in United States in 1996–1997 respiratory season. The Laboratory Investigator Group. Diagn. Microbiol. Infect. Dis. 1997; 29; 249–257
15. Grossman R, Mukherjee J, Vaughan D et al. A 1–year community–based health economic study of ciprofloxacin vs usual antibiotic treatment in acute exacerbations of chronic bronchitis: the Canadian Ciprofloxacin Health Economic Study Group. Chest 1998; 113; 131–141











