В настоящее время, по официальной статистике, число больных ХОБЛ в России составляет около 1 млн. человек, но по результатам подсчета с использованием эпидемиологических маркеров гипотетически больных должно быть около 11 млн. Предполагается, что имеющиеся статистические данные не отражают истинной распространенности этой патологии, которая в действительности значительно выше. Это объясняется тем, что значительное число случаев ХОБЛ не диагностируется на ранних этапах, поскольку больные, как правило, обращаются за помощью в поздней стадии заболевания, приобретающего уже тяжелое или среднетяжелое течение. Больные с легким течением ХОБЛ, у которых имеет место привычный кашель курильщика при отсутствии одышки или ее незначительной выраженности и относительно удовлетворительном самочувствии, не попадают в поле зрения врачей, ошибочно считая себя здоровыми.
Помимо повсеместно наблюдаемого роста распространенности ХОБЛ, в настоящее время еще более высокие цифры представляет показатель смертности от этого заболевания. Сейчас ХОБЛ занимает четвертое место в структуре причин смертности в мире, однако в ближайшие десятилетия прогнозируется дальнейший рост как распространенности, так и смертности от ХОБЛ.
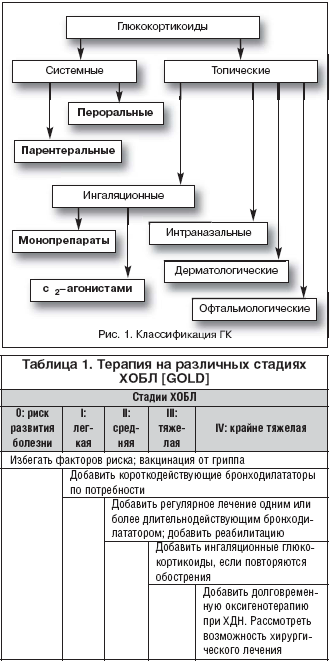
Ведение больных ХОБЛ регламентировано международными и национальными рекомендациями и в общем виде может быть представлено в таблице 1.
Воспалительная природа заболевания оправдывает применение у данной категории пациентов лекарственных средств с противовоспалительным механизмом действия, среди которых основное место занимают глюкокортикоиды (ГК).
Существуют различные принципы классификации ГК (длительность фармакологического эффекта, аффинность к глюкокортикоидным рецепторам, выраженность глюкокортикоидного и минералокортикоидного действия, лекарственная форма). Наиболее оправданным с позиций клинической практики и определения показаний к применению может быть классификация ГК на основе системного или топического действия (рис. 1).
Системные ГК оказывают свое действие при введении препаратов парентерально или внутрь.
Для парентерального применения используются как водорастворимые, так и не растворимые в воде ГК. Первые (фосфаты, сукцинаты и гемисукцинаты) обеспечивают быстрое достижение эффекта и относительную его кратковременность. Нерастворимые в воде ГК (аценаты и ацетониды) характеризуются медленно развивающимся и длительным эффектом. При внутривенном введении ГК терапевтический эффект является более быстрым и кратковременным в сравнении с внутримышечными инъекциями, при которых начало действия регистрируется в пределах 2 ч. Таблетированные ГК характеризуются высокой биодоступностью (60% для гидрокортизона и 90% для метилпреднизолона), обеспечиваемой устойчивостью к метаболизму в печени.
Ингаляционные глюкокортикоиды (ИГК). К ИГК относятся беклометазон, будесонид (Пульмикорт), флутиказон, мометазон, триамцинолон. В отличие от системных ГК ИГК обладают следующими свойствами:
• высокая аффинность к ГК–рецепторам
• действие в минимальных дозах
• выраженный местный противовоспалительный эффект
• низкая системная (пероральная, легочная) биодоступность
• быстрая инактивация
• короткий период полувыведения из крови.
ИГК угнетают все фазы воспаления в бронхах и снижают их повышенную реактивность, что позволяет считать их базисными препаратами для лечении бронхиальной астмы персистирующего течения, а также ХОБЛ средней тяжести и тяжелого течения. При применении ИГК у больных ХОБЛ важное значение приобретает их способность понижать бронхиальную секрецию (уменьшать объем трахеобронхиального секрета) и потенцировать действие ?2–агонистов. Кроме того, назначение ИГК позволяет уменьшить потребность в таблетированных ГК. Важной характеристикой ИГК является терапевтический индекс, т.е. соотношение местной противовоспалительной активности и системного действия. Наиболее благоприятный терапевтический индекс среди ИГК имеет Пульмикорт.
ИГК доступны в виде дозированных аэрозольных ингаляторов (ДАИ) и дозированных порошковых ингаляторов (ДПИ), а также растворов для небулизации. При использовании ДАИ целесообразно применение спейсера. ДАИ в сочетании со спейсером, ДПИ и небулайзер обеспечивают сопоставимое качество доставки ИГК у пациентов со стабильной ХОБЛ. При тяжелых обострениях ХОБЛ, когда больной не в состоянии использовать ДАИ, оправдана небулайзерная терапия ИГК. При правильном выборе системы и техники ингаляции системные побочные эффекты ИГК незначительны из–за низкой биодоступности и быстрой метаболической активации этих препаратов в печени. Следует иметь в виду, что все существующие ИГК в той или иной степени всасываются в легких. Местные побочные эффекты ИГК, особенно при длительном применении, заключаются в развитии ротоглоточного кандидоза (у 5–25% больных), реже — кандидоза пищевода, дисфонии (у 30–58% больных), кашля.
ИКГ в комбинации с ?2–агонистами длительного действия представлены в виде двух препаратов: флютиказон + сальметерол и будесонид + формотерол (Симбикорт). Комбинированные ингаляционные препараты, содержащие ГК и ?2–агонисты длительного действия, имеют определенные преимущества, поскольку ГК потенцируют действие бронхолитиков и препятствуют десенситизации b–рецепторов при изолированном применении ?2–агонистов. Эффект этих комбинаций обусловлен не простым суммированием лекарственных компонентов, а их комплементарностью, что позволяет рассматривать входящие в состав препараты как синергисты. Какое же место занимают ГК в лечении больных ХОБЛ?
Системные глюкокортикоиды
Высокая противовоспалительная активность ГК позволяет считать их препаратами первой линии при лечении больных с обострением ХОБЛ, поскольку выраженный воспалительный отек бронхиальных слизистых наряду с гиперсекрецией слизи при обострении заболевания затрудняют как доставку, так и абсорбцию препаратов при их ингаляционном введении. Имеются достоверные доказательства (уровень доказательности А), что короткие курсы системными ГК при обострении ХОБЛ способствуют более быстрому и более выраженному увеличению бронхиальной проходимости (по данным ОФВ1), сокращению продолжительности госпитализации и увеличению временного интервала до следующего обострения [1]. Продолжительность применения ГК у больных обострением ХОБЛ не должна превышать 2–3 нед, поскольку не удалось выявить преимуществ при назначении ГК в течение 8 недель по сравнению с 2–недельным лечением (уровень доказательности А). Более длительное применение ГК внутрь для терапии ХОБЛ являлось предметом двух ретроспективных исследований. Полученные в ходе этих исследований данные не позволяют рекомендовать больным ХОБЛ такое лечение из–за высокой частоты побочных эффектов (уровень доказательности А).
Эксперты GOLD рекомендуют при обострениях ХОБЛ применять внутрь преднизолон в суточной дозе 40 мг в течение 10 дней [3]. Это лечение показано всем больным с тяжелым обострением ХОБЛ при величине ОФВ1<50% от должной (уровень доказательности А). При наличии у пациента выраженной дыхательной недостаточности, а также в ситуациях с недостаточным комплайнсом (пожилые, дезориентированные пациенты и т.д.) предпочтительно внутривенное или внутримышечное введения одного из длительнодействующих ГК. При тяжелых обострениях ХОБЛ может быть оправдано назначение системных ГК парентерально. В частности, метилпреднизолона в дозе 1–2 мг каждые 6–12 часов с последующим переходом через 2–3 дня на пероральный прием ГК в суточной дозе 60 мг в течение двух недель.
Согласно некоторым рекомендациям предлагается проведение коротких курсов пробной терапии ГК внутрь в течение 10–14 дней. При этом считается, что увеличение показателей ОФВ1 после проведения такого пробного курса лечения или появление обратимости при пробах с бронхолитиками являются предикторами эффективности ИГК у таких больных. Однако в настоящее время целесообразность проведения пробных курсов таблетированных ГК для оценки потенциального ответа на терапию ИГК продолжает оставаться предметом дискуссии. Имеются данные как подтверждающие диагностическую ценность данного подхода, так и опровергающие ее.
Проведенные в последние годы исследования показали, что терапевтический ответ на короткий курс ГК имеет недостаточную прогностическую ценность в плане дальнейшего применения ИГКС. Отчетливое улучшение показателей бронхиальной проходимости после 2–недельного курса терапии преднизолоном в дозе около 30 мг/сут. позволяет с высокой долей вероятности предсказать положительный эффект при назначении ИГК, хотя отнюдь не гарантирует такового.
Несмотря на влияние ГК на весь воспалительный каскад в бронхиальной слизистой, их эффективность у больных ХОБЛ менее выражена, чем при бронхиальной астме. Тем не менее при обострениях ХОБЛ показаны курсы системных ГК. Однако терапия системными ГК должна быть максимально быстро отменена у пожилых больных, которые, как известно особенно чувствительны к развитию побочных эффектов, в том числе кожных повреждений, катаракты, диабета, остеопороза, склонности к инфекциям.
Ингаляционные глюкокортикоиды
Применение ИГК у больных ХОБЛ также долгое время оставалось предметом дискуссии, так как многочисленные клинические исследования эффективности длительной терапии ИГК демонстрировали неоднозначные результаты – от значительного улучшения показателей спирометрии до полного отсутствия лечебного действия ИГК.
Опираясь на данные рандомизированных клинических исследований, эксперты GOLD рекомендуют назначение ИГК только при умеренном и тяжелом течении ХОБЛ у тех больных, которые отвечают на лечение увеличением ОФВ1 или уменьшением симптомов. Другим показанием к длительной терапии ИГК являются частые обострения ХОБЛ (уровень доказательности В).
Данные многоцентровых рандомизированных двойных слепых плацебо–контролируемых исследований в 13 странах свидетельствуют об эффективности применения ИГК (флутиказона пропионат в дозе 500 мг/сут. до 6 месяцев) у больных ХОБЛ в возрасте 50–75 лет. При этом отмечено достоверное повышение толерантности к физической нагрузке, улучшение показателей бронхиальной проходимости (пиковая скорость выдоха, ОФВ1), снижение частоты обострений. Большая эффективность ИГК у больных ХОБЛ может ожидаться в случаях значительного бронхолитического эффекта b2–агонистов, наличия эозинофилов в мокроте, признаках атопии.
В более позднем и длительном плацебо–контролируемом исследовании ISOLDE показаны преимущества флутиказона пропионата 1000 мкг в течение 3 лет (улучшение показателей ОФВ1, уменьшение числа обострений ХОБЛ, сохранение качества жизни пациентов). Флутиказон пропионат оказывал минимальное влияние на темпы снижения показателей ОФВ1 на протяжении всего периода наблюдения. Кроме того, применение флутиказона пропионата у больных ХОБЛ уменьшало темпы ухудшения качества жизни, что было обусловлено, по–видимому, снижением частоты обострений заболевания.
Улучшение качества жизни у больных ХОБЛ наряду с уменьшением частоты обострений заболевания было продемонстрировано при применении в качестве ИГК триамсинолона, который, однако, не оказывал существенного влияния на динамику бронхиальной проходимости.
В другом исследовании – EUROSCOP сравнивалась эффективность будесонида (400 мг дважды в сутки) и плацебо у 1277 больных ХОБЛ, наблюдавшихся на протяжении 3 лет. В течение первых 6 месяцев отмечалось улучшение показателей ОФВ1 при лечении будесонидом по сравнению с плацебо, в то время как в последующие сроки наблюдения различия в темпах улучшения бронхиальной проходимости у больных, получавших будесонид и плацебо, исчезали.
Комбинированные ИГК + b2–агонисты длительного действия
Комбинированные препараты, содержащие в своем составе ИГК и b2–агонисты длительного действия, были первоначально разработаны для терапии больных бронхиальной астмой. При проведении рандомизированных клинических исследований этих лекарственных препаратов удалось выявить дополнительные преимущества, связанные в первую очередь с тем, что ГКС препятствуют десенситизации b–адренорецепторов. В последующем стали проводиться исследования, в которых была продемонстрирована эффективность использования комбинации ИГК и b2–агонистов длительного действия у больных ХОБЛ стабильного течения.
Крупное двойное слепое плацебо–контролируемое рандомизированное клиническое исследование
(TRISTAN) эффективности комбинации флутиказона (500 мкг) и сальметерола (50 мкг) у больных ХОБЛ дважды в день показало преимущество комбинированного препарата по сравнению с его компонентами (флутиказон 500 мкг и сальметерол 50 мкг). У больных, получавших комбинацию флутиказона и сальметерола, отмечалось достоверное увеличение показателей ОФВ1, уменьшение выраженности симптомов, снижение потребности в короткодействующих бронхолитиках, снижение частоты обострений ХОБЛ, а главное – значительное улучшение качества жизни по данным опросника госпиталя Святого Георга.
В одном из исследований показано, что комбинированная терапия ХОБЛ c использованием будесонида и формотерола оказывала более благоприятный эффект, чем использование каждого из этих компонентов в виде монотерапии. Примечательно, что в проведенном исследовании было продемонстрировано уменьшение темпов снижения показателей ОФВ1, в то время как на частоту обострений ХОБЛ и качество жизни больных препарат не оказывал существенного влияния.
По данным результатов одного мета–анализа, удалось продемонстрировать незначительное замедление скорости падения ОФВ1 на величину около 10 мл/год среди получавших ИГК при средних значениях этого показателя у больных ХОБЛ 60–100 мл/год [14]. Наряду с высокой эффективностью ингаляционные препараты с фиксированными комбинациями глюкокортикоидов и b2–агонистов длительного действия являются более удобными для использования, что имеет важное значение для обеспечения комплайнса у пациентов.
Ретроспективный анализ имеющейся большой базы данных позволяет говорить о возможном снижении летальности больных ХОБЛ на фоне лечения ИГК.
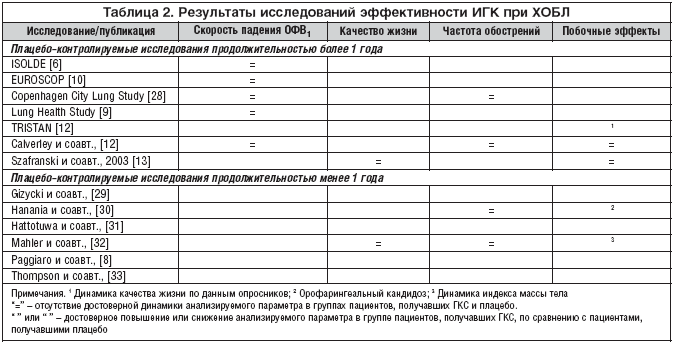
Косвенным подтверждением эффективности ИГК у больных ХОБЛ является ухудшение бронхиальной проходимости и качества жизни пациентов наряду с увеличением частоты обострений заболевания.
В таблице 2 представлены результаты исследования эффективности ИГК, в том числе и в комбинации с b2–агонистами длительного действия, у больных ХОБЛ в стабильной фазе заболевания (приводится фрагмент таблицы из статьи А.И. Синопальникова и А.В. Воробьева).
Место ИГК в рекомендациях
по лечению ХОБЛ
Согласно мнению экспертов Российского респираторного общества, ингаляционные ИГК являются препаратами второй линии базисной терапии, и целесообразность их назначения рассматривается у пациентов с ОФВ1<50%, получающих базисную ингаляционную бронходилатационную терапию, в случае, если обострения, требующие назначения системных ГК или антибиотиков, отмечаются 1 раз в год или чаще. Если необходимо назначить ИГК и b2–агонист длительного действия, то предпочтительна фиксированная комбинация флутиказона с сальметеролом или будесонида с формотеролом (Симбикорт). Эта рекомендация постулируется Американским торакальным обществом и Европейским респираторным обществом. По мнению авторов рекомендаций Британского торакального общества, ИГК следует применять в случаях, когда обострения ХОБЛ, требующие назначения системных ГКС или антибиотиков, происходят с частотой 2 раза в год и чаще независимо от реакции пациента на пробную терапию пероральных ГК. В последней редакции GOLD лечение ИГК рекомендуется всем пациентам с ОФВ1<50% при повторяющихся обострениях заболевания.
Побочные эффекты при лечении ГК
Побочные эффекты (ПЭ), развивающиеся на фоне применения ГК, можно условно разделить на системные и местные.
Системные ПЭ. Выраженность системных ПЭ определяется дозой, продолжительностью приема, путем введения и фармакокинетическими свойствами соответствующего ГК. В наибольшей степени системные ПЭ выражены при длительном приеме пероральных или парентеральных ГК. Относительно безопасным является использование системных ГК короткими курсами. По данным наиболее показательного исследования SCCOPE по оценке эффективности и переносимости курсового применения пероральных ГКС при обострении ХОБЛ, 2–недельная терапия была сопряжена лишь с незначительным риском развития гипергликемии; увеличение же продолжительности приема ГК до 8 недель сопровождалось развитием более тяжелых инфекционных осложнений ХОБЛ при сопоставимой частоте их развития. Наиболее частым и прогностически неблагоприятным ПЭ при использовании системных ГК у больных ХОБЛ является остеопороз, что обусловливает необходимость назначения антиостеопоротических препаратов при продолжительном приеме ГК, особенно у пожилых пациентов. Следует иметь в виду нередкое развитие при тяжелых обострениях ХОБЛ эрозий желудка вследствие усугубления гипоксии, гиперкапнии, микроциркуляторных нарушений, что в случаях назначения системных ГК повышает риск возникновения таких жизненно угрожающих состояний, как кровотечения и перфорации. Поэтому при принятии решения о назначении системных ГК необходима тщательная всесторонняя оценка состояния больного с учетом клинической ситуации (тяжесть обострения, наличие и характер сопутствующей патологии, степень риска развития осложнений).
Вероятность развития системного действия ИГК является минимальной, но зависит от выбора препарата, эффективности его доставки и возрастает по мере увеличения продолжительности терапии. Так, прием флунизолида, у которого системная биодоступность составляет около 20%, сопряжен с большей вероятностью развития системных ПЭ, чем прием флутиказона пропионата, обладающего весьма низкой системной биодоступностью (менее 1%). В то же время при доставке ИГК с помощью дозированного аэрозольного ингалятора (ДАИ) риск развития системных ПЭ выше, чем при использовании ДАИ со спейсером.
По данным различных исследований, длительная высокодозовая терапия ингаляционными ГКС способствует возрастанию риска развития подкожных гематом и снижению плотности костной ткани.
Поскольку одним из побочных эффектов ГК является развитие остеопороза (ОП), естественно, что основное внимание исследователей уделялось влиянию ИГК на минеральную плотность кости (МПК) и частоту костных переломов у больных ХОБЛ.
В рандомизированном проспективном 3–летнем исследовании у 359 больных ХОБЛ, леченных ИГК (триамсинолон в дозе 1200 мкг), отмечено снижение МПК шейки бедра на 2%. В контрольной группе, получавшей плацебо, снижение МПК составляло 0,22%.
В то же время в другом рандомизированном проспективном плацебо–контролируемом исследовании не выявлено достоверных изменений показателей МПК через 3 года ни в группе больных, получавших ИГК (будесонид 800 мкг в сутки), ни в группе плацебо.
По данным ретроспективного когортного анализа, риск вертебральных переломов оказался выше у больных ХОБЛ, леченных оральными ГК и составлял 2,6 по сравнению с контрольной группой. Примечательно, что эта же группа исследователей выявила повышенный риск переломов позвонков (2,5) у больных ХОБЛ, леченных высокими дозами ИГК (выше 700 мкг/сутки беклометазона) по сравнению с контрольной группой. Повышенный риск невертебральных переломов был отмечен среди больных ХОБЛ, получавших ИГК в дозах 700 мкг, эквивалентных беклометазону, по сравнению с пациентами, не леченными ИГК. Таким образом, назначение больным ХОБЛ системных ГК вносит существенный вклад в снижение МПК у данной категории пациентов и является дополнительным фактором риска развития ОП и переломов. Имеется корреляция риска ОП с длительностью лечения, суточной и кумулятивной дозой ГК. ИГК в высоких дозах могут вызывать снижение МПК, хотя риск развития остеопении и ОП ниже, чем при лечении системными ГК. Однако влияние ИГ на показатели МПК у больных ХОБЛ требует дальнейшего изучения.
Местные ПЭ при лечении ИГК встречаются достаточно часто: охриплость голоса отмечают до 50% пациентов, клинически выраженный орофарингеальный кандидоз регистрируется у около 5% больных. Данные явления, как правило, минимально выражены, не ведут к прекращению лечения и проходят самостоятельно либо после отмены препарата. На выраженность местных ПЭ влияет правильная техника ингаляции, использование спейсера или ингалятора более совершенной конструкции. Полоскание рта и ротоглотки непосредственно после ингаляции позволяет уменьшить вероятность развития орофарингеального кандидоза, а также системных эффектов ИГК.
Таким образом, в настоящее время доказанными можно считать следующие положения:
• ИГК способствуют снижению частоты обострений ХОБЛ, в наибольшей степени этот эффект выражен у пациентов с тяжелой ХОБЛ (ОФВ1<50%);
• ИГК способствуют меньшей частоте обращения больных за медицинской помощью. При оправданности назначения системных ГК и ИГК больным ХОБЛ как при обострениях, так и при стабилизации течения заболевания эффективность ГК у данной категории пациентов остается недостаточной. Основные направления на пути оптимизации лечения больных ХОБЛ с использованием ИГК могут быть сведены к разработке новых ИГК и совершенствованию средств доставки ИГК.
Литература
1. Aaron SD, Vandemheen KL, Hebert P et al. Outpatient oral prednisone after emergency treatment of chronic obstructive pulmonary disease. N Engl J Med 2003; 348: 2618–25.20
2. А.Н.Цой, В.В.Архипов. Доказательная фармакотерапия хронической обструктивной болезни легких. Consilium medicum 2002,4,9)
3. Niewoehner DE, Erbland ML, Deupree RH et al. Effect of systemic glucocorticoids on exacerbations of chronic obstructive pulmonary disease. Department of Veterans Affairs Cooperative Study Group. N Engl J Med 1999; 340: 1941–7
4. Global Strategy for the Diagnosis, Management and Prevention of Chronic Obstructive Pulmonary Disease. GOLD Executive Summary. Am.J.Respir.Crit. Care Med. 2007,176,532–555.
5.Davies L, Nisar M, Pearson MG, et al. Oral corticosteroid trials in the management of stable chronic obstructive pulmonary disease. QJM 1999; 92: 395
6. Burge PS, Calverley PM, Jones PW et al. Randomized, double blind, placebo controlled study of fluticasone propionate in patients with moderate to severe chronic obstructive pulmonary disease: the ISOLDE trial. Br Med J 2000
7. Celli BR, MacNee W; ATS/ERS Task Force. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004;23(6):932–46
8. Paggiaro L. P. – Multicentre randomised placebo–controlled trial of inhaled fluticason propionate in patients with COPD. Lancet, 1998, 351,773–780
9. Lung Health Study Research Group. Effect of inhaled triamcinolone on the decline in pulmonary function in chronic obstructive pulmonary disease. N Engl J Med 2000, 343,1902–1909)
10. Pauwels RA, Lofdahl CG, Laitinen LA et al. Long–term treatment with inhaled budesonide in persons with mild chronic obstructive pulmonary disease who continue smoking. European Respiratory Society Study on Chronic Obstructive Pulmonary Disease. N Engl J Med 1999; 340: 1948–53.
11. Pauwels R, Vestbo J, Jones P et al. Combined salmeterol and fluticasone in the treatment of chronic obstructive pulmonary disease: a randomised controlled trial. Lancet 2003; 361: 449–56
12. Calverley P, Pauwels R, Vestbo J et al. Combined salmeterol and fluticasone in the treatment of chronic obstructive pulmonary disease: a randomised controlled trial. Lancet 2003; 361: 449–56
13.Szafranski W, Cukier A, Ramirez A et al. Efficacy and safety of budesonide/formoterol in the management of chronic obstructive pulmonary disease. Eur Respir J 2003; 21: 74–81)
14. Sutherland ER, Allmers H, Ayas NT et al. Inhaled corticosteroids reduce the progression of airflow limitation in chronic obstructive pulmonary disease: a meta–analysis. Thorax 2003; 58: 937.
15. Sin DD, Tu JV. Inhaled corticosteroids and the risk of mortality and readmission in elderly patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2001;164(4):580–4.
16. Soriano JB, Vestbo J, Pride NB, et al. Survival in COPD patients after regular use of fluticasone propionate and salmeterol in general practice. Eur Respir J 2002;20(4):819–25
17. O’Brien A, Russo–Magno P, Karki A et al. Effects of withdrawal of inhaled steroids in men with severe irreversible airflow obstruction. Am J Respir Crit Care Med 2001; 164: 365–71
18. Van der Valk P, Monninkhof E, van der Palen J et al. Effect of discontinuation of inhaled corticosteroids in patients with chronic obstructive pulmonary disease: the COPE study. Am J Respir Crit Care Med 2002; 166: 1358–63
19. Синопальников А.И., Воробьев А.В. Фармакотерапия хронической обструктивной болезни легких: глюкокортикостероиды. Consilium medicum. 2006,8,3)
20. Niewoehner DE, Erbland ML, Deupree RH et al. Effect of systemic glucocorticoids on exacerbations of chronic obstructive pulmonary disease. Department of Veterans Affairs Cooperative Study Group. N Engl J Med 1999; 340: 1941–1947
21. Pauwels RA, Lofdahl CG, Laitinen LA et al. Long–term treatment with inhaled budesonide in persons with mild chronic obstructive pulmonary disease who continue smoking. European Respiratory Society Study on Chronic Obstructive Pulmonary Disease. N Engl J Med 1999; 340: 1948–53.
22. Wise R., Connet J., Weinmann G. et al. Effect of inhaled triamcinolone on the decline in pulmonary function in chronic obstructive pulmonary disease. N Engl.J.Med 2000, 343,1902–1909
23. Van Staa T.P., Leufkens H.G.M., Abenhaim L. et al. Use of oral corticosteroids and risk of fractures. J.Bone Miner.Res. 2000, 15,993–1000
24. Van Staa T.P., Leufkens H.G.M., Cooper C. Use of inhaled cjrticosteroids and risk of fracture. J.Bone Miner.Res. 2001, 16, 581–588
25. Lee T.A. Weiss K.B. Fracture risk associated with inhaled corticosteroid use in chronic obstructive pulmonary disease. Am. J.Respir.Crit.Care Med., 2004, 169, 855–859
26. Goldstein M.F., Fallon J.J., Harning R. Chronic glucocorticoid therapy–induced osteoporosis in patients with obstructive lung disease. Chest. 1999,116,1733–1749
27. Selroos O, Backman R, Forsen AB et al. Local side effects during 4–year treatment with inhaled corticosteroids; A comparison between pressurized metered–dose inhalers and Turbuhaler. Allergy 1994; 49: 888
28. Vestbo J, Sorensen T, Lange P et al. Long–term effect of inhaled budesomde in mild and moderate chronic obstructive pulmonary disease: a randomised controlled trial. Lancet 1999; 353: 1819–23.
29. Gizycki MJ, Hattotuwa KL, Barnes N et al. Effects of fluticasone propionate on inflammatory cells in COPD: an ultrastructural examination of endobronchial biopsy tissue. Thorax 2002; 57: 799–803
30. Hanania NA, Darken P, Horstman D et al. The efficacy and safety of fluticasone propionate (250 mcg)/salmeterol (50 mcg) combined in the Diskus inhaler for the treatment of COPD. Chest 2003; 124: 834–43.
31. Hattotuwa KL, Gizycki MJ, Ansari TW et al. The effects of inhaled fluticasone on airway inflammation in chronic obstructive pulmonary disease: a double–blind, placebo–controlled biopsy study. Am J Respir Crit Care Med 2002; 165: 1592–6.
32. Mahler DA, Wire P, Horstman D et al. Effectiveness of fluticasone propionate and salmeterol combination delivered via the Diskus device in the treatment of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2002; 166: 1084–91.
33. Thompson WH, Carvalho P, Souza JP et al. Controlled trial of inhaled fluticasone propionate in moderate to severe COPD. Lung 2002; 180: 191–201.












