Первичная легочная гипертензия (ПЛГ) является заболеванием неизвестной природы, при котором среднее давление в легочной артерии в покое превышает 25 мм рт.ст., а во время физической нагрузки более 30 мм рт. ст., при этом давление заклинивания в легочной артерии остается в норме [8]. Терапия ПЛГ довольна сложна, основное значение придается вазодилататорам (антагонистам кальция, простагландину Е1, простациклину) [2]. В течение последнего десятилетия при ПЛГ широко изучаются свойства недавно открытого вазодилататора - оксида азота (II) (NO). Мы представляем свой первый опыт использования ингаляционного NO при данном заболевании.
Больная С., 43 лет, поступила в октябре 2000 г. в НИИ пульмонологии МЗ РФ с жалобами на одышку при умеренной физической нагрузке (ходьба до 200 м), сердцебиение, повышенную утомляемость, слабость.
Из анамнеза известно, что впервые небольшая одышка при физической нагрузке появилась в 1974 г., а с 1996 г. изредка стали возникать эпизоды синкопе. За медицинской помощью больная не обращалась, не обследовалась. С 1998 г. стали беспокоить приступы учащенного сердцебиения, сопровождающиеся давящей болью за грудиной, усилилось диспное, резко снизилась толерантность к физической нагрузке.
При осмотре: состояние тяжелое, цианоз губ, пастозность стоп. Границы легких перкуторно не изменены, при аускультации дыхание везикулярное, хрипы не выслушиваются, ЧДД 16 в минуту. Границы сердечной тупости несколько расширены влево (на 1,5 см), при аускультации выслушивается систолический шум вдоль левого края грудины, акцент II тона над точкой легочной артерии, ЧСС 86 в минуту, тоны ритмичные, АД 130/80 мм рт.ст. Живот мягкий, безболезненный при пальпации, печень не пальпируется.
Рентгенография органов грудной клетки: легочные поля прозрачные, легочный рисунок обеднен по периферии легочных полей, корни легких расширены, в прямой проекции по левому контуру выбухает II дуга, увеличение тени сердца за счет правого желудочка.
ЭКГ: синусовый ритм, резкое отклонение электрической оси сердца вправо, признаки перегрузки правого предсердия и гипертрофии правого желудочка.
ФВД: нормальная бронхиальная проходимость, небольшое снижение воздушного потока по мелким бронхам (MСВ25-75 = 66% от должного).
Газовый состав артериальной крови: pH - 7,46; PaCO2 - 30,5 мм рт. ст.; PaO2 - 72,7 мм рт. ст.; SatO2 - 92,9%; HCO3 - 23,6 ммоль/л. При ходьбе до 50 м снижение SatO2 до 86%.
Исследование вентиляционно-перфузионного дисбаланса: P(A-a)O2 – 36 мм рт. ст., истинный шунт QS/QT (на фоне дыхания 100% О2) – 7%.
Эхокардиография: аорта не расширена, камеры левого предсердия и левого желудочка не увеличены, гипертрофии стенок левого желудочка не выявлено, правый желудочек увеличен: из парастернальной позиции - 3,0 см, из апикальной 4-камерной позиции - 3,2 см, правое предсердие: из апикальной 4-камерной позиции - 5,1 х 4,5 см. Показатели насосной и сократительной функции миокарда не изменены.
Допплерэхокардиография: систолическая регургитация в полость правого предсердия III cтепени; систолическое давление в легочной артерии повышено (расчет по скорости трикуспидальной регургитации) – 75 мм рт.ст.
Учитывая практически нормальные показатели ФВД при наличии клинических и инструментальных признаков высокой легочной гипертензии и при умеренных нарушениях газообмена, решено было применить более инвазивные методы диагностики для исключения пороков сердца и тромбоэмболической формы легочной гипертензии.
Ангиопульмонография: значительное расширение основного ствола легочной артерии и ее крупных ветвей, резкое сужение периферических ветвей легочных артерий с обеих сторон по типу синдрома “обгоревшего дерева”; данных за эмболию и пороки сердца не получено.
Катетеризация правых отделов сердца (Swan Ganz катетер): давление в легочной артерии 89/35 мм рт. ст. (в норме до 30/12 мм рт.ст.); среднее давление в легочной артерии 56 мм рт. ст. (в норме до 16 мм рт.ст.), давление в правом предсердии 4 мм рт.ст. (в норме 4-5 мм рт.ст.); давление заклинивания в легочной артерии 9 мм рт.ст. (в норме до 12 мм рт.ст.); сердечный индекс 4,2 л/мин (в норме 4-7 л/мин); легочное сосудистое сопротивление 895 дин/с/см5 (в норме 50-120 дин/с/см5), индекс ударной работы правого желудочка 24,9 г.м/м2 (в норме до 10 г.м/м2).
Гистологическое исследование ткани легких (торакоскопическая видеосопровождаемая биопсия): гипертрофия медии, пролиферация и фиброз интимы вплоть до полного сужения сосудов – признаки плексогенной легочной артериопатии (рис. 1).

Рис. 1. Гистологическая картина ткани легких
Учитывая данные проведенных исследований, был поставлен диагноз: Первичная легочная гипертензия, плексиформная артериопатия, НК II.Для оценки ответа на терапию вазодилататорами был проведен тест с ингаляционным NO. Последовательно назначались дозы NO 5, 10, 20 и 40 ppm. Эффект терапии оценивался по динамике показателей систолического давления в легочной артерии и сердечного выброса, измеряемых при помощи эхокардиографического метода, показателей системного артериального давления и газового состава артериальной крови. Максимальный эффект от терапии NO был получен при использовании концентраций 10 и 20 ppm: снижение легочного систолического давления более 30%, повышение PaO2, при умеренном снижении сердечного выброса и неизменных значениях системного артериального давления (рис. 2).

Рис. 2. Применение NO при первичной легочной гипертензии
В дальнейшем больной в ходе стационарного лечения (14 дней) проводилась терапия оксидом азота через носовые канюли в дозе 20 ppm. Эффективность оказалась довольно высокой: значительно уменьшилась одышка, выросла толерантность к физическим нагрузкам, снизилось давление в легочной артерии (в конце курса терапии систолическое легочное АД 61 мм рт.ст.), повысилась оксигенация артериальной крови (перед выпиской 78 мм рт.ст.).Обсуждение
ПЛГ является редким заболеванием (заболеваемость 1 случай на 2 млн в год), которым чаще страдают женщины молодого возраста, хотя оно может наблюдаться у мужчин, детей и у пожилых. Причиной повышенного давления в легочной артерии становятся изменения мелких сосудов легких, что приводит к повышению сопротивления кровотоку в этих сосудах [8]. Повышенное легочное сопротивление, в свою очередь, ведет к повышению нагрузки на правый желудочек, с его последующей гипертрофией, дилатацией, и в конечном итоге, развитию сердечной недостаточности.
При первичной легочной гипертензии описано несколько гистологических типов сосудистых изменений: гипертрофия медии, фиброз интимы, плексиформные, тромботические и вено-окклюзионные изменения. Данная патология не специфична для ПЛГ, так как может наблюдаться и при многих формах вторичной легочной гипертензии [4]. Часто перечисленным изменениям сопутствуют гипертрофия и гиперплазия гладких мышц легочных артерий, что также вносит существенный вклад в повышение легочного сосудистого сопротивления.
ПЛГ является очень сложным заболеванием как с точки зрения диагностики, так и лечения, что отражает недостаточно изученные механизмы заболевания. Кроме того, данное заболевание ассоциировано с крайне плохим прогнозом: средняя выживаемость больных через 5 лет от момента диагностики ПЛГ составляет около 21% [4].
К основным клиническим симптомам заболевания относятся прогрессирующая одышка при физическом напряжении, загрудинные ангинозноподобные боли, также чаще всего связанные с физической нагрузкой, изредка – кровохарканье. Появление синкопальных состояний считается неблагоприятным прогностическим признаком, свидетельствующем о снижении церебрального кровотока.
Следует подчеркнуть, что для постановки диагноза ПЛГ необходимо исключить вторичные причины легочной гипертензии, такие как тромбоэмболическая болезнь, врожденные пороки сердца, паренхиматозные заболевания легких, синдромы нарушения дыхания во время сна, системные заболевания соединительной ткани, легочные васкулиты, применение различных препаратов и субстанций (анорексигенные препараты, L-триптофан, токсическое рапсовое масло, кокаин), ВИЧ-инфекция, портальная гипертензия [10].
Выбор лекарственных препаратов, доступных для терапии ПЛГ, в настоящее время довольно ограничен. Системные вазодилататоры, такие как антагонисты кальция (АК), могут приводить к снижению артериального давления в легочной артерии и улучшению функции правого желудочка. У больных, “отвечающих” на прием антагонистов кальция снижением легочного давления, прогноз значительно лучше, чем у больных, не реагирующих на данный класс препаратов [4]. При ПЛГ используются очень высокие дозы АК: 40-180 мг нифедипина или 120-360 мг дилтиазема [1]. К сожалению, лишь 20-30% больных имеют положительный ответ на вазодилататоры. Серьезным препятствием для подбора эффективной дозы АК при ПЛГ является развитие значительных побочных эффектов: системной гипотензии и тахикардии. Для неотвечающих больных необходим подбор других препаратов.
Одним из наиболее мощных и эффективных препаратов для терапии больных ПЛГ является простациклин (PGI2), который назначается в виде длительной (годами!) внутривенной инфузии. Кроме снижения давления в системе легочной артерии, препарат обладает также антипролиферативным и антиагрегантным эффектами, что препятствует развитию ремоделирования сосудистой стенки. Длительная терапия простациклином приводит к улучшению клинических симптомов, увеличению толерантности к физическим нагрузкам, повышению качества жизни и выживаемости больных [2]. Однако простациклин обладает большим количеством побочных эффектов (диарея, головокружение, сыпь, боли в конечностях, гипотензия). Внутривенный путь введения препарата также существенно затрудняет его широкое использование: наличие центрального катетера часто ведет к развитию таких осложнений, как инфекции и тромбозы. Еще одним недостатком препарата является его высокая стоимость: годовой курс терапии простациклином стоит около 25 тыс долларов США.
В связи с перечисленными недостатками простациклина все большее значение придается альтернативным методам терапии легочной гипертензии, к числу которых относится и оксид азота.
Активное широкое изучение NO началось после 1987 г., когда две независимые группы ученых под руководством Palmer и Ignarro показали, что мощный эндогенный вазодилататор эндотелий-зависимый релаксирующий фактор является оксидом азота. Эндогенный NO образуется из L-аргинина при помощи кальций-зависимого энзима NO-синтазы III. Мишенью NO являются гладкомышечные клетки резистивных сосудов (артерий и артериол). Диффундируя через альвеолярную мембрану, NO попадает в эти клетки, где он повышает уровень циклического гуанозин-монофосфата, что приводит к запуску цепи реакций, результатом которых является снижение тонуса гладких мышц сосуда (рис. 3) [5]. Затем NO поступает к системный кровоток, где и происходит его инактивация вследствие связывания с оксигемоглобином и образования конечных продуктов - метгемоглобина и нитратов. Концентрация NO, достаточная для релаксации гладкой мускулатуры сосудов, составляет 10-10 М.
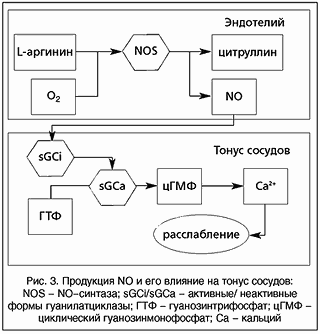
Рис. 3. Продукция NO и его влияние на тонус сосудов:
NOS - NO-синтаза; sGCi/sGCa - активные/ неактивные формы гуанилатциклазы; ГТФ - гуанозинтрифосфат; цГМФ - циклический гуанозинмонофосфат; Ca - кальций
Изначально при ПЛГ NO отводилась роль агента, позволяющего оценить реактивность сосудов легких, т.е. выявить больных, положительно отвечающих на вазодилататоры, что, как уже подчеркивалось, имеет важное прогностическое значение. Снижение тонуса сосудов легких может наблюдаться через несколько секунд от начала ингаляции NO. В нескольких исследованиях было показано, что острые тесты с ингаляционным NO позволяют выявить больных, которые реагируют на пероральные антагонисты кальция с точностью до 90% [9]. В то же время тест с NO более безопасен по сравнению с нифедипином или дилтиаземом (частота развития побочных эффектов при остром тесте с АК достигает 38%: системная гипотензия, шок и даже летальные исходы!). Кроме того, острый тест с NO занимает гораздо меньше времени (10-40 мин) по сравнению с пробой с АК ( до 6-8 часов). При проведении теста с NO обычно используют возрастающие концентрации 5, 10, 20, 40 ppm, время ингаляции во время каждого этапа не превышает 10 минут [8]. В нашем случае максимальный эффект наблюдался при концентрации NO 20 ppm, по данным ранее проведенных исследований чаще всего используются дозы от 10 до 40 ppm.
Другим перспективным направлением использования ингаляционного NO при ПЛГ является длительное назначение данного газа с лечебной целью. Число таких исследований пока очень мало. В нашем случае ингаляционная терапия NO в течение 14 дней привела к выраженному положительному клиническому эффекту, что позволяет в перспективе рекомендовать данный вид терапии больным с ПЛГ в условиях стационара. Техника назначения NO довольна проста, возможно назначение газа через носовые канюли, либо через лицевую маску, однако для точного титрования дозы необходимо использование мониторинга вдыхаемой смеси при помощи анализаторов NO/NO2. Необходимо также обратить внимание на такие технические детали, как использование регуляторов давления из нержавеющей стали и калибровка флоуметра для NO, а также на меры безопасности при терапии NO: контроль метгемоглобина крови пациента в первые дни лечения и контроль в контуре системы и в окружающем воздухе концентрации NO2 (токсичного метаболита реакции взаимодействия NO и O2), которая не должна превышать 2 ppm.
Имеются сообщения о длительном амбулаторном назначении NO больным ПЛГ: описано двое пациентов, получавших данный вид терапии в течение 9 месяцев и 1,5 лет. В обоих случаях ингаляция NO оказалась безопасным и высокоэффективным методом терапии больных ПЛГ [3, 6]. В настоящее время в нескольких центрах США и Европы планируется проведение долгосрочных исследований эффективности длительной терапии NO.
1. Чазова И.Е. Современные подходы к лечению легочного сердца. //Рус Мед Журн, 2000; 8(2): 83-6.
2. Barst RJ, Rubin LJ, McGoon MD, et al. Survival in primary pulmonary hypertension with long-term continuous intravenous prostacyclin. //Ann Intern Med 1994; 121:409-15
3. Channick RN, Newhart JW, Johnson FW, et al. Pulsed delivery of inhaled nitric oxide to patients with primary pulmonary hypertension. An ambulatory delivery system and initial clinical tests. //Chest, 1996; 109: 1545-9.
4. Groechenig E. Cor pulmonale. Treatment of pulmonary hypertension. Blackwell Science, Berlin- Vienna, 1999; 146.
5. Ignarro LJ. Biological actions and properties of endothelium-derived nitric oxide formed and released from artery and vein. //Circ Res, 1989; 65: 1-21
6. Koh E, Niimura J, Nakamura T, et al. Long-term inhalation of nitric oxide for a patient with primary pulmonary hypertension. //Jpn.Circ.J., 1998; 62: 940-2.
7. Rubin LJ. ACCP Consensus Statement: primiry pulmonary hypertension. //Chest, 1993; 104: 236-50.
8. Sitbon O, Brenot F, Denjean A, et al. Inhaled nitric oxide as a screening vasodilator agent in primary pulmonary hypertension. //Am J Respir Crit Care Med, 1995; 151: 384-9
9. Sitbon O, Humbert M, Jagot J, et al. Inhaled nitric oxide as a screening agent for safely identifying responders to oral calcium-channel blockers in primary pulmonary hypertension. //Eur Respir J, 1998; 12: 265-70.
10. Voelkel NF, Tuder RM. Severe pulmonary hypertensive diseases: a perspective. //Eur Respir J, 1999; 14: 1246-50.












