Хроническая обструктивная болезнь легких (ХОБЛ) в настоящее время является одним из наиболее распространенных заболеваний бронхолегочной системы, которое, особенно в отсутствие адекватного лечения, обусловливает тяжелую инвалидизацию и преждевременную смерть [1,2].
ХОБЛ – заболевание, характеризующееся прогрессирующей бронхиальной обструкцией, обратимой лишь частично. Патофизиологической основой нарушений бронхиальной проходимости является воспалительный «ответ» легких на ингаляционную экспозицию повреждающих частиц или газов [3].
У предрасположенных лиц вследствие длительной ингаляционной экспозиции ирритантов (компоненты табачного дыма, диоксиды серы, азота, озон и др.) происходит развитие последовательных и тесно взаимосвязанных между собой патологических процессов в стенке бронхов (гиперплазия слизеообразующих элементов, нарушения реологии бронхиального секрета) и в легочной ткани (эластолитическая деструкция), приводящих к формированию хронического бронхита и эмфиземы легких – основных составляющих ХОБЛ. При этом целесообразно выделять необратимую и обратимую бронхиальную обструкцию, прогнозируя тем самым возможности и ограничения доступной медикаментозной терапии этого заболевания.
Необратимый («эмфизематозный») компонент бронхиальной обструкции обусловлен развитием и прогрессированием эмфиземы легких и т.н. болезни мелких бронхов (снижение эластической тяги легочной ткани вследствие неравномерной преимущественно центриацинарной эмфиземы, ранний экспираторный коллапс, деформация и сужение мелких бронхов). Очевидно, что данные структурные изменения не могут быть точкой приложения бронхолитических и/или противовоспалительных лекарственных средств.
Обратимый («бронхитический») компонент бронхиальной обструкции представлен воспалительным отеком слизистой дыхательных путей, аккумуляцией клеток воспаления, слизи и плазмы в просвете бронхов, спазмом гладкой мускулатуры. При этом отек слизистой оболочки дыхательных путей, гиперплазия подслизистых желез и бокаловидных клеток, гиперпродукция слизи, объединенные термином «воспалительное ремоделирование стенки бронха», контролируются парасимпатическим отделом вегетативной нервной системы, тонус которой при этом заболевании закономерно повышен [4]. А поскольку холинергическая иннервация является доминирующим нейрогенным механизмом бронхоконстрикции, то, очевидно, антихолинергические препараты следует рассматривать, как приоритетное направление бронхолитической терапии ХОБЛ [5].
Парасимпатическая нервная система играет важнейшую роль в развитии бронхоконстрикции у человека [6]. Холинергические преганглионарные волокна берут свое начало от nucleus ambiguus и дорзальных моторных ядер в стволе головного мозга и в составе блуждающего нерва доходят до периферических парасимпатических ганглиев, локализующихся в стенке бронхов, а далее короткие постганглионарные волокна достигают гладкомышечных клеток бронхов и подслизистых желез. Стимуляция n.vagus, в частности, воспалительными медиаторами (брадикинин) приводит к высвобождению ацетилхолина, который активирует мускариновые рецепторы гладкомышечных клеток, подслизистых желез и бокаловидных клеток воздухоносных путей, вызывая бронхоконстрикцию и гиперсекрецию слизи. Холинергическая иннервация наиболее распространена на уровне крупных бронхов и в меньшей степени – на уровне периферических бронхов.
В настоящее время с помощью ауторадиографии установлены несколько подтипов человеческих мускариновых рецепторов, их локализация и основные физиологические функции (рис. 1) [6].
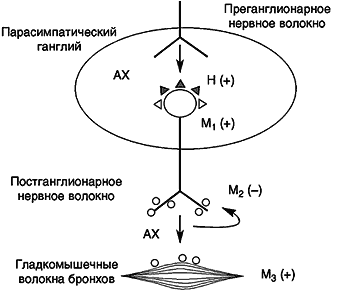
Рис. 1. Мускариновые рецепторы в дыхательных путях [5]
М1–рецепторы локализуются в парасимпатических ганглиях и контролируют процесс нейротрансмиссии через них. На окончаниях постганглионарных нервных волокон располагаются М2–рецепторы, которые действуют как ауторецепторы и ингибируют высвобождение ацетилхолина, а также могут противодействовать бронхолитическому эффекту b2–агонистов. Фармакологическая блокада М2–рецепторов приводит к высвобождению ацетилхолина и тем самым к развитию бронхоконстрикции. Стимуляция М3–рецепторов вызывает сокращение гладкомышечных клеток, гиперсекрецию подслизистых желез и бокаловидных клеток, отек слизистой бронхов. М4 и М5–рецепторы в бронхолегочной системе человека не обнаружены.Наибольшее представительство мускариновых рецепторов – преимущественно М3–рецепторов (64%) и М1–рецепторов (36%) – отмечено в крупных и средних бронхах [7].
Физиологический парасимпатический тонус обеспечивает определенный базальный бронхомоторный тонус, который может быть устранен назначением атропина или, напротив, усилен назначением ингибиторов ацетилхолинэстеразы. У больных ХОБЛ отмечается известная вариабельность бронхиальной проходимости с минимальными ее изменениями в ночные и предутренние часы [4].
Краеугольным камнем в лечении больных ХОБЛ является назначение ингаляционных бронхолитических препаратов. Предпочтительность ингаляционного пути введения лекарственных средств объясняется возможностью непосредственной доставки препаратов к органу–мишени, более быстрым достижением лечебного эффекта, минимальными числом и выраженностью нежелательных системных явлений. В терапии ХОБЛ могут применяться b2–агонисты, антихолинергические препараты или их комбинации. Выбор между отдельными направлениями бронхолитической терапии в каждом конкретном случае, очевидно, должен основываться на индивидуальном «ответе» при проведении бронхолитического теста. В то же время М–холинолитики признаны препаратами выбора в связи с тем, что парасимпатикотония является ведущим обратимым механизмом бронхиальной обструкции при этом заболевании.
Бронхолитическая терапия может назначаться «по требованию» или на регулярной основе. Но поскольку основными целями лечения больных ХОБЛ являются снижение темпов прогрессирования диффузного воспаления, ведущего к нарастанию бронхиальной обструкции, развитию и усугублению дыхательной недостаточности, уменьшение частоты и продолжительности обострений, улучшение качества жизни, то, очевидно, приоритет имеет длительное и регулярное лечение.
Антихолинергические препараты (или М–холинолитики), являющиеся конкурентными антагонистами ацетилхолина, блокируют мускариновые рецепторы и тем самым устраняют эффекты парасимпатикотонии на постсинаптические рецепторы гладкой мускулатуры и слизеобразующие элементы бронхов. Применяемые в настоящее время ингаляционные антихолинергические препараты относятся к четвертичным аммониевым производным, и наиболее широко распространен из них ипратропиум бромид (ИБ). Препарат хорошо переносится, эффективен и безопасен при длительном применении, не вызывает развития тахифилаксии, кардиотоксического действия. Чувствительность М–холинорецепторов с возрастом не уменьшается, что особенно важно в лечении больных ХОБЛ, так как это заболевание характерно для лиц старших возрастных групп. Существующие рекомендации предлагают применять ИБ «...так долго, как долго симптомы заболевания будут продолжать причинять неудобства пациенту» [8].
Представителем новой генерации антихолинергических препаратов является тиотропиум бромид (ТБ), также относящийся к четвертичным аммониевым производным [9]. ТБ взаимодействует со всеми типами мускариновых рецепторов. Однако при исследовании in vitro (на изолированных легких морской свинки и дыхательных путях человека) было показано, что ТБ диссоциирует с М1– и М3–рецепторами в 100 раз медленнее, чем ИБ, и, напротив, очень быстро – с М2–рецепторами (табл. 1). Это обстоятельство определяет уникальную кинетическую селективность лекарственного средства в отношении М3– и М1–рецепторов и минимальное взаимодействие с М2–рецепторами. Медленная же диссоциация ТБ с М3–рецепторами гладкомышечных клеток и слизеобразующих элементов дыхательных путей объясняет значительную продолжительность действия препарата, дающую возможность его однократного применения в сутки. Продолжительность бронхолитического действия является дозозависимой и, например, при ингаляции 40 мкг лекарственного средства достигает 48 часов [9–12]. Было установлено также, что холиноблокирующее действие ТБ примерно в 10 раз превосходит таковое ИБ [9].

К настоящему времени проведены многочисленные контролируемые клинические исследования по оценке эффективности и безопасности ТБ у больных ХОБЛ в сравнении с плацебо и ИБ. При этом стандартизованные критерии включения больных были следующими: ХОБЛ средней степени тяжести с возможностью ведения пациентов в амбулаторных условиях; возраст старше 40 лет; соответствующие показатели бронхиальной проходимости – объем форсированного выдоха за 1 сек (ОФВ1) и форсированная жизненная емкость легких (ФЖЕЛ): 30% < ОФВ1 < 65% и ОФВ1/ФЖЕЛ < 65% от должных значений; табакокурение более 10 «пачек/лет». Критериями исключения являлись: наличие у больного бронхиальной астмы или других бронхообструктивных заболеваний; атопическая сенсибилизация; потребность в регулярной кислородотерапии; перенесенный инфаркт миокарда (в течение последних 6 мес).
Так, в ходе одного из сравнительных плацебо–контролируемых исследований оценивалась эффективность и безопасность различных доз ТБ (4,5; 9,0; 18,0 и 36,0 мкг 1 раз в сутки), ингалируемого больными ХОБЛ с помощью дозированного порошкового ингалятора «HandiHaler». [13,14]. В течение всех 28 дней приема ТБ регистрировалось статистически достоверное увеличение показателей бронхиальной проходимости (ОФВ1, ФЖЕЛ спустя 6, 20 и 24 часа после ингаляции, а также пиковой скорости выдоха – ПСВ – в утренние и вечерние часы) по отношению к таковым показателям в группе больных, получавших плацебо. При этом ингаляция ТБ в диапазоне доз от 9,0 до 36,0 мкг/сутки сопровождалась более значимым и стабильным повышением ОФВ1 и ФЖЕЛ по сравнению с низкой дозой препарата (4,5 мкг/сутки). Одновременно был продемонстрирован прекрасный профиль безопасности ТБ и установлено, что интервал дозирования 9–18 мкг/сутки характеризуется наименьшей частой нежелательных явлений. Поэтому доза 18,0 мкг/сутки ТБ для однократного приема была признана оптимальной, как сочетающая максимальную эффективность с максимальной безопасностью [14]. Примечательным явилось то обстоятельство, что в течение 3 недель после прекращения приема ТБ показатели бронхиальной проходимости возвращались к исходным значениям, что еще раз подтверждало необходимость продолжительной терапии ингаляционными антихолинергическими препаратами данной категории больных.
Особый интерес представляют результаты недавно завершенных контролируемых исследований по оценке эффективности и безопасности ТБ в ходе его длительного приема (12 мес) больными ХОБЛ в сравнении с плацебо (American Study Group) и ИБ (Belgian/Dutch Study Group). Основными критериями эффективности были выбраны: оценка бронхолитического действия (динамика ОФВ1, ситуационная потребность в b2–агонистах короткого действия); динамика выраженности одышки в баллах; оценка качества жизни больных ХОБЛ с применением стандартизованного опросника SGRQ [15]; частота и выраженность обострений заболевания; комплаентность.
При годичном наблюдении за больными ХОБЛ, получавшими ТБ в дозе 18 мкг/сутки однократно (n=271) или плацебо (n=180), была отмечена хорошая переносимость препарата и отсутствие феномена тахифилаксии. Уже в самом начале лечения (на 8–й день приема препарата) регистрировалось снижение суточной потребности в b2–агонистах короткого действия (как по сравнению с исходными данными, так и по сравнению с плацебо), сохраняющееся далее на протяжении 12–месячного проспективного наблюдения [16]. При этом возрастали показатели ОФВ1 (на 100–120 мл), ФЖЕЛ (на 300 мл), и подобная тенденция удерживалась в течение всего года. Примечательно, что значения ОФВ1 и ФЖЕЛ, определявшиеся в утренние часы (до ингаляции ТБ), оставались стабильными, демонстрируя лишь минимальную динамику после ингаляции очередной дозы, что подтверждало пролонгированный характер бронхолитического эффекта препарата (рис. 2а, 2б) [16].

Рис. 2. Тиотропиум бромид vs. плацебо (American Study Group):
А - бронхолитический эффект [16]; Б - среднесуточная потребность в b2-агонистах [16];
В - динамика выраженности одышки [17]; Г - интегральная оценка качества жизни больных [16].
Указанные выше эффекты ТБ (оптимизация бронхиальной проходимости, снижение потребности в короткодействующих бронхолитиках, уменьшение выраженности одышки) корреспондировали с улучшением качества жизни, оцениваемого по стандартизованному опроснику SGRO – это касалось и оцениваемой больными динамики клинических проявлений, и повышения физической активности, и минимизации социальных «последствий» болезни [18]. Особенно показательной при этом была динамика интегральной оценки качества жизни, отличавшаяся в группах больных, принимавших ТБ и плацебо: достоверные различия отмечались уже на 50–й день лечения, достигая максимума к исходу 12–месячного наблюдения (рис. 2г).
Благоприятные эффекты ТБ проявились и в уменьшении частоты обострений ХОБЛ (на 18% по сравнению с плацебо; р=0,033), в том числе и требовавших госпитализации (на 48% по сравнению с плацебо; р=0,04) [19].
Особый интерес представляют результаты исследований по сравнительной оценке клинической эффективности ТБ и ИБ, препарата, до настоящего времени остающегося препаратом выбора для симптоматического контроля и медикаментозной профилактики прогрессирования ХОБЛ.
Для сопоставления эффективности и безопасности ТБ и ИБ было проведено 12–месячное многоцентровое рандомизированное двойное слепое исследование в параллельных группах (Belgian/Dutch Study Group).
В исследование было включено 535 больных, 356 из которых получали ТБ в дозе 18 мкг/сутки однократно в форме дозированного порошкового ингалятора «HandiHaler» и 171 – ИБ в дозе 40 мкг 4 раза в сутки в форме дозированного аэрозольного ингалятора.
При определении динамики показателей бронхиальной проходимости у больных в сравниваемых группах было установлено, что применение ТБ позволяет достичь более значительного их повышения [21]. Показатели ОФВ1 и ФЖЕЛ у этой группы больных увеличивались уже через полчаса после первой ингаляции, сохранялись в течение 24 часов и не снижались до исходного уровня на протяжении всего периода исследования. Скорость наступления и выраженность бронхолитического эффекта ТБ превосходили таковые ИБ.
Более выраженное влияние ТБ (по сравнению с ИБ) на состояние бронхиальной проходимости подтверждалось и соответствующей динамикой утренних и вечерних значений ПСВ, а также снижением потребности в b2–агонистах короткого действия. Наибольший бронхолитический эффект, оцениваемый в ходе мониторинга ПСВ, наблюдался к исходу 2–й недели приема обоих холиноблокаторов, но в случае ТБ этот эффект удерживался на протяжении всего периода наблюдения, а в группе больных, получавших ИБ, со временем отмечалась тенденция к снижению этого показателя [20, 21].
Особо следует отметить тот факт, что выраженность одышки, оцениваемой в баллах, более отчетливо регрессировала на фоне приема ТБ в сравнении с ИБ [22]. Здесь уместно привести слова известного пульмонолога P.Jones [23], высоко оценившего возможности ТБ, как средства симптоматического контроля ХОБЛ: «Чрезвычайно привлекательным и несколько неожиданным оказался саногенетический эффект тиотропиума бромида: больные, длительно принимавшие препарат, более не испытывали одышки при физической нагрузке и передвигались в темпе, привычном для лиц их возраста».
Длительный прием ТБ приводит не только к уменьшению количества, но и тяжести обострений, на что указывает и достоверно меньшее суммарное количество дней обострений в течение года, и меньшее число госпитализаций по сравнению с группой больных, получавших ИБ [24].
Улучшение показателей бронхиальной проходимости, уменьшение выраженности одышки, снижение частоты обострений и госпитализаций, и, наконец, однократное введение ТБ объясняют отчетливый благоприятный эффект препарата на соответствующие показатели, определяющие качество жизни (опросник SGRO) – симптомы заболевания, физическая активность, социальные «последствия». Особенно выражено влияние ТБ (по сравнению с ИБ) на интегральный показатель качества жизни [25].
При длительном лечении антихолинергическими препаратами не было выявлено каких–либо серьезных побочных эффектов, как и отсутствовали сколь–нибудь значительные различия в частоте нежелательных явлений при приеме ТБ и ИБ. Ни один больной не прекратил лечение в связи с развившейся сухостью во рту – единственным проявлением лекарственного воздействия на организм. В обеих группах на протяжении всего периода лечения не было отмечено значимых изменений при объективном обследовании, лабораторных исследованиях, электрокардиографии [21].
Однократный прием ТБ в сутки в сочетании с хорошим эффектом и привлекательным профилем безопасности способствуют повышению комплаентности больных ХОБЛ, что было показано при проведении масштабных исследований с включением 921 больного (мужчины –599, женщины–322; средний возраст больных – 65,2 года). Высокую комплаентность (> 90%) продемонстрировали более 85% больных, причем она оказалась выше у мужчин, лиц моложе 65 лет и больных с низкими значениями ОФВ1 (< 1 л) [26]. Для сравнения – в ранее проведенном исследовании Lung Health Study (1995) [27] удовлетворительную и хорошую комплаентность демонстрировали лишь 60% больных ХОБЛ.
Заключая симпозиум, проходивший в рамках Всемирного конгресса пульмонологов (Флоренция, 2000 г.) и посвященный окончанию длительных сравнительных исследований по применению ТБ у больных ХОБЛ, профессор P.Jones сказал: «Нет сомнений в том, что тиотропиум бромид – шаг вперед в лечении ХОБЛ... И сегодня уже необходимо представлять ХОБЛ, как потенциально курабельное заболевание» [23].
Ведущим направлением плановой длительной терапии ХОБЛ является назначение ингаляционных антихолинергических препаратов или М–холинолитиков (ипратропиум бромид – ИБ). К числу наиболее перспективных представителей нового поколения антихолинергических препаратов относится тиотропиум бромид (ТБ). Медленная диссоциация ТБ с М3– или постсинаптическими холинорецепторами гладкомышечных клеток и слизеобразующих элементов дыхательных путей объясняет возможность эффективного использования препарата 1 раз в сутки по сравнению с необходимостью 3–4–кратного применения ИБ. При этом холиноблокирующее действие ТБ примерно в 10 раз превосходит таковое ИБ. ТБ назначается в дозе 18 мкг/сутки однократно в форме дозированного порошкового ингалятора.
В ходе многочисленных контролируемых клинических исследований по оценке эффективности и безопасности ТБ при его 12–месячном приеме подтверждено достоверное превосходство препарата в сравнении с плацебо и ИБ во влиянии на показатели бронхиальной проходимости, «ситуационную» потребность в короткодействующих бронхолитиках, выраженность одышки, частоту и тяжесть обострений заболевания, показатели качества жизни. Принципиально важным является свойство ТБ замедлять темпы прогрессирующего падения показателей бронхиальной проходимости.
Однократный прием ТБ в сутки в сочетании с хорошим эффектом и привлекательным профилем безопасности объясняют высокую комплаентность (более 90%), продемонстрированную абсолютным большинством больных ХОБЛ при длительном назначении препарата.
Список литературы Вы можете найти на сайте http://www.rmj.ru
1. Хронические обструктивные болезни легких. Федеральная программа, М., 1999г.
2. BTS Guidelines for the management of chronic obstructive pulmonary disease. Thorax 1997;52 (suppl.5)
3. Global initiative on chronic Obstructive Lung Disease http://www/goldcopd.com
4. Barnes P. Tiotropium bromide: a new long–acting anticholinergic bronchodilator. In:Barnes P., Buist A.S., editors. The role of anticholinergics in chronic obstructive pulmonary disease and chronic asthma. Macclesfied Cheshire, UK: Gardiner–Caldwell Communications Limited; 1997. p.126–136.
5. Barnes P. Muscarinic receptor subtypes in airways. Life Sci 1993; 52: 521–527.
6. Gross N.J., Skorodin M.S. Anticholinergic antimuscarinic bronchodilators. Am Rev Respir Dis 1984;129: 856–870.
7. Mak J.C., Barnes P. Autoradiographic visualisation of muscarinic receptor subtypes in human and guinea pig lung. Am Rev Respir Dis 1990; 141: 1559–1568.
8. Standarts for the diagnosis and care of patient with chronic obstructive pulmonary disease (COPD). Am J Respir Crit Care Med 1995; 152: S77–121.
9. Barnes P. The pharmacological properties of tiotropium. Chest 2000;117: S63–69.
10. Disse B., Reichl R., Speck G., Traunecker W., Ludvig Rominger K.L., Hammer R. Ba 679 BR, a novel long acting anticholinergic bronchodilator Life Sci 1993; 52(5–6): 537–544.
11. Maesen F.P., Smeets J.J., Costongs M.A., Wald F.D., Cornelissen P.J. Ba 679BR, a new long–acting antimuscarinic bronchodilator: a pilot dose–escalation study in COPD. Eur Respir J 1993; 6:1031–1036.
12. Maesen F.P., Smeets J.J., Siedsens T.J., Cornelissen P.J. Tiotropium bromide, a new long–acting antimuscarinic bronchodilator: a pharmacodinamic study in patients with chronic obstructive pulmonary disease (COPD). Dutch Study Group. Eur Respir J 1995; 8: 1506–1513.
13. Littner M.R., Auerbach D., Campbell S., Dunn L., Friedman M., Illowite J.S. et al. The bronchodilator effects of tiotropium in stable COPD. Am J Respir Crit Care Med 1997; 155: A282.
14. Littner M.R., Illowite J.S., Tashkin D.P., Friedman M., Serby C.W., Menjoge S.S., Witek TJ. Long–acting bronchodilation with once–daily dosing of tiotropium (Spiriva) in stable chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2000; 161:1136–1142.
15. Jones P.W., Quirk F.N., Bareystock C.M., Littejohns P. A self–complete measure for chronic airflow limitation – the St Georges Respiratory Questionary. Am Rev Respir Dis 1992; 145:1321–1327.
16. San Pedro G., Ellias D.J., Serby C.W., Witek T.J. Tiotropium (Spiriva): 1–year bronchodilator efficiacy established with once–daily dosing in COPD patients. Am J Respir Crit Care Med 2000; 161(3): A749.
17. Mahler D.A., Montner P., Brazinsky S.A., Goodwin B., Menioge S.S., Witek T.J. Tiotropium (Spiriva): a new long–acting anticholinergic bronchodilator improves dispnea in patients with COPD. Am J Respir Crit Care Med 2000; 161: A892.
18. ZuWallck R., Jones P.W., Kotch A., Goodwin B., Menioge S.S., Serby C.W. Tiotropium (Spiriva) improves health status in patient with COPD. Am J Respir Crit Care Med 2000; 161:A892.
19. Casaburi R., Mahler D.A., Jones P.W., Serby C.W., Menioge S.S., Witek T.J. Tiotropium improves lung function, dyspnea and quality of life in patients with COPD. Presented (oral) at the Annual Meeting of the American College of Chest Physicians (ACCP), San Francisco, USA, 22–26 October 2000 (Chest 2000).
20. Wincken W., van Noord J.A., Greefhorst A.P.M., Bantje Th., Korducki L., Moonen D. et al. (Belgian/Dutch Study Group). Superior bronchodilator effects of tiotropium (TIO) vs ipratropium bromide (IB) in patients with COPD over 1–year clinical trial. Presented at the 10th European Respiratory Society Annual Conference (ERS), Florence, Italy, 30 August–3 Septemder 2000. Eur Respir J 2000; 16 (Suppl 31):55s.
21. Van Noord J.A., Bantje Th., Eland M.E., Korducki L., Cornelissen P.J.G. (Belgian/Dutch Study Group). A randomized controlled comparison of tiotropium and ipratropium in the treatment of chronic obstructive pulmonary disease. Thorax 2000; 55:289–294.
22. Greefhorst A.P.M., Wincken W., van Noord J.A., Korducki L., Moonen D., Cornelissen P.J.G. (Belgian/Dutch Study Group). Improvement in perceived dyspnea in COPD patients receiving tiotropium vs ipratropium bromide (Atrovent). Presented at the 10th European Respiratory Society Annual Conference (ERS), Florence, Italy, 30 August–3 September 2000. Eur Respir J 2000; 16 (Suppl 31):54s
23. Jones P. Personal communication. 10th European Respiratory Society Annual Conference (ERS), Florence, Italy, 30 August–3 September 2000. www.medscape.com/ConferenceSearchAlll.ctm/
24. Cremers J.P.H.M., Wincken W., van Noord J.A., Bantje Th., Korducki L., Moonen D., Cornelissen P.J.G. (Belgian/Dutch Study Group). Tiotropium (TIO) reduces the incidemce of COPD exacerbations compared to ipratropium (IB). Presented at the 10th European Respiratory Society Annual Conference (ERS), Florence, Italy, 30 August–3 September 2000. Eur Respir J 2000; 16 (Suppl 31):54s
25. van Noord J .A., Jones P.W., Wincken W., Greefhorst A.P.M., Moonen D., Korducki L., Cornelissen P.J.G. (Belgian/Dutch Study Group). Tiotropium (TIO): improved quality of life compared with ipratropium (IB). Presented at the 10th European Respiratory Society Annual Conference (ERS), Florence, Italy, 30 August– 3 September 2000. Eur Respir J 2000; 16 (Suppl 31):54s
26. Kesten S., Flanders J., Serby C.W., Witek T.J.Compliance with tiotropium a once–daily dry powder inhaled bronchodilator in 1–year COPD trials. Presented at the 10th European Respiratory Society Annual Conference (ERS), Florence, Italy, 30 August–3 September 2000. Chest 2000.
27. Rand C.S., Nides M., Cowles M.K., Wise R.A., Connett J. Long–term metered–dose inhaler adherence in a clinical trial: The Lung Health Study Research Group. Am J Respir Crit Care Med; 152: 580–588.












