Заболевание развивается преимущественно в возрасте 20–30 лет, при этом у мужчин наблюдается в 2–3 раза чаще [1]. Установление диагноза в России в отличие от стран Европы запаздывает в среднем на 9 лет [2–4]. Средняя длительность между появлением первых симптомов АС и постановкой диагноза в России составляет 8,7±6,7 года [2], в Москве – 8,1±6,0 лет [3], в Чебоксарах – 8,6±6,2 года [5], в Казани – 4,2±1,2 года [6]. Причинами столь поздней диагностики являются малосимптомное течение болезни и, вследствие этого, несвоевременное обращение пациентов за медицинской помощью, многообразие клинических проявлений в дебюте АС (зачастую имеет место, например, не только поражение аксиального скелета, но и вовлечение в патологический процесс периферических суставов, энтезисов и висцеральных органов), а также недостаточное знание врачами первичного звена особенностей воспалительных болей в нижней части спины [3, 6].
Как показывает практика, на поликлиническом уровне первым и основным на протяжении длительного времени диагнозом при АС становится «остеохондроз позвоночни-ка» с различными его проявлениями (тораколюмбалгия, люмбалгия, люмбоишиалгия, радикулопатия и др.). Такой диагноз выставляется при первичном обращении едва ли не каждому второму пациенту с АС. И это несмотря на то, что значительная часть обратившихся – лица молодого возраста. Так, по нашим данным, средний возраст больных АС в дебюте заболевания составлял 27,4±9,5 года [5], по данным Т.В. Дубининой – 21,9±6,9 года [3], Л.И. Мясоутовой с соавт. – 23,8±6,2 года [6], Е.В. Волнухина с соавт. – 25,1±7,6 года [2].
Неоправданная постановка диагноза «остеохондроз позвоночника» молодому пациенту, обратившемуся за медицинской помощью по поводу болей в нижней части спины, обусловливает смещение вектора диагностических процедур в сторону малоинформативных в плане выявления активного сакроилиита (остеита) методов клинического и инструментального исследования. Среди последних наиболее часто проводятся рентгенография, рентгеновская компьютерная и магнитно-резонансная томография (МРТ) различных отделов позвоночника. Как результат, пациент с воспалительной болью в спине неоправданно долго «идет» к «своему» врачу, сменив на пути к ревматологу несколько специалистов (терапевт, невролог, хирург, мануальный терапевт и др.), побывав у врачей различного профиля в общей сложности до 7 раз [3].
Поэтому уместным будет напомнить практическим врачам современные подходы к диагностике АС.
Согласно современным требованиям, диагноз АС продолжает устанавливаться в соответствии с модифицированными Нью-Йоркскими критериями (табл. 1), принятыми более 30 лет назад.

В соответствии с требованиями этих критериев, для подтверждения диагноза требуется обязательное наличие рентгенологически выявленного сакроилиита [1], что само по себе накладывает определенные ограничения в плане своевременной диагностики АС. Установлено, что достоверные изменения на рентгенограмме костей таза в 36% случаев появляются через 5 лет, а в 59% случаев – лишь через 10 и более лет от начала заболевания [7], что, по мнению D. van der Heijde и W. Maksymowych [8], является одним из основных препятствий для ранней диагностики АС у большинства пациентов.
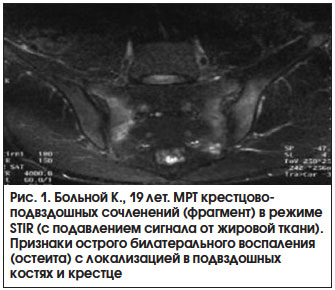
С учетом того, что в отсутствие структурных изменений в крестцово-подвздошных сочленениях может наблюдаться активное воспаление (остеит), выявляемое с помощью МРТ (рис. 1), использование этого метода визуализации положено в основу российской версии модифицированных Нью-Йоркских критериев АС (табл. 2) [9]. По мнению авторов, применение усовершенствованных критериев диагностики АС способствует более раннему выявлению заболевания на так называемой «дорентгенологической» стадии, когда в отсутствие рентгенологически достоверного сакроилиита имеет место субхондральный и/или костно-мозговой отек в области крестцово-подвздошных сочленений, что в свою очередь позволяет своевременно назначить пациентам эффективную терапию [9].

Воспалительная боль в спине, длящаяся более 3 мес. (согласно критериям экспертов ASAS), характеризуется 5 признаками:
1) возраст начала боли – до 40 лет;
2) постепенное начало;
3) улучшение после выполнения физических упражнений;
4) отсутствие улучшения в покое;
5) ночная боль (с улучшением при пробуждении) [11].
При этом хроническая боль в спине считается воспалительной при наличии как минимум 4-х признаков из 5.
Для врача-терапевта принципиально важным являются знание особенностей воспалительных болей в нижней части спины, умение дифференцировать их с механическими болями в позвоночнике, для последних характерен ряд признаков:
1) дебют болей в возрасте старше 40 лет;
2) острое начало;
3) длительность болей менее 4 нед.;
4) утренняя скованность, как правило, менее 30 мин;
5) отсутствие ночной боли;
6) физические упражнения могут усиливать болевой синдром;
7) ограничение подвижности в поясничном отделе позвоночника только в сагиттальной плоскости;
8) возможно развитие неврологических симптомов.
Воспалительная боль в спине в 75% случаев считается первым клиническим симптомом АС в дебюте заболевания [12]. Однако необходимо также принять во внимание тот факт, что вариантами дебюта АС могут стать периферический артрит (в 15–25% случаев), энтезиты (менее 3%), дактилиты (менее 1%), увеит (5%), псориаз кожи (менее 3%), воспалительные заболевания кишечника (менее 3%).
Показаниями для направления пациентов с хронической болью в спине длительностью более 3 мес., дебютировавшей в возрасте до 45 лет, на консультацию к ревматологу для своевременного распознавания АС являются:
1) воспалительная боль в спине по критериям ASAS (наличие данного клинического синдрома позволит установить диагноз АС у каждого 7-го пациента);
2) хороший ответ на нестероидные противовоспалительные препараты (НПВП), заключающийся в отчетливом уменьшении болей в спине после приема данных препаратов в течение 24–48 ч и возобновлении болей в течение этого же промежутка времени после их отмены;
3) наличие олиго-, моноартритов, энтезитов (в первую очередь ахиллобурсита, подошвенного фасциита) у лиц молодого возраста;
4) повышение острофазовых показателей крови (скорость оседания эритроцитов (СОЭ), С-реактивный белок (СРБ));
5) обнаружение антигена HLA-B27 (проведение данного теста сопряжено с однократными финансовыми затратами, но полезно для верификации АС у каждого 3-го пациента, направляемого к ревматологу);
6) выявление сакроилиита при рентгенографическом исследовании крестцово-подвздошных сочленений;
7) выявление активного сакроилиита по данным МРТ крестцово-подвздошных сочленений (характеризуется высокой специфичностью, но является дорогостоящим методом исследования, вследствие чего не рекомендуется для скрининга АС в рутинной общеврачебной практике) ([12] с доп. Ш. Эрдеса, 2013).
Первичной целью лечения больного АС является максимально длительное сохранение качества жизни, связанного со здоровьем, посредством контроля симптомов воспаления, предупреждения прогрессирования структурных повреждений, сохранения двигательной функции и социального статуса пациента. Это достигается применением нефармакологических (в первую очередь образование пациентов и регулярные физические упражнения) и фармакологических методов лечения АС.
К лекарственным препаратам, активно используемым в терапии АС, относятся НПВП, анальгетики, глюкокортикоиды (ГК), базисные противовоспалительные препараты в случае развития периферического артрита (сульфасалазин, в последнее время накапливаются данные об эффективности использования метотрексата в терапии одного из прогностически неблагоприятных проявлений АС – коксита [13]), ингибиторы фактора некроза опухоли (ФНО)-α.
Следует подчеркнуть, что из всего многообразия лекарственных средств, используемых в современной терапии АС, НПВП являются препаратами первой линии в лечении этого заболевания и назначаются всем пациентам с АС сразу после установления диагноза независимо от степени активности и стадии заболевания [1, 14]. При этом есть основания полагать, что НПВП при АС оказывают не только симптоматическое, но и (при длительном непрерывном применении) болезнь-модифицирующее действие, заключающееся в замедлении рентгенологического прогрессирования заболевания (оссификации позвоночника) за счет подавления воспаления [15–19]. Влияние НПВП на рентгенологическое прогрессирование в позвоночнике при АС в большей степени выражено у пациентов, имеющих такие факторы риска, как наличие синдесмофитов и высокие острофазовые показатели, в частности, СРБ [20].
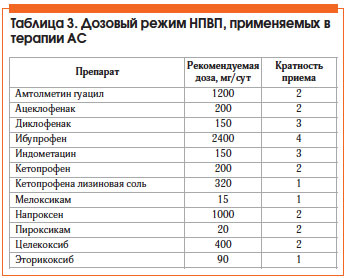
Спектр НПВП, применяемых в терапии АС, достаточно широк. Необходимо подчеркнуть, что эффективность НПВП носит дозозависимый характер и в полной мере реа-лизуется при назначении НПВП в адекватных противовоспалительных терапевтических дозах (табл. 3), в непрерывном режиме, с индивидуальным подбором оптимального препарата в каждом конкретном случае [21].
Важно осуществлять выбор НПВП с учетом наличия у пациента основных факторов риска НПВП-ассоциированных осложнений, в первую очередь это касается потенциальных осложнений со стороны желудочно-кишечного тракта (ЖКТ) (табл. 4) и сердечно-сосудистой системы [22].
Определение кардиоваскулярного риска у пациентов, принимающих НПВП, сводится к количественной оценке суммарного риска смерти от сердечно-сосудистых заболеваний в ближайшие 10 лет с помощью таблиц SCORE (Европейская шкала суммарного сердечно-сосудистого риска) [22]. При этом под «низким» кардиоваскулярным риском принимается показатель SCORE <1% в отсутствие заболеваний сердечно-сосудистой системы.

Пациенты с артериальной гипертонией, но без ишемической болезни сердца (ИБС) и с показателем SCORE 1–4% составляют группу «умеренного» риска, с неосложненными стабильными формами ИБС и SCORE ≥5% – группу «высокого» риска. В случаях «умеренного» и «высокого» риска кардиоваскулярных осложнений, связанных с приемом НПВП, рекомендуется использовать более безопасные НПВП, такие как напроксен, целекоксиб, кетопрофен, низкие дозы ибупрофена (не превышающие 1200 мг/сут).
«Очень высокий» риск осложнений со стороны сердечно-сосудистой системы на фоне приема НПВП имеют пациенты с ИБС, осложненной хронической сердечной недостаточностью ≥2 функционального класса (по NYHA), инфарктом миокарда, ишемическим инсультом в анамнезе, сахарным диабетом (СД) 2-го типа с поражением органов-мишеней, при развитии хронической болезни почек. В этом случае рекомендуется избегать назначения любых НПВП, а с обезболивающей целью применять простые и опиоидные анальгетики, актуальным также становится локальное введение инъекционных ГК [22].
Учитывая молодой возраст пациентов с АС, логичным будет предположить, что вероятность гастроэнтерологического и кардиоваскулярного рисков на фоне приема НПВП у них будет невысока.
Как показала отечественная ревматологическая практика, пациентам с АС чаще назначаются диклофенак, нимесулид и мелоксикам, доля которых составила примерно 3/4 от всех используемых НПВП [23]. Наибольший коэффициент эффективности был отмечен у неселективных НПВП (для диклофенака он составил 1,72, для индометацина – 1,68), однако именно эти препараты отменялись чаще всего из-за развития нежелательных явлений. С другой стороны, на фоне приема умеренно селективных ингибиторов ЦОГ-2 (коэффициент эффективности нимесулида и мелоксикама составил 1,49 и 1,32 соответственно) также наблюдался большой процент отмены НПВП по причине стойкого улучшения состояния, т. е. отсутствия необходимости в их приеме, по сравнению с индометацином и диклофенаком.
В России для лечения АС широко используются нимесулиды. Это объясняется высокой биодоступностью нимесулида, быстрым достижением максимальной концентрации в крови и быстрым развитием анальгетического действия. Наличие в молекуле нимесулида метилсульфониловой группы делает его нейтральным (рКа 6,5), т. е. более безопасным для слизистой оболочки верхних отделов ЖКТ, чем другие НПВП, обладающие свойствами кислот. Благодаря своим химическим свойствам нимесулид легко попадает в очаги воспаления, особенно в ткани сустава, где его концентрация выше, чем в плазме крови. Нимесулид, как и все НПВП, обладает ЦОГ-зависимым симптоматическим эффектом, но, кроме этого, приводит к блокаде синтеза основных провоспалительных цитокинов (интерлейкин-6, ФНО-α), фермента фосфодиэстеразы IV типа, активирующего макрофагальную и нейтрофильную активность, снижению активности матриксных металлопротеиназ.
Безусловно, в ряде случаев на фоне приема НПВП могут возникать класс-специфические нежелательные явления, вероятность которых резко возрастает при длительном применении НПВП. В первую очередь это касается развития патологии верхних отделов ЖКТ, связанной с системным влиянием НПВП, риск которого увеличивается по сравнению с таковым в общей популяции более чем в 4 раза (0,5–1,0 случай на 100 пациенто-лет). Больные, регулярно принимающие НПВП, погибают от серьезных осложнений со стороны ЖКТ (желудочно-кишечные кровотечения, перфорации) в 2-3 раза чаще, чем лица, не принимающие НПВП [24]. В эпидемиологическом исследовании J. Laporte et al. был проведен анализ причин 2813 случаев опасного желудочно-кишечного кровотечения на фоне приема НПВП, при этом нимесулид продемонстрировал большую безопасность (относительный риск кровотечения составил 3,2), чем диклофенак (3,7), мелоксикам (5,7) и рофекоксиб (7,2) [25]. Справедливости ради стоит отметить, что наименьший относительный риск кровотечения был у целекоксиба (0,3) и ацеклофенака (1,4). В другом исследо-вании, включившем 8830 пациентов, при оценке развития желудочно-кишечных кровотечений большая частота данной патологии была отмечена в группе больных, получавших диклофенак (12,1%), чем в группе принимавших нимесулид (8,1%) [26].
В 2013 г. были опубликованы результаты крупного популяционного исследования, в ходе которого проведена оценка риска развития НПВП-ассоциированных осложнений со стороны верхних отделов ЖКТ у 588 827 пациентов при более чем 3,5 млн назначений различных НПВП за 7-летний период (с 2001 по 2008 г.) [27]. Было показано, что применение в клинической практике целекоксиба и нимесулида сопряжено с низким риском развития серьезных гастроэнтерологических осложнений, тогда как использование напроксена, ибупрофена, диклофенака, эторикоксиба и мелоксикама приводит к более высокому риску осложнений со стороны ЖКТ.
В последние годы в мировой литературе обсуждается вопрос гепатотоксичности ряда препаратов из группы НПВП, но в большей степени взгляды врачей оказались прикованы к нимесулиду. Так, за 15-летний (с 1985 по 2000 г.) период применения препарата в мировой клинической практике было зафиксировано 192 эпизода значимых осложнений со стороны печени (клинически выраженный внутрипеченочный холестаз или острая печеночная недостаточность), что послужило причиной для ограничения использования нимесулида в странах Европы курсом не более 15 дней в дозе, не превышающей 200 мг/сут [28].
В то же время в ряде исследований было показано, что гепатотоксичность нимесулида не выше, чем у других НПВП. Так, при краткосрочном применении нимесулида (не более 30 дней) повышение уровня аминотрансфераз в 2 и более раза было отмечено лишь у 0,4% пациентов, а при длительном использовании (более 6 мес.) – у 1,5% больных [29, 30].
В одном из масштабных популяционных исследований проанализирована частота развития гепатотоксических реакций у 397 537 больных, получавших различные НПВП [31]. Частота серьезных осложнений со стороны печени в случае использования нимесулида составила 35,3 на 100 тыс. пациенто-лет, что оказалось меньше, чем при использовании диклофенака (39,2), ибупрофена (44,6) и кеторолака (66,8).
По мнению экспертов, факторами риска развития НПВП-индуцированного повреждения печени следует признать: женский пол, возраст >65 лет, патологию гепатобилиарной системы, тяжелые сопутствующие заболевания, гипоальбуминемию, сочетанный прием препаратов, влияющих на метаболизм НПВП, гепатотоксические реакции в анамнезе [32].
В исследовании, проведенном отечественными авторами, дана оценка частоты встречаемости нарушений функции печени у пациентов с аксиальным спондилоартритом [33]. Было установлено, что в 1/4 случаев больные, длительно принимающие нимесулид (более 6 мес), регулярно превышают рекомендованную среднетерапевтическую дозировку, несмотря на предупреждения врачей о недопустимости подобных действий. При этом даже на фоне длительного использования препарата, подчас в дозах, превышающих 200 мг/сут, минимальное повышение уровня аминотрансфераз было отмечено только в 7,14% случаев и купировалось спустя 1 нед. после отмены препарата без дополнительного назначения гепатопротекторов.
В 2010 г. в России был зарегистрирован отечественный дженерик нимесулида – Немулекс® в виде гранул для приготовления суспензии для приема внутрь. Отсутствие в его составе высококалорийного полисахарида мальтодекстрина делает более безопасным его применение у пациентов с сопутствующим СД, избыточной массой тела, нарушением обмена веществ [34].
В настоящее время опубликованы результаты нескольких клинических исследований, посвященных кратковременному использованию препарата Немулекс® в дозе 200 мг/сут у пациентов с остеоартрозом и АС [35–37].
Заслуживает внимания исследование И.З. Гайдуковой с соавт., продемонстрировавшее эффективность Немулекса® у 30 больных с активным АС [35]. Клинически значимого улучшения по критериям ASAS (Assessment of SpondyloArthritis International Society – Международное общество по изучению спондилоартритов) достигли 60% пациентов, интенсивность боли в спине уменьшилась практически в 2 раза. Серьезных нежелательных явлений в ходе исследования зарегистрировано не было, лишь у 3-х пациентов было отмечено повышение уровня аминотрансфераз до 3-х норм (купировалось в течение 1 нед. на фоне соблюдения диеты и назначения гепатопротекторов) и у 3-х больных – развитие диспепсии без наличия эрозивных повреждений слизистой оболочки ЖКТ.
Таким образом, сочетание у нимесулида выраженного анальгетического, противовоспалительного действия и хорошей переносимости позволяет рекомендовать его в качестве препарата выбора при лечении больных АС при условии индивидуальной оценки основных факторов риска НПВП-ассоциированных осложнений. Проведение долгосрочных исследований эффективности и безопасности препарата Немулекс® позволит врачу общей практики с уверенностью назначать его пациентам с хроническими ревматическими заболеваниями.












