Нестероидные противовоспалительные препараты (НПВП) в лекарственных формах для перорального и парентерального использования широко используются для лечения ревматических заболеваний. Эффективность традиционно используемых НПВП при лечении остеоартроза и ревматоидного артрита по результатам ряда исследований превышает таковую для ненаркотических анальгетиков, в частности парацетамола [1].
Однако профиль безопасности НПВП отличается серьезным недостатком – отрицательное влияние на слизистую органов желудочно–кишечного тракта. Кроме того, механизм действия НПВП – угнетение активности циклооксигеназ – связан с изменением адгезивных свойств тромбоцитов. При условии широкого использования традиционных НПВП указанные особенности приводят к относительно большому числу серьезных побочных эффектов. В Великобритании ежегодно регистрируется около 2,5 тысяч случаев смертей, связанных с использованием традиционных НПВП [2]. Для сравнения: в автокатастрофах в этой стране погибает около 3,5 тысяч человек в год. На этом фоне вполне обоснованно стремление фармацевтических компаний к созданию терапевтически эквивалентных в отношении эффективности лекарственных средств, но со значительно более благоприятным профилем безопасности. Воодушевление конца 90–х годов ХХ века, связанное с появлением ЦОГ–2 селективных НПВП, к настоящему моменту, после получения результатов ряда исследований, сменилось более сдержанной оценкой безопасности этой группы препаратов (табл. 1). При относительно равной эффективности с неселективными НПВП и более низкой частотой развития осложнений со стороны желудочно–кишечного тракта [3] эти препараты, по–видимому, обладают более выраженным негативным влиянием на сердечно–сосудистую систему.
Иной принцип повышения безопасности НПВП был реализован при создании лекарственных форм НПВП для местного применения (мази, гели, аэрозоли, растворы). За счет резкого уменьшения системного действия препарата удается избежать развития серьезных нежелательных явлений. Вопрос о достаточной клинической эффективности подобных препаратов был решен в ряде многочисленных плацебо–контролированных исследований.
В 2004 году были опубликованы результаты канадского исследования лечения больных остеоартрозом раствором, содержащим в качестве активного компонента диклофенак [4]. Исследование представляло собой рандомизированное слепое плацебо–контролированное, продолжительностью 4 недели. 248 больных, нуждающихся в использовании анальгетической терапии, но не принимавших пероральных НПВП, были рандомизированы в 3 группы, в которых использовались следующие варианты местной терапии: плацебо, состав, содержащий диметилсульфоксид (ДМСО), и состав, содержащий диклофенак и ДМСО (в качестве проводника, усиливающего проникновение диклофенака). Мазевые составы использовались 4 раза в день. Разница в частоте уменьшения интенсивности болей (подшкала боли WOMAC) между основной группой и двумя контрольными группами была очевидна (44%, 27% и 27% соответственно). Достоверно более благоприятный эффект оказывал состав с диклофенаком и при учете остальных подшкал WOMAC. В этой связи следует заметить, что эффективность плацебо при болевом синдроме традиционно принято считать равной 30%. Отсутствие разницы в эффекте между плацебо и состава, содержащего ДМСО, оказалось прямым свидетельством связи эффекта с содержанием в составе диклофенака. Отказ от продолжения терапии в группе плацебо отмечен в 12% и был связан с отсутствием эффекта; в группе, получавшей состав с диклофенаком и ДМСО, отказ от терапии отмечен в 6% и связывался с развитием местных побочных эффектов (сыпь, сухость кожи).
В соответствии с современной концепцией доказательной медицины наиболее высокой степенью доверия обладают результаты мета–анализа, обобщающего данные множества исследований обсуждаемого лекарственного средства. Относительно эффективности НПВП в лекарственных формах для местного применения к настоящему моменту опубликованы 2 мета–анализа. Работа 1998 года включала в себя исследования эффективности у больных с различными ревматическими заболеваниями [5]. Мета–анализ показал, что эффективность НПВП для местного применения при 2–недельном использовании у больных с «хроническим болевым синдромом» выше, чем в группе плацебо. В конце 90–х годов ХХ века была сформирована концепция о наиболее эффективных НПВП в лекарственных формах для наружного применения. К таким НПВП были отнесены препараты диклофенака и кетопрофена; отличий от эффективности плацебо не было обнаружено у препаратов, содержащих индометацин.
В ряде исследований было показано различие в способности абсорбции солей диклофенака через кожные покровы. Более липофильные свойства диэтиламина диклофенака в отличие от натриевой и калиевой соли стали полезны при создании гелей [6]. Одна из последних работ по исследованию эффективности диэтиламина диклофенака была проведена с участием 238 больных остеоартрозом. Дизайн работы представлял собой рандомизированное, плацебо контролированное исследование. Достоверная разница в уменьшении интенсивности боли начала обнаруживаться к 5–му дню использования препарата и достигла максимума к концу второй недели применения геля.
Мета–анализ, проведенный в 2004 году, обобщал результаты только рандомизированных, контролируемых исследований у больных остеоартрозом [7]. В работу вошли данные 13 исследований, в которых эффект сравнивался с плацебо либо с таблетированными препаратами. Результат работы вновь подтвердил эффективность НПВП для местного применения при использовании не менее 2–х недель.
Эффективность раствора диклофенака для местного применения при длительном использовании (в течение 6 недель) при сравнении с раствором плацебо была доказана в более позднем исследовании на 216 больных остеоартрозом [8]. В приведенном исследовании среди побочных эффектов отмечались исключительно местные явления: сыпь, сухость кожи. Учитывая низкую системную абсорбцию НПВП с поверхности кожи, становится очевидным, что риск развития системных побочных эффектов весьма незначителен.
Результаты фармакокинетических исследований лекарственных форм для наружного применения диклофенака, кетопрофена и ибупрофена приведены в таблице 2.
Приведенные данные свидетельствуют о проникновении НПВП при местном применении в подлежащие ткани и низкой концентрации препарата в плазме, что весьма важно для предотвращения развития системных побочных эффектов. Соотношение концентрации диклофенака для наружного применения в плазме и к таковой для таблетированных форм можно представить, если учитывать, что максимальные его концентрации при приеме таблетки 50 мг достигают 1500 нг/мл.
В одной из самых ранних работ по исследованию фармакокинетики диклофенака в форме геля при наружном использовании было показано, что в системный кровоток проникает не более 6% препарата [9].
В недавно проведенном сравнительном исследовании были изучены концентрации диклофенака в тканях при нанесении 4%–го геля 3 раза в сутки (суточная доза 150 мг) и приеме таблеток, покрытых оболочкой, по 50 мг 3 раза в сутки в течение 3 дней [10]. Относительная биодоступность диклофенака, при учете его содержания в подкожной клетчатке и мышечной ткани, была более чем в 1,5 раза выше после местного использования диклофенака, чем при пероральном приеме; концентрация в плазме была в 50 раз ниже, а максимальная концентрация в 250 раз ниже (4,89 нг/мл и 1240 нг/мл соответственно). Очевидно, что при использовании гелей, содержащих диклофенак, в подлежащих тканях воспаленной области создаются концентрации не ниже, чем при использовании таблетированных форм, а концентрация в плазме на 2 порядка ниже. Теоретически подобная фармакокинетическая характеристика гелей с диклофенаком может свидетельствовать об аналогичной эффективности препаратов при отсутствии серьезных побочных эффектов у лекарственных форм для местного применения.
Весьма демонстративна в отношении подтверждения высокой безопасности и равной с таблетированными формами эффективности НПВП для наружного применения работа Tugwell с соавт. [11]. Исследование отвечает всем современным требованиям доказательной медицины и выполнено в виде двойного слепого рандомизированного плацебо–контролируемого. Объем выборки – 622 больных остеоартрозом, продолжительность исследования – 12 недель. Больные первой группы получали диклофенак в дозе 150 мг/сут., вторая группа использовала только раствор диклофенака для местного применения, содержащий ДМСО. Завершили исследование 61% больных. Из выбывших пациентов по причине развития нежелательных явлений 20% было в группе, использовавшей диклофенак местно, 25% – таблетки диклофенака, из–за отсутствия эффекта выбыло 9 и 3% соответственно. Число больных, «ответивших» на терапию, в группах значимо не различалось (67% в группе, получавшей диклофенак местно; 70% – в группе принимавших диклофенак внутрь).
При использовании раствора диклофенака для наружного применения наиболее часто отмечались: сухость кожи (27%), сыпь (12%), зуд (6%). Довольно частое появление этих реакций может быть связано с содержащимся в растворе ДМСО, так как при использовании гелей подобные явления встречаются значительно реже.
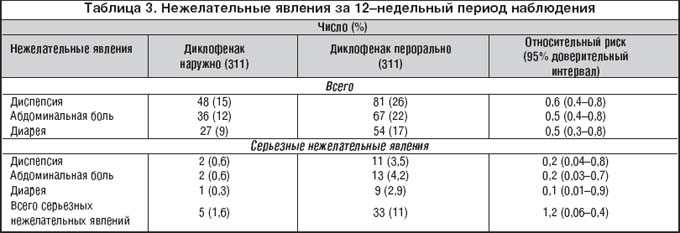
Нежелательные явления со стороны желудочно–кишечного тракта встречались в обеих группах, но значительно чаще при использовании таблетированного диклофенака (табл. 3).
Изменения лабораторных показателей также чаще отмечались в группе использовавшей таблетированный диклофенак, чем в группе больных, применявших диклофенак местно. Повышение АЛТ отмечалось в 18 и 2,7%; снижение гемоглобина в 12 и 2,7% соответственно.
Спектр нозологических форм, присутствующих в исследованиях по эффективности препаратов диклофенака, довольно широк и включает, помимо остеоартроза, спортивные травмы [12], ревматоидный артрит, ревматические заболевания мягких тканей [5].
В странах Европы лекарственные формы НПВП для наружного применения широко представлены на фармацевтическом рынке, в основном это касается препаратов диклофенака и кетопрофена. Обсуждается вопрос о необходимости включения этих препаратов в стандарты терапии остеоартроза в связи с полученными доказательствами их безопасности и эффективности [13]. Вместе с тем в США эти средства до настоящего момента не получили разрешения на использование у больных с ревматическими заболеваниями. Формально этот вопрос касается недостаточности аргументации в отношении эффективности этих лекарственных форм. В этой связи следует упомянуть, что FDA в 2000 году одобрила регистрацию крема диклофенака для лечения старческого кератоза (actinic keratosis) – предракового заболевания кожи в связи с доказанностью четкого терапевтического эффекта. Видимо, это проблема времени, так как в Канаде диклофенак в лекарственных формах для наружной терапии для лечения болевого синдрома уже занял нишу на фармацевтическом рынке. В США для лечения локального болевого синдрома широко распространены препараты для наружного применения, содержащие в качестве активных компонентов метилсалицилат, ментол, камфору [14]. При этом степень доказательности эффективности подобных препаратов ниже, чем для НПВП наружного применения.
В фармакокинетических исследованиях было подтверждено проникновение метилсалицилата в ткани при местном применении лекарственных форм [15]. Вместе с тем можно говорить о более высоком абсорбционном потенциале метилсалицилата из лекарственных форм по сравнению с НПВП [16]. Соотношение между содержанием метилсалицилата в подкожной клетчатке и концентрацией в плазме крови (около 30) явно выше, чем для НПВП [15].
В РФ зарегистрировано более 100 лекарственных форм НПВП для наружного применения (мази, гели). Основную их долю составляют препараты диклофенака. Среди этого обилия лекарственных средств, учитывая приведенные данные, особый интерес вызывают комбинированные препараты, содержащие в своем составе помимо диклофенака метилсалицилат, ментол и льняное масло (гель Диклоран Плюс, фармацевтическая компания «Юник Фармасьютикал»). Очевидно, что при комбинации в Диклоране Плюс активных веществ с различными механизмами действия значительно повышается вероятность усиления клинического эффекта. Отрицательного взаимодействия между НПВП и салицилатами при наружном применении лекарственных форм не описано. При пероральном применении салицилатов в комбинации с НПВП существует риск увеличения частоты нежелательных явлений со стороны ЖКТ, однако данный феномен не может относиться к лекарственным формам для наружного применения в связи с принципиальной разницей в фармакокинетическом профиле.
В заключение следует сказать, что лекарственные формы НПВП для наружного применения (Диклоран Плюс гель) обладают высокой безопасностью и эффективностью, сравнимой при остеоартрозе с использованием пероральных форм. Комбинирование активных компонентов этих лекарственных средств с метилсалицилатом теоретически обосновано в отношении повышения их терапевтической эффективности. Безопасность этих лекарственных форм является неоспоримым аргументом в пользу более широкого их применения.


Литература
1. Pincus T., Swearingen C., Cummins P., Callahan L.F. Preference for nonsteroidal antiinflammatory drugs versus acetaminophen and concomitant use of both types of drugs in patients with osteoarthritis. J Rheumatol 2000; 27:1020–7.
2. Tramer M.R., Moore R.A., Reynolds D.J., McQuay H.J. Quantitative estimation of rare adverse events which follow biological progression:a new model applied to chronic NSAID use. Pain 2000; 85:169–82.
3. Hunt R.H., Harper S., Watson D.J., Yu C., Quan H., Lee M., et al. The gastrointestinal safety of the COX–2 selective inhibitor etoricoxib assessed by both endoscopy and analysis of upper gastrointestinal events. Am J Gastroenterol 2003; 98(8):1725–33.
4. Bookman A.A. et al. Effect of a topical diclofenac solution for relieving symptoms of primary osteoarthritis of the knee: a randomized controlled study. Canadian Medical Association Journal 2004, 171: 333–338.
5. Moore R.A., Tramer M.R., Carroll D., Wiffen P.j. Quantitative systematic review of topical applied non–steroidal anti–inflammatory drugs. BMJ, 1998: 316:333–8
6. Niethard F.U., Gold M.S., Solomon G.S., et al. Efficacy of Topical Diclofenac Diethylamine Gel in Osteoarthritis of the Knee. J Rheumatol 2005;32:2384–92
7. Lin J., Zhang W., Jones A., Doherty M. Efficacy of topical non–steroidal anti–inflammatory drugs in the treatment of osteoarthritis: meta–analisis of randomized controlled trials. BMJ, Oct, 2004
8. Baer P.A., Thomas L.M., Shainhouse Z. Treatment of osteoarthritis of the knee with a topical diclofenac solution: a randomised controlled, 6–week trial. BMC Musculoskelet Disord. 2005; 6: 44.
9. Reiss W., Schmid K., Botta L., et al. Die perkutane resorbtion von diclofenac. Arzneimittelforschung Drug Res 1986; 36(II): 1092–6.
10. Brunner M., Dehghanyar P., Seigfried B., et al. Favourable dermal penetration of diclofenac after administration to the skin using a novel spray gel formulation. British Journal of Clinical Pharmacology, 60, 573.
11. Tugwell P.S. et al. Equivalence study of a topical diclofenac solution (PENNSAID) compared with oral diclofenac in the symptomatic treatment of osteoarthritis of the knee: a randomized controlled study. Journal of Rheumatology 2004 31: 2002–2012.
12. Predel H.G., Koll R, Pabst P., et al. Diclofenac patch for topical treatment of acute impact injuries : a randomised, double blind рlacebo controlled, multicentre study. Br. J. Sports Med. 2004; 38; 318–323.
13. Courtney P., and Doherty M. Key questions concerning paracetamol and NSAIDs for osteoarthritis. Ann Rheum Dis, 2002;61;767–773.
14. American Medical Directors Association. Chronic Pain Management in the Long–Term Care Setting: Clinical Practice Guidelines 1999.
15. Cross S.E., Anderson C., Roberts M.S. Topical penetration of commercial salicylate esters and salts using human isolated skin and clinical microdialisis studies. Br. J. Clin. Pharmacol., 1998; 46: 29–35.
16. Martin D., Valdez J., Boren J., Mayersohn M. J. Dermal absorbtion of camfor, menthol, and methyl salicylate in humans. Clin. Pharmacol 2004 Oct, 44 (10): 1151–7.












