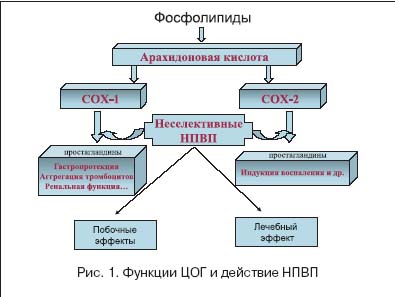
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Ї–Њ—Б—В–љ–Њ––Љ—Л—И–µ—З–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ–Њ —З–∞—Б—В–Њ—В–µ –Ј–∞–љ–Є–Љ–∞—О—В –≤—В–Њ—А–Њ–µ –Љ–µ—Б—В–Њ –њ–Њ—Б–ї–µ –Њ–±—А–∞—Й–µ–љ–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є [3], —З—В–Њ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 27% –≤—Б–µ—Е –Њ–±—А–∞—Й–µ–љ–Є–є –Ї –≤—А–∞—З—Г. –С–Њ–ї—М, —Б–≤—П–Ј–∞–љ–љ–∞—П —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–Њ–≤, —З–∞—Й–µ –≤—Б–µ–≥–Њ –Є–Љ–µ–µ—В —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П: –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є, –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є–є, —Б–Њ—Б—Г–і–Є—Б—В—Л–є, —З—В–Њ —В—А–µ–±—Г–µ—В –љ–µ–њ—А–µ—А—Л–≤–љ–Њ–є –Љ–љ–Њ–≥–Њ–ї–µ—В–љ–µ–є —В–µ—А–∞–њ–Є–Є –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е [4,5]. –Ъ –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –і–Њ–≤–Њ–ї—М–љ–Њ –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Э–Я–Т–Я, –Є–Љ–µ—О—Й–Є—Е —А–∞–Ј–ї–Є—З–љ—Г—О —Е–Є–Љ–Є—З–µ—Б–Ї—Г—О —Б—В—А—Г–Ї—В—Г—А—Г –Є —А–∞–Ј–ї–Є—З–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П. –Ю–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ–µ–є—И–Є—Е –Њ—В–Ї—А—Л—В–Є–є –•–• –≤–µ–Ї–∞ –≤ –Њ–±–ї–∞—Б—В–Є –Љ–µ–і–Є—Ж–Є–љ—Л —П–≤–ї—П–µ—В—Б—П –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ —В–Њ–≥–Њ, —З—В–Њ –Њ—Б–љ–Њ–≤–љ–Њ–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Э–Я–Т–Я —Б–≤—П–Ј–∞–љ —Б –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ–Љ —Б–Є–љ—В–µ–Ј–∞ —Д–µ—А–Љ–µ–љ—В–∞ —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л (–¶–Ю–У), –Њ—В–≤–µ—З–∞—О—Й–µ–≥–Њ –Ј–∞ –њ—А–Њ–і—Г–Ї—Ж–Є—О –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, —Г—З–∞—Б—В–≤—Г—О—Й–Є—Е –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞, –∞ —В–∞–Ї–ґ–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П—О—Й–Є—Е –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Љ–љ–Њ–≥–Є–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Д—Г–љ–Ї—Ж–Є–Є. –Р –Њ—В–Ї—А—Л—В–Є–µ –і–≤—Г—Е –Є–Ј–Њ—Д–Њ—А–Љ –¶–Ю–У, –Є–Љ–µ—О—Й–Є—Е —А–∞–Ј–ї–Є—З–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ (—А–Є—Б. 1), –њ—А–Є–≤–µ–ї–Њ –Ї —Б–Њ–Ј–і–∞–љ–Є—О –љ–Њ–≤–Њ–є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ (–Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ, –љ–Є–Љ–µ—Б—Г–ї–Є–і, –∞—Ж–µ–Ї–ї–Њ—Д–µ–љ–∞–Ї) –Є–ї–Є –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ (—Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±) –њ–Њ–і–∞–≤–ї—П–ї–Є —Н–Ї—Б–њ—А–µ—Б—Б–Є—О –¶–Ю–У–2, –Њ—В–≤–µ—З–∞—О—Й—Г—О –Ј–∞ –≤—Л—А–∞–±–Њ—В–Ї—Г –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, —Г—З–∞—Б—В–≤—Г—О—Й–Є—Е –≤ —А–∞–Ј–≤–Є—В–Є–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Т–љ–µ–і—А–µ–љ–Є–µ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –Э–Я–Т–Я —Б —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–µ–є—Б—В–≤–Є—П –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є—В—М —З–∞—Б—В–Њ—В—Г –≥–∞—Б—В—А–Њ–њ–∞—В–Є–є, —Н–љ—В–µ—А–Њ–њ–∞—В–Є–є, –≥–µ–њ–∞—В–Њ–њ–∞—В–Є–є, –Ї–Њ—В–Њ—А—Л–µ —Б–ї—Г–ґ–Є–ї–Є –њ—А–Є—З–Є–љ–Њ–є –њ—А–µ—А—Л–≤–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я —Г 30–70% –±–Њ–ї—М–љ—Л—Е —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ [6,7,8].
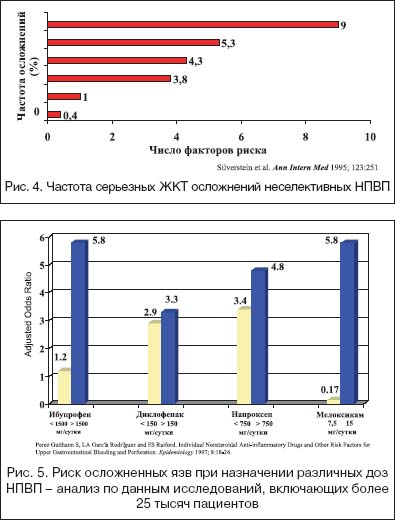
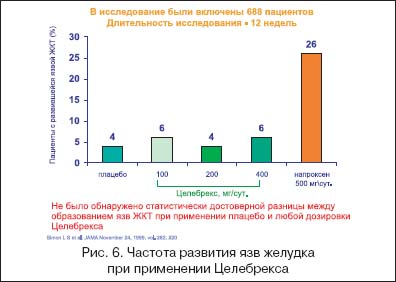
–Ю—В —З–µ–≥–Њ –ґ–µ –Ј–∞–≤–Є—Б–Є—В —Г—Б–њ–µ—Е
–ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я?
1. –Т—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–∞ —Б —Г—З–µ—В–Њ–Љ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є. –≠—В–Є —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞ —А–Є—Б—Г–љ–Ї–µ 2 –Є —Е–Њ—А–Њ—И–Њ –Ј–љ–∞–Ї–Њ–Љ—Л –Ї–ї–Є–љ–Є—Ж–Є—Б—В–∞–Љ. –Ю–і–љ–∞–Ї–Њ –≤–ї–Є—П–љ–Є–µ —Н—В–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Э–Я–Т–Я –Є–Љ–µ–µ—В —Б–≤–Њ—О —Б–њ–µ—Ж–Є—Д–Є–Ї—Г. –Ф–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є –њ—А–µ—А—Л–≤–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я —П–≤–ї—П–µ—В—Б—П –і–Є—Б–њ–µ–њ—Б–Є—П (—В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –≥–∞—Б—В—А–∞–ї–≥–Є–Є, —З—Г–≤—Б—В–≤–Њ —В—П–ґ–µ—Б—В–Є –≤ –≤–µ—А—Е–љ–µ–є —З–∞—Б—В–Є –ґ–Є–≤–Њ—В–∞) – –і–Њ 5% –≤—Б–µ—Е –Њ—В–Љ–µ–љ –Э–Я–Т–Я (—А–Є—Б. 3). –Ъ –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Н—В–Є —Б–Є–Љ–њ—В–Њ–Љ—Л –љ–µ –Ї–Њ—А—А–µ–ї–Є—А—Г—О—В —Б —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є –Є –љ–µ –Ї–Њ—А—А–µ–ї–Є—А—Г—О—В —Б —В—П–ґ–µ–ї—Л–Љ–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П–Љ–Є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Ц–Ъ–Ґ (—П–Ј–≤–∞, –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ, –њ–µ—А—Д–Њ—А–∞—Ж–Є—П). –†–∞–Ј–≤–Є—В–Є–µ –ґ–µ —Н—А–Њ–Ј–Є–≤–љ–Њ–—П–Ј–≤–µ–љ–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞ –≤ 58–80% —Б–ї—Г—З–∞–µ–≤ –љ–µ –Є–Љ–µ–µ—В —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є [9,10] –Є –њ–ї–Њ—Е–Њ –Ї–Њ—А—А–µ–ї–Є—А—Г–µ—В —Б —А–Є—Б–Ї–Њ–Љ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ —Н—А–Њ–Ј–Є–Є –Є —П–Ј–≤—Л –ґ–µ–ї—Г–і–Ї–∞ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞, –≤ –њ–µ—А–≤—Л–µ –Љ–µ—Б—П—Ж—Л –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Э–Я–Т–Я –Є –њ—А–Є –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є–Є –ї–µ—З–µ–љ–Є—П —Б–Ї–ї–Њ–љ–љ—Л –Ї —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є—О. –Т –љ–∞–Є–±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —П–Ј–≤–µ–љ–љ–Њ–—Н—А–Њ–Ј–Є–≤–љ—Л–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞ –Ї–Њ—А—А–µ–ї–Є—А—Г—О—В —Б –љ–∞–ї–Є—З–Є–µ–Љ «—П–Ј–≤–µ–љ–љ–Њ–≥–Њ» –∞–љ–∞–Љ–љ–µ–Ј–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –љ–∞—З–∞–ї–µ –ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я –Є –≤ –њ–µ—А–≤—Л–µ –Љ–µ—Б—П—Ж—Л –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –±–Њ–ї—М–љ—Л–µ –љ—Г–ґ–і–∞—О—В—Б—П –≤ —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–µ. –Я—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є —Н—А–Њ–Ј–Є–≤–љ–Њ–≥–Њ —П–Ј–≤–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞, —А–∞–Ј–≤–Є–≤—И–µ–≥–Њ—Б—П –њ—А–Є –њ—А–Є–µ–Љ–µ –Э–Я–Т–Я, –≤—А–∞—З –і–Њ–ї–ґ–µ–љ —Б–і–µ–ї–∞—В—М —Б–ї–µ–і—Г—О—Й–Є–µ –≤—Л–≤–Њ–і—Л: –∞) —Н—В–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2; –±) —Н—В–∞ –Ї–∞—В–µ–≥–Њ—А–Є—П –±–Њ–ї—М–љ—Л—Е –љ—Г–ґ–і–∞–µ—В—Б—П –≤ –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–Љ –Ї–ї–Є–љ–Є–Ї–Њ–—Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –¶–Ю–У–2 –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В —З–∞—Б—В–Њ—В—Г —А–∞–Ј–≤–Є—В–Є—П –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є, –љ–Њ –љ–µ –Є—Б–Ї–ї—О—З–∞–µ—В –њ–Њ–ї–љ–Њ—Б—В—М—О –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —А–µ—Ж–Є–і–Є–≤–∞ [11]; –≤) –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Э–Я–Т–Я––Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е —П–Ј–≤ –љ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –Э2––±–ї–Њ–Ї–∞—В–Њ—А—Л –Є–ї–Є –∞–љ—В–∞—Ж–Є–і—Л, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г –Љ–Њ–ґ–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –ї–Є—И—М –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л. –Р—Б—Б–Њ—Ж–Є–Є—А—Г—О—В—Б—П —Б —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —В—П–ґ–µ–ї—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ: –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –Є –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є. –Ш–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ, —З—В–Њ —Г –ї–Є—Ж —Б—В–∞—А—И–µ 65 –ї–µ—В –і–Њ 70% –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ–Љ –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л—Е —П–Ј–≤ –Ј–∞–Ї–∞–љ—З–Є–≤–∞—О—В—Б—П –ї–µ—В–∞–ї—М–љ—Л–Љ –Є—Б—Е–Њ–і–Њ–Љ. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Є–Љ–µ–љ–љ–Њ –њ–Њ–ґ–Є–ї–Њ–є –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В –±–Њ–ї—М–љ—Л—Е –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –љ—Г–ґ–і–∞–µ—В—Б—П –≤ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б—А–µ–і—Б—В–≤ —Б –љ–∞–Є–±–Њ–ї—М—И–µ–є —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –¶–Ю–У–2. –Ґ–µ–Љ –±–Њ–ї–µ–µ, —З—В–Њ —Г –ї–Є—Ж –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Є–Љ–µ—О—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Э–Я–Т–Я (—Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–∞—П —В–µ—А–∞–њ–Є—П, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —Б–Њ—З–µ—В–∞–љ–Є—П —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –Є–Љ–µ—О—Й–Є–Љ–Є —Б—Е–Њ–і–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є). –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є MUCOSA [12] –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ (—А–Є—Б. 4), —З—В–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —З–Є—Б–ї–∞ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–µ–Ј–Ї–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —З–∞—Б—В–Њ—В—Г —Б–µ—А—М–µ–Ј–љ—Л—Е –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Э–Я–Т–Я. –І–∞—Б—В–Њ—В–∞ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞ –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–Њ–Ј—Л –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я (—А–Є—Б. 5), –∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ —З–∞—Б—В–Њ—В–∞ —П–Ј–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —Б—Г—Б—В–∞–≤–Њ–≤ –љ–µ –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В —В–∞–Ї–Њ–≤–Њ–є –љ–∞ —Д–Њ–љ–µ –њ–ї–∞—Ж–µ–±–Њ, –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ (—А–Є—Б. 6) –Є –љ–µ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –≤–Њ–Ј—А–∞—Б—В–∞ –±–Њ–ї—М–љ–Њ–≥–Њ. –°–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ, –Ї—А–Њ–Љ–µ –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є, –Љ–Њ–≥—Г—В –њ–Њ—А–∞–ґ–∞—В—М—Б—П –Є –і—А—Г–≥–Є–µ –Њ—В–і–µ–ї—Л –Ц–Ъ–Ґ. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ—П–≤–ї–µ–љ–Є–µ –Ї–∞–њ—Б—Г–ї—М–љ–Њ–є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є–Є –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —Г—В–Њ—З–љ–Є—В—М —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Э–Я–Т–Я. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –Э–Я–Т–Я –љ–∞ —Н—В–Њ—В –Њ—В–і–µ–ї –Ї–Є—И–µ—З–љ–Є–Ї–∞ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ —П–Ј–≤–µ–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –Є –Ї–Є—И–µ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П. –Ґ–∞–Ї –Ї–∞–Ї –Э–Я–Т–Я –Є–Ј–Љ–µ–љ—П—О—В –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М –Ї–Є—И–µ—З–љ–Њ–є —Б—В–µ–љ–Ї–Є –Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ–Њ–µ –љ–∞—В—П–ґ–µ–љ–Є–µ –Ї–ї–µ—В–Њ–Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є, —В–Њ —П–Ј–≤–µ–љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б —Н—В–Њ–є –Њ–±–ї–∞—Б—В–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –і–Є—Б–њ–µ–њ—Б–Є–Є, –љ–µ —А–µ–∞–≥–Є—А—Г—О—Й–µ–є –љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л, –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ–Њ–є –∞–љ–µ–Љ–Є–Є, –љ–µ –њ–Њ–і–і–∞—О—Й–µ–є—Б—П –ї–µ—З–µ–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є Fe, –Є –≥–Є–њ–Њ–∞–ї—М–±—Г–Љ–Є–љ–µ–Љ–Є–µ–є. –Я—А–Є —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ –≤–ї–Є—П–љ–Є—П –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я (–љ–∞–њ—А–Њ–Ї—Б–µ–љ), –њ—А–Є–љ–Є–Љ–∞–µ–Љ—Л—Е —Б–Њ–≤–Љ–µ—Б—В–љ–Њ —Б –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–Њ–Љ, –Є –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ 9––Ї—А–∞—В–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ–і–Њ–±–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є [13].
2. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤—Б–µ—Е –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я –≤–µ–і–µ—В –Ї –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—О –Є–љ—В–µ—А—Б—В–Є—Ж–Є—П –њ–Њ—З–µ–Ї. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ—А–Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–Љ –∞—А—В—А–Є—В–µ (–†–Р), –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є, —В—А–µ–±—Г—О—Й–µ–Љ –Љ–љ–Њ–≥–Њ–ї–µ—В–љ–µ–≥–Њ –љ–µ–њ—А–µ—А—Л–≤–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Э–Я–Т–Я, –њ–Њ –і–∞–љ–љ—Л–Љ –њ–∞—В–Њ–ї–Њ–≥–Њ–∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —З–∞—Б—В–Њ—В–∞ –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ–Њ–≥–Њ –љ–µ—Д—А–Є—В–∞ –і–Њ—Б—В–Є–≥–∞–µ—В 100%. –§–µ—А–Љ–µ–љ—В –¶–Ю–У–2 –≤ –Є–љ—В–µ—А—Б—В–Є—Ж–Є–Є –њ–Њ—З–µ–Ї –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В, –њ–Њ—Н—В–Њ–Љ—Г –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –¶–Ю–У–2 –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –љ–µ –≤–ї–Є—П–µ—В –љ–∞ —Г—А–Њ–≤–µ–љ—М –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є. –≠—В–Є –і–∞–љ–љ—Л–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л –≤ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, —Б—А–∞–≤–љ–Є–≤—И–µ–Љ –≤–ї–Є—П–љ–Є–µ –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ (400–800 –Љ–≥/—Б—Г—В.) –Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–∞ (1000 –Љ–≥/—Б—Г—В.) –љ–∞ —Г—А–Њ–≤–µ–љ—М –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є —Г –ї–Є—Ж —Б—В–∞—А—И–µ 65 –ї–µ—В. –Я–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Є–µ–Љ –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї—Б—П –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є, –∞ –њ—А–Є–µ–Љ –љ–∞–њ—А–Њ–Ї—Б–µ–љ–∞ –њ—А–Є–≤–µ–ї –Ї –µ–µ —Б–љ–Є–ґ–µ–љ–Є—О —З–µ—А–µ–Ј 6 –і–љ–µ–є –њ—А–Є–µ–Љ–∞. –Ш—Б—Е–Њ–і—П –Є–Ј —Н—В–Є—Е –і–∞–љ–љ—Л—Е —Б–ї–µ–і—Г–µ—В, —З—В–Њ –¶–µ–ї–µ–±—А–µ–Ї—Б –Љ—Л –Љ–Њ–ґ–µ–Љ –њ—А–Є–Љ–µ–љ—П—В—М –њ—А–Є –•–Я–Э 1–2 —Б—В–µ–њ–µ–љ–Є –≤ –љ–µ–Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е —Б—Г—В–Њ—З–љ—Л—Е –і–Њ–Ј–Є—А–Њ–≤–Ї–∞—Е, —В—А–µ–±—Г–µ–Љ—Л—Е –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞.
3. –Э–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я –≤–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е –Њ–Ї–∞–Ј—Л–≤–∞—О—В –љ–µ–≥–∞—В–Є–≤–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –њ–µ—З–µ–љ–Є (–Њ—Б–Њ–±–µ–љ–љ–Њ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї). –Т–ї–Є—П–љ–Є–µ —Б–њ–µ—Ж–Є—Д–Є—З–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –љ–∞ –њ–µ—З–µ–љ—М —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ —Б –њ–ї–∞—Ж–µ–±–Њ.
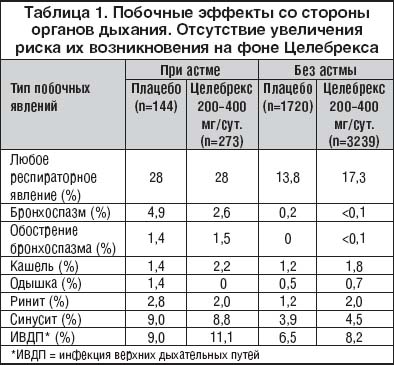
4. –Ю—Б–Њ–±—Л–µ —Б–ї–Њ–ґ–љ–Њ—Б—В–Є –≤—Л–Ј—Л–≤–∞–µ—В –ї–µ—З–µ–љ–Є–µ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –¶–Ю–У –±–Њ–ї—М–љ—Л—Е, –Є–Љ–µ—О—Й–Є—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±—А–Њ–љ—Е–Њ–≤, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –±–Њ–ї—М–љ—Л—Е —Б –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є. –†–µ–≥—Г–ї—П—Ж–Є—П –њ—А–Њ—Б–≤–µ—В–∞ –±—А–Њ–љ—Е–Њ–≤ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞–Љ–Є, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ—Л–Љ–Є –¶–Ю–У–1, –њ–Њ—Н—В–Њ–Љ—Г –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —Н—В–Њ–є –Є–Ј–Њ—Д–Њ—А–Љ—Л –¶–Ю–У –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ–∞–Љ –Є–ї–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—О —В–µ—З–µ–љ–Є—П –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ—Л (—Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–∞ –Њ—Б–Њ–±–∞—П —Д–Њ—А–Љ–∞ –∞—Б—В–Љ—Л – «–∞—Б–њ–Є—А–Є–љ–Њ–≤–∞—П –∞—Б—В–Љ–∞»). –Т —В–∞–±–ї–Є—Ж–µ 1 –њ—А–Є–≤–µ–і–µ–љ—Л –і–∞–љ–љ—Л–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ —З–∞—Б—В–Њ—В–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –љ–∞ —Д–Њ–љ–µ –¶–µ–ї–µ–±—А–µ–Ї—Б–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є. –Ш–Ј –і–∞–љ–љ—Л—Е —В–∞–±–ї–Є—Ж—Л –≤–Є–і–љ–∞ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –і–ї—П –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е.
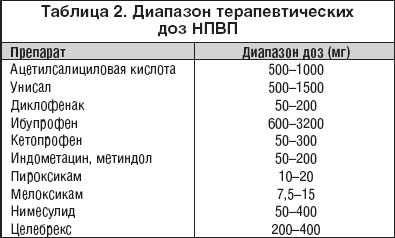
5. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї—О–±–Њ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ (–Є –Э–Я–Т–Я –љ–µ —П–≤–ї—П—О—В—Б—П –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ) –Ј–∞–≤–Є—Б–Є—В –Њ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј (—В–∞–±–ї. 2). –Ш–Ј –Є—Б—В–Њ—А–Є–Є –≤–љ–µ–і—А–µ–љ–Є—П –Э–Я–Т–Я —Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–µ–љ —Д–∞–Ї—В, —З—В–Њ –≤ 70––µ –≥–Њ–і—Л –њ—А–Њ—И–ї–Њ–≥–Њ —Б—В–Њ–ї–µ—В–Є—П, –Ї–Њ–≥–і–∞ –Ј–∞–Ї–Њ–љ—З–Є–ї–Є—Б—М –њ–µ—А–≤—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П –Є–±—Г–њ—А–Њ—Д–µ–љ–∞, —Н—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –±—Л–ї –њ—А–Є–Ј–љ–∞–љ –Ї–∞–Ї —Б—А–µ–і—Б—В–≤–Њ, –Є–Љ–µ—О—Й–µ–µ —В–Њ–ї—М–Ї–Њ –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Є–є –Є –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В, —В.–Ї. –њ—А–Є–Љ–µ–љ—П–ї—Б—П –≤ —Б—Г—В–Њ—З–љ—Л—Е –і–Њ–Ј–∞—Е 600 –Љ–≥. –Ю—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–Љ —Г—З–µ–љ—Л–Љ [–Ы.–Э. –Ф–µ–љ–Є—Б–Њ–≤, –Т.–Р. –Э–∞—Б–Њ–љ–Њ–≤–∞, –Р.–Р. –Ъ—А–µ–ї—М] –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –њ—А–Є–Њ—А–Є—В–µ—В –≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Є–±—Г–њ—А–Њ—Д–µ–љ–∞. –Ш–Љ–Є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–∞—П —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞, –і–∞—О—Й–∞—П –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В, —Б–Њ—Б—В–∞–≤–ї—П–µ—В 1200 –Љ–≥. –° —Н—В–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –Є –њ–Њ —Б–µ–є –і–µ–љ—М –Є–±—Г–њ—А–Њ—Д–µ–љ —И–Є—А–Њ–Ї–Њ –Є —Б —Г—Б–њ–µ—Е–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ. –≠—В–Њ—В –њ–Њ–і—Е–Њ–і —В–∞–Ї–ґ–µ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б—Г—В–Њ—З–љ—Л—Е –і–Њ–Ј —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2. –Т –њ—А–µ–і—Л–і—Г—Й–Є—Е –љ–∞—И–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [14,15] –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —З–Є—Б–ї–Њ –Њ—В–≤–µ—В—З–Є–Ї–Њ–≤ –љ–∞ –¶–µ–ї–µ–±—А–µ–Ї—Б –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П (—Б 70 –і–Њ 93%) –њ—А–Є –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–Љ –њ–Њ–і–±–Њ—А–µ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л –≤ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –і–Є–∞–њ–∞–Ј–Њ–љ–µ. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –≤—А–∞—З–µ–є –љ–µ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –і–Њ–Ј—Л –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –±–Њ–ї–µ–µ 200 –Љ–≥ –≤ —Б—Г—В–Ї–Є, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Є –Ї –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Н—Д—Д–µ–Ї—В–∞ —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б—Г—Б—В–∞–≤–Њ–≤ –Є —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Х—Б—В–µ—Б—В–≤–µ–љ–љ–Њ, —З—В–Њ –њ—А–Є –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–µ (–Ю–Р) –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –Э–Я–Т–Я. –° —Г—З–µ—В–Њ–Љ –Њ–њ–Є—Б–∞–љ–љ–Њ–≥–Њ –≤—Л—И–µ –і–Њ–Ј–∞–Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П —А–µ–∞–Ї—Ж–Є–є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ–±–Є—В—М—Б—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П —А–Є—Б–Ї/–њ–Њ–ї—М–Ј–∞.
6. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є —Б—Г—Б—В–∞–≤–Њ–≤ (–Ю–Р –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б—Г—Б—В–∞–≤–Њ–≤ –Є–ї–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞) —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –≤—Б–µ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ –≤–ї–Є—П—О—В –љ–∞ —Е—А—П—Й [16,17,18] –Є —Г—В—П–ґ–µ–ї—П—О—В —В–µ—З–µ–љ–Є–µ –∞—А—В—А–Њ–Ј–∞. –Ш–Љ–µ–љ–љ–Њ –њ–Њ—Н—В–Њ–Љ—Г –≤ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–є –∞–љ—В–Є—А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –ї–Є–≥–Є –Є–Љ–µ—О—В—Б—П —Г–Ї–∞–Ј–∞–љ–Є—П, —З—В–Њ –љ–∞—З–Є–љ–∞—В—М –ї–µ—З–µ–љ–Є–µ –Ю–Р —Б–ї–µ–і—Г–µ—В —Б –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–і—Б—В–≤, –∞ –Э–Я–Т–Я —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М –Ї–Њ—А–Њ—В–Ї–Є–Љ–Є –Ї—Г—А—Б–∞–Љ–Є –Є –≤ –љ–Є–Ј–Ї–Є—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е. –Ю–і–љ–∞–Ї–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Г —А—П–і–∞ –±–Њ–ї—М–љ—Л—Е –Ю–Р –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –њ—А–Њ—В–µ–Ї–∞–µ—В —Б —Г–њ–Њ—А–љ—Л–Љ –±–Њ–ї–µ–≤—Л–Љ –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—П –њ–Њ—З—В–Є –њ–Њ—Б—В–Њ—П–љ–љ—Г—О –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –Э–Я–Т–Я. –Ф–ї—П —Н—В–Њ–є –Ї–Њ–≥–Њ—А—В—Л –±–Њ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ —П–≤–ї—П—О—В—Б—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –Є–Љ–µ—О—В –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —Е—А—П—Й, –∞ –і–ї—П –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –і–∞–ґ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –∞–Ї—В–Є–≤–љ—Л—Е –≥–ї–Є–Ї–Њ–Ј–∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–∞–љ–Њ–≤ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —В–µ—З–µ–љ–Є–µ –Ю–Р –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –≤ 2––ї–µ—В–љ–µ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є TRIAL, –њ–Њ–Ї–∞–Ј–∞–≤—И–µ–Љ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–µ (–∞ –њ–Њ —А—П–і—Г –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –і–∞–ґ–µ –њ—А–µ–≤—Л—И–∞—О—Й–µ–µ) –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –±–Њ–ї—М, —Б–Ї–Њ–≤–∞–љ–љ–Њ—Б—В—М, —П–≤–ї–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є —Д—Г–љ–Ї—Ж–Є—О –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥–ї—О–Ї–Њ–Ј–∞–Љ–Є–љ–Њ–Љ, —Е–Њ–љ–і—А–Њ–Є—В–Є–љ —Б—Г–ї—М—Д–∞—В–Њ–Љ –Є –Є—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є [19].
7. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –¶–Ю–У–2 —Г—З–∞—Б—В–≤—Г–µ—В –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Њ—Б—В–µ–Њ–Ї–ї–∞—Б—В–Њ–≤, —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л –Є –≤ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е, –Є–Љ–µ—О—Й–Є—Е –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј –Є–ї–Є —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –µ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П.
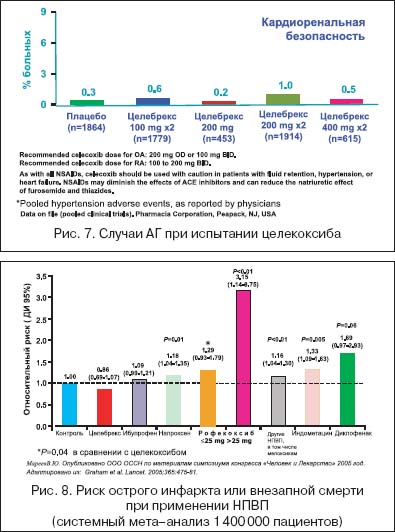
8. –Ю—Б–Њ–±–µ–љ–љ–Њ —З–∞—Б—В—Л –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є –±–Њ–ї–µ–Ј–љ–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П. –°—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Њ–њ–Њ—А–љ–Њ––і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П —А–µ–≥–Є—Б—В—А–Є—А—Г–µ—В—Б—П –±–Њ–ї–µ–µ —З–µ–Љ 1/3 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У, —В–Њ –µ—Б—В—М –≤—Б–µ –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–µ –Э–Я–Т–Я, —Б–њ–Њ—Б–Њ–±–љ—Л –њ–Њ–≤—Л—И–∞—В—М –Р–Ф –≤—Б–ї–µ–і—Б—В–≤–Є–µ –≤–ї–Є—П–љ–Є—П –љ–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ—Л –њ–Њ—З–µ–Ї –Є —Б–љ–Є–ґ–∞—О—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤: b––±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤, –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, –і–Є—Г—А–µ—В–Є–Ї–Њ–≤ (–Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –°–∞––Ї–∞–љ–∞–ї–Њ–≤) [20,21]. –Т –Њ—В–ї–Є—З–Є–µ –Њ—В –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 –љ–µ –≤–ї–Є—П—О—В –љ–∞ –Р–Ф –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф. –Э–∞ —А–Є—Б—Г–љ–Ї–µ 7 –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —З–∞—Б—В–Њ—В–∞ –њ–Њ–≤—Л—И–µ–љ–Є—П –Р–Ф –њ—А–Є –њ—А–Є–µ–Љ–µ –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –Њ–і–Є–љ–∞–Ї–Њ–≤–∞ —Б —В–∞–Ї–Њ–≤–Њ–є –љ–∞ —Д–Њ–љ–µ –њ–ї–∞—Ж–µ–±–Њ, –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В —Б–≤—П–Ј—М –њ–Њ–≤—Л—И–µ–љ–Є—П –Р–Ф —Б —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–Њ–є –њ—А–µ–њ–∞—А–∞—В–∞, –Ї–Њ—В–Њ—А–∞—П –≤ –і–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤–і–≤–Њ–µ –њ—А–µ–≤—Л—И–∞–ї–∞ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Г—О –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–љ—Г—О. –Ю—Ж–µ–љ–µ–љ–Њ –±—Л–ї–Њ –Є –≤–ї–Є—П–љ–Є–µ –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –љ–∞ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞ [22]: –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –¶–µ–ї–µ–±—А–µ–Ї—Б–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ –і–∞–љ–љ—Л–Љ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞, –≤–Ї–ї—О—З–Є–≤—И–µ–≥–Њ 1400000 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –Њ—Б—В—А–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ю–Ш–Ь) –Є–ї–Є –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–Љ–µ—А—В–Є (—А–Є—Б. 8). –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є–ї–Є –њ—А–Є —А–Є—Б–Ї–µ –Є—Е –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤—А–∞—З –і–Њ–ї–ґ–µ–љ –њ—А–Њ–≤–Њ–і–Є—В—М —Н–ї–µ–Љ–µ–љ—В–∞—А–љ—Л–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—А–Њ–њ—А–Є—П—В–Є—П: –Ї–Њ–љ—В—А–Њ–ї—М –Р–Ф, –≠–Ъ–У —Б –Ї–Њ—А—А–µ–Ї—Ж–Є–µ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –Э–Я–Т–Я –Ј–∞–≤–Є—Б–Є—В –Њ—В –≤–Ј–≤–µ—И–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є –Є –≤—Л–±–Њ—А–∞ —Б—А–µ–і—Б—В–≤ —Б –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ –ї—Г—З—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј –≤ –Ї–∞–ґ–і–Њ–Љ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–Љ —Б–ї—Г—З–∞–µ, –∞ —В–∞–Ї–ґ–µ –Њ—В —В—Й–∞—В–µ–ї—М–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞, —В–∞–Ї –Є –µ–≥–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є. –Ю—Б–Њ–±–µ–љ–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П –Ј–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В —Д–∞–Ї—В –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —В–µ—З–µ–љ–Є–µ –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞ –Є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–∞ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–1 –Є –¶–Ю–У–2. –°–ї–µ–і—Г–µ—В —В–∞–Ї–ґ–µ —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –Є–љ–і–Њ–ї—Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ, –Љ–µ—В–Є–љ–і–Њ–ї) –Є –Њ–Ї—Б–Є–Ї–∞–Љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ), –і–∞–ґ–µ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Љ–Њ–ї–Њ–і—Л–Љ –±–Њ–ї—М–љ—Л–Љ –±–µ–Ј —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —В—П–ґ–µ–ї—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Љ–Њ–≥—Г—В —В–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤—Л–Ј–≤–∞—В—М —Б–µ—А—М–µ–Ј–љ—Л–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Ц–Ъ–Ґ, –≤–њ–ї–Њ—В—М –і–Њ –ї–µ—В–∞–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ [23].

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. “–Э–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л”. –Ь–Њ—Б–Ї–≤–∞, 2000
2. –Х. –Э–∞—Б–Њ–љ–Њ–≤ «–С–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –њ—А–Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Њ–њ–Њ—А–љ–Њ––і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞» –Т—А–∞—З, 2002, вДЦ4, 15–19
3. Scott D. «Text book of rheumatology» 1999
4. Katz W.A. Pain management in rheumatologic disorders. A guide for Clinicians. Drugsmart Publ. 2000;1.
5. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –§–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –±–Њ–ї–Є: –≤–Ј–≥–ї—П–і —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–∞. –Ъ–Њ–љ—Б–Є–ї–Є—Г–Љ 2000
6. Lapane K.l., J.J. Spooner and D. Pettiti “The effect of nonsteroidal anti–inflammatory drugs on the use of gastroprotective medication in people with arthritis.” Am. J. Manag. Care, 2001, V.7: 402–408
7. –Ы.–С. –Ы–∞–Ј–µ–±–љ–Є–Ї, –Т.–Э. –Ф—А–Њ–Ј–і–Њ–≤, –Х.–Т. –Ъ–Њ–ї–Њ–Љ–Є–µ—Ж «–°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–∞, –ї–Њ—А–љ–Њ–Ї—Б–Є–Ї–∞–Љ–∞, –љ–Є–Љ–µ—Б—Г–ї–Є–і–∞ –Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ —Г –±–Њ–ї—М–љ—Л—Е –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–Њ–Љ.» –†–Ь–Ц, 2004, —В–Њ–Љ 12, вДЦ 14, 844–847
8. Feldman M., McMahon A.T. Do cyclooxigenase–2 inhibitors provide benefits similar to those of traditional nonsteroidal anti–inflammatory drugs, with less gastrointestinal toxicity? Ann. Intern. Med. 2000; 132:134–143
9. Armstrong C.P., Blower A.L. “Non–steroidal anti–inflammatory drugs and life threatening complication of peptic ulceration.” Gut., 1987, 28: 527–532
10. Singh G., Ramey D.R., Morfield D. et.al. “Gastrointestinal tract complications on nonsteroidal anti–inflammatory drug treatment in rheumatoid arthritis.” Arch. Intern. Med., 1996, 156: 1530–1536
11. –Р.–Х. –Ъ–∞—А–∞—В–µ–µ–≤, –Э.–Э. –Ъ–Њ–љ–Њ–≤–∞–ї–Њ–≤–∞, –Р.–Р. –Ы–Є—В–Њ–≤—З–µ–љ–Ї–Њ –Є –і—А. « –Э–Я–Т–Я––∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –њ—А–Є —А–µ–≤–Љ–∞—В–Є–Ј–Љ–µ –≤ –†–Њ—Б—Б–Є–Є.» –Ъ–ї–Є–љ. –Ь–µ–і., 2005, вДЦ%, 33–38
12. F.E. Silverstein, G. Faoch, J.L. Goldstein et.al. “Gastrointestinal toxicity with Celecoxib vs nonsteroidal anti–inflammatory drugs for osteoarthritis and rheumatoid arthritis. The CLASS study: a randomized controlled trial” JAMA, 2000, Vol. 284, вДЦ10, 1247–1255
13. Goldstein. Data presented at Digestive Disease Week (DDW)
New Orleans, LA, USA, 15–20 May 2004.
14. –Э.–Т. –І–Є—З–∞—Б–Њ–≤–∞ «–Ы–µ—З–µ–љ–Є–µ —Е—А–Њ–љ–Є—З–µ–Ї—Б–Ї–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є» –Ы–µ—З–∞—Й–Є–є –≤—А–∞—З, —П–љ–≤–∞—А—М 2003 –≥., вДЦ1, —Б—В—А.16–19
15. –Э.–Т. –І–Є—З–∞—Б–Њ–≤–∞, –У.–†. –Ш–Љ–∞–Љ–µ—В–і–Є–љ–Њ–≤–∞, –Х.–Ы. –Э–∞—Б–Њ–љ–Њ–≤ «–Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 —Г –±–Њ–ї—М–љ—Л—Е —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б—Г—Б—В–∞–≤–Њ–≤ –Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є» –Э–∞—Г—З–љ–Њ––њ—А–∞–Ї—В–Є—З–µ—Б–Ї–∞—П —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П, 2004, вДЦ2, —Б—В—А. 37–40
16. Haskinsson E.C., Berry H., Gishen P. et.al. “Effects of anti–inflammatory drugs on the progression of osteoarthritis of the knee” J. Rheum., 1995, 22: 1941–1946
17. Rashad S., Revell P., Hemingway A. et.al. “Effect of non–steroidal anti–inflammatory drugs on the course of osteoarthritis.” Lancet, 1989, i: 519–522
18. –Э.–Т. –І–Є—З–∞—Б–Њ–≤–∞ «–Ы–µ—З–µ–љ–Є–µ –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞: –≤–ї–Є—П–љ–Є–µ –љ–∞ —Е—А—П—Й–µ–≤—Г—О —В–Ї–∞–љ—М —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤» –†–Ь–Ц, 2005, —В–Њ–Љ 13, вДЦ8, 539–542
19. D.O.Clegg, D.J.Reda, C.L.Harris et.al. “Glucosamin, chondroitin sulfate, and the two in combination for painful knee osteoarthritis” N.Engl.J.Med., 2006, V.354:795–808
20. Ruoff G. Management of pain in patients with multiple health problems: a guide for the practicing physician. Amer. J. Med., 1998; 105 (1B):53S–60S
21. –Ь–∞—А–µ–µ–≤ –Т.–Ѓ. «–†–µ–∞–ї—М–љ–∞ –ї–Є –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤?» –°–µ—А–і—Ж–µ, —В–Њ–Љ 2, вДЦ4, 1–6
22. W.B.White, J.Kent, A.Taylor et.al. “Effect of Celecoxib on ambulatory blood pressure in hypertensive patientson ACE inhibitors” Hypertension, 2002, V.39: 929–934
23. –Т.–Э. –°–Њ—А–Њ—Ж–Ї–∞—П, –Р.–Х. –Ъ–∞—А–∞—В–µ–µ–≤ «–Ц–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Ї–∞–Ї –Њ–і–љ–∞ –Є–Ј –њ—А–Є—З–Є–љ —Б–Љ–µ—А—В–Є –±–Њ–ї—М–љ—Л—Е —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є» –Э–∞—Г—З–љ–Њ––њ—А–∞–Ї—В–Є—З–µ—Б–Ї–∞—П —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П, 2005, вДЦ4, 34–37












