Российским пациентам и врачам общей практики более привычен термин «остеохондроз» (М42 по МКБ-10) как причина болей в спине. В российской статистической отчетности по ревматологии отдельного учета синдромов болей в спине не отражено, а количество больных с остеоартрозом всех локализаций на 2013 г. составило более 4 млн [3]. Между тем Национальное руководство по ревматологии [4] выделяет главу, посвященную синдрому болей в нижней части спины (БНС) (М 54.5 по МКБ-10) как регистрационной категории с высокой распространенностью и частой невозможностью уточнения конкретной нозологической причины боли. Введено понятие «дорсопатия», под которым понимают болевой синдром в области туловища и конечностей, связанный с дегенеративными заболеваниями позвоночника, но не с патологией внутренних органов. Дорсопатии – широкое понятие, объединяющее поражения собственно позвоночника и мышечно-связочных структур спины. В 1987 г. G. Waddell сформулирована диагностическая триада болей в спине (цит. по: Н.А. Шостак, Н.Г. Правдюк, 2011), разделяющая их на 1) неспецифическую (механическую) патологию; 2) специфическую патологию; 3) радикулопатии [5]. Структура триады представлена на рисунке 1.

Наиболее распространенный первичный механический синдром может быть обусловлен дегенеративными и функциональными изменениями межпозвонковых дисков, фасций, мышц, сухожилий, связок, дугоотросчатых суставов. Остеоартроз последних (спондилоартроз, фасет-синдром, фасеточная артропатия) играет важнейшую роль в формировании хронической боли в спине – от 5 до 40% случаев в зависимости от диагностических критериев [6, 7]. Первичный спондилоартроз занимает 2-е место среди причин нарушения трудоспособности людей старше 50 лет [8].
Межпозвонковые суставы представляют собой классические синовиальные суставы с поверхностями, покрытыми суставным гиалиновым хрящом, с суставной капсулой, ограничивающей содержащуюся в их полости синовиальную жидкость [5]. Экспериментальная модель дегенеративного поражения фасеточных суставов поясничного отдела позвоночника у крыс создана традиционно – путем введения в них полного адъюванта Фрейнда. Помимо макроскопического соответствия остеоартриту и гистологического балльного счета OARSI (рекомендации Международного научного общества по изучению остеоартроза) получено повышение уровня ИЛ-1- и фактора некроза опухоли (ФНО)- в синовиальной оболочке этих суставов, что подтверждает единство патогенеза фасеточной артропатии и остеоартрита других локализаций [9]. Дегенеративные изменения позвоночника могут развиваться уже с 25–30 лет, что может быть связано с врожденными аномалиями позвоночника (люмбализация, сакрализация), гипермобильностью позвоночных сегментов, травматизацией, избыточным передним наклоном таза из-за генетических и поведенческих особенностей [10–12].
Диагностика фасеточной артропатии первоначально предполагает клинико-анамнестическое дифференцирование характерного для нее артропатического синдрома от синдрома сегментарной нестабильности, мышечно-тонического и миофасциального болевого синдрома (табл. 1).

На основе доказательств, базирующихся на большом количестве эпидемиологических и клинических данных, предложен комплексный интервенционный алгоритм ведения пациента с болью в спине. Так, при хронической БНС после оценки анамнеза и клинического обследования рекомендуется выполнение блокады фасеточного сустава либо эпидуральной, либо крестцово-подвздошной инъекции местного анестетика с (или без) ГК. При отсутствии эффекта от первой манипуляции рекомендуется выполнение следующей, причем при неудаче и эпидуральной, и крестцово-подвздошной интервенции вторым шагом предлагается блокада дугоотросчатого сустава. При хронической торакальной или цервикальной боли алгоритм предполагает выбор между фасеточной и эпидуральной блокадой. Подчеркивается важность тщательной оценки клинических, анамнестических, психосоциальных сведений для исключения противопоказаний к применению интервенционного алгоритма. Предпочтителен 2-недельный интервал между диагностическими инъекциями [13]. Интервенционный алгоритм выполним в условиях доступности высококвалифицированной медицинской помощи.
Внедрение в практику МСКТ сделало доступной визуализацию дугоотросчатых суставов, которая была затруднительна при стандартной рентгенографии. Представляем серию томограмм (рис. 2 и 3), демонстрирующих различные стадии спондилоартроза.
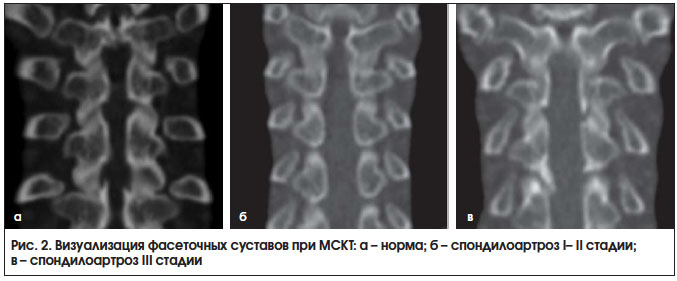
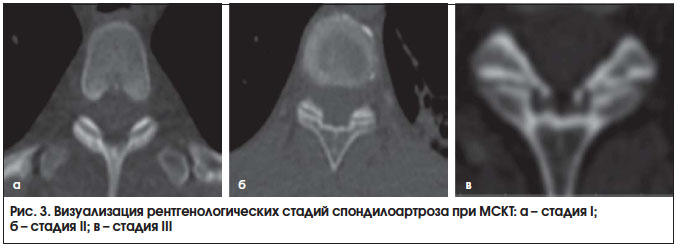
Начальные проявления фасеточной артропатии заключаются в незначительном сужении суставных щелей, склерозировании суставных поверхностей, появлении единичных мелких остеофитов. Артропатия II стадии характеризуется сужением и деформацией суставной щели, выраженным остеосклерозом и остеофитозом. При артропатии III стадии определяются резкое сужение и деформация суставных щелей, остеосклероз с выраженным остеофитозом, деформирующим позвоночный канал.
Лечение фасеточной артропатии является комплексной мультидисциплинарной проблемой. Назначение НПВП относится к первому ряду терапевтических мероприятий при болях в спине. Как показывают результаты многочисленных контролируемых исследований, отсутствуют убедительные данные о преимуществах какого-либо отдельного препарата данной группы для купирования болевого синдрома в спине. НПВП назначаются с момента развития клинических симптомов (с 1–2 сут от начала болевого синдрома). Рекомендуется начинать с более безопасных препаратов короткого действия в минимально эффективной дозе [14]. НПВП различаются по своей селективности в отношении циклооксигеназы 2-го типа (ЦОГ-2): неселективные (н-НПВП), селективные и высокоселективные (или специфические ЦОГ-2 ингибиторы) – так называемые коксибы. Блокада ЦОГ-1 (свойственная н-НПВП) приводит к существенному повышению риска развития серьезной, угрожающей жизни патологии желудочно-кишечного тракта (ЖКТ): НПВП-гастропатии и НПВП-энтеропатии. В этом плане коксибы значительно менее опасны. Селективное подавление ЦОГ-2 (без влияния на ЦОГ-1) может приводить к дисбалансу синтеза тромбоксана А2 и простациклина, что повышает риск сосудистого тромбоза и развития кардиоваскулярных катастроф. В клинической практике наиболее целесообразно рекомендовать коксибы относительно молодым пациентам без клинически выраженной патологии сердечно-сосудистой системы (ССС), имеющим факторы риска НПВП-гастропатии и/или диспепсию, нуждающимся в относительно кратковременном лечении боли. Неселективные НПВП (кроме кеторолака, пригодного лишь для очень кратковременного приема) целесообразно применять у пациентов старшей возрастной группы с умеренным кардиоваскулярным риском, но без существенных факторов риска НПВП-гастропатии. В большинстве случаев эти препараты могут быть использованы лишь в комбинации с мощными гастропротекторами, предпочтительно с ингибиторами протонной помпы [15, 16]. В практической деятельности лорноксикам с более коротким периодом полувыведения (3–4 ч) ) зарекомендовал себя лучше, чем другие оксикамы. Обладая способностью к сбалансированному ингибированию ЦОГ-1 и ЦОГ-2, лорноксикам проявляет выраженную анальгетическую и противовоспалительную активность в сочетании с низким риском развития нежелательных явлений [10, 17]. Подгруппа селективных НПВП, занимающих «промежуточное» положение между неселективными и специфическими, представлена нимесулидом и мелоксикамом. Оба препарата заняли свою терапевтическую нишу в лечении больных остеоартрозом, в т. ч. пациентов с болью в спине [16, 18–20].
В исследовании сравнительной эффективности эторикоксиба в дозе 60 мг/сут и диклофенака в дозе 150 мг/сут при лечении пациентов с хронической болью в спине в течение 4 нед. отмечено, что эторикоксиб сопоставим по анальгетическому эффекту с диклофенаком [21]. Применение эторикоксиба в течение 3 мес. приводило к статически значимомому снижению интенсивности боли и уменьшению ограничений движений по сравнению с таковыми при применении плацебо. Исследование по сравнению эффективности эторикоксиба в дозе 60 и 90 мг/сут не выявило преимуществ большей дозы препарата в этой популяции пациентов [22].
Различие между НПВП связано с их безопасностью, и это различие весьма существенно [16]. При длительном применении НПВП возрастает риск побочных явлений, в первую очередь желудочно-кишечных и кардиоваскулярных осложнений. Поэтому необходимо применять их недолго и с учетом индивидуальных особенностей пациента. Длительность применения НПВП при хронической боли в спине в клинических рекомендациях четко не оговаривается.
Европейское общество по клиническим и экономическим аспектам остеопороза и остеоартроза (ESCEO) предлагает алгоритм ведения больных остеоартрозом, в котором подчеркивается осторожный подход к применению НПВП и эффективность медленнодействующих средств: хондроитина сульфата (ХС) и глюкозамина (ГА). При этом эксперты считают, что хондропротекторы следует назначать уже на первых этапах лечения ОА, а НПВП – в случае недостаточного симптом-модифицирующего действия ХС и ГА [23].
ХС и ГА являются естественными хондропротекторами. ГА необходим для биосинтеза таких соединений, как гликолипиды, гликопротеины, гликозаминогликаны, гиалуронат и протеогликаны, ХС – для формирования протеогликанов суставного хряща [24]. Совместное применение ХС и ГА гидрохлорида (ГАХ) увеличивает продукцию гликозаминогликанов хондроцитами на 96,6% по сравнению с 32% при монотерапии [25]. Комбинацию ХС (400 мг) и ГАХ (500 мг) содержит лекарственный препарат для перорального приема Терафлекс, для старта терапии предложено сочетание ХС 200 мг, ГАХ 250 мг и низкой дозы относительно безопасного н-НПВП ибупрофена 100 мг (Терафлекс Адванс). В экспериментальном исследовании сочетание ГА и ибупрофена расценено как синергическое. Для достижения адекватного обезболивающего эффекта больным ОА требуется в 2,4 раза меньшая доза ибупрофена [26]. Терафлекс Адванс рекомендуют в начале терапии по 2 капсулы 2 р./сут в течение 3 нед. с последующим переходом на Терафлекс [27, 28]. Согласно прогностической модели, максимальный эффект Терафлекса следует ожидать на начальных этапах поражения суставного аппарата позвоночника, особенно при наличии симптомов, подозрительных в отношении фасеточного синдрома [29].
Открытое рандомизированное клиническое исследование с целью оценки симптом-модифицирующего эффекта препарата Терафлекс, его переносимости и длительности последействия, проведено у 60 больных ОА коленных суставов и спондилоартрозом позвоночника в течение 6-месячного периода наблюдения. В первой группе пациенты получали Терафлекс по 1 капсуле 2 р./сут в течение 1-го мес., затем по 1 капсуле 1 р./сут еще 2 мес. в сочетании с диклофенаком в дозе 75 мг/сут, во 2-й – диклофенак в суточной дозе 75 мг. Через 1 мес. уменьшение боли при приеме Терафлекса соответствовало наблюдаемому при приеме диклофенака, причем данный эффект сохранялся на протяжении всего срока наблюдения [25, 30].
Имеются данные о высокой эффективности препарата Терафлекс в лечении вертеброгенных синдромов, обусловленных дегенеративно-дистрофическими изменениями в позвоночнике. Проведено клиническое наблюдение за 30 больными с рефлекторными и компрессионными синдромами спондилоартроза (средний возраст – 49 лет). 18 пациентов получали комплексную терапию, включающую Терафлекс, НПВП, витамины, сосудистые препараты, физиолечение, 12 – только Терафлекс. Значительное улучшение состояния с купированием болевого синдрома и положительной неврологической симптоматикой зарегистрировано у 28 человек. Высокая эффективность монотерапии Терафлексом отмечена у 9 пациентов. Переносимость препарата расценена как хорошая у 27 больных, у 1 пациента появились диспептические расстройства, у 1 – незначительное головокружение, у 1 больного препарат был отменен из-за выраженного головокружения [31].
40 пациентам (средний возраст – 48,5 года) с дегенеративно-дистрофическими заболеваниями шейного, грудного и поясничного отделов позвоночника, сопровождавшимися острой и хронической болью разной интенсивности, назначался Терафлекс. Значительное улучшение состояния (в частности, купирование боли и положительная динамика неврологической симптоматики) достигнуто у 75% пролеченных, преимущественно молодого возраста. У 20% уменьшалась интенсивность болевого синдрома, эффект отсутствовал только в 5% случаев. Восстановление объема движений соответствовало редукции болевого синдрома. Переносимость препарата у всех больных была хорошей [32].
В настоящее время доказана эффективность сочетания ХС и ГС в дозировке 1200 мг/сут и 1500 мг/ сут у больных ОА коленных суставов с выраженной болью (Western Ontario and McMaster osteoarthritis index (WOMAC) score ≥301; 0–500 scale) при длительности приема 6 мес. [33]. Параартикулярная блокада фасеточного сустава анестетиком (с или без ГК) имеет не только диагностическое значение. Инъекции в фасеточные суставы – распространенный и безопасный метод лечения боли в спине при фасеточной артропатии. В США данный способ интервенции занимает 2-е место среди всех вмешательств, выполняемых для купирования боли [34]. Как интервенционные процедуры они отличаются ничтожно малым риском развития осложнений, включая инфекционные, повреждение нервных стволов.
100 больным с установленным диагнозом «спондилоартроз» выполняли диагностические блокады дугоотросчатых суставов и провоцирование болевого синдрома введением химического раздражителя к суставам. В случаях воспроизведения характерных болевых проявлений делали спирт-новокаиновую блокаду с целью денервации (дерецепции) пораженного сустава. Отличные результаты лечения отмечены у 24% пациентов, значительное улучшение – у 65%, незначительное улучшение – у 11%. Неудовлетворительных результатов или осложнений при проведении данной процедуры не отмечено [35].
Несмотря на эффективность и надежность пункций фасеточных суставов, изредка могут встречаться осложнения при их выполнении, в т. ч. и жизнеопасные. При проведении диагностической пункции фасеточных суставов С6-С7 билатерально у мужчины 36 лет через 1–2 мин после введения местного анестетика справа появились плохое самочувствие, беспокойство, двусторонние парестезии в конечностях, грудной клетке, верхней части живота. При объективном обследовании выявлен дефицит чувствительности без двигательных нарушений, сохранявшийся 35–40 мин. Следовательно, блокады фасеточных суставов должны проводиться только при наличии готового к работе реанимационного оборудования, а персонал, проводящий интервенционные процедуры, должен быть обучен выполнению реанимационных мероприятий [34].
Для достижения большей клинической эффективности рекомендуется проводить пункции фасеточных суставов под контролем ультразвукового исследования (УЗИ). Проведенное сравнительное исследование клинической эффективности пункций фасеточных суставов «вслепую» и под контролем УЗИ [36] продемонстрировало, что время пункции было достоверно меньше (p<0,05), а интенсивность боли по ВАШ через 30 мин после введения – значимо ниже (p<0,05). Из 37 блокад фасеточных суставов под контролем УЗИ 32 были безошибочно выполнены с первой попытки, что составляет 86,5%. В то же время из 35 пункций, проведенных «вслепую», первая попытка была корректной только у 11 пациентов, что составляет 31,4%. Через 6 нед. после манипуляции ремиссия была достигнута у 72,3%, пролеченных под контролем УЗИ, и у 56,7% – без УЗ-контроля [36].
Введение ГК для лечения болей в спине остается дискутабельным вопросом. В рекомендациях 2005 г. по терапии БНС Агентства по здравоохранению и научным исследованиям США инъекции в фасеточные суставы при хронической БНС отнесены к неэффективным или даже вредным процедурам [13, 37]. Однако ряд исследований доказывают эффективность данной манипуляции у больных с поражением фасеточных суставов. Обсуждается применение разных техник введения ГК: внутрисуставного введения и блокады срединных ветвей нервных стволов [38]. При интраартикулярном введении триамцинолона и лидокаина при патологии поясничных фасеточных суставов отмечалось снижение боли и функциональной недостаточности по индексу Освестри [38]. Однако другие исследователи не рекомендуют интраартикулярные фасеточные инъекции для снижения БНС [39]. Основное преимущество параартикулярной блокады перед внутрисуставным введением лекарственных средств заключается в том, что вокруг дугоотросчатых суставов имеется большое количество ноцицептивных вегетативных образований, которые играют основную роль в формировании многообразных рефлекторных синдромов спондилоартроза [35]. Поэтому сначала должны применяться параартикулярные блокады, т. к. они более эффективны и их легче выполнить. Периартикулярные инъекции 2% лидокаина были эффективны у всех 25 больных, тогда как интраартикулярные – только у 9 из 25 [40].
Определенная роль в лечении болей в спине отводится эпидуральному введению лекарственных препаратов (анестетиков, ГК). Больным с хронической болью в спине с отсутствием или наличием патологии фасеточных суставов, радикулопатии вводили 10 мл 0,5% лидокаина или 9 мл 0,5% лидокаина в смеси с 1 мл ГК (триамцинолон 40 мг). В 1-й группе пациентов значительное снижение интенсивности боли (на 50% и более) достигнуто в 72 и 81% случаев, среднее число повторных инъекций в течение года было 3,6 и 3,9 [41]. Во 2-й группе пациентов значительное уменьшение интенсивности боли (на 50% и более) через 12 мес. продемонстрировано в 79 и 81% случаев, функциональной недостаточности по опроснику Освестри (<40%) — в 83 и 91% [42].
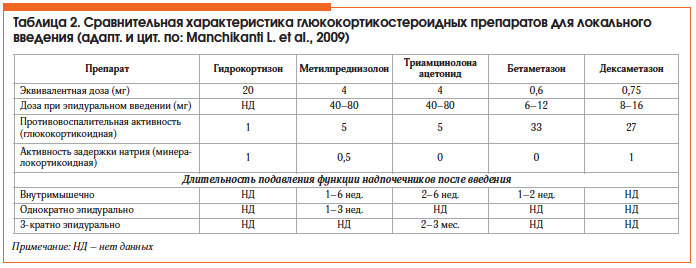
При выборе конкретного ГК для локального введения должны учитываться основные фармакологические характеристики [13], которые представлены в таблице 2.
«Золотым стандартом» лечения фасеточной суставной боли на сегодняшний день считается радиочастотная невротомия. К преимуществам методики можно отнести контролируемый размер деструкции, контроль термического воздействия за счет постоянного мониторинга нагревания и электрического сопротивления тканей на конце иглы, подтверждение правильности расположения иглы методом электростимуляции, проведение манипуляции под местной анестезией в амбулаторных условиях, короткий восстановительный период после проведения денервации, низкую частоту осложнений, возможность повторного проведения деструкции [43]. Техника процедуры, впервые описанной в 1975 г. Shealy, неоднократно усовершенствовалась. Снижение интенсивности боли, связанной с фасеточной артропатией, после выполнения радиочастотной невротомии сохраняется в течение 9–12 мес. и более [44]. Как интервенционная процедура метод радиочастотной невротомии имеет ничтожно малый риск развития осложнений, включая инфекционные и повреждение нервных волокон [45, 46]. Положительный результат методики радиочастотной денервации межпозвонковых суставов на поясничном уровне получен при лечении 124 пациентов с болью в поясничном отделе позвоночника, обусловленной фасеточным болевым синдромом. Оценка эффективности процедуры основывалась на применении шкалы оценки степени выраженности дегенеративного заболевания пояснично-крестцового отдела позвоночника, разработанной в НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН. У 80% (112 человек) установлен регресс болевого синдрома. Таким образом, в алгоритм лечения болевых синдромов, обусловленных дегенеративными изменениями поясничных фасеточных суставов, была внесена радиочастотная денервация межпозвонковых суставов в качестве хирургической методики, применяемой при неэффективности консервативной терапии [47].
Ударно-волновая терапия – неинвазивный метод лечения различных мышечно-скелетных патологий, основанный на трансдукции механической энергии, приводящей к каскаду различных биомеханических процессов в тканях. Существуют доказательства эффективности данной процедуры и у пациентов с фасеточной артропатией. У 62 пациентов с болью в люмбальных фасеточных суставах проведен сравнительный анализ эффективности ударно-волновой терапии, радиочастотной невротомии, локального введения ГК. Максимальный по длительности эффект достигнут в группе ударно-волновой терапии. Переносимость ежедневных нагрузок увеличивалась статистически сопоставимо у больных после ударно-волновой терапии и радиочастотной невротомии. Побочных эффектов и осложнений манипуляции не зарегистрировано [48].
Таким образом, анализ современного состояния проблемы фасеточной артропатии позволяет говорить о высокой распространенности данной патологии среди больных с болью в спине, повышении эффективности лечебно-диагностических процедур при комплексном междисциплинарном подходе к ведению пациентов.












