Однако существуют ссылки на публикации о нежелательных эффектах НПВП, возникавших после их местного применения, хотя, как правило, сообщается об отдельных случаях, или упоминаются отдельные НПВП [7–12]. Кроме того, со временем число лекарственных препаратов, использующихся для местного применения, увеличилось, и в итоге увеличилось число нежелательных реакций. Они отмечаются преимущественно со стороны кожи, но могут быть более генерализованными [13–16]. В некоторых странах, например, во Франции, были изменены условия применения отдельных НПВП, в частности, кетопрофена [17] вследствие сообщений о большом числе реакций фоточувствительности [18].
Поскольку реакции фоточувствительности наиболее известны именно для местно применяющихся НПВП, представляется важным установить число случаев аллергии и фотоаллергии, а также частоту применения этих препаратов. Это позволит проверить предположение об отсутствии прямой связи осложнений с использованием НПВП и о том, что определенные препараты более аллергенны. Учитывая, что диагноз аллергии и фотоаллергии обычно устанавливается в отделениях дерматологии госпиталей, было признано обоснованным проведение исследования на этом уровне оказания медицинской помощи в сопоставлении с анализом использования локальных НПВП в регионе, на который распространяется медицинская деятельность этих отделений.
Поскольку система фармаконадзора Испании (SEFV), начиная с 1982 г., собирала и регистрировала в своей базе данных все сообщения о подозреваемых неблагоприятных реакциях, имелась возможность применительно к НПВП для локального применения сопоставить частоту сообщений о реакциях контактной аллергии и использование этих препаратов, т.е. применить другой подход для проверки гипотезы о большей аллергенности некоторых НПВП.
Материалы и методы
Эти данные, собиравшиеся с 1996 по 2001 г. (включительно), изучались ретроспективно обсервационным методом. Основой являлся диагноз аллергии и/или фотоаллергии, установленный после проведения аппликационного и фотоаппликационного теста (патч–тест или фотопатч–тест) в отделениях дерматологии госпиталя de Cruces и госпиталя de Galdakao, которые обслуживают 73% популяции (828239 жителей) провинции Бискайя в Испании. Данные были получены только из историй болезни, в которых имелись положительные результаты в отношении контактной аллергии и фотоаллергии на местно применявшиеся НПВП. Использовалась следующая информация: возраст, пол и профессия пациента, локализация изменений, подозреваемые лекарственные препараты, персональный и семейный анамнез аллергии и результаты патч–теста и/или фотопатч–теста.
Для диагностики в отделениях дерматологии используются стандартные европейские наборы «True Test» [19], а также тесты с аллергенами из особых наборов, в данном случае с противовоспалительными препаратами и другими аллергенами (что зависело от истории болезни пациента). Фотопатч–тесты проводились в соответствии с методом, описанным испанской фотобиологической группой [20]. Патч–тесты проводились всем пациентам путем аппликации аллергенов из стандартного и особого наборов (избираемых на основании истории болезни) на верхнюю часть спины; аллергены закрывались гипоаллергенным пластырем. Первая оценка проводилась через 48 часов, повторная – через 96 часов [21]. Пациенты, в отношении которых имелось клиническое подозрение на фотоаллергию, также подвергались фотопатч–тесту: проводилась аппликация 2 серий аллергенов, одну из этих серий через 48 часов облучали лампой Waldmann 7001/k (10 Дж./см2; Tecnosa SA, Espluges de Llobregat, Испания), оценка обеих серий (облученной и необлученной) проводилась через 96 часов.
Помимо этого, подразделением фармаконадзора Страны басков (сеть центров испанской системы фармаконадзора, SEFV) были предоставлены данные сообщений, содержащихся во всей системе SEFV, для расчета отношения шансов сообщений (ОШС) и взаимосвязи этой величины с отношением пропорций сообщений (ОПС). Оба показателя являются индикаторами, которые используются в системах фармаконадзора для обнаружения предостерегающих признаков. В Великобритании считается, что эти признаки существуют, если величина ОПС составляет >=2, величина x2>= 4, а число сообщений, в которых выявляется анализируемая связь, >=3 [22]. В Голландии считается, что предостерегающий признак обнаруживается, если нижняя граница 95% доверительного интервала ОШС превышает 1 [23].
Сведения об использовании каждого аппликационного НПВП были получены из счетов, присылаемых в Национальную систему здравоохранения (NHS), Министерство по делам здравоохранения и потребителей и из базы данных RAEFAR (Register and Authorization of Pharmaceuticals), которая основывается на «единицах продаж», поскольку для этой группы препаратов не установлены суточные дозы (DDD), определяющиеся системой ATC/DDD (установить поддерживающую суточную дозу для аппликационных форм НПВП трудно).
Результаты
Установлено 139 случаев контактных реакций на местно применявшиеся НПВП, 56 (40,3%) случаев аллергии и 83 (59,7%) случая фотоаллергии у 101 пациента. Средний возраст пациентов составлял 48 лет (диапазон 14–99 лет), 95 (68,3%) реакций наблюдались у женщин и 44 (31,7%) у мужчин. В возрастном интервале до 14 лет отмечены 2 случая (1,4%), в интервале 15–30 лет – 31 (22,3%) случай, в интервале 31–45 лет – 30 (21,6%) случаев, в интервале 46–60 лет – 33 (23,7%) случая, в интервале 61–75 лет – 29 (20,8%) случаев и в интервале 76–99 лет – 11 (7,9%) случаев; в 3 (2,1%) случаях возраст был неизвестен.
Среди местно применявшихся НПВП наибольшее число случаев аллергии – 16 (28,6%), были связаны с применением кетопрофена. На втором месте был пироксикам – 12 случаев аллергии (в 4 из этих случаев одновременно выявлена контактная аллергия на другие НПВП: кетопрофен, напроксен, диклофенак, этофенамат и салицилаты). На третьем месте находился этофенамат (10 случаев). Затем следовали салицилаты (4 случая), диклофенак и фепрадинол (по 3 случая). Интерес вызывал единичный случай аллергии на пикетопрофен у пациента с одновременно выявленной фотоаллергией на кетопрофен.
Кетопрофен также выделялся как причина фотоаллергии (68 случаев, 81,9%). Другие НПВП были далеко позади, с ними связывались только 15 случаев, 9 – с пироксикамом, 4 – с пикетопрофеном и по одному – с фенилбутазоном и бензидамином. Среди 9 случаев фотоаллергии на пироксикам в 7 случаях определялась аллергия на тимеросал, в одном – на кетопрофен и в одном случае тестирование не проводилось. В случаях фотоаллергии на пикетопрофен у 3 пациентов установлена перекрестная реакция на кетопрофен (в 1 случае также на смесь ароматизирующих компонентов), а у четвертого пациента выявлена аллергия на смесь ароматизаторов.
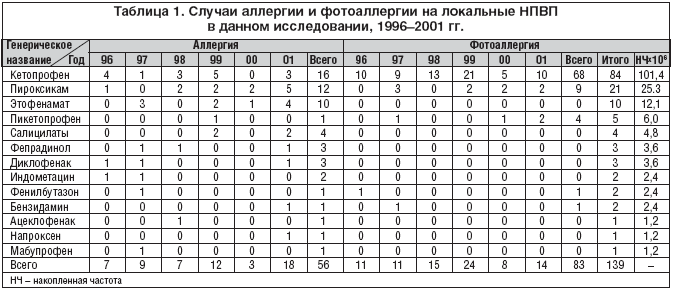
Все распределение случаев аллергии и фотоаллергии по годам (1996–2001 гг.) приведено в таблице 1, где также указана накопленная частота (НЧ) случаев для каждого НПВП в расчете на 1 млн. жителей.
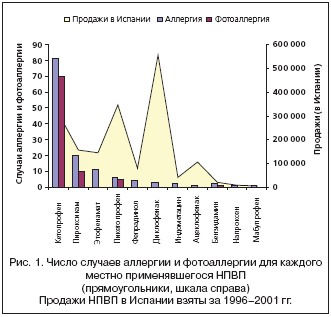
Данные об использовании различных НПВП для местного применения в течение 1996–2001 гг. показывают, что первое место по продажам занимает диклофенак (554332 единицы), намного опережая пикетопрофен (346563), кетопрофен (310095), пироксикам (156977), этофенамат (14 698), ацеклофенак (112142) и другие (Прим. ред.: данные о продажах НПВП в Испании. В России на первом месте кетопрофен (40%), на втором – диклофенак (20%) – данные RMBC, 2007). Как видно на рисунке 1, где одновременно приведены данные об использовании каждого НПВП и число случаев аллергии и фотоаллергии, для большинства аппликационных НПВП (пироксикам, этофенамат, фепрадинол, метиндол, ацеклофенак, бензидамин и напроксен) существует соответствие между частотой использования и числом случаев аллергии. Однако для некоторых широко использующихся НПВП (диклофенак и пикетопрофен) число случаев аллергии очень мало. С другой стороны, отмечается диспропорция в отношении кетопрофена, с применением которого связано большинство случаев аллергии, хотя он используется наполовину реже диклофенака и даже реже, чем пикетопрофен.
Величина ОШС для кетопрофена в отношении реакций фоточувствительности по сравнению с другими НПВП для местного применения и другими неблагоприятными реакциями (иными, чем фоточувствительность), зарегистрированными в базе данных FEDRA испанской системы фармаконадзора, составляла 3,9 (95% доверительный интервал 2,4–6,4). В то же время связь между величиной ОПС для кетопрофена и реакциями фоточувствительности по сравнению с другими аппликационными НПВП и другими неблагоприятными реакциями (иными, чем фоточувствительность) составляла 3,4 (95% доверительный интервал 2,1–5,5) (табл. 2). Обе величины превышают минимальную границу, которая рассматривается, как предостерегающий сигнал.
Обсуждение
В этом исследовании установлено, что кетопрофен среди НПВП для местного применения чаще всего вызывал контактную аллергию/фотоаллергию, что совпадает с данными других авторов [24,25]. При этом сведения о продажах (учет активного вещества) показывают, что такой не самый часто продаваемый препарат, как кетопрофен, используется на 79% реже, чем диклофенак, и на 12% реже, чем пикетопрофен, препараты, вызывавшие всего 2,1 и 3,6% контактных реакций по данным настоящего исследования.
Среди объяснений установленной диспропорции между использованием кетопрофена и числом случаев фотоаллергии, важно обратить внимание на два обстоятельства. С одной стороны, фотохимические и фотобиологические исследования местно применяющихся НПВП показывают, что наиболее фотоактивными были производные 2–арилпропионовой кислоты (напроксен, ибупрофен, кетопрофен и супрофен) [26]; действие ультрафиолетового света приводило главным образом к превращению кетопрофена в CO2 и 3–этилбензофенон, молекулу, ответственную за фотоаллергию [27–30]. С другой стороны, в данном исследовании было установлено только 5 случаев фотоаллергии на пикетопрофен (в 4 из них имелась перекрестная реакция на кетопрофен), хотя он также относится к числу НПВП aрилпропионовой группы и был получен в результате модификации бензофенона. При этом продажи пикетопрофена даже превышали продажи кетопрофена. Одним из объяснений такого низкого числа случаев фотоаллергии на пикетопрофен может быть то, что он, как и другие активные вещества арилпропионовой группы (например, ибупрофен), характеризуется очень слабым спектром поглощения, что затрудняет образование фотоактивного производного (3–этилбензофенона) [26], хотя, если это производное образуется, оно должно было бы быть одинаково фотоактивным, независимо от особенностей структуры препарата из арилпропионовой группы. Это может объяснять случаи фотоаллергии и перекрестные реакции, отмеченные как на кетопрофен, так и на пикетопрофен.
Установленное в этом исследовании совпадение фотоаллергии на пироксикам с аллергией на тимеросал (в 7 из 9 случаев) аналогично наблюдениям Vasconcelos et al. [31], которые сообщили о 10 случаях аллергии на тимеросал у 11 пациентов с фотоаллергией на пироксикам, даже если этот препарат применялся внутрь. Эти реакции, вероятно, возникают вследствие воздействия ультрафиолета А, что приводит к образованию фотоактивного соединения, обладающего перекрестной реакцией на тиосалициловую кислоту. 4 случая аллергии на пироксикам, которые характеризовались перекрестной аллергией на кетопрофен, напроксен и этофенамат, возможно, обусловлены совместной сенсибилизацией, поскольку химическая структура каждого из этих НПВП не имеет сходства с оксикамом.
Диклофенак, хотя и был самым часто продававшимся НПВП для местного применения, послужил причиной только 3 случаев аллергии и не вызывал фотоаллергии. Этот факт, как и небольшое число опубликованных подобных случаев [32], может объясняться биохимической теорией, выдвинутой Moore [26]. Он описал, что диклофенак под действием ультрафиолетового облучения теряет заместители хлора, его кольцо замыкается, и образуется карбазол–1–уксусная кислота, – вещество со слабым фототоксическим действием. При этом формируются короткоживущие свободные радикалы, которым трудно достичь биологических структур для осуществления фоточувствительной реакции.
Это исследование характеризовалось несколькими ограничениями. С одной стороны, несмотря на то, что диагноз аллергии/фотоаллергии устанавливался специалистами на основании рекомендаций Международной группы по изучению контактного дерматита (ICDRG), нельзя исключить возможность ошибочной диагностики в некоторых случаях вследствие присутствия субъективного компонента при оценке патч–теста или фотопатч–теста. Другое ограничение состоит в том, что использовавшиеся данные отражают только рецептурные препараты, применение которых финансируется национальной системой здравоохранения (NHS), тогда как некоторые из этих препаратов могут приобретаться без рецепта или по рецепту, который не оплачивается NHS. Кроме того, были включены не все случаи, возникавшие в пределах географической территории, на которой проводилось исследование. В некоторых случаях не выполнялись подтверждающие диагностические тесты, поскольку было очень обоснованным клиническое подозрение. В исследование могли быть не включены пациенты, посещавшие частные клиники, и, наконец, в данном исследовании медицинской помощью было охвачено только 73% популяции территории. Тем не менее эти ограничения, по–видимому, существенно не влияют ни на представительность каждого из местно применявшихся НПВП в полученных результатах, ни на их использование, ни на число наблюдавшихся случаев; не влияют они и на вывод о большей аллергенности кетопрофена среди всей группы местно применяющихся НПВП.
Полученные результаты подтверждают необходимость административного действия в отношении местного применения кетопрофена.
По материалам статьи, опубликованной
в Contact Dermatitis 2006, 54: 239–243
Безопасны ли местные НПВП?
Комментарий к статье ассистента курса
ревматологии РМАПО к.м.н. А.А. Годзенко
Нестероидные противовоспалительные препараты (НПВП) в виде мазей и гелей пользуются большой популярностью у пациентов, страдающих заболеваниями опорно–двигательного аппарата. На сегодняшний день имеется достаточный арсенал средств для локального применения, содержащих тот или иной противовоспалительный препарат. Традиционно и небезосновательно считается, что мазевые формы НПВП более безопасны по сравнению с таблетированными. При применении мазей значительно уменьшается поступление препарата в общий кровоток и, следовательно, уменьшается его накопление в органах, чувствительных к отрицательному воздействию НПВП. Кроме того, использование современных мазей, кремов и гелей в некоторых случаях позволяет снизить дозу принимаемых перорально и парентерально НПВП.
Спектр применения НПВП–содержащих мазей чрезвычайно широк: воспалительные и дегенеративные заболевания суставов, травматические поражения суставов и околосуставных тканей, радикулиты, невралгии и т.д. Препараты этой категории доступны для пациентов без рецепта и во многих случаях без предварительной консультации врача. Тем более настораживающими представляются публикации о значительной частоте кожных реакций в виде контактного дерматита и фотодерматита на фоне применения мазей, содержащих НПВП, в частности, кетопрофена. Авторы предлагаемой статьи обращают внимание не только на достаточно высокую частоту, но и на тяжесть кожных реакций, которые нередко были пролонгированными, напоминали мультиформную эритему, рожу, буллезные элементы.
Наши собственные данные, касающиеся переносимости местных НПВП, основаны на исследовании препарата Быструмгель, содержащего активное вещество кетопрофен, а также вспомогательные компоненты – трометамол, карбомер, нипагин, спирт, ароматические масла – лавандовое и неролиевое. Из 30 пациентов, получавших этот препарат для локальной терапии остеоартроза, аллергический фотодерматит наблюдался у 1 пациентки (3,33%). Данное нежелательное явление отмечалось у женщины 50 лет в летний период. Локализация поражения соответствовала зоне нанесения геля – область коленного сустава и нижняя треть бедра. Следует отметить также, что пациентка в период применения геля подвергалась инсоляции. Нежелательное явление было купировано после отмены препарата и назначения антигистаминных средств.
Сообщения об аллергических реакциях на кетопрофен–содержащие средства в виде дерматита и фотодерматита не следует рассматривать, как неожиданные. Эти нежелательные явления хорошо известны и описаны в справочниках лекарственных средств. Тем не менее, основываясь на материалах статьи, при назначении противовоспалительных мазей и гелей (кетопрофен) не стоит игнорировать возможность развития такой реакции, о чем пациент должен быть непременно проинформирован. Уместно также перед началом лечения провести пробу на переносимость на небольшом участке кожи, а в период лечения избегать попадания прямых солнечных лучей на область нанесения препарата. Эти простые меры позволяют снизить вероятность развития кожных реакций на НПВП–содержащие наружные средства.

Литература
1. Lin J, Zhang W, Jones A, Doherty M. Efficacy of topical non–steroidal anti–inflammatory drugs in the treatment of osteoarthritis: meta–analysis of randomised controlled trials. BMJ 2004: 329: 324–330.
2. Green S, Buchbinder R, Barnsley L et al. Non–steroidal anti–inflammatory drugs (NSAIDs) for treating lateral elbow pain in adults. Cochrane Database Syst Rev 2002: 2:CD003686.
3. Rovensky J, Micekova D, Gubzova Z et al. Treatment of knee osteoarthritis with a topical non–steroidal antiinflammatory drug. Results of a randomized, double–blind, placebo–controlled study on the efficacy and safety of a 5% ibuprofen cream. Drugs Exp Clin Res 2001: 27: 209–221.
4. van Haselen R A, Fisher P A. A randomized controlled trial comparing topical piroxicam gel with a homeopathic gel in osteoarthritis of the knee. Rheumatology (Oxford) 2000: 39: 714–719.
5. Anonymous. Topical analgesics: A review of reviews and a bit of perspective. Bandolier Extra 2004 (August): 1–20 (available from http://www.bandolier.com).
6. Bookman A A M, Williams K S A, Shainhouse J Z. Effect of a topical diclofenac solution for relieving symptoms of primary osteoarthritis of the knee: a randomized controlled trial. CMAJ 2004: 171: 333–338.
7. Hindsen M, Isaksson M, Persson L, Zimersson E, Bruze M. Photoallergic contact dermatitis from ketoprofen induced by drug–contaminated personal objects. J Am Acad Dermatol 2004: 50: 215–219.
8 Durbize E, Vigan M, Puzenat E et al. Spectrum of crossphotosensitization in 18 consecutive patients with contact photoallergy to ketoprofen: associated photoallergies to non–benzophenone–containing molecules. Contact Dermatitis 2003: 48: 144–149.
9. Durieu C, Marguery M C, Giordano–Labadie F, Journe F, Loche F, Bazex J. Allergies de contact photoaggraveґ es et photoallergies de keґ toprofe` ne: 19 cas. Ann Dermatol Venereol 2001: 128: 1020–1024.
10. Bastien M, Milpied–Homsi B, Baudot S, Dutartre H, Litoux P. Photosensibilisation de contact au keґ toprofe` ne. 5 Observations. Ann Dermatol Venereol 1997: 124: 523–526.
11. Tosti A, Gaddoni G, Valeri F, Bardazzi F. Contact allergy to ketoprofen. report of 7 cases. Contact Dermatitis 1990:23: 112–113.
12. Matthieu L, Meuleman L, Van Hecke E, Blondeel A, Dezfoulian B, Constandt L, Goossens A. Contact and photocontact allergy to ketoprofen. The Belgian experience. Contact Dermatitis 2004: 50: 238–241.
13. Whittle B J. Gastrointestinal effects of nonsteroidal anti–inflammatory drugs. Fundam Clin Pharmacol 2003:17: 301–313.
14. Sharir M. Exacerbation of asthma by topical diclofenac. Arch Ophthalmol 1997: 115: 294–295.
15. Sitenga G L, Ing E B, Van Dellen R G, Younge B R, Leavitt J A. Asthma caused by topical application of ketorolac. Ophthalmology 1996: 103: 890–892.
16. Fernando A H, Thomas S, Temple R M, Lee H A. Renal failure after topical use of NSAIDs. BMJ 1994: 308: 533.
17. Agence Francё aise de Securiteґ Sanitaire des Produits de Santeґ . Gels de keґ toprofe` ne et reґ actions de photosensibiliteґ . Communiqueґ 7 julliet 2003 (http://afssaps.santefr/htm/10/filltrpsc/lp030701.htm).
18. Veyrac G, Paulin M, Milpied B, Bourin M, Jolliet P. Bilan de l’enquete nationale sur les effets indersirables cutanes du ketoprofen gel enregistres entre le 01/09/1996 et le 31/08/ 2000. Therapie 2002: 57: 55–64.
19. Bruynzeel DP, Andersen KE, Camarasa J G, Lachapelle JM, Menne T, White I R. The European Standard series. European Environmental and Contact Dermatitis Research Group (EECDRG). Contact Dermatitis 1995: 33:145–148.
20. Ortiz de Frutos F J, De la Cuadra Oyanguren J. Fotodermatitis de Contacto. En: Dermatitis de contacto, Gimenez Camarasa J M (ed): Madrid, Aula Medica SA, 1999: pp. 39–51.
21. Serra–Baldrich E, Gimenez J M. La Prueba Epicutanea. En: Dermatitis de contacto, Gimenez Camarasa J M (ed): Madrid, Aula Medica SA, 1999: pp. 77–86.
22. van Puijenbroek E P, Bate A, Leufkens H G, Lindquist M, Orre R, Egberts A C. A comparison of measures of isproportionality for signal detection in spontaneous reporting systems for adverse drug reactions. Pharmacoepidemiol Drug Saf 2002: 11: 3–10.
23. Evans S J, Waller P C, Davis S. Use of proportional reporting ratios (PRRs) for signal generation from spontaneous adverse drug reaction reports. Pharmacoepidemiol Drug Saf 2001: 10: 483–486.
24. Adamski H, Benkalfate L, Delaval Y et al. Photodermatitis from non–steroidal anti–inflammatory drugs. Contact Dermatitis 1998: 38: 171–174.
25. Jeanmougin M, Petit A, Manciet J R, Sigal M, Dubertret L. Eczema photo–allergique de contact au ketoprofene. Ann Dermatol Venereol 1996: 123: 251–255.
26. Moore D E. Drug–induced cutaneous photosensitivity. Incidence, mechanism, prevention and management. Drug Saf 2002: 25: 345–372.
27. Pigatto P, Bogardi A, Legori A, Valsecchi R, Picardo M. Cross–reactions in patch testing and photopatch testing with ketoprofen, thiaprophenic acid, and cinnamic aldehyde. Am J Contact Dermat 1996: 7: 220–223.
28. Le Coz C J, Bottlaender A, Scrivener J N et al. Photocontact dermatitis from ketoprofen and tiaprophenic acid: Cross–reactivity study in 12 consecutive patients. Contact Dermatitis 1998: 38: 245–252.
29. Horn H M, Humphreys F, Aldridge R D. Contact dermatitis and prolonged photosensitivity by ketoprofen and associated with sensitivity to benzophenone–3. Contact Dermatitis 1998: 38: 353–354.
30. Kawada A, Aragane Y, Asai M, Tezuka T. Simultaneous photocontact sensitivity to ketoprofen and oxybenzone. Contact Dermatitis 2001: 44: 370.
31. Vasconcelos C, Magina S, Quirino P, Barros M A, Mesquita–Guimara` es J. Cutaneous drug reactions to piroxicam. Contact Dermatitis 1998: 39: 145.
32. Montoro J, Rodr?guez M, D?az M, Bertomeu F. Photoallergic contact dermatitis due to diclofenac. Contact Dermatitis 2003: 48: 115.












