Возбудитель заболевания – Воrreliа burgdorferi (боррелия Бургдорфери) проявляет тропность к тканям кожи, нервной системы и соединительнотканным структурам с развитием картины поражения мышц, суставов, подкожно-жировой клетчатки и др. Из-за разнообразия клиники ряд авторов называют ЛБ «новым великим имитатором» [2, 3].
Частота выявления случаев ЛБ в РФ составляет от 6–8 тыс. пациентов ежегодно, из них в г. Москве и Московской области заражаются до 1 тыс. человек (по данным ФГБУ «НИИ эпидемиологии» Роспотребнадзора за 2012 г.). ЛБ занимает одно из ведущих мест по уровню заболеваемости среди природно-очаговых зоонозов и относится к одной из наиболее актуальных проблем в современной инфекционной патологии. Наиболее часто болеют дети до 15 лет и взрослые в возрасте 25–44 лет [4]. В настоящее время ЛБ внесен в МКБ-10 под шифром А69.2 – болезнь Лайма.
Особое место в клинической картине болезни занимает поражение нервной системы, или нейроборрелиоз, частота выявления которого зависит от географической зоны, наблюдается в России у 10–60% больных [5]. Колебание в частоте его развития связано с особенностью геновидов боррелии и недостаточной изученностью проблемы в ряде регионов. Наиболее высокая частота поражения нервной системы наблюдается на Северо-Западе и в Центре России – 43–64%.
Широкий спектр клинических симптомов и синдромов при нейроборрелиозе объясняется способностью Воrreliа burgdorferi поражать все отделы нервной системы на любой стадии болезни [6, 7]. При нейроборрелиозе описаны:
- сенестонейропатии, нейропатии и радикулопатии;
- поражения черепно-мозговых нервов (ЧМН): моно(поли)неврит (лицевого, языкоглоточного, блуждающего нервов, зрительного, слухового нервов);
- синдром Банавартца (менингорадикулоневрит);
- периферические невриты, плексит. У 1/3 больных выявляется периферический судорожный синдром (тремор кистей рук и судороги в мышцах голеней);
- миелит;
- миелорадикулоневрит;
- лимфоцитарный менингит;
- очаговый или диффузный энцефалит;
- пароксизмальные расстройства сознания;
- эпилептические припадки, церебральный васкулит;
- прогрессирующий энцефаломиелит.
Хронический боррелиоз, или III стадия ЛБ, развивается у 10% больных через 6 мес. – 2 года после острого периода [8]. Наиболее изученными в этом периоде являются хронические неврологические синдромы, напоминающие по срокам развития третичный период нейросифилиса, названные хроническим нейроборрелиозом. При этом развиваются хронический энцефаломиелит, спастический парапарез, некоторые расстройства памяти, деменция, хроническая аксональная полирадикулопатия. Эта стадия характеризуется чередованием ремиссий и рецидивов, однако в некоторых случаях болезнь имеет непрерывно рецидивирующий характер.
Частота развития хронических форм нейроборрелиоза, по данным разных авторов, составляет от 4 до 20% всех больных ЛБ. Однако имеются данные о том, что реальный показатель может быть значительно выше и после перенесенной безэритематозной формы заболевания достигать 85% [9–11]. Считается, что диагностика этих форм заболевания затруднена в связи с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [12].
Для хронической нейроинфекции наиболее характерно постепенное поражение нервной системы с развитием патологического процесса, имитирующим другие нозологические формы, в частности рассеянный склероз, рассеянный энцефаломиелит. Большинство больных c хронической нейроинфекцией не указывают на предшествующую мигрирующую эритему или укус клеща. Полагают, что укусы самцов и незрелых особей клещей часто проходят незаметно для людей [13]. Кроме того, могут встречаться безэритематозные формы ЛБ в 2–20% случаев [14–15]. Известно, что в 6–8% случаев возможно субклиническое течение боррелиозной инфекции, при этом отсутствуют клинические проявления болезни. Отсутствие симптомов болезни не исключает развития в последующем II и III стадий заболевания. Все это является фактором риска развития хронической нейроинфекции, т. к. обусловливает отсроченную диагностику [16–18]. Латентный период инфекции при позднем нейроборрелиозе может составлять от 1,5 до 17 лет. Столь длительное латентное течение заболевания связывают с возможным переходом боррелии в неактивные L-формы с последующей их активацией [19–21].
В начале ХХ в. шведский врач-дерматолог А. Афзелиус установил взаимосвязь между появлением на коже кольцевидной мигрирующей эритемы («эритема Афзелиуса») и присасыванием клеща. Позднее у таких больных были описаны другие клинические симптомы: боли и парестезии в месте присасывания клещей с последующими неврологическими нарушениями в виде менингита, пареза лицевой мускулатуры и радикулита. В отечественной литературе середины XX в. описаны случаи развития острых лихорадочных состояний и появления кожных эритем у больных, подвергшихся укусам иксодовых клещей в регионах, эндемичных по клещевому энцефалиту [22].
Впервые хронический боррелиозный энцефаломиелит был описан R. Ackermann et al. в 1985 г. [23]. Позже была изучена группа из 44 больных, у которых встречались преимущественно церебральные проявления, напоминающие мультифокальный энцефалит, или спинальные симптомы. В настоящее время частота выявления энцефаломиелита при ЛБ невысока и составляет в среднем 4–5% от всех случаев нейроборрелиоза. Хроническое течение ЛБ в России изучено мало, что связано с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [24].
В литературе выделяют разные варианты течения нейроинфекции при хроническом ЛБ, включая прогрессирующий энцефаломиелит, хроническую радикулополиневропатию, хронический лимфоцитарный менингит, церебральный васкулит, энцефалопатию и др. Прогрессирующий энцефаломиелит при ЛБ нередко имитирует рассеянный склероз [25, 26]. Согласно наблюдению ряда исследователей, при хроническом ЛБ процесс носит генерализованный характер поражения нервной системы, несмотря на то, что клинически определяется изолированное поражение какого-либо нерва [27, 28]. Пo данным магнитно-резонансной томографии (МРТ) отмечаются поражения очагового характера преимущественно белого вещества головного мозга [29], которые могут определяться после длительного латентного периода.
Ведущие симптомы прогрессирующего боррелиозного энцефаломиелита – это спастические пара- и тетрапарезы, атаксия, дисфункция тазовых органов, когнитивные расстройства в виде снижения памяти и концентрации внимания. Больше чем у 50% больных ЛБ с поражением ЦНС наблюдаются сопутствующее поражение корешков и периферических нервов, множественные парезы черепных нервов, преимущественно вестибулокохлеарного.
Диагностические критерии хронической нейроинфекции включают:
- Наличие признаков поражения ЦНС при боррелиозе после перенесенных I и II стадий заболевания.
- Развитие неврологической симптоматики позднее 6 мес. от появления мигрирующей эритемы и/или факта присасывания клеща или сохранение симптоматики на протяжении более 6 мес.
- Обнаружение умеренных или высокоположительных титров антител к Borrelia burgdorferi в сыворотке крови больного при двукратном обследовании.
- Исключение другой этиологии патологического процесса, протекающего в нервной системе, который мог явиться причиной развития имеющейся у больного клинической симптоматики.
Поражение нервной системы на поздних стадиях ЛБ у 40% больных бывает изолированным и почти в 60% сочетается с экстраневрональными проявлениями ЛБ [6, 30]. Наиболее часто отмечаются поражения опорно-двигательного аппарата в виде артралгии, миалгии и других проявлений. В связи с развитием ревматических синдромов до 30% больных с ЛБ ежегодно обращаются к ревматологам.
Особая сложность диагностики наблюдается при отсроченном развитии поражения нервной системы, когда трудно определить связь развития поражения нервной системы с фактом присасывания клеща, особенно в случае безэритематозных форм. Также позитивность по антителам к Borrelia burgdorferi в ликворе выявляется только у 18% больных ЛБ [31–35].
В патогенезе хронического нейроборрелиоза играют роль проникновение инфекции и лимфоцитов в ткани нервной системы, чему способствуют активация или повреждение эндотелиальных клеток, нарастание уровня растворимой формы одной из основных клеточных молекул адгезии – ICAM-1, металлопротеиназы-9 [32]. В ряде исследований имеются доказательства развития аутоиммунных процессов в виде обнаружения антител, направленных против протеинов Borrelia burgdorferi и белков нервной ткани, вызывающих воспаление и демиелинизацию [33]. Высказывается предположение о возможном участии боррелии в инициации аутоиммунного процесса в результате активации миелин-специфичных Т-клеток и обнаружения аутореактивных антител к миелину и компонентам миелина при ЛБ [34]. По мере прогрессирования заболевания расширяется спектр антител ко многим белкам боррелии, что может приводить к перекрестному реагированию иммунной системы с антигенами боррелии и макроорганизма. Ведущая роль в этом отводится длительной персистенции возбудителя в тканях и его внутриклеточному расположению [35].
Комплексная оценка эпидемиологических, клинико-лабораторных и инструментальных данных, отражающих поражения нервной системы при хроническом ЛБ, демонстрирует отличие клинической картины хронической нейроинфекции в России от таковой в Европе в виде более частого поражения периферической нервной системы (радикулополиневропатии) и энцефалопатии, а также отсутствия сочетания полиневропатии с хроническим атрофическим акродерматитом.
Факторами риска развития хронического нейроборрелиоза названы: множественные присасывания клещей, отсутствие у больных мигрирующей эритемы на месте присасывания клеща в острый период ЛБ, раннее развитие признаков диссеминации, отсроченный и неполный курс лечения в острый период заболевания.
Спектр редких проявлений хронического нейроборрелиоза включает изолированное поражение черепных нервов, множественные мононевропатии, церебральный васкулит, синдромы паркинсонизма и бокового амиотрофического склероза, описан миастеноподобный синдром как проявление хронического ЛБ [36].
Представляют клинический интерес особенности течения хронической микст-инфекции ЛБ с клещевым энцефалитом и эрлихиозом, анаплазмозом. Так, в единичных случаях возможно хроническое течение клещевой микст-инфекции с характерными клинико-лабораторными проявлениями данных заболеваний. Показано, что в единичных случаях возможно хроническое течение клещевого энцефалита и ЛБ с типичными клиническими проявлениями последних. В случае возможной хронической микст-инфекции ЛБ и эрлихиоза по сравнению с изолированным течением ЛБ преобладает системность проявлений в сочетании с общеинфекционным синдромом и изменением лабораторных показателей крови (лейкопения, повышение уровня трансаминаз).
Диагностика и течение ЛБ в целом и нейроборрелиоза в частности при ревматических заболеваниях осложняется некоторым атипизмом клинический картины и скоростью прогрессирования ее проявлений, связанных со скомпрометированностью иммунной системы этой группы пациентов на фоне терапии высокими дозами глюкокортикоидов (ГК) и цитостатиками.
Клинический случай
Пациент Г., 1972 г. р. Анамнез болезни: считает себя больным с июля 2013 г., когда без объективной причины возникли повышение температуры до 37,4°С, параорбитальный отек, первые признаки мышечной слабости, утомляемость, боли в области правого тазобедренного сустава. При обследовании (июль 2013 г.) в общем анализе крови: гемоглобин – 148 г/л, скорость оседания эритроцитов (СОЭ) – 8 мм/ч, лейкопения – 2,82х109 (норма 4,0–9,0), тромбоцитопения, аспартатаминотрансфераза (АСТ) – 49 Ед/л (норма до 35 Ед/л), аланинаминотрансфераза (АЛТ) – 26,2 Ед/л, показатели креатинфосфокиназы (КФК) не исследовали. Белковые фракции: альбумины – 57,3%, (норма 55,7–66,1%), α1 – 6,3% (норма 2,9–11,8%), α2 – 9,1% (норма 7,1–11,8%), β1 – 5,5% (норма 4,7–7,2%), β2 – 5,9% (норма 3,2–6,5%), γ – 15,9% (норма 11,1–18,8%). Общий анализ мочи – без особенностей.
С августа 2013 г. – нарастание параорбитального отека, эритема на лице, груди (в зоне декольте), шее, лихорадка, общая слабость, утомляемость, появление признаков мышечной слабости преимущественно нижних конечностей. При обследовании в сентябре 2013 г. впервые выявлено повышение КФК до 841 Ед/л, лактатдегидрогеназы (ЛДГ) – до 657 Ед/л, креатинина – до 118 мкмоль/л (61–115), сохранялись тромбоцитопения (150х109) и лейкопения (2,8х109).
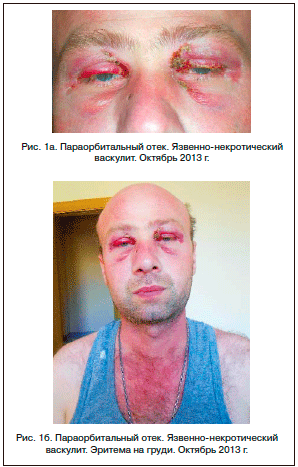
С учетом наличия в клинической картине параорбитального отека, эритемы на лице и в зоне декольте, проксимальной мышечной слабости, миопатических изменений по данным игольчатой электромиографии, повышения уровня КФК у больного диагностирован дерматомиозит (ДМ), начата терапия ГК в дозе 40 мг/сут, на фоне которой отмечены нормализация температуры тела и уменьшение отека вокруг глаз, снижение уровня КФК, АСТ, АЛТ, нормализации уровня лейкоцитов и тромбоцитов. Однако через 2 нед., на фоне быстрого снижения ГК, при достижении дозы преднизолона 30 мг/сут вновь отмечались возобновление лихорадки, усиление выраженности параорбитального отека, появление и нарастание признаков язвенно-некротического васкулита параорбитальной области (рис. 1 а, б). В связи с обострением заболевания и нарастанием признаков язвенно-некротического васкулита параорбитальной области было назначено повышение дозы ГК до 60 мг/сут, к терапии добавлен циклофосфамид 1000 мг в сочетании с метилпреднизолоном 500 мг в/в капельно 1 р./мес.
За период наблюдения пациенту проведен онкопоиск, включающий КТ грудной клетки, консультации специалистов, в т. ч. уролога – патологии не выявлено. Тогда же (до начала терапии циклофосфамидом в октябре 2013 г.) больному впервые выполнена МРТ головного мозга, каких-либо изменений не выявлено.
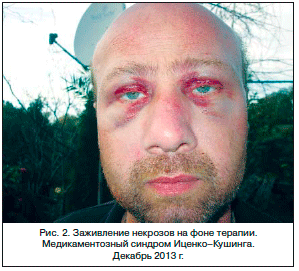
На фоне вышеуказанной терапии наблюдались: нормализация температуры тела, заживление язвенно-некротических изменений (рис. 2), нарастание мышечной силы, снижение КФК – 145 Ед/л, ЛДГ– 256 Ел/л, АСТ – 26 Ед/л, АЛТ – 35 Ед/л. Показатели гемоглобина и СОЭ, как и в начале заболевания, сохранялись в пределах нормы.
Однако на фоне положительной динамики картины основного заболевания (с декабря 2013 г.) возникло быстрое нарастание признаков очагового поражения ЦНС (амимия, двусторонний парез лицевого нерва (чувствительность сохранена), неполное смыкание век за счет пареза нижних век (рис. 3 а, б), односторонняя потеря слуха, головокружение, ощущение «сдавливания» в затылочной области в вертикальном положении). Появились слабость нижних конечностей и неуверенность при ходьбе, что в данном случае было не признаком основного заболевания (ДМ), а проявлением полинейропатии, подтвержденной результатами стимуляционной электронейромиографии (декабрь 2013 г.).
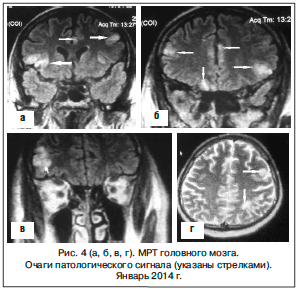
В январе 2014 г. проведена повторная МРТ головного мозга, при которой выявлено появление множественных инфильтративных очагов в кортикальном слое лобных областей, левой теменной области, супраорбитальный области, признаков отека мозга, нарушение гемодинамики (рис. 4 а–г).
Обсуждение возможности активизации латентно протекающей ранее инфекции привело к дополнительным исследованиям: реакция непрямой гемагглютинации на псевдотуберкулез – отрицательно, Yersinia enterocolitica IgG, IgМ – отрицательно; HSV (Herpes simplex virus) IgM – отрицательно, VZV (Varicella-Zoster virus) IgM – отрицательно, CMV (Сytomegalovirus) IgG – 80,4 Ед/мл, IgМ <5,0 Ед/мл (норма). RW (реакция Вассермана), ВИЧ – отрицательны.
Обращали на себя внимание высокие титры к Borrelia burgdorferi: IgМ – 45,0 Ед/мл (норма 12–17), IgG – 78,7 Ед/мл (до 15), однако исследование спинномозговой жидкости показало отрицательный результат.
В динамике дополнительно сыворотка крови пациента была исследована с помощью методики иммуночипа для подтверждения данных иммуноферментного анализа на боррелиоз. Методика «Иммуночипборрелиоз» разработана и проводится на базе ФГБУН «Центральный НИИ эпидемиологии» Роспотребнадзора. Иммуночип является модификацией методики имммуноблоттинга с использованием отечественных изолятов боррелий для определения антительного ответа классов M и G к 14 специфическим антигенным детерминантам возбудителя. Иммуночип зарекомендовал себя как высокоспецифичная и чувствительная методика для диагностики ЛБ. При обследовании у пациента были выявлены положительные показатели в иммуночипе. Выявлены 2 антитела класса IgМ (p41 B/afz p 17 B/ afz/) и антительный ответ класса IgG к 5 антигенным детерминантам (VlsE Borrelia afzelius и к VlsE Borrelia garinii, p58 B/afz., к Osp С Borrelia garinii и Borrelia afzelii, к p17 afz.), при этом в высоких титрах.
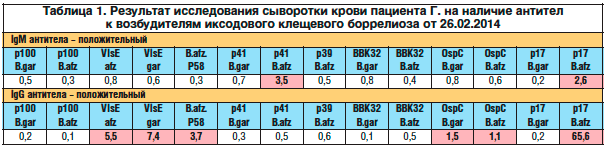
В таблице 1 приведен результат исследования сыворотки крови пациента Г. на наличие антител к возбудителям иксодового клещевого боррелиоза, проведенного в ФГБУН «Центральный НИИ эпидемиологии» (г. Москва).
Зараженность эрлихиозом и анаплазмозом исключена в лабораторном обследовании.
Таким образом, с учетом неоднократно подтвержденной в динамике позитивности по антителам к Borrelia burgdorferi при проведении как иммуноферментного анализа, так и методики иммуночипа, МРТ- и клинической картины очагового демиелинизирующего поражения ЦНС, факта пребывания пациента в течение более чем 2-х лет в эндемичном районе (в центре европейской части России) и после исключения других причин патологического процесса, протекающего в нервной системе, который мог бы явиться причиной развития имеющейся клинической симптоматики, у больного был диагностирован ЛБ III стадии с поражением нервной системы по типу нейроборрелиоза, наиболее вероятно в виде энцефаломиелита.
Полученные результаты обследования потребовали коррекции лечения: циклофосфамид был отменен, начато снижение дозы ГК и подключение антибактериальной терапии: цефтриаксон 4,0 г/сут в/в капельно № 30, а также ипидакрин 20 х 2 р./сут – 1 мес., тиоктовая кислота 600 мг/сут – 1 мес., витамин Е 400 мг/сут.
В настоящее время на фоне вышеуказанной антибактериальной терапии, приема преднизолона 40 мг/сут (снижение дозы продолжает) и отмены циклофосфамида отмечена стабилизация клинической картины, некоторое уменьшение выраженности амимии и признаков полинейропатии нижних конечностей.
Диагностическая и терапевтическая особенность ведения пациента обусловлена сложностью проведения дифференциальной диагностики. Так, с одной стороны, присутствие в клинической картине выраженного язвенно-некротического васкулита, энантемы, лихорадки, неоднократно выявляемых до лечения ГК лейкопении, тромбоцитопении, требовали исключения прежде всего системной красной волчанки, а также системного васкулита, однако отрицательные результаты анти-ДНК, антинуклеарного фактора, Sm, р-АNCA в иммунологическом анализе крови не позволили с уверенностью говорить об обсуждаемых диагнозах. С другой стороны, с учетом множественного прогрессирующего поражения головного мозга в круг дифференциального диагноза были включены рассеянный склероз и прогрессирующая мультифокальная лейкоэнцефалопатия. Последняя является прогрессирующим демиелинизирующим заболеванием ЦНС, вызываемым реактивацией латентно существующего JC-вируса семейства Papovaviridae, рода Polyomavirus и проявляющимся на фоне иммуносупрессии: СПИД, лимфомиелопролиферативные заболевания, злокачественные опухоли, трансплантация органов и аутоиммунные воспалительные заболевания [37]. При анализе клинико-лабораторной картины, данных анамнеза вопрос диагноза был решен в пользу ЛБ, о чем свидетельствовали картина МРТ-изменений (консультация по поводу результатов МРТ головного мозга в Центре неврологии, г. Москва), наличие высоких титров классов IgG и IgМ к Borrelia burgdorferi, а также клинически-положительная динамика неврологического статуса на фоне антибактериальной терапии.
Остается актуальным вопрос причинно-следственного диагноза. Можно ли рассматривать дебют ДМ как самостоятельный, с последующей манифестацией нейроинфекции на фоне иммуносупрессивной терапии? Или латентно протекающий ЛБ послужил триггером для ревматического заболевания?
Так, на сегодняшний день наиболее вероятным остается диагноз ДМ (параорбитальный отек, эритема в зоне декольте, на шее, язвенно-некротический васкулит, проксимальная мышечная слабость, первично-мышечные электромиографические изменения, повышение КФК).
Клещевой иксодовый боррелиоз (болезнь Лайма) III стадия: нейроборрелиоз, изменения ЦНС (по данным МРТ – очаговые изменения в кортикальном слое лобных областей, левой теменной области, супраорбитальной области), поражение ЧМН, периферическая полинейропатия; миопатический синдром, высокая серопозитивность по антителам к боррелиям классов IgG и IgМ.
Описанный случай интересен не только как клиническое наблюдение – манифестация латентно протекающего ранее ЛБ в виде быстропрогрессирующей нейроинфекции на фоне иммуносупрессивной терапии. Представляют интерес также широта дифференциально-диагностического поиска, осложненного некоторым атипизмом дебюта и течения ДМ, и начало наблюдения авторами за больным уже на фоне лечения ГК.