–Я–∞—Ж–Є–µ–љ—В—Л –Є –Љ–µ—В–Њ–і—Л
–Я–∞—Ж–Є–µ–љ—В—Л
–Ь–µ–ґ–і—Г –Љ–∞–µ–Љ 2001 –≥. –Є –Є—О–љ–µ–Љ 2002 –≥. —З–ї–µ–љ—Л BCEDG –Њ–±—Б–ї–µ–і–Њ–≤–∞–ї–Є 20 –µ–≤—А–Њ–њ–µ–Њ–Є–і–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (16 –ґ–µ–љ—Й–Є–љ –Є 4 –Љ—Г–ґ—З–Є–љ) –≤ –≤–Њ–Ј—А–∞—Б—В–µ 18–70 –ї–µ—В (–≤ —Б—А–µ–і–љ–µ–Љ – 42 –≥–Њ–і–∞).
–£ 17 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Љ–µ–ї–Є—Б—М —Б–≤–µ–і–µ–љ–Є—П –Њ —Б–Њ–ї–љ–µ—З–љ–Њ–Љ –Њ–±–ї—Г—З–µ–љ–Є–Є. –£ 1 –њ–∞—Ж–Є–µ–љ—В–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–ґ–Є –љ–∞—З–∞–ї–Є—Б—М –њ–Њ—Б–ї–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≥–µ–ї—П —Н—В–Њ—Д–µ–љ–∞–Љ–∞—В–∞, –љ–Њ —Г –љ–µ–≥–Њ —В–∞–Ї–ґ–µ –њ—А–Є–Љ–µ–љ—П–ї—Б—П –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ –≥–µ–ї—М.
–Ч—Г–і—П—Й–Є–є –њ–∞–њ—Г–ї–Њ–≤–µ–Ј–Є–Ї—Г–ї—П—А–љ—Л–є –і–µ—А–Љ–∞—В–Є—В –љ–∞–±–ї—О–і–∞–ї—Б—П —Г 10 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П –±—Г–ї–ї–µ–Ј–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Г 6 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –£ 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–±–ї—О–і–∞–ї—Б—П –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –Њ—В–µ–Ї, –љ–∞–њ–Њ–Љ–Є–љ–∞—О—Й–Є–є —А–Њ–ґ—Г. –£ 1 –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –љ–∞–њ–Њ–Љ–Є–љ–∞—О—Й–Є–µ –Љ—Г–ї—М—В–Є—Д–Њ—А–Љ–љ—Г—О —Н—А–Є—В–µ–Љ—Г. –Т—Л—Б—Л–њ–∞–љ–Є—П —А–∞—Б–њ–Њ–ї–∞–≥–∞–ї–Є—Б—М –≤ –Љ–µ—Б—В–µ –∞–њ–њ–ї–Є–Ї–∞—Ж–Є–Є —Г 8 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ф–Є—Б—Б–µ–Љ–Є–љ–∞—Ж–Є—П –≤–Њ–Ј–љ–Є–Ї–ї–∞ —Г 11 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. 9 –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М —Б–Є—Б—В–µ–Љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤, –Є 5 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л. –Ф–ї–Є—В–µ–ї—М–љ–∞—П —Д–Њ—В–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М (4 –Љ–µ—Б—П—Ж–∞) –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞.
–Я–∞—В—З– –Є —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л
–Ґ–µ—Б—В—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–∞–Ї –Љ–Є–љ–Є–Љ—Г–Љ, —З–µ—А–µ–Ј 1 –Љ–µ—Б—П—Ж –њ–Њ—Б–ї–µ –њ–Њ–ї–љ–Њ–≥–Њ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –і–µ—А–Љ–∞—В–Є—В–∞. –£ 13 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –њ–∞—В—З–—В–µ—Б—В—Л —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –±–µ–ї—М–≥–Є–є—Б–Ї–Є—Е —Б—В–∞–љ–і–∞—А—В–љ—Л—Е –љ–∞–±–Њ—А–Њ–≤. –§–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л, –њ—А–Њ–≤–Њ–і–Є–≤—И–Є–µ—Б—П –і–≤–∞–ґ–і—Л —Б –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ –≥–µ–ї–µ–Љ (—Г 16 –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –Є –µ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є (—Г 20 –њ–∞—Ж–Є–µ–љ—В–Њ–≤). –Ю–љ–Є —Б–Њ–і–µ—А–ґ–∞–ї–Є 2% –Є 5% –Ъ–Я –≤ –±–µ–ї–Њ–Љ –≤–∞–Ј–µ–ї–Є–љ–µ (–≤–∞–Ј.), 2% –љ–µ—А–Њ–ї–Є–µ–≤–Њ–µ –Љ–∞—Б–ї–Њ (Citrus aurantium dulcis) –≤ –≤–∞–Ј. –Є 5% –Љ–∞—Б–ї–Њ –≤ —Б–њ–Є—А—В–µ, 2% –Љ–∞—Б–ї–Њ –ї–∞–≤–∞–љ–і—Л (Lavandula augustifolia) –≤ –≤–∞–Ј. –Є 5% –Љ–∞—Б–ї–Њ –≤ —Б–њ–Є—А—В–µ, 1% –і–Є—Н—В–∞–љ–Њ–ї–∞–Љ–Є–љ –≤ –≤–∞–Ј. –Є 10% –Ї–∞—А–±–Њ–Љ–µ—А 940 –≤ –≤–Њ–і–µ. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —Б –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ–Є –Р–Я–Ъ, 2% –Є–±—Г–њ—А–Њ—Д–µ–љ–Њ–Љ –≤ –≤–∞–Ј. (—Г 18 –њ–∞—Ж–Є–µ–љ—В–Њ–≤), 2% –љ–∞–њ—А–Њ–Ї—Б–µ–љ–Њ–Љ –≤ –≤–∞–Ј. (—Г 17 –њ–∞—Ж–Є–µ–љ—В–Њ–≤), –∞ —В–∞–Ї–ґ–µ —Б –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ –∞—А–Є–ї—Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л, 5% –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ –≤ –≤–∞–Ј. (—Г 6 –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –Є 2% –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ –≤ –≤–∞–Ј. (—Г 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤). –Я—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–∞, 10% 2––≥–Є–і—А–Њ–Ї—Б–Є–4––Љ–µ—В–Њ–Ї—Б–Є–±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ (o–Ї—Б–Є–±–µ–љ–Ј–Њ–љ, –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–3) –≤ –≤–∞–Ј. –Є 10% 2––≥–Є–і—А–Њ–Ї—Б–Є–4– –Љ–µ—В–Њ–Ї—Б–Є–±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–5–—Б—Г–ї—М—Д–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (—Б—Г–ї–Є—Б–Њ–±–µ–љ–Ј–Њ–љ, –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–4) –≤ –≤–∞–Ј. (Chemotechnique Diagnostics AB), –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В–Њ–≤ —Г 15 –Є 12 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Ю–і–љ–∞ —Б–µ—А–Є—П –њ–ї–∞—Б—В—Л—А–µ–є —Г–і–∞–ї—П–ї–∞—Б—М —З–µ—А–µ–Ј 1 –і–µ–љ—М –Є –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї–Њ—Б—М –Њ–±–ї—Г—З–µ–љ–Є–µ —Г–ї—М—В—А–∞—Д–Є–Њ–ї–µ—В–Њ–Љ –Р (–£–§––Р) –≤ –і–Њ–Ј–µ 5 –Ф–ґ./—Б–Љ2. –†–µ–Ј—Г–ї—М—В–∞—В—Л —В–µ—Б—В–Њ–≤ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є—Б—М —З–µ—А–µ–Ј 1 –Є 3 –і–љ—П –њ–Њ—Б–ї–µ –Њ–±–ї—Г—З–µ–љ–Є—П. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —А–∞–Ј–і–µ–ї—П–ї–Є—Б—М –љ–∞ 3 –≥—А—Г–њ–њ—Л (–Њ—В «+» –і–Њ «+++») –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –≥—А—Г–њ–њ—Л –њ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О –Ї–Њ–љ—В–∞–Ї—В–љ–Њ–≥–Њ –і–µ—А–Љ–∞—В–Є—В–∞ (International Contact Dermatitis Research Group) [4].
–†–µ–Ј—Г–ї—М—В–∞—В—Л
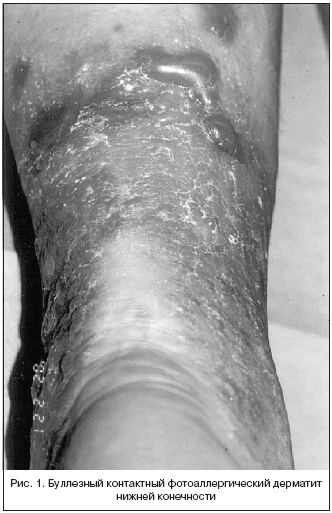
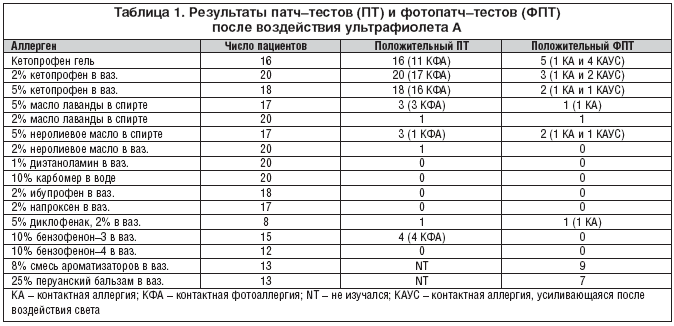
–Т —В–∞–±–ї–Є—Ж–µ 1 –њ–Њ–Ї–∞–Ј–∞–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–∞—В—З–—В–µ—Б—В–Њ–≤ –Є —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В–Њ–≤ –≤ –і–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –°—А–µ–і–Є 16 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е –њ—А–Њ–≤–Њ–і–Є–ї—Б—П —В–µ—Б—В —Б –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ –≥–µ–ї–µ–Љ, –Ї–Њ–љ—В–∞–Ї—В–љ–∞—П —Д–Њ—В–Њ–∞–ї–ї–µ—А–≥–Є—П (–Ъ–§–Р) –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —Г 11 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –Ї–Њ–љ—В–∞–Ї—В–љ–∞—П –∞–ї–ї–µ—А–≥–Є—П (–Ъ–Р) –Є —Г 4 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Љ–µ–ї–∞ –Љ–µ—Б—В–Њ –Ї–Њ–љ—В–∞–Ї—В–љ–∞—П –∞–ї–ї–µ—А–≥–Є—П, —Г—Б–Є–ї–Є–≤–∞—О—Й–∞—П –њ–Њ—Б–ї–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —Б–≤–µ—В–∞ (–Ъ–Р–£–°) (—А–Є—Б. 1, 2). –§–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л —Б –Ъ–Я –≤—Л—П–≤–Є–ї–Є –Ъ–§–Р —Г 17 –Є–Ј 20 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ъ–Р —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞ –Є –Ъ–Р–£–° —Г 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –І–µ—В–Ї–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є (++ –Є +++) –±—Л–ї–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї—А–Њ–Љ–µ 1 –њ–∞—Ж–Є–µ–љ—В–∞, –њ—А–Є—З–µ–Љ —А–∞–Ј–ї–Є—З–Є–є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –і–≤—Г—Е –Є–Ј—Г—З–∞–≤—И–Є—Е—Б—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –Ъ–Я –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М.
–£ 5 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ (+ –Є ++) —А–µ–∞–Ї—Ж–Є–Є –љ–∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А–Њ–≤ –≥–µ–ї—П. 5% –Љ–∞—Б–ї–Њ –ї–∞–≤–∞–љ–і—Л –≤ —Б–њ–Є—А—В–µ –≤—Л–Ј—Л–≤–∞–ї–Њ –§–Ъ–Р —Г 3 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –Ъ–Р —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞, –∞ 5% –љ–µ—А–Њ–ї–Є–µ–≤–Њ–µ –Љ–∞—Б–ї–Њ –≤ —Б–њ–Є—А—В–µ –≤—Л–Ј—Л–≤–∞–ї–Њ –Ъ–§–Р —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞, –Ъ–Р —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞ –Є –Ъ–Р–£–° —Г –і—А—Г–≥–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞. –£ 3 –Є–Ј 5 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–µ–∞–Ї—Ж–Є–Є –љ–∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –Њ—Б–љ–Њ–≤—Л –≥–µ–ї—П –±—Л–ї–Є –Љ–µ–љ–µ–µ —П—А–Ї–Є–Љ–Є, —З–µ–Љ —А–µ–∞–Ї—Ж–Є–Є –љ–∞ –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ. –Э–∞ –і—А—Г–≥–Є–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –Њ—Б–љ–Њ–≤—Л –≥–µ–ї—П —З–µ—В–Ї–Є—Е –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М.
–Я–∞—В—З– –Є —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л —Б –Є–±—Г–њ—А–Њ—Д–µ–љ–Њ–Љ –Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–Њ–Љ –±—Л–ї–Є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ–Є —Г –≤—Б–µ—Е –Є–Ј—Г—З–∞–≤—И–Є—Е—Б—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ъ–Р –љ–∞ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –≤—Л—П–≤–ї–µ–љ–∞ —Г –Њ–і–љ–Њ–≥–Њ –Є–Ј 8 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –§–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л —Б –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–Њ–Љ–3 –±—Л–ї–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ–Є —Г 4 –Є–Ј 15 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –†–µ–∞–Ї—Ж–Є—П –љ–∞ –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–4 –±—Л–ї–∞ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–є —Г 12 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ 9 –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ –њ–∞—В—З–—В–µ—Б—В —Б–Њ —Б–Љ–µ—Б—М—О –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А–Њ–≤ —Г 9 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є 7 –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ –њ–µ—А—Г–∞–љ—Б–Ї–Є–є –±–∞–ї—М–Ј–∞–Љ (—Б–Љ–Њ–ї–∞ Myroxylon pereirae) —Г 13 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —В–µ—Б—В–Є—А–Њ–≤–∞–ї–Є—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –±–µ–ї—М–≥–Є–є—Б–Ї–Є—Е —Б—В–∞–љ–і–∞—А—В–љ—Л—Е –љ–∞–±–Њ—А–Њ–≤.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Э–∞—И–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В —Б–≤—П–Ј—М —Б –Ъ–Я –≤—Б–µ—Е 20 —Б–ї—Г—З–∞–µ–≤ –∞–ї–ї–µ—А–≥–Є–Є –љ–∞ –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ –≥–µ–ї—М –Є –і–Њ–њ–Њ–ї–љ—П—О—В –≤—Б–µ —Г–≤–µ–ї–Є—З–Є–≤–∞—О—Й–µ–µ—Б—П —З–Є—Б–ї–Њ —Б–Њ–Њ–±—Й–µ–љ–Є–є –Њ —А–∞–Ј–≤–Є—В–Є–Є –Ъ–§–Р –Є –Ъ–Р–£–° –љ–∞ —Н—В–Њ—В –Э–Я–Т–Я. –•–Њ—В—П –Љ—Л —В–µ—Б—В–Є—А–Њ–≤–∞–ї–Є —В–Њ–ї—М–Ї–Њ 2 –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —А–µ–∞–Ї—Ж–Є–Є –љ–∞ —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л —Б –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–Њ–Љ, —В–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ–Њ–ї–љ–Њ—Б—В—М—О –Є—Б–Ї–ї—О—З–Є—В—М —А–∞–Ј–≤–Є—В–Є–µ —Д–Њ—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ. –Ю–і–љ–∞–Ї–Њ —Е–∞—А–∞–Ї—В–µ—А —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–∞–Ј–ї–Є—З–Є–є –≤ —В–µ—Б—В–—А–µ–∞–Ї—Ж–Є—П—Е –љ–∞ 2% –Є 5% –Ъ–Я, –∞ —В–∞–Ї–ґ–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Ъ–Р–£–° —Г 4 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ –љ–∞–ї–Є—З–Є–µ –Є–Љ–µ–љ–љ–Њ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ–Њ–≥–Њ –і–µ—А–Љ–∞—В–Є—В–∞, –∞ –љ–µ —Д–Њ—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є. –Т –Њ–і–љ–Њ–Љ –Є–Ј —Б–Њ–Њ–±—Й–µ–љ–Є–є [5] —Г–Ї–∞–Ј—Л–≤–∞–ї–Њ—Б—М, —З—В–Њ –љ–∞–±–Њ—А—Л –њ–∞—В—З–—В–µ—Б—В–Њ–≤ –Є —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В–Њ–≤ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М —Г 12 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ —Д–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ–Њ–≥–Њ –і–µ—А–Љ–∞—В–Є—В–∞ –љ–∞ –Ъ–Я (—Г 10 –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –Є–ї–Є –љ–∞ —В–Є–∞–њ—А–Њ—Д–µ–љ–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г (—Г 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤), –∞ —В–∞–Ї–ґ–µ —Г 15 –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤: –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –љ–µ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –љ–Є —Г –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –Є–Ј –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л, —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–ї–Њ –љ–∞ —Д–Њ—В–Њ–∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї—Г—О –њ—А–Є—А–Њ–і—Г —А–µ–∞–Ї—Ж–Є–є –љ–∞ –Ъ–Я.
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Б–њ–µ–Ї—В—А –і–µ–є—Б—В–≤–Є—П –Ъ–Я –њ—А–µ–Њ–±–ї–∞–і–∞–µ—В –≤ –і–Є–∞–њ–∞–Ј–Њ–љ–µ –£–§–A [5,6]. –£ 47% –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —Б–µ—А—М–µ–Ј–љ—Л–µ –Є –∞—В–Є–њ–Є—З–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л, –∞ –±–Њ–ї–µ–µ —З–µ–Љ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (58%) –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –і–Є—Б—Б–µ–Љ–Є–љ–∞—Ж–Є—П –≤—Л—Б—Л–њ–∞–љ–Є–є. –°–Є—Б—В–µ–Љ–љ–∞—П —В–µ—А–∞–њ–Є—П –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–∞–Љ–Є –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–∞—Б—М 47%, –∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є—П – 26% –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ю–њ–Є—Б—Л–≤–∞–ї–∞—Б—М –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ–∞—П —Д–Њ—В–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –±–µ–Ј –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Ъ–Я [6,7], —Н—В–Њ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –Є –≤ –Њ–і–љ–Њ–Љ –Є–Ј –љ–∞—И–Є—Е —Б–ї—Г—З–∞–µ–≤. –£ 5 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В–∞–Ї–ґ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –Ъ–§–Р, –Ъ–Р–£–° –Є –Ъ–Р –Ї 5% –Љ–∞—Б–ї—Г –ї–∞–≤–∞–љ–і—Л –Є/–Є–ї–Є –љ–µ—А–Њ–ї–Є–µ–≤–Њ–Љ—Г –Љ–∞—Б–ї—Г –≤ —Б–њ–Є—А—В–µ. –Ч–љ–∞—З–Є–Љ–Њ—Б—В—М —Н—В–Є—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞. –£ 4 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ–ї—М–Ј—П –±—Л–ї–Њ –њ–Њ–ї–љ–Њ—Б—В—М—О –Є—Б–Ї–ї—О—З–Є—В—М —А–µ–∞–Ї—Ж–Є–Є —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П –љ–∞ —Б–њ–Є—А—В–Њ–≤—Л–µ —А–∞—Б—В–≤–Њ—А—Л, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–±–∞ –≤–µ—Й–µ—Б—В–≤–∞ –љ–µ –≤—Л–Ј—Л–≤–∞–ї–Є —А–µ–∞–Ї—Ж–Є–Є, –Ї–Њ–≥–і–∞ —В–µ—Б—В–Є—А–Њ–≤–∞–ї–Є—Б—М –≤ 2% –≤–∞–Ј–µ–ї–Є–љ–µ. –Ф—А—Г–≥–Є–Љ –Њ–±—К—П—Б–љ–µ–љ–Є–µ–Љ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є—П, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Љ–∞—Б–ї–Њ –ї–∞–≤–∞–љ–і—Л –Є –љ–µ—А–Њ–ї–Є–µ–≤–Њ–µ –Љ–∞—Б–ї–Њ —П–≤–ї—П—О—В—Б—П –Ї–Њ–љ—В–∞–Ї—В–љ—Л–Љ–Є –Є —Д–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ—Л–Љ–Є –∞–ї–ї–µ—А–≥–µ–љ–∞–Љ–Є. –•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–∞ –њ–µ—А–µ–Ї—А–µ—Б—В–љ–∞—П —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ–ґ–і—Г –Ъ–Я –Є —В–Є–∞–њ—А–Њ—Д–µ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є, —Д–µ–љ–Њ—Д–Є–±—А–∞—В–Њ–Љ –Є –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–∞–Љ–Є, —З—В–Њ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–Њ–≤–Њ–є —З–∞—Б—В—М—О –Љ–Њ–ї–µ–Ї—Г–ї—Л –Ъ–Я [5]. –Э–µ –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —А–µ–∞–Ї—Ж–Є–є –љ–∞ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –Р–Я–Ъ, –Є–±—Г–њ—А–Њ—Д–µ–љ –Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ, –љ–µ –Є–Љ–µ—О—Й–Є—Е –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–Њ–≤–Њ–є —Б—В—А—Г–Ї—В—Г—А—Л. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В –њ–∞—В—З–—В–µ—Б—В–∞ –љ–∞ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї (–њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–µ –∞—А–Є–ї—Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л) –±—Л–ї –≤—Л—П–≤–ї–µ–љ —Г –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞. –Ь—Л —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ–Љ —Н—В–Њ—В —Б–ї—Г—З–∞–є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є–Є.
–Я–µ—А–µ–Ї—А–µ—Б—В–љ–∞—П —Д–Њ—В–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —З–∞—Б—В–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Љ–µ–ґ–і—Г –Ъ–Я –Є –љ–µ–Ј–∞–Љ–µ—Й–µ–љ–љ—Л–Љ–Є –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–∞–Љ–Є, –Љ–µ–љ–µ–µ —З–∞—Б—В–Њ —Н—В–Њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ј–∞–Љ–µ—Й–µ–љ–љ—Л—Е –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–Њ–≤. –Ъ–∞–Ї –Є –≤ —А—П–і–µ –і—А—Г–≥–Є—Е –њ—Г–±–ї–Є–Ї–∞—Ж–Є–є [5,6], –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л –љ–∞ –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–3 –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –Љ–µ–љ–µ–µ —З–µ–Љ —Г 30% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –∞ –љ–∞ –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–4 – –љ–Є —А–∞–Ј—Г. –≠—В–Њ, –Ї–∞–Ї –њ–Њ–ї–∞–≥–∞—О—В, —П–≤–ї—П–µ—В—Б—П —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ—Л—Е –Ј–∞–Љ–µ–љ –±–Њ–Ї–Њ–≤—Л—Е —Ж–µ–њ–µ–є –≤ —Б—В—А—Г–Ї—В—Г—А–µ –±–µ–љ–Ј–Њ—Д–µ–љ–Њ–љ–∞ [5].
–£ 69% –љ–∞—И–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –Ї–Њ–љ—В–∞–Ї—В–љ–∞—П –∞–ї–ї–µ—А–≥–Є—П –љ–∞ —Б–Љ–µ—Б—М –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А–Њ–≤. –Т 2 –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л—Е —Б–µ—А–Є—П—Е –љ–∞–±–ї—О–і–µ–љ–Є–є [6,8] –Ъ–Р –Є –§–Ъ–Р –љ–∞ —Б–Љ–µ—Б—М –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А–Њ–≤ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Г 68 –Є 83% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞–ї–ї–µ—А–≥–Є–µ–є –љ–∞ –Ъ–Я, —З—В–Њ —Б—А–∞–≤–љ–Є–Љ–Њ —Б –љ–∞—И–Є–Љ–Є —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є. –Т–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –Њ–±—К—П—Б–љ–µ–љ–Є–µ–Љ —Н—В–Њ–≥–Њ —П–≤–ї–µ–љ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–ї–Є—З–Є–µ —Г –Ъ–Я —Д—Г–љ–Ї—Ж–Є–Є –∞–ї—М–і–µ–≥–Є–і–∞ –Є –њ—А–Є—Б—Г—В—Б—В–≤–Є–µ –∞–ї—М–і–µ–≥–Є–і–∞ –Ї–Њ—А–Є—З–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ —Б–Љ–µ—Б–Є –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А–Њ–≤ –Є –њ–µ—А—Г–∞–љ—Б–Ї–Њ–≥–Њ –±–∞–ї—М–Ј–∞–Љ–∞.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–С–µ–ї—М–≥–Є–є—Б–Ї–Є–є –Њ–њ—Л—В –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є, –≤—Л—Б–Ї–∞–Ј–∞–љ–љ—Л–µ –і—А—Г–≥–Є–Љ–Є –∞–≤—В–Њ—А–∞–Љ–Є, –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є–Ј–±–µ–≥–∞—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ъ–Я –і–ї—П –Љ–µ—Б—В–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ —Б–Њ–ї–љ–µ—З–љ—Л–µ –њ–µ—А–Є–Њ–і—Л –≤—А–µ–Љ–µ–љ–Є –љ–∞ –Њ—В–Ї—А—Л—В—Л–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Њ–ґ–Є, —Г—З–Є—В—Л–≤–∞—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А—М–µ–Ј–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є, –і–ї–Є—В–µ–ї—М–љ–Њ —Б–Њ—Е—А–∞–љ—П—О—Й—Г—О—Б—П —Д–Њ—В–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Г—О —Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є—О.
–Я–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ —Б—В–∞—В—М–Є, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–є –≤
Contact Dermatitis 2004: 50: 238–241
–Ъ–Њ–Љ–Љ–µ–љ—В–∞—А–Є–є –Ї —Б—В–∞—В—М–µ –њ—А–Њ—Д–µ—Б—Б–Њ—А–∞ –Ї—Г—А—Б–∞ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –†–Ь–Р–Я–Ю –Т.–Т. –С–∞–і–Њ–Ї–Є–љ–∞
–Э–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я) —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ —И–Є—А–Њ–Ї–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є. –Э–Я–Т–Я –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Њ—В–ї–Є—З–∞—О—В—Б—П —Б–≤–Њ–Є–Љ –∞–љ—В–Є–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–Љ –Є –≤ –±–Њ–ї—М—И–µ–є – —Б–≤–Њ–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О. –°—А–µ–і–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –љ–µ—А–µ–і–Ї–Њ —Д–Є–≥—Г—А–Є—А—Г—О—В —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –Ї–Њ–ґ–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –Ј—Г–і–Њ–Љ, –Љ–∞–Ї—Г–ї–Њ––њ–∞–њ—Г–ї–µ–Ј–љ—Л–Љ–Є –≤—Л—Б—Л–њ–∞–љ–Є—П–Љ–Є, –Ї—А–∞–њ–Є–≤–љ–Є—Ж–µ–є, –∞–љ–≥–Є–Њ–љ–µ–≤—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ –Њ—В–µ–Ї–Њ–Љ, —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є, –Љ–љ–Њ–≥–Њ—Д–Њ—А–Љ–љ–Њ–є —Н—А–Є—В–µ–Љ–Њ–є, –≤–µ–Ј–Є–Ї—Г–ї–Њ––±—Г–ї–ї–µ–Ј–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є, —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –°—В–Є–≤–µ–љ—Б–∞––Ф–ґ–Њ–љ—Б–Њ–љ–∞, —Н–Ї—Б—Д–Њ–ї–Є–∞—В–Є–≤–љ—Л–Љ –і–µ—А–Љ–∞—В–Є—В–Њ–Љ –Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ —Н–њ–Є–і–µ—А–Љ–∞–ї—М–љ—Л–Љ –љ–µ–Ї—А–Њ–ї–Є–Ј–Њ–Љ. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ —В–∞–Ї–ґ–µ —А–∞–Ј–≤–Є—В–Є–µ –Є —Д–Њ—В–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –і–µ—А–Љ–∞—В–Њ–Ј–Њ–≤.
–§–Њ—В–Њ–∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–є –Ї–Њ–љ—В–∞–Ї—В–љ—Л–є –і–µ—А–Љ–∞—В–Є—В —П–≤–ї—П–µ—В—Б—П –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ —А–µ–∞–Ї—Ж–Є–Є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї–Њ–ґ–Є, –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ–є –Ґ––ї–Є–Љ—Д–Њ—Ж–Є—В–∞–Љ–Є, –≤ –Њ—В–≤–µ—В –љ–∞ –і–µ–є—Б—В–≤–Є–µ —Д–Њ—В–Њ–∞–ї–ї–µ—А–≥–µ–љ–∞ –Є–ї–Є —Д–Њ—В–Њ–∞–љ—В–Є–≥–µ–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–∞, —А–∞–љ–µ–µ —Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —В–µ–Љ –ґ–µ —Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ–Љ –Є–ї–Є –≤–µ—Й–µ—Б—В–≤–Њ–Љ. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Д–Њ—В–Њ–∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В–∞–Ї—В–љ–Њ–≥–Њ –і–µ—А–Љ–∞—В–Є—В–∞ –±–ї–Є–Ј–Ї–Є –Ї —Н–Ї–Ј–µ–Љ–∞—В–Њ–Ј–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є, –њ—А–Є—З–µ–Љ –њ–Њ —В–µ—З–µ–љ–Є—О –Њ–љ–Є –Љ–Њ–≥—Г—В –±—Л—В—М –Њ—Б—В—А—Л–Љ–Є, –њ–Њ–і–Њ—Б—В—А—Л–Љ–Є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є. –†–µ–і–Ї–Њ —Д–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ—Л–є –і–µ—А–Љ–∞—В–Є—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б–Є—Б—В–µ–Љ–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є, —В–∞–Ї–Є–Љ–Є –Ї–∞–Ї –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –і–Є–∞—А–µ—П –Є–ї–Є –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–µ—З–µ–љ–Є. –Т—Л—Б—Л–њ–∞–љ–Є—П –ї–Њ–Ї–∞–ї–Є–Ј—Г—О—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –≤ –Њ–±–ї–∞—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –∞–ї–ї–µ—А–≥–µ–љ–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —Б–≤–µ—В–∞, –љ–Њ –Є–љ–Њ–≥–і–∞ –Є –≤ –Љ–µ—Б—В–µ, –і–∞–ї–µ–Ї–Њ –Њ—В—Б—В–Њ—П—Й–Є–Љ –Њ—В –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ–є –∞–њ–њ–ї–Є–Ї–∞—Ж–Є–Є. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ —В–∞–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–Є—А—Г—О—Й–Є—Е –≤–µ—Й–µ—Б—В–≤, –љ–Њ –Є —Б–Є—Б—В–µ–Љ–љ–Њ–Љ.
–•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ –±–Њ–ї—М—И–Њ–µ —З–Є—Б–ї–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –≤—Л–Ј–≤–∞—В—М —В–∞–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Б–Њ–ї–љ—Ж–µ–Ј–∞—Й–Є—В–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Є –Э–Я–Т–Я, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е —Д–Є–≥—Г—А–Є—А—Г–µ—В –Є –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ. –Т —А–∞–Ј–≤–Є—В–Є–Є —Д–Њ—В–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –і–µ—А–Љ–∞—В–Њ–Ј–Њ–≤ –љ–µ—А–µ–і–Ї–Њ –Є–Љ–µ—О—В –Ј–љ–∞—З–µ–љ–Є–µ –Є –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —Б —Е–Є–Љ–Є—З–µ—Б–Ї–Є —Б—Е–Њ–і–љ—Л–Љ–Є –Є–ї–Є –Њ—В–ї–Є—З–∞—О—Й–Є–Љ–Є—Б—П –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є, —З—В–Њ —Б–ї–µ–і—Г–µ—В –Є–Љ–µ—В—М –≤ –≤–Є–і—Г –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —Д–Њ—В–Њ–і–µ—А–Љ–∞—В–Њ–Ј–Њ–≤. –Ґ–∞–Ї, –Є–Ј–≤–µ—Б—В–љ—Л –њ–µ—А–µ–Ї—А–µ—Б—В–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –Љ–µ–ґ–і—Г –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–Њ–Љ –Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–Њ–Љ –Є–ї–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–Њ–Љ –Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–Њ–Љ. –≠—В–Є –і–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –±–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б, —В–∞–Ї –Ї–∞–Ї —Г—Б—В—А–∞–љ–µ–љ–Є–µ –≤—Л—П–≤–ї–µ–љ–љ–Њ–≥–Њ —Д–Њ—В–Њ–∞–ї–ї–µ—А–≥–µ–љ–∞ –Њ–±—Л—З–љ–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—В–Є—Е–∞–љ–Є—О –і–µ—А–Љ–∞—В–Њ–Ј–∞.
–Т —А–µ—Ж–µ–љ–Ј–Є—А—Г–µ–Љ–Њ–є —Б—В–∞—В—М–µ –њ—А–Є–≤–Њ–і—П—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Њ—В–Ї—А—Л—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П 20 –±–Њ–ї—М–љ—Л—Е —Б —Д–Њ—В–Њ–і–µ—А–Љ–∞—В–Є—В–Њ–Љ, –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –≤—Л–Ј–≤–∞–љ–љ—Л–Љ –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–Њ–Љ. –Ф–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П —Н—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–∞ –≤ —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –Ї–Њ–љ—В–∞–Ї—В–љ–Њ–є –Є —Д–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ–Њ–є –∞–ї–ї–µ—А–≥–Є–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –њ–∞—В—З–—В–µ—Б—В—Л –Є —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В—Л. –Т—Б–µ –±–Њ–ї—М–љ—Л–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ –≥–µ–ї—М. –§–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ–∞—П –∞–ї–ї–µ—А–≥–Є—П –њ—А–Њ—П–≤–ї—П–ї–∞—Б—М –њ–∞–њ—Г–ї–µ–Ј–љ–Њ–є –Є–ї–Є –±—Г–ї–ї–µ–Ј–љ–Њ–є —Б—Л–њ—М—О, –Њ—В–µ–Ї–Њ–Љ –Ї–Њ–ґ–Є. –£ 47% –±–Њ–ї—М–љ—Л—Е –і–µ—А–Љ–∞—В–Є—В –±—Л–ї —Б—А–µ–і–љ–µ—В—П–ґ–µ–ї—Л–Љ –Є —В—П–ґ–µ–ї—Л–Љ, –Є –і–ї—П –µ–≥–Њ –ї–µ—З–µ–љ–Є—П –њ—А–Є–Љ–µ–љ—П–ї–Є —Б–Є—Б—В–µ–Љ–љ—Л–µ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і—Л. –Ф–Є—Б—Б–µ–Љ–Є–љ–∞—Ж–Є—П —Б—Л–њ–Є –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е.
–° –њ–Њ–Љ–Њ—Й—М—О —Д–Њ—В–Њ–њ–∞—В—З–—В–µ—Б—В–Њ–≤ –±—Л–ї–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ —А–Њ–ї—М –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–∞ –≤ —А–∞–Ј–≤–Є—В–Є–Є —Д–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ–Њ–≥–Њ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—А–Љ–∞—В–Є—В–∞ —Г –≤—Б–µ—Е 20 –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Љ–µ–љ—П–ї–Є —Б –ї–µ—З–µ–±–љ–Њ–є —Ж–µ–ї—М—О –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ –≥–µ–ї—М, –Є –≤ —В–Њ –ґ–µ –≤—А–µ–Љ—П —В–∞–Ї–Њ–є –і–µ—А–Љ–∞—В–Є—В –љ–µ –±—Л–ї –≤—Л—П–≤–ї–µ–љ –љ–Є —Г –Њ–і–љ–Њ–≥–Њ –Є–Ј —В–µ—Е –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ –Є–ї–Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї. –£ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –±–Њ–ї—М–љ—Л—Е –±—Л–ї–∞ –≤—Л—П–≤–ї–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –њ–µ—А–µ–Ї—А–µ—Б—В–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –љ–∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –∞—А–Њ–Љ–∞—В–Є–Ј–∞—В–Њ—А–Њ–≤, –љ–∞—Е–Њ–і—П—Й–Є—Е—Б—П –≤ –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ –≥–µ–ї–µ.
–†–µ–Ј—Г–ї—М—В–∞—В—Л, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤ —А–µ—Ж–µ–љ–Ј–Є—А—Г–µ–Љ–Њ–є —Б—В–∞—В—М–µ, –Є–Љ–µ—О—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є –Є—Е —Б–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –ї–Њ–Ї–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Э–Я–Т–Я. –Р–≤—В–Њ—А—Л —Б—В–∞—В—М–Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –Є–Ј–±–µ–≥–∞—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–∞ –љ–∞ –Њ—В–Ї—А—Л—В—Л–µ —Г—З–∞—Б—В–Ї–Є –Ї–Њ–ґ–Є –≤ —Б–Њ–ї–љ–µ—З–љ—Л–µ –і–љ–Є, –∞ —Н—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –њ–Њ–Ј–≤–Њ–ї–Є—В –њ—А–µ–і—Г–њ—А–µ–і–Є—В—М —А–∞–Ј–≤–Є—В–Є–µ —Д–Њ—В–Њ–Ї–Њ–љ—В–∞–Ї—В–љ–Њ–є –∞–ї–ї–µ—А–≥–Є–Є –љ–∞ —Н—В–Њ—В –Э–Я–Т–Я.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Valsecchi R, Falgheri G, Cainelli T. Contact dermatitis from ketoprofen. Contact Dermatitis 1983: 9: 163–164.
2. Bastien M, Milpied–Homsi B, Baudot S, Dutartre H, Litoux P. Photosensibilisation de contact au ke“С toprofene: 5 observations. Ann Dermatol Venereol 1997: 124: 523–526.
3. Sugiura M, Hayakawa R, Kato Y, Sugiura K, Veda H. 4 Cases of photocontact dermatitis due to ketoprofen. Contact Dermatitis 2000: 43: 16–19.
4. Adams R M. Patch testing – a recapitulation. J Am Acad Dermatol 1981: 5: 629–643.
5. Le Coz C, Bottlaender A, Scrivener J et al. Photocontact dermatitis from ketoprofen and tiaprofenic acid: cross–reactivity study in 12 consecutive patients. Contact Dermatitis 1998: 38: 245–252.
6. Durieu C, Marguery M–C, Giordano–Labadie F, Journe F, Loche F, Bazex J. Allergies de contact photoaggravees et photoallergies de contact au ketoprofene: 19 Cas. Ann Dermatol Venereol 2001: 128: 1020–1024.
7. Offidani A M, Cellini A, Amerio P, Simonetti O, Bossi G. A case of persistent light reaction phenomenon to ketoprofen? Eur J Dermatol 2000: 10: 153–154.
8. Durbize E, Vigan M, Puzenat E et al. Spectrum of crossphotosensitization in 18 consecutive patients with contact photoallergy to ketoprofen: associated photoallergies to non–benzophenone–containing molecules. Contact Dermatitis 2003: 48: 144–149.












