Лечение РА основано на применении базисных противовоспалительных препаратов (БПВП). К БПВП относят группу различных по химической структуре лекарственных средств, объединяемых способностью «модифицировать» течение РА, приводя к стойкому уменьшению активности заболевания, замедлению темпов рентгенологического прогрессирования и достижению клинико–лабораторной ремиссии [1,2].
Основными базисными препаратами для лечения РА является лефлуномид и метотрексат. Различаются подходы к назначению этих препаратов. Согласно рекомендациям АСR, оба препарата являются препаратами 1-го выбора при стартовой терапии РА. В то же время разработанные EULAR рекомендации предлагают начинать терапию с назначения метотрексата, а при его непереносимости или неэффективности использовать лефлуномид.
Арава® (лефлуномид) принадлежит к классу базисных противоревматических препаратов и обладает антипролиферативными, иммуномодулирующими, иммуносупрессивными и противовоспалительными свойствами. Активный метаболит лефлуномида А771726 ингибирует фермент дегидрооротат дегидрогеназу и обладает антипролиферативной активностью. А771726 в условиях in vitro тормозит вызванную митогенами пролиферацию и синтез ДНК Т–лимфоцитов. Антипролиферативная активность А771726 проявляется, по–видимому, на уровне биосинтеза пиримидина, поскольку добавление в клеточную культуру уридина устраняет тормозящее действие метаболита А771726. С использованием радиоизотопных лигандов показано, что А771726 избирательно связывается с ферментом дегидрооротат дегидрогеназой, чем объясняется его свойство тормозить этот фермент и пролиферацию лимфоцитов на стадии G1. Пролиферация лимфоцитов является одним из ключевых этапов развития РА. Одновременно А771726 тормозит экспрессию рецепторов к интерлейкину–2 (СВ–25) и антигенов ядра Ki–67 и PCNA, связанных с клеточным циклом.
Терапевтическое действие лефлуномида было показано на нескольких экспериментальных моделях аутоиммунных заболеваний, включая РА. Лефлуномид (Арава®) уменьшает симптомы и замедляет прогрессирование поражения суставов при активной форме РА. Терапевтический эффект обычно проявляется через 4–6 нед. и может нарастать в дальнейшем на протяжении 4–6 мес. Лефлуномид быстро превращается в свой активный метаболит А771726 (первичный метаболизм в кишечной стенке и печени). В плазме, моче или кале были замечены лишь следовые количества неизмененного лефлуномида. Единственным определяемым метаболитом, ответственным за основные свойства препарата in vivo, является А771726. При приеме внутрь абсорбируется 82–95% препарата. Максимальные плазменные концентрации А771726 определяются в течение 1–24 ч после однократно принятой дозы. Лефлуномид может приниматься вместе с пищей.
Из–за очень длительного периода полувыведения А771726 (около 2 нед.) использовалась нагрузочная доза 100 мг в сут. в течение 3 дней. Это позволило быстро достигнуть равновесного состояния плазменной концентрации А771726. Без нагрузочной дозы для достижения равновесной концентрации потребовался бы 2–месячный прием препарата. В исследованиях с многократным назначением препарата фармакокинетические параметры А771726 были дозозависимыми в диапазоне доз от 5 до 25 мг. В этих исследованиях клинический эффект был тесно связан с плазменной концентрацией А771726 и суточной дозой лефлуномида. При дозе 20 мг в сут. средние плазменные концентрации А771726 при равновесном состоянии имели значение 35 мкг/мл. В плазме происходит быстрое связывание А771726 с альбуминами. Несвязанная фракция А771726 составляет примерно 0,62%. Связывание А771726 более вариабельно и несколько снижается у больных РА или пациентов с хронической почечной недостаточностью.
Надо отметить, что оригинальный препарат лефлуномида (Арава®) уже содержит некоторое количество активного метаболита, процентное содержание которого запатентовано. Доказательства клинической эффективности и безопасности получены именно в отношении оригинального препарата (Арава®). Основываясь на данном факте, можно предположить, что терапевтическая эффективность оригинального препарата лефлуномида может превосходить таковую генерика.
Лефлуномид метаболизируется до одного главного (А771726) и нескольких второстепенных метаболитов, включая 4–трифлюорометилаланин. Биотрансформация лефлуномида в А771726 и последующий метаболизм самого А771726 контролируются несколькими ферментами и происходят в микросомальных и других клеточных фракциях. Исследования взаимодействия с циметидином (неспецифическим ингибитором цитохрома Р450) и рифампицином (неспецифическим индуктором цитохрома Р450) показали, что in vivo СYP–энзимы вовлечены в метаболизм лефлуномида только в незначительной степени.
Выведение А771726 из организма медленное и характеризуется клиренсом 31 мл/ч. Лефлуномид выводится с фекалиями (вероятно, за счет билиарной экскреции) и мочой. Период полувыведения составляет около 2 нед.
Фармакокинетика А771726 у пациентов, находящихся на ХАПД, подобна таковой у здоровых добровольцев. Более быстрое выведение А771726 наблюдается у пациентов, находящихся на гемодиализе, что связано не с экстракцией препарата в диализат, а с вытеснением его из связи с белком. Хотя клиренс А771726 увеличивается приблизительно в 2 раза, конечный период полувыведения является подобным таковому у здоровых лиц, т. к. одновременно увеличивается объем распределения [3,4,13].
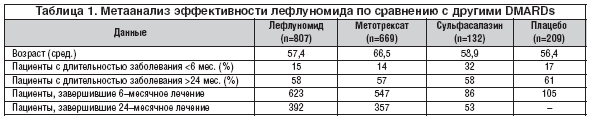
Данные метаанализа основных рандомизированных плацебо–контролируемых исследований (РПКИ), касающихся эффективности лефлуномида при РА, суммированы в таблицах 1 и 2 [5–11].
В исследование III фазы были включены 1817 пациентов с РА. Исходные демографические данные и число пациентов в исследовании приведены в таблице 1 [4–10]. По данным этих исследований была проанализирована сравнительная оценка эффективности лефлуномида в группе пациентов, получавших метотрексат и сульфасалазин. По результатам метаанализа опубликованных исследований по лефлуномиду, ACR–ответ был лучше в группе пациентов, получавших лефлуномид, чем в группе пациентов, получавших плацебо. На 6 мес. и 12 мес. соответственно ACR20 (20% улучшение в соответствии с критериями ACR) достигли 60 и 53% пациентов, получавших лефлуномид, и 27 и 26% пациентов из группы плацебо. Точно так же ACR50 (50% улучшение в соответствии с критериями ACR) было отмечено у 29 и 34% пациентов, получавших лефлуномид, и у 11 и 8% из группы плацебо в тех же точках.
В группе пациентов, получавших лефлуномид, наблюдалось значительное снижение индекса HAQ на 0,37 (95% доверительный интервал (ДИ) 0,33, 0,41) в течение 12 мес., а по сравнению с увеличением в группе плацебо – на 0,06 (95% ДИ 0,03, 0,16). Сопоставимые результаты терапии лефлуномидом наблюдались у пациентов, принимавших сульфасалазин и метотрексат в течение 2–летнего исследования, показали более значимое снижение индекса HAQ в группе пациентов, получавших лефлуномид. Также анализ индекса Sharp показал значительно меньшую радиологическую прогрессию в группе лефлуномида, чем в группе плацебо (лефлуномид по сравнению с плацебо: 6–месячное исследование, p=0,0004; 12–месячное исследование, р = 0,0007) [5–11].
В исследовании MN302 оценивались эффективность и безопасность применения лефлуномида и метотрексата у больных РА. В исследование было включено 999 пациентов с активным РА. Все рандомизированные пациенты были разделены на 2 группы: группа больных, получавших лефлуномид (n=501, 100 мг/сут. в течение 3 дней, затем 20 мг/сут.), и группа пациентов, получавших метотрексат (в дозе 10–15 мг/нед.) в течение 52 нед. Установлено, что эффективность лефлуномида, применяемого как 1–й базисный препарат, несколько выше, чем у больных, которым лефлуномид был назначен после приема метотрексата [17, 18].
Анализ исследования US301 (12 мес., двойное слепое рандомизированное контролируемое) показал клинические преимущества лефлуномида (20 мг/сут., нагрузочная доза 100 мг) по сравнению с метотрексатом. Безопасность и эффективность лефлуномида и метотрексата сохранялись в течение 2 лет наблюдения. Лефлуномид статистически значительно превосходит метотрексат в улучшении функционального состояния суставов в соответствии с индексом HAQ DI. Результаты исследования показывают, что лефлуномид является безопасным и эффективным в начальной терапии для активного РА, с клинически устойчивым эффектом в течение 2 лет лечения [19,20].
В другом открытом исследовании [19,20] у 30 больных с ранней стадией РА (длительность болезни менее 1 года) за 18 мес. лечения лефлуномидом в качестве 1–го БПВП ремиссия по критериям ACR была зарегистрирована у 43,3% больных, еще у 26,7% больных было достигнуто 70–процентное улучшение (ACR70), у 16,7% больных – 50–процентное улучшение (ACR50). То есть при назначении лефлуномида в 1–й год болезни развитие хорошего, очень хорошего эффекта и ремиссии зарегистрировано у 86,7% пациентов.
Результаты исследования RELIEF продемонстрировали, что комбинация лефлуномида и сульфасалазина позволяет увеличить эффективность терапии РА без ухудшения переносимости лечения. Получены данные о достоверно более выраженном эффекте комбинации лефлуномида (10–20 мг/сут.) и метотрексата (10–20 мг/нед.) по сравнению с эффектом монотерапии метотрексатом при удовлетворительной переносимости комбинации БПВП [6–8].
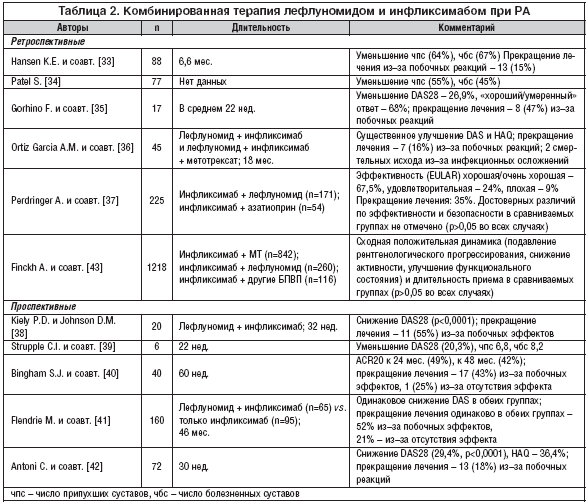
Особенный интерес представляет опыт использования лефлуномида в сочетании с биологическими агентами, в первую очередь с ингибиторами ФНО–α (табл. 2). Уже сообщалось, что комбинация лефлуномида и инфликсимаба эффективна. К настоящему времени отсутствуют проспективные рандомизированные исследования эффективности и переносимости этой комбинации. Имеется ряд открытых исследований – как проспективных, так и ретроспективных (табл. 2), в которых зафиксирован выраженный эффект применения инфликсимаба в комбинации с лефлуномидом. Ретроспективные исследования свидетельствуют и о приемлемой переносимости, тогда как в проспективных исследованиях данные о частоте побочных эффектов различны.
Было высказано мнение, что число аутоиммунных осложнений при комбинации лефлуномида и инфликсимаба (кожный васкулит, волчаночноподобный синдром, церебральный васкулит, синдром Стивена–Джонса) увеличивается у больных, имевших АНФ в сыворотке крови к началу терапии или при его появлении на этапах лечения. Авторы зарегистрировали наличие позитивности по АНФ к началу комбинированной терапии у 12% больных, а к концу – у 75%. Однако количество больных с позитивным АНФ на фоне лечения инфликсимабом увеличивается и при комбинации с метотрексатом.
На сегодняшний день показано, что от присутствия АНФ не зависят ни эффективность, ни переносимость комбинации инфликсимаба с метотрексатом или лефлуномидом. Сравнение эффективности комбинации инфликсимаба с лефлуномидом или другими БПВП показало их примерную равнозначность. Некоторое преимущество комбинации инфликсимаба именно с лефлуномидом заключается в длительности сохранения эффекта и даже увеличении числа больных с хорошим эффектом терапии через 18 и 24 мес. лечения.
Комбинация инфликсимаба и лефлуномида вызывает большее количество слабых побочных реакций за счет симптомов непереносимости со стороны кожи (кожные реакции являются самым часто возникающим симптомом непереносимости при монотерапии лефлуномидом). Выраженные побочные реакции в результате применения комбинации инфликсимаба с лефлуномидом встречаются не чаще, чем при использовании комбинации с другими БПВП, а тяжелые инфекции – даже реже.
Таким образом, можно заключить, что комбинация лефлуномида с инфликсимабом является эффективной; профиль безопасности схож с профилем безопасности применения лефлуномида в виде монотерапии; частые кожные реакции могут приводить к отмене терапии [15,16].
Подводя итог, можно сказать, что лефлуномид (Арава®) эффективен в лечении больных с любой длительностью заболевания. Однако на ранней стадии болезни наблюдаются более быстрое действие, высокая частота выраженного эффекта лечения и клинической ремиссии. Отмечается быстрое развитие эффекта препарата Арава® с достоверным снижением показателей суставного синдрома и лабораторных параметров активности воспаления через 1 мес. лечения, далее эффект лечения нарастает в течение 4–5 мес. Арава® демонстрирует базисную активность, достоверно уменьшая титр РФ, внесуставные проявления РА (в том числе и проявления васкулита), достоверно замедляя темп рентгенологического прогрессирования, а у большинства больных с хорошим и отличным эффектом – останавливая деструктивный процесс.
Литература
1. Мазуров В.И. Современные методы диагностики и лечения ревматических заболеваний // Медицинская иммунология. 2001. Т. 3. № 2. С. 187–193.
2. Scott D.L., Pugner K., Kaarela K. et al. The links between joint damage and disability in rheumatoid arthritis // Rheumatology (Oxford). 2000. Vol. 39. P. 122–132.
3. Cutolo M., Sulli A., Ghiorzo P. et.al Anti–inflammatory effects of leflunomide on cultured synovial macrophages from patients with rheumatoid arthritis. // Ann. Rheum. Dis. 2003. Vol. 62 (4). Р. 297–302.
4. Насонов Е.Л., Чичасова Н.В., Чижова К.А. Перспективы применения лефлуномида в ревматологии // РМЖ. 2004. № 12 (20). С. 1147–1151.
5. Strand V., Cohen S., Schiff M. et al. Treatment of active rheumatoid arthritis with leflunomide compared with placebo and methotrexate. Leflunomide Rheumatoid Arthritis Investigators Group // Arch Int Med. 1999. Vol. 159. Р. 2542–2550.
6. Smolen J.S., Kalden J.R., Scott D.L. et al. Efficacy and safety of leflunomide compared with placebo and sulfasalazine in active rheumatoid arthritis: a double blind, randomised, multicentre trial. European Leflunomide Study Group // Lancet. 1999. Vol. 353. Р. 259–266.
7. Emery P., Breedfeld C., Lemmel E.M. et al. and the multinational leflunomide study group. A comparison of the efficacy and safety of leflunomide and methotrexate for the treatment of rheumatoid arthritis // Rheumatology. 2000. Vol. 39. Р. 655–665.
8. Cohen S., Cannon G.W., Schiff M. et al. Two–year blinded randomized controlled treatment of active rheumatoid arthritis with leflunomide compared with methotrexate. Utilization of Leflunomide in theTreatment of Rheumatoid Arthritis Trial Investigator Group // Arthritis Rheum. 2001. Vol. 44. Р. 1984–1992.
9. Scott D.L., Smolen J.S., Kalden J.R. et al. Treatment of active rheumatoid arthritis with leflunomide: two year follow up of a double blind, placebo controlled trial versus sulfasalazine // Ann Rheum Dis. 2001. Vol. 60. Р. 913–923.
10. Kalden J.R., Schattenkirchner M., Sorensen H. et al. The efficacy and safety of leflunomide in patients with active rheumatoid arthritis: a five–year follow up study // Arthritis Rheum. 2003. Vol. 48. Р. 1513–1520.
11. Scott D.L., Strand V. The effects of disease–modifying anti–rheumatic drugs on the Health Assessment Questionnaire score. Lessons from the leflunomide clinical trials database // Rheumatology. 2002. Vol. 41. Р. 899–909.
12. Scott D.L., Smolen J.S., Kalden J.R. et al. Treatment of active rheumatoid ar–thritis with leflunomide: two year follow up of a double–blind, placebo–controlled trial versus sulfasalasine // Ann Rheum Dis. 2001. Vol. 60. Р. 913–923.
13. Cutolo M., Sulli A., Ghiorzo P. et Al. Anti–inflammatory effects of leflunomide on cultured synovial macrophages from patients with rheumatoid arthritis // Ann. Rheum. Dis. 2003. Vol. 62 (4). Р. 297–302.
14. Osiri M., She A.B., Robinson V. et al. Leflunomide for the treatment of rheumatoid arthritis: a systematic review and meta–analysis. // J. Rheum. 2003. Vol. 30. Р. 1182–1190.
15. Kalden J. R., Antoni C., Alvaro–Gracia J.M. et al. Use of combination of leflunomide with biological agents in treatment of rheumatoid arthritis // J. Rheum. 2005. Vol. 32. Р. 1620–1631.
16. Dougados M., Emery P., Lemmel E.M. et al. Maintenance rate of leflunomide in patients with rheumatoid arthritis: RELIEF 1–year data // Arthritis Rheum. 2001. Vol. 44. Р. 173.
17. Scott D.L., Smolen J.S., Kalden J.R. et al. Treatment of active rheumatoid ar–thritis with leflunomide: two year follow up of a double–blind, placebo–controlled trial versus sulfasalasine. // Ann Rheum Dis. 2001. Vol. 60. Р. 913–923.
18. Cohen S, Weaver A, Schiff M, Strand V. Two–year treatment of active RA with leflunomide compared with placebo or methotrexate // Arthritis Rheum. 2001. Vol. 44. Р. 1984–1992.
19. Yaremenko O.V., Mikitenko A.M. Comparative evaluation of effects of le–flunomide and methotrexate for early rheumatoid arthritis. In Leflunomide. A selection of communications presented at the annual congress of the European League Against Rheumatism. Netherlands, Amsterdam. June 21–24 2006. P. 22.
20. Karateev D., Luchikhina E.L., Nasonov E.L. High frequency of clinical remission in patients with early rheumatoid arthritis treated with le–flunomide. In Leflunomide. A selection of communications presented at the annual congress of the European League Against Rheumatism, Netherlands, Amsterdam. June 21–24 2006. P. 23.












