–°—А–µ–і–Є —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л—Е –њ—А–Є–Љ–µ–љ—П—О—Й–Є—Е—Б—П –≤ –Љ–µ–і–Є—Ж–Є–љ–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –Њ—Б–Њ–±–Њ–µ –Љ–µ—Б—В–Њ –Ј–∞–љ–Є–Љ–∞—О—В –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я), –Ї–Њ—В–Њ—А—Л–µ –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л –і–ї—П –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –±–Њ–ї–Є –Є –ї–Є—Е–Њ—А–∞–і–Ї–Є [1].
–•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –≤–µ–і—Г—Й–Є–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Э–Я–Т–Я —Б–≤—П–Ј–∞–љ —Б –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–µ–Ј—Л (–¶–Ю–У) – —Д–µ—А–Љ–µ–љ—В–∞, —А–µ–≥—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є—О –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ—Л (–Я–У), –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ (PGI2) –Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ (TxA2). –Ш–і–µ–љ—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Њ –і–≤–µ –Њ—Б–љ–Њ–≤–љ—Л–µ –Є–Ј–Њ—Д–Њ—А–Љ—Л –¶–Ю–У, –Ї–Њ—В–Њ—А—Л–µ –Њ–±–Њ–Ј–љ–∞—З–∞—О—В—Б—П, –Ї–∞–Ї –¶–Ю–У–1 –Є –¶–Ю–У–2. –≠—В–Є –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В—Л –Є–≥—А–∞—О—В —А–∞–Ј–ї–Є—З–љ—Г—О (—Е–Њ—В—П –Є –њ–µ—А–µ–Ї—А–µ—Й–Є–≤–∞—О—Й—Г—О—Б—П) —А–Њ–ї—М –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є –Љ–љ–Њ–≥–Є—Е —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е, –∞–і–∞–њ—В–∞—Ж–Є–Њ–љ–љ—Л—Е –Є –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ —З–µ–ї–Њ–≤–µ–Ї–∞ [2,3] (—А–Є—Б. 1).
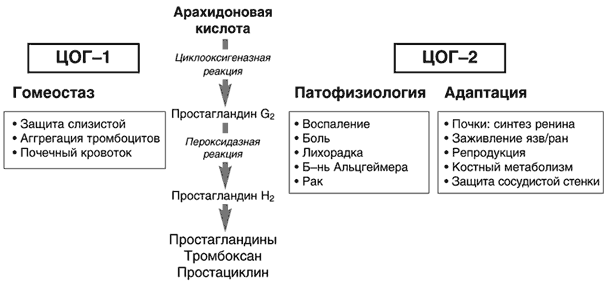
–†–Є—Б. 1. –Я—Г—В–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤
–°–Њ–≥–ї–∞—Б–љ–Њ –Њ–±—Й–µ–њ—А–Є–љ—П—В–Њ–є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Ї–Њ–љ—Ж–µ–њ—Ж–Є–Є –Є–љ–≥–Є–±–Є—Ж–Є—П –¶–Ю–У–2 – –Њ–і–Є–љ –Є–Ј –≤–µ–і—Г—Й–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –Є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Э–Я–Т–Я, –∞ –Є–љ–≥–Є–±–Є—Ж–Є—П –¶–Ю–У–1 – —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ —Б–Њ —Б—В–Њ—А–Њ–љ—Л –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–Ц–Ъ–Ґ) [2,3]. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М «—Б—В–∞–љ–і–∞—А—В–љ—Л—Е» –Э–Я–Т–Я —Б–≤—П–Ј—Л–≤–∞—О—В —Б –Є—Е –љ–Є–Ј–Ї–Њ–є —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —В–Њ –µ—Б—В—М —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –≤ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —Б—В–µ–њ–µ–љ–Є –њ–Њ–і–∞–≤–ї—П—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–±–Њ–Є—Е –Є–Ј–Њ—Д–Њ—А–Љ –¶–Ю–У. –Э–∞ —Н—В–Њ–є –Њ—Б–љ–Њ–≤–µ –∞–Ї—В–Є–≤–љ–Њ —А–∞–Ј—А–∞–±–∞—В—Л–≤–∞–µ—В—Б—П –љ–Њ–≤—Л–є –Ї–ї–∞—Б—Б –Э–Я–Т–Я – —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2, –Ї–Њ—В–Њ—А—Л–µ –Њ–±–ї–∞–і–∞—О—В –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–є —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М—О –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ «—Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є» –Э–Я–Т–Я. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –њ–Њ —А—П–і—Г –њ–∞—А–∞–Љ–µ—В—А–Њ–≤, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М, –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–є —З–∞—Б—В–Њ—В–µ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 –Є–Љ–µ—О—В –Њ—Й—Г—В–Є–Љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–µ—А–µ–і «—Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є» –Э–Я–Т–Я. –Ю–і–љ–∞–Ї–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ—П–≤–Є–ї–Є—Б—М –љ–Њ–≤—Л–µ —Д–∞–Ї—В—Л –Њ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є (–Є–ї–Є –∞–і–∞–њ—В–∞—Ж–Є–Њ–љ–љ–Њ–є) —А–Њ–ї–Є –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –Я–У (—А–Є—Б. 1) [4].–Ю—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ—А–Є–≤–ї–µ–Ї–∞—О—В –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Э–Я–Т–Я. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–∞–Љ–Є. –Т–Њ––њ–µ—А–≤—Л—Е, –≤ –љ–Њ—А–Љ–µ –њ—А–Њ–і—Г–Ї—В—Л –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л – –†GI2 –Є TxA2 –Є–≥—А–∞—О—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ (—В–∞–±–ї. 1).
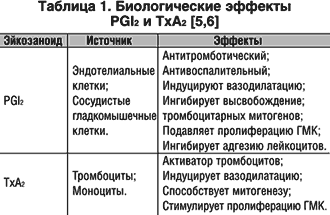

–°–Њ—Б—Г–і–Є—Б—В—Л–µ —Н—Д—Д–µ–Ї—В—Л –Э–Я–Т–Я
–С–Њ–ї—М—И–Њ–є —А–µ–Ј–Њ–љ–∞–љ—Б –≤—Л–Ј–≤–∞–ї–Є –Љ–∞—В–µ—А–Є–∞–ї—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П VIGOR (Vioxx Gastrointestinal Outcomes Research), —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—Й–Є–µ –Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є —З–∞—Б—В–Њ—В–µ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–µ–≤–Љ–∞—В–Њ–Є–і–љ—Л–Љ –∞—А—В—А–Є—В–Њ–Љ (–†–Р), –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А –¶–Ю–У–2 – —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–± (0,5%), —З–µ–Љ –Э–Я–Т–Я (–љ–∞–њ—А–Њ–Ї—Б–µ–љ) (0,1%) [8]. –Я—А–Є —Н—В–Њ–Љ –і–Њ–Ј–∞ —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞, –њ—А–Є–Љ–µ–љ—П–≤—И–∞—П—Б—П –≤ —Н—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–∞ –≤ 2 —А–∞–Ј–∞ –≤—Л—И–µ, —З–µ–Љ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–∞—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л–ї–Њ –Њ–њ–Є—Б–∞–љ–Њ —З–µ—В—Л—А–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –љ–∞–±–ї—О–і–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–Є—Б—В–µ–Љ–љ–Њ–є –Ї—А–∞—Б–љ–Њ–є –≤–Њ–ї—З–∞–љ–Ї–Њ–є (–°–Ъ–Т) –Є –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ (–Р–§–°), –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± [9]. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –∞–љ–∞–ї–Є–Ј–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ [8] –Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ [10] –±—Л–ї–Њ –≤—Л—Б–Ї–∞–Ј–∞–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –Њ —В–Њ–Љ, —З—В–Њ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П – «–Ї–ї–∞—Б—Б–—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є» –њ–Њ–±–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 [11]. –Т —В–∞–±–ї–Є—Ж–µ 2 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є—П –¶–Ю–У–1 –Є –¶–Ю–У–2 –≤ –Ї–ї–µ—В–Ї–∞—Е —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –≤ –љ–Њ—А–Љ–µ –Є –њ—А–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ.
–°–Њ–≥–ї–∞—Б–љ–Њ –Њ–і–љ–Њ–є –Є–Ј –њ–Њ–њ—Г–ї—П—А–љ—Л—Е –≥–Є–њ–Њ—В–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–Њ–і–µ–ї–µ–є —Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –Ї–∞–Ї –±—Л –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ—Л –і–µ–є—Б—В–≤–Є—О –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е [12]. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –Њ–љ–Є –Љ–Њ–≥—Г—В —Б–љ–Є–ґ–∞—В—М –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ—Л–є —Б–Є–љ—В–µ–Ј PGI2 –Ї–ї–µ—В–Ї–∞–Љ–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П, –љ–Њ –љ–µ –≤–ї–Є—П—О—В –љ–∞ –¶–Ю–У–1 –Ј–∞–≤–Є—Б–Є–Љ—Л–є —Б–Є–љ—В–µ–Ј T—ЕA2 —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞–Љ–Є,—З—В–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –љ–∞—А—Г—И–µ–љ–Є—О –±–∞–ї–∞–љ—Б–∞ PGI2/T—ЕA2, –∞ —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ – –Ї –∞–Ї—В–Є–≤–∞—Ж–Є–Є, –∞–≥–≥—А–µ–≥–∞—Ж–Є–Є –Є –∞–і–≥–µ–Ј–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—О —А–Є—Б–Ї–∞ —В—А–Њ–Љ–±–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П (—А–Є—Б. 2). –Я—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–∞—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Н—В–Њ–≥–Њ –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ —Б—Ж–µ–љ–∞—А–Є—П –њ–Њ–ї—Г—З–Є–ї–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П. Y. Cheng –Є —Б–Њ–∞–≤—В. [13] —Г—Б—В–∞–љ–Њ–≤–Є–ї–Є, —З—В–Њ —Г –Љ—Л—И–µ–є, –і–µ—Д–Є—Ж–Є—В–љ—Л—Е –њ–Њ PGI2 (IP) —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ, –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г—Б–Є–ї–µ–љ–Є–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є –Є –∞–≥–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Љ—Л—И–µ–є —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ T—ЕA2 (TP) —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є–ї–Є –Љ—Л—И–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л TP —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Т –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 —Г—Б–Є–ї–Є–≤–∞—О—В —В—А–Њ–Љ–±–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –љ–∞ –Љ–Њ–і–µ–ї–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–є –∞—А—В–µ—А–Є–Є —Г —Б–Њ–±–∞–Ї [14], –∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є—П –¶–Ю–У–2 –Є–≥—А–∞–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О —А–Њ–ї—М –≤ –Ј–∞—Й–Є—В–µ –Љ–Є–Њ–Ї–∞—А–і–∞ –≤ –њ–Њ–Ј–і–љ—О—О —Д–∞–Ј—Г –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–µ–Ї–Њ–љ–і–Є—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П [15]. –Ю–і–љ–∞–Ї–Њ –Є—Б—В–Є–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ —Н—В–Є—Е —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ–Ї–∞ –љ–µ —П—Б–љ–Њ. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 —В–Њ–ї—М–Ї–Њ —З–∞—Б—В–Є—З–љ–Њ –њ–Њ–і–∞–≤–ї—П—О—В –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ—Л–є –Є –љ–µ –Ј–∞—В—А–∞–≥–Є–≤–∞—О—В –¶–Ю–У–1 –Ј–∞–≤–Є—Б–Є–Љ—Л–є —Б–Є–љ—В–µ–Ј PGI2, –∞ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П PGI2 –≤ —Б–Є—Б—В–µ–Љ–љ–Њ–є —Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–Є–ґ–µ, —З–µ–Љ —Н—В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–ї—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Є–љ–≥–Є–±–Є—Ж–Є–Є –∞–≥–≥–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ [16]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, PGI2 –ї–Є—И—М –Њ–і–љ–∞ –Є–Ј –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Љ–Њ–ї–µ–Ї—Г–ї, —Б–Є–љ—В–µ–Ј–Є—А—Г—О—Й–Є—Е—Б—П —Н–љ–і–Њ—В–µ–ї–Є–µ–Љ (NO, CD39/—Н–Ї—В–Њ––Р–Ф–§––∞–Ј–∞, —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–∞—П —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–∞—П –Љ–Њ–ї–µ–Ї—Г–ї–∞ –∞–і–≥–µ–Ј–Є–Є –Є –і—А.), –њ–Њ–і–∞–≤–ї—П—О—Й–Є—Е –∞–і–≥–µ–Ј–Є—О –Є –∞–≥–≥—А–µ–≥–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ [17]. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –і–∞–ґ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –Є–љ–≥–Є–±–Є—Ж–Є–Є PGI2 —П–≤–љ–Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–ї—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –љ–∞—А—Г—И–µ–љ–Є—П —В—А–Њ–Љ–±–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П [16]. –Я—А–Є–Љ–µ—З–∞—В–µ–ї—М–љ–Њ, —З—В–Њ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ —В–∞–Ї–ґ–µ –Њ–±–ї–∞–і–∞–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –Њ—В –і–Њ–Ј—Л –Њ–±—А–∞–Ј–Њ–Љ (20–1200 –Љ–≥) –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М —Б–Є–љ—В–µ–Ј PGI2. –Я–Њ—Н—В–Њ–Љ—Г, –µ—Б–ї–Є —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–∞—П –њ—А–Њ–і—Г–Ї—Ж–Є—П PGI2 –і–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ –Є–Љ–µ–µ—В –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —В—А–Њ–Љ–±–Њ–Ј–∞, –љ–Є–Ј–Ї–Є–µ (PGI2–—Б–±–µ—А–µ–≥–∞—О—Й–Є–µ) –і–Њ–Ј—Л –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –і–Њ–ї–ґ–љ—Л –±—Л—В—М –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л, —З–µ–Љ –≤—Л—Б–Њ–Ї–Є–µ. –Ю–і–љ–∞–Ї–Њ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Љ–µ–ґ–і—Г –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Є –і–Њ–Ј–Њ–є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–µ –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞–µ—В—Б—П.
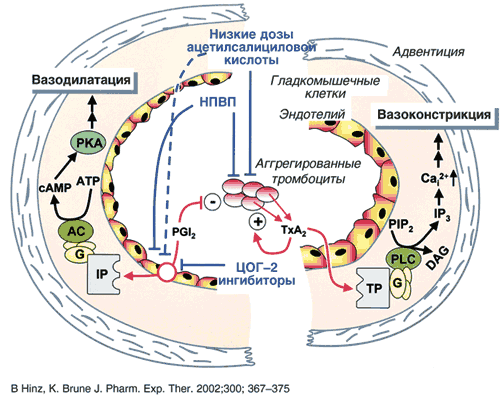
–†–Є—Б. 2. –°–Њ—Б—Г–і–Є—Б—В—Л–µ —Н—Д—Д–µ–Ї—В—Л –Э–Я–Т–Я –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У-2
–Ь–µ—В–∞––∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 – —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –њ—А–Є –†–Р –Є –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≤–ї–Є—П–љ–Є—П —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ —А–Є—Б–Ї —В—А–Њ–Љ–±–Њ–Ј–Њ–≤, –њ–Њ –Ї—А–∞–є–љ–µ–є –Љ–µ—А–µ, –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ—Л—Е –і–Њ–Ј–∞—Е [18–23]. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М —В–∞–Ї–ґ–µ, —З—В–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є VIGOR –њ–Њ—З—В–Є –њ–Њ–ї–Њ–≤–Є–љ–∞ –≤—Б–µ—Е —Б–ї—Г—З–∞–µ–≤ –Њ—Б—В—А–Њ–≥–Њ –Ш–Ь –њ—А–Є—И–ї–∞—Б—М –љ–∞ 4% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–Љ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ «–Ї–∞—А–і–Є–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ» –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –°–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞—В—М —А–∞–Ј–≤–Є—В–Є–µ —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ –њ—А–Є –°–Ъ–Т —В–∞–Ї–ґ–µ –љ–µ –љ–∞—И–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –≤ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [24]. –Я—А–Њ–≤–µ–і–µ–љ–љ—Л–є –љ–∞–Љ–Є –∞–љ–∞–ї–Є–Ј —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —В–Њ–Љ, —З—В–Њ —А–∞–Ј–≤–Є—В–Є–µ —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ —Г —В—П–ґ–µ–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–§–°, –Є–Љ–µ—О—Й–Є—Е –≤—Л—Б–Њ–Ї–Є–є «–±–∞–Ј–∞–ї—М–љ—Л–є» —А–Є—Б–Ї —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–љ–Є—П —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ (3 –Є–Ј –љ–Є—Е –≤–Њ–Њ–±—Й–µ –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–љ–Њ–є/–∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –∞ —Г –Њ–і–љ–Њ–≥–Њ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л–µ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Њ–љ–љ—Л–µ –Њ—В–љ–Њ—И–µ–љ–Є—П (–Ь–Э–Ю) –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–ї–Є—Б—М –љ–µ –љ–∞ –∞–і–µ–Ї–≤–∞—В–љ–Њ–Љ —Г—А–Њ–≤–љ–µ), –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —Б–≤—П–Ј–∞—В—М —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 (—В–∞–±–ї. 3).
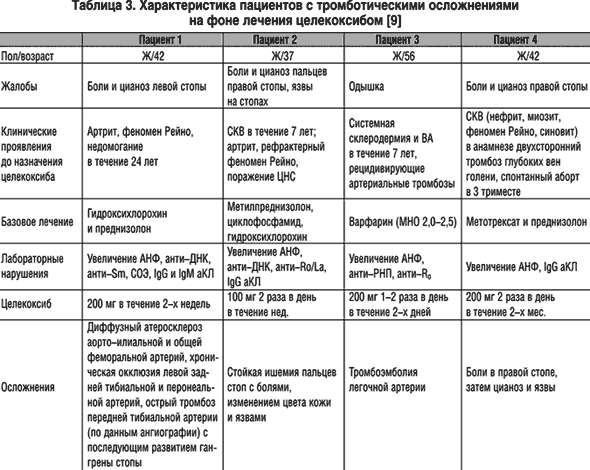
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —И–Є—А–Њ–Ї–Њ–Љ–∞—Б—И—В–∞–±–љ—Л—Е —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Ї–∞—Б–∞—О—Й–Є—Е—Б—П –≤–ї–Є—П–љ–Є—П –њ—А–Є–µ–Љ–∞ –Э–Я–Т–Я –љ–∞ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Г—О –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М.
–Я–Њ –і–∞–љ–љ—Л–Љ –Њ–і–љ–Є—Е –∞–≤—В–Њ—А–Њ–≤, –њ—А–Є–µ–Љ –ї—О–±—Л—Е –Э–Я–Т–Я (–≤ —Б–Њ—З–µ—В–∞–љ–Є–Є –Є–ї–Є –±–µ–Ј –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л) —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Њ—Б—В—А—Л–є –Ш–Ь [33,34]. –Э–∞–њ—А–Њ—В–Є–≤, –і—А—Г–≥–Є–µ –∞–≤—В–Њ—А—Л –љ–µ –≤—Л—П–≤–Є–ї–Є –≤–ї–Є—П–љ–Є—П –Э–Я–Т–Я (–≤–Ї–ї—О—З–∞—П –љ–∞–њ—А–Њ–Ї—Б–µ–љ) –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ —Н—В–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [35,36]. –Э–µ–і–∞–≤–љ–Њ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є–µ–Љ –Э–Я–Т–Я –љ–µ –≤–ї–Є—П–µ—В –љ–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ [37]. –Я—А–Є–µ–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2, –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞ [38], —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ (–≤ –Њ–±—Л—З–љ–Њ–є –і–Њ–Ј–µ) –љ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —А–Є—Б–Ї–∞ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ї–∞—В–∞—Б—В—А–Њ—Д –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ «—Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є» –Э–Я–Т–Я. –Я—А–Є–Љ–µ—З–∞—В–µ–ї—М–љ–Њ, —З—В–Њ –њ—А–Є–µ–Љ —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ –≤ –≤—Л—Б–Њ–Ї–Њ–є –і–Њ–Ј–µ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї—Б—П —Б –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ (–љ–Њ –≤–µ—Б—М–Љ–∞ —Г–Љ–µ—А–µ–љ–љ—Л–Љ) –љ–∞—А–∞—Б—В–∞–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л —Н—В–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (—А–Є—Б. 3).
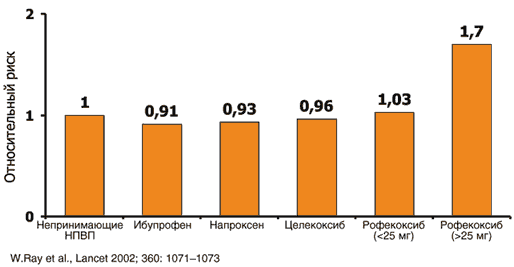
–†–Є—Б. 3. –†–Є—Б–Ї –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ї–∞—В–∞—Б—В—А–Њ—Д —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Э–Я–Т–Я
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤–Њ–њ—А–Њ—Б –Њ —В–Њ–Љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –ї–Є –ї–µ—З–µ–љ–Є–µ –Э–Я–Т–Я (–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –¶–Ю–У–2) –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —А–Є—Б–Ї–∞ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є–ї–Є –љ–∞–Њ–±–Њ—А–Њ—В –Њ–±–ї–∞–і–∞—О—В –ї–Є –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Э–Я–Т–Я «–Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ» –і–µ–є—Б—В–≤–Є–µ–Љ –Њ—Б—В–∞–µ—В—Б—П –Њ—В–Ї—А—Л—В—Л–Љ. –Я–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ —Б—В–∞–љ–і–∞—А—В–∞–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є–Љ –Э–Я–Т–Я (–љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Є—Е –¶–Ю–У–—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є), –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ—О—В –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л [16,39].–° –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –і–∞–љ–љ—Л–µ –Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е –љ–µ –ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П—Е –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є –Э–Я–Т–Я. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –њ–Њ –і–∞–љ–љ—Л–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е (in vitro) –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е (ex vivo) [40] –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Э–Я–Т–Я (–Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ, –Є–±—Г–њ—А–Њ—Д–µ–љ) –Љ–Њ–≥—Г—В –Ї–Њ–љ–Ї—Г—А–Є—А–Њ–≤–∞—В—М —Б –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –Ј–∞ —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ —Б –∞–Ї—В–Є–≤–љ—Л–Љ —Ж–µ–љ—В—А–Њ–Љ –¶–Ю–У–1 –Є –Њ—В–Љ–µ–љ—П—В—М «–∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–є» —Н—Д—Д–µ–Ї—В –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Ю–і–љ–∞–Ї–Њ –і—А—Г–≥–Є–µ –Э–Я–Т–Я, —В–∞–Ї–Є–µ –Ї–∞–Ї –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ, –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї, –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 (—Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±, —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±) [41–43], –љ–µ –њ—А–Њ—П–≤–ї—П—О—В —Н—В–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ (—А–Є—Б. 4). –≠—В–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–ї–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –±–Њ–ї–µ–µ –і–µ—В–∞–ї—М–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Ї–∞—Б–∞—О—Й–Є—Е—Б—П «–Ї–∞—А–і–Є–Њ–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є» —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Э–Я–Т–Я. –Ґ–∞–Ї, –њ–Њ –і–∞–љ–љ—Л–Љ –Њ–і–љ–Њ–≥–Њ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–±—Г–њ—А–Њ—Д–µ–љ –Є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г, —З–∞—Б—В–Њ—В–∞ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ї–∞—В–∞—Б—В—А–Њ—Д —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є —В–Њ–ї—М–Ї–Њ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г (–Ю–†=1,73), –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Є–µ–Љ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ –Є –і—А—Г–≥–Є—Е –Э–Я–Т–Я (–≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є) –љ–µ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Њ—Б—М —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ «–Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ» —А–Є—Б–Ї–∞ [44]. –Р–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ 5––ї–µ—В–љ–µ–≥–Њ –і–≤–Њ–є–љ–Њ–≥–Њ —Б–ї–µ–њ–Њ–≥–Њ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (Physician`s Health Study – PHS) (–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Њ—И–ї–Є 22071 –Ј–і–Њ—А–Њ–≤—Л–є –Љ—Г–ґ—З–Є–љ–∞, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г) –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Є–µ–Љ –Э–Я–Т–Я (>60 –і–љ–µ–є) –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ –Ш–Ь (–Ю–†=2,86), –∞ –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –њ—А–Є–µ–Љ –Э–Я–Т–Я –љ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А–∞—Б—В–∞–љ–Є—О –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ (<60 –і–љ–µ–є) [45].
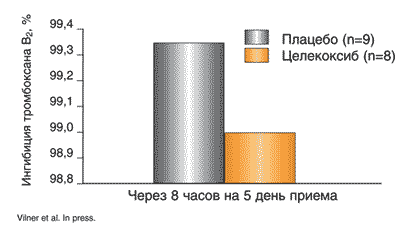
–†–Є—Б. 4. –¶–µ–ї–µ–Ї–Њ–Ї—Б–Є–± + –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞: –і–µ–є—Б—В–≤–Є–µ –љ–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В—Л
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —В–∞–Ї–ґ–µ –Њ—Б–Њ–±–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ, –Ї—А–Њ–Љ–µ –њ—А–Њ–±–ї–µ–Љ—Л –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є, —Б–Њ—З–µ—В–∞–љ–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є –Э–Я–Т–Я –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М –µ—Й–µ –Њ–і–љ–Њ –љ–µ–≥–∞—В–Є–≤–љ–Њ–µ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–µ, —Б–≤—П–Ј–∞–љ–љ–Њ–µ —Б —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ [46] (—А–Є—Б. 5). –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –Њ—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б —А–µ–Ј—Г–ї—М—В–∞—В—Л, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—Й–Є–µ –Њ —З–µ—В–Ї–Њ–є —В–µ–љ–і–µ–љ—Ж–Є–Є –Ї —Б–љ–Є–ґ–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л –Ї–∞–Ї —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, —В–∞–Ї –Є —В—П–ґ–µ–ї—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–Њ–Љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Э–Я–Т–Я [47–49]. –Э–∞–њ—А–Є–Љ–µ—А, –њ–Њ –і–∞–љ–љ—Л–Љ J. Deeks –Є —Б–Њ–∞–≤—В. [47], —З–∞—Б—В–Њ—В–∞ —В—П–ґ–µ–ї—Л—Е –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –±—Л–ї–∞ –љ–∞ 51% –љ–Є–ґ–µ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞, —З–µ–Љ –Э–Я–Т–Я (—А–Є—Б. 6)
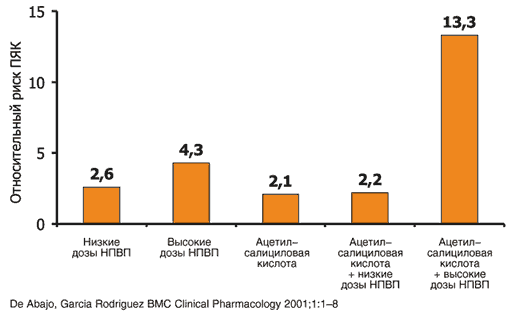
–†–Є—Б. 5. –Р—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –Э–Я–Т–Я –Є —А–Є—Б–Ї —В—П–ґ–µ–ї—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ
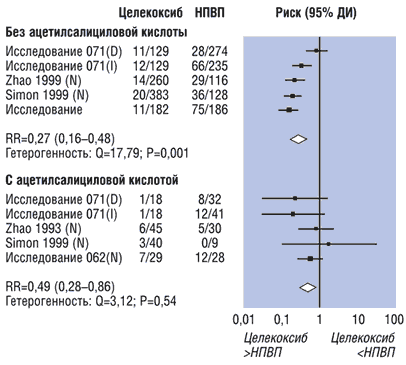
–†–Є—Б. 6. –†–Є—Б–Ї –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Э–Я–Т–Я –Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –љ–Є–Ј–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л
–Р–љ—В–Є–∞—В–µ—А–Њ–≥–µ–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Э–Я–Т–Я–Т –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Њ—Б—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–Љ –≤—Л—И–µ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ –Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П—Е –љ–∞—А—Г—И–µ–љ–Є—П –±–∞–ї–∞–љ—Б–∞ PGI2/TXA2 –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Є—Б—В–µ–Љ—Г –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ–ї—Г—З–µ–љ—Л –і–∞–љ–љ—Л–µ –Њ –≤–∞–ґ–љ–Њ–є —А–Њ–ї–Є –¶–Ю–У–2––Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ —А–∞–Ј–≤–Є—В–Є–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤. –£—З–Є—В—Л–≤–∞—П —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Г—О –Ї–Њ–љ—Ж–µ–њ—Ж–Є—О –Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –њ—А–Є—А–Њ–і–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ [50,51], —Н—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ––љ–Њ–≤–Њ–Љ—Г –≤–Ј–≥–ї—П–љ—Г—В—М –љ–∞ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є.
–Т –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Њ—Б—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–Љ –≤—Л—И–µ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ –Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П—Е –љ–∞—А—Г—И–µ–љ–Є—П –±–∞–ї–∞–љ—Б–∞ PGI/TXA –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Є—Б—В–µ–Љ—Г –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ–ї—Г—З–µ–љ—Л –і–∞–љ–љ—Л–µ –Њ –≤–∞–ґ–љ–Њ–є —А–Њ–ї–Є –¶–Ю–У–2––Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ —А–∞–Ј–≤–Є—В–Є–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤. –£—З–Є—В—Л–≤–∞—П —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Г—О –Ї–Њ–љ—Ж–µ–њ—Ж–Є—О –Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –њ—А–Є—А–Њ–і–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ [50,51], —Н—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ––љ–Њ–≤–Њ–Љ—Г –≤–Ј–≥–ї—П–љ—Г—В—М –љ–∞ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є.–£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≤ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–є –±–ї—П—И–Ї–µ (—Г —З–µ–ї–Њ–≤–µ–Ї–∞ –Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –ґ–Є–≤–Њ—В–љ—Л—Е) –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≥–Є–њ–µ—А—Н–Ї—Б–њ—А–µ—Б—Б–Є—П –¶–Ю–У–2, —З—В–Њ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ–Љ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤, –∞ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 —В–Њ—А–Љ–Њ–Ј—П—В —Н—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б [52–56]. –Т—Л—Б–Ї–∞–Ј–∞–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —З—В–Њ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–ї—Г—З—И–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П (–љ–∞–њ—А–Є–Љ–µ—А, –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞), —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –±–ї—П—И–Ї–Є [55]. –Ф–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ, –њ–Њ –і–∞–љ–љ—Л–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Г –Љ—Л—И–µ–є —Б –і–µ—Д–Є—Ж–Є—В–Њ–Љ –Ы–Э–Я–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –њ—А–Њ–і—Г–Ї—В–Њ–≤ –њ–Є—В–∞–љ–Є—П —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –ґ–Є—А–∞ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —В—П–ґ–µ–ї–Њ–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ —Б–Њ—Б—Г–і–Њ–≤, –≤–≤–µ–і–µ–љ–Є–µ –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ–∞ –Є —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ —В–Њ—А–Љ–Њ–Ј–Є—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ [54]. –≠—В–Њ—В —Н—Д—Д–µ–Ї—В –љ–∞–±–ї—О–і–∞–ї—Б—П –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ PGI2. –Ш–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2 —Г–ї—Г—З—И–∞—О—В —Д—Г–љ–Ї—Ж–Є—О –Љ–Є–Њ–Ї–∞—А–і–∞ –њ—А–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–Љ –Ш–Ь [57]. –Т –љ–µ–і–∞–≤–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В—П–ґ–µ–ї–Њ–є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞ (–≤ —Б—А–µ–і–љ–µ–Љ —Б—В–µ–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ >2,6 –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є) –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О —Н–љ–і–Њ—В–µ–ї–Є–є––Ј–∞–≤–Є—Б–Є–Љ–Њ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–Є (—А=0,026), —Б–љ–Є–ґ–µ–љ–Є—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –°–—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ (—А=09,019) –Є –Њ–Ы–Я–Э–Я (—А=0,028) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –њ–Њ–ї—Г—З–∞–≤—И–Є–Љ–Є –њ–ї–∞—Ж–µ–±–Њ [58] (—А–Є—Б. 7).
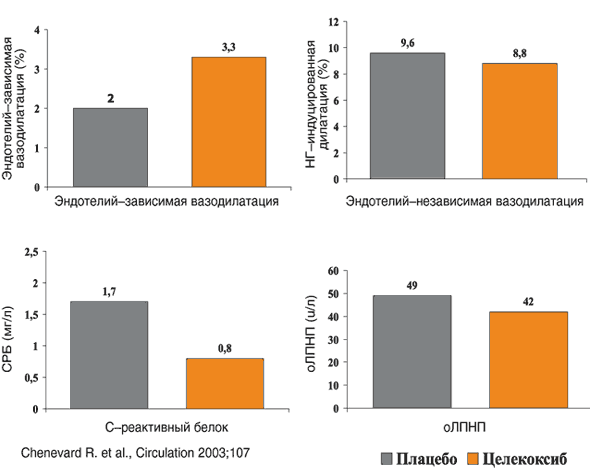
–†–Є—Б. 7. –Т–ї–Є—П–љ–Є–µ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О —Н–љ–і–Њ—В–µ–ї–Є—П, –°–†–С –Є –Њ–Ы–Я–Э–Я –њ—А–Є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–Љ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–µ
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–µ–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –Є–љ—Б—Г–ї—М—В–∞ –Є –Ш–Ь, –њ—А–Є–Љ–µ—А–љ–Њ —Г 8–45% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П [59]. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–є —Н—Д—Д–µ–Ї—В –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —П–≤–ї—П–µ—В—Б—П –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –¶–Ю–У–1 –Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–µ–љ–Њ–Љ–µ–љ–Њ–Љ, –Њ–і–љ–Є–Љ –Є–Ј –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–µ —Б–≤—П–Ј–∞–љ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –Ґ—Е–Р2 —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞–Љ–Є –Є–ї–Є –Љ–Њ–љ–Њ—Ж–Є—В–∞–Љ–Є, –Є–љ—Д–Є–ї—М—В—А–Є—А—Г—О—Й–Є–Љ–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї—Г—О –±–ї—П—И–Ї—Г [60,61]. –Т –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є—П –¶–Ю–У–2 –≤–Њ –≤–љ–Њ–≤—М –Њ–±—А–∞–Ј—Г—О—Й–Є—Е—Б—П –≤ –Ї–Њ—Б—В–љ–Њ–Љ –Љ–Њ–Ј–≥–µ –Ї–ї–µ—В–Ї–∞—Е––њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–∞—Е —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ – –Љ–µ–≥–∞–Ї–∞—А–Є–Њ—Ж–Є—В–∞—Е [62]. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –і–ї—П —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ >90% –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –Ґ—Е–Р2, –і–∞–ґ–µ —Г–Љ–µ—А–µ–љ–љ—Л–є –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ—Л–є —Б–Є–љ—В–µ–Ј –Ґ—Е–Р2, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –±—Л—Б—В—А–Њ–є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ —А–Њ—Б—В–Ї–∞, –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ –Є –њ—А–Є–≤–Њ–і–Є—В—М –Ї —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –љ–Є–Ј–Ї–Є–Љ –і–Њ–Ј–∞–Љ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л [16,63].
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –Є–љ—Б—Г–ї—М—В–∞ –Є –Ш–Ь, –њ—А–Є–Љ–µ—А–љ–Њ —Г 8–45% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П [59]. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–є —Н—Д—Д–µ–Ї—В –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л —П–≤–ї—П–µ—В—Б—П –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ –¶–Ю–У–1 –Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–µ–љ–Њ–Љ–µ–љ–Њ–Љ, –Њ–і–љ–Є–Љ –Є–Ј –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–µ —Б–≤—П–Ј–∞–љ —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –Ґ—Е–Р —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞–Љ–Є –Є–ї–Є –Љ–Њ–љ–Њ—Ж–Є—В–∞–Љ–Є, –Є–љ—Д–Є–ї—М—В—А–Є—А—Г—О—Й–Є–Љ–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї—Г—О –±–ї—П—И–Ї—Г [60,61]. –Т –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Н–Ї—Б–њ—А–µ—Б—Б–Є—П –¶–Ю–У–2 –≤–Њ –≤–љ–Њ–≤—М –Њ–±—А–∞–Ј—Г—О—Й–Є—Е—Б—П –≤ –Ї–Њ—Б—В–љ–Њ–Љ –Љ–Њ–Ј–≥–µ –Ї–ї–µ—В–Ї–∞—Е––њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–∞—Е —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ – –Љ–µ–≥–∞–Ї–∞—А–Є–Њ—Ж–Є—В–∞—Е [62]. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –і–ї—П —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ >90% –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –Ґ—Е–Р, –і–∞–ґ–µ —Г–Љ–µ—А–µ–љ–љ—Л–є –¶–Ю–У–2 –Ј–∞–≤–Є—Б–Є–Љ—Л–є —Б–Є–љ—В–µ–Ј –Ґ—Е–Р, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –±—Л—Б—В—А–Њ–є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ —А–Њ—Б—В–Ї–∞, –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ –Є –њ—А–Є–≤–Њ–і–Є—В—М –Ї —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –љ–Є–Ј–Ї–Є–Љ –і–Њ–Ј–∞–Љ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л [16,63].–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 –њ—А–Є–≤–ї–µ–Ї–ї–Њ –≤–љ–Є–Љ–∞–љ–Є–µ –Ї —А—П–і—Г –љ–Њ–≤—Л—Е –∞—Б–њ–µ–Ї—В–Њ–≤ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є. –°–Њ–Ј–і–∞–µ—В—Б—П –≤–њ–µ—З–∞—В–ї–µ–љ–Є–µ, —З—В–Њ —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –њ–Њ–Ј–≤–Њ–ї—П—В –љ–µ —В–Њ–ї—М–Ї–Њ –њ–Њ–≤—Л—Б–Є—В—М –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є (–Є –љ–µ —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є), —Б—В—А–∞–і–∞—О—Й–Є—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –љ–Њ –Є –Є–Љ–µ—О—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї –≤ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–Њ–і–∞–≤–ї–µ–љ–Є—П «–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ» –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤.
1. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Э–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Я–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Љ–µ–і–Є—Ж–Є–љ–µ) –Ь–Њ—Б–Ї–≤–∞, –Ш–Ј–і–∞—В–µ–ї—М—Б—В–≤–Њ «–Р–љ–Ї–Њ», 2000, 143 —Б—В—А.
2. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –°–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2: —А–µ—И–µ–љ–љ—Л–µ –Є –љ–µ—А–µ—И–µ–љ–љ—Л–µ –њ—А–Њ–±–ї–µ–Љ—Л. –Ъ–ї–Є–љ. –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—П –Є —В–µ—А–∞–њ–Є—П 2000; 1:57–64.
3. FitzGerald GA, Patrono C. The Coxibs, selective inhibitors of cyclooxygenase–2. New Engl J Med 2001; 345: 433–442.
4. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Љ–µ–і–Є—Ж–Є–љ–µ –≤ –љ–∞—З–∞–ї–µ 21 –≤–µ–Ї–∞. –†–Ь–Ц, 2003; 11 (7), 375–378
5. Davidge ST. Prostaglandin H synthase and vascular function. Circ Res 2001; 89: 650–660.
6. Belton O, Fitzgerald DJ. Cycloxygenase isoform and atherosclerosis. Expert reviews in molecular medicine. http//www.expertreviews.org/
7. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Я—А–Њ–±–ї–µ–Љ–∞ –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ–Ј–∞ –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є. –Т–µ—Б—В–љ–Є–Ї –†–Р–Ь–Э 2003; 7: 6–10.
8. Bombardier C, Lane L, Reicin A, et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis. New Engl J Med 2000; 343: 1520–1528.
9. Crofford LJ, Oates JC, McCune WI et al. Thrombosis in patients with connective tissue disease treated with specific cycloxygenase–2 inhibitors: a report of four cases. Arthritis Rheum 2000; 3: 1891–1896.
10. Silverstein FE, Faich G, Goldstein JL et al. Gastrointestinal toxicity with celecoxib versus nonsteroidal anti–inflammatory drugs for osteoarthritis and rheumatoid arthritis: the CLASS study: a randomized controlled trial. Celecoxid long–term arthritis saferty study. JAMA 2000; 284:1247–1255.
11. Mukherjee D, Nissen SE, Topol EJ. Risk of cardiovascular events associated with selective COX–2 inhibitors. JAMA 2001; 286: 954–959/
12. McAdam BF, Catella–Lawson F, Mardini IA, et al. Systemic biosynthesis of prostacyclin by cyclooxygenase (COX)–2: the human pharmacology of a selective inhibitors of COX–2. PNAS 1999; 96: 272–277.
13. Cheng Y, Austin SC, Rocca B., et al. Role of prostacyclin in the cardiovascular response to thromboxane A2. Science 2002; 296: 539–541.
14. Hennan JK, Huang J, Barrett TD, et al. Effects of selective cyclooxygenase–2 inhibition on vascular response and thrombosis in canine arteries. Circulation 2001; 104: 820–825.
15. Shinmura K, Tang XL, Wang Y et al. Cyclooxygenase–2 mediates the cardioprotective effects of the late phase ischemic preconditioning in conscious rabbits. Proc Nat Acad Sci USA 2000;97:10197–10202.
16. Baigent C, Patrono C. Selective cyclooxygenase 2 inhibitors, aspirin, and cardiovascular disease. A reappraisal. Arthritis Rheum., 2003; 48: 12–20.
17. Marcus AJ, Broekman MJ, Pinsky GJ. COX inhibition and thromboregulation. N Engl J Med., 2002; 347: 1025–1026.
18. White WB, Faich G, Whelton A, et al. Comparison of thromboembolic events in patients treated with celecoxib, a cyclooxygenase–2 specific inhibitor, versus ibuprofen or diclofenac. Am J Cardiol 2002; 89: 425–430.
19. Konstam MA, Weir AR. Current persective on the cardiovascular effects of coxibs. Clev Clin J Med 2002; (suppl 1): SI–47–SI–52.
20. Strand V, Hochberg MC. The risk of cardiovascular thrombotic events with selective cyclooxygenase–2 inhibitors. Arthritis Rheum (Arthritis Care&Res) 2002;47:349–355.
21. White WB, Faich G, Borer JS, Makuch R. Cardiovascular thrombotic events are not increased on the cyclooxygenase–2 inhibitor – celecoxib. ACR 66th Annual Scientific Meeting, New Orleans, 2002;485.
22. Reicin AS, Shapiro D, Sperlong RS et al. Comparison of cardiovascular thrombotic events in patients with osteoarthritis treated with rofecoxib versus nonselective nonsteroidal anti–inflammatory druds (ibuprofen, diclofenac and nabumeton). Am Cardiol. 2002; 89: 204–209.
23. Singh GS, Garnier P, Hwang E. et al. Meloxicam does not increase the risk of cardiovascular adverse events compared to other NSAIDs: results from the IMPROVE trial, a multi–center, randomized parallel–group, open label study of 1309 patients in a managed case setting. EULAR Annual Congress of Rheumatology, Stockholm. Sweden, THU0259 (abst).
24. Lander SA, Wallace DJ, Weisman MH Celecoxib for systemic lupus erythematosus: case series and literature review of the use of NSAIDs in SLE. Lupus 2002; 11: 340–347
25. Knijff–Dutmer EAJ, Kalsbeek–Batenburg EM, Koerts J, van Laar MAFJ. Platelet function is inhibited by non–selective non–steroidal anti–inflammatory drugs but not by cyclo–oxygenase–2–selective inhibitors in patients with rheumatoid arthritis. Rheumatology 2002; 41: 458–461.
26. Van Hecken A., Schwarts JL, Depre M., et al. Comparative inhibitory activity of rofecoxib, meloxicam, diclofenac, ibuprofen and naproxen on COX–2 versus COX–1 in healthy volunteers. J. Clin Pharm 2000; 40: 1109–1120.
27. Rahme E, Pilote L, LeLorier J. Association between naproxen use and protection against acute myocardial infarction. Arch Intern Med 2002; 162; 1111–1115.
28. Solomon DH, Glynn RJ, Levone R, et al. Nonsteroidal anti–inflammatory drug use and acute myocardial infarction Arch Intern Med 2002; 162: 1099–1104.
29. Watson DJ, Rhodes T, Cai B, Guess HA. Lower risk of thromboembolic cardiovascular events with naproxen among patients with rheumatoid arthritis. Arch Intern Med 2002; 162: 1105–1110.
30. Brochier ML. Evaluation of flurbiprofen for prevention of reinfarction and reocclusion after successful thrombolysis or angioplasty in acute myocardial infarction. The Flurbiprofen French Trial. Eur Heart J 1993; 14: 951–957.
31. Cataldo G. Heiman F, Lavenzzari M., Marubini E. Indobufen compared with aspirin and dipiridamol on graft patency after coronary bypass surgery: results of a combined analysis. Coron Arter Dis 1998; 9: 217–222.
32. Sajadieh A, Wendelboe O, Hansen JF., Mostensen LS. Non steroidal anti–inflammatory drugs after myovardial infarction. DAVIT Study Groiu, Danish Verapamil Infarction Trial. Am J Vardiol 1999; 83: 1263–1265.
33. Hudson M, Baron M, Rahme E, Pilot L. Anti–inflammatory drugs with a decrease risk of recurrent acute myocardial infarction in patients on aspirin. ACR 66th Annual Scientific Meeting, New Orleans, 2002; 1663 (abst).
34. Ko D., Wang Y, Berger AK et al. Nonsteroidal anti–inflammatory drugs after acute myocardial infarction. Am Heart J 2002; 143: 475–481.
35. Garcia Rodriguez LA. The effect of NSAIDs on the risk of coronary heart disease: fusion of clinical pharmacology and pharmacoepidemilogic data. Clin Exp. Rheumatol. 2001; 19 (suppl. 25): S41–S45.
36. Ray WA, Stein CM, Hall K., et al. Non–steroidal anti–inflammatory drugs and risk of serious coronary heart disease: an observational cohort study. Lancet 2002; 359: 118–123.
37. Bak S, Andersen M, Tsiropoulos I., et al. Risk of stroke associated with nonstweroidal anti–inflammatory drugs, Stroke 2003; 34:379–395
38. Layton D, Hughes K, Harris S, Shakir SAW. Comparison of the incidence rates of thromboembolic events reported for patients prescribed celecoxib and meloxicam in general practice in England using Prescribtion–Events Monitoring (PEM) data. Rheumatology 2003; 42: 1–11.
39. Vane JB. Back to an aspirin a day. Science 2002; 296: 474–475.
40. –°atella–Lawson F, Reilly MP, Kapoor SC et al. Cyclooxygenase inhibitors and the antiplatelet effect of aspirin. N Engl J Med 2001; 345: 1809–1817.
41. Van Solingen R.M., Rosenstein E.D., Mihailescu G., et al. Comparison of the effects of ketoprofen on platelet function in the presence and absence of aspirin Am. J. Med., 2001; 111: 285–289.
42. Ouellett M, Riendeau D, Percival D. A high level of cyclooxygenase–2 inhibitor selectivity is associated with a reduced intereference of platelet cyclooxygenase–1 inactivation by aspirin. PNAS 2001; 98: 14583–14588.
43. Greenberg H, Gottesdiener K, Huntington M, et al. A new cyclooxygenase–2 inhibitor, rofecoxib (VIOXX), did not alter the antiplatelet effects of low–dose aspirin in healthy volunteers. J Clin Pharm 2000; 40: 1509–1515.
44. MacDonald TN, Wei L. Effect of ibuprofen on cardioprotective effect of aspirin. Lancet 2003; 361: 573–574.
45. Kurth T, Glynn RJ, Walker AM, et al. Inhibition of clinical benefits of aspirin on first myocardial infarction by nonsteroidal anti–inflammatory drugs. Circulation 2003; 108: 1191–1195.
46. Derry S, Loke YK. Risk of gastrointestinal haemorrage with long term use of aspirin. BMJ 2000; 321: 1183–1187.
47. Deeks JJ, Smith LA, Bradley MD. Efficacy, tolerability, and upper gastrointestinal safety of celecocib for treatment of osteoarthritis and rheumatoid arthritis: systemic review of randomized controlled trials. BMJ 2002; 325: 1–8
48. Goldstein H, Bello A, Fort J, et al. Differential rates of UGI symptoms in patients receiving celecoxib vs rofecoxib with and without low–dose aspirin for cardiovascular prophylaxis. EULAR Annual Congress of Rheumatology, Stockholm. Sweden, THU0246 (abst).
49. Singh G, Goldstein J, Bello A, et al. Efect of concurrent low–dose aspirin use on the incidence of UGI symptoms in patients receiving celecoxib or conventional NSAIDs: analysis of two largr randomized, double–blind controlled clinical studies. 2002 EULAR Annual Congress of Rheumatology, Stockholm. Sweden, THU0267 (abst).
50. Ross R. Atherosclerosis – an inflammatory disease. N. Engl. J. Med. 1999; 340:115–126.
51. Tousoulis D, Davies G, Stefanadis C, Toutouzas P, Ambrose JA. Inflammatory and thrombotic mechanisms in coronary atherosclerosis. Heart 2003; 89:993–997.
52. Baker CS, Hall RJ, Evans TJ et al. Cyclooxygenase 2 is widely expressed in atherosclerotic lesions affecting native and transplanted human coronary arteries and colocalized with inducible nitric oxide synthase and nitrotyrosine particularly macrophages. Atheroscler Thromb Vasc Biol 1999; 19: 646–655.
53. Schonbeck U, Sukhova GK, Graber P, et al. Augmented expression of cyclooxigenase–2 in human atherosclerotic lesions. Am J Pathol., 1999; 155: 1281–1291.
54. Burleigh ME, Babaev VR, Oates JA, et al. Cyclooxygenase –2 promotes early atherosclerotic lesion formation in LDL receptor deficiency mice. Circulation 2002; 105: 1816–1823.
55. Cippilone F, Prontera C., Pini B., et al. Overexpression of functionally coupled cyclooxygenase E synthase in symptomatic atherosclerotic plaques as a basis of prostaglandin E2–dependent plaque instability. Circulation 2001; 104: 921–930.
56. Belton O, Byrne D, Kearney D., et al. Cyclooxygenase–1 and – 2 dependent prostacyclin formation in patients with atherosclerosis. Circulation 2000; 102: 840–845.
57. Saito T, Rodger IW, Hu E., et al. Inhibition of cyclooxygenase–2 improves cardiac function in myocardial infarction. Biochem Biophys Res Commun 2000; 273: 772–775.
58. Chenevard R., Hurlimann D., Bechir M., et al. Selective COX–2 inhibition improves endothelial function in coronary artery disease. Circulation 2003; 107:
59. Howard PA. Aspirin resistance Ann Pharmacotherapy 2002; 36: 1620–1624.
60. Gum PA, Kottke–Marchant K, Poggio Ed, et al. Profile and prevalence of aspirin resistence in patients with cardiovascular disease. Am J Cardiol 2001; 88: 230–234.
61. Weber AA, Zimmermann KC, Meyer–Kirchrath J, Schor K. Cyclooxygenase–2 in human platelets as a possible factor in aspirin resistence. Lancet 1999; 353: 900.
62. Rocca B, Secchiero P, Giabattoni G, et al. Cycloxygenase–2 expression is induced during human megakaryopoiesis and characterizes newly formed platelets. PNAS 2002; 99: 7634–7639.
63. Halushka MK, Halushka PV. Why are some individuals resistant to the cardioprotective effects of aspirin. Could it be thromboxane A2. Circulation 2002; 105: 1620–1622.












