Основным клиническим проявлением остеоартроза является боль, нередко предшествующая рентгенологическим проявлениям болезни [1]. Боль сопровождается нарушением функции пораженного сустава. И боль, и ограничение подвижности крупных суставов нижних конечностей способствуют развитию значительных функциональных ограничений в ежедневной активности [5], поэтому лечение заболевания направлено в первую очередь на уменьшение болевого синдрома и, как результат этого – улучшение функции сустава.
Лечение остеоартроза должно включать различные нефармакологические методы: образование больных, физическая терапия, чрескожная стимуляция и др. Однако при недостаточной эффективности нефармакологических методов лечения требуется лекарственная терапия [4]. Широко используются в терапии остеоартроза неопиоидные (парацетамол) и центральные (трамадол) анальгетики, нестероидные противовоспалительные препараты (НПВП), кортикостероиды для внутрисуставного введения, а также препараты гиалуроновой кислоты. Простые анальгетики обычно применяют на ранней стадии заболевания или при наличии интенсивных болей в суставах, а также как дополнение к НПВП. Внутрисуставные введения кортикостероидов проводят редко, т.к. они усугубляют дегенерацию хряща. Наиболее широко применяются НПВП, без которых не мыслится комплексная терапия остеоартроза. Позитивное действие НПВП при остеоартрозе определяется не только их антивоспалительным эффектом, но и отчетливым анальгетическим действием [2].
К сожалению, эффективное применение нестероидных противовоспалительных препаратов лимитируется угрозой развития серьезных нежелательных эффектов, прежде всего со стороны желудочно–кишечного тракта. Наибольшее клиническое значение имеет НПВП–гастропатия – эрозии и язвы желудка и/или двенадцатиперстной кишки, которые могут осложниться желудочно–кишечным кровотечением, перфорацией и нарушением проходимости [3]. НПВП снижают эффективность некоторых антигипертензивных средств, а у больных с артериальной гипертензией могут приводить к повышению артериального давления [9,10].
Представляет несомненный интерес создание лекарственных средств, обладающих не только влиянием на симптомы болезни, но и способностью замедлять прогрессирование заболевания. Таковыми средствами являются структурно–модифицирующие препараты: хондроитин сульфат (ХС) и глюкозамина сульфат (ГС) [7].
По заключению экспертов Европейской антиревматической лиги (EULAR), пероральные хондропротекторы (ГС и ХС) являются средствами лечения артроза с наиболее доказанной эффективностью. Благоприятные ближайшие и отдаленные результаты их применения были получены во многих исследованиях, заслуживающих доверия [8,11,12].
С целью оказания структурно–модифицирующего эффекта костной и хрящевой тканей, а также противовоспалительного и анальгетического действия рассчитано создание препарата Бора–Бора (ББ). В состав 1 капсулы ББ входят 2 мг бора, в форме легко усвояемой и хорошо зарекомендовавшей себя в США биологически активной добавки фирмы FutureCeuticals «Фрутекс–Б»–«FruiteX–B» (патент США: US Patent № 5962049). В ББ также входит комплекс ингредиентов, содержащий 13 мг изофлавонов сои, 48 мг бромелайна, 15 мг олигопроантацидов, 9 мг куркумина, 33 мг экстракта босвелии, 67 мг экстракта имбиря, 50 мг витамина С и 200 МЕ витамина D3.
Целью нашего исследования явилось изучение клинической эффективности и безопасности препарата Бора–Бора у пациентов с остеоартрозом.
Материалы и методы
В исследовании приняли участие 45 пациентов (все женщины в возрасте от 40 до 70 лет; средний возраст составил 53,2±9,25 года) с остеоартрозом коленных суставов согласно классификационным критериям Альтмана и др. (1991 г.). У 27 (60%) больных была диагностирована I, у 14 (31%) – II, у 4 (9%) – III стадия заболевания. Средняя продолжительность заболевания составила 6,2±0,98 лет (от 1 года до 20 лет). Ухудшение состояния в виде нарастания болевого синдрома, уменьшение подвижности суставов наблюдалось у 24 (53%) обследованных на протяжении от 1 до 3 недель, у 21 (47%) больных – в течение 1 месяца.
26 (58%) пациенток в течение 2 мес. до включения в исследование постоянно принимали различные нестероидные противовоспалительные препараты (НПВП): 7 больных (16%) – диклофенак натрия в дозе 100 мг/сут., 6 (13%) – ибупрофен 800 мг/сут., 10 (22%) – нимесулид 200 мг/сут., 3 (7%) – мелоксикам 15 мг/сут. Эпизодически принимали НПВП 19 (42%) пациенток. Все больные на время исследования в качестве анальгетика получали парацетамол.
У 21 (46,7%) обследованной пациентки была выявлена артериальная гипертензия: у 12 (26,7%) – I степени, у 9 (20%) – II степени. Пять пациенток страдали хроническим гастритом вне обострения. У 3 больных был выявлен хронический пиелонефрит вне обострения, у 4 пациенток ранее была диагностирована миома матки.
В качестве гипотензивной терапии пациенты получали ингибиторы АПФ (эналаприл, фозиноприл), антагонист кальция амлодипин, индапамид.
Критериями включения в исследование были: диагноз гонартроза с рентгенологически I–III стадией, при наличии болевого синдрома не менее 40 мм по визуальной аналоговой шкале, возраст пациентов от 40 до 70 лет, пациентки детородного возраста, использующие методы контрацепции, или пациентки, находящиеся в менопаузе не менее 2 лет. Все пациентки подписывали информированное согласие на участие в исследовании. В исследование не включались пациентки с вторичным остеоартрозом, беременные, кормящие матери или женщины детородного возраста, отказывающиеся использовать методы контрацепции в течение периода исследования, пациенты, проводившие внутрисуставные инъекции глюкокортикостероидов в течение 4 недель до начала исследования, пациентки, не желающие прекратить прием НПВП и хондропротекторов на время исследования, пациентки с тяжелыми сопутствующими заболеваниями (ИБС, сердечная недостаточность, цереброваскулярные заболевания, сахарный диабет), а также пациентки, имеющие нарушение функции печени и почек.
Пациенты были рандомизированы в две подгруппы: больные основной группы (25 больных) получали Бора–Бора, пациенты группы сравнения (20 больных) – только анальгетики. Длительность терапии составила 2 месяца. Пациенты были обследованы трижды. Во время первичного обследования проводилось подписание информированного согласия, определение критериев включения/исключения (стадия гонартроза, интенсивность боли, функциональная активность). При включении пациента в исследование проводился забор крови для анализов (биохимические показатели функции почек и печени, общий анализ крови, ЭКГ). Все пациенты вели дневники, где указывали потребность в анальгетиках (количество таблеток парацетамола ежедневно), цифры АД. Бора–Бора назначался в течение двух месяцев по одной капсуле 3 раза в сутки. Повторное обследование проводилось через месяц (визит 1), заключительный визит осуществляли через 2 месяца (визит 2). Эффективность Бора–Бора оценивали по общепринятым критериям оценки препаратов для лечения остеоартроза: суммарному индексу Лекена, боли в покое по визуально–аналоговой шкале (ВАШ), при ходьбе (по ВАШ), потребности в анальгетике (парацетамол), оценке эффективности лечения врачом и больным. Больные двух групп были сопоставимы по возрасту, полу, основным клиническим проявлениям (табл. 1).
Результаты и обсуждение
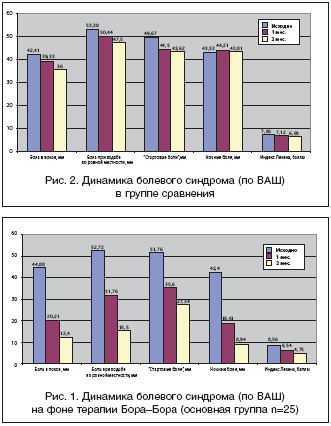
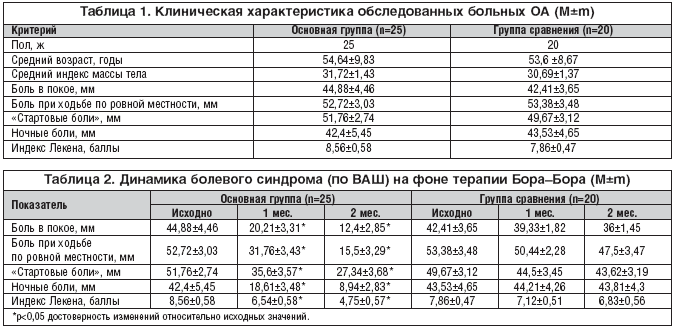
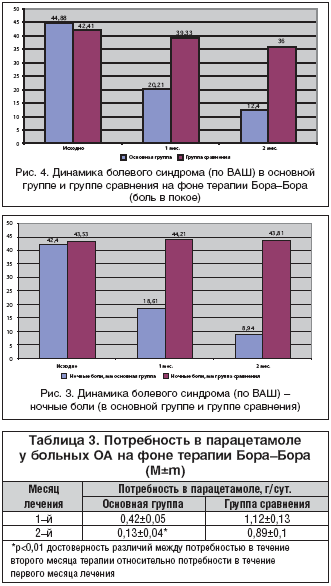
На фоне терапии Бора–Бора выявлена отчетливая положительная динамика – уменьшение индекса Лекена на протяжении всего времени наблюдения. Через 1 мес. от начала лечения было отмечено увеличение функциональной подвижности пораженных суставов. У всех пациентов, получавших Бора–Бора, подтверждено уменьшение и изменение характера болевого синдрома, оцениваемого пациентами по ВАШ. Изучали интенсивность болей в покое, при ходьбе по ровной местности, наличие «стартовой боли» в исследуемом коленном суставе, интенсивность ночных болей (табл. 2). Анальгетический эффект достигался на 2–й неделе терапии и нарастал к 4–й неделе. Выявлено достоверное уменьшение боли в покое (р<0,05), ночной боли (р<0,05), болей при физической нагрузке (р<0,05), «стартовой боли» (р<0,05) при приеме Бора–Бора (рис. 1–4).
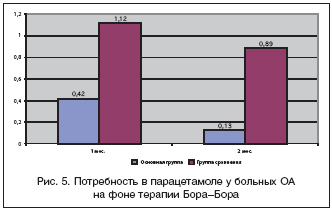
В основной группе отмечено уменьшение числа пациентов, нуждающихся в дополнительном приеме парацетамола, что позволило со 2–й недели проводить монотерапию Бора–Бора у 60% больных, у 40% больных отмечено достоверное (p<0,01) уменьшение потребляемой дозы парацетамола.
В группе сравнения, получавшей парацетамол при болях, отмечено уменьшение потребляемой дозы к 6–й неделе, однако изменение дозы препарата было статистически не значимо (табл. 3, рис. 5).
В основной группе у больных без артериальной гипертензии не было зафиксировано повышения артериального давления, у больных с артериальной гипертензией не было увеличения дозы гипотензивных препаратов.
На протяжении всего периода исследования переносимость Бора–Бора была хорошей, нежелательные явления при приеме Бора–Бора отмечались у 4 (2%) пациентов в виде неприятных ощущений в эпигастральной области. Однако эти симптомы были слабо выражены, непродолжительны и не потребовали прекращения лечения. Все лабораторные параметры и показатели ЭКГ в процессе терапии не отличались от исходных.
Положительный (хороший и умеренный) эффект терапии по оценке врача отмечен у 85% пролеченных больных. По мнению пациентов, положительные результаты лечения достигнуты в 90% наблюдений.
Таким образом, проведенное исследование показало терапевтическую эффективность Бора–Бора в лечении гонартроза. Препарат оказывает выраженный симптомо–модифицирующий эффект, проявляющийся значительным уменьшением болевого синдрома, увеличением функциональной активности пораженных суставов, значительным снижением дозы анальгетика. Бора–Бора характеризовался хорошей переносимостью.
Литература
1. Балабанова Р.М., Запрягаева М.Е. Роль нестероидных противовоспалительных препаратов в комплексной терапии остеоартроза // CONSILIUM MEDICUM. –2006.–№12.–С.1030–1033.
2. Бадокин В.В. Медикаментозная терапия первичного (идиопатического) остеоартроза //Русский медицинский журнал.–2003.–№11(5).–С.243–245.
3. Каратеев А.Е. Профилактика опасных осложнений со стороны желудочно–кишечного тракта при лечении НПВП в клинической практике: проблемы и их решение// Клиническая фармакология и терапия.– 2007.–№16.–С.81–84.
4. Коршунов Н.И., Ершова О.Б. Современные подходы к фармакотерапии остеоартроза //CONSILIUM MEDICUM.– 2006.–№ 2.–С.34–38.
5. Лесняк О.М. Боль при остеоартрите крупных суставов//CONSILIUM MEDICUM.–2006.–№2.–С. 34–38.
6. Мазуров В.И., Онущенко И.А. Остеоартроз.–Санкт–Петербург: СПбМАНО, 2000.–116с.
7. Стрюк Р.И. Структурно–модифицирующая терапия остеартроза // Фарматека.– 2006.–№9.С.1–5.
8. Leeb B.Scbweizer H. et al. A metaanalysis of chondroitin sulfate in the treatment of osteoarthritis.//Y Rheumatol.–2000.–№27.–С.205–211.
9. Jobnson AG, Nguyen TV et al. Do nonsteroidal anti–inflammatory drugs affect blood pressure? A meta–analysis.// Ann Intern Med.–1994.–№121.–С.289–300.
10. Pope YE, AndersonYY et al. A meta–analysis of tbe effect of nonsteroidal anti– inflammatory drugs on blood pressure.// ArcbIntern Med.–1993.–№153.–С.477–484.
11. Mazieres B, Combe B,et al Chondroitin sulfate in osteoarthritis of the knee: a prospective double blind placebo–controlled multicenter clinical study.//Y Rheum.– 2001.–№28.–С.173–81.
12.Mc Alindon TE, La Valley MP et al.Glucosamine and chondroitin for the treatment of osteoarthritis. A systematic quality assessment and meta–analysis.//YAMA.–2000.–№283–С.1469–75.












