–С–Њ–ї—М —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ –љ–µ–њ—А–Є—П—В–љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –Њ—Б—В—А—Л—Е –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —З–µ–ї–Њ–≤–µ–Ї–∞. –Э–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –њ—А–Є—З–Є–љ—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –±–Њ–ї—М –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Б–µ—А—М–µ–Ј–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞, –њ—А–µ–і–Њ–њ—А–µ–і–µ–ї—П—П —В—П–ґ–µ—Б—В—М —Б—В—А–∞–і–∞–љ–Є–є, —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –Є –љ–∞—А—Г—И–µ–љ–Є–µ —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –∞–і–∞–њ—В–∞—Ж–Є–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–∞–ї–Є—З–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –±–Њ–ї–Є —Б–∞–Љ–Њ –њ–Њ —Б–µ–±–µ –≤—Л—Б—В—Г–њ–∞–µ—В –≤ —А–Њ–ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞, –њ–Њ–≤—Л—И–∞—О—Й–µ–≥–Њ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –≥–Є–±–µ–ї–Є –њ–∞—Ж–Є–µ–љ—В–∞ (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Б–Є–Љ–њ–∞—В–Є–Ї–Њ––∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л –љ–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ї–∞—В–∞—Б—В—А–Њ—Д) [1,2]. –Э–µ–Љ–∞–ї–Њ–≤–∞–ґ–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л –Ј–∞—З–∞—Б—В—Г—О –Њ—Ж–µ–љ–Є–≤–∞—О—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –Є –Ї–≤–∞–ї–Є—Д–Є–Ї–∞—Ж–Є—О –≤—А–∞—З–∞ –Є–Љ–µ–љ–љ–Њ –њ–Њ –±—Л—Б—В—А–Њ—В–µ –Є –Ї–∞—З–µ—Б—В–≤—Г –ї–µ—З–µ–љ–Є—П –±–Њ–ї–Є. –Я–Њ—Н—В–Њ–Љ—Г –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–Є – –Ї–∞–Ї–Њ–є –±—Л –љ–µ –±—Л–ї–∞ –µ–µ —Н—В–Є–Њ–ї–Њ–≥–Є—П, –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –њ–µ—А–≤–Њ–Њ—З–µ—А–µ–і–љ–Њ–є –Ј–∞–і–∞—З–µ–є, —Б—В–Њ—П—Й–µ–є –њ–µ—А–µ–і –≤—А–∞—З–Њ–Љ –ї—О–±–Њ–є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ—Б—В–Є. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б—В—А–µ–Љ–ї–µ–љ–Є–µ –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –±—Л—Б—В—А–µ–µ –њ–Њ–ї—Г—З–Є—В—М –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Ј–∞—З–∞—Б—В—Г—О –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–ї–Є—З–љ—Л–Љ –Њ—И–Є–±–Ї–∞–Љ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Ж–µ–љ–∞ –Ї–Њ—В–Њ—А—Л—Е – —А–∞–Ј–≤–Є—В–Є–µ —Б–µ—А—М–µ–Ј–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Э–∞–Є–±–Њ–ї–µ–µ –њ–Њ–њ—Г–ї—П—А–љ—Л–Љ –Ї–ї–∞—Б—Б–Њ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –Ї–Њ—В–Њ—А—Л–є –њ–Њ–≤—Б–µ–Љ–µ—Б—В–љ–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є, —П–≤–ї—П—О—В—Б—П –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я). –Ш—Е –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–Љ–Є –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–∞–Љ–Є —П–≤–ї—П–µ—В—Б—П —Е–Њ—А–Њ—И–Њ –і–Њ–Ї–∞–Ј–∞–љ–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М (–Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –±–Њ–ї–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –ї–Њ–Ї–∞–ї—М–љ—Л–Љ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ), –њ—А–Њ—Б—В–Њ—В–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Є —Д–Є–љ–∞–љ—Б–Њ–≤–∞—П –і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М [3,4]. –Т —Г–Љ–µ–ї—Л—Е —А—Г–Ї–∞—Е –Њ–њ—Л—В–љ–Њ–≥–Њ —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–∞ –Э–Я–Т–Я —П–≤–ї—П—О—В—Б—П –њ–Њ––љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –і–µ–є—Б—В–≤–µ–љ–љ—Л–Љ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–Њ–Љ –ї–µ—З–µ–љ–Є—П –±–Њ–ї–Є —Б–∞–Љ–Њ–≥–Њ —А–∞–Ј–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞. –Э–Њ, —Б –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Є–Љ–µ–љ–љ–Њ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Э–Я–Т–Я —Б–≤—П–Ј–∞–љ–Њ –љ–∞–Є–±–Њ–ї—М—И–µ–µ —З–Є—Б–ї–Њ —Б–µ—А—М–µ–Ј–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —Н—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ [4–6].
–Ю–і–љ–∞–Ї–Њ —П–≤–ї—П–µ—В—Б—П –ї–Є —А–∞–Ј–≤–Є—В–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–µ–Є–Ј–±–µ–ґ–љ—Л–Љ —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Э–Я–Т–Я –Є–ї–Є –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –љ–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н—В–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ —Г—З–µ—В–Њ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є –Є—Е –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Њ–є? –Э–∞ –љ–∞—И –≤–Ј–≥–ї—П–і, —Н—В–Њ –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –≤–∞–ґ–љ—Л–є –≤–Њ–њ—А–Њ—Б, —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–Є—О –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ–Њ—Б–≤—П—Й–µ–љ–∞ –љ–∞—Б—В–Њ—П—Й–∞—П —А–∞–±–Њ—В–∞.
–Э–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ
–Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Э–Я–Т–Я
–Ъ –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –Њ—И–Є–±–Њ–Ї –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Э–Я–Т–Я —Б–ї–µ–і—Г–µ—В –Њ—В–љ–µ—Б—В–Є –Є—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤ –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—А–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤ —Н—В–Њ–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –≥—А—Г–њ–њ—Л [4–6].
–Т–µ—А–Њ—П—В–љ–Њ—Б—В—М –њ—А–µ–≤—Л—И–µ–љ–Є—П –і–Њ–Ј—Л –Э–Я–Т–Я –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–∞, –µ—Б–ї–Є –Є—Е –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –±–Њ–ї–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —В–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є, –Ї–Њ–≥–і–∞ –µ–µ –≥–µ–љ–µ–Ј –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ –љ–µ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –≤–µ—Б—М–Љ–∞ —З–∞—Б—В–Њ–є –Њ—И–Є–±–Ї–Њ–є —П–≤–ї—П–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Э–Я–Т–Я –њ—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–Є —В–∞–Ї–Є—Е —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, –Ї–∞–Ї –њ–Њ—Б—В–≥–µ—А–њ–µ—В–Є—З–µ—Б–Ї–∞—П –Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є—П [7]. –Ґ–∞–Ї, –≤ –Љ–∞—Б—И—В–∞–±–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Gore M. –Є —Б–Њ—В—А. (2007) –Њ—Ж–µ–љ–Є–≤–∞–ї—Б—П —Е–∞—А–∞–Ї—В–µ—А –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–љ–Њ–є —Г 16690 –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б –љ–µ –≤—Л–Ј—Л–≤–∞—О—Й–µ–є —Б–Њ–Љ–љ–µ–љ–Є—П «—З–Є—Б—В–Њ–є» –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї—М—О. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –ї–Є—И—М –Љ–µ–љ—М—И–∞—П —З–∞—Б—В—М –±–Њ–ї—М–љ—Л—Е –њ–Њ–ї—Г—З–∞–ї–∞ –∞–і–µ–Ї–≤–∞—В–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б —Е–Њ—А–Њ—И–Њ –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є –њ—А–Є –і–∞–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О – —В—А–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л 16,6%, –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л 2––є –≥–µ–љ–µ—А–∞—Ж–Є–Є 11,0%, –∞–љ—В–Є–Ї–Њ–љ–≤—Г–ї—М—Б–∞–љ—В—Л 12,2%. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Љ–∞–ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –Э–Я–Т–Я –Є –Њ–њ–Є–Њ–Є–і—Л –њ—А–Є–љ–Є–Љ–∞–ї–Є 43,1 –Є 8,5% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [8].
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–∞–ґ–µ –≤ —Б–Є—В—Г–∞—Ж–Є—П—Е, –Ї–Њ–≥–і–∞ —А–∞–Ј–≤–Є—В–Є–µ –±–Њ–ї–Є –њ—А—П–Љ–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —В–Ї–∞–љ–µ–≤—Л–Љ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ, —Г –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є —З–∞—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Э–Я–Т–Я –Љ–Њ–≥—Г—В –љ–µ –і–∞–≤–∞—В—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П. –Э–∞–њ—А–Є–Љ–µ—А, –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —Б—Г—Б—В–∞–≤–Њ–≤ –ї–Є—И—М –њ—А–Є–Љ–µ—А–љ–Њ –њ–Њ–ї–Њ–≤–Є–љ–∞ –±–Њ–ї—М–љ—Л—Е, –њ–Њ –і–∞–љ–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї —З–Є—Б–ї—Г «—Е–Њ—А–Њ—И–Є—Е –Њ—В–≤–µ—В—З–Є–Ї–Њ–≤» –љ–∞ –Э–Я–Т–Я, —В.–µ. —Б–љ–Є–ґ–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–Є –Є —Г–ї—Г—З—И–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П –і–Њ—Б—В–Є–≥–∞–µ—В —Г –љ–Є—Е 50% –Є –±–Њ–ї–µ–µ [9,10]. –Я—А–Є —Н—В–Њ–Љ –Њ—Ж–µ–љ–Є—В—М —А–µ–∞–ї—М–љ—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–Њ–≥–Њ –Є–ї–Є –Є–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Є–Ј –≥—А—Г–њ–њ—Л –Э–Я–Т–Я –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —Г —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е) –Љ–Њ–ґ–љ–Њ –љ–µ —А–∞–љ–µ–µ, —З–µ–Љ —З–µ—А–µ–Ј 7–14 –і–љ–µ–є –њ–Њ—Б–ї–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –µ–≥–Њ –њ–Њ–ї–љ–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л [4].
–Я—А–µ–Њ–і–Њ–ї–µ–љ–Є–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Э–Я–Т–Я –њ—Г—В–µ–Љ —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–і–±–Њ—А–∞ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–ї–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –і–Њ–Ј—Л (–≤–њ–ї–Њ—В—М –і–Њ —Б—Г–њ—А–∞—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є), —П–≤–ї—П–µ—В—Б—П –њ–Њ—А–Њ—З–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–Њ–є, —З—А–µ–≤–∞—В–Њ–є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Т–Њ–Њ–±—Й–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Э–Я–Т–Я –≤ –і–Њ–Ј–∞—Е, –њ—А–µ–≤—Л—И–∞—О—Й–Є—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ, –љ–µ –Љ–Њ–ґ–µ—В —Б—З–Є—В–∞—В—М—Б—П —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ, —З—В–Њ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Б–≤—П–Ј–∞–љ–Њ —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —З–µ—В–Ї–Є—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ –Є—Е –±–Њ–ї—М—И–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ —Б—А–µ–і–љ–Є–Љ–Є –Є –≤—Л—Б–Њ–Ї–Є–Љ–Є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є. –Ґ–∞–Ї, –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ 4––љ–µ–і–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Э–Я–Т–Я –њ—А–Є —А–∞–љ–љ–µ–Љ –†–Р (n=297) –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–Є–Љ–µ—Б—Г–ї–Є–і–∞ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 200 –Є 400 –Љ–≥, –Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 100 –Є 200 –Љ–≥. –•–Њ—В—П –≤ —Ж–µ–ї–Њ–Љ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Э–Я–Т–Я –±—Л–ї –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Е–Њ—А–Њ—И–Є–Љ – 50% –Є –±–Њ–ї–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –±–Њ–ї–Є (–њ–Њ —И–Ї–∞–ї–µ –Т–Р–®) –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Г 30–40% –±–Њ–ї—М–љ—Л—Е, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л –њ–Њ –і–µ–є—Б—В–≤–Є—О –Љ–µ–ґ–і—Г —Б—А–µ–і–љ–Є–Љ–Є –Є –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ [11].
–Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Dougados M. –Є —Б–Њ—В—А., –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞ –≤ –і–Њ–Ј–µ 15 –Є 22,5 –Љ–≥/—Б—Г—В. (–≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ –Є –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ–Њ–Љ 20 –Љ–≥/—Б—Г—В.) —Г 473 –±–Њ–ї—М–љ—Л—Е –Р–°. –Р–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞ –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Є —Б–Њ—Б—В–∞–≤–Є–ї —З–µ—А–µ–Ј 6 –љ–µ–і–µ–ї—М – 32±27 –Љ–Љ –Є – 32±28 –Љ–Љ, —З–µ—А–µ–Ј 1 –≥–Њ–і – 29±28 –Љ–Љ –Є – 31±30 –Љ–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (–њ–Њ –Т–Р–®). –Э–µ –±—Л–ї–Њ —А–∞–Ј–љ–Є—Ж—Л –Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤–ї–Є—П–љ–Є—П –љ–∞ —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є. –°—Г–Љ–Љ–∞—А–љ–Њ–µ —З–Є—Б–ї–Њ «–Њ—В–≤–µ—В—З–Є–Ї–Њ–≤» –љ–∞ —В–µ—А–∞–њ–Є—О –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –≤—Л—Б–Њ–Ї–Њ–є –Є —Б–≤–µ—А—Е–≤—Л—Б–Њ–Ї–Њ–є –і–Њ–Ј—Л –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞ —В–∞–Ї–ґ–µ –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Њ—Б—М –љ–Є —З–µ—А–µ–Ј 6 –љ–µ–і–µ–ї—М, –љ–Є —З–µ—А–µ–Ј 12 –Љ–µ—Б—П—Ж–µ–≤ –Њ—В –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П [12].
–° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є—П, —З—В–Њ —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –і–Њ–Ј—Л –Э–Я–Т–Я –љ–µ–Є–Ј–±–µ–ґ–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –њ–Њ—Н—В–Њ–Љ—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї —З–Є—Б–ї—Г –Њ–±—Й–µ–њ—А–Є–Ј–љ–∞–љ–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є. –≠—В–Њ –Њ—В–љ–Њ—Б–Є—В—Б—П –Є –Ї —В–µ–Љ –Э–Я–Т–Я, –Ї–Њ—В–Њ—А—Л–µ –≤ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е —Б—З–Є—В–∞—О—В—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є –Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В—Б—П –і–ї—П –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞. –Э–∞–њ—А–Є–Љ–µ—А, –Є–±—Г–њ—А–Њ—Д–µ–љ, –Ї–Њ—В–Њ—А—Л–є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–≥–Њ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞, –≤ –≤—Л—Б–Њ–Ї–Є—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ј–∞—Е (–±–Њ–ї–µ–µ 1800 –Љ–≥/—Б—Г—В.) –≤—Л–Ј—Л–≤–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –Њ–њ–∞—Б–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б—В–Њ–ї—М –ґ–µ —З–∞—Б—В–Њ, –Ї–∞–Ї –Є –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ [13].
–Т–µ—Б—М–Љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–Њ–є –Ј–љ–∞—З–µ–љ–Є—П —Н—В–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Є—Б–Ї–∞ —П–≤–ї—П–µ—В—Б—П —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ Lewis S. (2002). –Т —Н—В–Њ–є —А–∞–±–Њ—В–µ, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –Є–Ј—Г—З–µ–љ–Є–Є –≥—А—Г–њ–њ—Л –Є–Ј 2472 –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–≤–Є–≤—И–Є–Љ—Б—П –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ–Љ (5877 –Ї–Њ–љ—В—А–Њ–ї—М), –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї (–њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О –Њ—В–љ–Њ—И–µ–љ–Є—П —И–∞–љ—Б–Њ–≤, –Ю–®) —А–∞–Ј–≤–Є—В–Є—П —Н—В–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –і–Њ–Ј—Л —А–∞–Ј–ї–Є—З–љ—Л—Е –Э–Я–Т–Я, –∞ —В–∞–Ї–ґ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ –і–Њ 100 –Љ–≥ –Ю–® —Б–Њ—Б—В–∞–≤–ї—П–ї 2,2, –Њ—В 100 –і–Њ 150 –Љ–≥ – 3,2, –∞ 150 –Љ–≥ –Є –≤—Л—И–µ – 12,2. –Р–љ–∞–ї–Њ–≥–Є—З–љ–∞—П –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ—Б—В—М –±—Л–ї–Є –њ–Њ–Ї–∞–Ј–∞–љ–∞ –і–ї—П –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ–∞, –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ–∞ –Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ [14].
–Ю–і–љ–∞–Ї–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –њ—А–µ–≤—Л—И–µ–љ–Є–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –Э–Я–Т–Я – –Ї —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –љ–µ—А–µ–і–Ї–∞—П —Б–Є—В—Г–∞—Ж–Є—П, —Б –Ї–Њ—В–Њ—А–Њ–є –њ—А–Є—Е–Њ–і–Є—В—Б—П —Б—В–∞–ї–Ї–Є–≤–∞—В—М—Б—П –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Ґ–∞–Ї, —Б—А–µ–і–Є 3088 –±–Њ–ї—М–љ—Л—Е –†–Р, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –Є –њ—А–Њ—И–µ–і—И–Є—Е —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤ –Ї–ї–Є–љ–Є–Ї–µ –У–£ –Ш–љ—Б—В–Є—В—Г—В —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –†–Р–Ь–Э (1996–2005 –≥–≥.), 494 (15,9%) –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –і–Њ–Ј—Г –±–Њ–ї–µ–µ 150 –Љ–≥/—Б—Г—В., –∞ 85 –±–Њ–ї—М–љ—Л—Е (2,7%) – –±–Њ–ї–µ–µ 200 –Љ–≥/—Б—Г—В. [15].
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–Њ–і–Њ–±–љ—Л—Е —Б–ї—Г—З–∞–µ–≤ —Б–≤—П–Ј–∞–љ–Њ —Б —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є–µ–Љ, –Ї–Њ–≥–і–∞ –њ–∞—Ж–Є–µ–љ—В—Л, –љ–µ –њ–Њ–ї—Г—З–∞—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–є –Є–Љ –і–Њ–Ј—Л –Э–Я–Т–Я, —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞—О—В –µ–µ, –љ–µ —Б—В–∞–≤—П –≤ –Є–Ј–≤–µ—Б—В–љ–Њ—Б—В—М –≤—А–∞—З–∞. –Т –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –њ—А–Њ–±–ї–µ–Љ–∞ —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ—Б–ї–Њ–ґ–љ—П–µ—В—Б—П —В–µ–Љ, —З—В–Њ –≤—Б–µ –њ—А–µ–њ–∞—А–∞—В—Л —Н—В–Њ–є –≥—А—Г–њ–њ—Л, –≤–Ї–ї—О—З–∞—П –љ–∞–Є–±–Њ–ї–µ–µ —В–Њ–Ї—Б–Є—З–љ—Л–µ, –ї–µ–≥–Ї–Њ –і–Њ—Б—В—Г–њ–љ—Л –±–Њ–ї—М–љ—Л–Љ, –∞ –љ–∞ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –Њ—З–µ–љ—М –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–µ—И–µ–≤—Л—Е –≥–µ–љ–µ—А–Є–Ї–Њ–≤ –Э–Я–Т–Я (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞).
–°–∞–Љ–Њ–ї–µ—З–µ–љ–Є–µ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Њ–є –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л—Е –њ—А–Є—З–Є–љ —А–∞–Ј–≤–Є—В–Є—П –Њ–њ–∞—Б–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т–µ–і—М —Г—А–Њ–≤–µ–љ—М –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ —А–Є—Б–Ї–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Љ—П–≥–Ї–Њ –≥–Њ–≤–Њ—А—П, –Њ—Б—В–∞–≤–ї—П–µ—В –ґ–µ–ї–∞—В—М –ї—Г—З—И–µ–≥–Њ. –Ґ–∞–Ї, –њ–Њ –і–∞–љ–љ—Л–Љ Roumie C. –Є Griffin M. (2004), 20–30% –њ–Њ–ґ–Є–ї—Л—Е –∞–Љ–µ—А–Є–Ї–∞–љ—Ж–µ–≤ –µ–ґ–µ–і–љ–µ–≤–љ–Њ –њ—А–Є–љ–Є–Љ–∞—О—В –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є, –њ—А–Є —Н—В–Њ–Љ –±–Њ–ї–µ–µ 60% –Є–Ј –љ–Є—Е –љ–µ –Љ–Њ–≥—Г—В –љ–∞–Ј–≤–∞—В—М –і–µ–є—Б—В–≤—Г—О—Й–µ–µ –≤–µ—Й–µ—Б—В–≤–Њ, –≤—Е–Њ–і—П—Й–µ–µ –≤ —Б–Њ—Б—В–∞–≤ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –∞ 40% —Б—З–Є—В–∞—О—В —Н—В–Є –ї–µ–Ї–∞—А—Б—В–≤–∞ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є [16]. –С–ї–Є–Ј–Ї–Є–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є Wilcox H. –Є —Б–Њ—В—А. (2005), –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–Є–µ –∞–љ–∞–ї–Є–Ј –і–≤—Г—Е –Њ–њ—А–Њ—Б–Њ–≤ –ґ–Є—В–µ–ї–µ–є –°–®–Р, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ 1997 –Є 2002 –≥–≥. (—Б—Г–Љ–Љ–∞—А–љ–Њ 9062 —А–µ—Б–њ–Њ–љ–і–µ–љ—В–Њ–≤). –°–Њ–≥–ї–∞—Б–љ–Њ –Є—Е —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Э–Я–Т–Я –≤—А–µ–Љ—П –Њ—В –≤—А–µ–Љ–µ–љ–Є (–≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л–µ, —В.–љ. –Ю–Ґ–°) –њ—А–Є–љ–Є–Љ–∞–ї–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Њ–њ—А–Њ—И–µ–љ–љ—Л—Е – 54 –Є 83% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –£–і–Є–≤–Є—В–µ–ї—М–љ–Њ, –љ–Њ 47 –Є 30% –Њ–њ—А–Њ—И–µ–љ–љ—Л—Е —Б—З–Є—В–∞–ї–Є –Ю–Ґ–° –Э–Я–Т–Я –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є, –Є —В–Њ –ґ–µ –Њ–њ–∞—Б–љ–Њ–µ –Ј–∞–±–ї—Г–ґ–і–µ–љ–Є–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –±–Њ–ї–µ–µ —З–µ–Љ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –ї–Є—Ж, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —А–µ—Ж–µ–њ—В—Г—А–љ—Л–µ –Э–Я–Т–Я. –Я—А–Є —Н—В–Њ–Љ 30% —А–µ—Б–њ–Њ–љ–і–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л–µ –Э–Я–Т–Я, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Є—Е –≤ –і–Њ–Ј–Є—А–Њ–≤–Ї–∞—Е, –њ—А–µ–≤—Л—И–∞—О—Й–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л–µ (!) [17].
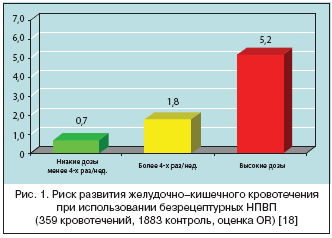
–Ъ —З–µ–Љ—Г –њ—А–Є–≤–Њ–і–Є—В —Н—В–∞ –Њ—И–Є–±–Ї–∞, –љ–∞–≥–ї—П–і–љ–Њ –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ Lewis J. –Є —Б–Њ—В—А. (2005), –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –њ–Њ–≤—Л—И–µ–љ–Є–µ —А–Є—Б–Ї–∞ –Њ–њ–∞—Б–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –ї–Є—Ж, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л–µ –Э–Я–Т–Я. –†–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Њ–є —А–∞–±–Њ—В—Л, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л–µ –љ–∞ –∞–љ–∞–ї–Є–Ј–µ 359 –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е —Б–ї—Г—З–∞–µ–≤ –Ц–Ъ–Ъ, –њ–µ—А—Д–Њ—А–∞—Ж–Є–є –Є –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Њ—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Ц–Ъ–Ґ (1889 –Ї–Њ–љ—В—А–Њ–ї—М) –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ—А–Є–µ–Љ –Ю–Ґ–° –Э–Я–Т–Я –≤ –Њ—З–µ–љ—М –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е –Є –љ–µ —З–∞—Й–µ 4 —А–∞–Ј –≤ –љ–µ–і–µ–ї—О –љ–µ –њ–Њ–≤—Л—И–∞–ї —А–Є—Б–Ї —Б–µ—А—М–µ–Ј–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є: –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї (–Ю–†) —Б–Њ—Б—В–∞–≤–Є–ї 0,67 –Є 0,74. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є–µ–Љ –Ю–Ґ–° –Э–Я–Т–Я –±–Њ–ї–µ–µ 4 —А–∞–Ј –≤ –љ–µ–і–µ–ї—О –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї—Б—П —Б —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ – 1,83 (1,14–2,95). –°–∞–Љ–Њ–µ –≤–∞–ґ–љ–Њ–µ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ю–Ґ–° –Э–Я–Т–Я –≤ –і–Њ–Ј–∞—Е, –њ—А–µ–≤—Л—И–∞—О—Й–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л–µ –і–ї—П –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П, –њ—А–Є–≤–Њ–і–Є–ї –Ї –Њ—З–µ–љ—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є – –Ю–† 5,21 (2,32–11,7) [18] (—А–Є—Б. 1).
–Ш–љ–Њ–≥–і–∞ –њ—А–µ–≤—Л—И–µ–љ–Є–µ –і–Њ–Ј—Л –Э–Я–Т–Я, —Б–≤—П–Ј–∞–љ–љ–Њ–µ —Б –љ–µ–≤–љ–Є–Љ–∞—В–µ–ї—М–љ—Л–Љ –Є–ї–Є –љ–µ–±—А–µ–ґ–љ—Л–Љ –Њ—В–љ–Њ—И–µ–љ–Є–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞ –Ї —Г–Ї–∞–Ј–∞–љ–Є—П–Љ –≤—А–∞—З–∞, –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Ї–∞—В–∞—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–Љ –Њ—И–Є–±–Ї–∞–Љ. –Р–≤—В–Њ—А—Г –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —А–∞–Ј –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М –љ–∞–±–ї—О–і–∞—В—М —Б–ї–µ–і—Г—О—Й—Г—О —Б–Є—В—Г–∞—Ж–Є—О. –С–Њ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ–Њ–њ—Г–ї—П—А–љ—Л–є –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –≥–µ–љ–µ—А–Є–Ї –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞, –Є–Љ–µ—О—Й–Є–є –і–Њ–Ј–Є—А–Њ–≤–Ї—Г 25 –Љ–≥, —Б —Г–Ї–∞–Ј–∞–љ–Є–µ–Љ –њ—А–Є–љ–Є–Љ–∞—В—М —Н—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –њ–Њ 2 —В–∞–±. 3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є (—Б—Г–Љ–Љ–∞—А–љ–∞—П –і–Њ–Ј–∞ 150 –Љ–≥/—Б—Г—В.). –С–Њ–ї—М–љ—Л–µ –њ—А–Є–Њ–±—А–µ—В–∞–ї–Є –њ—А–µ–њ–∞—А–∞—В –≤ –∞–њ—В–µ–Ї–∞—Е, –љ–µ –њ—А–Є–і–∞–≤–∞—П –Ј–љ–∞—З–µ–љ–Є—П —Г–Ї–∞–Ј–∞–љ–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–µ, –њ–Њ–ї—Г—З–∞–ї–Є –≤ –Є—В–Њ–≥–µ –љ–∞ —А—Г–Ї–Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–—А–µ—В–∞—А–і (100 –Љ–≥), –Є –Ј–∞—В–µ–Љ –њ—А–Є–љ–Є–Љ–∞–ї–Є –µ–≥–Њ –њ–Њ 2 —В–∞–±. 3 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є, —В.–µ. 600 –Љ–≥/—Б—Г—В. (!).
–Я–Њ–і–Њ–±–љ—Л–є —Б–ї—Г—З–∞–є –Њ–њ–Є—Б–∞–љ –У—А–Є–љ—М–Ї–Њ –Р.–Т. –Є –Р–Ј–∞—А–Њ–≤–Њ–є –Х.–Р. –£ –±–Њ–ї—М–љ–Њ–≥–Њ, –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ–ї—Г—З–∞–≤—И–µ–≥–Њ –µ–ґ–µ–і–љ–µ–≤–љ–Њ 500–600 –Љ–≥ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞, –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —П–Ј–≤—Л –ґ–µ–ї—Г–і–Ї–∞ (1,5 —Б–Љ) –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є – –Ф–Я–Ъ (2,0 —Б–Љ), —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–≤—И–Є—Е—Б—П –њ–Њ–≤—В–Њ—А–љ—Л–Љ–Є –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П–Љ–Є, —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ–Њ–є –∞–љ–µ–Љ–Є–Є (—Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Э–≤ –і–Њ 60 –≥/–ї) [19].
–І–∞—Б—В—М –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ—Б—В–Є –Ј–∞ –њ–Њ–і–Њ–±–љ—Л–µ –Њ—И–Є–±–Ї–Є –ї–µ–ґ–Є—В, –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, –Є –љ–∞ –ї–µ—З–∞—Й–µ–Љ –≤—А–∞—З–µ. –Э–µ—А–µ–і–Ї–Њ –≤ –Є—Б—В–Њ—А–Є—П—Е –±–Њ–ї–µ–Ј–љ–Є –Є –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –Ї–∞—А—В–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Љ–Њ–ґ–љ–Њ —Г–≤–Є–і–µ—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –Э–Я–Т–Я –≤ –њ–Њ–і–Њ–±–љ–Њ–Љ –≤–Є–і–µ: «–Э–Я–Т–Я –њ—А–Є –±–Њ–ї—П—Е», «–Я—А–Є –±–Њ–ї—П—Е – –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ, –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ, –љ–Є–Љ–µ—Б—Г–ї–Є–і» –Є —В.–і., –±–µ–Ј –Ї–Њ–љ–Ї—А–µ—В–Є–Ј–∞—Ж–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –і–Њ–Ј—Л –Є —А–µ–ґ–Є–Љ–∞ –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Ш–Љ–µ–љ–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є —В–∞–Ї–Њ–≥–Њ —А–Њ–і–∞ –Љ–Њ–≥—Г—В —Б—В–∞—В—М –њ—А–Є—З–Є–љ–Њ–є –±–µ–Ј–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ –≤—Б–µ–Љ–Є –≤—Л—В–µ–Ї–∞—О—Й–Є–Љ–Є –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ–Є. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Э–Я–Т–Я, –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ —З–µ—В–Ї–Њ —Г–Ї–∞–Ј–∞—В—М –і–Њ–Ј—Г –Є –Ї—А–∞—В–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞: «—Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± 200 –Љ–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є», «–њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є –±–Њ–ї–Є – –њ—А–Є–µ–Љ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ 200 –Љ–≥, –љ–µ –±–Њ–ї–µ–µ 4 –њ—А–Є–µ–Љ–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї» –Є —В.–і. –Т–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е –±–Њ–ї—М–љ–Њ–≥–Њ —Б–ї–µ–і—Г–µ—В –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—В—М –Њ–± –Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–µ–≤—Л—И–µ–љ–Є—П —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л—Е –і–Њ–Ј –Э–Я–Т–Я, –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е, –∞ —В–∞–Ї–ґ–µ –Њ–љ –і–Њ–ї–ґ–µ–љ –±—Л—В—М –њ–Њ—Б—В–∞–≤–ї–µ–љ –≤ –Є–Ј–≤–µ—Б—В–љ–Њ—Б—В—М –Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –і–Њ–њ—Г—Б—В–Є–Љ—Л—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–∞.
–Ъ—Б—В–∞—В–Є, –њ—А–Њ–±–ї–µ–Љ–∞ —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є—П –Ї–∞—Б–∞–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –Э–Я–Т–Я, –љ–Њ –Є –≤–µ—Б—М–Љ–∞ –њ–Њ–њ—Г–ї—П—А–љ–Њ–≥–Њ –≤ –°–®–Р –Є –Ч–∞–њ–∞–і–љ–Њ–є –Х–≤—А–Њ–њ–µ «–њ—А–Њ—Б—В–Њ–≥–Њ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞» –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ–Њ–≥–Њ —А—П–і–Њ–Љ —Н–Ї—Б–њ–µ—А—В–Њ–≤ –≤ –Ї–∞—З–µ—Б—В–≤–µ «–±–µ–Ј–Њ–њ–∞—Б–љ–Њ–≥–Њ» –њ—А–µ–њ–∞—А–∞—В–∞ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –і–ї—П –ї–µ—З–µ–љ–Є—П —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –±–Њ–ї–Є. –Ю–і–љ–∞–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –≤ –і–Њ–Ј–µ, –ї–Є—И—М –≤ 2,5 —А–∞–Ј–∞ –њ—А–µ–≤—Л—И–∞—О—Й–µ–є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –і–Њ–њ—Г—Б—В–Є–Љ—Г—О (4 –≥/—Б—Г—В.), –њ—А–Є–≤–Њ–і–Є—В –Ї —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–Љ—Г –њ–Њ—А–∞–ґ–µ–љ–Є—О –њ–µ—З–µ–љ–Є. –Э–µ–і–∞—А–Њ–Љ –Є–Љ–µ–љ–љ–Њ –Ј–∞ «–±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ» –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–Њ–Љ –Ј–∞–Ї—А–µ–њ–Є–ї–Њ—Б—М –њ–µ—З–∞–ї—М–љ–Њ–µ –њ–µ—А–≤–Њ–µ –Љ–µ—Б—В–Њ –≤ —Б–њ–Є—Б–Ї–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е —Д–∞—В–∞–ї—М–љ—Г—О –Њ—Б—В—А—Г—О –њ–µ—З–µ–љ–Њ—З–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М [20]. –Ґ–∞–Ї, –≤ —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е —Ж–µ–љ—В—А–∞—Е –°–®–Р, –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є–Ј 662 —Н–њ–Є–Ј–Њ–і–Њ–≤ –Њ—Б—В—А–Њ–є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П –Ј–∞ –њ–µ—А–Є–Њ–і —Б 1998 –њ–Њ 2003 –≥., 275 (42%) –±—Л–ї–Є —Б–≤—П–Ј–∞–љ—Л —Б –њ—А–Є–µ–Љ–Њ–Љ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞. 74 –±–Њ–ї—М–љ—Л—Е (27%) —Б–Ї–Њ–љ—З–∞–ї–Є—Б—М –Њ—В –і–∞–љ–љ–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П, –∞ 23 (8%) –њ–µ—А–µ–љ–µ—Б–ї–Є –њ–µ—А–µ—Б–∞–і–Ї—Г –њ–µ—З–µ–љ–Є. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г 131 –±–Њ–ї—М–љ–Њ–≥–Њ —В—П–ґ–µ–ї—Л–µ –≥–µ–њ–∞—В–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є –љ–µ –±—Л–ї–Є —Б–≤—П–Ј–љ—Л —Б —Б—Г–Є—Ж–Є–і–∞–ї—М–љ—Л–Љ–Є –њ–Њ–њ—Л—В–Ї–∞–Љ–Є, –∞ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В—А–Њ–є –Є–ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є (–Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤ –і–Њ–Ј–∞—Е, –њ—А–µ–≤—Л—И–∞—О—Й–Є—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ) [21].
–Ф—А—Г–≥–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–є –Њ—И–Є–±–Ї–Њ–є –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Э–Я–Т–Я —П–≤–ї—П–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –і–≤—Г—Е –Є –±–Њ–ї–µ–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ. –Т —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —Б–Њ–Ј–љ–∞—В–µ–ї—М–љ—Л–Љ–Є –і–µ–є—Б—В–≤–Є—П–Љ–Є –ї–µ—З–∞—Й–µ–≥–Њ –≤—А–∞—З–∞. –Я–Њ–і–Њ–±–љ–∞—П —Б–Є—В—Г–∞—Ж–Є—П –≤–Њ–Ј–љ–Є–Ї–∞–µ—В, –љ–∞–њ—А–Є–Љ–µ—А, –Ї–Њ–≥–і–∞ –і–ї—П —Г—Б–Є–ї–µ–љ–Є—П –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–∞ —Д–Њ–љ–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ —Б—А–µ–і–љ–µ–є –Є–ї–Є –≤—Л—Б–Њ–Ї–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –Э–Я–Т–Я —Б –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–µ—А–Є–Њ–і–Њ–Љ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П (–љ–∞–њ—А–Є–Љ–µ—А, 15 –Љ–≥ –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞) –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–∞—П —Д–Њ—А–Љ–∞ –і—А—Г–≥–Њ–≥–Њ –Э–Я–Т–Я (–ї–Њ—А–љ–Њ–Ї—Б–Є–Ї–∞–Љ, –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ, –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –Є –і—А.).
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –Э–Я–Т–Я, –Ї—Б—В–∞—В–Є –≥–Њ–≤–Њ—А—П, –љ–µ –і–Њ–Ї–∞–Ј–∞–љ–∞. –Ч–∞—В–Њ —Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –і–≤—Г—Е –Є–ї–Є –±–Њ–ї–µ–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Т —Ж–Є—В–Є—А–Њ–≤–∞–љ–љ–Њ–є –≤—Л—И–µ —А–∞–±–Њ—В–µ Lewis S. –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—А–Є–µ–Љ –Э–Я–Т–Я –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї –Њ–њ–∞—Б–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –і–∞–ґ–µ –≤ –±–Њ–ї—М—И–µ–є –Љ–µ—А–µ, —З–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–≤–µ—А—Е–≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞: —В–∞–Ї, –µ—Б–ї–Є –і–ї—П –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є —Б—А–µ–і–љ–Є–є —А–Є—Б–Ї —Б–Њ—Б—В–∞–≤–ї—П–ї 4,9, —В–Њ –і–ї—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –і–≤—Г—Е –Э–Я–Т–Я – 10,7, –∞ –і–ї—П —В—А–µ—Е –Є –±–Њ–ї–µ–µ – 60,0 (!) [14] (—А–Є—Б. 2).
–Ш–љ–Њ–≥–і–∞ –љ–µ–≥–∞—В–Є–≤–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –і–≤—Г—Е –Є–ї–Є –±–Њ–ї–µ–µ –Э–Я–Т–Я –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–µ—Г—З—В–µ–љ–љ–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –±–Њ–ї—М–љ—Л–Љ «–∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤» – –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –Э–Я–Т–Я. –Ю—Б–Њ–±–µ–љ–љ–Њ —З–∞—Б—В–Њ —В–∞–Ї–∞—П —Б–Є—В—Г–∞—Ж–Є—П –≤–Њ–Ј–љ–Є–Ї–∞–µ—В, –Ї–Њ–≥–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–∞ –Є–Љ–µ—О—В—Б—П —Б–Њ—З–µ—В–∞–љ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є–ї–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ –±–Њ–ї—М (–љ–∞–њ—А–Є–Љ–µ—А, —Б–Њ—З–µ—В–∞–љ–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –≤–љ–Є–Ј—Г —Б–њ–Є–љ—Л –Є –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є). –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –∞–≤—В–Њ—А—Г –љ–µ —А–∞–Ј –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М —Б—В–∞–ї–Ї–Є–≤–∞—В—М—Б—П —Б —Б–Є—В—Г–∞—Ж–Є–µ–є, –Ї–Њ–≥–і–∞ –±–Њ–ї—М–љ—Л–µ, –њ–Њ–ї—Г—З–∞—О—Й–Є–µ —Б—В–∞–љ–і–∞—А—В–љ—Г—О –і–Њ–Ј—Г –Э–Я–Т–Я –і–ї—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ –њ—А–Є–љ–Є–Љ–∞–ї–Є –њ—А–µ–њ–∞—А–∞—В—Л –љ–∞ –Њ—Б–љ–Њ–≤–µ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Є–ї–Є –њ–Њ–њ—Г–ї—П—А–љ—Л–є –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –∞–љ–∞–ї—М–≥–µ—В–Є–Ї —Ж–Є—В—А–∞–Љ–Њ–љ, —Б–Њ–і–µ—А–ґ–∞—Й–Є–є –Р–°–Ъ, –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є.
–Э–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–є —Г—З–µ—В —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞
–•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–µ —З–Є—Б–ї–Њ –Њ–њ–∞—Б–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В —Г –±–Њ–ї—М–љ—Л—Е, –Є–Љ–µ—О—Й–Є—Е —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ «—Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞». –°—А–µ–і–Є –љ–Є—Е –≤–∞–ґ–љ–µ–є—И–Є–Љ–Є —П–≤–ї—П—О—В—Б—П –њ–Њ–ґ–Є–ї–Њ–є –≤–Њ–Ј—А–∞—Б—В (65 –ї–µ—В –Є —Б—В–∞—А—И–µ), –љ–∞–ї–Є—З–Є–µ —П–Ј–≤–µ–љ–љ–Њ–≥–Њ –∞–љ–∞–Љ–љ–µ–Ј–∞ –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ–Њ–≤—Л—И–∞—О—Й–Є—Е —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П (–љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –Р–°–Ъ, –Є–љ—Л–µ –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В—Л) [4–6]. –Э–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –≤—А–∞—З–µ–є –Ї –Є—Е –љ–∞–ї–Є—З–Є—О —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —Б–µ—А—М–µ–Ј–љ–Њ–є, –Є, –Ї —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –љ–µ—А–µ–і–Ї–Њ–є –Њ—И–Є–±–Ї–Њ–є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –Э–Я–Т–Я.
–§–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –±–Њ–ї–Є —Г –ї–Є—Ж –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —В—А–µ–±—Г–µ—В –≤–Ј–≤–µ—И–µ–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Є –Њ—Б–Њ–±–µ–љ–љ–Њ–є –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ—Б—В–Є. –Э–∞–ї–Є—З–Є–µ –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –њ–Њ–ї–Є–њ—А–∞–≥–Љ–∞–Ј–Є—П (—З—А–µ–≤–∞—В–∞—П –љ–µ–≥–∞—В–Є–≤–љ—Л–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ–Љ), –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–є —Б–∞–Љ–Њ–Ї–Њ–љ—В—А–Њ–ї—М, –∞ —В–∞–Ї–ґ–µ –≤—Л—Б–Њ–Ї–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —Б–ї–Є–Ј–Є—Б—В–Њ–є –Ц–Ъ–Ґ –Ї —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–Љ—Г –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–Љ—Г –і–µ–є—Б—В–≤–Є—О –Э–Я–Т–Я –Њ–њ—А–µ–і–µ–ї—П—О—В –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б—А–µ–і–Є —Н—В–Њ–≥–Њ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–∞ –±–Њ–ї—М–љ—Л—Е [22]. –Ч–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ–њ–∞—Б–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞ –±–Њ–ї—М–љ—Л—Е —Д–∞–Ї—В–Є—З–µ—Б–Ї–Є –Є–Љ–µ–µ—В –ї–Є–љ–µ–є–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Ґ–∞–Ї, —Б–Њ–≥–ї–∞—Б–љ–Њ –і–∞–љ–љ—Л–Љ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П Perez Gutthan S. et al. (1997), —Г 50––ї–µ—В–љ–Є—Е –±–Њ–ї—М–љ—Л—Е, —А–µ–≥—Г–ї—П—А–љ–Њ –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Э–Я–Т–Я, —З–∞—Б—В–Њ—В–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г –Ц–Ъ–Ґ––Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є –Є –њ–µ—А—Д–Њ—А–∞—Ж–Є–є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 3, —Г 65––ї–µ—В–љ–Є—Е 5, –∞ —Г 75––ї–µ—В–љ–Є—Е —Г–ґ–µ 10 –љ–∞ 1000 –њ–∞—Ж–Є–µ–љ—В–Њ–≤––ї–µ—В [23]. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –љ–∞—И–µ–є —А–∞–±–Њ—В—Л, –њ—А–Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 4471 –±–Њ–ї—М–љ–Њ–≥–Њ, —А–µ–≥—Г–ї—П—А–љ–Њ –њ—А–Є–љ–Є–Љ–∞–≤—И–µ–≥–Њ –Э–Я–Т–Я, –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ —Н—А–Њ–Ј–Є–Є –Є —П–Ј–≤—Л –≤—Л—П–≤–ї—П–ї–Є—Б—М —Б—А–µ–і–Є –ї–Є—Ж 18–35 –ї–µ—В —Г 12,5%, 36–49 –ї–µ—В – 16,9%, 50–64 –ї–µ—В – —Г 18,9%, –∞ 65 –ї–µ—В –Є —Б—В–∞—А—И–µ – 21,0% [15].
–Т—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –і–µ–ї–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е, –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я (–љ––Э–Я–Т–Я) —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ. –Ю–і–љ–∞–Ї–Њ —В–∞–Ї–∞—П —Б–Є—В—Г–∞—Ж–Є—П –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —З–∞—Б—В–Њ, –Ї–Њ–≥–і–∞ –ї–µ—З–∞—Й–Є–є –≤—А–∞—З –Є–і–µ—В «–љ–∞–≤—Б—В—А–µ—З—Г» –ґ–µ–ї–∞–љ–Є—П–Љ —Б–≤–Њ–Є—Е –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б–Ї–ї–Њ–љ–љ—Л—Е –±–Њ–ї–µ–µ –і–Њ–≤–µ—А—П—В—М «—Б—В–∞—А—Л–Љ –њ—А–Њ–≤–µ—А–µ–љ–љ—Л–Љ –ї–µ–Ї–∞—А—Б—В–≤–∞–Љ», –Є –≤—Л–њ–Є—Б—Л–≤–∞–µ—В –Є–Љ —В–µ –Э–Я–Т–Я, –Ї–Њ—В–Њ—А—Л–µ –Њ–љ–Є —Г–ґ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –ї–µ—В. –Э–Њ –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ, –µ—Б–ї–Є –њ–Њ–ґ–Є–ї—Л–µ –±–Њ–ї—М–љ—Л–µ –≤—Б–µ –ґ–µ –≤—Л–љ—Г–ґ–і–µ–љ—Л (–Є–ї–Є –Њ—З–µ–љ—М –ґ–µ–ї–∞—О—В) –њ–Њ–ї—Г—З–∞—В—М –љ––Э–Я–Т–Я, –њ–Њ—Б–ї–µ–і–љ–Є–µ, —Б–Њ–≥–ї–∞—Б–љ–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞—В—М —Б —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–∞–Љ–Є.
–Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –≤—А–∞—З–Є —З–∞—Б—В–Њ –Ј–∞–±—Л–≤–∞—О—В –Њ–± —Н—В–Њ–Љ –Є –љ–∞–Ј–љ–∞—З–∞—О—В —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–µ –Э–Я–Т–Я –±–µ–Ј –Ї–∞–Ї–Њ–є––ї–Є–±–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –ї—О–і—П–Љ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Э–∞–њ—А–Є–Љ–µ—А, —Б—А–µ–і–Є 1078 –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ш–љ—Б—В–Є—В—Г—В–∞ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –†–Р–Ь–Э (–≤–Њ–Ј—А–∞—Б—В 65 –ї–µ—В –Є –±–Њ–ї–µ–µ), –њ—А–Њ—И–µ–і—И–Є—Е —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤ 2002–2006 –≥–≥., 61,0% –њ—А–Є–љ–Є–Љ–∞–ї–Є –љ––Э–Я–Т–Я (–њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї) –±–µ–Ј –Ї–∞–Ї–Њ–є––ї–Є–±–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ–њ–∞—Б–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ. –Ъ—Б—В–∞—В–Є, —Н—В–Њ –љ–µ —В–Њ–ї—М–Ї–Њ —А–Њ—Б—Б–Є–є—Б–Ї–∞—П, –љ–Њ –Є –Њ–±—Й–µ–Љ–Є—А–Њ–≤–∞—П –њ—А–Њ–±–ї–µ–Љ–∞. –Ґ–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Smolley W. –Є —Б–Њ—В—А. –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–µ—А—М–µ–Ј–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г 76765 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я, –≤ —И—В–∞—В–µ –Ґ–µ–љ–µ—Б—Б–Є, –°–®–Р (1999–2000 –≥–≥.). –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Є–Љ–µ–≤—И–Є—Е –Ї —В–Њ–Љ—Г –ґ–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ (—П–Ј–≤–µ–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј, –њ—А–Є–µ–Љ –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤ –Є–ї–Є –У–Ъ), –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я, —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –ї–Є—И—М —Г 30%, —В.–µ. –њ–Њ–і–∞–≤–ї—П—О—Й–µ–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Ј –љ–Є—Е –њ–Њ–ї—Г—З–∞–ї–Є –љ––Э–Я–Т–Я –±–µ–Ј –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є [24]. –Я–Њ –і–∞–љ–љ—Л–Љ Hartnell N. –Є —Б–Њ—В—А., —Б—А–µ–і–Є 14587 –њ–Њ–ґ–Є–ї—Л—Е –њ–Њ—В—А–µ–±–Є—В–µ–ї–µ–є –Э–Я–Т–Я –≤ –Э–Њ–≤–Њ–є –®–Њ—В–ї–∞–љ–і–Є–Є (–Ъ–∞–љ–∞–і–∞), –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —А–µ–≥–Є—Б—В—А –≤ 2001–2002 –≥–≥., —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–µ –Э–Я–Т–Я –±–µ–Ј –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –њ–Њ–ї—Г—З–∞–ї–Є 9412 (64,5%) [25].
–£–і–Є–≤–Є—В–µ–ї—М–љ–Њ, –љ–Њ –Ј–∞—З–∞—Б—В—Г—О –ї–µ—З–∞—Й–Є–µ –≤—А–∞—З–Є –Є–≥–љ–Њ—А–Є—А—Г—О—В –і–∞–ґ–µ —Б—В–Њ–ї—М –≤–∞–ґ–љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є, –Ї–∞–Ї —П–Ј–≤–µ–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј. –Ю—З–µ–љ—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Л –і–∞–љ–љ—Л–µ –Њ–њ—А–Њ—Б–∞ 3037 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –†–Ч, —А–µ–≥—Г–ї—П—А–љ–Њ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я, –≤ –Ь–Њ—Б–Ї–≤–µ –Є 6 —А–µ–≥–Є–Њ–љ–∞—Е –†–Њ—Б—Б–Є–Є. –°—А–µ–і–Є —А–µ—Б–њ–Њ–љ–і–µ–љ—В–Њ–≤ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М 239 –±–Њ–ї—М–љ—Л—Е, –Є–Љ–µ–≤—И–Є—Е –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ —П–Ј–≤—Г –ґ–µ–ї—Г–і–Ї–∞ –Є–ї–Є 12––њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є. –Ш–Ј –љ–Є—Е –ї–Є—И—М 41% –њ—А–Є–љ–Є–Љ–∞–ї–Є –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я (—Б––Э–Я–Т–Я) –Є 12,9% – —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–µ –Э–Я–Т–Я –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–∞–Љ–Є, —В.–µ. –±–Њ–ї–µ–µ 40% –Є–Љ–µ–≤—И–Є—Е —П–Ј–≤–µ–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј –Є —А–µ–≥—Г–ї—П—А–љ–Њ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [26]. –≠—В–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї–љ–Њ—Б—В—М—О —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—В –і–∞–љ–љ—Л–Љ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–Љ –Ј–∞–њ–∞–і–љ—Л–Љ–Є –Ї–Њ–ї–ї–µ–≥–∞–Љ–Є. –Э–∞–њ—А–Є–Љ–µ—А, Lanas A. –Є Ferrandez A. (2007) —Б–Њ–Њ–±—Й–∞—О—В, —З—В–Њ —Е–Њ—В—П –≤—Б–µ –≤—А–∞—З–Є —Е–Њ—А–Њ—И–Њ –Њ—Б–≤–µ–і–Њ–Љ–ї–µ–љ—Л –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є—В–Є—П –Њ–њ–∞—Б–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Э–Я–Т–Я –Є –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ, –ї–Є—И—М –Љ–µ–љ–µ–µ –њ–Њ–ї–Њ–≤–Є–љ—Л –Є–Ј –љ–Є—Е –њ—А–Њ–≤–Њ–і—П—В —Н—Д—Д–µ–Ї—В–Є–≤–љ—Г—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–Њ–ґ–Є–ї—Л–Љ –±–Њ–ї—М–љ—Л–Љ, –Є–Љ–µ—О—Й–Є–Љ —Б–µ—А—М–µ–Ј–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —Н—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є [27].
–Э–µ—А–µ–і–Ї–Є —Б–ї—Г—З–∞–Є, –Ї–Њ–≥–і–∞ –≤—А–∞—З—Г –њ—А–Є—Е–Њ–і–Є—В—Б—П —Б—В–∞–ї–Ї–Є–≤–∞—В—М—Б—П —Б–Њ —Б–≤–Њ–µ–Њ–±—А–∞–Ј–љ—Л–Љ «—Б–Ї—А—Л—В—Л–Љ» —П–Ј–≤–µ–љ–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ. –Я—А–Є –Ї–Њ—А–Њ—В–Ї–Њ–Љ –Њ–њ—А–Њ—Б–µ –њ–Њ–і–Њ–±–љ—Л–µ –±–Њ–ї—М–љ—Л–µ –Њ—В—А–Є—Ж–∞—О—В –љ–∞–ї–Є—З–Є–µ —П–Ј–≤—Л –ґ–µ–ї—Г–і–Ї–∞ –Є–ї–Є –Ф–Я–Ъ, –Њ–і–љ–∞–Ї–Њ –≤—А–µ–Љ—П –Њ—В –≤—А–µ–Љ–µ–љ–Є –Є—Б–њ—Л—В—Л–≤–∞—О—В –і–Є—Б–њ–µ–њ—Б–Є—О, –Ї–Њ—В–Њ—А—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Ї—Г–њ–Є—А—Г—О—В –њ—А–Є–µ–Љ–Њ–Љ —В–µ—Е –Є–ї–Є –Є–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤. –Ь–љ–Њ–≥–Є–µ –Є–Ј —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ –њ—А–Њ—Е–Њ–і–Є–ї–Є —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ц–Ъ–Ґ, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –±—Л –≤—Л—П–≤–Є—В—М –Є–ї–Є –Њ—В–Ї—А—Л—В—Г—О —П–Ј–≤—Г, –Є–ї–Є —З–µ—В–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –µ–µ –љ–∞–ї–Є—З–Є—П –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ (–њ–Њ—Б—В—П–Ј–≤–µ–љ–љ—Л–є —А—Г–±–µ—Ж). –Я–Њ–і–Њ–±–љ–∞—П —Б–Є—В—Г–∞—Ж–Є—П –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤—Б–µ —З–∞—Й–µ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –≤ —Б–≤—П–Ј–Є —Б —В–µ–Љ, —З—В–Њ –±–Њ–ї—М–љ—Л–µ –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –љ–µ–њ—А–Є—П—В–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –њ—А–Є–љ–Є–Љ–∞—О—В –љ–µ —В–Њ–ї—М–Ї–Њ –∞–љ—В–∞—Ж–Є–і–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞, –љ–Њ –Є –≤–µ—Б—М–Љ–∞ –і–Њ—Б—В—Г–њ–љ—Л–µ –Љ–Њ—Й–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ—П–Ј–≤–µ–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, —В–∞–Ї–Є–µ –Ї–∞–Ї –Э2––±–ї–Њ–Ї–∞—В–Њ—А—Л –Є–ї–Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л (–Ш–Я–Я). –Я—А–Є —Н—В–Њ–Љ —З–∞—Б—В—М –±–Њ–ї—М–љ—Л—Е –љ–µ —Б—З–Є—В–∞—О—В –љ—Г–ґ–љ—Л–Љ —Б–Њ–Њ–±—Й–∞—В—М –Њ –љ–∞–ї–Є—З–Є–Є –љ–µ–њ—А–Є—П—В–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –Є —Д–∞–Ї—В–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П. –Ю—Б–Њ–±–µ–љ–љ–Њ –Љ–љ–Њ–≥–Њ –њ–Њ—В—А–µ–±–Є—В–µ–ї–µ–є –Э2––±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є –Ш–Я–Я —Б—А–µ–і–Є –ї–Є—Ж, —Б—В—А–∞–і–∞—О—Й–Є—Е –≥–∞—Б—В—А–Њ—Н–Ј–Њ—Д–∞–≥–µ–∞–ї—М–љ–Њ–є —А–µ—Д–ї—О–Ї—Б–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О (–У–≠–†–С) –Є —З–∞—Б—В–Њ –Є—Б–њ—Л—В—Л–≤–∞—О—Й–Є—Е –Є–Ј–ґ–Њ–≥—Г.
–Э–µ—А–µ–≥—Г–ї—П—А–љ—Л–є –њ—А–Є–µ–Љ –Э2––±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є–ї–Є –Ш–Я–Я –≤ —А–µ–ґ–Є–Љ–µ «–њ–Њ —В—А–µ–±–Њ–≤–∞–љ–Є—О» –Љ–Њ–ґ–µ—В –Љ–∞—Б–Ї–Є—А–Њ–≤–∞—В—М —В–Є–њ–Є—З–љ—Л–µ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –њ–µ–њ—В–Є—З–µ—Б–Ї–Њ–є —П–Ј–≤—Л, –љ–Њ –љ–µ —Б–њ–Њ—Б–Њ–±–µ–љ —Г—Б—В—А–∞–љ–Є—В—М –љ–Є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —А–µ—Ж–Є–і–Є–≤–∞ —П–Ј–≤—Л, –љ–Є –Њ–њ–∞—Б–љ—Л—Е —П–Ј–≤–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є – –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –Є –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є –Њ–њ—А–Њ—Б–µ –±–Њ–ї—М–љ—Л—Е —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–µ —В–Њ–ї—М–Ї–Њ —Г–Ј–љ–∞—В—М –Њ –љ–∞–ї–Є—З–Є–Є –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —П–Ј–≤–µ–љ–љ–Њ–≥–Њ –∞–љ–∞–Љ–љ–µ–Ј–∞, –љ–Њ –Є –Ј–∞–і–∞—В—М –≤–Њ–њ—А–Њ—Б –Њ –ґ–∞–ї–Њ–±–∞—Е —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –Є –њ—А–µ–њ–∞—А–∞—В–∞—Е –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Љ.
–Ф—А—Г–≥–Њ–є —Б–µ—А—М–µ–Ј–љ–Њ–є –Њ—И–Є–±–Ї–Њ–є —П–≤–ї—П–µ—В—Б—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–є —Г—З–µ—В —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–≥–Њ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –њ–Њ–≤—Л—И–∞—В—М —А–Є—Б–Ї –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П.
–Т –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Н—В–Њ –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –љ–Є–Ј–Ї–Є–Љ –і–Њ–Ј–∞–Љ –Р–°–Ъ, —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–Њ–≥–Њ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –љ–µ —В–Њ–ї—М–Ї–Њ —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е, –љ–Њ –Є —Б—А–µ–і–Є –Љ–љ–Њ–≥–Є—Е –≤—А–∞—З–µ–є —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Љ–љ–µ–љ–Є–µ, —З—В–Њ –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–µ –і–Њ–Ј—Л –Р–°–Ъ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –±–µ–Ј–Њ–њ–∞—Б–љ—Л. –Ю–і–љ–∞–Ї–Њ —Н—В–Њ –љ–µ —В–∞–Ї. –Ю–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –Ї—А—Г–њ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е –Є–Ј—Г—З–µ–љ–Є—О –і–∞–љ–љ–Њ–≥–Њ –≤–Њ–њ—А–Њ—Б–∞, —П–≤–ї—П–µ—В—Б—П –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј Derry S. –Є Loke Y. (2000). –Ю–љ –Њ—Б–љ–Њ–≤–∞–љ –љ–∞ –Њ—Ж–µ–љ–Ї–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ 24 –†–Ъ–Ш, –≤–Ї–ї—О—З–∞–≤—И–Є—Е –±–Њ–ї–µ–µ 66000 –±–Њ–ї—М–љ—Л—Е, –≤ –Ї–Њ—В–Њ—А—Л—Е —Б—А–∞–≤–љ–Є–≤–∞–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ –Ц–Ъ–Ъ —Г –ї–Є—Ж, —Г –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Р–°–Ъ, –њ–ї–∞—Ж–µ–±–Њ –Є–ї–Є –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–µ—А–∞–њ–Є–Є. –Я–Њ–ї—Г—З–µ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —З–∞—Б—В–Њ—В–∞ –Ц–Ъ–Ъ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –±–Њ–ї–µ–µ —З–µ–Љ –≤ 1,5 —А–∞–Ј–∞ –≤—Л—И–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ї–Є—Ж–∞–Љ–Є, –љ–µ –њ–Њ–ї—Г—З–∞—О—Й–Є–Љ–Є —Н—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –Є –і—А—Г–≥–Є–µ –Э–Я–Т–Я – 2,47 –Є 1,42% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (OR=1,68) [28].
–Э–µ —В–Њ–ї—М–Ї–Њ –Р–°–Ъ, –љ–Њ –Є –Є–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —В—А–Њ–Љ–±–Њ–Ј–Њ–≤, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞—О—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —А–∞–±–Њ—В–∞ Lanas A. –Є —Б–Њ—В—А. (2006), –≥–і–µ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Г—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 2777 –±–Њ–ї—М–љ—Л—Е —Б –Ц–Ъ–Ъ, –∞ –Ї–Њ–љ—В—А–Њ–ї—М – 5532 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є—Е –њ–Њ –њ–Њ–ї—Г –Є –≤–Њ–Ј—А–∞—Б—В—Г –ї–Є—Ж. –°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ—Г –∞–љ–∞–ї–Є–Ј—Г –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Р–°–Ъ –≤ –і–Њ–Ј–µ 100 –Љ–≥ –Є –Љ–µ–љ–µ–µ, –Є–љ—Л—Е –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ—Л—Е —Б—А–µ–і—Б—В–≤ (–Ї–ї–Њ–њ–Є–і–Њ–≥—А–µ–ї, —В–Є–Ї–ї–Њ–њ–Є–і–Є–љ) –Є –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤ (–≤–∞—А—Д–∞—А–Є–љ) —Д–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ —А–∞–Ј–ї–Є—З–∞–ї—Б—П –Є —Б–Њ—Б—В–∞–≤–Є–ї 2,7, 2,8 –Є 2,8 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [29].
–°–∞–Љ–Њ–µ –≤–∞–ґ–љ–Њ–µ, —З—В–Њ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤–ї–Є—П—О—Й–Є—Е –љ–∞ —В—А–Њ–Љ–±–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ (–≤ 2,5–4 —А–∞–Ј–∞) —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Њ–њ–∞—Б–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Э–Я–Т–Я. –Я—А–Є —Н—В–Њ–Љ —А–µ—З—М –Є–і–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е —А–µ—Ж–µ–њ—В—Г—А–љ—Л—Е –Э–Я–Т–Я, –љ–Њ –Є –њ—А–Є–µ–Љ–µ «–±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л—Е» –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –љ–Є–Ј–Ї–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–µ.
–Я—А–Њ–±–ї–µ–Љ—Г –љ–µ—Г—З—В–µ–љ–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ —Г –њ–Њ—В—А–µ–±–Є—В–µ–ї–µ–є –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л—Е –Э–Я–Т–Я –Є–ї–ї—О—Б—В—А–Є—А—Г–µ—В —А–∞–±–Њ—В–∞ Biskupiak J. –Є —Б–Њ—В—А. (2006). –Р–≤—В–Њ—А—Л –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Њ–њ–∞—Б–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б—А–µ–і–Є 11957 –ї–Є—Ж, –Ї–Њ—В–Њ—А—Л–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л–є –љ–∞–њ—А–Њ–Ї—Б–µ–љ (–≤ –і–Њ–Ј–µ 220 –Љ–≥) –Є 38507 –ї–Є—Ж, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–≤—И–Є—Е –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л–є –Є–±—Г–њ—А–Њ—Д–µ–љ (–≤ –і–Њ–Ј–µ 200 –Љ–≥). –£ –ї—О–і–µ–є, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –њ—А–µ–њ–∞—А–∞—В—Л –≤ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ–Њ–є «–±–µ–Ј–Њ–њ–∞—Б–љ–Њ–є» –і–Њ–Ј–Є—А–Њ–≤–Ї–µ, —А–Є—Б–Ї –і–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Њ–Ї–∞–Ј–∞–ї—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–±–Њ–ї—М—И–Є–Љ – 1,54 (1,04–2,28) –Є 1,38 (1,07–1,78). –Ю–і–љ–∞–Ї–Њ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–є –њ—А–Є–µ–Љ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Ї–Њ—В–Њ—А—Л–є –њ–Њ–ї—Г—З–∞–ї–Є 2328 –њ–Њ—В—А–µ–±–Є—В–µ–ї–µ–є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–∞ –Є 4843 –њ–Њ—В—А–µ–±–Є—В–µ–ї–µ–є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞, –њ–Њ–≤—Л—И–∞–ї —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Ц–Ъ–Ґ –±–Њ–ї–µ–µ —З–µ–Љ –≤ 2 —А–∞–Ј–∞ (–Ю–† 2,07: 1,23–3,49 –Є 3,36: 2,36–4,8 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) [30].
–Э–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –Р–°–Ъ –њ–Њ–≤—Л—И–∞—О—В —А–Є—Б–Ї –Ц–Ъ–Ґ––Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Э–Я–Т–Я, –љ–Њ –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞. –Т —А–∞–±–Њ—В–µ Garcia Rodriquez L. –Є Hernandez–Diaz S., —Б—А–∞–≤–љ–Є–≤—И–Є—Е –≤–ї–Є—П–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Ц–Ъ–Ъ (2105 —Б–ї—Г—З–∞–µ–≤, 11500 –Ї–Њ–љ—В—А–Њ–ї—М, –Њ—Ж–µ–љ–Ї–∞ –Ю–†), –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —А–Є—Б–Ї —Н—В–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —В–Њ–ї—М–Ї–Њ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ —Б–Њ—Б—В–∞–≤–ї—П–ї 1,3, –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е –Р–°–Ъ 2,1, –∞ –њ—А–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –±–Њ–ї–µ–µ 2 –≥/—Б—Г—В. –Є –Р–°–Ъ —Г–ґ–µ 3,3 [31].
–°–ї–µ–і—Г–µ—В —Г—З–µ—Б—В—М, —З—В–Њ –Љ–љ–Њ–≥–Є–µ –њ–∞—Ж–Є–µ–љ—В—Л – –љ–µ –Ј–љ–∞—П, —З—В–Њ –њ—А–Є–µ–Љ –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤, –љ–∞–Ј–љ–∞—З–µ–љ–љ—Л–є –Њ–і–љ–Є–Љ –≤—А–∞—З–Њ–Љ (–Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–Љ, —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —Е–Є—А—Г—А–≥–Њ–Љ –Є —В.–і.), —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Ј–∞—З–∞—Б—В—Г—О –љ–µ —Б—З–Є—В–∞—О—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ —Б–Њ–Њ–±—Й–∞—В—М –Њ–± —Н—В–Њ–Љ –≤—А–∞—З—Г –і—А—Г–≥–Њ–є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ—Б—В–Є, –љ–∞–Ј–љ–∞—З–∞—О—Й–µ–Љ—Г –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–∞—П —З–∞—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –Р–°–Ъ –≤ –њ–Њ—А—П–і–Ї–µ —Б–∞–Љ–Њ–ї–µ—З–µ–љ–Є—П, —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤—Г—П—Б—М —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –Ј–љ–∞–Ї–Њ–Љ—Л—Е –Є–ї–Є –њ–Њ–њ—Г–ї—П—А–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –ї–Є—В–µ—А–∞—В—Г—А—Л. –Я–Њ—Н—В–Њ–Љ—Г –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –њ—А—П–Љ–Њ–є –≤–Њ–њ—А–Њ—Б: «–Я—А–Є–љ–Є–Љ–∞–µ—В–µ –ї–Є –Т—Л –Ї–∞–Ї–Є–µ––ї–Є–±–Њ –њ—А–µ–њ–∞—А–∞—В—Л –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —В—А–Њ–Љ–±–Њ–≤?» –і–Њ–ї–ґ–µ–љ —Б—З–Є—В–∞—В—М—Б—П –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ —Б–±–Њ—А–∞ –∞–љ–∞–Љ–љ–µ–Ј–∞ –і–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є.
–Т–∞–ґ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ —Б—З–Є—В–∞—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –ї—О–±—Л—Е –і–Њ–Ј –Р–°–Ъ –≤ –≤–Є–і–µ –ї—О–±–Њ–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л. –Т–Њ–њ—А–µ–Ї–Є —А–µ–Ї–ї–∞–Љ–љ—Л–Љ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ —А—П–і–∞ —Д–Є—А–Љ––њ—А–Њ–Є–Ј–≤–Њ–і–Є—В–µ–ї–µ–є, –љ–µ—В —З–µ—В–Ї–Є—Е –і–∞–љ–љ—Л—Е –Є–ї–Є —В–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–є, —З—В–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –∞–љ—В–∞—Ж–Є–і–∞–Љ–Є (–љ–∞–њ—А–Є–Љ–µ—А, –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Љ–∞–≥–љ–Є—П), –≤ –≤–Є–і–µ –Ї–Є—И–µ—З–љ–Њ–—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–є, —А–µ–Ї—В–∞–ї—М–љ–Њ–є –Є–ї–Є –Є–љ–Њ–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л –Љ–Њ–ґ–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –Ц–Ъ–Ґ – –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–≤–µ—А—Е–љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ –±—Г–і–µ—В —Г–Љ–µ—Б—В–љ–Њ –њ—А–Є–≤–µ—Б—В–Є –і–∞–љ–љ—Л–µ Cryer B. –Є Feldman M., –њ–Њ–Ї–∞–Ј–∞–≤—И–Є—Е, —З—В–Њ –њ—А–Є–µ–Љ –і–∞–ґ–µ 10 –Љ–≥ (!) –Р–°–Ъ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –≤—Л–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є–Љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ –Х1 –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –ґ–µ–ї—Г–і–Ї–∞ –Є –њ–Њ—П–≤–ї–µ–љ–Є–µ —Н—А–Њ–Ј–Є–є [32].
–Э–µ–∞–і–µ–Ї–≤–∞—В–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞
–Њ–њ–∞—Б–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є
–Я–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П–Љ, –Є–Љ–µ—О—В—Б—П –ї–Є—И—М –і–≤–∞ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л—Е –Љ–µ—В–Њ–і–∞ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ, —З—М—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Е–Њ—А–Њ—И–Њ –і–Њ–Ї–∞–Ј–∞–љ–∞ –Ї–∞–Ї –±–Њ–ї—М—И–Є–Љ —З–Є—Б–ї–Њ–Љ –†–Ъ–Ш, —В–∞–Ї –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Њ–є: –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б––Э–Я–Т–Я –Є–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е –Э–Я–Т–Я (–љ––Э–Я–Т–Я) –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Љ–Њ—Й–љ—Л–Љ–Є –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–∞–Љ–Є [4–6].
–Э–Є–ґ–µ –Љ—Л –њ—А–Є–≤–µ–і–µ–Љ –і–∞–љ–љ—Л–µ, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—Й–Є–µ –Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б––Э–Я–Т–Я —Г –±–Њ–ї—М–љ—Л—Е —Б —В–∞–Ї–Є–Љ–Є —Б–µ—А—М–µ–Ј–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞, –Ї–∞–Ї —П–Ј–≤–µ–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј –Є–ї–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤–ї–Є—П—О—Й–Є—Е –љ–∞ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —В—А–Њ–Љ–±–Њ–≤.
–І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤, —В–Њ –і–µ–є—Б—В–≤–µ–љ–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —В–∞–Ї–Є—Е –Ї–∞–Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —П–Ј–≤ –Є –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –Є–Ј –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –Ц–Ъ–Ґ, –і–Њ–Ї–∞–Ј–∞–љ–∞ –і–ї—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л (–Ш–Я–Я) –Є –Љ–Є–Ј–Њ–њ—А–Њ—Б—В–Њ–ї–∞ [4,5].
–Э2––±–ї–Њ–Ї–∞—В–Њ—А—Л –≤ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е (—А–∞–љ–Є—В–Є–і–Є–љ 150–300 –Љ–≥/—Б—Г—В. –Є —Д–∞–Љ–Њ—В–Є–і–Є–љ 20–40 –Љ–≥/—Б—Г—В.) –љ–µ –і–∞—О—В –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —П–Ј–≤ –ґ–µ–ї—Г–і–Ї–∞ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Э–Я–Т–Я –Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—Б—В—Г–њ–∞—О—В –Ш–Я–Я –њ–Њ —Б–≤–Њ–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —П–Ј–≤ –Ф–Я–Ъ. –Я–Њ—Н—В–Њ–Љ—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е –і–Њ–Ј –Э2––±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–µ –Љ–Њ–ґ–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П, –Ї–∞–Ї –∞–і–µ–Ї–≤–∞—В–љ—Л–є –Љ–µ—В–Њ–і –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–µ—А—М–µ–Ј–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [4,5]. –Р–љ—В–∞—Ж–Є–і–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ –Њ–±—Л—З–љ—Л—Е –і–Њ–Ј–∞—Е —В–∞–Ї–ґ–µ –Љ–∞–ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Э–Я–Т–Я––∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –њ–Њ—Н—В–Њ–Љ—Г –≤—Б—В—А–µ—З–∞—О—Й–∞—П—Б—П –Є–љ–Њ–≥–і–∞ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П «–Ј–∞–њ–Є–≤–∞—В—М» –Э–Я–Т–Я –ґ–Є–і–Ї–Є–Љ–Є –∞–љ—В–∞—Ж–Є–і–∞–Љ–Є —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ, –Љ—П–≥–Ї–Њ –≥–Њ–≤–Њ—А—П, –≤—Л–Ј—Л–≤–∞–µ—В –љ–µ–і–Њ—Г–Љ–µ–љ–Є–µ.
–°–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ —П–Ј–≤ –Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ–µ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ —Б–≤—П–Ј–∞–љ—Л —Б —Б–Є—Б—В–µ–Љ–љ—Л–Љ, –∞ –љ–µ –Ї–Њ–љ—В–∞–Ї—В–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Э–Я–Т–Я, –њ–Њ—Н—В–Њ–Љ—Г —Н—В–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Љ–Њ–≥—Г—В –≤–Њ–Ј–љ–Є–Ї–∞—В—М –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –ї—О–±—Л—Е —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я–Њ—Н—В–Њ–Љ—Г –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Э–Я–Т–Я –≤ –≤–Є–і–µ —Б–≤–µ—З–µ–є –Є–ї–Є –Є–љ—К–µ–Ї—Ж–Є–є –љ–µ –Љ–Њ–ґ–µ—В —Б—З–Є—В–∞—В—М—Б—П –∞–і–µ–Ї–≤–∞—В–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т —Н—В–Њ–Љ –њ–ї–∞–љ–µ –Њ—З–µ–љ—М –Є–љ—В–µ—А–µ—Б–љ—Л –і–∞–љ–љ—Л–µ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П Mellemkjaer L. –Є —Б–Њ—В—А., (2002), –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –≤ –Ф–∞–љ–Є–Є. –†–Є—Б–Ї –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–Ю–†) —Г 131139 –±–Њ–ї—М–љ—Л—Е, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ—Л–µ –Э–Я–Т–Я, –±—Л–ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–Є–ґ–µ, —З–µ–Љ —Г 4659 –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Э–Я–Т–Я –≤ –≤–Є–і–µ —Б–≤–µ—З–µ–є – 3,25 (2,9–3,7) –Є 8,47 (4,4–14,8) —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [33]. –Э–∞—И–Є –і–∞–љ–љ—Л–µ —В–∞–Ї–ґ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Б–≤–µ—З–µ–є. –£ 343 –±–Њ–ї—М–љ—Л—Е —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, –љ–µ –Љ–µ–љ–µ–µ –Љ–µ—Б—П—Ж–∞ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я –≤ —Б–≤–µ—З–∞—Е, —З–∞—Б—В–Њ—В–∞ —П–Ј–≤ –Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л—Е —Н—А–Њ–Ј–Є–є (–њ–Њ –і–∞–љ–љ—Л–Љ –≠–У–Ф–°) —Б—А–µ–і–Є –љ–µ –Є–Љ–µ–≤—И–Є—Е —П–Ј–≤–µ–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј —Б–Њ—Б—В–∞–≤–Є–ї–∞ 15,6% –Є 35,2% – —Г –Є–Љ–µ–≤—И–Є—Е. –Я—А–Є —Н—В–Њ–Љ —Г 3574 –±–Њ–ї—М–љ—Л—Е, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я –≤–љ—Г—В—А—М, —З–∞—Б—В–Њ—В–∞ –њ–Њ–і–Њ–±–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Ц–Ъ–Ґ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 14,1 –Є 33,6% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [15].
–†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Э–Я–Т–Я: –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П –Є —Б––Э–Я–Т–Я —Г –±–Њ–ї—М–љ—Л—Е
—Б —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞
–Ъ–∞–Ї –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –≤—Л—И–µ, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –Э–Я–Т–Я –љ–µ –Љ–Њ–ґ–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М—Б—П, –Ї–∞–Ї –∞–і–µ–Ї–≤–∞—В–љ—Л–є –Љ–µ—В–Њ–і –њ–Њ–≤—Л—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –±–Њ–ї–Є. –С–Њ–ї–µ–µ –њ—А–∞–≤–Є–ї—М–љ—Л–Љ –њ—А–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–µ —Б—А–µ–і–љ–µ–є –Є–ї–Є –≤—Л—Б–Њ–Ї–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л –Э–Я–Т–Я –≤ —В–µ—З–µ–љ–Є–µ 7–14 –і–љ–µ–є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є. –Ю—Б–љ–Њ–≤–љ—Л–µ –Њ—И–Є–±–Ї–Є, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–≤–Њ–і—П—В –Ї —А–∞–Ј–≤–Є—В–Є—О —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.
–†–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –±—Г–і–µ—В —Б–Њ—З–µ—В–∞–љ–Є–µ –Э–Я–Т–Я —Б –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–Њ–Љ –Є «–Љ—П–≥–Ї–Є–Љ–Є» –Њ–њ–Є–Њ–Є–і–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є (—В—А–∞–Љ–∞–і–Њ–ї, –Ї–Њ–і–µ–Є–љ). –Э–∞–ї–Є—З–Є–µ –Љ—Л—И–µ—З–љ–Њ–≥–Њ —Б–њ–∞–Ј–Љ–∞ –Є–ї–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Љ—Л—И–µ—З–љ–Њ–≥–Њ –љ–∞–њ—А—П–ґ–µ–љ–Є—П –≤ –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–є –Њ–±–ї–∞—Б—В–Є —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤ (—В–Њ–ї–њ–µ—А–∞–Ј–Њ–љ, —В–Є–Ј–∞–љ–Є–і–Є–љ), –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –∞–љ—В–Є—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ (–±–∞–Ї–ї–Њ—Д–µ–љ). –≠—В–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Њ–±–ї–∞–і–∞—О—В —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–Љ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–Є–Љ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–Љ –Є —Б–њ–Њ—Б–Њ–±–љ—Л —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—Б–Є–ї–Є–≤–∞—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і—А—Г–≥–Є—Е –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [34–36]. –Я—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Њ—Б—В–∞–≤–ї—П—О—Й–µ–є –±–Њ–ї–Є (—В–∞–Ї–∞—П —Б–Є—В—Г–∞—Ж–Є—П –љ–µ—А–µ–і–Ї–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є –і–Њ—А—Б–Њ–њ–∞—В–Є—П—Е, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–Є –±–Њ–ї—П—Е –≤ –Њ–±–ї–∞—Б—В–Є —И–µ–Є –Є–ї–Є –≤–љ–Є–Ј—Г —Б–њ–Є–љ—Л) —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ —А–∞—Б—Б–Љ–Њ—В—А–µ—В—М –≤–Њ–њ—А–Њ—Б –Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї –∞–љ—В–Є–Ї–Њ–љ–≤—Г–ї—М—Б–∞–љ—В—Л –≥–∞–±–∞–њ–µ–љ—В–Є–љ, –њ—А–µ–≥–∞–±–∞–ї–Є–љ –Є –і—А.
–Я–Њ–і–∞–≤–ї–µ–љ–Є–µ –ї–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –њ—Г—В–µ–Љ –≤–≤–µ–і–µ–љ–Є—П –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤ (–У–Ъ) –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–Љ –Є –≤–µ—Б—М–Љ–∞ –і–µ–є—Б—В–≤–µ–љ–љ—Л–Љ –Љ–µ—В–Њ–і–∞–Љ –ї–µ—З–µ–љ–Є—П –±–Њ–ї–Є. –У–Ъ —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –њ—А–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є —Б—Г—Б—В–∞–≤–Њ–≤ –Є –Њ–Ї–Њ–ї–Њ—Б—Г—Б—В–∞–≤–љ—Л—Е –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є (–≤ –≤–Є–і–µ –≤–љ—Г—В—А–Є– –Є –Њ–Ї–Њ–ї–Њ—Б—Г—Б—В–∞–≤–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є), –∞ —В–∞–Ї–ґ–µ –њ—А–Є –і–Њ—А—Б–Њ–њ–∞—В–Є—П—Е –Є –Љ–Є–Њ—Д–∞—Б—Ж–Є–∞–ї—М–љ–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ (–і–ї—П –≤–≤–µ–і–µ–љ–Є—П –≤ –Њ–±–ї–∞—Б—В—М –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л—Е —В–Њ—З–µ–Ї, –Њ–±—Л—З–љ–Њ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Љ–µ—Б—В–љ—Л–Љ–Є –∞–љ–µ—Б—В–µ—В–Є–Ї–∞–Љ–Є) [37,38].
–Я—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ—Л–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–µ–Љ –≤ —В–µ—А–∞–њ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є —П–≤–ї—П–µ—В—Б—П –њ–Њ–Є—Б–Ї –Є —Г—Б—В—А–∞–љ–µ–љ–Є–µ, –µ—Б–ї–Є —Н—В–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –µ–µ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞. –•–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —А–∞–љ–љ–µ–µ –љ–∞—З–∞–ї–Њ —В–µ—А–∞–њ–Є–Є –±–∞–Ј–Є—Б–љ—Л–Љ–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –њ–Њ–і–∞–≤–ї—П—О—Й–Є–Љ–Є —А–∞–Ј–≤–Є—В–Є–µ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е, –∞ —В–∞–Ї–ґ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Е–Њ–љ–і—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–≤ –њ—А–Є –Ю–Р –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є—З—М –љ–µ —В–Њ–ї—М–Ї–Њ –Ј–∞–Љ–µ–і–ї–µ–љ–Є—П –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–Њ –Є –њ–Њ–ї—Г—З–Є—В—М —Е–Њ—А–Њ—И–Є–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В [4,37].
–Я—А–Є –љ–∞–ї–Є—З–Є–Є —Б–µ—А—М–µ–Ј–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ–є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –≤–∞–ґ–љ–µ–є—И–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –≤—Л–±–Њ—А –љ–∞–Є–±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –Э–Я–Т–Я, —В–∞–Ї–Є—Е –Ї–∞–Ї —Б––Э–Я–Т–Я. –Я—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–Љ —Н—В–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –Э–Я–Т–Я –љ–∞ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ —П–≤–ї—П–µ—В—Б—П —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±. –Т–∞–ґ–љ—Л–Љ –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–Њ–Љ —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, –≤—Л–≥–Њ–і–љ–Њ –Њ—В–ї–Є—З–∞—О—Й–Є–Љ –µ–≥–Њ –Њ—В –і—А—Г–≥–Є—Е –Э–Я–Т–Я, —П–≤–ї—П–µ—В—Б—П —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –≤ —И–Є—А–Њ–Ї–Њ–Љ –і–Є–∞–њ–∞–Ј–Њ–љ–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј – –Њ—В 200 –і–Њ 800 –Љ–≥/—Б—Г—В., —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–µ —Б—Е–µ–Љ—Л –њ—А–Є–µ–Љ–∞ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е [39].
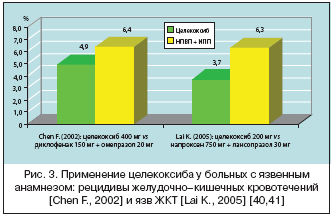
–¶–µ–ї–µ–Ї–Њ–Ї—Б–Є–± —Б—В–Њ–ї—М –ґ–µ (–Є–ї–Є –і–∞–ґ–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї–µ–µ) –±–µ–Ј–Њ–њ–∞—Б–µ–љ —Г –±–Њ–ї—М–љ—Л—Е —Б —П–Ј–≤–µ–љ–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ, —З–µ–Љ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–µ –Э–Я–Т–Я –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–∞–Љ–Є. –Ф–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —П–Ј–≤–µ–љ–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М –і–≤–∞ —Е–Њ—А–Њ—И–Њ —Б–њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Т —Е–Њ–і–µ –њ–µ—А–≤–Њ–≥–Њ, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ Chan F. –Є —Б–Њ—В—А. (2002), –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е, –Є–Љ–µ–≤—И–Є—Е –≤ –±–ї–Є–ґ–∞–є—И–µ–Љ –∞–љ–∞–Љ–љ–µ–Ј–µ –Ї—А–Њ–≤–Њ—В–Њ—З–∞—Й–Є–µ —П–Ј–≤—Л –ґ–µ–ї—Г–і–Ї–∞ –Є–ї–Є –Ф–Я–Ъ, –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ 400 –Љ–≥/—Б—Г—В. –Є–ї–Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ 150 –Љ–≥/—Б—Г—В. –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Њ–Љ–µ–њ—А–∞–Ј–Њ–ї–Њ–Љ 20 –Љ–≥. –≠—В–∞ —В–µ—А–∞–њ–Є—П –љ–∞–Ј–љ–∞—З–∞–ї–∞—Б—М –љ–∞ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ—Б–ї–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П —Г—Б–њ–µ—И–љ–Њ–≥–Њ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —П–Ј–≤ –Є –Њ—В—Б—Г—В—Б—В–≤–Є—П –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ—Б—В–Є H. pylori (–∞–љ—В–Є—Е–µ–ї–Є–Ї–Њ–±–∞–Ї—В–µ—А–љ–∞—П —В–µ—А–∞–њ–Є—П –±—Л–ї–∞ –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –њ—А–Њ—В–Є–≤–Њ—П–Ј–≤–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П). –Ъ—А–Є—В–µ—А–Є–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П. –Т —В–µ—З–µ–љ–Є–µ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П —Н—В–Њ –Њ–њ–∞—Б–љ–Њ–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ –≤–Њ–Ј–љ–Є–Ї–ї–Њ —Г 4,9% –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±, —З—В–Њ –±—Л–ї–Њ –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–µ–ґ–µ, —З–µ–Љ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–Љ – 6,4% [40] (—А–Є—Б. 3).
–С–ї–Є–Ј–Ї–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л Lai K. –Є —Б–Њ—В—А. (2005). –†–∞–±–Њ—В–∞ –±—Л–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–∞ –њ–Њ —Б—Е–Њ–і–љ–Њ–Љ—Г –і–Є–Ј–∞–є–љ—Г, –Њ–і–љ–∞–Ї–Њ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Г—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 244 –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–Љ–Є –Э–Я–Т–Я––Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є —П–Ј–≤–∞–Љ–Є. –Я–Њ—Б–ї–µ —Г—Б–њ–µ—И–љ–Њ–≥–Њ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —П–Ј–≤ –Є —Н—А–∞–і–Є–Ї–∞—Ж–Є–Є H. pylori –±–Њ–ї—М–љ—Л–µ –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ–ї—Г—З–∞–ї–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± 200 –Љ–≥ –Є–ї–Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ 750 –Љ–≥ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б 30 –Љ–≥ –ї–∞–љ—Б–Њ–њ—А–∞–Ј–Њ–ї–∞. –Э–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ —А–µ—Ж–Є–і–Є–≤—Л —П–Ј–≤ –≤–Њ–Ј–љ–Є–Ї–ї–Є —Г 4 –±–Њ–ї—М–љ—Л—Е (3,7%), –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ – —Г 7 (6,3%) [41] (—А–Є—Б. 3).
–Х—Б–ї–Є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А—М–µ–Ј–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї (–љ–∞–њ—А–Є–Љ–µ—А, –Ї–Њ–≥–і–∞ –Є–Љ–µ–µ—В—Б—П —Б–Њ—З–µ—В–∞–љ–Є–µ —П–Ј–≤–µ–љ–љ–Њ–≥–Њ –∞–љ–∞–Љ–љ–µ–Ј–∞ –Є –Є–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –Є–ї–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П —П–Ј–≤–∞ —Г–ґ–µ –љ–µ —А–∞–Ј —А–µ—Ж–Є–і–Є–≤–Є—А–Њ–≤–∞–ї–∞, –Є–ї–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ —Г–ґ–µ –Є–Љ–µ–µ—В—Б—П —Н–њ–Є–Ј–Њ–і –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –Є–ї–Є –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є) —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–Њ–Љ. –≠—В–∞ —Б—Е–µ–Љ–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —А–∞–і–Є–Ї–∞–ї—М–љ–Њ —Б–љ–Є–Ј–Є—В—М –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ—Л—Е –Ї–∞—В–∞—Б—В—А–Њ—Д. –Ш–Ј—Г—З–µ–љ–Є—О —Н—В–Њ–≥–Њ –≤–Њ–њ—А–Њ—Б–∞ –±—Л–ї–Њ –њ–Њ—Б–≤—П—Й–µ–љ–Њ —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ Chan F. –Є —Б–Њ—В—А. (2007). –Ш—Б—Б–ї–µ–і—Г–µ–Љ—Г—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї –±–Њ–ї—М–љ—Л–µ (n=441), –њ–µ—А–µ–љ–µ—Б—И–Є–µ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–µ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ –Є –љ–µ –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ H. pylori (–Є–ї–Є –њ—А–Њ—И–µ–і—И–Є–µ –Ї—Г—А—Б —Н—А–∞–і–Є–Ї–∞—Ж–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є). –Т —В–µ—З–µ–љ–Є–µ 12 –Љ–µ—Б—П—Ж–µ–≤ –Њ–љ–Є –њ—А–Є–љ–Є–Љ–∞–ї–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± 400 –Љ–≥ –Є–ї–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± 400 –Љ–≥ + —Н–Ј–Њ–Љ–µ–њ—А–∞–Ј–Њ–ї 20 –Љ–≥. –Ч–∞ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–µ–љ–Є—П –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О, –љ–µ –≤–Њ–Ј–љ–Є–Ї–ї–Њ –љ–Є –Њ–і–љ–Њ–≥–Њ —Н–њ–Є–Ј–Њ–і–∞ —А–µ—Ж–Є–і–Є–≤–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е —П–Ј–≤ (!), –∞ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —В–∞–Ї–Є—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –±—Л–ї–Њ 12 (8,9%), p<0,001 [42] (—А–Є—Б. 4).
–І—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–∞–љ–љ—Л–µ –њ–Њ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —П–Ј–≤–µ–љ–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ –љ–µ —Б–ї–µ–і—Г–µ—В —Н–Ї—Б—В—А–∞–њ–Њ–ї–Є—А–Њ–≤–∞—В—М –љ–∞ –≤—Б—О –≥—А—Г–њ–њ—Г —В.–љ. «—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е» –Э–Я–Т–Я. –Т–µ–і—М –Ї —Н—В–Є–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ –Њ—В–љ–Њ—Б—П—В –љ–µ —В–Њ–ї—М–Ї–Њ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±, –љ–Њ —В–∞–Ї–ґ–µ –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ –Є –љ–Є–Љ–µ—Б—Г–ї–Є–і. –Э–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, —З—В–Њ —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –±–µ–Ј–Њ–њ–∞—Б–љ–µ–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —А–∞–Ј–≤–Є—В–Є—П –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, —З–µ–Љ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я – —В–∞–Ї–Є–µ –Ї–∞–Ї –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ, –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ, –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ, –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї (–Њ—Б–Њ–±–µ–љ–љ–Њ –µ–≥–Њ –і–µ—И–µ–≤—Л–µ –≥–µ–љ–µ—А–Є–Ї–Є). –Ю–і–љ–∞–Ї–Њ –љ–µ—В —З–µ—В–Ї–Є—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ (–њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –≤ —Е–Њ–і–µ —Е–Њ—А–Њ—И–Њ –Њ—А–≥–∞–љ–Є–Ј–Њ–≤–∞–љ–љ—Л—Е –Є –і–ї–Є—В–µ–ї—М–љ—Л—Е –†–Ъ–Ш) —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б —П–Ј–≤–µ–љ–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ –Є –љ–Є–Љ–µ—Б—Г–ї–Є–і. –Э–∞–њ—А–Є–Љ–µ—А, –≤ –Њ–і–љ–Њ–є –Є–Ј –љ–∞—И–Є—Е —А–∞–±–Њ—В –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞ —Г 425 –±–Њ–ї—М–љ—Л—Е —Б —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є —Б—А–µ–і–Є –ї–Є—Ж —Б —П–Ј–≤–µ–љ–љ—Л–Љ –∞–љ–∞–Љ–љ–µ–Ј–Њ–Љ —А–Є—Б–Ї —А–µ—Ж–Є–і–Є–≤–∞ —П–Ј–≤—Л –±—Л–ї –Љ–µ–љ—М—И–µ, —З–µ–Љ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ (n=2428), –Њ–і–љ–∞–Ї–Њ –≤—Б–µ –ґ–µ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї. –°—А–µ–і–Є –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ –±–Њ–ї—М–љ—Л—Е –њ—А–Є –≠–У–Ф–° —П–Ј–≤—Л –Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ —Н—А–Њ–Ј–Є–Є –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —Г 24,5% (—Г 40,1% –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞) [43].
–Т —В–Њ–Љ —Б–ї—Г—З–∞–µ, –µ—Б–ї–Є –њ–∞—Ж–Є–µ–љ—В –њ–Њ–ї—Г—З–∞–µ—В –Р–°–Ъ –Є–ї–Є –і—А—Г–≥–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є –љ—Г–ґ–і–∞–µ—В—Б—П –≤ –∞–Ї—В–Є–≤–љ–Њ–є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, —В–∞–Ї–ґ–µ —Б–ї–µ–і—Г–µ—В –Њ—В–і–∞–≤–∞—В—М –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ –≤ —Н—В–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –Э–Я–Т–Я (—Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±) [44].
–Ф–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ–Љ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є —В–∞–Ї–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ Goldstein J. –Є —Б–Њ—В—А. (2006), –≤ —Е–Њ–і–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ 662 –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞–Љ –љ–∞ 7 –і–љ–µ–є –±—Л–ї –љ–∞–Ј–љ–∞—З–µ–љ –Р–°–Ъ 81 –Љ–≥ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–Њ–Љ 200 –Љ–≥/—Б—Г—В., –љ–∞–њ—А–Њ–Ї—Б–µ–љ–Њ–Љ 1000 –Љ–≥ –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –І–µ—А–µ–Ј 7 –і–љ–µ–є –і–∞–љ–љ—Л–µ –≠–У–Ф–° –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —З–∞—Б—В–Њ—В–∞ —П–Ј–≤ –ґ–µ–ї—Г–і–Ї–∞ –Є 12––њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –±–Њ–ї–µ–µ —З–µ–Љ –≤ 4 —А–∞–Ј–∞ –Љ–µ–љ—М—И–µ, —З–µ–Љ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–∞ (—Е–Њ—В—П –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —П–Ј–≤ –ґ–µ–ї—Г–і–Ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ, —З–µ–Љ –љ–∞ –њ–ї–∞—Ж–µ–±–Њ) [45].
–£–Љ–µ–љ—М—И–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –Њ–њ–∞—Б–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ (–њ–Њ—З—В–Є –љ–∞ 40%) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є –љ––Э–Я–Т–Я –Є –Р–°–Ъ –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ Rahme E. et al. (2006). –Т —Е–Њ–і–µ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї–Њ–≥–Њ—А—В–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –∞–≤—В–Њ—А—Л –Њ–њ—А–µ–і–µ–ї–Є–ї–Є —А–Є—Б–Ї —Н—В–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –њ—А–Є 1522307 –Ї—Г—А—Б–∞—Е —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є 863464 –љ––Э–Я–Т–Я (–Є–Ј –љ–Є—Е 430214 –Є 195369 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —Б –љ–Є–Ј–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –Р–°–Ъ). –Ю–† –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –±–µ–Ј/—Б –Р–°–Ъ —Б–Њ—Б—В–∞–≤–Є–ї 0,41 (0,33–0,5) –Є 0,62 (0,48–0,8) —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [46].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Э–Я–Т–Я –Ј–∞—З–∞—Б—В—Г—О –≤–Њ–Ј–љ–Є–Ї–∞—О—В –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Њ—И–Є–±–Њ–Ї –≤—А–∞—З–∞ –Є –њ–∞—Ж–Є–µ–љ—В–∞. –Ш–Ј–±–µ–≥–∞—П —Н—В–Є—Е –Њ—И–Є–±–Њ–Ї, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –љ–µ—А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –Э–Я–Т–Я –Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ —Г—З–µ—В–Њ–Љ —Б–µ—А—М–µ–Ј–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –њ–Њ–≤—Л—И–∞—П —Г—А–Њ–≤–µ–љ—М –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Ј–љ–∞–љ–Є–є –±–Њ–ї—М–љ—Л—Е, –ї–µ—З–∞—Й–Є–є –≤—А–∞—З –Љ–Њ–ґ–µ—В –њ–Њ–і–Њ–±—А–∞—В—М –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Г—О –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Г—О —Б—В—А–∞—В–µ–≥–Є—О –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –і–ї—П –Ї–∞–ґ–і–Њ–≥–Њ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–ї—Г—З–∞—П. –°–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Є –∞–і–µ–Ї–≤–∞—В–љ—Л–µ –Љ–µ—А—Л –њ–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Б–µ—А—М–µ–Ј–љ—Л—Е –Ц–Ъ–Ґ––Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я —Г –±–Њ–ї—М–љ—Л—Е —Б —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞), –њ–Њ–Ј–≤–Њ–ї—П—О—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—Б–Є—В—М –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я –Є —А–∞—Б—И–Є—А–Є—В—М —Б—Д–µ—А—Г —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н—В–Є—Е –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.




–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Phillips DM. JCAHO pain standart are unveiled. JAMA 2000; 284: 428–429
2. Clark JD. Chronic pain prevalence and analgestic prescribing in a general medical population. J Pain Symp Manag 2002; 23: 131–137
3. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Э–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Я–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Љ–µ–і–Є—Ж–Є–љ–µ). –Ь–Њ—Б–Ї–≤–∞, –Ш–Ј–і–∞—В–µ–ї—М—Б—В–≤–Њ «–Р–љ–Ї–Њ», 2000; 142 —Б—В—А.
4. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы., –Ы–∞–Ј–µ–±–љ–Є–Ї –Ы.–С., –Ь–∞—А–µ–µ–≤ –Т.–Ѓ. –Є —Б–Њ—В—А. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є. –Ь–Њ—Б–Ї–≤–∞, 2006.
5. Lanas A. Prevention and treatment of NSAID–induced gastrointestinal injury. Curr Treat Options Gastroenterol 2006; 9: 147–156.
6. Dubois R., Melmed G., Henning J., Lane L. Guidelines for the appropriate use of non–steroidal anti–inflammatory drugs, cyclooxygenase–2 specific inhibitors and proton pump inhibitors in patients requiring chronic anti–inflammatory therapy. Aliment Pharmacol Ther 2004; 19: 197–208.
7. –Ф–∞–љ–Є–ї–Њ–≤ –Р.–С., –Ф–∞–≤—Л–і–Њ–≤ –Ю.–°. –Э–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М. –Ь. «–С–Њ—А–≥–µ—Б», 2007.
8. Gore M.Dukes E., Rowbotham D. et al. Clinical characteristics and pain management among patients with painful peripheral neuropathic disorders in general practice settings. Eur J Pain. 2007, 11(6), 652–664.
9. Walker J., Sheather–Reid R., Carmody J., et al. Nonsteroidal antiinflammatory drugs in rheumatoid arthritis and osteoarthritis: Support for the concept of ‘responders’ and ‘non–responders’. Arthritis Rheum., 1997, 40, 1944.
10. Schaible H–G., Ebersberger A., von Banchet G. Mechanism of pain in arthritis. Ann N Y Acad Sci 2002; 966; 343–354.
11. –Ъ–∞—А–∞—В–µ–µ–≤ –Р.–Х., –Ъ–∞—А–∞—В–µ–µ–≤ –Ф.–Х., –Ы—Г—З–Є—Е–Є–љ–∞ –Х.–Ы. –Є –і—А. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –Э–Я–Т–Я –њ—А–Є —А–∞–љ–љ–µ–Љ –∞—А—В—А–Є—В–µ. –†–Ь–Ц, 2006, 16, 24–29.
12. Dougados M., Gueguen A., Nakache J., et al. Ankylosing spondylitis: what is the optimum duration of a clinical study? A one year versus a 6 weeks non–steroidal anti–inflammatory drug trial. Rheumatology (Oxford). 1999, 38(3):235–244.
13. Henry D, Lim L, Garcia Rodriguez L. et al. Variability in risk of gastrointestinal complications with individual non–steroidal anti–inflammatory drugs: results of a collaborative meta–analysis. BMJ 1996; 312, 1563–1566.
14. Lewis S., Langman M., Laporte J. et al. Dose–response relationship between individual nonaspirine antiinflammatory drug (NANSAIDS) and serious upper gastrointestinal bleeding: a meta–analysis based on individual patient data. Br. J. Clin. Pharmacol., 2002, 54, 320–326
15. –Ъ–∞—А–∞—В–µ–µ–≤ –Р–Х. –Я–∞—В–Њ–ї–Њ–≥–Є—П –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О. –Ф–Є—Б—Б. –і.–Љ.–љ., –Ь–Њ—Б–Ї–≤–∞, 2006.
16. Roumie C., Griffin M. Over–the–counter analgesics in older adults: a call for improved labelling and consumer education. Drugs Aging. 2004, 21(8), 485–498.
17. Wilcox C., Cryer B., Triadafilopoulos G. Patterns of use and public perception of over–the–counter pain relievers: focus on nonsteroidal antiinflammatory drugs. J Rheumatol., 2005, 32(11), 2218–2224.
18. Lewis J., Kimmel S., Localio A. et al. Risk of serious upper gastrointestinal toxicity with over–the–counter nonaspirin nonsteroidal anti–inflammatory drugs. Gastroenterology. 2005, 129(6), 1865–1874.
19. –У—А–Є–љ—М–Ї–Њ –Р.–Т., –Р–Ј–∞—А–Њ–≤–∞ –Х.–Р. –С–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–∞—П —П–Ј–≤–∞ –ґ–µ–ї—Г–і–Ї–∞ –Є –Ї—А–Њ–≤–Њ—В–Њ—З–∞—Й–∞—П —П–Ј–≤–∞ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є, –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ—А–Є–µ–Љ–Њ–Љ –±–Њ–ї—М—И–Є—Е –і–Њ–Ј –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ –љ–∞—В—А–Є—П. –Ъ–ї–Є–љ. —А–µ–≤–Љ., 1996, 3, 54–57.
20. Lazerow S., Abdi M., Lewis J. Drug–induced liver disease 2004. Curr Opin Gastroenterol. 2005, 21(3), 283–292.
21. Larson A., Polson J., Fontana R. et al. Acetaminophen–induced acute liver failure: results of a United States multicenter, prospective study. Hepatology. 2005, 42(6), 1364–1372.
22. Gurwitz J., Field T., Harrold L., et al. Incidence and preventability of adverse drug events among older persons in the ambulatory setting. JAMA. 2003, 289(9), 1107–1116.
23. Perez Guttham S., Garcia Rodriguez L., raiford D., et al. Individual NSAIDs and other risk factor for upper gastrointestinal bleeding and perforation. Epidemiology, 1997, 8, 18–24.
24. Smolley W., Stein C., Arbogast P. et al. Underutilization of gastroprotective measures in patients receiving nonsteroidal antiinflammatory drugs. Arthritis Rheum., 2002, 46, 2195–2280.
25. Hartnell N., Flanagan P., MacKinnon N., Bakowsky V. Use of gastrointestinal preventive therapy among elderly persons receiving antiarthritic agents in Nova Scotia, Canada. Am J Geriatr Pharm. 2004, 2(3), 171–180.
26. –Ъ–∞—А–∞—В–µ–µ–≤ –Р.–Х., –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Э–Я–Т–Я––∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П –Ц–Ъ–Ґ: —А–µ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –і–µ–ї –≤ –†–Њ—Б—Б–Є–Є. –†–Ь–Ц, 2006, 15, 1073–1078.
27. Lanas A., Ferrandez A. Inappropriate prevention of NSAID–induced gastrointestinal events among long–term users in the elderly. Drugs Aging. 2007, 24(2), 121–131.
28. Derry S, Loke Y. Risk of gastrointestinal haemorrhage with long term use of aspirin: meta–analysis. BMJ, 2002; 521: 1183–1187.
29. Lanas A., Garsia–Rodriguez L., Arroyo M., et al. Risk of upper gastrointestinal ulcer bleeding associated with selective COX–2 inhibitors, traditional non–steroidal non–aspirin NSAID, aspirin, and combinations. Gut published online 10 may 2006; doi: 10.1136/gut.2005.080754
30. Biskupiak J., Brixner D., Howard K., Oderda G. Gastrointestinal complications of over–the–counter nonsteroidal antiinflammatory drugs. J Pain Palliat Care Pharmacother. 2006, 20(3), 7–14.
31. Rodriquez L., Hernandez–Diaz S. The risk of upper gastrointestinal complications associated with non–steroidal anti–inflammatory drugs, glucocorticoids, acetaminophen, and combination of these agents.
32. Cryer B., Feldman M. Effect of very low dose daily long–term therapy on gastric, duodenal, and rectal prostaglandin levels and mucosal injury in healthy human. Gastroenterology, 1999, 117, 17–25.
33. Mellemkjaer L., Blot W., Sorensen H., et al. Upper gastrointestinal bleeding among users of NSAIDs: a population–based cohort study in Denmark. Br. J. Clin. Pharmacol., 2002, 53, 173–181.
34. –Ъ—Г–Ї—Г—И–Ї–Є–љ –Ь.–Ы., –•–Є—В—А–Њ–≤ –Э.–Ъ. –Ю–±—Й–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П –±–Њ–ї–Є. –Ь–Њ—Б–Ї–≤–∞, «–Ь–µ–і–Є—Ж–Є–љ–∞», 2004.
35. Airaksinen O., Brox J., Cedraschi C., et al. European guidelines for the management of chronic non specific low back pain. Eur. Spine J., 2006, 15 (suppl.2), 192–300.
36. Van Tulder M. Chronic Low Back Pain. Am. Fam. Phys. 2007, 74, вДЦ9
37. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Я—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є. –Ь–Њ—Б–Ї–≤–∞, «–Ь––°–Є—В–Є», 1996.
38. Boswell M., Colson J., Sehgal N., et al. A systematic rewiew of therapeutic facet joint interventions in chronic spinal pain. Pain Physician, 2007, 10, 229–253
39. Moore R., Derry S., Makinson G., McQuay H. Tolerability and adverse events in clinical trials of celecoxib in osteoarthritis and rheumatoid arthritis: systemic review and meta–analysis on information from company clinical reports. Arthritis Res Ther 2005; 7: 644–665.
40. Chan F., Hung L., Suen B. et al. Celecoxib versus diclofenac and omeprasole in reducing the risk of recurrent ulcer bleeding in patients with arthritis. N Engl J Med 2002, 947, 2104–2110
41. Lai K., Chu K., Hui W. et al. Celecoxib compared with lansoprazole and naproxen to prevent gastrointestinal ulcer complications. Am J Med. 2005, 118(11), 1271–1278.
42. Chan F., Wong V., Suen B., et al. Combination of a cyclo–oxygenase–2 inhibitor and a proton–pump inhibitor for prevention of recurrent ulcer bleeding in patients at very high risk: a double–blind, randomised trial. Lancet, 2007, 369, 1621–1626.
43. –Ъ–∞—А–∞—В–µ–µ–≤ –Р.–Х. –У–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2. –Э–∞—Г—З–љ–Њ – –Я—А–∞–Ї—В. –†–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П, 2006, 2, 34–39.
44. Strand V. Are COX–2 inhibitors preferable to non–selective non–steroidal anti–inflammatory drugs in patients with risk of cardiovascular events taking low–dose aspirin? Lancet. 2007, 370(9605), 2138–2151.
45. Goldstein J., Aisenbeg J., Berger M., et al. Effects of concominant aspirin (81 mg) –Њn incidence the of gastric and/or duodenal ulcers in healthy subjects taking celecoxib or naproxen: a randomized placebo–controlled trial. Ann Rheum Dis 2006; 65 (Suppl. II): 229 (TH0327 abst).
46. Rachme E., Bardon M., Dasgupta K., et al. Hospitalisation for gastrointestinal bleeding associated with non–steroidal anti–inflammatory drugs among elderly patients using low–dose aspirin: a retrospective cohort study. Rheumatology, 2006, jul 13 (Epub ahead of print).












