–†–µ–≤–Љ–∞—В–Њ–Є–і–љ—Л–є –∞—А—В—А–Є—В (–†–Р) –Є –і—А—Г–≥–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ (–∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ) —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ—В–љ–Њ—Б—П—В—Б—П –Ї —З–Є—Б–ї—Г –≤–µ—Б—М–Љ–∞ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Є –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Д–Њ—А–Љ –њ–∞—В–Њ–ї–Њ–≥–Є–Є —З–µ–ї–Њ–≤–µ–Ї–∞ [1]. –Ю–љ–Є –Љ–Њ–≥—Г—В –±—Л—Б—В—А–Њ –њ—А–Є–≤–Њ–і–Є—В—М –Ї –Є–љ–≤–∞–ї–Є–і–љ–Њ—Б—В–Є, –∞ –љ–µ—А–µ–і–Ї–Њ –Є –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [2]. –Э–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –ґ–Є–Ј–љ–µ–љ–љ—Л–є –њ—А–Њ–≥–љ–Њ–Ј –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤, —Б–≤—П–Ј–∞–љ–љ—Л–Љ –Ї–∞–Ї —Б —В—П–ґ–µ—Б—В—М—О —Б–∞–Љ–Њ–≥–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –ї–µ—З–µ–љ–Є—П, —В–∞–Ї –Є —Б —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–•–Њ—В—П —Н—В–Є–Њ–ї–Њ–≥–Є—П –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є –Њ—Б—В–∞–µ—В—Б—П –љ–µ–Є–Ј–≤–µ—Б—В–љ–Њ–є, –Њ—Б–љ–Њ–≤–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Љ–љ–Њ–≥–Є—Е –Є–Ј –љ–Є—Е –Є–Ј—Г—З–µ–љ—Л –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –њ–Њ–і—А–Њ–±–љ–Њ [2]. –≠—В–Њ –Є –њ–Њ—Б–ї—Г–ґ–Є–ї–Њ –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –Ї–Њ–љ—Ж–µ–њ—Ж–Є–Є “–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є” —В–µ—А–∞–њ–Є–Є. –Ъ —З–Є—Б–ї—Г “–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е” –Њ—В–љ–Њ—Б—П—В –±–Њ–ї—М—И–Њ–µ —З–Є—Б–ї–Њ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л—Е –њ–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ –Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤: –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і—Л, –∞–Љ–Є–љ–Њ—Е–Є–љ–Њ–ї–Є–љ–Њ–≤—Л–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ, —Б–Њ–ї–Є –Ј–Њ–ї–Њ—В–∞, —Б—Г–ї—М—Д–∞—Б–∞–ї–∞–Ј–Є–љ, –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В, –ї–µ—Д–ї—О–љ–∞–Љ–Є–і, —Ж–Є–Ї–ї–Њ—Б–њ–Њ—А–Є–љ –Р, —Ж–Є—В–Њ—В–Њ–Ї—Б–Є–Ї–Є (—Ж–Є–Ї–ї–Њ—Д–Њ—Б—Д–∞–Љ–Є–і, —Е–ї–Њ—А–∞–Љ–±—Г—Ж–Є–ї, –∞–Ј–∞—В–Є–Њ–њ—А–Є–љ) –Є –і—А. [3]. –Ш—Е –Њ–±—К–µ–і–Є–љ—П–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –≤ –±–Њ–ї—М—И–µ–є –Є–ї–Є –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Є –Ј–∞ —Б—З–µ—В —А–∞–Ј–ї–Є—З–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –њ–Њ–і–∞–≤–ї—П—В—М –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –Є/–Є–ї–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–∞—Ж–Є—О —Б–Є—Б—В–µ–Љ—Л –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞. –Ю–і–љ–∞–Ї–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Ј —Н—В–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —А–∞–Ј—А–∞–±–∞—В—Л–≤–∞–ї–Є—Б—М –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–µ —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е, –∞ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є–ї–Є –і–ї—П –љ—Г–ґ–і —В—А–∞–љ—Б–њ–ї–∞–љ—В–Њ–ї–Њ–≥–Є–Є.
–•–Њ—В—П “–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–∞—П” —В–µ—А–∞–њ–Є—П –і–µ–є—Б—В–≤–Є—В–µ–ї—М–љ–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–ї—Г—З—И–Є—В—М –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є, –±–ї–Є–ґ–∞–є—И–Є–є –Є –Њ—В–і–∞–ї–µ–љ–љ—Л–є –њ—А–Њ–≥–љ–Њ–Ј —Г –Љ–љ–Њ–≥–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ—Б—В–∞–µ—В—Б—П –љ–µ–Љ–∞–ї–Њ –±–Њ–ї—М–љ—Л—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –Њ–љ–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞. –Ъ —Д–∞–Ї—В–Њ—А–∞–Љ, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—Й–Є–Љ –µ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є, –Њ—В–љ–Њ—Б—П—В—Б—П –њ–ї–Њ—Е–Њ –њ—А–Њ–≥–љ–Њ–Ј–Є—А—Г–µ–Љ–∞—П —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М –Є/–Є–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –≠—В–Њ –і–Є–Ї—В—Г–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –љ–Њ–≤—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї “–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є” —В–µ—А–∞–њ–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є [4].
–Ю–і–љ–Њ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —П—А–Ї–Є—Е –і–Њ—Б—В–Є–ґ–µ–љ–Є–є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —З–µ–ї–Њ–≤–µ–Ї–∞ –Ї–Њ–љ—Ж–∞ XX –≤–µ–Ї–∞ —Б–≤—П–Ј–∞–љ–Њ —Б —А–∞–Ј—А–∞–±–Њ—В–Ї–Њ–є –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –љ–Њ–≤–Њ–є –≥—А—Г–њ–њ—Л –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–Є–ї–Є –љ–∞–Ј–≤–∞–љ–Є–µ “–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ” –∞–≥–µ–љ—В—Л (“biologic” agents) [4,5]. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Ї –љ–Є–Љ –Њ—В–љ–Њ—Б—П—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –±–Є–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –њ—Г—В–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤: –Љ–Њ–љ–Њ–Ї–ї–Њ–љ–∞–ї—М–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ (–Љ–Р–Ґ) –њ—А–Њ—В–Є–≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –і–µ—В–µ—А–Љ–Є–љ–∞–љ—В –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Є–ї–Є “–њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е” —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤, —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л–µ “–∞–љ—В–Є–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ” —Ж–Є—В–Њ–Ї–Є–љ—Л –Є –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ (—А–∞—Б—В–≤–Њ—А–Є–Љ—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л, –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л) [4,5].
–Ю—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –≤—Л–Ј—Л–≤–∞—О—В –Љ–Р–Ґ, —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –±—Л—Б—В—А–Њ–µ –њ–Њ—П–≤–ї–µ–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Б–≤—П–Ј–∞–љ–Њ —Б –љ–µ—Б–Ї–Њ–ї—М–Ї–Є–Љ–Є –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–∞–Љ–Є. –Т–Њ-–њ–µ—А–≤—Л—Е, –±–ї–∞–≥–Њ–і–∞—А—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П–Љ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –±–Є–Њ–ї–Њ–≥–Є–Є –Є –њ—А–Њ–Љ—Л—И–ї–µ–љ–љ–Њ–є –±–Є–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є, –±—Л–ї–∞ —А–µ—И–µ–љ–∞ –≤–∞–ґ–љ–µ–є—И–∞—П –њ—А–Њ–±–ї–µ–Љ–∞ – —И–Є—А–Њ–Ї–Њ–Љ–∞—Б—И—В–∞–±–љ–Њ–µ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–Њ –Љ–Р–Ґ (—Е–Є–Љ–µ—А–љ—Л–µ, –≥—Г–Љ–∞–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ), –±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –њ—А–Є –≤–≤–µ–і–µ–љ–Є–Є —З–µ–ї–Њ–≤–µ–Ї—Г [6]. –Т–Њ-–≤—В–Њ—А—Л—Е, –њ—А–Њ–≥—А–µ—Б—Б –≤ –Є–Ј—Г—З–µ–љ–Є–Є –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є–Є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є –њ–Њ–Ј–≤–Њ–ї–Є–ї —Г—Б—В–∞–љ–Њ–≤–Є—В—М –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–µ “–Љ–Є—И–µ–љ–Є” –і–ї—П —В–µ—А–∞–њ–Є–Є –Љ–Р–Ґ, –Ї –Ї–Њ—В–Њ—А—Л–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М “–њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ” —Ж–Є—В–Њ–Ї–Є–љ—Л. –Ъ –≤–∞–ґ–љ—Л–Љ –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–∞–Љ “–∞–љ—В–Є—Ж–Є—В–Њ–Ї–Є–љ–Њ–≤—Л—Е” –Љ–Р–Ґ –Њ—В–љ–Њ—Б–Є—В—Б—П –Є—Е –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–∞—П —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М, –Ї–Њ—В–Њ—А–∞—П –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –Ј–≤–µ–љ—М—П –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –Ј–∞—В—А–∞–≥–Є–≤–∞—П –љ–Њ—А–Љ–∞–ї—М–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –≠—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –≥–µ–љ–µ—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–Њ–є –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є–Є, –Ї–Њ—В–Њ—А–∞—П —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –і–ї—П –Љ–љ–Њ–≥–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤ –Є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є–Ї–Њ–≤. –Э–∞–Ї–Њ–љ–µ—Ж, –Є–Ј—Г—З–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ “–∞–љ—В–Є—Ж–Є—В–Њ–Ї–Є–љ–Њ–≤—Л—Е” –Љ–Р–Ґ –љ–µ—А–µ–і–Ї–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–Є—В—М –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –љ–Њ–≤—Л–µ —Д–∞–Ї—В—Л –Њ —А–Њ–ї–Є —В–µ—Е –Є–ї–Є –Є–љ—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є.
–Э–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ–Њ–є “–Љ–Є—И–µ–љ—М—О” –і–ї—П “–∞–љ—В–Є—Ж–Є—В–Њ–Ї–Є–љ–Њ–≤–Њ–є” —В–µ—А–∞–њ–Є–Є –Љ–Р–Ґ —П–≤–ї—П–µ—В—Б—П “–њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є” —Ж–Є—В–Њ–Ї–Є–љ – —Д–∞–Ї—В–Њ—А –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є (–§–Э–Ю) -a. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ —Н—В–Њ—В —Ж–Є—В–Њ–Ї–Є–љ –Є–≥—А–∞–µ—В –≤–µ–і—Г—Й—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є —Б–∞–Љ—Л—Е —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є, —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –і–ї—П –Љ–љ–Њ–≥–Є—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —З–µ–ї–Њ–≤–µ–Ї–∞ [7,8]. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞–Є–±–Њ–ї–µ–µ –≤–µ—Б–Ї–Є–µ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П –§–Э–Ю-a –њ–Њ–ї—Г—З–µ–љ—Л –њ—А–Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–Љ –∞—А—В—А–Є—В–µ (–†–Р). –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Є–Љ–µ–љ–љ–Њ –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–∞—П –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є—П —Н—В–Њ–≥–Њ —Ж–Є—В–Њ–Ї–Є–љ–∞ –ї–µ–ґ–Є—В –≤ –Њ—Б–љ–Њ–≤–µ —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є –Ї–Њ—Б—В–љ–Њ–є –і–µ—Б—В—А—Г–Ї—Ж–Є–Є [9]. –Ш–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ–± —Г—З–∞—Б—В–Є–Є –§–Э–Ю-a –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –Є –і—А—Г–≥–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є (—В–∞–±–ї. 1). –Я–Њ—Н—В–Њ–Љ—Г –µ—Б—В—М –≤–µ—Б–Ї–Є–µ –Њ—Б–љ–Њ–≤–∞–љ–Є—П –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—В—М, —З—В–Њ –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –†–Р, –љ–Њ –Є –њ—А–Є –і—А—Г–≥–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є–љ–≥–Є–±–Є—Ж–Є—П –§–Э–Ю-a —Б –њ–Њ–Љ–Њ—Й—М—О –Љ–Р–Ґ –Љ–Њ–ґ–µ—В –Њ–Ї–∞–Ј–∞—В—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —В–µ—З–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П, –Є –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –і–∞–ґ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г—Б—В–Њ–є—З–Є–≤—Л—Е –Ї –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–є “—Б—В–∞–љ–і–∞—А—В–љ–Њ–є” —В–µ—А–∞–њ–Є–Є.

• –†–Р
• —Б–µ—А–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–њ–∞—В–Є–Є (–∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–Є–є —Б–њ–Њ–і–Є–ї–Њ–∞—А—В—А–Є—В, –њ—Б–Њ—А–Є–∞—В–Є—З–µ—Б–Ї–Є–є –∞—А—В—А–Є—В)
• —О–≤–µ–љ–Є–ї—М–љ—Л–є –∞—А—В—А–Є—В –Є —Г–≤–µ–Є—В —Г –і–µ—В–µ–є
• –±–Њ–ї–µ–Ј–љ—М –°—В–Є–ї–ї–∞ —Г –≤–Ј—А–Њ—Б–ї—Л—Е
• —Б–Є—Б—В–µ–Љ–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П
• –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Љ–Є–Њ–њ–∞—В–Є–Є (–њ–Њ–ї–Є–Љ–Є–Њ–Ј–Є—В –Є –і–µ—А–Љ–∞—В–Њ–Љ–Є–Њ–Ј–Є—В)
• –≥—А–∞–љ—Г–ї–µ–Љ–∞—В–Њ–Ј –Т–µ–≥–µ–љ–µ—А–∞
• –±–Њ–ї–µ–Ј–љ—М –Ъ—А–Њ–љ–∞
• –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А—Г—О—Й–Є–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л
• –Ј–∞—Б—В–Њ–є–љ–∞—П —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М.
–Я–µ—А–≤—Л–Љ–Є –≤–љ–µ–і—А–µ–љ–љ—Л–Љ–Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –њ—А–∞–Ї—В–Є–Ї—Г –Љ–Р–Ґ –Ї –§–Э–Ю-a, —А–∞–Ј—А–µ—И–µ–љ–љ—Л–Љ–Є –і–ї—П –ї–µ—З–µ–љ–Є—П –†–Р, —П–≤–ї—П—О—В—Б—П —Е–Є–Љ–µ—А–љ—Л–µ –Љ–Р–Ґ – –Є–љ—Д–ї–Є–Ї—Б–Є–Љ–∞–± (–†–µ–Љ–Є–Ї–µ–є–і) [10-13]. –Ю–љ–Є —Б–Њ—Б—В–Њ—П—В –Є–Ј –≤–∞—А–Є–∞–±–Є–ї—М–љ–Њ–є (Fv) –Њ–±–ї–∞—Б—В–Є –≤—Л—Б–Њ–Ї–Њ –∞—Д–Є–љ–љ—Л—Е –љ–µ–є—В—А–∞–ї–Є–Ј—Г—О—Й–Є—Е –Љ—Л—И–Є–љ—Л—Е –Љ–Р–Ґ –Ї –§–Э–Ю-a, —Б–Њ–µ–і–Є–љ–µ–љ–љ—Л—Е —Б —Д—А–∞–≥–Љ–µ–љ—В–Њ–Љ –Љ–Њ–ї–µ–Ї—Г–ї—Л IgG1k —З–µ–ї–Њ–≤–µ–Ї–∞, –≤ —Ж–µ–ї–Њ–Љ –Ј–∞–љ–Є–Љ–∞—О—Й–µ–є –і–≤–µ —В—А–µ—В–Є –Љ–Њ–ї–µ–Ї—Г–ї—Л –Р–Ґ –Є –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–µ–є —Н—Д—Д–µ–Ї—В–Њ—А–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є –Р–Ґ. –Я—А–µ–њ–∞—А–∞—В –Њ–±–ї–∞–і–∞–µ—В –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–Њ–є –∞—Д–Є–љ–љ–Њ—Б—В—М—О –Ї —В—А–Є–Љ–µ—А–љ–Њ–Љ—Г –§–Э–Ю-a (Kd – 100 pM). –Я–Њ –і–∞–љ–љ—Л–Љ –Њ–њ—Л—В–Њ–≤ in vitro, –њ—А–µ–њ–∞—А–∞—В, –Њ–±—А–∞–Ј—Г—П —Б—В–∞–±–Є–ї—М–љ—Л–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б—Л —Б –§–Э–Ю-a, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ–Њ–і–∞–≤–ї—П–µ—В –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–µ–Ї—А–µ—Ж–Є—А—Г–µ–Љ–Њ–≥–Њ –Є –Љ–µ–Љ–±—А–∞–љ-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –§–Э–Ю-b (–љ–Њ –љ–µ –ї–Є–Љ—Д–Њ—В–Њ–Ї—Б–Є–љ–∞ –§–Э–Ю-b), –Є –Є–љ–і—Г—Ж–Є—А—Г–µ—В –ї–Є–Ј–Є—Б –§–Э–Ю-–њ—А–Њ–і—Г—Ж–Є—А—Г—О—Й–Є—Е –Ї–ї–µ—В–Њ–Ї, –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В-–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –њ—Г—В–µ–Љ –Є–ї–Є –Ј–∞ —Б—З–µ—В –∞–љ—В–Є—В–µ–ї–Њ-–Ј–∞–≤–Є—Б–Є–Љ–Њ–є –Ї–ї–µ—В–Њ—З–љ–Њ–є —Ж–Є—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є. –Э–µ–і–∞–≤–љ–Њ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е –†–Р –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Є–љ–≥–Є–±–Є—Ж–Є—П —Б–Є–љ—В–µ–Ј–∞ –§–Э–Ю-a —Б–Є–љ–Њ–≤–Є–∞–ї—М–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є [14].
–§–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞
–Ю—Б–љ–Њ–≤–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ–Њ–ї—Г—З–µ–љ—Л –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –њ—А–µ–њ–∞—А–∞—В–∞ —Г –±–Њ–ї—М–љ—Л—Е –†–Р [10,11]. –Я—А–Є –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є (1, 3, 5, 10 –Є–ї–Є 20 –Љ–≥/–Ї–≥) –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ –њ–ї–∞–Ј–Љ–µ (–°max) –Є –њ–ї–Њ—Й–∞–і—М –њ–Њ–і –Ї—А–Є–≤–Њ–є (AUC) –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ—Л –≤–≤–Њ–і–Є–Љ–Њ–є –і–Њ–Ј–µ –њ—А–µ–њ–∞—А–∞—В–∞. –Ю–±—К–µ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –≤–љ—Г—В—А–Є—Б–Њ—Б—Г–і–Є—Б—В–Њ–Љ—Г, –∞ –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–ґ–Є–Ј–љ–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 8-12 –і–љ–µ–є. –£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е –†–µ–Љ–Є–Ї–µ–є–і –≤—Л—П–≤–ї—П–µ—В—Б—П –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–∞—Е –њ–Њ –Љ–µ–љ—М—И–µ–є –Љ–µ—А–µ –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і–µ–ї—М –њ—А–Є –њ–Њ–≤—В–Њ—А–љ—Л—Е –≤–≤–µ–і–µ–љ–Є—П—Е –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–µ 3 –Љ–≥/–Ї–≥, –Њ–і–љ–∞–Ї–Њ –∞–љ–Њ–Љ–∞–ї—М–љ–Њ–≥–Њ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—П –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ, –∞ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ –Ї—А–Њ–≤—П–љ–Њ–Љ —А—Г—Б–ї–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –≤–≤–Њ–і–Є–Љ–Њ–є –і–Њ–Ј–µ. –Я—А–µ–њ–∞—А–∞—В –љ–µ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П –≤ –Љ–Њ—З–µ. –Ч–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Ї–ї–Є—А–µ–љ—Б–∞ –Є–ї–Є –Њ–±—К–µ–Љ–∞ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤–Њ–Ј—А–∞—Б—В–∞ –Є–ї–Є –≤–µ—Б–∞ –±–Њ–ї—М–љ—Л—Е –†–Р –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ. –С—Г–і—Г—З–Є –±–µ–ї–Ї–Њ–≤—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –Њ–љ –љ–µ –њ–Њ–і–≤–µ—А–≥–∞–µ—В—Б—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ—Г –≤ –њ–µ—З–µ–љ–Є —Ж–Є—В–Њ—Е—А–Њ–Љ–Њ–Љ –†-450. –Я–Њ—Н—В–Њ–Љ—Г –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–Њ–≤ –†-450, –љ–µ—А–µ–і–Ї–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—Й–Є–є —А–∞–Ј–ї–Є—З–љ—Г—О —З–∞—Б—В–Њ—В—Г —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–µ –Є–Љ–µ–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ.
–†–µ–≤–Љ–∞—В–Њ–Є–і–љ—Л–є –∞—А—В—А–Є—В
–Ю—Б–љ–Њ–≤–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –і–ї—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ —П–≤–ї—П–µ—В—Б—П –†–Р, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ —Е–Њ—А–Њ—И–Њ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–∞ –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е (—В–∞–±–ї. 2) –Є –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –≤ 2 –Њ—В–Ї—А—Л—В—Л—Е –Є 4 –њ–ї–∞—Ж–µ–±–Њ – –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е, —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е, –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –≤–Ї–ї—О—З–∞–≤—И–Є—Е –±–Њ–ї–µ–µ 650 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ь–∞—В–µ—А–Є–∞–ї—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –≤ –љ–∞—И–µ–є –њ—А–µ–і—Л–і—Г—Й–µ–є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є [10] –Є –Њ–±–Ј–Њ—А–∞—Е –і—А—Г–≥–Є—Е –∞–≤—В–Њ—А–Њ–≤ [11-13]. –Я–Њ—Н—В–Њ–Љ—Г –Њ—Б–љ–Њ–≤–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –±—Г–і–µ—В —Г–і–µ–ї–µ–љ–Њ –∞–љ–∞–ї–Є–Ј—Г –љ–Њ–≤—Л—Е –і–∞–љ–љ—Л—Е, –Ї–∞—Б–∞—О—Й–Є—Е—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –Є –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В–∞ (–Ь–Ґ). –≠—В–Њ—В –њ–Њ–і—Е–Њ–і —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П, –Ї–∞–Ї –љ–∞–Є–±–Њ–ї–µ–µ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–є –і–ї—П –ї–µ—З–µ–љ–Є—П –†–Р, –љ–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г—О—Й–µ–≥–Њ—Б—П “—Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є” –Љ–µ—В–Њ–і–∞–Љ–Є –ї–µ—З–µ–љ–Є—П [15]. –•–Њ—В—П –Ь–Ґ – –Њ–і–Є–љ –Є—Е –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –†–Р [16], —Г –Љ–љ–Њ–≥–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ —Г–і–∞–µ—В—Б—П –і–Њ—Б—В–Є–≥–љ—Г—В—М —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Є –Ј–∞–Љ–µ–і–ї–µ–љ–Є—П –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —Б—Г—Б—В–∞–≤–љ–Њ–є –і–µ—Б—В—А—Г–Ї—Ж–Є–Є, –∞ —Г –і—А—Г–≥–Є—Е – —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Ј–∞–≤–Є—Б–Є–Љ—Л–µ –Њ—В –і–Њ–Ј—Л —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–љ—Д—Г–Ј–Є–Є –†–µ–Љ–Є–Ї–µ–є–і–∞ –Љ–Њ–≥—Г—В –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞—В—М —Б–Є–љ—В–µ–Ј –Р–Ґ –Ї –Љ—Л—И–Є–љ–Њ–Љ—Г —Д—А–∞–≥–Љ–µ–љ—В—Г –Љ–Њ–ї–µ–Ї—Г–ї—Л –њ—А–µ–њ–∞—А–∞—В–∞ (—З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–µ –∞–љ—В–Є—Е–Є–Љ–µ—А–љ—Л–µ –∞–љ—В–Є—В–µ–ї–∞ – –І–Р–•–Р), –њ—А–Є–≤–Њ–і—П—Й–Є–є –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є —А–∞–Ј–≤–Є—В–Є—О –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є. –Я–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ь–Ґ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–і–∞–≤–Є—В—М —Б–Є–љ—В–µ–Ј –І–Р–•–Р –Є —В–µ–Љ —Б–∞–Љ—Л–Љ –њ–Њ–≤—Л—Б–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є. –Т—Б–µ —Н—В–Њ –≤–Љ–µ—Б—В–µ –≤–Ј—П—В–Њ–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –Є–Љ–µ–љ–љ–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Г—О —В–µ—А–∞–њ–Є—О c –Ь–Ґ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ —Б–њ–Њ—Б–Њ–±–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Є –†–Р [17].


–І–µ—А–µ–Ј 30 –љ–µ–і–µ–ї—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–Њ –Ї—А–Є—В–µ—А–Є—П–Љ –Р–Ъ–†20 –Њ—В–Љ–µ—З–µ–љ —Г 50% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е 3 –Љ–≥/–Ї–≥, —Г 52% – 10 –Љ–≥/–Ї–≥ –њ—А–µ–њ–∞—А–∞—В–∞ –Є –ї–Є—И—М —Г 20% –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ (—А<0,001). –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ –Ј–∞–≤–Є—Б–µ–ї–∞ –Њ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –≤–Њ–Ј—А–∞—Б—В–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –І–µ—А–µ–Ј 54 –љ–µ–і–µ–ї–Є —З–Є—Б–ї–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –њ–Њ –Ї—А–Є—В–µ—А–Є—П–Љ –Р–Ъ–†20 —Б–Њ—Б—В–∞–≤–Є–ї–Њ 42% (3 –Љ–≥/–Ї–≥) –Є 59% (10 –Љ–≥/–Ї–≥), –∞ –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ – 17% (—А<0,001).
–Ю—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ —В–Њ–Љ, —З—В–Њ —Г —З–∞—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –ї–µ—З–µ–љ–Є–µ –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Є–≤–Њ–і–Є–ї–Њ –љ–µ —В–Њ–ї—М–Ї–Њ –Ї —Г–Љ–µ—А–µ–љ–љ–Њ–Љ—Г (–љ–∞ 20%), –љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г – –љ–∞ 50% (–Р–Ъ–†50) –Є 70% (–Р–Ъ–†70) —Г–ї—Г—З—И–µ–љ–Є—О. –І–µ—А–µ–Ј 30 –љ–µ–і–µ–ї—М —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ –Ї—А–Є—В–µ—А–Є—О –Р–Ъ–†50 –Њ—В–Љ–µ—З–µ–љ–Њ —Г 27% –Є 31% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –†–µ–Љ–Є–Ї–µ–є–і –≤ –і–Њ–Ј–µ 3 –Љ–≥/–Ї–≥ –Є 10 –Љ–≥/–Ї–≥ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ – —В–Њ–ї—М–Ї–Њ —Г 5% (—А<0,001). –І–µ—А–µ–Ј 54 –љ–µ–і–µ–ї–Є –Њ—В–≤–µ—В –њ–Њ –Р–Ъ–†50 –Њ—В–Љ–µ—З–µ–љ —Г 33%, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –†–µ–Љ–Є–Ї–µ–є–і, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ – —В–Њ–ї—М–Ї–Њ —Г 18%. –Э–∞–Ї–Њ–љ–µ—Ж, —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ –Ї—А–Є—В–µ—А–Є—О –Р–Ъ–†70 —З–µ—А–µ–Ј 30 –љ–µ–і–µ–ї—М –Є–Љ–µ–ї–Њ –Љ–µ—Б—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ —Г 8% (p<0,05) –Є 18% (—А<0,001) –ї–µ—З–µ–љ–љ—Л—Е –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –Є –љ–Є —Г –Ї–Њ–≥–Њ –Є–Ј –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ–ї–∞—Ж–µ–±–Њ, –∞ —З–µ—А–µ–Ј 54 –љ–µ–і–µ–ї–Є – —Г 11% (—А<0,05), 26% (p<0,001) –Є 3%. –Т–∞–ґ–љ–Њ, —З—В–Њ —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –ї–µ—З–µ–љ–љ—Л—Е –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ, –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–Њ –Р–Ъ–†50 –Є –Р–Ъ–†70 –Њ—В–Љ–µ—З–∞–ї—Б—П —Г–ґ–µ —З–µ—А–µ–Ј 2 –љ–µ–і–µ–ї–Є –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–є –Є–љ—Д—Г–Ј–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞. –Э–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —П–≤–љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –°–†–С, —Б—А–µ–і–љ—П—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Ї–Њ—В–Њ—А–Њ–≥–Њ —З–µ—А–µ–Ј 54 –љ–µ–і–µ–ї–Є —Б–љ–Є–Ј–Є–ї–∞—Б—М –і–Њ –љ–Њ—А–Љ—Л (< 1 –Љ–Ї–≥/–Љ–ї) —Г –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е, –∞ –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ –Њ—Б—В–∞–≤–∞–ї–∞—Б—М –±–µ–Ј –Є–Ј–Љ–µ–љ–µ–љ–Є–є.
–Ъ –Ї–Њ–љ—Ж—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –љ–∞ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–њ–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞–Љ —Б–Њ—Б—В–Њ—П–љ–Є—П –Ј–і–Њ—А–Њ–≤—М—П HAQ –Є SF-36) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ (p<0,001). –°–ї–µ–і—Г–µ—В –Њ—Б–Њ–±–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –±—Л–ї–Њ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е —В—П–ґ–µ–ї—Л–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ –Ї “–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є” —В–µ—А–∞–њ–Є–Є –†–Р (–љ–µ –Љ–µ–љ–µ–µ 3 –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є) –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 8 –ї–µ—В.
–Р–љ–∞–ї–Є–Ј —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є –≤ –Ї–Њ–љ—Ж–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —В–µ—А–∞–њ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –Ј–∞–Љ–µ–і–ї—П–µ—В –Є –і–∞–ґ–µ –њ—А–Є–Њ—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ —Б—Г—Б—В–∞–≤–љ–Њ–є –і–µ—Б—В—А—Г–Ї—Ж–Є–Є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –†–Р –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –і–Є–љ–∞–Љ–Є–Ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –£—Б—А–µ–і–љ–µ–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є–љ–і–µ–Ї—Б–∞ –®–∞—А–њ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –†–µ–Љ–Є–Ї–µ–є–і –≤ –і–Њ–Ј–∞—Е 3 –Љ–≥/–Ї–≥ –Є 10 –Љ–≥/–Ї–≥, —Б–Њ—Б—В–∞–≤–Є–ї–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ 1,2 –Є 0,4, –∞ –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ 7,0. –£–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є–љ–і–µ–Ї—Б–∞ –®–∞—А–њ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –†–µ–Љ–Є–Ї–µ–є–і –і–Њ–Ј–µ 3 –Љ–≥/–Ї–≥ (45%) –Є 10 –Љ–≥/–Ї–≥ (39%), —З–µ–Љ –њ–ї–∞—Ж–µ–±–Њ (14%) (p<0,001).
–Ф—А—Г–≥–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П
–Я—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Њ—В–Ї—А—Л—В—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є–є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Є —Б–µ—А–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л—Е —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–њ–∞—В–Є—П—Е (—В–∞–±–ї. 4). –≠—В–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ, –µ—Б–ї–Є –њ—А–Є–љ–Є–Љ–∞—В—М –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –†–Р –њ–Њ–і—Е–Њ–і—Л –Ї “–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є” —В–µ—А–∞–њ–Є–Є —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Д–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ —А–∞–Ј—А–∞–±–Њ—В–∞–љ—Л [29].
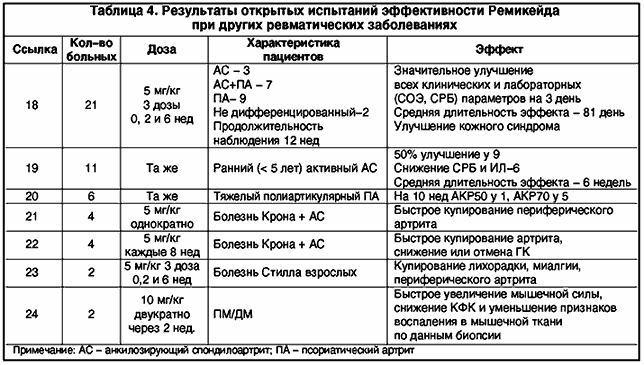
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є J. Brandt –Є —Б–Њ–∞–≤—В. [23], –≤ –Ї–Њ—В–Њ—А–Њ–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 11 –±–Њ–ї—М–љ—Л—Е —Б –∞–Ї—В–Є–≤–љ—Л–Љ “—А–∞–љ–љ–Є–Љ” (–Љ–µ–љ–µ–µ 5 –ї–µ—В) –∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–Є–Љ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–Љ (–±–Њ–ї–µ–Ј–љ—М –С–µ—Е—В–µ—А–µ–≤–∞), —Г –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е (—Г 9 –Є–Ј 10) –Њ—В–Љ–µ—З–µ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ (>50%) –њ–Њ –Є–љ–і–µ–Ї—Б–∞–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ (SF-36) –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–Є. –Я–Њ –Є–љ–і–µ–Ї—Б—Г BASD–РI (Bath Ankylosing Spondilitis Activity Index) —З–µ—А–µ–Ј 4 –љ–µ–і–µ–ї–Є —Б—А–µ–і–љ–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —Б–Њ—Б—В–∞–≤–Є–ї 70%, —З—В–Њ –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ —Г–ї—Г—З—И–µ–љ–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–Њ—Е—А–∞–љ—П–ї—Б—П –≤ —В–µ—З–µ–љ–Є–µ 6 –љ–µ–і–µ–ї—М –њ–Њ—Б–ї–µ —В—А–µ—В—М–µ–є –Є–љ—Д—Г–Ј–Є–Є –†–µ–Љ–Є–Ї–µ–є–і–∞ —Г 8 –Є–Ј 10 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ю—В–Љ–µ—З–µ–љ–Њ —В–∞–Ї–ґ–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –°–†–С (–≤ —Б—А–µ–і–љ–µ–Љ —Б 15,5 –Љ–Ї–≥/–Љ–ї –і–Њ –љ–Њ—А–Љ—Л) –Є –Ш–Ы-6 (–≤ —Б—А–µ–і–љ–µ–Љ —Б 12,4 –љ–≥/–ї –і–Њ –љ–Њ—А–Љ—Л, –Љ–µ–љ–µ–µ 5 –љ–≥/–ї).
C. Antony –Є —Б–Њ–∞–≤—В [24] –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –†–µ–Љ–Є–Ї–µ–є–і —Г 10 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В—П–ґ–µ–ї—Л–Љ –њ–Њ–ї–Є–∞—А—В–Є–Ї—Г–ї—П—А–љ—Л–Љ –њ—Б–Њ—А–Є–∞—В–Є—З–µ—Б–Ї–Є–Љ –∞—А—В—А–Є—В–Њ–Љ (–Я–Р). –°–Њ–њ—Г—В—Б—В–≤—Г—О—Й–∞—П —В–µ—А–∞–њ–Є—П –≤–Ї–ї—О—З–∞–ї–∞ –Ь–Ґ (7 –њ–∞—Ж–Є–µ–љ—В–Њ–≤), —Б—Г–ї—М—Д–∞—Б–∞–ї–∞–Ј–Є–љ (1). –£ –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–Њ 70% —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ (–Р–Ъ–†70) —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –і–ї–Є—В–µ–ї—М–љ–Њ–є —А–µ–Љ–Є—Б—Б–Є–µ–є –≤ —В–µ—З–µ–љ–Є–µ 5 –Љ–µ—Б –љ–∞–±–ї—О–і–µ–љ–Є—П. –£ 5 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї 10-–є –љ–µ–і–µ–ї–µ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ–∞ –≤—Л—А–∞–ґ–µ–љ–љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ –Ї—А–Є—В–µ—А–Є—П–Љ –Р–Ъ–† 70. –Я—А–Є –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–Љ (–≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞) –љ–∞–±–ї—О–і–µ–љ–Є–Є —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Г 3 – —Б–Њ—Е—А–∞–љ—П–ї–∞—Б—М —А–µ–Љ–Є—Б—Б–Є—П –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –ї–µ—З–µ–љ–Є—П, –∞ —Г 5 – –µ–µ —Г–і–∞–≤–∞–ї–Њ—Б—М –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—В—М –љ–∞ —Д–Њ–љ–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –†–µ–Љ–Є–Ї–µ–є–і–∞ –≤ –і–Њ–Ј–µ 3-4 –Љ–≥/–Ї–≥ —З–µ—А–µ–Ј –Ї–∞–ґ–і—Л–µ 8-10 –љ–µ–і–µ–ї—М [30]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —А–µ–Ј—Г–ї—М—В–∞—В—Л –Њ—В–Ї—А—Л—В—Л—Е –Є—Б–њ—Л—В–∞–љ–Є–є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –†–µ–Љ–Є–Ї–µ–є–і —П–≤–ї—П–µ—В—Б—П –≤–µ—Б—М–Љ–∞ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ—Е –Њ—Б–љ–Њ–≤–љ—Л—Е —Д–Њ—А–Љ —Б–µ—А–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л—Е —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–њ–∞—В–Є–є, –Ї–∞–Ї –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В—А–Є—В–∞, —В–∞–Ї, –≤–µ—А–Њ—П—В–љ–Њ, –Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞. –С–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –і–∞–љ–љ—Л–µ –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–µ –†–µ–Љ–Є–Ї–µ–є–і–∞ —Г –љ–∞–Є–±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є [31]. –Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –і–ї—П —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ –≤–ї–Є—П–љ–Є–Є —В–µ—А–∞–њ–Є–Є –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –љ–∞ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Є –Њ—В–і–∞–ї–µ–љ–љ—Л–є –Є—Б—Е–Њ–і –±–Њ–ї–µ–Ј–љ–Є —В—А–µ–±—Г—О—В—Б—П —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–С–Њ–ї–µ–Ј–љ—М –Ъ—А–Њ–љ–∞
–Ф–∞–љ–љ—Л–µ, –Ї–∞—Б–∞—О—Й–Є–µ—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Ъ—А–Њ–љ–∞, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 5. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –†–µ–Љ–Є–Ї–µ–є–і –≤—Л–Ј—Л–≤–∞–µ—В –Њ—З–µ–љ—М –±—Л—Б—В—А–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –±–Њ–ї–µ–µ —З–µ–Љ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е –љ–∞ 4 –Є 12 –љ–µ–і–µ–ї–µ –љ–∞–±–ї—О–і–µ–љ–Є—П, –∞ —Г —В—А–µ—В–Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –і–ї–Є—В–µ–ї—М–љ–∞—П —А–µ–Љ–Є—Б—Б–Є—П. –Ш–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ —Г —В—А–µ—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Н—Д—Д–µ–Ї—В –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї –Ї–∞–Ї –љ–∞ –њ–µ—А–≤–Њ–µ, —В–∞–Ї –Є –љ–∞ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–µ –≤–≤–µ–і–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞. –Ю—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –і–∞–љ–љ—Л–µ –Њ —В–Њ–Љ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ —Г 62% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —З–∞—Б—В–Є—З–љ–Њ–µ, –∞ —Г 46% – –њ–Њ–ї–љ–Њ–µ –Ј–∞–Ї—А—Л—В–Є–µ –њ–µ—А–Є–∞–љ–∞–ї—М–љ—Л—Е —Д–Є—Б—В—Г–ї, –Ї–Њ—В–Њ—А—Л–µ —З–∞—Б—В–Њ —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л –Ї —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Я–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ —Н—Д—Д–µ–Ї—В –і–ї–Є–ї—Б—П –њ—А–Є–Љ–µ—А–љ–Њ 6-12 –љ–µ–і, –∞ –њ–Њ–≤—В–Њ—А–љ—Л–µ –≤–≤–µ–і–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П–ї–Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—В—М —А–µ–Љ–Є—Б—Б–Є—О –њ—А–Є–Љ–µ—А–љ–Њ —Г –њ–Њ–ї–Њ–≤–Є–љ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°–Њ—З–µ—В–∞–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–Ј–∞—В–Є–Њ–њ—А–Є–љ–∞ –њ–Њ–Ј–≤–Њ–ї—П–ї–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —А–µ–Љ–Є—Б—Б–Є–є. –Т —Ж–µ–ї–Њ–Љ –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Ъ—А–Њ–љ–∞, –Њ–і–љ–∞–Ї–Њ –Є—Б—В–Є–љ–љ–Њ–µ –Љ–µ—Б—В–Њ —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —В—А–µ–±—Г–µ—В –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П [35].

–Я–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ATTRACT –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –±—Л —Б–≤—П–Ј–∞—В—М —Б –і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞, –љ–∞–±–ї—О–і–∞–ї–Є—Б—М —Г 57% –±–Њ–ї—М–љ—Л—Е. –°–ї–µ–і—Г–µ—В, –Њ–і–љ–∞–Ї–Њ, –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –≤ –≥—А—Г–њ–њ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–Њ–ї—М–Ї–Њ –Ь–Ґ, –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –Є–Љ–µ–ї–Є –Љ–µ—Б—В–Њ –≤ 36% —Б–ї—Г—З–∞–µ–≤. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є –њ—А–µ—А—Л–≤–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П –±—Л–ї–Є –Њ–і—Л—И–Ї–∞, –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞ –Є –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М. –Ю—Б—В—А—Л–µ —В—А–∞–љ—Б—Д—Г–Ј–Є–Њ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤ —Ж–µ–ї–Њ–Љ –Є–Љ–µ–ї–Є –Љ–µ—Б—В–Њ —А–µ–і–Ї–Њ (19%), —З–∞—Й–µ —А–∞–Ј–≤–Є–≤–∞–ї–Є—Б—М –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–є (8%) –Є–ї–Є –≤—В–Њ—А–Њ–є (7%) –Є–љ—Д—Г–Ј–Є–є, –љ–µ—А–µ–і–Ї–Њ –±—Л–ї–Є —Б–≤—П–Ј–∞–љ—Л —Б –Њ—З–µ–љ—М –±—Л—Б—В—А—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Є –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Є –њ—А–µ—А—Л–≤–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П —В–Њ–ї—М–Ї–Њ —Г 1,9% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б–њ—Л—В–∞–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Ъ—А–Њ–љ–∞ 40 –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ–Њ–≤—В–Њ—А–љ–Њ —З–µ—А–µ–Ј 2-4 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ —Г 10 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —А–µ–∞–Ї—Ж–Є—П –Ј–∞–Љ–µ–і–ї–µ–љ–љ–Њ–є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є (–Љ–Є–∞–ї–≥–Є—П, –ї–Є—Е–Њ—А–∞–і–Ї–∞, –∞—А—В—А–∞–ї–≥–Є–Є), –Ї–Њ—В–Њ—А–∞—П –≤ 6 —Б–ї—Г—З–∞—П—Е —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М, –Ї–∞–Ї —В—П–ґ–µ–ї–∞—П. –Ю–і–љ–∞–Ї–Њ –≤ –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –≤–Ї–ї—О—З–∞–≤—И–Є—Е 771 –њ–∞—Ж–Є–µ–љ—В–∞, –Ї–Њ—В–Њ—А—Л–µ –≤ —Ж–µ–ї–Њ–Љ –њ–Њ–ї—Г—З–Є–ї–Є 4794 –њ–Њ–≤—В–Њ—А–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –њ—А–µ–њ–∞—А–∞—В–∞ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ (1-55 –љ–µ–і–µ–ї—М), —Н—В–Њ–≥–Њ –њ–Њ–±–Њ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М. –Ъ–∞–Ї —Г–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М, –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –Љ–Њ–≥—Г—В –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М—Б—П –І–Р–•–Р, —З—В–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ —А–µ–∞–Ї—Ж–Є—П–Љ. –Э–∞ —Д–Њ–љ–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –Є –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –≤ –і–Њ–Ј–∞—Е –Њ—В 1 –і–Њ 20 –Љ–≥/–Ї–≥ –І–Р–•–Р –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є—Б—М —Г 24% (47/199) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О –Є —Г 37% (33/90) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј —Н—В–Њ–є —В–µ—А–∞–њ–Є–Є. –Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–µ–ґ–µ (—Г 6 –Є–Ј 77, 8%) –І–Р–•–Р –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є—Б—М —Г –±–Њ–ї—М–љ—Л—Е –†–Р, –ї–µ—З–µ–љ–љ—Л—Е –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Ь–Ґ. –°–ї–µ–і—Г–µ—В, –Њ–і–љ–∞–Ї–Њ, –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–Є—В—А–Њ–≤ –І–Р–•–Р –љ–µ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї–Њ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –Є–ї–Є —А–∞–Ј–≤–Є—В–Є–µ–Љ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –§–Э–Ю-a –Є–≥—А–∞–µ—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ –њ—А–Њ—В–Є–≤–Њ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–Љ –Є–Љ–Љ—Г–љ–Є—В–µ—В–µ, –Њ—Б–Њ–±–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –±—Л–ї–Њ —Г–і–µ–ї–µ–љ–Њ —З–∞—Б—В–Њ—В–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т —Ж–µ–ї–Њ–Љ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –±—Л–ї–Є –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ—Л —Г 32% –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –†–µ–Љ–Є–Ї–µ–є–і, –Є —Г 22%, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ–ї–∞—Ж–µ–±–Њ. –Я—А–Є —Н—В–Њ–Љ —В—П–ґ–µ–ї—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є (–њ–љ–µ–≤–Љ–Њ–љ–Є—П) –Є–Љ–µ–ї–Є –Љ–µ—Б—В–Њ –≤ —Б—А–∞–≤–љ–Є–≤–∞–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е —Б –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —З–∞—Б—В–Њ—В–Њ–є (5%). –†–∞–Ј–≤–Є—В–Є–µ –Њ–њ–њ–Њ—А—В—Г–љ–Є—Б—В–Є—З–µ—Б–Ї–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є (–≥–Є—Б—В–Њ–њ–ї–∞–Ј–Љ–Њ–Ј, –Ї–Њ–Ї—Ж–Є–і–Є–Њ–Љ–Є–Ї–Њ–Ј, –∞—Б–њ–µ—А–≥–Є–ї–ї–µ–Ј –Є —В—Г–±–µ—А–Ї—Г–ї–µ–Ј) –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Ї—А–∞–є–љ–µ —А–µ–і–Ї–Њ. –°—В–Њ–ї—М –ґ–µ —А–µ–і–Ї–Њ –Њ–њ–Є—Б–∞–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ –ї–Є–Љ—Д–Њ–њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л—Е –Њ–њ—Г—Е–Њ–ї–µ–є, —З–∞—Б—В–Њ—В–∞ –Ї–Њ—В–Њ—А—Л—Е –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞ —Б —В–∞–Ї–Њ–≤–Њ–є –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є. –°–≤–Њ–µ–Њ–±—А–∞–Ј–љ—Л–є –њ–Њ–±–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В, –≤—Л—П–≤–ї–µ–љ–љ—Л–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ, —Б–≤—П–Ј–∞–љ —Б —Б–Є–љ—В–µ–Ј–Њ–Љ –∞–љ—В–Є–љ—Г–Ї–ї–µ–∞—А–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ –Є–ї–Є –∞–љ—В–Є—В–µ–ї –Ї –Ф–Э–Ъ –Є –Њ—З–µ–љ—М —А–µ–і–Ї–Њ – —А–∞–Ј–≤–Є—В–Є–µ–Љ –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –≤–Њ–ї—З–∞–љ–Њ—З–љ–Њ–њ–Њ–і–Њ–±–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (0,39%) [36]. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —В—А–µ—Е–ї–µ—В–љ–µ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –і–Њ–Ї–∞–Ј–∞–љ–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г —Б–Љ–µ—А—В–µ–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –Є –Њ—В–і–∞–ї–µ–љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ (–Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, —В—П–ґ–µ–ї—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є). –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ –њ–Њ—Б–ї–µ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є —Г –±–Њ–ї–µ–µ —З–µ–Љ 25000 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є “–љ–Њ–≤—Л—Е” –Є–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є —З–∞—Б—В–Њ—В—Л —А–∞–љ–µ–µ –Њ–њ–Є—Б–∞–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [37].
–Я–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П ATTRACT –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–ґ–љ–Њ –±—Л–ї–Њ –±—Л —Б–≤—П–Ј–∞—В—М —Б –і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞, –љ–∞–±–ї—О–і–∞–ї–Є—Б—М —Г 57% –±–Њ–ї—М–љ—Л—Е. –°–ї–µ–і—Г–µ—В, –Њ–і–љ–∞–Ї–Њ, –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –≤ –≥—А—Г–њ–њ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–Њ–ї—М–Ї–Њ –Ь–Ґ, –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –Є–Љ–µ–ї–Є –Љ–µ—Б—В–Њ –≤ 36% —Б–ї—Г—З–∞–µ–≤. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є –њ—А–µ—А—Л–≤–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П –±—Л–ї–Є –Њ–і—Л—И–Ї–∞, –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞ –Є –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М. –Ю—Б—В—А—Л–µ —В—А–∞–љ—Б—Д—Г–Ј–Є–Њ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤ —Ж–µ–ї–Њ–Љ –Є–Љ–µ–ї–Є –Љ–µ—Б—В–Њ —А–µ–і–Ї–Њ (19%), —З–∞—Й–µ —А–∞–Ј–≤–Є–≤–∞–ї–Є—Б—М –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–є (8%) –Є–ї–Є –≤—В–Њ—А–Њ–є (7%) –Є–љ—Д—Г–Ј–Є–є, –љ–µ—А–µ–і–Ї–Њ –±—Л–ї–Є —Б–≤—П–Ј–∞–љ—Л —Б –Њ—З–µ–љ—М –±—Л—Б—В—А—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Є –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Є –њ—А–µ—А—Л–≤–∞–љ–Є—П –ї–µ—З–µ–љ–Є—П —В–Њ–ї—М–Ї–Њ —Г 1,9% –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б–њ—Л—В–∞–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Ъ—А–Њ–љ–∞ 40 –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ–Њ–≤—В–Њ—А–љ–Њ —З–µ—А–µ–Ј 2-4 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ —Г 10 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —А–µ–∞–Ї—Ж–Є—П –Ј–∞–Љ–µ–і–ї–µ–љ–љ–Њ–є –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є (–Љ–Є–∞–ї–≥–Є—П, –ї–Є—Е–Њ—А–∞–і–Ї–∞, –∞—А—В—А–∞–ї–≥–Є–Є), –Ї–Њ—В–Њ—А–∞—П –≤ 6 —Б–ї—Г—З–∞—П—Е —А–∞—Б—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М, –Ї–∞–Ї —В—П–ґ–µ–ї–∞—П. –Ю–і–љ–∞–Ї–Њ –≤ –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –≤–Ї–ї—О—З–∞–≤—И–Є—Е 771 –њ–∞—Ж–Є–µ–љ—В–∞, –Ї–Њ—В–Њ—А—Л–µ –≤ —Ж–µ–ї–Њ–Љ –њ–Њ–ї—Г—З–Є–ї–Є 4794 –њ–Њ–≤—В–Њ—А–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –њ—А–µ–њ–∞—А–∞—В–∞ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ (1-55 –љ–µ–і–µ–ї—М), —Н—В–Њ–≥–Њ –њ–Њ–±–Њ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М. –Ъ–∞–Ї —Г–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М, –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –Љ–Њ–≥—Г—В –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М—Б—П –І–Р–•–Р, —З—В–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ —А–µ–∞–Ї—Ж–Є—П–Љ. –Э–∞ —Д–Њ–љ–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –Є –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –≤ –і–Њ–Ј–∞—Е –Њ—В 1 –і–Њ 20 –Љ–≥/–Ї–≥ –І–Р–•–Р –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є—Б—М —Г 24% (47/199) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О –Є —Г 37% (33/90) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј —Н—В–Њ–є —В–µ—А–∞–њ–Є–Є. –Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ —А–µ–ґ–µ (—Г 6 –Є–Ј 77, 8%) –І–Р–•–Р –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є—Б—М —Г –±–Њ–ї—М–љ—Л—Е –†–Р, –ї–µ—З–µ–љ–љ—Л—Е –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Ь–Ґ. –°–ї–µ–і—Г–µ—В, –Њ–і–љ–∞–Ї–Њ, –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —В–Є—В—А–Њ–≤ –І–Р–•–Р –љ–µ –Ї–Њ—А—А–µ–ї–Є—А–Њ–≤–∞–ї–Њ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –Є–ї–Є —А–∞–Ј–≤–Є—В–Є–µ–Љ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –§–Э–Ю-a –Є–≥—А–∞–µ—В –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ –њ—А–Њ—В–Є–≤–Њ–Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–Љ –Є–Љ–Љ—Г–љ–Є—В–µ—В–µ, –Њ—Б–Њ–±–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ –±—Л–ї–Њ —Г–і–µ–ї–µ–љ–Њ —З–∞—Б—В–Њ—В–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Т —Ж–µ–ї–Њ–Љ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –±—Л–ї–Є –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ—Л —Г 32% –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –†–µ–Љ–Є–Ї–µ–є–і, –Є —Г 22%, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ–ї–∞—Ж–µ–±–Њ. –Я—А–Є —Н—В–Њ–Љ —В—П–ґ–µ–ї—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є (–њ–љ–µ–≤–Љ–Њ–љ–Є—П) –Є–Љ–µ–ї–Є –Љ–µ—Б—В–Њ –≤ —Б—А–∞–≤–љ–Є–≤–∞–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е —Б –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —З–∞—Б—В–Њ—В–Њ–є (5%). –†–∞–Ј–≤–Є—В–Є–µ –Њ–њ–њ–Њ—А—В—Г–љ–Є—Б—В–Є—З–µ—Б–Ї–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є (–≥–Є—Б—В–Њ–њ–ї–∞–Ј–Љ–Њ–Ј, –Ї–Њ–Ї—Ж–Є–і–Є–Њ–Љ–Є–Ї–Њ–Ј, –∞—Б–њ–µ—А–≥–Є–ї–ї–µ–Ј –Є —В—Г–±–µ—А–Ї—Г–ї–µ–Ј) –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Ї—А–∞–є–љ–µ —А–µ–і–Ї–Њ. –°—В–Њ–ї—М –ґ–µ —А–µ–і–Ї–Њ –Њ–њ–Є—Б–∞–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ –ї–Є–Љ—Д–Њ–њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л—Е –Њ–њ—Г—Е–Њ–ї–µ–є, —З–∞—Б—В–Њ—В–∞ –Ї–Њ—В–Њ—А—Л—Е –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞ —Б —В–∞–Ї–Њ–≤–Њ–є –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є. –°–≤–Њ–µ–Њ–±—А–∞–Ј–љ—Л–є –њ–Њ–±–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В, –≤—Л—П–≤–ї–µ–љ–љ—Л–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ, —Б–≤—П–Ј–∞–љ —Б —Б–Є–љ—В–µ–Ј–Њ–Љ –∞–љ—В–Є–љ—Г–Ї–ї–µ–∞—А–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ –Є–ї–Є –∞–љ—В–Є—В–µ–ї –Ї –Ф–Э–Ъ –Є –Њ—З–µ–љ—М —А–µ–і–Ї–Њ – —А–∞–Ј–≤–Є—В–Є–µ–Љ –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –≤–Њ–ї—З–∞–љ–Њ—З–љ–Њ–њ–Њ–і–Њ–±–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (0,39%) [36]. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —В—А–µ—Е–ї–µ—В–љ–µ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –і–Њ–Ї–∞–Ј–∞–љ–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г —Б–Љ–µ—А—В–µ–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –Є –Њ—В–і–∞–ї–µ–љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ (–Ј–ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –љ–Њ–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, —В—П–ґ–µ–ї—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є). –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–∞ –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ –њ–Њ—Б–ї–µ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є —Г –±–Њ–ї–µ–µ —З–µ–Љ 25000 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є “–љ–Њ–≤—Л—Е” –Є–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є —З–∞—Б—В–Њ—В—Л —А–∞–љ–µ–µ –Њ–њ–Є—Б–∞–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [37].–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤–љ–µ–і—А–µ–љ–Є–µ –†–µ–Љ–Є–Ї–µ–є–і–∞ –Њ—В–Ї—А—Л–≤–∞–µ—В –љ–Њ–≤—Л–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –≤ –ї–µ—З–µ–љ–Є–Є –љ–∞–Є–±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л—Е —Д–Њ—А–Љ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —З–µ–ї–Њ–≤–µ–Ї–∞. –Т –±–ї–Є–ґ–∞–є—И–Є–µ –≥–Њ–і—Л –Ї—А—Г–≥ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —В–µ—А–∞–њ–Є—П –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ, –Љ–Њ–ґ–µ—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —А–∞—Б—И–Є—А–Є—В—М—Б—П. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –≤ –љ–µ–і–∞–≤–љ–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л —Г–±–µ–і–Є—В–µ–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –±–ї–Њ–Ї–∞–і—Л –§–Э–Ю-a —Г –±–Њ–ї—М–љ—Л—Е —Б –Ј–∞—Б—В–Њ–є–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О [38]. –Ю—Б–Њ–±–µ–љ–љ–Њ –±–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –њ—А–Є–≤–ї–µ–Ї–∞—О—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –†–µ–Љ–Є–Ї–µ–є–і–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Є–ї–Є “–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є” –∞–≥–µ–љ—В–∞–Љ–Є [39]. –Ґ–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і, –≤–µ—А–Њ—П—В–љ–Њ, –њ–Њ–Ј–≤–Њ–ї–Є—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—Б–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М, —Г–Љ–µ–љ—М—И–Є—В—М —А–Є—Б–Ї –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є —Б–љ–Є–Ј–Є—В—М —Б—В–Њ–Є–Љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П.
–°–њ–Є—Б–Њ–Ї –ї–Є—В–µ—А–∞—В—Г—А—Л –Т—Л –Љ–Њ–ґ–µ—В–µ –љ–∞–є—В–Є –љ–∞ —Б–∞–є—В–µ http://www.rmj.ru
–Ш–љ—Д–ї–Є–Ї—Б–Є–Љ–∞–± –
–†–µ–Љ–Є–Ї–µ–є–і (—В–Њ—А–≥–Њ–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ)
(Shering Plough)
1. Silman A.J., Hochberg M.C. Epidemilogy of rheumatic disease. Oxford: Oxford university press.,1993.
2. Autoimmune rheumatic disease. Ed. J. Morrow., L. Nelson, R. Watts, D. Isenberg. Secong Ed. 1999. Oxford University Press.
3. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Я—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–Ј–љ–µ–є. –Ь–Њ—Б–Ї–≤–∞. –Ь-–°–Є—В–Є. 1996, 345 —Б—В—А.
4. Novel therapy agents for the treatment of autoimmune disease. Ed. V. Strand, D.L. Scott, L.S. Simon.1997. Marcel Dekker, Inc. New York, 308 p.
5. Moreland L.W., Heck L.W., Koopman W.I. Biologic agents for treating rheumatoid arthritis. Arthritis Rheum., 1997;40:397-409.
6. Breedveld F. Therapeutic monoclonal antibodies. Lancet 2000;355:735-740.
7. Zhang M., Tracey K.J. Tumor necr–Њsis factor. In: Thompson A.W., er. The cytokine handbook, 3rd ed. New York. Academic press, 1998:515-548.
8. Beutler B.A. The role of tumor necrosis factor in health and disease. J. Rheumatol., 1999; 26 (Suppl. 57): 16-21.
9. Feldman M., Brennan F., Maini R.N. Role of cytokines in rheumatoid arthritis. Annu. Rev. Immunol. 1996; 14:397-440.
10. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –§–∞–Ї—В–Њ—А –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є-a - –љ–Њ–≤–∞—П –Љ–Є—И–µ–љ—М –і–ї—П –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–≥–Њ –∞—А—В—А–Є—В–∞. –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї 2000; 8 (17):718-722.
11. Camussi G., Lupia E. The future role of anti-tumor necrosis factor (TNF) products in the treatment of rheumatoid arthritis. Drugs 1998;55:613-620.
12. Markham A., Lamb H.M. Infliximab. A review of its use in the management of rheumatoid arthritis. Drug 2000;59 :1341-1359.
13. Maini R.N., Taylor P.C. Anti-cytokine therapy for rheumatoid arthritis. Annu. Rev. Med., 2000;51:207-209.
14. Urfgren A-K., Anderson U., Engstrom M., et al. Systemic anti-tumor necrosis factor alpha therapy in rheumatoid arthritis down-regulate synovial tumor necrosis factor alpha synthesis. Arthritis Rheum., 200: 11:2391-2396.
15. Kremer J.M. Combination therapy with biologic agents in rheumatoid arthritis: perils and promise. Arthritis Rheum., 1998; 41: 1548-1551.
16. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. 50 –ї–µ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В–∞ –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є. –†—Г—Б—Б–Ї–Є–є –Љ–µ–і. –ґ—Г—А–љ–∞–ї. 2000; 9: 372-376.
17. Furst D.E., Keystone E., Maini R.N., Smolen J.S. Recapulation of the round-table discussion - assessing the role of anti-tumor necrosis factor therapy in the treatment of rheumatoid arthritis. Rheumatol., 1999;38 (suppl.):50-53.
18. Maini R., St Clair E.W., Breedveld F., et al. Infliximab (chimeric anti-tumor necrosis factor alpha monoclonal antibody) versus placebo in rheumatoid arthritis patients receiving concomitant methotrexate: a randomized phase III trial. Lancet 1999;354:1932-1939.
19. Lipsky P., St Clair W., Furst D., et al. 54-week clinical and radiographic results from the ATTRACT trial: a phase III study of infliximab (–†–Х–Ь–Ш–Ъ–Х–Щ–Ф) in patients with active RA on MT. Arthritis Rheum., 1999;42(Suppl.):S401
20. Felson D.T., Anderson J.J., Boers M., et al. American College of Rheumatology preliminary definition of improvement in rheumatoid arthritis. Arthritis Rheum., 1993;36:729-740.
21. Robert-Thompson P.J., Smith M.D., Ahern M.J. Similarities in the mechanisms of action of pulse corticosteroids and anti-tumor necrosis factor alpha therapy in rheumatoid arthritis. Arthritis Rheum. 1998;41:564-565.
22. Bosch van den F., Kruithof E., Baeten D., et al. Effects of a loading dose regimen of three infusions of chimeruic monoclonal antibody to tumor necrosis factor a (infliximab) in spondyloarthropathy: an open pilot study. Ann. Rheum. Dis., 2000; 59:428-433.
23. Brandt J., Haibel H., Cornely D., et al. Succesful treatment of active ankilosing spondilitis with anti-tumor necrosis factor a monoclonal antibody infliximab. Arthritis Rheum., 2000;43:1346-1352.
24. Antony C., Dechant C., Lorenz H., et al. Successful treatment of severe psoriatic arthritis with infliximab, Arthritis Rheum., 1999;42 (Suppl.):S371.
25. Bosch van den F., Kruithof M., de Vas M., et al. Crohn`s disease with spondiloarthropathy: effect of tumor necrosis factor alpha blockade with infliximab on the articular symptoms. Arthritis Rheum., 2000;43 (supplement):S102.
26. Ellman M.H., Hanauer S., Sitran M., Cohen R. Infliximab treatment for Crohn`s arthritis. Arthritis Rheum., 2000;43 (Suppl.):S299.
27. Dechant C., Antoni C., Lorenz H-M., et al. Treatment of severe adult onset Still`s disease with infliximab. Ann. Rheum. Dis., 2000;59 (Suppl. 4):162.
28. Hengstman G., van den Hoogen F., Engelen B., et al. Anti-TNF blocksade with infliximab (–†–Х–Ь–Ш–Ъ–Х–Щ–Ф) in polymiositis and dermatomyositis. Arthritis Rheum., 2000;43 (Suppl.):S193.
29. Leirisalo-Repo M., Prognosis, course of disease, and treatment of the spondyloartropathies.Rheum. Dis. Clin North. Amer., 1998;24:737-751.
30. Dechant C., Antoni C., Wendler J., et al. One year outcome of patients with severe psoriatic arthritis treated with infliximab. Arthritis Rheum., 2000;43 (Suppl.):S102
31. Braun J., Sieper J. Anti-TNF-a: a new dimension in the pharmacotherapy of the spondyloarthropathies? Ann. Rheum. Dis., 2000;59:404-406/
32. Targan S.R., Hanauer S.B., van Deventer S.J., et al. A short-term study of chimeric monoclonal antibody cA2 to tumor necrosis factor alpha for Crohn`s disease. Crohnis disease cA2 study group. N. Engl. J. Med., 1997;337:1029-1035.
33. Present D.H., Rutgeets P., Targan S.m, et al. Infliximab for the treatment of fistula in patients with Crohn`s disease. N. Engl. J. Med., 1999;340:1398-1405.
34. Rutgeets P., D`Haens G., Targan S,., et al. Efficacy and safety of treatment with anti-tumor necrosis factor antibody (infliximab) to maintain remission in Crohn`s disease. Gastroenterology 1999;117:761-769.
35. Bell S., Kamm M.A. Antibodies to tumor necrosis factor ( as treatment for Crohn`s disease. Lancet 2000;355:858-860.
36. Charles P.J., Smeenk R.J.T., De Jong J., Feldman M., Maini R.N. Assesment of antibodies to double-stranded DNA induced in the rheumatoid arthritis patients following treatment with infliximab, a monoclonal antibody to tumor necrosis factor alpha. Arthritis Rheum., 2000; 43:2383-2390.
37. Smolen J., Schaiber T., DeWoody K., et al. Long-term follow-up of patients treated with infliximab (anti-TNF-alpha antibody) in clinical trials. Ann. Rheum. Dis., 2000; 59 (Suppl. 1):164.
38. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы., –°–∞–Љ—Б–Њ–љ–Њ–≤ –Ь.–Ѓ. –Э–Њ–≤—Л–µ –∞—Б–њ–µ–Ї—В—Л –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є: —А–Њ–ї—М —Д–∞–Ї—В–Њ—А–∞ –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є. –°–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, 2000;1 (4):139-143.
39. Feldman M., Miotla J., Paleolog E., et al. Future prospects for anti-cytokine treatment. Ann. Rheum. Dis., 2000;59 (Suppl. 1):i119-122.












