Лефлуномид – БПВП с противовоспалительной и иммуномодулирующей активностью, который специально разработан для лечения РА [5]. Напомним, что по химической структуре лефлуномид – низкомолекулярное (270 аминокислот) синтетическое производное изоксазола. В организме человека лефлуномид быстро трансформируется в активный метаболит – малононитриламид (А 77 1726 или терифлуномид), составляющий 95% препарата, присутствующего в кровяном русле [5–7].
Очень хорошее соотношение эффективность/токсичность лефлуномида при РА (а также при псориатическом артрите) доказано в серии широкомасштабных плацебо–контролируемых рандомизированных исследований [8–17], их мета–анализе [18,19] и подтверждено длительным опытом применения препарата в реальной клинической практике [20,21]. Материалы, касающиеся результатов клинических испытаний лефлуномида и тактики его применения при РА, суммированы в наших предыдущих публикациях [22,23] и обзорах других авторов [24,25]. В целом анализ полученных данных позволяет рассматривать лефлуномид, наряду с метотрексактом (МТ), в качестве препарата «первого ряда» для лечения РА, что нашло свое отражение в рекомендациях Ассоциации ревматологов России [2].
Однако поскольку монотерапия любым БПВП не всегда эффективно контролирует деструкцию суставов и редко индуцирует развитие ремиссии, важное направление фармакотерапии РА – комбинированное применение БПВП [26,27], Концепция комбинированной терапии основана на том, что БПВП могут обладать комплементарными механизмами действия, которые обеспечивают более мощное воздействие на патогенетические механизмы ревматоидного воспаления. Комбинированная терапия лефлуномидом и МТ теоретически хорошо обоснована [28] и превосходит по эффективности монотерапию МТ без существенного увеличения частоты побочных эффектов [16,17,22,29], однако не всегда соответствует современным требованиям, предъявляемым к терапии РА (недостаточное число пациентов с «хорошим» ответом по критерием EULAR или ACR50/70) и сопровождается нарастанием частоты потенциально тяжелых побочных эффектов, таких как гепатотоксичность и лейкопения.
Начало XXI века ознаменовалось внедрением в клиническую практику нового класса БПВП – так называемых генно–инженерных биологических препаратов, среди которых наиболее эффективными являются химерные мноклональные антитела к фактору некроза опухоли (ФНО) – инфликсимаб [31]. Более высокая эффективность комбинированной терапии инфликсимабом и МТ (по сравнению с монотерапией МТ) у пациентов с тяжелым РА подтверждена в серии РКИ и в процессе их мета–анализа [32].
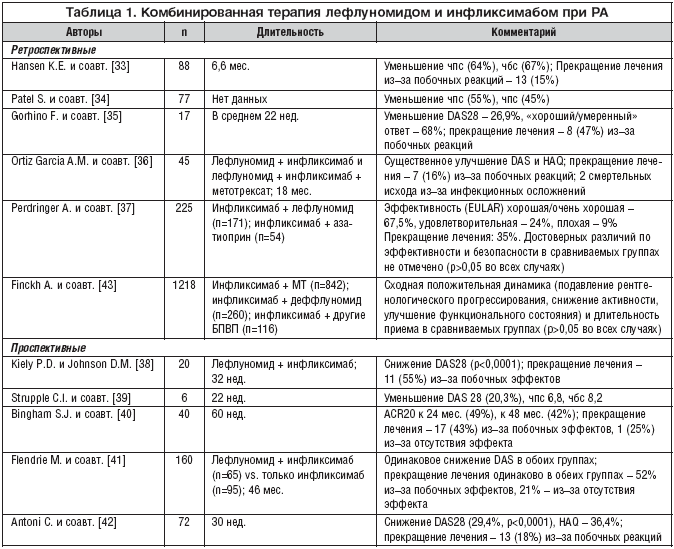
Хотя специальных плацебо–контролируемых исследований комбинированной терапии лефлуномидом и инфликсимабом до сих пор не проводилось, в настоящее время получены многочисленные результаты ретроспективных наблюдательных исследований (включая данные регистров биологических препаратов) и проспективных открытых исследований, свидетельствующих о том, что эта терапия может быть не менее эффективна, чем комбинация инфликсимаба и МТ, которая начала применяться раньше (табл. 1) [23,30].
По данным Patel S. и соавт. [34], которые наблюдали 77 пациентов (51 женщина, средний возраст 56,7 лет, длительность заболевания 9,6 лет), получавших лефлуномид (20 мг/сут.) и инфликсимаб (3 мг/кг по стандартной схеме), на фоне комбинированной терапии отмечается снижение числа болезненных (45%) и припухщих суставов (55%), улучшение функционального класса (16%), и дозы ГК (33%). Побочные эффекты включали тошноту и рвоту (6%), алопецию (2%), у 3 пациентов отмечены анафилактоидные реакции, у 2 – головные боли, усиление болей в суставах (1), диарея (1), гриппоподобная реакция (1).
В открытом многоцентровом ретроспективном исследовании Hansen K.E. и соавт. [33] наблюдали 88 пациентов, страдающих РА (63 женщины, средний возраст 53 года, длительность заболевания 10,3 лет). Предшествующая терапия МТ (91%) и сульфасалазином (49%) была прекращена из–за недостаточной эффективности и/или развития побочных эффектов. Комбинированная терапия лефлуномидом и инфликсимабом проводилась в среднем в течение 6,6 мес. (581 пациент–месяц). Средняя доза лефлуномида составила 17, 8 мг/сут., среднее число инфузий инфликсимаба – 4,8, а среднее доза – 3.3 мг/кг. У подавляющего большинства пациентов лечение инфликсимабом было начало после назначения лефлуномида. На фоне комбинированной терапии отмечено снижение числа припухших (64%) и болезненных (67%) суставов, приема глюкокортикоидов (ГК) на 41%, уменьшение концентрации С–реактивного белка (СРБ) на 45% и СОЭ на 39%. У 34% пациентов развились побочные реакции, в том числе у 6 – тяжелые. У 10 пациентов отмечены инфекционные осложнения: 9 эпизодов завершились полным выздоровлением, 1 – смертельным исходом от бактериальной пневмонии. Прием лефлуномида и инфликсимаба был прекращен у 4 пациентов из–за развития кожной сыпи, рака легких (пациент был тяжелым курильщиком), пневмонии в сочетании с дистресс–синдромом (1) и рака кишечника и целлюлита (1). Лефлуномид был отменен в 3–х случаях (отсутствие эффекта – 1, кожная сыпь – 1), а инфликсимаб – у 6 (отсутствие эффекта – 4, сыпь – 1, артралгии – 1). У 7 пациентов имело место временное прерывание лечения лефлуномидом (диарея – 3, кожная сыпь – 1, кожный зуд – 1, опоясывающий лишай – 1). Инфузионные реакции развились у 3 пациентов (0,7% всех инфузий).
Godinho F. и соавт. [35] проанализировали результаты лечения 17 пациентов (7 женщин, средний возраст 56,7 лет) с активным РА и неэффективностью БПВП, 13 из которых до назначения инфликсимаба в течение не менее 3 мес. получали лефлуномид, а у 4 – оба препарата были назначены одновременно. На фоне лечения отмечалось уменьшение активности заболевания (снижение DAS c 5,94±0,88 до 4,34±1,25 ед.), у 65% имел место хороший/умеренный ответ по критериям EULAR. В целом побочные эффекты были отмечены у 13 пациентов, причем у 8 – послужили основанием для прерывания лечения (сердечная декомпенсация – 1, гипертонический криз – 2, экзематозное поражение кожи – 2, нейтропения – 3).
Ortiz Garcia A.M. и соавт. [36] оценили результаты комбинированной терапии лефлуномидом и инфликсимабом у 45 пациентов (женщины 78%, средний возраст 57±14 лет, продолжительность болезни 141±123 мес.), с неэффективностью предшествующей терапии БПВП (в среднем 3,2±1,6 препарата). Отмечена достоверная положительная динамика стандартных показателей активности РА (индексов DAS и HAQ). В целом у пациентов отмечено 64 эпизода побочных реакций у 29 пациентов (64,4%), причем в 7 случаях это привело к прерыванию лечения. У 16 пациентов имели место 23 эпизода инфекционных осложнений.
Perdringer А. и соавт [37] провели ретроспективный анализ 225 пациентов (средний возраст 56±12,4 лет, продолжительность болезни 13,4±8,1 лет), страдающих РА. 203 (90,2%) пациента в прошлом получали МТ, который был отменен из–за неэффективности – у 33,2% и из–за побочных эффектов – у 66,8%. 171 пациент получал комбинированную терапию инфликсимабом и лефлуномидом (средняя доза 20±2,7 мг/сут.), а 75 пациентов – инфликсимабом и азатиоприном. У 144 пациентов (84,2%) лечение лефлуномидом начинали до назначения инфликсимаба, в остальных случаях одновременно с инфликсимабом. Средняя доза инфликсимаба составила 3,09±0,38 мг/кг, а средняя длительность комбинированной терапии была 8,8±6 мес. (164,6 пациента–год). В целом по группе очень хороший эффект по критериям EULAR отмечен у 29,7%, хороший – у 38,8%, удовлетворительный – у 11,6% и неудовлетворительный у 8,6%. У 41,7% переносимость терапии расценивалась как очень хорошая, у 35,6% – хорошая, у 11,6% – удовлетворительная, плохая – только у 11,1%. Достоверных различий по эффективности и переносимости в сравниваемых группах не отмечено. Частота побочных эффектов у пациентов, получавших различные варианты комбинированной терапии, также была примерно одинаковой – соответственно 35% (48/100 пациентов–год) и 27% (37/100 пациентов–год). Примечательно, что побочные эффекты чаше имели место у пациентов, которым лефлуномид назначали на фоне лечения (или одновременно) с инфликсимабом, чем до начала лечения инфликсимабом (51,8: vs 32%, p=0,047). В целом в обеих группах лечение было прекращено у 161 пациента (71,5%), у 53 (23,5%) из–за побочных эффектов, в 10 случаях (4%) из–за неэффективности, причем различия по частоте прерывания лечения в сравниваемых группах также не наблюдалось. Основной причиной отмены лефлуномида и азатиоприна была гепатотоксичность, а инфликсимаба – инфекционные осложнения (4,4%) и инфузионные реакции (4,8%)
Проспективные исследования комбинированной терапии лефлуномидом и инфликсимабом немногочисленны и включают относительно небольшое число пациентов. В исследование Kiely PD и Johnson DM [38] было включено 20 пациентов с активным РА (средняя продолжительность болезни 10 лет), с множественной неэффективностью БПВП (в среднем 4 препарата). Лефлуномид назначали по стандартной схеме, включающей насыщающую дозу (100 мг в сутки – 3 дня), а затем поддерживающую дозу (20 мг/сут.). Общая продолжительность исследования составила 32 недели. На второй неделе все пациенты начали получать инфликсимаб (всего 5 инфузий в дозе 3 мг/кг). Побочные эффекты имели место у всех пациентов, наиболее часто кожные реакции (79%). У 11 пациентов лечение было прекращено до окончания исследования из–за побочных эффектов, в том числе кожных реакций – 5, инфузионных реакций – 3, синдрома Стивенса–Джонсона – 1, диареи – 1, меланомы (имела место до начала терапии) – 1. В то же время эффективность комбинированной терапии была достаточно высока. Уже к 4 нед. среднее значение индекса DAS28 снизилось с 7,18 до 5,18 ед. (p<0,0001), а к 8–32 нед до 3,85–4,85 ед. (p<0,001), у 46% имело место 70%–е улучшение по критерию ACR. Следует особо подчеркнуть, что в этом исследовании (в отличие от подавляющего большинства других работ) лефлуномид и инфликсимаб назначались одновременно.
Struppler C.I. и соавт. [39] включили в исследование 6 женщин с длительно текущим РА с недостаточной эффективностью МТ, которые в течение 22 недель получали комбинированную терапию лефлуномидом (20 мг/сут.) и инфликсимабом (3 мг/кг по стандартной схеме). На фоне лечения отмечено снижение числа болезненных суставов ( с 6,4 до 5,1), DAS28 (c 6,4 до 5,1 ед.), СОЭ (с 48 мм/ч до 40 мм/ч), концентрации СРБ (с 3,9 мг% до 2,8 мг%), показателя обшей оценки состояния здоровья, по мнению врача (с 68 мм до 40 мм), и пациента (с 76 мм до 62 мм). В целом переносимость терапии была очень хорошей, побочных эффектов, потребовавших прерывания лечения не отмечено.
Результаты проспективного исследования Bingham S.J. и соавт. [40] обращают внимание на потенциальную возможность развития иммуноопосредованных побочных реакций на фоне комбинированной терапии лефлуномидом и инфликсимабом. Авторы провели открытое проспективное исследование эффективности и безопасности комбинированной терапии этими препаратами у 40 пациентов с РА, которые не отвечали на монотерапию лефлуномидом (отсутствие эффекта, по крайней мере, в течение 3 мес.). Эффективность терапии к 24 нед. по критериям ACR20 составила 49%, а к 48 нед. – 42%. В этом исследование особое внимание обращено на очень высокую частоту прерывания лечения, связанную как с неэффективностью (25%), так и с развитием побочных эффектов (42,5%). Среди них особенно часто встречались иммуноопосредованные реакции, включая васкулит (3), инфузионные реакции (2), волчаночноподобное заболевание (2), церебральный васкулит (1), синдром Стивенса–Джонсона (1).
Fleindrie M. и соавт. [41] провели анализ большой группы пациентов (n=162), получавших инфликсимаб, которые не отвечали на лечение МТ и, по крайней мере, еще на один БПВП и имели высокую активность (среднее значение индекса DAS28 – 5,8 ед.). Пациенты были разделены на 2 группы: получавшие лефлуномид на фоне лечения инфликсимабом (или, как минимум, в течение 6 мес. до начала терапии инфликсимабом) (n=57) и впервые начавшие лечение лефлуномидом (n=105). Кроме того, специально была проанализирована подгруппа пациентов, которым инфликсимаб назначили на фоне активной терапии лефлуномидом (n=33). Продолжительность наблюдения составила в среднем 46 недель. На фоне комбинированной терапии лефлуномидом и инфликсимабом отмечено снижение активности заболевания (хороший эффект по критериям EULAR – 14–44% в различные периоды лечения). При этом каких–либо достоверных отличий в сравниваемых группах как в отношении эффективности, стойкости эффекта и частоты побочных эффектов выявлено не было. Частота и причины прерывания лечения также не различались и были связаны с неэффективностью (21%), развитием побочных эффектов (52%) или и тем и другим (19%).
Antoni С. и соавт. [42] проследили в динамике 72 пациента с активным РА, которым инфликсимаб (3 мг/кг по стандартной схеме) был назначен на фоне неэффективной монотерапии (по крайней мере, 16 нед.) лефлуномидом (20 мг/сут.). Клиническое улучшение отмечено уже на второй неделе терапии, а к 30–й неделе отмечено достоверное снижение индекса DAS c 6,8 до 4,8 ед. (p<0,0001). В целом «хороший» ответ по критериям EULAR имел место у 19,4%, а «удовлетворительный», у 43,6% пациентов. Среднее значение индекса HAQ снизилось с 1,65 до 1,21 (p<0,0001), наблюдалось достоверное улучшение общего состояния пациентов, как, по мнению врача (–34,8 мм, p<0,0001), так и пациента (–31,1 мм: p<0,0001).
Особый интерес представляет исследование Finckh A. и соавт. [43], которые проанализировали большую группу пациентов с РА, получавших инфликсимаб и другие БПВП в период с 1996 по 2006 гг. (база данных Swiss Clinical Quality Management in Rheumatoid Arthritis). Всего было проанализировано 1218 пациентов (из 2097, включенных в базу данных), среди которых 842 получали ингибиторы ФНО в сочетании с МТ, 260 – в сочетании с лефлуномидом и 116 – с другими БПВП. Установлено, что достоверных различий между сравниваемыми группами пациентов как в отношении длительности лечения (рис. 1), эффективности (клинической и рентгенологической) (рис. 2–4), так и частоты побочных эффектов не выявлено.
В целом анализ материалов, касающихся комбинированной терапии лефлуномидом и инфликсимабом, позволил сделать следующие выводы и рекомендации [30]:
• Комбинированная терапия лефлуномидом и инфликсимабом весьма эффективна, хорошо переносится и может быть рекомендована пациентам, не отвечающим на монотерапию лефлуномидом (и другими БПВП) или при быстром прогрессировании деструкции суставов.
• Учитывая, что при проведении комбинированной терапии возможно увеличение частоты побочных эффектов, целесообразно проводить более тщательный мониторинг побочных реакций. К факторам риска побочных эффектов относятся плохая переносимость терапии БПВП в анамнезе, высокое значение индекса HAQ, наличие внесуставных проявлений и сопутствующих заболеваний
• Принимая во внимание отсутствие РКИ по комбинированной терапии лефлуномидом и инфликсимабом, перед назначением терапии пациенты должны быть детально проинформированы об ее достоинствах и недостатках.
• Рекомендации по проведению комбинированной терапии лефлуномидом и ингибиторами ФНО:
– не использовать насыщающую (100 мг/сут. в течение 3–х дней) дозу лефлуномида;
– не назначать лефлуномид и ФНО одномоментно, а начинать лечение одним препаратом на фоне терапии другим;
– при низком риске побочных эффектов использовать лефлуномид в дозе 20 мг/сут.;
– при риске развития побочных эффектов или при назначении лефлуномида на фоне терапии ингибиторами ФНО начинать лечение с дозы 10 мг/сут. с последующим увеличением дозы (в течение 2–3 мес.) до 20 мг/сут.
В заключение необходимо подчеркнуть, что комбинированная терапия лефлуномидом и инфликсимабом потенциально может улучшить прогноз у пациентов с тяжелым РА. Необходимо проведение дальнейших исследований, в том числе в рамках Российского регистра генно–инженерных биологических препаратов.


Литература
1. Gabriel SE. The epidemiology of rheumatoid arthritis. Rheum Dis Clin North Аmer 2001;27: 269–281
2. Сигидин Я.А., Лукина Г.В. Ревматоидный артрит. Москва, «АНКО», 2001, 328 стр
3. Лечение ревматоидного артрита. Клинические рекомендации. /Под ред. Насонова Е.Л. – Москва: Издательство «Алмаз», 2006. – 118 стр.
4. Насонов Е.Л. Фармакотерапия ревматоидного артрита – взгляд в 21 век. //Клин. медицина, 2005; 6: 8–12
5. Решетняк Д.В., Насонов Е.Л. Новые направления лечения ревматоидного артрита: механизмы действия и клиническая эффективность лефлюномида. Научно–практическая ревматология 2001; 5:39–45
6. Fox RI, Herrmann ML, Frangou CG, et al. Mechanism of action for leflunomide in rheumatoid arthritis. Clin Immunol 1999; 93: 198–208.
7. Breedveld FC, Dayer J–M. Leflunomide: mode of action in the treatment of rheumatoid arthritis. Ann Rheum Dis 2000; 59: 841–9.
8. Cohen S, Cannon G, Schiff M, et al. Two–year, blinded, randomized, controlled trial of treatment of active rheumatoid arthritis with leflunomide compared with methotrexate. Utilisation of leflunomide in the treatment of Rheumatoid Arthritis Investigator Group. Arthritis Rheum 2001; 44: 44: 1984–1992.
9. Strand V, Cohen S, Schiff M, Weaver A, Fleischmann R, Cannon G, et al. Treatment of active rheumatoid arthritis with leflunomide compared to placebo and methotrexate. Arch. Intern. Med. 1999; 159: 2542–50.
10. Kalden JR, Scott DL, Smolen JS, et al. Improved functional ability in patients with rheumatoid arthritis – long–term treatment with leflunomide versus sulfasalazine. European Leflunomide Study Group. J Rheumatol 2001; 28: 1983–1991.
11. Еmery P, Breedveld FC, Lemmel EM, Kaltwasser JP, Dawes PT, Gomor B, et al. A comparison of the efficacy and safety of leflunomide and methotrexate for the treatment of rheumatoid arthritis. Rheumatology 2000; 39: 655–65.
12. Smolen JS, Kalden JR, Scott DL, Rozman B, Kvien TK, Loew–Friedrich I, et al. Efficacy and safety of leflunomide compared with placebo and sulphasalazine in active rheumatoid arthritis: a double–blind, randomised, multi–centre trial. Lancet 1999;353:259–66
13. Scott DL, Smolen JS, Kalden JR, et al. Treatment of active rheumatoid arthritis with leflunomide, two year follow up of a double–blind, placebo controlled trial versus sulfasalasine. Ann Rheum Dis 2001; 60: 913–923.
14. Smolen JS, Emery P, Kalden JR et al. The efficacy of leflunomide monotherapy in rheumatoid arthritis: towards the goals of disease modifying antirheumatic drug therapy. J Rheumatol 2004; 31: Suppl. 7: 13020.
15. Kalden JR, Schattenkirchner M, Sorensen H et al. The efficacy and safety of leflunomide in patients with active rheumatoid arthritis: a five–year followup study. Arthritis Rheum 2003; 48:1513–20.
16. Kremer I, Genovese M, Cannon G, et al. Concominant leflunomide therapy in patients with active rheumatoid arthritis despite stable doses of metotrexate, A randomized, double–blind, placebo–controlled trial. Ann Intern Med 2002; 137: 726–733.
17. Kremer JM, Genovese MC, Cannon GM, et al. Combination leflunomide and methotrexatr (MTX) therapy for patients with active rheumatoid arthritis failinf MTX monotherapy; open–label exyension of a randomized, double–blind, placebo controlled trial. J Rheumatol 2004; 31: 1521–1531.
18. Osiri M, Shea B, Robinson V, et al. Leflunomide for the treatment of rheumatoid arthritis: a systemic review and metaanalysis. J Rheumatol 2003; 30: 1183–1190.
19. Donahue KE, Gartlehner G, Jonas DE, et al. Systemic review: comparative effectiveness and harm of disease–modifying medications for rheumatoid arthritis. Ann Rheum Dis 2008; 148: 124–134.
20. Балабанова Р.М., Маколкин В.И., Шостак Н.А., Чичасова Н.В. и др. Динамика показателей воспалительной активности у больных ревматоидным артритом на ранних этапах базисной терапии лефлюномидом. Терапевт архив 2004; 5: 28–32.
21. Чичасова НВ, Бродецкая КА, Иголкина ЕВ, Иммаметдинова ГР, Насонов ЕЛ. Опыт применения лефлуномида (препарата Арава) у больных активным ревматоидным артритом. РМЖ 2005; 13 (8); 518–524
22. Насонов ЕЛ, Чичасова НВ, Чижова КА. Перспективы применения лефлуномида в ревматологии. РМЖ 2004; 20: 1147–1151
23. Насонов ЕЛ, Каратеев ДЕ,. Чичасова НВ. Новые возможности применения лефлуномида при ревматоидном артрите – ранняя и комбинированная терапия. РМЖ, 2005; 13 (24): 1573–1576
24. Maddison P, Kiely P, Kirkham B, et al. Leflunomide in rheumatoid arthritis: recommendations through a process of consensus. Rheumatology 2005; 44: 280–286
25. Kremer JM, Cannon GW. Benefit/risk of leflunomide in rheumatoid arthritis. Clin Exp Rheumatol 2004; 22 (Suppl. 35): S95–S100
26. Dale J, Alcorn N, Cappel H, Madhol R. Combination therapy for rheumatoid arthritis: methotrexate and sulfasalazine together or with other DMARDs. Nat Clin Pract Rheumatol 2007; 3: 450–
27. Machold KP, Nell VPK, Stamm TA, Smolen JS. Traditional DMARD therapy: is it sufficient? Arthritis Res Therapy 2006; 8:21ArtTHER
28. Kremer JM. Methotrexate and leflunomide; Biochemical basis for combination therapy in the treatment of rheumatoid arthritis. Semin Arthritis Rheum 1999; 29: 14–26.
29. Kalden JR, Smolen JS, Emery P, et al. Leflunomide in combination therapy. J Rheumatol 2004; 31 (Suppl): 25–30
30. Kalden JR, Antoni C, Alvaro–Gracia JM, et al. Use of combination of leflunomide with biological agents in treatment of rheumatoid arthritis. J Rheumatol 2005; 32: 1620–1631
31. Насонов Е.Л. Применение инфликсимаба (моноклональные антитела к фактору некроза опухоли) в ревматологии: новые данные. РМЖ 2004; 20: 1123–1127
32. Chen Y–F, Jobanputra P, Barton P, et al. A systemic review of the effectiveness of adalimumab, etanercept and infliximab for the treatment of rheumatoid arthritis in adults and an economic evaluation of their cost–effectiveness. Health Technol Asses 2006; 10; p1–172
33. Hansen KE, Cush J, Singhal A, et al. The safety and efficacy of leflunomide in combination with infliximab in rheumatoid arthritis. Arthritis Rheum 2004; 51: 228–232.
34. Patel S, Bergen W, Kraemer A, Keenan GF. Efficacy and safety of remicade (infliximab) plus arava (leflunomide) in rheumatoid arthritis (RA) [abstract]. Arthritis Rheum 2001; 44 Suppl: S84.
35. Godinho F, Godfrin B, El Mahou S, Navaux F, Zabraniecki L, Cantagrel A. Safety of leflunomide plus infliximab combination therapy in rheumatoid arthritis. Clin Exp Rheumatol 2004; 22:328–30.
36. Ortiz Garcia AM, Gonzalez–Alvaro I, Rosello Pardo R, Carmona L, Fabregas Canales MD, Monteagudo Saez I. Infliximab and leflunomide study group. Effectivines and safety in infliximab combined with leflunomide in chronic polyarthritis.. Clin Exp. Rheumatol. 2004; 22: 790
37. Perdringer A, Mariette X, Kunitz J–L, et al. Safety of infliximab used in combination with leflunomide or azathyoprine in daily clinical practice. J Rheumatol 2006; 33: 865–869.
38. Kiely PD, Johnson DM. Infliximab and leflunomide combination therapy in rheumatoid arthritis: an open–label study. Rheumatology Oxford 2002; 41:631–7.
39. Struppler CI, Thies W, Schattenkirchner M, Kellner H. Safety and efficacy of leflunomide and infliximab in rheumatoid arthritis (RA) patients [abstract]. Ann Rheum Dis 2002; 61:S388.
40. Bingham SJ, Buch MH, Kerr MA, et al. Induction of antinuclear antibodies in patients with rheumatoid arthritis treated with infliximab and leflunomide. Arthritis Rheum 2004; 50: 4072–4073.
41. Flendrie M, Creemers MC, Welsing PM, van Riel PL. The influence of previous and concomitant leflunomide on the efficacy and safety of infliximab therapy in patients with rheumatoid arthritis; a longitudinal observational study. Rheumatology Oxford 2005; 44:472–8.
42. Antoni C, Manger B. Treatment of psoriatic arthritis with TNF alpha–antagonists. Z Rheumatol 2003; 62:235–9.
43. Finckh A, Dehler S, Gabay C et al. The effectiveness of leflunomide as co–therapy of TNF inhibitors in rheumatpid arthritis. A population based study. Ann Rheum Dis 2008;January 29 on line.












