Среди болевых синдромов боли в спине занимают лидирующее положение как по локализации, так и по количеству дней нетрудоспособности среди работающего населения. 58–84% взрослой популяции испытывали когда–либо боль в пояснице, среди них 13,8% – длительность болей не менее двух недель в течение последних 6 месяцев, 17% страдают хроническими болями, 11% – испытывают социальную дезадаптацию из–за болевого синдрома [9,17]. В связи с тем, что пик заболеваемости приходится на трудоспособный возраст, проблема болей в пояснице имеет и экономическую значимость. Экономический ущерб присутствия болевого синдрома включает в себя не только прямые потери в виде непосредственных затрат на оказание медицинской помощи и социальные выплаты (в связи с временной или постоянной потерей трудоспособности), но и непрямые – в виде ущерба от непроизведенной работы и снижения работоспособности [4,11].
Известно, что выраженность остеохондроза позвоночника не коррелирует с клинической картиной, поэтому его наличие не должно определять ни лечебной, ни экспертной тактики. Дегенеративно–дистрофические поражения позвоночника встречаются в различных вариантах: деформирующий спондилез, спондилоартроз, остеохондроз диска, фиброз диска, остеопороз позвоночника, включая гормональную спондилопатию, и их сочетание. Каждый из этих видов патологии составляющих позвоночника имеет свои особенности в патогенезе поражения нервной системы. Главными патогенетическими факторами являются: компрессионные механизмы и рефлекторные влияния, сопровождающиеся воспалительным процессом, микроциркуляторными расстройствами и их сочетанием. Совокупность этих процессов с клинической точки зрения можно представить как синдромы компрессионного поражения пояснично–крестцовых корешков и рефлекторные: миофасциальные, мышечно–тонические, поражение связочного и суставного аппарата позвоночника [2,10]. Наиболее часто в клинической практике встречаются рефлекторные болевые синдромы (около 85% больных с болями в спине) [12]. Особенность болевых синдромов поясничного отдела позвоночника – сочетание рефлекторных мышечно–тонических и миофасциальных синдромов с изменениями в эмоциональной сфере, способствующими хронизации состояния. Наряду с другими причинами в части случаев именно этот фактор создает основные интригующие моменты патогенеза поясничных болей: отсутствие корреляции между выраженностью дегенеративных изменений и болевого синдрома; отсутствие корреляции болевого синдрома с размером и локализацией межпозвоночной грыжи; рецидивирующее течение при сохранности патологических изменений анатомических структур.
Ноцицептивная афферентация может исходить из поврежденного фиброзного кольца, мышц, суставов, связок и нервных корешков, в результате чего происходит выброс альгогеных соединений (ионы водорода и калия, серотонин, гистамин, простагландины, брадикинин, субстанция Р) в межклеточную жидкость, окружающую ноцицепторы. Эти вещества играют ключевую роль в формировании боли, обусловленной повреждением, ишемией и воспалением. Кроме прямого возбуждающего действия на мембраны ноцицепторов, имеется непрямой механизм, связанный с нарушением локальной микроциркуляции. Повышенная проницаемость капилляров способствует экстравазации таких активных веществ, как кинины плазмы и серотонин. Это, в свою очередь, нарушает физиологическую и химическую среду вокруг ноцицепторов и усиливает их возбуждение. Продолжающийся выброс медиаторов воспаления может вызывать длительную импульсацию с развитием сенситизации ноцицептивных нейронов и формированием «вторичной гипералгезии» поврежденной ткани, способствующей хронизации патологического процесса [12]. Поэтому, исходя из общих принципов терапии болевых синдромов, в первую очередь воздействие оказывается на источник боли, рецепторы и периферические волокна, а затем на задние рога спинного мозга, проводящие системы боли, мотивационно–аффективную сферу и регуляцию поведения.
Анальгетиками первого ряда для лечения люмбоишиалгий наряду с опиоидами являются нестероидные противовоспалительные препараты (НПВП). К анальгетикам второго ряда относят: антидепрессанты, антиконвульсанты, миорелаксанты, блокаторы Са2+–каналов и др.
Механизм действия НПВП состоит в ингибировании циклооксигеназы (ЦОГ) – ключевого фермента в каскаде метаболизма арахидоновой кислоты, которая является предшественником простагландинов (ПГ), простациклинов и тромбоксанов [15]. В настоящее время выделены два изофермента ЦОГ. ЦОГ–1 является структурным ферментом, постоянно присутствующим в большинстве тканей и участвующим в регуляции множества физиологических процессов [3,8]. ЦОГ–2 в норме в большинстве тканей не присутствует, ее экспрессия увеличивается на фоне воспаления, приводя к повышению уровня провоспалительных субстанций (простагландины групп F и I) [5]. Именно ингибирование ЦОГ–2 рассматривается, как один из важнейших механизмов противовоспалительной, анальгетической активности, а ингибирование ЦОГ–1 – как механизм развития большинства побочных эффектов [8].
НПВП относятся к числу наиболее часто применяемых в практической медицине лекарственных препаратов. Известно также, что препараты этой группы регулярно используют в своей работе более 80% врачей различных специальностей [19]. НПВП представляют собой гетерогенную группу, в которую входит не менее ста веществ, относящихся к нескольким основным химическим группам (производные салициловой, индоловой, пропионовой, гетероарилуксусной, энолиоковой кислот). К сожалению, «химическая» классификация мало что дает для прогнозирования как клинической эффективности, так и выраженности различных побочных эффектов препаратов. Непрекращающиеся исследования в области синтеза новых нестероидных противовоспалительных препаратов связаны именно с неудовлетворенностью критерием отношения «риск/польза» при их использовании. Так, за последнее десятилетие 18 препаратов из этой группы были изъяты из обращения или сняты с клинических испытаний из–за неприемлемых осложнений при их использовании [1]. Однако даже разрешенные к применению препараты способны вызывать побочные эффекты уже при кратковременном приеме в небольших дозах. В целом количество пациентов, у которых отмечаются побочные эффекты, достигает 25%, в то время как у 5% пациентов могут развиться опасные для жизни осложнения [8]. Закономерность их появления обусловлена механизмом действия НПВП.
Гастроэнтерологические побочные эффекты НПВП условно подразделяются на несколько основных категорий: симптоматические (такие как тошнота, рвота, диарея или запоры, боли в животе, изжога); НПВП–гастропатии (эрозии и язвы желудка или двенадцатиперстной кишки, в том числе перфоративные и сопровождающиеся кровотечениями); поражения кишечника. В то время как побочные эффекты наблюдаются в среднем у 30–40% больных и зачастую служат причиной отказа от дальнейшего лечения, их частота слабо коррелирует с более тяжелыми осложнениями [8]. По частоте развития этих побочных эффектов все неселективные НПВП стоят приблизительно на одном уровне за исключением таких препаратов, как индометацин, пироксикам, которые обусловливают значительно большее число тяжелых осложнений такого рода [1]. Факторами риска развития патологии со стороны ЖКТ на фоне приема НПВП являются: возраст старше 65 лет; патология ЖКТ в анамнезе; сопутствующие заболевания в виде застойной сердечной недостаточности, артериальной гипертензии, печеночной недостаточности; прием диуретиков, ингибиторов АПФ и антикоагулянтов; высокие дозы или одновременный прием нескольких НПВП (кроме низких доз ацетилсалициловой кислоты), глюкокортикоидов, НПВП с длительным периодом полувыведения и неселективных в отношении изоформ ЦОГ.
Боли, обусловленные воспалительным процессом, давно привлекают к себе самое серьезное внимание, и в настоящее время эти механизмы все активнее изучаются. Показано, что любая периферическая боль связана с повышением чувствительности ноцицепторов, создающих импульсацию, распознаваемую как боль. Повышение чувствительности первичного ноцицептора в пораженной периферической ткани приводит к повышению активности нейронов, посылающих импульсацию в спинной мозг и ЦНС. Однако необходимо подчеркнуть, что в очаге воспаления может генерироваться спонтанная электрическая активность, обусловливающая стойкий болевой синдром. Таким мощным индуктором болевой чувствительности являются провоспалительные компоненты: брадикины, гистамин, нейрокинины, оксид азота, которые обычно обнаруживаются в очаге воспаления. Простагландины сами по себе не являются модераторами боли, они лишь повышают чувствительность ноцицепторов к различным стимулам, а их накопление коррелирует с развитием интенсивности воспаления и гипералгезией. Простагландины как бы опосредуют вовлечение «спящих» ноцицепторов в процесс формирования вторичной воспалительной гипералгезии и периферической сенситизации. С тех пор как было установлено значение индуцибельной циклооксигеназы–2 (ЦОГ–2) в каскаде превращения арахидоновой кислоты в провоспалительпые простагландины, интерес к роли ЦОГ–2 в развитии болевого стимула и снижении боли при подавлении ЦОГ–2 существенно возрос. Специальные исследования показали, что активность ЦОГ–2 в развитии гипералгезий, действительно, играет большую роль. Это касается гиперпродукции этого фермента в очаге воспаления и его депрессии в спинном мозге при гипералгезии. Показано, что ЦОГ–2 mРНК может индуцироваться и спинном мозге после развития периферического воспаления, а селективные ингибиторы ЦОГ–2, непосредственно воздействующие на поясничный отдел спинного мозга, прекращают воспалительную гипералгезию. При воспалительной реакции на периферии в спинномозговой жидкости повышается уровень простагландинов, которые проявляют чрезвычайную чувствительность к ингибиции ЦОГ–2. Исследования последних лет продемонстрировали, что ЦОГ–2 является естественным (конститутивным) ферментом, экспрессируемым в ЦНС, поэтому участие ЦОГ–2 в развитии боли приобретает большое практическое значение [7,20].
На сегодняшний день наиболее известными селективными ЦОГ–2 ингибиторами являются: мелоксикам (Мовалис), целекоксиб и рофекоксиб. В инъекционной форме пока существует только мелоксикам. Результаты клинического применения этой формы свидетельствуют о достаточно низкой частоте развития побочных гастроэнтерологических осложнений [18] и достаточной эффективности в лечении люмбоишиалгического синдрома [14,16].
В данном сообщении представлены предварительные результаты применения мелоксикама в инъекционнной форме при лечении обострения люмбоишиалгического синдрома. Под наблюдением находилось 20 пациентов, средний возраст – 45,83±13,86 лет. В половине случаев клинически определялись симптомы радикулопатии, в остальных доминировали миофасциальные и мышечнотонические расстройства. Структура исследования состояла из оценки исходного состояния пациента по показателям 10–балльной шкалы в категориях: спонтанная боль; боль при движении; степень ограничения двигательной функции. Оценка тех же показателей через 1 час после 1–й и 3–й инъекции препарата (15 мг). Оральное применение препарата (15 мг) в течение 2 недель с оценкой тех же показателей в конце 1–й и 2–й недели.
Результаты исследования (рис. 1 и 2) показали достаточную эффективность инъекционной формы мелоксикама, закрепляемую последующим двухнедельным оральным применением препарата. При этом ни в одном случае побочных эффектов при применении препарата выявлено не было.
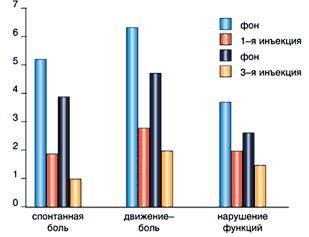
Рис. 1. Динамика болевого синдрома под влиянием инъекций мелоксикама
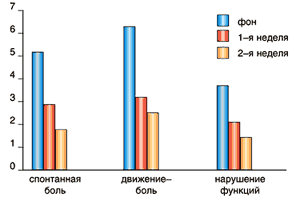
Рис. 2. Динамика болевого синдрома в процессе курсового лечения мелоксикамом
Несомненно, эффективность терапии повышается при сочетанном применении инъекционного мелоксикама со средствами, уменьшающими спазм мышц: постизометрической релаксацией, массажем, миорелаксантами, блокадами триггерных зон с местными анестетиками (новокаином), при которых отмечается повышение устойчивости клеточной мембраны к деполяризующему действию ионов калия, ограничивается повышенная ионная проницаемость. Блокады с новокаином ослабляют отек, а также снижают возбудимость мышц, что способствует изменению их биоколлоидного состояния [10].Таким образом, учитывая, что ЦОГ–2 играет огромную роль в индукции боли как в очаге воспаления, так и при ее передаче в спинной мозг, подавление воспалительной боли должно осуществляться в первую очередь НПВП, в частности, таким специфическим ингибитором ЦОГ–2, как мелоксикам (Мовалис), который оказался эффективным и безопасным препаратом для применения в комплексной терапии болей в спине, обусловленных мышечно–тоническим, миофасциальным синдромом или компрессионой радикулопатией.
1. Астахова А.В. Нестероидные противовоспалительные средства (НПВС): спектр побочных реакций // Безопасность лекарств. – 2000. – Бюллетень №1. – С.26–30.
2. Богачева Л.А., Снеткова Е.П. Дорсалгии: классификация, механизмы патогенеза, принципы ведения (опыт работы специализированного отделения боли) // Неврологический журнал. – 1996. – №2. – С. 8–12.
3. Златкина А.Р. Лечение хронических болезней органов пищеварения. – М. «Медицина», 1994.
4. Иваничев Г.А. Мануальная терапия. – М. «Медпресс». – 1998.– 470 С.
5. Лоуренс Д.Р., Бенитт П.Н. Клиническая фармакология. – М. «Медицина». – 1993. – Т.1.
6. Морган–мл. Д.Э., Михаил М.С. Клиническая анестезиология: книга 1–я. – М–СПб., Издательство БИНОМ–Невский Диалект, 2000.
7. Насонова В. А. Значение циклооксигеназы–2 в развитии боли. // Терапевтический архив, 2001, № 5, С. 56–57).
8. Насонов Е.Л. Нестероидные противовоспалительные препараты: проблемы безопасности лечения // Consilium medicum. – 1999. – Т.1.– №5.– С.207–211.
9. Павленко С.С. Эпидемиология боли. // Неврологический журнал, 1999, том 4, № 1, с.41–46.
10. Попелянский Я.Ю. Ортопедическая неврология. Вертеброневрология, т2, Казань, –1997.– 487 С.
11. Хабиров Ф.А. Клиническая неврология позвоночника. Казань, 2002г – 472 С.
12. Черненко О.А. Лечение болевых скелетно–мышечных поясничных синдромов//Рус. мед. журн. Т.8, №10.– С.408–410.
13. Adams N., Taylor D.N., Rose M.J. The psychophysiology of low back pain. – New York, Churchill Livingstone, 1997.
14. Bosch H.C., Sigmund R., Hettich M. Efficacy and tolerability of intramuscular and oral meloxicam in patients with acute lumbago: a comparison with intramuscular and oral piroxicam. // Cur. Med. Res. Opinion, 1997, Vol.14, N1, pp.29–38.
15. Carr D.B., Goudas L.C. Acute pain // Lancet. –1999. –Vol.353. – P. 2051–2058.
16. Colberg K., Hettich M., Sigmund R. et al. Efficacy and tolerability of an 8–day administration of intravenous and oral meloxicam: a comparison with intramuscular and oral diclofenac in patient with acute lumbago. // Cur. Med. Res. Opinion, 1996, Vol.13, N7, pp.363–377
17. Crombie I.K., Croft P.R., et al. Epidemiology of pain. IASP Press, 1999
18. Del Tacca M., Colucci R., Fornai M., Blandizzi C. Efficacy and tolerability of meloxicam, COX–2 preferential nonsteroidal anti–inflammatory drug. // Clin.Drug Ivest. 2002, 22 (12), pp. 799–818
19. Henry D., Lim L. L.–Y., Rodriguez L. A. G. et al. Variability in risk of gastrointestinal complications with individual non–steroidal anti–inflammatory drugs: results of a collaborative meta–analysis. // BMJ. – 1996. –Vol.312. – P.1563–1566.
20. Shipton E.A. Pain acute and chronic. 1999. Arnold Press.












