–Т–≤–µ–і–µ–љ–Є–µ
–Ш–Ј–Љ–µ–љ–µ–љ–Є—П, –њ—А–Њ–Є–Ј–Њ—И–µ–і—И–Є–µ –≤ –њ–Њ–љ–Є–Љ–∞–љ–Є–Є —Н—В–Є–Њ–ї–Њ–≥–Є–Є, –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–≤ (–°–њ–Р), —П–≤–Є–ї–Є—Б—М –Њ–і–љ–Є–Љ –Є–Ј –Ј–љ–∞—З–Є–Љ—Л—Е —Б–Њ–±—Л—В–Є–є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є XXI –≤. [1вАУ3]. –Э–∞—З–Є–љ–∞—П —Б 2009 –≥. –Љ–Є—А–Њ–≤–Њ–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–µ —Б–Њ–Њ–±—Й–µ—Б—В–≤–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В –њ–Њ–љ—П—В–Є—П –∞–Ї—Б–Є–∞–ї—М–љ—Л—Е —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–≤ (–∞–Ї—Б–°–њ–Р) –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–≤ (–њ–°–њ–Р), –њ—А–Є—З–µ–Љ –њ–µ—А–≤—Л–µ –њ–Њ–і—А–∞–Ј–і–µ–ї—П—О—В—Б—П –љ–∞ —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є (—А-–∞–Ї—Б–°–њ–Р) –Є –љ–µ—А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є (–љ—А-–∞–Ї—Б–°–њ–Р) —Д–µ–љ–Њ—В–Є–њ—Л. –Ш –µ—Б–ї–Є —А-–∞–Ї—Б–°–њ–Р, –Є–ї–Є –±–Њ–ї–µ–Ј–љ—М –С–µ—Е—В–µ—А–µ–≤–∞, –Є–Ј—Г—З–µ–љ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –њ–Њ–і—А–Њ–±–љ–Њ, —В–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П –Њ –љ—А-–∞–Ї—Б–°–њ–Р —Б–Ї—Г–і–љ—Л –Є –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л, –∞ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –≤–µ–і–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ—А-–∞–Ї—Б–°–њ–Р –Ј–∞–Є–Љ—Б—В–≤–Њ–≤–∞–љ—Л –Є–Ј —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –≤–µ–і–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А-–∞–Ї—Б–°–њ–Р [1вАУ3]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Ї 2020 –≥. —Б—В–∞–ї–Њ –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –≤—Л–±–Њ—А–Ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ—А-–∞–Ї—Б–°–њ–Р –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ —А–∞–Ј–љ–Њ—А–Њ–і–љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–µ–є, —Б–Њ—Б—В–Њ—П—Й–µ–є –Є–Ј –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Њ—А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –±–Њ–ї–µ–Ј–љ–Є –С–µ—Е—В–µ—А–µ–≤–∞ (¬Ђ–±—Г–і—Г—Й–Є–µ –њ–∞—Ж–Є–µ–љ—В—Л —Б –±–Њ–ї–µ–Ј–љ—М—О –С–µ—Е—В–µ—А–µ–≤–∞¬ї) –Є –Є–Ј –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б—В–Є–љ–љ–Њ –љ–µ—А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –∞–Ї—Б–°–њ–Р, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –±–Њ–ї–µ–Ј–љ–Є –≤ —А-–∞–Ї—Б–°–њ–Р –і–∞–ґ–µ –њ—А–Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–Љ —В–µ—З–µ–љ–Є–Є [4]. –Э–µ —Б–Ї–ї–Њ–љ–љ—Л–µ –Ї —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –≤ —А-–∞–Ї—Б–°–њ–Р –њ–∞—Ж–Є–µ–љ—В—Л —Б –Є—Б—В–Є–љ–љ–Њ –љ–µ—А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–њ–Р –і–∞–ґ–µ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —З–∞—Б—В–Њ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В –љ–Є–Ј–Ї—Г—О –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —З–∞—Й–µ –њ—А–Є–љ–∞–і–ї–µ–ґ–∞—В –Ї –ґ–µ–љ—Б–Ї–Њ–Љ—Г –њ–Њ–ї—Г, —А–µ–ґ–µ —П–≤–ї—П—О—В—Б—П –љ–Њ—Б–Є—В–µ–ї—П–Љ–Є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –ї–µ–є–Ї–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ –∞–љ—В–Є–≥–µ–љ–∞ –Т27 (HLA-B27) –Є —Е—Г–ґ–µ –Њ—В–≤–µ—З–∞—О—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є —Д–∞–Ї—В–Њ—А–∞ –љ–µ–Ї—А–Њ–Ј–∞ –Њ–њ—Г—Е–Њ–ї–Є-ќ± (–Є–§–Э–Ю) [4]. –Я–Њ–і–Њ–±–љ–∞—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –Ї –ї–µ—З–µ–љ–Є—О –Є–§–Э–Ю –Њ–њ—А–µ–і–µ–ї–Є–ї–∞ –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –њ–Њ–Є—Б–Ї–µ –љ–Њ–≤—Л—Е –ї–µ—З–µ–±–љ—Л—Е –Њ–њ—Ж–Є–є –і–ї—П —Г–Ї–∞–Ј–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ—А-–∞–Ї—Б–°–њ–Р. –Я–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –≤–∞—А–Є–∞–љ—В–Њ–Љ –њ–Њ–і–Њ–±–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —П–≤–Є–ї–Њ—Б—М –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Є–љ—В–µ—А–ї–µ–є–Ї–Є–љ–∞-17–Р (–Є–Ш–Ы-17–Р), –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є —Б–≤–Њ—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ —Е–Њ–і–µ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (PREVENT), –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–Є–Ј–Ї–Њ–є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П (—Б –љ–µ–≤—Л—Б–Њ–Ї–Є–Љ –Є–ї–Є –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ C-—А–µ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ [–°–†–С] –Є/–Є–ї–Є —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В–∞ –њ–Њ –і–∞–љ–љ—Л–Љ –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є [–Ь–†–Ґ]) [5].
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л —Б –љ—А-–∞–Ї—Б–°–њ–Р –≤ —Ж–µ–ї–Њ–Љ —А–µ–ґ–µ –њ–Њ–ї—Г—З–∞—О—В –≥–µ–љ–љ–Њ-–Є–љ–ґ–µ–љ–µ—А–љ—Г—О –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О, —З–µ–Љ –њ–∞—Ж–Є–µ–љ—В—Л —Б —А-–∞–Ї—Б–°–њ–Р, —З—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –Љ–µ–љ—М—И–µ–є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є —Г –љ–Є—Е –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є –Љ–µ–љ—М—И–µ–є —А–µ–Ј—Г–ї—М—В–∞—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Є–§–Э–Ю. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П, —З—В–Њ –њ–Њ –Љ–µ—А–µ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –њ–Њ–ї–љ–Њ–є —А–µ–Љ–Є—Б—Б–Є–Є —Б —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–µ–Љ —Б—В—А—Г–Ї—В—Г—А–љ–Њ–≥–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Њ—Б–µ–≤–Њ–≥–Њ —Б–Ї–µ–ї–µ—В–∞ –Ј–љ–∞—З–Є–Љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П, –і–∞–ґ–µ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б–∞–Љ—Л—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –≥–µ–љ–љ–Њ-–Є–љ–ґ–µ–љ–µ—А–љ—Л—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–ї–Є —В–∞—А–≥–µ—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–°–Њ–±—Б—В–≤–µ–љ–љ—Л–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ—А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –∞–Ї—Б–Є–∞–ї—М–љ—Л–Љ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–Љ
–Т –і–∞–љ–љ–Њ–є —А–∞–±–Њ—В–µ –љ–∞–Љ–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л 2 –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –љ–∞–±–ї—О–і–µ–љ–Є—П, –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—Й–Є—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Б—В–Њ–є–Ї–Њ–є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –±–µ–Ј–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є, —А–µ–Љ–Є—Б—Б–Є–Є –њ—А–Є —А–∞–љ–љ–µ–Љ (–Љ–µ–љ–µ–µ 6 –Љ–µ—Б. –Њ—В –Љ–Њ–Љ–µ–љ—В–∞ –њ–Њ—П–≤–ї–µ–љ–Є—П –њ–µ—А–≤—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П) –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ—А-–∞–Ї—Б–°–њ–Р. –Ю–±–∞ –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В–≤–µ—З–∞–ї–Є –Ї—А–Є—В–µ—А–Є—П–Љ –∞–Ї—Б–°–њ–Р –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–≤ (Assessment of SpondyloArthritis International Society, ASAS; 2009, 2011). –Ю—Ж–µ–љ–Ї–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–Ї—Б–°–њ–Р –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–љ—Л—Е –Ю–±—Й–µ—А–Њ—Б—Б–Є–є—Б–Ї–Њ–є –Њ–±—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–µ–є ¬Ђ–Р—Б—Б–Њ—Ж–Є–∞—Ж–Є—П —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Њ–≤ –†–Њ—Б—Б–Є–Є¬ї (–Ю–Ю–Ю –Р–†–†) [6]. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ—Г—В–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї—А–Є—В–µ—А–Є—П –љ–µ–∞–Ї—В–Є–≤–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є —Б–Њ–≥–ї–∞—Б–љ–Њ –Є–љ–і–µ–Ї—Б—Г –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р–° (Ankylosing Spondylitis Disease Activity Score, ASDAS) –Є –°–†–С вАУ ASDAS–°–†–С (ASDAS вАФ –љ–µ–∞–Ї—В–Є–≤–љ–∞—П –±–Њ–ї–µ–Ј–љ—М) –Є –њ—Г—В–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Є –Ї—А–Є—В–µ—А–Є–µ–≤ —А–µ–Љ–Є—Б—Б–Є–Є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –≥—А—Г–њ–њ—Л —Н–Ї—Б–њ–µ—А—В–Њ–≤ –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–≤ (–≠–Ї–°–њ–Р) –њ—А–Є –Ю–Ю–Ю –Р–†–† [7].
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ вДЦ 1
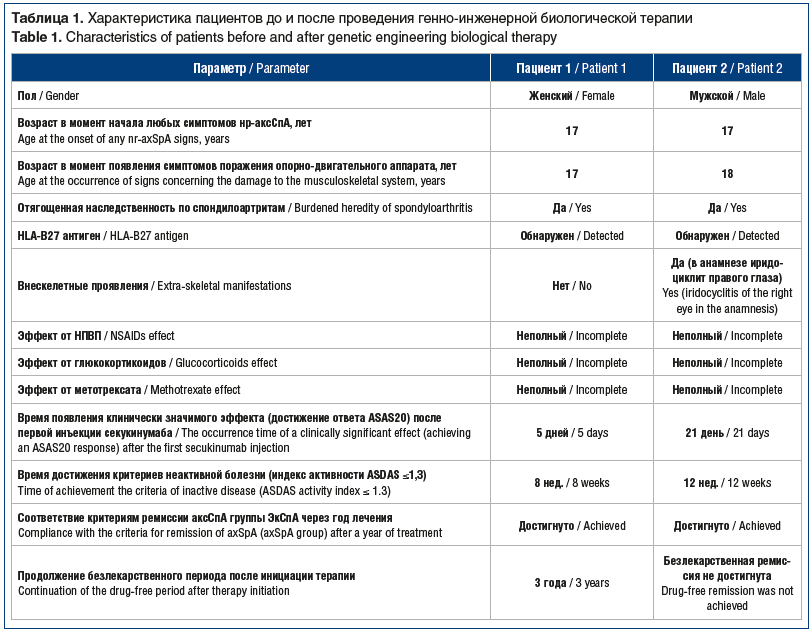
–Я–∞—Ж–Є–µ–љ—В–Ї–∞ –У. 1997 –≥–Њ–і–∞ —А–Њ–ґ–і–µ–љ–Є—П, –Є–Љ–µ—О—Й–∞—П –Њ—В—П–≥–Њ—Й–µ–љ–љ—Г—О –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В—М –њ–Њ –∞–Ї—Б–°–њ–Р (–∞–Ї—Б–°–њ–Р —Г –Љ–∞—В–µ—А–Є, —В–µ—В–Ї–Є –Є –і–µ–і–∞ –њ–Њ –Љ–∞—В–µ—А–Є–љ—Б–Ї–Њ–є –ї–Є–љ–Є–Є). –Я–µ—А–≤—Л–є —Н–њ–Є–Ј–Њ–і –∞—А—В—А–Є—В–∞ –≥–Њ–ї–µ–љ–Њ—Б—В–Њ–њ–љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞ –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –±–Њ–ї–µ–є –≤ —И–µ–є–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –љ–∞–±–ї—О–і–∞–ї—Б—П –≤ –≤–Њ–Ј—А–∞—Б—В–µ 17 –ї–µ—В –Є —А–∞–Ј—А–µ—И–Є–ї—Б—П –њ–Њ–ї–љ–Њ—Б—В—М—О –≤ —В–µ—З–µ–љ–Є–µ 2 –љ–µ–і. –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ —Н—В–Њ—А–Є–Ї–Њ–Ї—Б–Є–±–∞ –≤–љ—Г—В—А—М –≤ –і–Њ–Ј–µ 90 –Љ–≥/—Б—Г—В. –Я–∞—Ж–Є–µ–љ—В–Ї–∞ –љ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–ї–∞—Б—М, –Ї –≤—А–∞—З—Г –љ–µ –Њ–±—А–∞—Й–∞–ї–∞—Б—М.
–Я–Њ–≤—В–Њ—А–љ—Л–є —Н–њ–Є–Ј–Њ–і –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–∞–±–ї—О–і–∞–ї—Б—П –≤ –≤–Њ–Ј—А–∞—Б—В–µ 18 –ї–µ—В, —З–µ—А–µ–Ј 4 –Љ–µ—Б. –њ–Њ—Б–ї–µ –і–µ–±—О—В–∞ –±–Њ–ї–µ–Ј–љ–Є. –†–µ—Ж–Є–і–Є–≤ –∞–Ї—Б–°–њ–Р –њ—А–Њ—П–≤–Є–ї—Б—П –±–Њ–ї—М—О –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ –≤–Њ –≤—Б–µ—Е –Њ—В–і–µ–ї–∞—Е –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ–Њ–є –≤ 7вАУ8 –±–∞–ї–ї–Њ–≤ –њ–Њ 10-–±–∞–ї–ї—М–љ–Њ–є —З–Є—Б–ї–Њ–≤–Њ–є —А–µ–є—В–Є–љ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ (–І–†–®). –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –Є –њ–Њ –і–∞–љ–љ—Л–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–є –Ї–Њ–Ї—Б–Є—В, –≥–Њ–љ–Є—В, —Н–љ—В–µ–Ј–Є—В—Л (–Ь–∞–∞—Е—Б—В—А–Є—Е—В—Б–Ї–Є–є –Є–љ–і–µ–Ї—Б —Н–љ—В–µ–Ј–Є—В–Њ–≤ [Maastrich Ankylosing Spondylitis Enthesitis Score, MASES] –±—Л–ї —А–∞–≤–µ–љ 6 –±–∞–ї–ї–∞–Љ –Є–Ј –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е 13 –±–∞–ї–ї–Њ–≤). –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ –∞–љ—В–Є–≥–µ–љ–∞ HLA-B27, —Г—А–Њ–≤–µ–љ—М –°–†–С –Ї—А–Њ–≤–Є –љ–µ –њ–Њ–≤—Л—И–∞–ї—Б—П. –Я–Њ –і–∞–љ–љ—Л–Љ –Ь–†–Ґ –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л—Е —Б–Њ—З–ї–µ–љ–µ–љ–Є–є —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї. –Ы–µ—З–µ–љ–Є–µ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Э–Я–Т–Я) (–њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–∞–ї–Є –≤–љ—Г—В—А—М —В–∞–±–ї–µ—В–Ї–Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ –љ–∞—В—А–Є—П –њ–Њ 150 –Љ–≥/—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 7 –і–љ–µ–є, –Ј–∞—В–µ–Љ —В–∞–±–ї–µ—В–Ї–Є —Н—В–Њ—А–Є–Ї–Њ–Ї—Б–Є–±–∞ –≤–љ—Г—В—А—М –њ–Њ 90 –Љ–≥/—Б—Г—В), –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤ (–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ –≤–љ—Г—В—А—М –њ–Њ 10 –Љ/—Б—Г—В) –Є –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В–∞ (–њ–Њ 25 –Љ–≥ 1 —А/–љ–µ–і. –њ–Њ–і–Ї–Њ–ґ–љ–Њ) –Є–Љ–µ–ї–Њ –љ–µ–њ–Њ–ї–љ—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ –љ–∞ 1вАУ2 –±–∞–ї–ї–∞ –њ–Њ –І–†–®. –° 6-–є –љ–µ–і–µ–ї–Є –Њ—В –љ–∞—З–∞–ї–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є (—З–µ—А–µ–Ј 5,5 –Љ–µ—Б. —Б –Љ–Њ–Љ–µ–љ—В–∞ –і–µ–±—О—В–∞ –±–Њ–ї–µ–Ј–љ–Є) –њ–∞—Ж–Є–µ–љ—В–Ї–µ –±—Л–ї –љ–∞–Ј–љ–∞—З–µ–љ –њ–Њ–і–Ї–Њ–ґ–љ–Њ —А–∞—Б—В–≤–Њ—А —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ (–Ъ–Њ–Ј—Н–љ—В–Є–Ї—Б) –≤ –і–Њ–Ј–µ 150 –Љ–≥ 1 —А/–Љ–µc., –±–µ–Ј –Є–љ–Є—Ж–Є–∞—Ж–Є–Є (–Є–љ–Є—Ж–Є–∞—Ж–Є—П вАФ –≤–≤–µ–і–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ –љ–µ–і–µ–ї—П—Е 0, 1, 2, 3, 4). –≠—Д—Д–µ–Ї—В –Њ—В –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Ї–∞ –Њ—В–Љ–µ—В–Є–ї–∞ —З–µ—А–µ–Ј 5 –і–љ–µ–є –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ, –Ї–Њ–ї–µ–љ–љ—Л—Е –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–∞—Е (–і–Њ—Б—В–Є–≥–љ—Г—В –Њ—В–≤–µ—В ASAS 20).
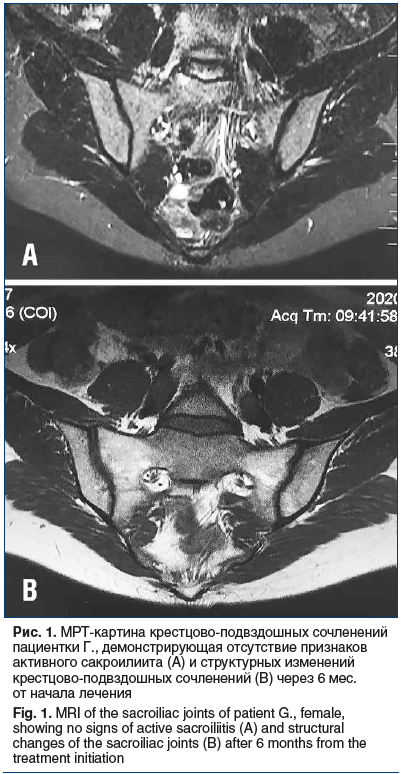
–Я–Њ–ї–љ–Њ–µ —А–∞–Ј—А–µ—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —З–µ—А–µ–Ј 8 –љ–µ–і. –Њ—В –љ–∞—З–∞–ї–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞, –њ–Њ—Б–ї–µ —З–µ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–Ї–∞ –Њ—В–Љ–µ–љ–Є–ї–∞ –Э–Я–Т–Я, –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ –Є –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В вАФ –±–µ–Ј —Г—Е—Г–і—И–µ–љ–Є—П. –І–µ—А–µ–Ј 6 –Љ–µ—Б. –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–Њ–Љ —Б —Г—З–µ—В–Њ–Љ –њ–Њ–ї–љ–Њ–є –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є –Є –Ь–†–Ґ-—А–µ–Љ–Є—Б—Б–Є–Є (—А–Є—Б. 1) –њ–∞—Ж–Є–µ–љ—В–Ї–∞ —Г–≤–µ–ї–Є—З–Є–ї–∞ –Є–љ—В–µ—А–≤–∞–ї—Л –Љ–µ–ґ–і—Г –≤–≤–µ–і–µ–љ–Є—П–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ 3 –Љ–µ—Б. –І–µ—А–µ–Ј –≥–Њ–і –ї–µ—З–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ —Б–Њ—Е—А–∞–љ—П—О—Й–µ–є—Б—П –њ–Њ–ї–љ–Њ–є –±–µ–Ј–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —А–µ–Љ–Є—Б—Б–Є–Є —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ь–†–Ґ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –Є —Б—Г—Б—В–∞–≤–Њ–≤ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–± –±—Л–ї –Њ—В–Љ–µ–љ–µ–љ. –†–µ—И–µ–љ–Є–µ –Њ–± –Њ—В–Љ–µ–љ–µ –ї–µ—З–µ–љ–Є—П –њ—А–Є–љ—П—В–Њ —Б —Г—З–µ—В–Њ–Љ –љ–Є–Ј–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ —Б—В—А—Г–Ї—В—Г—А–љ–Њ–≥–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Ї–Є (–ґ–µ–љ—Б–Ї–Є–є –њ–Њ–ї, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ –∞–Ї—Б–°–њ–Р —Г –±–Њ–ї—М–љ—Л—Е —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤, –љ–Є–Ј–Ї–Є–є –°–†–С –Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В–∞ –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ь–†–Ґ). –Т —В–µ—З–µ–љ–Є–µ 3 –ї–µ—В –њ–Њ—Б–ї–µ –Њ—В–Љ–µ–љ—Л –ї–µ—З–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Ї–Є —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –њ–Њ–ї–љ–∞—П –±–µ–Ј–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П —А–µ–Љ–Є—Б—Б–Є—П. –†–µ–і–Ї–Є–µ –∞—А—В—А–∞–ї–≥–Є–Є, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–µ –њ—А–Є –њ–µ—А–µ–Љ–µ–љ–µ –њ–Њ–≥–Њ–і—Л, –Ї—Г–њ–Є—А—Г—О—В—Б—П –њ—А–Є–µ–Љ–Њ–Љ –Э–Я–Т–Я (—Н—В–Њ—А–Є–Ї–Њ–Ї—Б–Є–± –≤–љ—Г—В—А—М –њ–Њ 90 –Љ/—Б—Г—В). –Я–Њ–ї–љ–∞—П –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –њ–∞—Ж–Є–µ–љ—В–Ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1, –і–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Њ—В—А–∞–ґ–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 2.

–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ вДЦ 2
–Я–∞—Ж–Є–µ–љ—В –°. 2001 –≥–Њ–і–∞ —А–Њ–ґ–і–µ–љ–Є—П, –Є–Љ–µ—О—Й–Є–є –Њ—В—П–≥–Њ—Й–µ–љ–љ—Г—О –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В—М –њ–Њ –∞–Ї—Б–°–њ–Р (–∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–Є–є —Б–њ–Њ–љ–і–Є–ї–Є—В —Г –Њ—В—Ж–∞). –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –і–µ–±—О—В–Є—А–Њ–≤–∞–ї–Њ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 17 –ї–µ—В —Б –њ–Њ—П–≤–ї–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Є—А–Є–і–Њ—Ж–Є–Ї–ї–Є—В–∞ –њ—А–∞–≤–Њ–≥–Њ –≥–ї–∞–Ј–∞, –Ї—Г–њ–Є—А–Њ–≤–∞–≤—И–µ–≥–Њ—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Ї–∞–њ–µ–ї—М —Б –і–µ–Ї—Б–∞–Љ–µ—В–∞–Ј–Њ–љ–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 2 –љ–µ–і. –Т–Њ–≤–ї–µ—З–µ–љ–Є–µ –≤ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –љ–∞—З–∞–ї–Њ—Б—М –≤ –≤–Њ–Ј—А–∞—Б—В–µ 18 –ї–µ—В –Є –њ—А–Њ—П–≤–ї—П–ї–Њ—Б—М –±–Њ–ї—М—О –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ –≤ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–µ, –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ–Њ–є –≤ 7вАУ8 –±–∞–ї–ї–Њ–≤ –њ–Њ –І–†–®, –Ї–Њ–Ї—Б–Є—В–Њ–Љ, –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–Љ –∞—Е–Є–ї–ї–Њ–±—Г—А—Б–Є—В–Њ–Љ (MASES —А–∞–≤–µ–љ 2 –±–∞–ї–ї–∞–Љ –Є–Ј 13), –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Г—А–Њ–≤–љ—П –°–†–С –і–Њ 7,5 –Љ–≥/–ї (–љ–Њ—А–Љ–∞–ї—М–љ—Л–µ –Ј–љ–∞—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–ї—П—О—В 0вАУ5 –Љ–≥/–ї). –Я—А–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤—Л—П–≤–ї–µ–љ–Њ –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ –∞–љ—В–Є–≥–µ–љ–∞ HLA-B27, –њ—А–Є –Ь–†–Ґ –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л—Е —Б–Њ—З–ї–µ–љ–µ–љ–Є–є –≤—Л—П–≤–ї–µ–љ —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В —Б–њ—А–∞–≤–∞ (—А–Є—Б. 2).
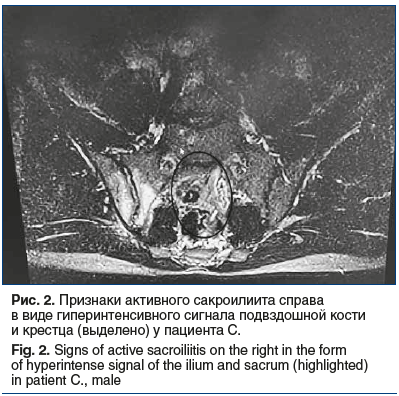
–Ы–µ—З–µ–љ–Є–µ —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Э–Я–Т–Я (–њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–∞–ї–Є –≤–љ—Г—В—А—М –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –љ–∞—В—А–Є—П –њ–Њ 150 –Љ–≥/—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є, –Ј–∞—В–µ–Љ —Н—В–Њ—А–Є–Ї–Њ–Ї—Б–Є–± –≤–љ—Г—В—А—М –њ–Њ 90 –Љ–≥/—Б—Г—В), –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤ (–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ –≤–љ—Г—В—А—М –њ–Њ 10вАУ20 –Љ–≥/—Б—Г—В) –Є –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В–∞ (–њ–Њ 25 –Љ–≥ 1 —А/–љ–µ–і. –њ–Њ–і–Ї–Њ–ґ–љ–Њ) –Є–Љ–µ–ї–Њ –љ–µ–њ–Њ–ї–љ—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ –љ–∞ 2вАУ3 –±–∞–ї–ї–∞ –њ–Њ –І–†–®. –І–µ—А–µ–Ј 4 –Љ–µ—Б. —Б –Љ–Њ–Љ–µ–љ—В–∞ –≤–Њ–≤–ї–µ—З–µ–љ–Є—П –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –њ–∞—Ж–Є–µ–љ—В—Г –±—Л–ї –љ–∞–Ј–љ–∞—З–µ–љ –њ–Њ–і–Ї–Њ–ґ–љ–Њ —А–∞—Б—В–≤–Њ—А —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ (–Ъ–Њ–Ј—Н–љ—В–Є–Ї—Б) –≤ –і–Њ–Ј–µ 150 –Љ–≥ 1 —А/–Љ–µ—Б. —Б 5-–є –љ–µ–і–µ–ї–Є –њ–Њ—Б–ї–µ –Є–љ–Є—Ж–Є–∞—Ж–Є–Є. –≠—Д—Д–µ–Ї—В –Њ—В –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В –Њ—В–Љ–µ—В–Є–ї —З–µ—А–µ–Ј 21 –і–µ–љ—М –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–∞—Е, –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—П –∞—Е–Є–ї–ї–Њ–±—Г—А—Б–Є—В–∞.
–Я–Њ–ї–љ–Њ–µ —А–∞–Ј—А–µ—И–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —З–µ—А–µ–Ј 12 –љ–µ–і. –Њ—В –љ–∞—З–∞–ї–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞, –њ–Њ—Б–ї–µ —З–µ–≥–Њ –њ–∞—Ж–Є–µ–љ—В –Њ—В–Љ–µ–љ–Є–ї –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ –Є –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В вАФ –±–µ–Ј —Г—Е—Г–і—И–µ–љ–Є—П. –•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –њ–∞—Ж–Є–µ–љ—В–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 2. –Я–Њ –Њ–±–Њ—О–і–љ–Њ–Љ—Г —А–µ—И–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–∞ –Є –≤—А–∞—З–∞ –њ–∞—Ж–Є–µ–љ—В –°. –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В –ї–µ—З–µ–љ–Є–µ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–Њ–Љ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –і–Њ—Б—В–Є–≥–љ—Г—В—Г—О —А–µ–Љ–Є—Б—Б–Є—О, —Б —Г—З–µ—В–Њ–Љ –Є–Љ–µ—О—Й–µ–≥–Њ—Б—П —А–Є—Б–Ї–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ —Б–ї—Г—З–∞–µ –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Є –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ —Б—В—А—Г–Ї—В—Г—А–љ–Њ–≥–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є –≤ —А-–∞–Ї—Б–°–њ–Р. –С—Л–ї–Є –њ—А–Є–љ—П—В—Л –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ —В–∞–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞, –Ї–∞–Ї –Љ—Г–ґ—Б–Ї–Њ–є –њ–Њ–ї, –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–Њ –∞–љ—В–Є–≥–µ–љ–∞ HLA-B27, –≤—Л—Б–Њ–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –і–µ–±—О—В–µ –±–Њ–ї–µ–Ј–љ–Є, –∞–Ї—В–Є–≤–љ—Л–є —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ь–†–Ґ –≤ –і–µ–±—О—В–µ –±–Њ–ї–µ–Ј–љ–Є, –±—Л—Б—В—А–Њ–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–µ–≥–Њ —Б–њ–Њ–љ–і–Є–ї–Є—В–∞ —Г –Њ—В—Ж–∞ –њ–∞—Ж–Є–µ–љ—В–∞ —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ ¬Ђ–±–∞–Љ–±—Г–Ї–Њ–≤–Њ–≥–Њ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞¬ї, –њ–Њ–ї–љ—Л–Љ –∞–љ–Ї–Є–ї–Њ–Ј–Њ–Љ –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л—Е —Б–Њ—З–ї–µ–љ–µ–љ–Є–є –Є —В–Њ—В–∞–ї—М–љ—Л–Љ —Н–љ–і–Њ–њ—А–Њ—В–µ–Ј–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Њ–±–Њ–Є—Е —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 28 –ї–µ—В. –Я—А–Є–µ–Љ —Н—В–Њ—А–Є–Ї–Њ–Ї—Б–Є–±–∞ –њ–∞—Ж–Є–µ–љ—В –°. –Њ—В–Љ–µ–љ–Є–ї —З–µ—А–µ–Ј –≥–Њ–і –ї–µ—З–µ–љ–Є—П вАФ –±–µ–Ј —Г—Е—Г–і—И–µ–љ–Є—П. –Я–ї–∞–љ–Є—А—Г–µ—В—Б—П –≤—Л–њ–Њ–ї–љ–µ–љ–Є–µ –Ь–†–Ґ –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л—Е —Б–Њ—З–ї–µ–љ–µ–љ–Є–є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –і–ї—П –Њ—Ж–µ–љ–Ї–Є –љ–∞–ї–Є—З–Є—П –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В–∞ –Є —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –њ–Њ—Б—В–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Б—Г—Б—В–∞–≤–Њ–≤.
–Ю–±–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–∞ –±—Л–ї–Є –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ —Е–Њ—А–Њ—И–Њ –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ—Л –Њ —Б—Г—В–Є —Б–≤–Њ–µ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –њ—А–Є–Љ–µ–љ—П–ї–Є –љ–µ–Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П (–њ–Њ—Б—В–Њ—П–љ–љ–∞—П –ї–µ—З–µ–±–љ–∞—П –≥–Є–Љ–љ–∞—Б—В–Є–Ї–∞, –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞, –Њ—В–Ї–∞–Ј –Њ—В –Ї—Г—А–µ–љ–Є—П).
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ —Б–ї—Г—З–∞–Є —П–≤–ї—П—О—В—Б—П –њ–µ—А–≤—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Њ–њ—Л—В–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ—А-–∞–Ї—Б–°–њ–Р –≤–љ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ —Е–Њ–і–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –љ–∞–±–ї—О–і–µ–љ–Є–є —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї–љ–Њ—Б—В—М—О —Б–Њ–≥–ї–∞—Б—Г—О—В—Б—П —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П PREVENT, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –±—Л–ї –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є, –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–є –Є –Ь–†–Ґ-—Н—Д—Д–µ–Ї—В—Л —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ –њ—А–Є –љ—А-–∞–Ї—Б–°–њ–Р, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–Є–Ј–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –°–†–С –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ь–†–Ґ –Ї—А–µ—Б—В—Ж–Њ–≤–Њ-–њ–Њ–і–≤–Ј–і–Њ—И–љ—Л—Е —Б–Њ—З–ї–µ–љ–µ–љ–Є–є [5]. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ–Њ–і–Њ–±–љ—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л —Б –љ—А-–∞–Ї—Б–°–њ–Р —Б–Њ —Б–ї–∞–±–Њ–≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ —З–∞—Й–µ, —З–µ–Љ –њ–∞—Ж–Є–µ–љ—В—Л —Б –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤—Л—Б–Њ–Ї–Њ–є –≥—А–∞–і–∞—Ж–Є–Є, –Њ–Ї–∞–Ј—Л–≤–∞—О—В—Б—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –Ї –Э–Я–Т–Я –Є/–Є–ї–Є –Є–§–Э–Ю [4]. –£–Ї–∞–Ј–∞–љ–љ—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л –Є–Љ–µ—О—В –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –Љ–µ–љ—М—И—Г—О —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї —Б—В—А—Г–Ї—В—Г—А–љ–Њ–Љ—Г –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О, –Є —П–≤–ї—П—О—В—Б—П —Б–ї–Њ–ґ–љ—Л–Љ–Є –і–ї—П –ї–µ—З–µ–љ–Є—П [4]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ PREVENT –і–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–± –Љ–Њ–ґ–µ—В –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–∞–Ї –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–љ–Є—Ж–Є–Є—А—Г—О—Й–µ–є –љ–∞–≥—А—Г–Ј–Њ—З–љ–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞, —В–∞–Ї –Є –±–µ–Ј –Є–љ–Є—Ж–Є–∞—Ж–Є–Є [5]. –Ґ–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–± –њ—А–Є –∞–Ї—Б–°–њ–Р —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –Њ—В–≤–µ—З–∞–ї–Є –љ–∞ –Є–§–Э–Ю. –° —Г—З–µ—В–Њ–Љ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ –љ–µ—Г–і–∞—З–Є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–§–Э–Ю –≤–≤–Є–і—Г –Њ—В—Б—Г—В—Б—В–≤–Є—П –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤—Л—Б–Њ–Ї–Њ–є –≥—А–∞–і–∞—Ж–Є–Є —Г –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞–Љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–∞ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –њ—А–Є–Љ–µ–љ–Є–ї–Є –Є–Ш–Ы-17–Р (—Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –і–Њ–±–Є—В—М—Б—П –Њ—Ж–µ–љ–Ї–Є ASDAS вАУ –љ–µ–∞–Ї—В–Є–≤–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –Є –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є —А–µ–Љ–Є—Б—Б–Є–Є —Б–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –≠–Ї–°–њ–Р —Г –Њ–±–Њ–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–Є –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В–∞ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –≥–µ–љ–љ–Њ-–Є–љ–ґ–µ–љ–µ—А–љ–Њ–є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є (–У–Ш–С–Ґ) —В–Њ–ґ–µ —П–≤–ї—П–µ—В—Б—П –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е —Б–ї—Г—З–∞–µ–≤ –Є —Б–Њ–≥–ї–∞—Б—Г–µ—В—Б—П —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –≥—А—Г–њ–њ—Л –≠–Ї–°–њ–Р –њ—А–Є –Р–†–† [8].
–Э–∞—Б—В–Њ—П—Й–∞—П —А–∞–±–Њ—В–∞ –Ј–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В –≤–љ–Є–Љ–∞–љ–Є—П –µ—Й–µ –Є –њ–Њ—В–Њ–Љ—Г, —З—В–Њ –≤ –љ–µ–є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Б–ї—Г—З–∞–Є, –≤ –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –і–µ–±—О—В–∞ –∞–Ї—Б–°–њ–Р, –њ—А–Є –Њ—В—П–≥–Њ—Й–µ–љ–љ–Њ–є –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В–Є –Є –љ–Њ—Б–Є—В–µ–ї—М—Б—В–≤–µ HLA-B27 –њ—А–Њ–≥–љ–Њ–Ј —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —А–∞–Ј–љ—Л–є –≤–≤–Є–і—Г —А–∞–Ј–љ—Л—Е —Д–µ–љ–Њ—В–Є–њ–Њ–≤ –љ—А-–∞–Ї—Б–°–њ–Р. –Я–∞—Ж–Є–µ–љ—В –Љ—Г–ґ—Б–Ї–Њ–≥–Њ –њ–Њ–ї–∞ вАФ –љ–Њ—Б–Є—В–µ–ї—М –∞–љ—В–Є–≥–µ–љ–∞ HLA-B27 —Б –∞–Ї—В–Є–≤–љ—Л–Љ —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В–Њ–Љ –Є–Љ–µ–µ—В –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –≤ –∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–Є–є —Б–њ–Њ–љ–і–Є–ї–Є—В —Б —В—П–ґ–µ–ї—Л–Љ–Є —Б—В—А—Г–Ї—В—Г—А–љ—Л–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є, –Ї–∞–Ї –Є –µ–≥–Њ –Њ—В–µ—Ж [4, 8]. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ –њ—А–Є–Љ–µ–љ–µ–љ–∞ —Б—Е–µ–Љ–∞ –ї–µ—З–µ–љ–Є—П —Б –Є–љ–Є—Ж–Є–∞—Ж–Є–µ–є (–њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–љ–Є—Ж–Є–Є—А—Г—О—Й–µ–є —Б—Е–µ–Љ—Л —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–∞–Є–±–Њ–ї–µ–µ –±—Л—Б—В—А–Њ–Љ—Г –њ–Њ—П–≤–ї–µ–љ–Є—О –њ–µ—А–≤–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Њ—В –ї–µ—З–µ–љ–Є—П) –Є –љ–µ –њ–ї–∞–љ–Є—А—Г–µ—В—Б—П –Њ—В–Ї–∞–Ј –Њ—В –ї–µ—З–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ —А–µ–Љ–Є—Б—Б–Є–Є [5]. –£–Ї–∞–Ј–∞–љ–љ—Л–є –њ–∞—Ж–Є–µ–љ—В, –њ–Њ –љ–∞—И–µ–Љ—Г –Љ–љ–µ–љ–Є—О, –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Ї–Њ–≥–Њ—А—В—Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ—А-–∞–Ї—Б–°–њ–Р вАФ ¬Ђ–±—Г–і—Г—Й–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–Ј–љ—М—О –С–µ—Е—В–µ—А–µ–≤–∞¬ї [4], –∞ –њ—А–Є–Љ–µ–љ–µ–љ–љ—Л–є –љ–∞–Љ–Є –њ–Њ–і—Е–Њ–і, —Б —Г—З–µ—В–Њ–Љ –і–∞–љ–љ—Л—Е –њ–Њ —В–Њ—А–Љ–Њ–ґ–µ–љ–Є—О –Є–Ш–Ы-17–Р —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –∞–Ї—Б–Є–∞–ї—М–љ–Њ–≥–Њ —Б–Ї–µ–ї–µ—В–∞, –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–њ–Њ—Б–Њ–±–Њ–Љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є [9, 10]. –†–∞–љ–љ–µ–µ –љ–∞—З–∞–ї–Њ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –У–Ш–С–Ґ –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–µ–Ј–љ–Є.
–Я–∞—Ж–Є–µ–љ—В–Ї–∞ –ґ–µ–љ—Б–Ї–Њ–≥–Њ –њ–Њ–ї–∞, —Б —Г—З–µ—В–Њ–Љ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –µ–µ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В–Є, –Њ—В—Б—Г—В—Б—В–≤–Є—П –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П –°–†–С –Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В–∞, –Њ—В–љ–µ—Б–µ–љ–∞ –љ–∞–Љ–Є –Ї –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б ¬Ђ–Є—Б—В–Є–љ–љ—Л–Љ¬ї –љ—А-–∞–Ї—Б–°–њ–Р [4], —З—В–Њ –Њ–њ—А–µ–і–µ–ї–Є–ї–Њ –ї–µ—З–µ–љ–Є–µ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–Њ–Љ –±–µ–Ј –Є–љ–Є—Ж–Є–∞—Ж–Є–Є –Є –Њ—В–Љ–µ–љ—Г –ї–µ—З–µ–љ–Є—П –њ–Њ—Б–ї–µ —А–∞–Ј—А–µ—И–µ–љ–Є—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л. –Т —Б–ї—Г—З–∞–µ —А–µ—Ж–Є–і–Є–≤–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Љ—Л —А–∞—Б—Б—З–Є—В—Л–≤–∞–µ–Љ –≤–Њ–Ј–Њ–±–љ–Њ–≤–Є—В—М –ї–µ—З–µ–љ–Є–µ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–Њ–Љ —Б —Г—З–µ—В–Њ–Љ –љ–Є–Ј–Ї–Њ–є –Є–Љ–Љ—Г–љ–Њ–≥–µ–љ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ—Л –њ—А–µ–і—Б—В–∞–≤–Є–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –љ–∞–±–ї—О–і–µ–љ–Є—П, –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Г—Б–њ–µ—И–љ–Њ–≥–Њ —А–∞–љ–љ–µ–≥–Њ –ї–µ—З–µ–љ–Є—П –љ—А-–∞–Ї—Б–°–њ–Р —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ–µ—А–≤–Њ–≥–Њ –≥–µ–љ–љ–Њ-–Є–љ–ґ–µ–љ–µ—А–љ–Њ–≥–Њ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–љ—Л–Љ–Є —Д–µ–љ–Њ—В–Є–њ–∞–Љ–Є –љ—А-–∞–Ї—Б–°–њ–Р.
–£–Ї–∞–Ј–∞–љ–љ—Л–µ –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ –Љ–Њ–≥—Г—В –±—Л—В—М –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –≥–ї–Њ–±–∞–ї—М–љ—Л—Е –≤—Л–≤–Њ–і–Њ–≤, –љ–Њ –Љ–Њ–≥—Г—В —Б—В–∞—В—М —З–∞—Б—В—М—О —В–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–њ—Л—В–∞, –Ї–Њ—В–Њ—А—Л–є –±—Г–і–µ—В –њ–Њ–ї–Њ–ґ–µ–љ –≤ –Њ—Б–љ–Њ–≤—Г –Є–Ј—Г—З–µ–љ–Є—П –љ—А-–∞–Ї—Б–°–њ–Р —Б –і–∞–ї—М–љ–µ–є—И–Є–Љ —Б–Њ–Ј–і–∞–љ–Є–µ–Љ –Њ—В–і–µ–ї—М–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –ї–µ—З–µ–љ–Є—О –љ—А-–∞–Ї—Б–°–њ–Р [11]. –Я—А–Є–Љ–µ–љ—П–µ–Љ–Њ–µ –≤ –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В –Ј–∞–Є–Љ—Б—В–≤–Њ–≤–∞–љ–Є–µ –њ–Њ–і—Е–Њ–і–Њ–≤ –Є–Ј —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А-–∞–Ї—Б–°–њ–Р –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Њ–њ—А–∞–≤–і–∞–љ–љ—Л–Љ —Б —Г—З–µ—В–Њ–Љ —В–Њ–≥–Њ, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В –Є–і–µ—В –њ–µ—А–≤–Є—З–љ–Њ–µ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –Ј–љ–∞–љ–Є–є –≤ –Њ–±–ї–∞—Б—В–Є –љ—А-–∞–Ї—Б–°–њ–Р. –Э–∞—З–∞–ї–Њ–Љ —Н—А—Л –љ—А-–∞–Ї—Б–°–њ–Р –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М 2009 –≥., –Ї–Њ–≥–і–∞ –≤–њ–µ—А–≤—Л–µ –±—Л–ї–Є —Б—Д–Њ—А–Љ—Г–ї–Є—А–Њ–≤–∞–љ—Л –Ї—А–Є—В–µ—А–Є–Є –∞–Ї—Б–Є–∞–ї—М–љ—Л—Е —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–≤, –њ—А–Є–Ј–љ–∞—О—Й–Є–µ –љ–µ–Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є—О —Б–∞–Ї—А–Њ–Є–ї–Є–Є—В–∞ –Є –Њ–±–Њ–Ј–љ–∞—З–Є–≤—И–Є–µ –љ–∞–ї–Є—З–Є–µ ¬Ђ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —А—Г–Ї–∞–≤–∞¬ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –∞–Ї—Б–Є–∞–ї—М–љ—Л—Е —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–≤ [11]. –Ю–і–љ–∞–Ї–Њ —Б —Г—З–µ—В–Њ–Љ –≤—Л—Б–Њ–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –њ—А–Њ–±–ї–µ–Љ—Л –љ—А-–∞–Ї—Б–°–њ–Р —Б–ї–µ–і—Г–µ—В –Њ–ґ–Є–і–∞—В—М –±—Л—Б—В—А–Њ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –љ–∞—Г—З–љ–Њ–є –±–∞–Ј—Л, –Ї–Њ—В–Њ—А–∞—П –њ–Њ—Б–ї—Г–ґ–Є—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –Њ—Б–љ–Њ–≤–∞–љ–љ—Л—Е –љ–∞ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –ї–µ—З–µ–љ–Є—О –љ—А-–∞–Ї—Б–°–њ–Р [11]. –Т –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ–Њ–є —А–∞–±–Њ—В–µ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –±—Л—Б—В—А–Њ–≥–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –љ–µ–∞–Ї—В–Є–≤–љ–Њ–є —Д–∞–Ј—Л –±–Њ–ї–µ–Ј–љ–Є —Б –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–є –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –љ–∞ —Д–Њ–љ–µ —А–∞–љ–љ–µ–≥–Њ (–і–Њ 6 –Љ–µ—Б. –Њ—В –Љ–Њ–Љ–µ–љ—В–∞ –њ–Њ—П–≤–ї–µ–љ–Є—П –њ–µ—А–≤—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤) –ї–µ—З–µ–љ–Є—П –љ—А-–∞–Ї—Б–°–њ–Р —Б–µ–Ї—Г–Ї–Є–љ—Г–Љ–∞–±–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Д–µ–љ–Њ—В–Є–њ–∞–Љ–Є –±–Њ–ї–µ–Ј–љ–Є.
–С–ї–∞–≥–Њ–і–∞—А–љ–Њ—Б—В—М
–†–µ–і–∞–Ї—Ж–Є—П –±–ї–∞–≥–Њ–і–∞—А–Є—В –Ї–Њ–Љ–њ–∞–љ–Є—О ¬Ђ–Э–Њ–≤–∞—А—В–Є—Б¬ї –Ј–∞ –Њ–Ї–∞–Ј–∞–љ–љ—Г—О –њ–Њ–Љ–Њ—Й—М –≤ —В–µ—Е–љ–Є—З–µ—Б–Ї–Њ–є —А–µ–і–∞–Ї—В—Г—А–µ –љ–∞—Б—В–Њ—П—Й–µ–є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є.
Aknowledgement
The technical edition is supported by Novartis.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–∞—Е:
–У–∞–є–і—Г–Ї–Њ–≤–∞ –Ш–љ–љ–∞ –Ч—Г—А–∞–±–Є–µ–≤–љ–∞ вАФ –і.–Љ.–љ., –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М –і–Є—А–µ–Ї—В–Њ—А–∞ –Э–Ш–Ш —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, –њ—А–Њ—Д–µ—Б—Б–Њ—А –Ї–∞—Д–µ–і—А—Л —В–µ—А–∞–њ–Є–Є, —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, —Н–Ї—Б–њ–µ—А—В–Є–Ј—Л –≤—А–µ–Љ–µ–љ–љ–Њ–є –љ–µ—В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Є –Ї–∞—З–µ—Б—В–≤–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –Є–Љ. –≠.–≠. –≠–є—Е–≤–∞–ї—М–і–∞ –§–У–С–Ю–£ –Т–Ю –°–Ч–У–Ь–£ –Є–Љ. –Ш.–Ш. –Ь–µ—З–љ–Є–Ї–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 191015, –†–Њ—Б—Б–Є—П, –≥. –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, —Г–ї. –Ъ–Є—А–Њ—З–љ–∞—П, –і. 41; –°–Я–± –У–С–£–Ч ¬Ђ–Ъ–†–С вДЦ 25¬ї; 190068, –†–Њ—Б—Б–Є—П, –≥. –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, —Г–ї. –С–Њ–ї—М—И–∞—П –Я–Њ–і—К—П—З–µ—Б–Ї–∞—П, –і. 30; ORCID iD 0000-0003-3500-7256.
–Ь–∞–Ј—Г—А–Њ–≤ –Т–∞–і–Є–Љ –Ш–≤–∞–љ–Њ–≤–Є—З вАФ –і.–Љ.–љ., –∞–Ї–∞–і–µ–Љ–Є–Ї –†–Р–Э, –Ј–∞—Б–ї—Г–ґ–µ–љ–љ—Л–є –і–µ—П—В–µ–ї—М –љ–∞—Г–Ї–Є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є, –њ—А–Њ—Д–µ—Б—Б–Њ—А, –≥–ї–∞–≤–љ—Л–є –љ–∞—Г—З–љ—Л–є –Ї–Њ–љ—Б—Г–ї—М—В–∞–љ—В, –і–Є—А–µ–Ї—В–Њ—А –Э–Ш–Ш —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –Ј–∞–≤–µ–і—Г—О—Й–Є–є –Ї–∞—Д–µ–і—А–Њ–є —В–µ—А–∞–њ–Є–Є, —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, —Н–Ї—Б–њ–µ—А—В–Є–Ј—Л –≤—А–µ–Љ–µ–љ–љ–Њ–є –љ–µ—В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Є –Ї–∞—З–µ—Б—В–≤–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –Є–Љ. –≠.–≠. –≠–є—Е–≤–∞–ї—М–і–∞
–§–У–С–Ю–£ –Т–Ю –°–Ч–У–Ь–£ –Є–Љ. –Ш.–Ш. –Ь–µ—З–љ–Є–Ї–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 191015, –†–Њ—Б—Б–Є—П, –≥. –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, —Г–ї. –Ъ–Є—А–Њ—З–љ–∞—П, –і. 41; —А—Г–Ї–Њ–≤–Њ–і–Є—В–µ–ї—М —Ж–µ–љ—В—А–∞ –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –°–Я–± –У–С–£–Ч ¬Ђ–Ъ–†–С вДЦ 25¬ї; 190068, –†–Њ—Б—Б–Є—П, –≥. –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, —Г–ї. –С–Њ–ї—М—И–∞—П –Я–Њ–і—К—П—З–µ—Б–Ї–∞—П, –і. 30; ORCID iD 0000-0002-0797-2051.
–Ш–љ–∞–Љ–Њ–≤–∞ –Ю–Ї—Б–∞–љ–∞ –Т–ї–∞–і–Є–Љ–Є—А–Њ–≤–љ–∞ вАФ –Ї.–Љ.–љ., –≥–ї–∞–≤–љ—Л–є –≤—А–∞—З –°–Я–± –У–С–£–Ч ¬Ђ–Ъ–†–С вДЦ 25¬ї; 190068, –†–Њ—Б—Б–Є—П, –≥. –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, —Г–ї. –С–Њ–ї—М—И–∞—П –Я–Њ–і—К—П—З–µ—Б–Ї–∞—П, –і. 30; –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М –і–Є—А–µ–Ї—В–Њ—А–∞ –Э–Ш–Ш —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, –∞—Б—Б–Є—Б—В–µ–љ—В –Ї–∞—Д–µ–і—А—Л —В–µ—А–∞–њ–Є–Є, —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, —Н–Ї—Б–њ–µ—А—В–Є–Ј—Л –≤—А–µ–Љ–µ–љ–љ–Њ–є –љ–µ—В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Є –Ї–∞—З–µ—Б—В–≤–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –Є–Љ. –≠.–≠. –≠–є—Е–≤–∞–ї—М–і–∞ –§–У–С–Ю–£ –Т–Ю –°–Ч–У–Ь–£ –Є–Љ. –Ш.–Ш. –Ь–µ—З–љ–Є–Ї–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 191015, –†–Њ—Б—Б–Є—П, –≥. –°–∞–љ–Ї—В-–Я–µ—В–µ—А–±—Г—А–≥, —Г–ї. –Ъ–Є—А–Њ—З–љ–∞—П, –і. 41; ORCID iD 0000-0001-9126-3639.
–Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –У–∞–є–і—Г–Ї–Њ–≤–∞ –Ш–љ–љ–∞ –Ч—Г—А–∞–±–Є–µ–≤–љ–∞, e-mail: ubp1976@list.ru.
–Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: –љ–Є–Ї—В–Њ –Є–Ј –∞–≤—В–Њ—А–Њ–≤ –љ–µ –Є–Љ–µ–µ—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є –Љ–µ—В–Њ–і–∞—Е.
–Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.
–°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞ 13.07.2021.
–Я–Њ—Б—В—Г–њ–Є–ї–∞ –њ–Њ—Б–ї–µ —А–µ—Ж–µ–љ–Ј–Є—А–Њ–≤–∞–љ–Є—П 05.08.2021.
–Я—А–Є–љ—П—В–∞ –≤ –њ–µ—З–∞—В—М 30.08.2021.
About the authors:
Inna Z. Gaydukova вАФ Dr. Sc. (Med.), Head of the Research Institute of Rheumatology, Professor of the Department of Therapy, Rheumatology, Temporary Disability Examination and Quality of Medical Care named after E.E. Eichwald, North-Western State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., Saint Petersburg, 191015, Russian Federation; Clinical Rheumatological Hospital No. 25; 30, Bolshaya Podyacheskay–∞ str., Saint Petersburg, 190068, Russian Federation; ORCID iD 0000-0003-3500-7256.
Vadim I. Mazurov вАФ Academician of the Russian Academy of Sciences, Honored Scientist of the Russian Federation, Dr. Sc. (Med.), Professor, Chief Scientific Consultant, Director of the Research Institute of Rheumatology, Head of the Department of Therapy, Rheumatology, Temporary Disability Examination and Quality of Medical Care named after E.E. Eichwald, North-Western State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., Saint Petersburg, 191015, Russian Federation; Head of the Center of Autoimmune Diseases, Clinical Rheumatological Hospital No. 25; 30, Bolshaya Podyacheskay–∞ str., Saint Petersburg, 190068, Russian Federation; ORCID iD 0000-0002-0797-2051.
Oksana V. Inamova вАФ C. Sc. (Med.), Chief Officer of Clinical Rheumatological Hospital No. 25; 30, Bolshaya Podyacheskay–∞ str., Saint Petersburg, 190068, Russian Federation; Head of the Research Institute of Rheumatology, Assistant Professor of the Department of Therapy, Rheumatology, Temporary Disability Examination and Quality of Medical Care named after E.E. Eichwald, North-Western State Medical University named after I.I. Mechnikov; 41, Kirochnaya str., Saint Petersburg, 191015, Russian Federation; ORCID iD 0000-0001-9126-3639.
Contact information: Inna Z. Gaydukova, e-mail: ubp1976@list.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 13.07.2021.
Revised 05.08.2021.
Accepted 30.08.2021.












