–Ґ–Є–Ј–∞–љ–Є–і–Є–љ (–°–Є—А–і–∞–ї—Г–і) – –Є–Љ–Є–і–∞–Ј–Њ–ї–Є–љ–Њ–≤—Л–є –∞–≥–Њ–љ–Є—Б—В a2––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –њ—А–Є–Љ–µ–љ—П—О—Й–Є–є—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–∞ –њ—А–Є —Б–Њ—Б—В–Њ—П–љ–Є—П—Е, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –Љ—Л—И–µ—З–љ—Л–Љ —Б–њ–∞–Ј–Љ–Њ–Љ (–Є–љ—Д–∞—А–Ї—В –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, —Б–Є—Б—В–µ–Љ–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П, –Њ—Б—В—А–∞—П –±–Њ–ї—М –≤ —Б–њ–Є–љ–µ) [9–12].
–°–Є—А–і–∞–ї—Г–і –њ–Њ–Ї–∞–Ј–∞–ї –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –ї–µ—З–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А–Њ–є –±–Њ–ї—М—О –≤ —Б–њ–Є–љ–µ [9,13]. –Т 1988 –≥. Berry H. —Б —Б–Њ–∞–≤—В. —Г—Б—В–∞–љ–Њ–≤–Є–ї–Є, —З—В–Њ –њ—А–Є –Њ—Б—В—А–Њ–є –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –°–Є—А–і–∞–ї—Г–і–∞ —Б –Є–±—Г–њ—А–Њ—Д–µ–љ–Њ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–µ–µ, —З–µ–Љ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Є–±—Г–њ—А–Њ—Д–µ–љ–Њ–Љ [14]. –Т –і–∞–ї—М–љ–µ–є—И–µ–Љ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–µ–њ–∞—А–∞—В –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Г–Љ–µ–љ—М—И–∞–µ—В –±–Њ–ї—М –Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–∞—Е (–Э–Я–Т–Я) –њ—А–Є –љ–∞–ї–Є—З–Є–Є –±–Њ–ї–Є –≤ –њ–Њ–Ї–Њ–µ, —З–µ–Љ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –±–Њ–ї–Є –≤–Њ –≤—А–µ–Љ—П –і–≤–Є–ґ–µ–љ–Є—П [15,16], —З—В–Њ, –≤–µ—А–Њ—П—В–љ–Њ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –±–Њ–ї—М—И–µ–є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –љ–Њ—З–љ–Њ–є –±–Њ–ї–Є. Pareek A. —Б —Б–Њ–∞–≤—В. —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –і–Њ–±–∞–≤–ї–µ–љ–Є–µ —В–Є–Ј–∞–љ–Є–і–Є–љ–∞ –Ї –∞—Ж–µ–Ї–ї–Њ—Д–µ–љ–∞–Ї—Г –љ–µ —В–Њ–ї—М–Ї–Њ —Г–Љ–µ–љ—М—И–∞–µ—В –±–Њ–ї—М –≤ —Б–њ–Є–љ–µ, –љ–Њ –Є –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, —З–µ–Љ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –∞—Ж–µ–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ [16].
–Т—Б–µ –њ—А–Є–≤–µ–і–µ–љ–љ—Л–µ –≤—Л—И–µ —Б–≤–µ–і–µ–љ–Є—П –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –ї–µ—З–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—Б—В—А–Њ–є –±–Њ–ї—М—О –≤ —Б–њ–Є–љ–µ. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –љ–∞—Б –Є–љ—В–µ—А–µ—Б—Г–µ—В –ї–µ—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–° —Б –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ –±–Њ–ї–Є, –Ї–Њ—В–Њ—А–∞—П —П–≤–ї—П–µ—В—Б—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є. –Ф–∞–љ–љ—Л–µ –Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –°–Є—А–і–∞–ї—Г–і–∞ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ —Б–Ї—Г–і–љ—Л –Є –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л. –Т –Њ–±–Ј–Њ—А–µ –ї–Є—В–µ—А–∞—В—Г—А—Л, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–Љ White A.P. —Б —Б–Њ–∞–≤—В., –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –Є–Љ–µ—О—Й–Є–µ—Б—П —Б–≤–µ–і–µ–љ–Є—П –љ–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В—Л –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї—М—О –≤ —Б–њ–Є–љ–µ, —В–∞–Ї –Ї–∞–Ї –≤ –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В –≤ –љ–∞—И–µ–Љ —А–∞—Б–њ–Њ—А—П–ґ–µ–љ–Є–Є –Є–Љ–µ–µ—В—Б—П –ї–Є—И—М –љ–µ–±–Њ–ї—М—И–Њ–µ —З–Є—Б–ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤–Ї–ї—О—З–∞–≤—И–Є—Е –љ–µ–Њ–і–љ–Њ—А–Њ–і–љ—Л—Е –њ–Њ –≥–µ–љ–µ–Ј—Г –±–Њ–ї–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—Б —В—А–∞–≤–Љ–∞–Љ–Є, –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ––і–µ—Б—В—А—Г–Ї—В–Є–≤–љ—Л–Љ–Є, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Є –і—А—Г–≥–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞) [17].
–¶–µ–ї—М—О –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–Є–ї–Њ—Б—М –Є–Ј—Г—З–µ–љ–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –°–Є—А–і–∞–ї—Г–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–° –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е —А–∞–Ј–ї–Є—З–љ—Л–µ –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –њ—А–µ–њ–∞—А–∞—В–∞.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–µ–љ–Њ 116 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ «–∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–Є–є —Б–њ–Њ–љ–і–Є–ї–Є—В»: 96 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є–µ –Њ–±–ї–∞—Б—В–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї—М–љ–Є—Ж—Л –≥. –°–∞—А–∞—В–Њ–≤–∞ –≤ 2010 –≥., 20 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ – –≤ 2012 –≥. –Ф–Є–∞–≥–љ–Њ–Ј —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–ї–Є –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є—П —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞ –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Э—М—О––Щ–Њ—А–Ї—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є—П–Љ (1984) [2]. –Я–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Є –Њ–±—Й–µ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Є –Њ–±—Й–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є (–Ю–Р–Ъ), –Њ–±—Й–Є–є –∞–љ–∞–ї–Є–Ј –Љ–Њ—З–Є (–Ю–Р–Ь), –°––†–С (–≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ); –Њ–±—Й–Є–є –±–µ–ї–Њ–Ї, –∞–ї—М–±—Г–Љ–Є–љ—Л, –Љ–Њ—З–µ–≤–Є–љ—Г, –Ї—А–µ–∞—В–Є–љ–Є–љ, –≥–ї—О–Ї–Њ–Ј—Г, –±–Є–ї–Є—А—Г–±–Є–љ, –∞—Б–њ–∞—А—В–∞—В– –Є –∞–ї–∞–љ–Є–љ–∞–Љ–Є–љ–Њ—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Г —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є. –Р–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–° –Њ–њ—А–µ–і–µ–ї—П–ї–Є –њ—Г—В–µ–Љ —А–∞—Б—З–µ—В–∞ –Є–љ–і–µ–Ї—Б–∞ BASDAI (Bath Ankylosing Spondylitis Disease Activity Index) [18]. –Ф–ї—П –Њ—Ж–µ–љ–Ї–Є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –Њ—Б–µ–≤–Њ–≥–Њ —Б–Ї–µ–ї–µ—В–∞ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —А–∞—Б—Б—В–Њ—П–љ–Є–µ –Ј–∞—В—Л–ї–Њ–Ї – —Б—В–µ–љ–∞, —А–Њ—В–∞—Ж–Є—О –≤ —И–µ–є–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –±–Њ–Ї–Њ–≤—Г—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –і–ї—П –Њ—Ж–µ–љ–Ї–Є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –≤—Л–њ–Њ–ї–љ—П–ї–Є –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є —В–µ—Б—В –®–Њ–±–µ—А–∞ [19]. –Р–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є —В–µ—А–∞–њ–Є—О, –њ–Њ–ї—Г—З–∞–µ–Љ—Г—О –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є –љ–∞ –Љ–Њ–Љ–µ–љ—В –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є, –Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –ї–µ—З–∞—Й–Є—Е –≤—А–∞—З–µ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –≤—Л–њ–Є—Б–Ї–µ.
–Я–∞—Ж–Є–µ–љ—В—Л, –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –≤ 2012 –≥., –Ј–∞–њ–Њ–ї–љ—П–ї–Є –≤–Њ–њ—А–Њ—Б–љ–Є–Ї, —Г—В–Њ—З–љ—П—О—Й–Є–є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –°–Є—А–і–∞–ї—Г–і–∞. –Т —Б–ї—Г—З–∞–µ –µ—Б–ї–Є –њ–∞—Ж–Є–µ–љ—В –љ–µ –њ—А–Є–љ–Є–Љ–∞–ї –њ—А–µ–њ–∞—А–∞—В, —Г—В–Њ—З–љ—П–ї–Є—Б—М –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –њ—А–Є—З–Є–љ—Л –Њ—В–Ї–∞–Ј–∞ –Њ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞.
–Я—А–Њ—В–Њ–Ї–Њ–ї –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ–і–Њ–±—А–µ–љ —Н—В–Є—З–µ—Б–Ї–Є–Љ –Ї–Њ–Љ–Є—В–µ—В–Њ–Љ –У–С–Ю–£ –Т–Я–Ю «–°–∞—А–∞—В–Њ–≤—Б–Ї–Є–є –У–Ь–£ –Є–Љ. –Т.–Ш. –†–∞–Ј—Г–Љ–Њ–≤—Б–Ї–Њ–≥–Њ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є».
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї—Г—О –Њ–±—А–∞–±–Њ—В–Ї—Г –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ—А–Њ–≥—А–∞–Љ–Љ Microsoft Office Ex—Бel 2007 (Microsoft Corp., –°–®–Р) –Є Statistica 8.0 (StatSoft Inc., –°–®–Р). –•–∞—А–∞–Ї—В–µ—А —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –і–∞–љ–љ—Л—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—В–Њ–і–Њ–Љ –Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї—А–Є—В–µ—А–Є—П –®–∞–њ–Є—А–Њ––£–Є–ї–Ї–∞. –Ю–њ–Є—Б–∞–љ–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, –Є–Љ–µ—О—Й–Є—Е –љ–Њ—А–Љ–∞–ї—М–љ–Њ–µ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –≤ –≤–Є–і–µ M±SD, –≥–і–µ –Ь – —Б—А–µ–і–љ–µ–µ –∞—А–Є—Д–Љ–µ—В–Є—З–µ—Б–Ї–Њ–µ, SD – —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ; –і–ї—П –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ, –Њ—В–ї–Є—З–љ—Л–Љ –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ, —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ –≤–Є–і–µ –Ь–µ [Q1; Q3], –≥–і–µ Me – –Љ–µ–і–Є–∞–љ–∞, Q1 –Є Q3 – –њ–µ—А–≤—Л–є –Є —В—А–µ—В–Є–є –Ї–≤–∞—А—В–Є–ї–Є. –Ф–ї—П –Њ–±—А–∞–±–Њ—В–Ї–Є –і–∞–љ–љ—Л—Е —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —В–Є–њ–Њ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л: t–—В–µ—Б—В –і–ї—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≥—А—Г–њ–њ–Є—А–Њ–≤–Њ–Ї, –њ–∞—А–љ—Л–є t–—В–µ—Б—В. –Я—А–Є —Е–∞—А–∞–Ї—В–µ—А–µ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –і–∞–љ–љ—Л—Е, –Њ—В–ї–Є—З–љ–Њ–Љ –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ, –њ—А–Є–Љ–µ–љ—П–ї–Є –љ–µ–њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л: –Ї—А–Є—В–µ—А–Є–є –Ь–∞–љ–љ–∞––£–Є—В–љ–Є, –Ї—А–Є—В–µ—А–Є–є –Т–∞–ї—М–і–∞––Т–Њ–ї—М—Д–Њ–≤–Є—Ж–∞, –Ї—А–Є—В–µ—А–Є–є χ2, –Ї—А–Є—В–µ—А–Є–є –Т–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞, –Ї—А–Є—В–µ—А–Є–є –Ј–љ–∞–Ї–Њ–≤. –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є –±–Њ–ї–µ–µ —З–µ–Љ –і–≤—Г—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≥—А—Г–њ–њ–Є—А–Њ–≤–Њ–Ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Љ–µ—В–Њ–і—Л –і–Є—Б–њ–µ—А—Б–Є–Њ–љ–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞: –њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–є –і–Є—Б–њ–µ—А—Б–Є–Њ–љ–љ—Л–є –∞–љ–∞–ї–Є–Ј –і–ї—П –љ–Њ—А–Љ–∞–ї—М–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –Є —А–∞–љ–≥–Њ–≤—Л–є –∞–љ–∞–ї–Є–Ј –≤–∞—А–Є–∞—Ж–Є–є –њ–Њ –Ъ—А–∞—Б–Ї–µ–ї—Г––£–Њ–ї–ї–Є—Б—Г –і–ї—П –і–∞–љ–љ—Л—Е —Б —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ, –Њ—В–ї–Є—З–љ—Л–Љ –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ.
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–° (2010 –≥.) —Б–Њ—Б—В–∞–≤–Є–ї 42,63±10,95 –≥–Њ–і–∞, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П – 14,91±8,4 –≥–Њ–і–∞, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–µ–љ 81 –Љ—Г–ґ—З–Є–љ–∞ (84,75%). –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Љ–µ–ї–Є –≤—Л—Б–Њ–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (—Г 85 (89,4%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ BASDAI≥4), –°––†–С – 19,44 [2,2; 36,2] –Љ–≥/–ї, –°–Ю–≠ – 20 [14; 26] –Љ–Љ/—З. –Т 2010 –≥. 79 (82,2%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –∞ –≤ 2012 –≥. – 8 (40%) –±–Њ–ї—М–љ—Л—Е –њ–Њ—Б—В–Њ—П–љ–љ–Њ –њ—А–Є–љ–Є–Љ–∞–ї–Є –°–Є—А–і–∞–ї—Г–і –±–Њ–ї–µ–µ 1 –≥–Њ–і–∞, p<0,05. –Ш–Ј 12 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (2012 –≥.), –љ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –њ—А–µ–њ–∞—А–∞—В, 9 –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–µ–њ–∞—А–∞—В –љ–µ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤—А–∞—З–Њ–Љ, 2 –Њ—В–Ї–∞–Ј–∞–ї–Є—Б—М –Њ—В –њ—А–Є–µ–Љ–∞ –Є–Ј––Ј–∞ —Б–љ–Є–ґ–µ–љ–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Љ–µ–љ–µ–µ 100/80 –Љ–Љ —А—В. —Б—В., 1 –њ–∞—Ж–Є–µ–љ—В – –Є–Ј––Ј–∞ «–Њ—В—Б—Г—В—Б—В–≤–Є—П» —Н—Д—Д–µ–Ї—В–∞.
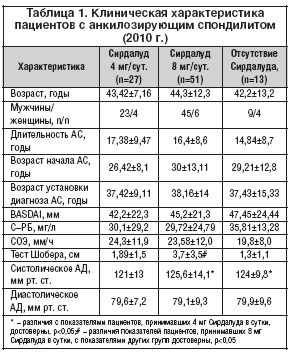
–Ш–Ј 96 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (2010 –≥.) 27 –±–Њ–ї—М–љ—Л—Е –њ—А–Є–љ–Є–Љ–∞–ї–Є –°–Є—А–і–∞–ї—Г–і 4 –Љ–≥/—Б—Г—В., 51 – 8 –Љ–≥/—Б—Г—В., 1 – 12 –Љ–≥/—Б—Г—В., 13 – –љ–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є –њ—А–µ–њ–∞—А–∞—В (–љ–µ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤—А–∞—З–Њ–Љ). –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –≤—Л–њ–Є—Б–Њ–Ї –Є–Ј –Є—Б—В–Њ—А–Є–є –±–Њ–ї–µ–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2010 –≥. —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –±–Њ–ї—М–љ—Л–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є –њ—А–µ–њ–∞—А–∞—В –≤ —В–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–µ, –≤ –Ї–Њ—В–Њ—А–Њ–є –њ—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –Є—Б—Е–Њ–і–љ–Њ (—В–Є—В—А–Њ–≤–∞–љ–Є–µ –і–Њ–Ј—Л –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–ї–Њ—Б—М). –Я–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ 4 –Є 8 –Љ–≥ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —Б—Г—В–Ї–Є, –Є –њ–∞—Ж–Є–µ–љ—В—Л, –љ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤, –љ–µ —А–∞–Ј–ї–Є—З–∞–ї–Є—Б—М –њ–Њ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (—В–∞–±–ї. 1), –Є–Љ–µ–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Г—О —В–µ—А–∞–њ–Є—О –Э–Я–Т–Я –Є —Б—Е–Њ–і–љ—Г—О –±–∞–Ј–Є—Б–љ—Г—О —В–µ—А–∞–њ–Є—О. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –љ–∞–Љ –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ—Л–Љ–Є: –°–Є—А–і–∞–ї—Г–і —П–≤–ї—П–µ—В—Б—П –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–Љ –Є –љ–µ –Њ–±–ї–∞–і–∞–µ—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, —З–µ–Љ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –њ—А–µ–њ–∞—А–∞—В –≤ —А–∞–Ј–љ—Л—Е –і–Њ–Ј–∞—Е, –Є —Г –љ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –µ–≥–Њ. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —В—А–µ—Е –≥—А—Г–њ–њ –≤ —Г—А–Њ–≤–љ–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–Р–Ф): –њ–∞—Ж–Є–µ–љ—В—Л —Б –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф –њ—А–Є–љ–Є–Љ–∞–ї–Є –°–Є—А–і–∞–ї—Г–і 4 –Љ–≥/—Б—Г—В., —Б –±–Њ–ї—М—И–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –Р–Ф – 8 –Љ–≥/—Б—Г—В. (—В–∞–±–ї. 1). –§–∞–Ї—В –љ–∞–ї–Є—З–Є—П –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Њ–≥–Њ –Р–Ф —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ–љ—М—И–µ–є –і–Њ–Ј–Њ–є –°–Є—А–і–∞–ї—Г–і–∞, –≤–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ, –Њ–±—К—П—Б–љ—П–µ—В—Б—П —В–µ–Љ, —З—В–Њ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–Є–њ–Њ—В–Њ–љ–Є–µ–є –≤—А–∞—З–Є –≤—Л–±–Є—А–∞–ї–Є –Љ–µ–љ—М—И–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞.
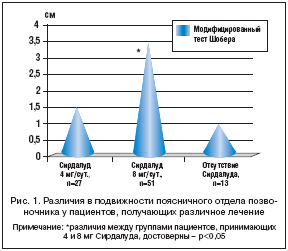
–Э–∞–ї–Є—З–Є–µ –≤–ї–Є—П–љ–Є—П –°–Є—А–і–∞–ї—Г–і–∞ –љ–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Б–њ–∞–Ј–Љ–∞ —Б–Ї–µ–ї–µ—В–љ–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —Д—Г–љ–Ї—Ж–Є—О –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —А–∞–Ј–љ—Л–µ –і–Њ–Ј—Л –°–Є—А–і–∞–ї—Г–і–∞. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –°–Є—А–і–∞–ї—Г–і –≤ –і–Њ–Ј–∞—Е 4 –Є 8 –Љ–≥/—Б—Г—В., —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –Ј–љ–∞—З–Є–Љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ (–Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–є —В–µ—Б—В –®–Њ–±–µ—А–∞) (—А–Є—Б. 1). –†–∞–Ј–ї–Є—З–Є–є –≤ –±–Њ–Ї–Њ–≤–Њ–є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –Є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є —И–µ–є–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ. –Э–∞—Б–Ї–Њ–ї—М–Ї–Њ –Ј–љ–∞—З–Є–Љ—Л–Љ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞ —П–≤–ї—П–µ—В—Б—П –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –њ–Њ–Ї–∞–Ј–∞–љ–Њ –≤ –њ—А–Є–Љ–µ—А–∞—Е –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1.
–Я–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ –°–Є—А–і–∞–ї—Г–і 8 –Љ–≥/—Б—Г—В., —З–∞—Й–µ, —З–µ–Љ –њ–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ 4 –Љ–≥/—Б—Г—В., –Њ—В–Ї–∞–Ј—Л–≤–∞–ї–Є—Б—М –Њ—В –њ—А–Є–µ–Љ–∞ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤: 5 (50%) –Є 2 (20%) —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, p<0,05.
–Я—А–Є —Н—В–Њ–Љ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ –∞–љ–∞–ї–Є–Ј–∞—Е –Ї—А–Њ–≤–Є –Є –Љ–Њ—З–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–°, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —А–∞–Ј–ї–Є—З–љ—Л–µ –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –°–Є—А–і–∞–ї—Г–і–∞, –Є –љ–µ –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е –њ—А–µ–њ–∞—А–∞—В, –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ.
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Ю—Б–љ–Њ–≤–љ–Њ–є —Ж–µ–ї—М—О –ї–µ—З–µ–љ–Є—П –Р–°, —Б–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ ASAS/EULAR (Assessment of Spondyloarthritis International Society/European Lique Against Rheumatism), —П–≤–ї—П–µ—В—Б—П –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –і–Њ–ї–≥–Њ–µ —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–∞ –њ—Г—В–µ–Љ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞–і –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ, –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Њ–њ–Њ—А–љ–Њ––і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞, –∞ —В–∞–Ї–ґ–µ —Б–Њ—Е—А–∞–љ–µ–љ–Є—П/–љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–∞ –Є –µ–≥–Њ —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –∞–і–∞–њ—В–∞—Ж–Є–Є [20]. –Ф–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Н—В–Њ–є —Ж–µ–ї–Є –≤—Л–Ј—Л–≤–∞–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —Б–ї–Њ–ґ–љ–Њ—Б—В–Є, —В–∞–Ї –Ї–∞–Ї –њ–∞—Ж–Є–µ–љ—В—Л —Б –Р–° –Є–Ј––Ј–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П —Б–Є–љ–і–µ—Б–Љ–Њ—Д–Є—В–Њ–≤ –Є –і–µ—Д–Њ—А–Љ–∞—Ж–Є–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —З–∞—Б—В–Њ –Є—Б–њ—Л—В—Л–≤–∞—О—В –±–Њ–ї—М –≤ —Б–њ–Є–љ–µ –љ–µ —В–Њ–ї—М–Ї–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ, –љ–Њ –Є –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –Љ–Є–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞, –∞, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –і–ї—П —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –≤ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Њ–і–љ–Њ–є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±—Л–≤–∞–µ—В –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Б–∞–Љ—Л—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї—Г–њ–Є—А—Г—О—Й–Є—Е –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –≤–Ї–ї—О—З–∞—П –≥–µ–љ–љ–Њ––Є–љ–ґ–µ–љ–µ—А–љ—Л–µ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –∞–≥–µ–љ—В—Л, –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є–≥–љ—Г—В—М –Њ—В–≤–µ—В–∞ ASAS40 —В–Њ–ї—М–Ї–Њ —Г 40% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ c –Р–° [21–24]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–є –њ–Њ–і—Е–Њ–і –Ї –ї–µ—З–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –±–Њ–ї—М—О –≤ —Б–њ–Є–љ–µ.
–Ф–ї—П –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–° —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є —З–∞—Б—В–Њ –љ–∞–Ј–љ–∞—З–∞—О—В –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В—Л. –Ш–љ—В–µ—А–µ—Б–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –і–Њ–Ј—Л –°–Є—А–і–∞–ї—Г–і–∞ –Њ—В 2 –і–Њ 36 –Љ–≥/—Б—Г—В., –∞ –≤ –Є–љ—Б—В—А—Г–Ї—Ж–Є–Є –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –њ—А–µ–њ–∞—А–∞—В–∞ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М –°–Є—А–і–∞–ї—Г–і –≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–µ 2–6 –Љ–≥/—Б—Г—В., –њ–Њ—Б–ї–µ —З–µ–≥–Њ –≤—Л–њ–Њ–ї–љ—П—В—М —В–Є—В—А–Њ–≤–∞–љ–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ —Б —Г—З–µ—В–Њ–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є [12]. –Т —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–ї—Г—З–∞—О—В, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —Б—В–∞–±–Є–ї—М–љ—Г—О –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞ –±–µ–Ј –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ —В–Є—В—А–Њ–≤–∞–љ–Є—П. –Т –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–∞–Љ–Є –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–° —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –°–Є—А–і–∞–ї—Г–і–∞ –і–∞–ґ–µ –≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е –і–Њ–Ј–∞—Е –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є—З—М –ї—Г—З—И–Є—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤, —З–µ–Љ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Э–Я–Т–Я, –∞ —Б–∞–Љ–∞ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є.
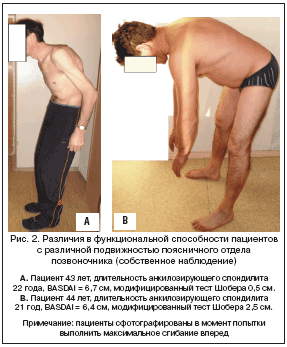
–Э–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–ї—П–µ—В—Б—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ –°–Є—А–і–∞–ї—Г–і –≤ –±–Њ–ї—М—И–µ–є (8 –Љ–≥/—Б—Г—В.) –і–Њ–Ј–Є—А–Њ–≤–Ї–µ, –Є–Љ–µ—О—В –±–Њ–ї—М—И—Г—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, —З–µ–Љ –њ–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–Љ–µ–љ—П–≤—И–Є–µ 4 –Љ–≥/—Б—Г—В., –њ—А–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Я–∞—Ж–Є–µ–љ—В—Л, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ –°–Є—А–і–∞–ї—Г–і –≤ –і–Њ–Ј–Є—А–Њ–≤–Ї–µ 4 –Љ–≥/—Б—Г—В., –Є–Љ–µ–ї–Є –ї—Г—З—И—Г—О –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, —З–µ–Љ –њ–∞—Ж–Є–µ–љ—В—Л, –љ–µ –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–µ –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В—Л –≤–Њ–Њ–±—Й–µ, —Е–Њ—В—П —А–∞–Ј–ї–Є—З–Є—П –Є –љ–µ –і–Њ—Б—В–Є–≥–ї–Є —Б—В–µ–њ–µ–љ–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є. –Ю–≥—А–∞–љ–Є—З–µ–љ–Є–µ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Р–° (—А–Є—Б. 2). –Э–∞—А—Г—И–µ–љ–Є–µ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –Є –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е [25]. –Ф–∞–љ–љ–Њ–µ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Ї–∞–Ї –љ–µ–Њ–±—А–∞—В–Є–Љ—Л–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –≤ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–µ (–∞–љ–Ї–Є–ї–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ), —В–∞–Ї –Є –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Є —Б–њ–∞–Ј–Љ–Њ–Љ. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, —З—В–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ –Є —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ—П—В—М —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ–Љ –±–Њ–ї—М—И–µ–є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —Г –ї–Є—Ж, –і–ї–Є—В–µ–ї—М–љ–Њ –њ—А–Є–Љ–µ–љ—П–≤—И–Є—Е –±–Њ–ї—М—И—Г—О –і–Њ–Ј—Г –°–Є—А–і–∞–ї—Г–і–∞, –Є —П–≤–ї—П—В—М—Б—П –Њ–і–љ–Є–Љ –Є–Ј —Д–∞–Ї—В–Њ—А–Њ–≤, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є—Е –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–Њ—Е—А–∞–љ–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ–Њ–≥–Њ –Р–°, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Њ—Б–љ–Њ–≤–љ–Њ–є —Ж–µ–ї–Є –µ–≥–Њ –ї–µ—З–µ–љ–Є—П [20]. –Ш–љ—В–µ—А–µ—Б–љ–Њ, —З—В–Њ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –°–Є—А–і–∞–ї—Г–і–∞ 8 –Љ–≥/—Б—Г—В. –њ–∞—Ж–Є–µ–љ—В—Л —З–∞—Й–µ –Њ—В–Ї–∞–Ј—Л–≤–∞–ї–Є—Б—М –Њ—В –њ—А–Є–µ–Љ–∞ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤, —З–µ–Љ –њ—А–Є –њ—А–Є–µ–Љ–µ 4 –Љ–≥/—Б—Г—В., —З—В–Њ –Ї–Њ—Б–≤–µ–љ–љ–Њ —Б–Њ–≥–ї–∞—Б—Г–µ—В—Б—П —Б –і–∞–љ–љ—Л–Љ–Є Gorska J. —Б —Б–Њ–∞–≤—В. [5], –њ–Њ–Ї–∞–Ј–∞–≤—И–Є—Е, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –°–Є—А–і–∞–ї—Г–і–∞ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї—М—О –≤ —Б–њ–Є–љ–µ –≤ –Э–Я–Т–Я.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ј–∞ –њ–µ—А–Є–Њ–і —Б 2010 –њ–Њ 2012 –≥. –љ–∞–Љ–µ—В–Є–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–∞—Б—В–Њ—В—Л –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤ –±–Њ–ї—М–љ—Л–Љ –Р–°, –њ—А–Є—З–Є–љ–∞ –Ї–Њ—В–Њ—А–Њ–є –љ—Г–ґ–і–∞–µ—В—Б—П –≤ –Њ—В–і–µ–ї—М–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ. –Ю–і–љ–Њ–є –Є–Ј –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –њ—А–Є—З–Є–љ —В–∞–Ї–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ —З–µ—В–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –ї–µ—З–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≤ —Б–њ–Є–љ–µ –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–∞–Љ–Є. –Т —Б–≤—П–Ј–Є —Б –≤—Л—И–µ—Б–Ї–∞–Ј–∞–љ–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ –≤—Л–њ–Њ–ї–љ–µ–љ–Є–µ –і–∞–ї—М–љ–µ–є—И–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е –Р–°. –Ф–ї—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П –≤–∞–ґ–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –Њ—В–≤–µ—В—Л –љ–∞ –≤–Њ–њ—А–Њ—Б—Л:
1. –Ъ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Є–Ј–Љ–µ–љ–Є—В—Б—П —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –њ–Њ–ї—М–Ј–∞/—А–Є—Б–Ї –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –і–Њ–Ј—Л –°–Є—А–і–∞–ї—Г–і–∞ –±–Њ–ї–µ–µ 8 –Љ–≥/—Б—Г—В. —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –±–Њ–ї—М—О –≤ —Б–њ–Є–љ–µ?
2. –Ш–Љ–µ–µ—В –ї–Є –њ–Њ—Б—В–Њ—П–љ–љ—Л–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –њ–µ—А–µ–і –њ—А–µ—А—Л–≤–Є—Б—В—Л–Љ –њ—А–Є–µ–Љ–Њ–Љ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —А–∞–Ј –≤ –≥–Њ–і?
3. –Ъ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –і–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –Є –Ї–∞—З–µ—Б—В–≤–Њ–Љ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е –Р–°?
4. –Э–∞—Б–Ї–Њ–ї—М–Ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ—А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–Љ –∞–Ї—Б–Є–∞–ї—М–љ—Л–Љ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–Љ?
–Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, —З—В–Њ –Њ—В–≤–µ—В—Л –љ–∞ –њ–Њ—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –≤–Њ–њ—А–Њ—Б—Л –Љ–Њ–≥—Г—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —Б–Њ–Ј–і–∞–љ–Є—О —З–µ—В–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –°–Є—А–і–∞–ї—Г–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–°.
–Т—Л–≤–Њ–і—Л
1. –Ю—В 40 –і–Њ 82,2% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–° –і–ї–Є—В–µ–ї—М–љ–Њ –њ—А–Є–љ–Є–Љ–∞—О—В —В–Є–Ј–∞–љ–Є–і–Є–љ (–°–Є—А–і–∞–ї—Г–і).
2. –Э–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ —А–µ–ґ–Є–Љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –°–Є—А–і–∞–ї—Г–і–∞ —П–≤–ї—П–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–Є—А–Њ–≤–Ї–µ 4 –Є–ї–Є 8 –Љ–≥/—Б—Г—В. –≤ 2 –њ—А–Є–µ–Љ–∞.
3. –Т —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —А–µ–і–Ї–Њ –њ—А–Њ–≤–Њ–і–Є—В—Б—П —В–Є—В—А–Њ–≤–∞–љ–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Р–°.
4. –Я—А–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–ї–Є—В–µ–ї—М–љ–Њ–µ (–±–Њ–ї–µ–µ 1 –≥–Њ–і–∞) –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –°–Є—А–і–∞–ї—Г–і–∞ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 8 –Љ–≥/—Б—Г—В. –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–Њ–ї—М—И–µ–є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, —З–µ–Љ –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –і–Њ–Ј–µ 4 –Љ–≥/—Б—Г—В.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. ed. –†–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П. –Ь.: –У–Х–Ю–Ґ–Р–†––Ь–µ–і–Є–∞, 2005.
2. Van der Linden S., Valkenburg H.A., Cats A. Evaluation of diagnostic criteria for ankylosing spondylitis. A proposal for modification of the New York criteria // Arthritis Rheum. 1984 Apr. Vol. 27 (4). –†. 361–368.
3. Rozenberg S. [Chronic low back pain: definition and treatment] // Rev Prat. 2008 Feb 15. Vol. 58 (3). –†. 265–272.
4. Brattwall M., Turan I., Jakobsson J. Musculoskeletal pain: prescription of NSAID and weak opioid by primary health care physicians in Sweden 2004–2008 – a retrospective patient record review // J Pain Res. 2010. Vol. 3. –†. 131–135.
5. Gorska J. [Effects of back pain treatment with tizanidine] // Ortop Traumatol Rehabil. 2005 Jun 30. Vol. 7 (3). –†. 306–309.
6. Nance P.W., Bugaresti J., Shellenberger K., Sheremata W., Martinez–Arizala A. Efficacy and safety of tizanidine in the treatment of spasticity in patients with spinal cord injury.North American Tizanidine Study Group Neurology. 1994 Nov. Vol. 44 (11 Suppl 9). –†. 44–51; discussion 51–42.
7. Iakhno N.N., Damulin I.V., Chernenko O.A., Ianakaeva T.A., Kondrat'eva O.N., Kur'ianova P.T. [The efficacy of sirdalud in the drug therapy of pain in the spine] // Terapevticheskii arkhiv. 1994. Vol. 66 (10). –†. 10–12.
8. Damulin I.V. [The use of sirdalud in painful muscle tonic syndromes] // Terapevticheskii arkhiv. 1997. Vol. 69 (10). –†. 68–72.
9. Kamen L., Henney H.R., 3rd, Runyan J.D. A practical overview of tizanidine use for spasticity secondary to multiple sclerosis, stroke, and spinal cord injury // Current medical research and opinion. 2008 Feb. Vol. 24 (2). –†. 425–439.
10. Malanga G., Reiter R.D., Garay E. Update on tizanidine for muscle spasticity and emerging indications // Expert Opin Pharmacother. 2008 Aug. Vol. 9 (12). –†. 2209–2215.
11. Groves L., Shellenberger M.K., Davis C.S. Tizanidine treatment of spasticity: a meta–analysis of controlled, double–blind, comparative studies with baclofen and diazepam // Adv Ther. 1998 Jul–Aug. Vol. 15 (4). –†. 241–251.
12. Wagstaff A.J., Bryson H.M. Tizanidine. A review of its pharmacology, clinical efficacy and tolerability in the management of spasticity associated with cerebral and spinal disorders // Drugs. 1997 Mar. Vol. 53 (3). –†. 435–452.
13. Ketenci A., Ozcan E., Karamursel S. Assessment of efficacy and psychomotor performances of thiocolchicoside and tizanidine in patients with acute low back pain // Int J Clin Pract. 2005 Jul. Vol. 59 (7). –†. 764–770.
14. Berry H., Hutchinson D.R. Tizanidine and ibuprofen in acute low–back pain: results of a double–blind multicentre study in general practice // J Int Med Res. 1988 Mar–Apr. Vol. 16 (2). –†. 83–91.
15. Berry H., Hutchinson D.R. A multicentre placebo–controlled study in general practice to evaluate the efficacy and safety of tizanidine in acute low–back pain // J Int Med Res. 1988 Mar–Apr. Vol. 16 (2). –†. 75–82.
16. Pareek A., Chandurkar N., Chandanwale A.S., Ambade R., Gupta A., Bartakke G. Aceclofenac–tizanidine in the treatment of acute low back pain: a double–blind, double–dummy, randomized, multicentric, comparative study against aceclofenac alone // European spine journal : official publication of the European Spine Society, the European Spinal Deformity Society, and the European Section of the Cervical Spine Research Society. 2009 Dec. Vol. 18 (12). –†. 1836–1842.
17. White A.P., Arnold P.M., Norvell D.C., Ecker E., Fehlings M.G. Pharmacologic management of chronic low back pain: synthesis of the evidence // Spine. 2011 Oct 1. Vol. 36 (21 Suppl). –†. 131–143.
18. Garrett S., Jenkinson T., Kennedy L.G., Whitelock H., Gaisford P., Calin A. A new approach to defining disease status in ankylosing spondylitis: the Bath Ankylosing Spondylitis Disease Activity Index // J Rheumatol. 1994 Dec. Vol. 21 (12). –†. 2286–2291.
19. Sieper J., Rudwaleit M., Baraliakos X., Brandt J., Braun J., Burgos–Vargas R. et al. The Assessment of SpondyloArthritis international Society (ASAS) handbook: a guide to assess spondyloarthritis // Ann Rheum Dis. 2009 Jun. Vol. 68. Suppl 2. –†. 1–44.
20. Zochling J., van der Heijde D., Burgos–Vargas R., Collantes E., Davis J.C., Jr., Dijkmans B. et al. ASAS/EULAR recommendations for the management of ankylosing spondylitis // Ann Rheum Dis. 2006 Apr. Vol. 65 (4). –†. 442–452.
21. Van der Heijde D, Dijkmans B, Geusens P, Sieper J, DeWoody K, Williamson P, et al. Efficacy and safety of infliximab in patients with ankylosing spondylitis: results of a randomized, placebo–controlled trial (ASSERT) // Arthritis and rheumatism. 2005 Feb. Vol. 52 (2). –†. 582–591.
22. Van der Heijde D., Kivitz A., Schiff M.H., Sieper J., Dijkmans B.A., Braun J. et al. Efficacy and safety of adalimumab in patients with ankylosing spondylitis: Results of a multicenter, randomized, double–blind, placebo–controlled trial // Arthritis Rheum. 2006 Jun 26. Vol. 54 (7). –†. 2136–2146.
23. Davis J.C., van der Heijde D.M., Braun J., Dougados M., Cush J., Clegg D. et al. Sustained durability and tolerability of etanercept in ankylosing spondylitis for 96 weeks // Ann Rheum Dis. 2005 Nov. Vol. 64 (11). –†. 1557–1562.
24. Rudwaleit M., Claudepierre P., Wordsworth P., Cortina E.L., Sieper J., Kron M. et al. Effectiveness, safety, and predictors of good clinical response in 1250 patients treated with adalimumab for active ankylosing spondylitis // J Rheumatol. 2009 Apr. Vol. 36 (4). –†. 801–808.
25. Scholich S.L., Hallner D., Wittenberg R.H., Hasenbring M.I., Rusu A.C. The relationship between pain, disability, quality of life and cognitive–behavioural factors in chronic back pain // Disabil Rehabil. 2012. Vol. 34 (23). –†. 1993–2000.












