–Ю–і–љ–Њ–є –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л—Е –Є —Б–ї–Њ–ґ–љ—Л—Е –Ј–∞–і–∞—З, —Б—В–Њ—П—Й–Є—Е –њ–µ—А–µ–і –≤—А–∞—З–Њ–Љ–—А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Њ–Љ, —П–≤–ї—П–µ—В—Б—П –≤—Л–±–Њ—А —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –і–ї—П –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –њ–Њ—Б–ї–µ–і–љ–Є—Е –њ–Њ—Б—В–Њ—П–љ–љ–Њ —А–∞—Б—В–µ—В, –Є –Њ–±—Й–µ–µ —З–Є—Б–ї–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –Ї–Њ—Б—В–љ–Њ–—Б—Г—Б—В–∞–≤–љ–Њ––Љ—Л—И–µ—З–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –і–Њ—Б—В–Є–≥–ї–Њ –≤ 2000 –≥. 12,7 –Љ–ї–љ. —З–µ–ї–Њ–≤–µ–Ї. –Я—А–Є —Н—В–Њ–Љ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ–Њ—А–∞–ґ–∞–µ–Љ–Њ—Б—В—М –≤—Б–µ—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ –љ–∞—Б–µ–ї–µ–љ–Є—П: –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤, –ї—О–і–µ–є –Ј—А–µ–ї–Њ–≥–Њ, –њ–Њ–ґ–Є–ї–Њ–≥–Њ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є (–∞—А—В—А–Є—В—Л, —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В—Л, —Б–Є—Б—В–µ–Љ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є) –Є –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ––і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Њ–њ–Њ—А–љ–Њ––і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ (–Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј—Л, —Б–њ–Њ–љ–і–Є–ї–µ–Ј—Л, –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј –Є –і—А.). –Ф–ї—П –≤—Б–µ—Е –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Е–∞—А–∞–Ї—В–µ—А–љ—Л —А–∞–Ј–љ–Њ–є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –њ—А–Є–Ј–љ–∞–Ї–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ —Б—Г—Б—В–∞–≤–∞—Е –Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–µ —Б –±–Њ–ї—П–Љ–Є –Є –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —Д—Г–љ–Ї—Ж–Є–Є –≤ —Н—В–Є—Е —Б—В—А—Г–Ї—В—Г—А–∞—Е. –Х—Б–ї–Є –љ–∞–ї–Є—З–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–Љ –∞—А—В—А–Є—В–µ (–†–Р) –Є –і—А—Г–≥–Є—Е –∞—А—В—А–Є—В–∞—Е, —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–∞—Е –Є —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–њ–∞—В–Є—П—Е –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–Њ–Љ–љ–µ–љ–Є—П, –Ї–∞–Ї –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —А–∞–љ–љ–µ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Э–Я–Т–Я), —В–Њ –њ—А–Є –Њ—Б—В–µ–Њ–∞—А—В—А–Є—В–∞—Е (–Ю–Р) –≤—Б–µ –µ—Й–µ –љ–µ —А–µ—И–µ–љ –≤–Њ–њ—А–Њ—Б –Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є —А–∞–љ–љ–µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Э–Я–Т–Я –њ—А–Є –±–Њ–ї—П—Е –≤ –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–∞—Е. –Ю–і–љ–∞–Ї–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л —Б—В–∞–ї–Є –≤—Л–і–µ–ї—П—В—М –Њ—Б–Њ–±—Л–є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є —Д–µ–љ–Њ—В–Є–њ –Ю–Р, –і–ї—П –Ї–Њ—В–Њ—А–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–љ—Л –Њ—В—З–µ—В–ї–Є–≤—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П – –љ–∞–ї–Є—З–Є–µ –ґ–Є–і–Ї–Њ—Б—В–Є –≤ –њ–Њ–ї–Њ—Б—В–Є –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞, –љ–Њ—З–љ–Њ–є —Е–∞—А–∞–Ї—В–µ—А –±–Њ–ї–µ–є –Є –љ–µ–њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–∞—П —Г—В—А–µ–љ–љ—П—П —Б–Ї–Њ–≤–∞–љ–љ–Њ—Б—В—М. –Я—А–Є —Н—В–Њ–Љ —В–Є–њ–µ –Ю–Р –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Э–Я–Т–Я –љ–∞–Є–±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–Њ (F. Wolfe —Б —Б–Њ–∞–≤—В., 2000).
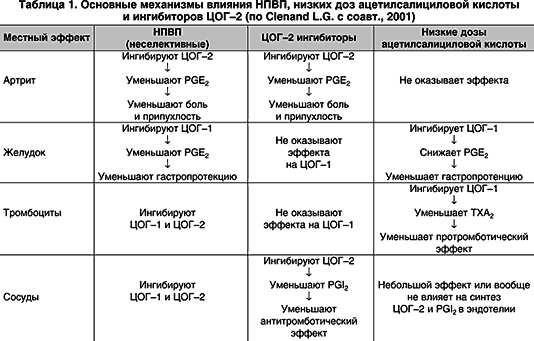
–Ю–±—Й–Є–Љ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Э–Я–Т–Я —П–≤–ї—П–µ—В—Б—П –Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ —Г—Б—В—А–∞–љ–µ–љ–Є–Є –±–Њ–ї–Є –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –њ–Њ–і–∞–≤–ї—П—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л – –Ї–ї—О—З–µ–≤–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ –њ—А–µ–≤—А–∞—Й–µ–љ–Є—П –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ—Л (—В–∞–±–ї. 1). –Ч–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е, –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ –±–ї–Њ–Ї–Є—А—Г—О—Й–µ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–є —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л–1 (–¶–Ю–У–1), –≤—Б–µ –љ–µ–∞—Б–њ–Є—А–Є–љ–Њ–≤—Л–µ –Э–Я–Т–Я –Њ–±—А–∞—В–Є–Љ–Њ –±–ї–Њ–Ї–Є—А—Г—О—В –і–Њ—Б—В—Г–њ—Л –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤ –∞–Ї—В–Є–≤–љ—Л–є —Б–∞–є—В, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–є –≤ –≤–µ—А—Е–љ–µ–є —З–∞—Б—В–Є –≥–Є–і—А–Њ—Д–Њ–±–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –≤–љ—Г—В—А–Є –¶–Ю–У–1 –Є –¶–Ю–У–2 —Д–µ—А–Љ–µ–љ—В–Њ–≤. –Р –љ–Њ–≤—Л–µ – —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Э–Я–Т–Я –±–ї–Њ–Ї–Є—А—Г—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Є–ї–Є –Є—Б–Ї–ї—О—З–Є—В–µ–ї—М–љ–Њ (—Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) –¶–Ю–У–2. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Д–∞—А–Љ–∞–Ї–Њ–і–Є–љ–∞–Љ–Є–Ї–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –Э–Я–Т–Я (–љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–ї–Є —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е) –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—Ж–Є–Є –¶–Ю–У —Д–µ—А–Љ–µ–љ—В–Њ–≤ –≤–µ—Б—М–Љ–∞ –≤–∞—А–Є–∞–±–µ–ї—М–љ–∞ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–Њ–є (Fitz–Gerald Y.A., –†atrono C., 2001). –Э–∞–њ—А–Є–Љ–µ—А, –Ї–Њ–Ї—Б–Є–±—Л (—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2) –Њ–±–ї–∞–і–∞—О—В —Б—В—А—Г–Ї—В—Г—А–Њ–є, –Ї–Њ—В–Њ—А–∞—П –њ–Њ–і—Е–Њ–і–Є—В –Ї –±–Њ–ї—М—И–Њ–Љ—Г –≥–Є–і—А–Њ—Д–Њ–±–љ–Њ–Љ—Г –Ї–∞–љ–∞–ї—Г –¶–Ю–У–2. –Э–∞–њ—А–Њ—В–Є–≤, –∞—Ж–µ—В–∞–Љ–Є–љ–Њ—Д–µ–љ –љ–µ –Њ–±–ї–∞–і–∞–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –±–ї–Њ–Ї–Є—А–Њ–≤–∞—В—М –≥–Є–і—А–Њ—Д–Њ–±–љ—Л–µ –Ї–∞–љ–∞–ї—Л –Њ–±–Њ–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, –∞ —Б–љ–Є–ґ–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ–Ї–Є—Б–ї–µ–љ–љ—Л—Е —Д–Њ—А–Љ –Њ–±–Њ–Є—Е –¶–Ю–У–—Д–µ—А–Љ–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –ї–Њ–Ї–∞–ї–Є–Ј—Г—О—В—Б—П –≤ –¶–Э–° –Є –≤ —Б–њ–Є–љ–љ–Њ–Љ –Љ–Њ–Ј–≥—Г –Є –і–ї—П –Ї–Њ—В–Њ—А—Л—Е —Е–∞—А–∞–Ї—В–µ—А–љ—Л –љ–Є–Ј–Ї–Њ–њ–µ—А–Њ–Ї—Б–Є–і–љ—Л–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –¶–Ю–У (Ouellet M., Percival M.D., 2001).
–°–ї–Њ–ґ–љ–Њ—Б—В—М –≤—Л–±–Њ—А–∞ –ї–µ—З–µ–±–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В–∞–Ї–ґ–µ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –Њ—З–µ–≤–Є–і–љ–Њ–є –њ—А–Є —Б–Є—Б—В–µ–Љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, —Б–Њ—З–µ—В–∞—О—Й–Є—Е—Б—П —Б –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ. Crofford J. —Б —Б–Њ–∞–≤—В. (2000) –Њ–њ–Є—Б–∞–ї–Є 4–—Е –±–Њ–ї—М–љ—Л—Е, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –і–≤–Њ–µ —Б—В—А–∞–і–∞–ї–Є —Б–Є—Б—В–µ–Љ–љ–Њ–є –Ї—А–∞—Б–љ–Њ–є –≤–Њ–ї—З–∞–љ–Ї–Њ–є —Б —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –∞ –і–≤–Њ–µ –і—А—Г–≥–Є—Е – –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ (—Г –љ–Є—Е —А–∞–Ј–≤–Є–ї–Є—Б—М —В—А–Њ–Љ–±–Њ–Ј—Л –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–Њ–Љ). –Э–Њ –≤–Њ–њ—А–Њ—Б —В—А–µ–±—Г–µ—В –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П.
–Т –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–Њ–Љ–љ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А—П–Љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г —В—А–Њ–Љ–±–Њ–Ј–∞–Љ–Є –Є –њ—А–Є–µ–Љ–Њ–Љ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ —Б–ї–µ–і—Г–µ—В –њ—А–Є–љ—П—В—М –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ –Ј–∞–Љ–µ—З–∞–љ–Є—П –љ–∞ —Н—В—Г —Б—В–∞—В—М—О Murray R. (2001), –Ї–Њ—В–Њ—А—Л–є –њ–Њ–і—З–µ—А–Ї–Є–≤–∞–µ—В, —З—В–Њ —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –Є –і–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –±—Л–ї–Є —Г–ґ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ – –Ї—Г—А–µ–љ–Є–µ —Г –Њ–і–љ–Њ–є –±–Њ–ї—М–љ–Њ–є, –≤–∞–Ј–Њ—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ –Є –∞–љ—В–Є—В–µ–ї–∞ –Ї –Ї–∞—А–і–Є–Њ–ї–Є–њ–Є–љ—Г —Г –≤—В–Њ—А–Њ–є, –∞ 3–—П –Є 4–—П –±–Њ–ї—М–љ—Л–µ –±—Л–ї–Є —Б –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–Љ –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, –Ї–Њ—В–Њ—А–Њ–Љ—Г —Б–≤–Њ–є—Б—В–≤–µ–љ–љ—Л —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є–µ —В—А–Њ–Љ–±–Њ–Ј—Л, –Є –Њ–љ–Є –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Ф–∞–љ–љ—Л–µ —Н—В–Њ–є –і–Є—Б–Ї—Г—Б—Б–Є–Є, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –Є–љ—В–µ—А–µ—Б–љ—Л –і–ї—П –Ї–ї–Є–љ–Є—Ж–Є—Б—В–∞, –ї–Є—И–љ–Є–є —А–∞–Ј –Њ–±—А–∞—Й–∞—О—В –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —Г–ґ–µ –Є–Ј–≤–µ—Б—В–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞.
–Ч–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В –≤–љ–Є–Љ–∞–љ–Є—П –Є–Ј—Г—З–µ–љ–Є–µ –≤–ї–Є—П–љ–Є—П —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е «–љ–µ–∞—Б–њ–Є—А–Є–љ–Њ–≤—Л—Е» –Э–Я–Т–Я –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л. Ray W.A. —Б —Б–Њ–∞–≤—В. (2002) –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –∞–љ–∞–ї–Є–Ј–∞ 181441 –±–Њ–ї—М–љ–Њ–≥–Њ, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Є —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є –њ—А–Є–љ–Є–Љ–∞—О—Й–Є–µ –Є –љ–µ –њ—А–Є–љ–Є–Љ–∞—О—Й–Є–µ –Э–Я–Т–Я, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –љ–µ–∞—Б–њ–Є—А–Є–љ–Њ–≤—Л–µ, —В.–µ. –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я –љ–µ –Њ–±–ї–∞–і–∞—О—В –Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ (–њ–Њ–і–Њ–±–љ–Њ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–µ –≤ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј–∞—Е) –Є –њ–Њ—Н—В–Њ–Љ—Г –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –і–Њ–ї–ґ–љ—Л –њ—А–Є–љ–Є–Љ–∞—В—М—Б—П —Б–Њ–≤–Љ–µ—Б—В–љ–Њ —Б –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є.
–Э–µ –Љ–µ–љ—М—И–Є–µ —Б–ї–Њ–ґ–љ–Њ—Б—В–Є –≤–Њ–Ј–љ–Є–Ї–∞—О—В –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ —В–µ—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –њ—А–Њ–±–ї–µ–Љ—Л. –Т –љ–µ–і–∞–≤–љ–µ–є –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є Pasej —Б —Б–Њ–∞–≤—В. (2000) –њ–Њ–Ї–∞–Ј–∞–ї–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –Ј–∞—Б—В–Њ–є–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Г –њ–Њ–ґ–Є–ї—Л—Е –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞—О—Й–Є—Е –Ю–Р –Є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є, –њ–Њ –њ–Њ–≤–Њ–і—Г –Ї–Њ—В–Њ—А–Њ–є –Њ–љ–Є –њ—А–Є–љ–Є–Љ–∞—О—В –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л. –Я—А–Њ–±–ї–µ–Љ–∞ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є –Э–Я–Т–Я –Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–∞–Ї –Є –≤–Ј–∞–Є–Љ–Њ–Њ—В–љ–Њ—И–µ–љ–Є–є –Э–Я–Т–Я –Є –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є, —Б—В–∞–ї–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ –∞–Ї—В—Г–∞–ї—М–љ–Њ–є –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я –Љ–Њ–≥—Г—В –Њ—В–Љ–µ–љ—П—В—М —Н—Д—Д–µ–Ї—В –Љ–љ–Њ–≥–Є—Е –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є b––±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –≤ —Б–≤—П–Ј–Є —Б –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ–Љ –¶–Ю–У–1, –Ї–Њ—В–Њ—А–∞—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –і–ї—П –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –Љ–љ–Њ–≥–Є—Е —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –≤–Ї–ї—О—З–∞—П –њ–Њ—З–µ—З–љ–Њ–µ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є–µ. –Э–Њ –≤ —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–є —Н—Д—Д–µ–Ї—В –¶–Ю–У–2 —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –µ—Й–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Є–Ј—Г—З–µ–љ. Whelton A. et al. (2001) –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ (200 –Љ–≥/–і–µ–љ—М) –Є —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ (25 –Љ–≥/—Б—Г—В) –±–Њ–ї–µ–µ —З–µ–Љ —Г 800 –±–Њ–ї—М–љ—Л—Е, —Б—В—А–∞–і–∞–≤—И–Є—Е –Ю–Р –Є –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ–Њ –њ–Њ–≤–Њ–і—Г –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф –њ–Њ–≤—Л—Б–Є–ї–Њ—Б—М —Г 17% –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є —Г 11% –≤ –≥—А—Г–њ–њ–µ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞, –∞ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ – —Г 2,3% –Є 1,5%, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –І–µ—А–µ–Ј 6 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±, —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф –њ–Њ–≤—Л—Б–Є–ї–Њ—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 2,5 –Љ–Љ —А—В.—Б—В. –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ, –∞ –≤ –≥—А—Г–њ–њ–µ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –і–∞–ґ–µ —Б–љ–Є–Ј–Є–ї–Њ—Б—М –љ–∞ 0,5 –Љ–Љ —А—В.—Б—В. –Р–≤—В–Њ—А—Л –њ—А–Є—Е–Њ–і—П—В –Ї –≤—Л–≤–Њ–і—Г –Њ —Б–Њ–≤–Љ–µ—Б—В–Є–Љ–Њ—Б—В–Є –Ї–Њ–Ї—Б–Є–±–Њ–≤ –Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ–і–љ–∞–Ї–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –±—Л–ї–∞ –ї—Г—З—И–µ–є – —А–µ–ґ–µ —А–∞–Ј–≤–Є–≤–∞–ї–Є—Б—М –Њ—В–µ—З–љ—Л–є —Б–Є–љ–і—А–Њ–Љ –Є –і–µ—Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є—П –Р–Ф. –Я–Њ—З—В–Є –њ–Њ–ї–Њ–≤–Є–љ–∞ –±–Њ–ї—М–љ—Л—Е –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е —Б—А–µ–і–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≥–Є–њ–Њ–љ—В–µ–љ–Ј–Є–≤–љ–Њ–≥–Њ —А—П–і–∞ –њ–Њ–ї—Г—З–∞–ї–Є –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ –і–Є—Г—А–µ—В–Є–Ї–Є, –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П, b––±–ї–Њ–Ї–∞—В–Њ—А—Л, –Њ—Б—В–∞–ї—М–љ—Л–µ –њ–∞—Ж–Є–µ–љ—В—Л –≤ –Ї–∞–ґ–і–Њ–є –≥—А—Г–њ–њ–µ (48,5% –Є 44,9%, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± –Є —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±) –њ–Њ–ї—Г—З–∞–ї–Є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Г—О —В–µ—А–∞–њ–Є—О –Є –±–Њ–ї–µ–µ —В—А–µ—В–Є (37,9% –Є 37,1%) –≤ –Ї–∞–ґ–і–Њ–є –≥—А—Г–њ–њ–µ – –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б–Њ–≤–Љ–µ—Б—В–Є–Љ–Њ—Б—В—М —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У–2 —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Є–ї–Є –Є—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П–Љ–Є, –Ї–∞–Ї –Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –њ—А–Є –љ–∞–ї–Є—З–Є–Є —А–Є—Б–Ї–∞ —В—А–Њ–Љ–±–Њ–Ј–Њ–≤. –Э–Њ –≤—Б–µ –ґ–µ –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–і–Њ–ї–ґ–Є—В—М, –њ—А–Њ–≤–Њ–і—П —В—Й–∞—В–µ–ї—М–љ—Л–є –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Э–µ –Љ–µ–љ—М—И–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –Ї–Њ–љ—В—А–Њ–ї—М —Б–Њ—Б—В–Њ—П–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Њ–±—А–∞—Й–∞–µ—В—Б—П –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є –Є –Э–Я–Т–Я––љ–µ—Д—А–Њ–њ–∞—В–Є–є —Г –±–Њ–ї—М–љ—Л—Е, –і–ї–Є—В–µ–ї—М–љ–Њ –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–∞. –°—А–µ–і–Є –њ—А–Њ—П–≤–ї–µ–љ–Є–є —В–∞–Ї–Є—Е –љ–µ—Д—А–Њ–њ–∞—В–Є–є –Њ–њ–Є—Б–∞–љ—Л –Њ–±—А–∞—В–Є–Љ–∞—П –њ–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Є –њ–Њ—З–µ—З–љ–∞—П –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–Њ–љ–Є—П, –∞ —Б—А–µ–і–Є –љ–µ–Њ–±—А–∞—В–Є–Љ—Л—Е – —Б–Њ—Б–Њ—З–Ї–Њ–≤—Л–є –љ–µ–Ї—А–Њ–Ј –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ—Л–є –љ–µ—Д—А–Є—В.
–Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –Њ–њ–∞—Б–љ–Њ—Б—В—М –∞—Ж–µ—В–Њ–Љ–Є–љ–Њ—Д–µ–љ–Њ–≤–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є –≤—Б–µ –µ—Й–µ –љ–µ–і–Њ–Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П, —Е–Њ—В—П —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В —В—А–Њ–њ–Є–Ј–Љ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –Ї —Б–Њ—Б–Њ—З–Ї–∞–Љ –њ–Њ—З–µ–Ї —Б –Є–Ј–±—Л—В–Њ—З–љ—Л–Љ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –µ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –≤ —В–Ї–∞–љ–Є —Б–Њ—Б–Њ—З–Ї–Њ–≤, —Б —З–µ–Љ –Є —Б–≤—П–Ј–∞–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ–≥–Њ –і–ї—П –∞—Ж–µ—В–Њ–Љ–Є–љ–Њ—Д–µ–љ–∞ –њ–∞–њ–Є–ї–ї—П—А–љ–Њ–≥–Њ –љ–µ–Ї—А–Њ–Ј–∞.
Fored —Б —Б–Њ–∞–≤—В. (2001) –љ–∞ –Љ–∞—В–µ—А–Є–∞–ї–µ –®–≤–µ–і—Б–Ї–Њ–≥–Њ –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–≥–Њ —А–µ–≥–Є—Б—В—А–∞ –Ј–∞ 1996–1998 –≥–≥., –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —А–µ–≥—Г–ї—П—А–љ—Л–є –њ—А–Є–µ–Љ –∞—Ж–µ—В–Њ–Љ–Є–љ–Њ—Д–µ–љ–∞, –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є–ї–Є –Њ–±–Њ–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Ю—Б–Њ–±–µ–љ–љ–Њ –њ–Њ–і—З–µ—А–Ї–Є–≤–∞–µ—В—Б—П, —З—В–Њ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ—З–µ–Ї –Є–ї–Є —Б–Є—Б—В–µ–Љ–љ–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П —П–≤–ї—П—О—В—Б—П –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –С—Л–ї–Њ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–Њ 926 –±–Њ–ї—М–љ—Л—Е —Б –≤–њ–µ—А–≤—Л–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л–Љ –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є 998 –Ї–Њ–љ—В—А–Њ–ї—М–љ—Л—Е —Б—Г–±—К–µ–Ї—В–Њ–≤, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е 918 –Є 980 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –Є–Љ–µ–ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Г—О –і–Њ–Ї—Г–Љ–µ–љ—В–∞—Ж–Є—О. –°—А–µ–і–Є —Б—В—А–∞–і–∞–≤—И–Є—Е –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ –Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї —Г–њ–Њ—В—А–µ–±–ї—П–ї–Є —А–µ–≥—Г–ї—П—А–љ–Њ 37% –Є 25% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –∞ –≤ –Ї–Њ–љ—В—А–Њ–ї–µ 19% –Є 12%. –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –≤–Њ–Ј—А–∞—Б—В–∞–ї —Б –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –њ—А–Є–µ–Љ–∞ –Є –і–Њ–Ј–Њ–є –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–Њ—В–Њ—А–∞—П –±—Л–ї–∞ –±–Њ–ї–µ–µ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є —Г –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –∞—Ж–µ—В–Њ–Љ–Є–љ–Њ—Д–µ–љ, —З–µ–Љ –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г, –Њ–і–љ–∞–Ї–Њ –∞–≤—В–Њ—А—Л –љ–µ –Љ–Њ–≥–ї–Є –Є—Б–Ї–ї—О—З–Є—В—М —А–Њ–ї—М –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є—Е —Г—Б–ї–Њ–≤–Є–є.
–Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–є –і–∞–ї–µ–Ї–Њ –љ–µ –њ–Њ–ї–љ—Л–є –њ–µ—А–µ—З–µ–љ—М –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, —А–∞–Ј–≤–Є–≤–∞—О—Й–Є—Е—Б—П —Г –±–Њ–ї—М–љ—Л—Е –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Э–Я–Т–Я —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–ї–∞—Б—Б–Њ–≤, –њ–Њ —Б—Г—Й–µ—Б—В–≤—Г –љ–∞–њ—А–∞–≤–ї–µ–љ –љ–∞ –њ—А–Є–≤–ї–µ—З–µ–љ–Є–µ –≤–љ–Є–Љ–∞–љ–Є—П –Ї–Њ –≤—В–Њ—А–Њ–є —Б—В–Њ—А–Њ–љ–µ –ї–µ—З–µ–±–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ – –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О –Є –Ї —А–∞–љ–љ–µ–Љ—Г —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є—О —А–∞–Ј–≤–Є—В–Є—П –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, –µ–≥–Њ –Њ–±—А–∞—В–Є–Љ–Њ—Б—В–Є, —З—В–Њ–±—Л —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –Њ–±–µ—Б–њ–µ—З–Є—В—М —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О, –њ—А–Є –Ї–Њ—В–Њ—А–Њ–є –љ–∞—А—П–і—Г —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –ї–µ–Ї–∞—А—Б—В–≤–∞ —Б–Њ–±–ї—О–і–∞–ї–∞—Б—М –±—Л –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ—Е –Э–Я–Т–Я –і–Њ–Ї–∞–Ј–∞–љ–∞ –љ–∞ –±–Њ–ї—М—И–Њ–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Љ–∞—В–µ—А–Є–∞–ї–µ, –њ—А–Є —Н—В–Њ–Љ –Є–Љ–µ–љ–љ–Њ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –њ—А–Є–Ј–љ–∞–љ «–Ј–Њ–ї–Њ—В—Л–Љ —Б—В–∞–љ–і–∞—А—В–Њ–Љ» —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, —Б –Ї–Њ—В–Њ—А—Л–Љ —Б—А–∞–≤–љ–Є–≤–∞—О—В—Б—П –Є –љ–Њ–≤—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞, —В–∞–Ї–Є–µ –Ї–∞–Ї –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ, –љ–Є–Љ–µ—Б—Г–ї–Є–і, —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± –Є —А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±.
–Ф–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –≤ –і–Њ–Ј–µ 50 –Љ–≥ –≤ 2 –Є–ї–Є 3 –њ—А–Є–µ–Љ–∞, –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–є –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Є –†–Р, —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–∞—Е (–∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–µ–Љ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–µ –Є —А–µ–∞–Ї—В–Є–≤–љ—Л—Е –∞—А—В—А–Є—В–∞—Е), –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—Е —Б—Г—Б—В–∞–≤–Њ–≤ –Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –≤–љ–µ—Б—Г—Б—В–∞–≤–љ—Л—Е –Љ—П–≥–Ї–Є—Е —В–Ї–∞–љ–µ–є, —Б–њ–Њ—А—В–Є–≤–љ—Л—Е —В—А–∞–≤–Љ–∞—Е –Є –і—А. –Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ —П–≤–ї—П–µ—В—Б—П –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–µ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ, –≤–Ї–ї—О—З–∞—О—Й–µ–µ –њ—А–µ–њ–∞—А–∞—В—Л –±—Л—Б—В—А–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Є –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–љ—Л–µ (—А–µ—В–∞—А–і–љ—Л–µ), –Љ–∞–Ј–Є, –≥–µ–ї–Є, —Б—Г–њ–њ–Њ–Ј–Є—В–Њ—А–Є–Є. –Я–Њ—Н—В–Њ–Љ—Г –љ–µ —Г–і–Є–≤–Є—В–µ–ї—М–љ–Њ, —З—В–Њ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї, –Ї–∞–Ї –Є 30 –ї–µ—В —В–Њ–Љ—Г –љ–∞–Ј–∞–і, –Њ—Б—В–∞–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –њ–Њ–њ—Г–ї—П—А–љ—Л—Е –Э–Я–Т–Я –Є –љ–µ —В–Њ–ї—М–Ї–Њ –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є McKenna F. —Б —Б–Њ–∞–≤—В. (2001) —Б—А–∞–≤–љ–Є–≤–∞–ї—Б—П —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± (100 –Љ–≥ 2 —А/—Б—Г—В) –Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –љ–∞—В—А–Є—П (50 –Љ–≥ 3 —А/—Б—Г—В) –њ—А–Є –Ю–Р. –Э–∞–Ј—Л–≤–∞—П –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї «—Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –Љ–Є—А–Њ–≤—Л–Љ —Б—В–∞–љ–і–∞—А—В–Њ–Љ –ї–µ—З–µ–љ–Є—П» (Current world wide standard of care), —Н—В–Є –∞–≤—В–Њ—А—Л –њ—А–Є—Е–Њ–і—П—В –Ї –≤—Л–≤–Њ–і—Г, —З—В–Њ –Є –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї, –Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± –њ—А–Њ—П–≤–Є–ї–Є —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Ї–∞–Ї –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–∞—З–∞–ї–∞ –Є –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П –≤ —Е–Њ–і–µ –ї–µ—З–µ–љ–Є—П –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, —В–∞–Ї –Є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Г–ї—Г—З—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є —Б—Г—Б—В–∞–≤–Њ–≤, –Њ–і–љ–∞–Ї–Њ –њ—А–Њ—Д–Є–ї—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М/–±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —Г —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –±—Л–ї –ї—Г—З—И–µ. –Ш–љ—В–µ—А–µ—Б —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є –љ–Њ–≤–Њ–≥–Њ (—Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±) –Є «—Б—В–∞—А—В–Њ–≤–Њ–≥–Њ» (–і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї) –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г–ґ–µ –≤ –љ–∞—З–∞–ї–µ XXI –≤–µ–Ї–∞ –Љ–Њ–ґ–љ–Њ —А–∞—Б—Ж–µ–љ–Є—В—М, –Ї–∞–Ї –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ —Б–Њ—Е—А–∞–љ—П—О—Й–µ–≥–Њ—Б—П –Ј–љ–∞—З–µ–љ–Є—П –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞.
–Я–Њ––њ—А–µ–ґ–љ–µ–Љ—Г –њ—А–Є–≤–ї–µ–Ї–∞–µ—В –Ї —Б–µ–±–µ –≤–љ–Є–Љ–∞–љ–Є–µ –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ. –Я–Њ–і–≤–Њ–і—П –Є—В–Њ–≥–Є –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є/–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞, Degner F. —Б —Б–Њ–∞–≤—В (2001) –њ–Њ–і—З–µ—А–Ї–Є–≤–∞—О—В —И–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Х–≤—А–Њ–њ–µ –Є –°–®–Р –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –Ю–Р, –љ–Њ –≤ –Х–≤—А–Њ–њ–µ –Є –њ—А–Є –†–Р, –Є –∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–µ–Љ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–µ (–Р–°). –Т –≥–Њ–і–Є—З–љ–Њ–Љ –Є—Б–њ—Л—В–∞–љ–Є–Є –њ—А–Є –Р–° –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ –≤ –і–Њ–Ј–µ 15 –Љ–≥/—Б—Г—В –±—Л–ї —В–∞–Ї –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, –Ї–∞–Ї –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ (20 –Љ–≥/—Б—Г—В).
–Ь–∞–Ј—Г—А–Њ–≤ –Т.–Ш. —Б —Б–Њ–∞–≤—В. (2001) –ї–µ—З–Є–ї–Є –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–Њ–Љ 15 –±–Њ–ї—М–љ—Л—Е –Р–°, —Г 9 –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Є —В–∞–Ї–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–∞–Ї —П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –ґ–µ–ї—Г–і–Ї–∞ –Є 12––њ. –Ї–Є—И–Ї–Є (6 —З–µ–ї.), –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М (2 —З–µ–ї.) –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —Е–Њ–ї–µ—Ж–Є—Б—В–Є—В (1 —З–µ–ї.). –£ 12 –±–Њ–ї—М–љ—Л—Е –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –±—Л–ї–∞ –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞, –ї–Є—Е–Њ—А–∞–і–Ї–∞, –±–Њ–ї–Є –≤ —Н–њ–Є–≥–∞—Б—В—А–Є–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Э–Я–Т–Я. –І–µ—А–µ–Ј 4 –љ–µ–і. –ї–µ—З–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї–Є—Б—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Є–љ–і–µ–Ї—Б–∞ –†–Є—З–Є, –±–Њ–ї–Є –њ–Њ –Т–Р–® –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —Г—В—А–µ–љ–љ–µ–є —Б–Ї–Њ–≤–∞–љ–љ–Њ—Б—В–Є, –Ї–∞–Ї –Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Г–ї—Г—З—И–µ–љ–Є—П –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М «—Е–Њ—А–Њ—И–∞—П» –Є «–Њ—З–µ–љ—М —Е–Њ—А–Њ—И–∞—П» –±—Л–ї–∞ –Њ—В–Љ–µ—З–µ–љ–∞ —Г 2/3 –±–Њ–ї—М–љ—Л—Е, –Њ–і–љ–∞–Ї–Њ 7% –љ–µ –Њ—В–Љ–µ—В–Є–ї–Є —Н—Д—Д–µ–Ї—В–∞. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ—В—П–≥–Њ—Й–µ–љ–љ—Л–є –њ–Њ –±–Њ–ї–µ–Ј–љ—П–Љ –Ц–Ъ–Ґ –∞–љ–∞–Љ–љ–µ–Ј, –∞–≤—В–Њ—А—Л –љ–µ –Њ—В–Љ–µ—В–Є–ї–Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є. –Ы–Є—И—М 1 –±–Њ–ї—М–љ–Њ–є –±—Л–ї –Є—Б–Ї–ї—О—З–µ–љ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–Ј––Ј–∞ –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л, –∞ —Г 2––≥–Њ –љ–∞ 7––є –і–µ–љ—М –ї–µ—З–µ–љ–Є—П –њ–Њ—П–≤–Є–ї–Є—Б—М –±–Њ–ї–Є –≤ –њ—А–∞–≤–Њ–Љ –њ–Њ–і—А–µ–±–µ—А—М–µ, –Є—Б—З–µ–Ј–љ—Г–≤—И–Є–µ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ.
–І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞, —В–Њ –≤ –і–≤—Г—Е –±–Њ–ї—М—И–Є—Е –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е MELLISS–Р –Є SELECT –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ —А–∞–Ј–≤–Є—В–Є—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, –Њ—В–µ—З–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є–ї–Є –њ–Њ—З–µ—З–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –Ї–Њ—В–Њ—А—Л–µ –њ—А–µ–≤—Л—И–∞–ї–Є –±—Л –љ–∞–±–ї—О–і–∞–µ–Љ—Л–µ –≤ –≥—А—Г–њ–њ–∞—Е —Б—А–∞–≤–љ–µ–љ–Є—П –њ—А–Є –њ—А–Є–µ–Љ–µ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ –Є–ї–Є –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ–∞ (—Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –°–њ–µ—Ж–Є–∞–ї—М–љ–Њ–Љ—Г –∞–љ–∞–ї–Є–Ј—Г –њ–Њ–і–≤–µ—А–≥–ї–Є—Б—М —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Г 32539 –±–Њ–ї—М–љ—Л—Е, –ї–µ—З–µ–љ–љ—Л—Е –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–Њ–Љ. –С—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ 93 —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П (44 –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є 48 –Є–љ—Б—Г–ї—М—В–Њ–≤), —З—В–Њ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 0,28% –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б 0,36% –Є–Ј 1397 —З–µ–ї. –≤ –њ–ї–∞—Ж–µ–±–Њ––≥—А—Г–њ–њ–µ. –Э–µ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г —Г–Ї–∞–Ј–∞–љ–љ—Л–Љ–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є –Є –і–Њ–Ј–Є—А–Њ–≤–Ї–Њ–є –њ—А–µ–њ–∞—А–∞—В–∞ – —В–Њ—З–Ї–Є –Њ—Ж–µ–љ–Ї–Є –і–ї—П —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –±—Л–ї–Є 1,66, 2,02 –Є 1,38 –љ–∞ 100 —З–µ–ї–Њ–≤–µ–Ї–Њ/–ї–µ—В –і–ї—П –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –≤ –і–Њ–Ј–∞—Е 7,5 –Љ–≥, 15 –Љ–≥ –Є 22,5 –Љ–≥. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —В–Њ—З–Ї–Є –Њ—Ж–µ–љ–Ї–Є –і–ї—П –њ–ї–∞—Ж–µ–±–Њ, –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞ (100 –Љ–≥/—Б—Г—В) –Є –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ–∞ (20 –Љ–≥/—Б—Г—В) –±—Л–ї–Є 3,70, 3,05 –Є 1,19 –љ–∞ 100 —З–µ–ї–Њ–≤–µ–Ї–Њ/–ї–µ—В —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –≠—В–Є –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–Њ–Љ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ—Б—В–Љ–∞—А–Ї–µ—В–Є–љ–≥–Њ–≤—Л–µ –љ–∞–±–ї—О–і–µ–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –±–Њ–ї–µ–µ, —З–µ–Љ –≤ 100 —Б—В—А–∞–љ–∞—Е, –≤ –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Њ –≤—Л–њ–Є—Б–∞–љ–Њ –Ї –љ–∞—З–∞–ї—Г 2000 –≥. –±–Њ–ї–µ–µ 30 –Љ–ї–љ. —А–µ—Ж–µ–њ—В–Њ–≤, –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ – –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ—Л–є –њ—А–µ–њ–∞—А–∞—В, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Г —В–µ—Е –±–Њ–ї—М–љ—Л—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б–µ—А–і–µ—З–љ–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П.
–Ъ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –Э–Я–Т–Я, –Ї—А–Њ–Љ–µ –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞, —В–∞–Ї–ґ–µ –Њ—В–љ–Њ—Б–Є—В—Б—П –Є –љ–Є–Љ–µ—Б—Г–ї–Є–і, –Ї–Њ—В–Њ—А—Л–є –њ–Њ –і–∞–љ–љ—Л–Љ Famey J.P. (1997) –Є Bennet A., Villa W. (2000) –≤ 5–20 —А–∞–Ј –±–Њ–ї–µ–µ –∞–Ї—В–Є–≤–µ–љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –¶–Ю–У–2, —З–µ–Љ –і—А—Г–≥–Є–µ –Э–Я–Т–Я. –Т –і–Њ–Ј–µ 100 –Љ–≥ 2 —А/—Б—Г—В –љ–Є–Љ–µ—Б—Г–ї–Є–і –њ—А–Њ—П–≤–Є–ї —В–∞–Ї—Г—О –ґ–µ –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М, –Ї–∞–Ї –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ, –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї –Є –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ, –Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Е–Њ—А–Њ—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М.
–Я—А–µ–і—Б—В–∞–≤–ї—П—О—В –Є–љ—В–µ—А–µ—Б –і–∞–љ–љ—Л–µ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ 12––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–Є–Љ–µ—Б—Г–ї–Є–і–∞ —Г –±–Њ–ї—М–љ—Л—Е –†–Р (–С–∞–ї–∞–±–∞–љ–Њ–≤–∞ –†.–Ь. –Є —Б–Њ–∞–≤—В., 2002). –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 52 –±–Њ–ї—М–љ—Л—Е –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 22 –і–Њ 75 –ї–µ—В, —Б—В—А–∞–і–∞–≤—И–Є—Е –†–Р, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є –њ—А–µ–њ–∞—А–∞—В –≤ –і–Њ–Ј–µ 200–400 –Љ–≥ –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–Є –њ–Њ–і–Њ–±—А–∞–љ–љ–Њ–є —А–∞–љ–љ–µ–µ –±–∞–Ј–Є—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ —Г–ї—Г—З—И–µ–љ–Є—П –Є —Г–ї—Г—З—И–µ–љ–Є–µ –±—Л–ї–Є –і–Њ—Б—В–Є–≥–љ—Г—В—Л —Г 23,4% –Є 70,2% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Ы–Є—И—М —Г —В—А–µ—Е –±–Њ–ї—М–љ—Л—Е (6,4%) —В–µ—А–∞–њ–Є—П –љ–Є–Љ–µ—Б—Г–ї–Є–і–Њ–Љ –±—Л–ї–∞ –±–µ–Ј—Г—Б–њ–µ—И–љ–Њ–є, –Њ–і–љ–∞–Ї–Њ –Є –і—А—Г–≥–Є–µ –Э–Я–Т–Я (–њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ, –Є–±—Г–њ—А–Њ—Д–µ–љ) —Г —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е –±—Л–ї–Є –Љ–∞–ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л. –Я–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –љ–Є–Љ–µ—Б—Г–ї–Є–і–∞ –±—Л–ї–∞ —Г –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ —Е–Њ—А–Њ—И–µ–є. –£ 9,6% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –ї–µ—З–µ–љ–Є–µ –±—Л–ї–Њ –њ—А–µ–Ї—А–∞—Й–µ–љ–Њ –Є–Ј––Ј–∞ –Ц–Ъ–Ґ––≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є. –Я—А–Є–≤–ї–µ–Ї–∞–µ—В –Ї —Б–µ–±–µ –≤–љ–Є–Љ–∞–љ–Є–µ, —З—В–Њ –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є —Г 23 –±–Њ–ї—М–љ—Л—Е, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –љ–Є–Љ–µ—Б—Г–ї–Є–і –Є –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В –≤ –і–Њ–Ј–µ 7,5–15 –Љ–≥/–љ–µ–і.
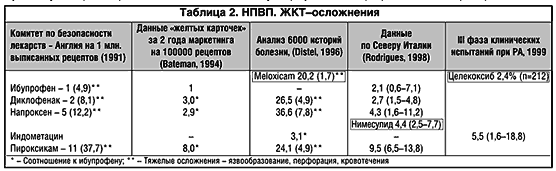
–Т –љ–∞—Б—В–Њ—П—Й–Є–є —Б—В–∞—В—М–µ –љ–µ –њ–Њ–і—З–µ—А–Ї–Є–≤–∞–µ—В—Б—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є–є (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ –Э–Я–Т–Я––≥–∞—Б—В—А–Њ–њ–∞—В–Є—П–Љ –Њ—В—А–∞–ґ–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2), –Ї–Њ—В–Њ—А—Л–µ –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ —Б–Њ—Е—А–∞–љ—П—О—В —Б–≤–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ, –љ–Њ —Г–ґ–µ –Є–Ј–≤–µ—Б—В–љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –њ—А–Є —Г—З–µ—В–µ —В–∞–Ї–Є—Е –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –Ї–∞–Ї –љ–∞–ї–Є—З–Є–µ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –±–Њ–ї—М–љ—Л—Е —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –ґ–µ–ї—Г–і–Ї–∞ –Є–ї–Є 12––њ. –Ї–Є—И–Ї–Є, –∞ –≤ –Љ–Њ–Љ–µ–љ—В –ї–µ—З–µ–љ–Є—П – –Ї—Г—А–µ–љ–Є—П, —Б–Њ—З–µ—В–∞–љ–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤. –Ю—Б–Њ–±–∞—П –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ—Б—В—М –љ—Г–ґ–љ–∞ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –Э–Я–Т–Я –±–Њ–ї—М–љ—Л–Љ —Б—В–∞—А—И–µ 65 –ї–µ—В –Є–ї–Є —А–µ–Ј–Ї–Њ –Њ—Б–ї–∞–±–ї–µ–љ–љ—Л–Љ –±–Њ–ї–µ–Ј–љ—П–Љ–Є. –Ю–і–љ–∞–Ї–Њ —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я –њ—А–Є –†–Р, –Р–° (–Є –і–∞–ґ–µ –Ю–Р) –Є –љ–∞–ї–Є—З–Є–Є —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б –Љ–Є–Ј–Њ–њ—А–Њ—Б—В–Њ–ї–Њ–Љ –Є–ї–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –њ—А–Њ—В–Њ–љ–љ–Њ–≥–Њ –љ–∞—Б–Њ—Б–∞ –Љ–Њ–ґ–µ—В –Њ–±–µ—Б–њ–µ—З–Є—В—М –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Г—О –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї—Г—О –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О.
–°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–µ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–≥–Њ –Є –њ—А–Є–µ–Љ–ї–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞, —Е–Њ—А–Њ—И–µ–µ –Ј–љ–∞–љ–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –і–µ–є—Б—В–≤–Є—П, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ—А–Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є, –Ї–∞–Ї –Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –і–µ–є—Б—В–≤–Є—П –Є –њ—Г—В–µ–є –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П. –Ґ–Њ–ї—М–Ї–Њ —В–∞–Ї–Є–Љ –њ—Г—В–µ–Љ –≤—А–∞—З –Љ–Њ–ґ–µ—В –Њ–±–µ—Б–њ–µ—З–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ.
–Т –љ–∞—Б—В–Њ—П—Й–µ–є —Б—В–∞—В—М–µ —Б–Њ–±—А–∞–љ–∞ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П, –Ї–∞—Б–∞—О—Й–∞—П—Б—П –љ–Њ–≤—Л—Е –і–ї—П –≤—А–∞—З–∞ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ – –Є–љ–і—Г–Ї—Ж–Є—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Э–Я–Т–Я —В—А–Њ–Љ–±–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –Є–љ—Б—Г–ї—М—В–∞, –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–Њ–ї–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –Є —Б—В–∞—А—Л–µ, —Г–ґ–µ —Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є (–Ц–Ъ–Ґ– –≥–∞—Б—В—А–Њ–њ–∞—В–Є—П) –њ–Њ––њ—А–µ–ґ–љ–µ–Љ—Г —Б–Њ—Е—А–∞–љ—П—О—В —Б–≤–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –І—В–Њ –ґ–µ –љ—Г–ґ–љ–Њ –і–µ–ї–∞—В—М, —З—В–Њ–±—Л –Њ–±–µ—Б–њ–µ—З–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ?
1. –Ґ—Й–∞—В–µ–ї—М–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±–Њ–ї—М–љ–Њ–≥–Њ –і–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Ц–Ъ–Ґ–—В—А–∞–Ї—В–∞ –Є –њ–Њ—З–µ–Ї.
2. –С–Њ–ї—М–љ—Л–Љ, —Г –Ї–Њ—В–Њ—А—Л—Е –Є–Љ–µ–µ—В—Б—П —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≥–∞—Б—В—А–Њ–њ–∞—В–Є–є, –Љ–Њ–≥—Г—В –љ–∞–Ј–љ–∞—З–∞—В—М—Б—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У–2, –ї–Є–±–Њ, –њ—А–Є –Є—Е –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Г –Ї–Њ–љ–Ї—А–µ—В–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Э–Я–Т–Я, –љ–Њ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ —Б–Њ–≤–Љ–µ—Б—В–љ–Њ —Б –Љ–Є–Ј–Њ–њ—А–Њ—Б—В–Њ–ї–Њ–Љ (—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–є –Ј–∞—Й–Є—В—Г —Б–ї–Є–Ј–Є—Б—В–Њ–є –Ц–Ъ–Ґ) –Є–ї–Є –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –њ—А–Њ—В–Њ–љ–Њ–≤–Њ–є –њ–Њ–Љ–њ—Л (–Њ–Љ–µ–њ—А–∞–Ј–Њ–ї).
3. –£ –±–Њ–ї—М–љ—Л—Е —Б –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–њ–Њ–≤—Л—И–µ–љ–Є–µ —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞) –Э–Я–Т–Я —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–µ –љ–∞–Ј–љ–∞—З–∞—В—М, –ї–Є–±–Њ –њ–Њ–і —В—Й–∞—В–µ–ї—М–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ – —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л.
4. –С–Њ–ї—М–љ—Л–µ –і–Њ–ї–ґ–љ—Л –њ—А–Њ–і–Њ–ї–ґ–∞—В—М –њ—А–Є–µ–Љ –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–Є–ї–Є –љ–µ–њ—А—П–Љ—Л—Е –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤) –њ—А–Є –љ–∞–ї–Є—З–Є–Є —А–Є—Б–Ї–∞ —В—А–Њ–Љ–±–Њ–Ј–Њ–≤, –µ—Б–ї–Є –±—Г–і—Г—В –њ—А–Њ–≤–Њ–і–Є—В—М –ї–µ—З–µ–љ–Є–µ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –¶–Ю–У–2. –Э–Њ –≤ —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ —В—Й–∞—В–µ–ї—М–љ—Л–є –Љ–Њ–љ–Є—В–Њ—А–Є–љ–≥ —Б–Њ—Б—В–Њ—П–љ–Є—П –Ц–Ъ–Ґ (–≥–∞—Б—В—А–Њ—Б–Ї–Њ–њ–Є—П –љ–µ –Љ–µ–љ–µ–µ 2–—Е —А–∞–Ј –≤ –≥–Њ–і), –і–ї—П —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Н—А–Њ–Ј–Є–≤–љ–Њ–—П–Ј–≤–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є.
5. –С–Њ–ї—М–љ—Л–Љ, –њ–µ—А–µ–љ–µ—Б—И–Є–Љ –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –Є–ї–Є –Є–љ—Б—Г–ї—М—В –Є –љ—Г–ґ–і–∞—О—Й–Є–Љ—Б—П –≤ –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є–Є –ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —Б–Њ–±–ї—О–і–µ–љ–Є–µ –і–Є–µ—В—Л, —В.–µ. –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—А, –Ј–∞—А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–≤—И–Є—Е —Б–µ–±—П, –Ї–∞–Ї –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е –Є–љ—Д–∞—А–Ї—В–Њ–≤ –Љ–Є–Њ–Ї–∞—А–і–∞, –Є–љ—Б—Г–ї—М—В–Њ–≤.
6. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –µ—Й–µ —А–∞–Ј –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –≤–µ—Б—М–Љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е, –љ–Њ –љ–µ–±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –Њ—Б–Њ–±–µ–љ–љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б–Њ—В—А—Г–і–љ–Є—З–µ—Б—В–≤–Њ –≤—А–∞—З–∞ —Б –±–Њ–ї—М–љ—Л–Љ–Є, –њ–Њ–≤—Л—И–µ–љ–Є–µ –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї—М–љ–Њ–≥–Њ –≤–Њ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є—П –Є —Г—Б—В—А–∞–љ–µ–љ–Є–µ —В–µ—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, –Ї–Њ—В–Њ—А—Л–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В –±–Њ–ї–µ–µ —З–∞—Б—В–Њ–Љ—Г —А–∞–Ј–≤–Є—В–Є—О –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –° —Н—В–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ —З—Г–≤—Б—В–≤–Њ –Њ–±–Њ—О–і–љ–Њ–є –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ—Б—В–Є –≤—А–∞—З–∞ –Є –±–Њ–ї—М–љ–Њ–≥–Њ –њ—А–Є –њ—А–Є–µ–Љ–µ –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е, –љ–Њ –љ–µ–±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤, –Ї–∞–Ї–Њ–≤—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –Э–Я–Т–Я. –Ш –≤ —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤–∞–ґ–љ–Њ —Б–Њ–Ј–љ–∞–љ–Є–µ —В–Њ–≥–Њ —Д–∞–Ї—В–∞, —З—В–Њ –і–∞–ґ–µ —Г –Њ—З–µ–љ—М —В—П–ґ–µ–ї—Л—Е –±–Њ–ї—М–љ—Л—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Э–Я–Т–Я –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Є–ї–Є –і–∞–ґ–µ –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—О —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–є –Є –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є.
1. –С–∞–ї–∞–±–∞–љ–Њ–≤–∞ –†.–Ь., –С–µ–ї–Њ–≤ –С.–°., –І–Є—З–∞—Б–Њ–≤–∞ –Э.–Т. –Є —Б–Њ–∞–≤—В. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–Є–Љ–µ—Б–Є–ї–∞ –њ—А–Є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–Љ –∞—А—В—А–Є—В–µ. –Ъ–ї–Є–љ. –Љ–µ–і. 2002 (–≤ –њ–µ—З–∞—В–Є).
2. –Э–∞—Б–Њ–љ–Њ–≤–∞ –Т.–Р. –Э–µ–љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–µ –∞–љ–∞–ї–≥–µ—В–Є–Ї–Є, –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –Є –њ–Њ—З–Ї–Є. –Т –Ї–љ.: –£—Б–њ–µ—Е–Є –љ–µ—Д—А–Њ–ї–Њ–≥–Є–Є. 2001, —Б—В—А. 201–208.
3. –Ь–∞–Ј—Г—А–Њ–≤ –Т.–Ш., –С–µ–ї—П–µ–≤ –Ш.–С., –Ю–љ—Г—Й–µ–љ–Ї–Њ –Ш.–Р. –Ю–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ–ї–Њ–Ї—Б–Є–Ї–∞–Љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–Є–Љ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–Њ–Љ. –Ъ–ї–Є–љ.–Ь–µ–і. 2001, 5, 53–55.
4. Bennett A. Nimesulide: a well established cyclooxygenase–2 inhibitor with many other pharmacological properties relevant to inflammatory disease. In: Therapeutic robes of Selective COX–2 inhibitors Ed. Vane J.R. and Batting R.M., 2001, part24, p.524–540.
5. Bennet A., Villa W. Nimesulide: an NSAID that preferentially inhibits COX–2 and his rarions unique pharmacological activities. Exp. Opin. Pharmacotherapy 2000, 1, 277–286.
6. Catella–Lawson F., Reilly M.P., Kupoor S.C. et al. Cyclooxygenase inhibitors and the antiplatelet effects of aspirin. N. Engl. J. Med, 2001, 345, 1809–1817.
7. Crofford L.J., Oates J.C., Mc Cune WJ et al. Thrombosis in patients with connective tissue diseases treated with specific cyclooxygenase 2 inhibitors: a report of four. Arthritis Rheum, 2000,43,1891–1896.
8. Degner F., Lanes S., van Ryn J., Sigmund R. Pharmacological and clinical profill of meloxicam/ In: Therapeutic robes of Selective COX–2 inhibitors Ed. Vane J.R. and Batting R.M., 2001, part 23, p.498–523.
9. Famey J.P. In vitro and in vivo pharmacological evidence of selective cyclooxygenase–2 inhibition by nimesulide: an overview. Inflamm. REF. 1997, 46, 437–446.
10. Fitz–Gerald G.A., Patrono C. The ovibs, selective inhibition of cyclooxygenase–2. N.Engl.J.Med, 2001, 345, 433–442.
11. Fored C.M., Ejerblad E., Lindblad P. Et al. Acetominophen, aspirin, and chromic renal faifure. N. Engl. J. Med, 2001, 345, 1801–1808.
12. Hennan J.K., Huang J., Barrett T.D. et al Effects of selective cyclooxygenase–2 inhibition on vascular responses and thrombosis in canine coronary arteries, Circulation, 2001,104, 820–828.
13. McMurray R. Cyclooxygenase 2 inhibition and thrombosis comment on the article by crofford et al. Arthritis Rheum, 2001,44,984.
14. Ouellet M., Percival M.D. Mechanism of acetaminophen inhibition of cyclooxigenase isoforms. Arch. Biochem. Biophys, 2001, 387, 273–280.
15. Ray W.A., Stein C.M., Hall K. et al Non–steroidal anti–inflammatory drugs and risk of serious coronary heart disease: an observational cohort study. Lancet, 2002, 359, jan.12, 118–123.
16. Whelton A., Fort J.G., Puma J.A. et al. Cyclooxygenase–2 specific Inhibitors and cardiorenal function: a randomized, controlled trial of celecoxib and rofecoxib in older hypertensive Osteoarthritis patients. Amer. J. Therap.2001,8,2,85–95.
17. Wolfe F., Zhao S., Lane N. Preference for nonsteroidal antiinflammatory drugs over acetaminophen by rheumatic disease patients. Arthritis Rheum. 2000, 43, 378–385.












