Широкое использование ингибиторов фактора некроза опухоли–a (ФНО–a) при ревматоидном артрите (РА), псориатическом артрите, анкилозирующем спондилоартрите и других воспалительных заболеваниях суставов привело к значительному улучшению результатов лечения. Эти препараты позволяют за короткий период времени значительно уменьшить клинико–лабораторные проявления заболевания и замедлить костную деструкцию. Отмечено, что они уменьшают потребность больных РА в срочной медицинской помощи и улучшают их трудоспособность [1]. Смертность больных РА при лечении ингибиторами ФНО–a снижается (за счет уменьшения количества причин смерти, не связанных с инфекционными заболеваниями) [2], что является ярким показателем их значения в лечении ревматических заболеваний.
Основными ингибиторами ФНО–a являются инфликсимаб, этанерцепт и адалимумаб.
Инфликсимаб представляет собой химерное моноклональное антитело к ФНО–a, состоящее на 75% из человеческого белка и на 25% – из мышиного. Вариабельная часть молекулы, включающая область связывания с антигеном (т.е. с ФНО–a), состоит именно из мышиного белка. Инфликсимаб с высокой специфичностью связывается как с растворимым, так и с мембранно–связанным ФНО–a (но не с ФНО–b, известным также как лимфотоксин–a и имеющим меньшее биологическое значение).
Адалимумаб является полностью человеческим белком (иммуноглобулином G1). Будучи моноклональным антителом к ФНО–a, он, как и инфликсимаб, блокирует соединение этого цитокина с его главными рецепторами – р55 и р75 – и лизирует клетки, содержащие ФНО–a на своей мембране (за счет прямого эффекта антител и комплемент–зависимой цитотоксичности).
Этанерцепт (Энбрел) является димерным комбинированным белком, состоящим из человеческого растворимого рецептора ФНО–a р75, соединенного с Fc–фрагментом человеческого иммуноглобулина G1. Этанерцепт отличается от инфликсимаба и адалимумаба своей способностью нейтрализовать не только ФНО–a, но и ФНО–b.
Каждый из этих препаратов в значительной степени нейтрализует ФНО–a и тем самым существенно тормозит ряд патологических процессов, обусловленных преимущественно данным цитокином. При этом связывание ФНО–a осуществляется разными путями: специфическими антителами при назначении инфликсимаба и адалимумаба или растворимыми рецепторами при использовании этанерцепта. В ревматологической литературе лечение любым из этих антицитокинов все чаще склонны обобщенно рассматривать как применение определенного класса биологических препаратов (ингибиторов ФНО–a), приводящее к тождественному эффекту независимо от того, какой конкретный препарат этого класса был использован.
Несмотря на высокую эффективность данный вид терапии сопряжен с определенным риском развития серьезных инфекций, в том числе туберкулеза [3]. Это объясняется важной и многообразной ролью ФНО–a в противоинфекционном иммунитете:
– стимуляция продукции других провоспалительных цитокинов (включая ИЛ–1–b, ИЛ–6, ИФН–g) и хемокинов;
– усиление продукции непосредственных медиаторов воспаления – простагландинов, лейкотриенов, токсических дериватов кислорода и др.;
– влияние на созревание и активацию клеток, участвующих в воспалении (прежде всего нейтрофилов и моноцитов/макрофагов);
– усиление экспрессии молекул адгезии (ICAM–1) на эндотелии, что облегчает миграцию клеток в зону воспаления;
– усиление выработки протеолитических ферментов;
– участие в уничтожении внутриклеточных микроорганизмов – таких, как микобактерия туберкулеза, Listeria, Salmonella и др.;
– участие (в качестве одного из ключевых факторов) в образовании гранулем и их сохранении.
Снижение этих функций ФНО–a его ингибиторами не только тормозит иммуно–воспалительный процесс, но приводит также к определенному снижению уровня иммунной защиты организма и к повышению его восприимчивости к различным инфекциям, включая туберкулез [4]. В частности, в исследованиях на мышах показана защитная роль ФНО–a по отношению к туберкулезу: данный цитокин оказался существенным фактором в формировании и сохранении гранулем, ограничивающих распространение микобактерий [5].
Реальная клиническая практика подтвердила теоретические представления. В настоящее время нет сомнений в том, что при использовании ингибиторов ФНО–α существует определенный риск развития туберкулеза или обострения его латентных форм. S. Ehlers высказывает гипотезу, что опасность реактивации латентного туберкулеза возникает при общем угнетении активности ФНО–a более чем на 70–90% [6].
Ряд исследователей находят, что РА по сравнению с невоспалительными болезнями свойствен больший риск развития инфекций, что демонстрировалось даже до введения в практику глюкокортикоидов [7]. Поэтому нельзя исключить, что и без применения ингибиторов ФНО–a туберкулез у больных РА развивается чаще, чем в популяции, но при назначении данных препаратов, особенно инфликсимаба, эта частота значительно возрастает. Своеобразно, что при развитии туберкулеза на фоне назначения ингибиторов ФНО–a приблизительно в половине случаев речь идет о внелегочных или диссеминированных формах заболевания, хотя в общей популяции не менее чем у 80% туберкулез проявляется только легочным поражением. Так, J. Antolin и соавт. наблюдали больную РА, у которой на фоне терапии адалимумабом развился туберкулезный перитонит [8] – весьма редкое проявление современного туберкулеза.
По мнению большинства современных ревматологов, клинический эффект различных ингибиторов ФНО–a у больных РА существенно не различается. В то же время риск развития туберкулеза при применении конкретных представителей этого класса препаратов оказался неодинаковым. Хотя безопасность различных ингибиторов ФНО–a в прямых параллельных сопоставлениях не анализировалась, было отмечено, тем не менее, что развитие туберкулеза регистрируется заметно чаще при использовании антител к ФНО–a (инфликсимаба и адалимумаба), чем при назначении растворимых рецепторов этого цитокина, т.е. этанерцепта [9].
Оказалось, в частности, что применение инфликсимаба и адалимумаба увеличивает риск реактивации туберкулеза в 5–10 раз по сравнению с небиологическими методами лечения в тех же популяционных группах [3,11–13].
J. Keane и соавт. [14] проанализировали сообщения о 70 случаях развития туберкулеза среди приблизительно 147 тыс. пациентов, лечившихся инфликсимабом. Эта частота значительно превышает фоновые показатели, тем более что 64 из 70 пациентов были из стран с низкой заболеваемостью туберкулезом. У 40 больных были внелегочные проявления болезни. У 48 больных заболевание развилось уже после 3–й инфузии инфликсимаба или еще раньше. Существенно, что на фоне терапии этим препаратом частота развития туберкулеза была заметно выше, чем заболеваемость другими серьезными инфекциями.
Среди 297 пациентов Российского регистра инфликсимаба развитие туберкулеза к 46–й неделе после начала лечения было отмечено у 4 больных, что составило 1,3%. У 2 среди них до лечения инфликсимабом проба Манту не проводилась, и у одного из этих пациентов клинические проявления туберкулеза были обнаружены уже после второй инфузии, а у другого – после пятой. У остальных двух больных результаты пробы Манту составляли 2 и 5 мм, и туберкулез развился у них после 4–й и 8–й инфузий соответственно [15].
При назначении этанерцепта, напротив, отмечается умеренный риск развития туберкулеза. Так, в работе L. Klareskog и соавт. [16] показано, что при длительном (в среднем около 4 лет) назначении этого препарата частота серьезных побочных эффектов (0,1–0,2 на одного пациента в год), в том числе частота серьезных инфекций (0,03–0,06 на пациента в год), не отличалась от соответствующих цифр в контроле. Только у одного больного было подозрение на туберкулез, а других оппортунистических инфекций вообще не отмечалось.
По обобщенным материалам португальских ревматологов среди 960 пациентов, лечившихся ингибиторами ФНО–a, наиболее безопасным оказался этанерцепт: туберкулез развился при терапии инфликсимабом у 1,5% больных, адалимумабом – у 2,3%, этанерцептом – у 0,3% [17].
S. Seong и соавт. выявили, что по сравнению с общей Южнокорейской популяцией риск заболевания туберкулезом для больных РА, не применявших ингибиторы ФНО–a, составляет 8,9, а для лечившихся инфликсимабом – 30,1. Обращает внимание, что при назначении этанерцепта случаев развития туберкулеза в этом исследовании не было зарегистрировано [18].
Сравнение общей частоты серьезных побочных эффектов инфликсимаба и этанерцепта обнаружило, что не только туберкулез, но и другие оппортунистические инфекции (цитомегаловирусная, гистоплазмоз, листереллез, пневмоцистоз, аспергиллез и др.) чаще регистрировались при лечении инфликсимабом [19–21].
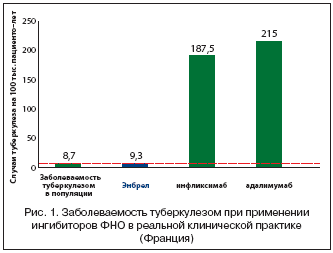
Привлекает внимание работа F. Tubach и соавт., которые в крупном трехлетнем проспективном исследовании оценили риск развития туберкулеза у французских пациентов, получавших лечение ингибиторами ФНО–α (рис. 1). Оказалось, что среди лечившихся моноклональными антителами к ФНО–α туберкулез в расчете на 100 тыс. пациенто–лет был зарегистрирован у 187,5 при назначении ифликсимаба и 215 при назначении адалимумаба, а среди получавших этанерцепт только у 9,3, т.е. на порядок реже. Показательно, что в общей французской популяции частота туберкулеза составляет 8,7 на 100 тыс. человеко–лет, т.е. этанерцепт значительно не повлиял на нее.
Первые симптомы туберкулеза диагностировались через различные сроки после начала лечения ингибиторами ФНО–α (от 6 до 321 недели, медиана – 12 мес.), но чаще в течение первого года терапии. Авторы считают, что это обстоятельство свидетельствует скорее об обострении латентного процесса, чем о новом заболевании. Обращает также внимание, что из 69 больных с туберкулезом, развившимся в процессе терапии ингибиторами ФНО–α, проба Манту до лечения была проведена у 45, причем у 30 она оказалась отрицательной. Профилактику туберкулеза посредством назначения изониазида или другого противотуберкулезного препарата не получал ни один пациент [22].
Аналогичные закономерности были продемонстрированы W. Dixon и соавт. на большом материале Британского регистра. В их исследовании 9882 больных лечились ингибиторами ФНО–α и 2883 – традиционными противовоспалительными базисными препаратами. За время наблюдения (до августа 2007 г.) было отмечено 29 случаев туберкулеза, причем только среди получавших ингибиторы ФНО–α. Частота развития туберкулеза на 100 тыс. пациенто–лет составила для адалимумаба 171, для инфликсимаба – 103 и для этанерцепта – 39. Таким образом, по сравнению с лечением этанерцептом риск заболевания туберкулезом при назначении адалимумаба оказался выше в 4 раза, а при назначении инфликсимаба – в 2,8 раза. Диссеминированный туберкулез встретился только у получавших адалимумаб (4 больных) и инфликсимаб (один пациент). Достойно внимания, что у 9 больных туберкулез развился не в период назначения ингибиторов ФНО–α, а после их отмены, причем у двух пациентов – через год после получения последней дозы. Это делает необходимым проявление соответствующей настороженности и после завершения терапии ингибиторами ФНО–α [23].
Очень важно выяснить причину существенно меньшей частоты заболеваемости туберкулезом при лечении этанерцептом по сравнению с инфликсимабом и адалимумабом. Наиболее вероятно, что она связана со способностью двух последних препаратов (в отличие от этанерцепта) лизировать клетки, содержащие ФНО–a на своей поверхности. Очевидно, что это относится и к клеткам гранулем, формирующихся вокруг туберкулезных микобактерий и отграничивающих их от здоровых тканей, препятствуя тем самым активации и распространению инфекции. Соединяясь с молекулами ФНО–a на поверхности клеток гранулемы, антитела к данному цитокину (инфликсимаб и адалимумаб) вызывают гибель этих клеток посредством апоптоза [24]. Целостность гранулемы нарушается, и она перестает выполнять свою роль ограничения инфекции. По–видимому, именно это обстоятельство объясняет высокую частоту диссеминированных форм туберкулеза при использовании указанных препаратов. В отличие от них этанерцепт нейтрализует циркулирующий ФНО–a, но не способен взаимодействовать с молекулами ФНО–a, уже связанными с рецепторами на поверхности клеток. В результате гранулемные клетки остаются неповрежденными.
Относительно малое влияние этанерцепта на структуру гранулем объясняет как его безопасность в ситуациях, где гранулемы играют защитную роль (туберкулезная инфекция), так и недостаточный эффект при тех болезнях, где образование гранулем является морфологической основой патологического процесса (болезнь Крона, синдром Вегенера, саркоидоз).
Еще одной причиной снижения противотуберкулезного иммунитета инфликсимабом и адалимумабом может явиться тот факт, что пролиферация и функция цитотоксических Т–лимфоцитов, специфически направленных против микобактерий туберкулеза, подавляются им значительно больше, чем этанерцептом [25,26].
Установленный риск развития туберкулеза при назначении ингибиторов ФНО–a (особенно инфликсимаба и адалимумаба) делает необходимым целенаправленное обследование пациентов перед назначением этих препаратов, включающее прежде всего пробу Манту и при показаниях рентгенографию грудной клетки. В США по требованию Агенства по пищевым продуктам и лекарственным препаратам (FDA) в инструкцию по применению инфликсимаба внесена официальная рекомендация проводить предварительный скрининг пациентов на наличие туберкулеза [27].
В исследовании J. Perez и соавт., проведенном в Северной Америке и странах Европы на 11 439 больных РА, такой скрининг заключался в целенаправленном анализе анамнеза, проведении пробы Манту и – у большинства пациентов – рентгенографии грудной клетки. Для оценки результатов пробы Манту использовались нормы, принятые в соответствующих странах. Если эта проба оказывалась положительной или исследователь считал реальным риск активации латентного туберкулеза по каким–либо иным соображениям, то с профилактической целью назначался изониазид. Следование этим правилам и повышенная настороженность относительно туберкулеза привели к сокращению его развития на фоне терапии ингибиторами ФНО–α на 85% [28]. Аналогичные данные приводят и другие авторы [29].
R. Aggarwal и соавт. лечили этанерцептом 84 больных с положительной пробой Манту. Размеры папулы колебались от 6 до 50 мм (в среднем 21,5 мм). 78 из 84 пациентов получали противотуберкулезную профилактику: изониазид – 76, рифампицин – 1, комбинацию рифампицина и пиразинамида – 1. Шесть человек не получали профилактику в связи с различными противопоказаниями. Средняя продолжительность терапии этанерцептом составила 24,6 мес. (196 пациенто–лет). Ни у одного из этих больных с высоким риском туберкулезной инфекции не развился активный туберкулез [30].
В процессе терапии ингибиторами ФНО–a сответствующая настороженность должна постоянно сохраняться, т.к. на фоне их назначения возможно не только обострение латентного процесса, но и развитие новых случаев туберкулеза. Как уже указывалось, определенный риск туберкулезной инфекции сохраняется и после отмены терапии ингибиторами ФНО–α. При наличии активного туберкулеза данные препараты противопоказаны. Однако для пациентов, перенесших это заболевание в прошлом, лечение ингибиторами ФНО–a возможно на фоне длительного применения противотуберкулезных препаратов, в частности, изониазида. То же относится к больным, у которых нет указания на ранее перенесенный туберкулез, но проба Манту оказалась положительной. В подобных случаях предполагается латентный туберкулез и, в соответствии с одной из предлагаемых схем, назначается изониазид по 300 мг в сутки в течение 9 мес., начиная за 2 недели до первого введения ингибитора ФНО–a. В России проба Манту считается положительной, если диаметр папулы составляет 5 мм и более.
Некоторые авторы сомневались в целесообразности проведения пробы Манту у лиц, которые ранее получали противотуберкулезную вакцинацию с помощью вакцины BCG. Действительно, у таких лиц эта проба в течение ряда лет может быть положительной, хотя размеры папулы бывают обычно не столь велики, как при заболевании туберкулезом. Однако более важно, что через 10 лет после вакцинации BCG проба Манту становится отрицательной и поэтому может использоваться в диагностических целях без ограничений. Многие ревматологи считают, что при лечении ингибиторами ФНО–a пробу Манту следует проводить один раз в 6 мес.
В соответствии с практикой испанского регистра BIOBADASER J. Gomez–Reino и соавт. рекомендуют в случае отрицательной пробы Манту проводить ее повторно через неделю и при положительном результате назначать лечение изониазидом [31. Многие авторы, однако, сомневаются в целесообразности такой практики.
Высказывались также опасения, что в результате терапии ингибиторами ФНО–a кожные туберкулиновые реакции у части больных могут стать ложноотрицательными. С другой стороны, В. Joven и соавт., наблюдая 61 больного РА в течение 54 недель, нашли, что инфликсимаб, напротив, не снижает, а несколько повышает реактивность по отношению к туберкулину. У их пациентов с исходной положительной туберкулиновой пробой диаметр кожной инфильтрации после лечения увеличился в среднем на 4 мм. Авторы объясняют это тем, что больным активным РА якобы свойственна определенная степень клеточной анергии, которая устраняется успешной терапией инфликсимабом [32].
Литература
1. Beevor C.P., Hull R., Thomas A. et al. Anti TNFa therapy reduce emergency health services usage. Ann.Rheum.Dis., 2006, 65, suppl.II, 176.
2. Gomez–Reino J.J., Dasgupta B., Haugeberg G. et al. Mortality rate is reduced in RA patients treated with TNF antagonists. Data from Biobadaser. Ann.Rheum.Dis., 2006, 65, suppl.II, 318
3. Gomez–Reino J.J., Carmona L., Valverde V.R., et al., Treatment of rheumatoid arthritis wth tumor necrosis factor inhibitors may predispose to significant increase in tuberculosis risk: a multicenter active–surveillance report. Arthritis Rheum., 2003, 48, 2122–2127.
4. Насонов Е.Л., Козлов Р.С., Якушин С.Б., Инфекционные осложнения терапии блокаторами фактора некроза опухоли: предупрежден – значит вооружен. Клин. Микробиол. и Антимикроб. Химиотерап., 2006, 4, 1–11.
5. Flynn J.L., Goldstein M.M., Chan J., et al., Tumor necrosis factor–alpha is required in the protective immune response against Mycobacterium tuberculosis in mice. Immunity, 1995, 2, 561–72.
6. Ehlers S., Why does tumor necrosis factor targeted therapy reactivate tuberculosis? J.Rheumatol., 2005:32, Suppl. 74:35–39.
7. Baum J. Infection in rheumatoid arthritis. Arthr.Rheum., 1971, 14, 135–137.
8. Antolin J., Azahara M., Hernandez C. et al. Tuberculous peritonitis after treatment with adalimumab. Scand.J.Infect.Dis., 2008, 40, 677–678.
9. Fleischmann R., Iqbal I., Nandeshwar P., et al., Safety and efficacy of disease–modifying anti–rheumatic agents: focus on the benefits and risk of etanercept., Drug Saf., 2002, 25, 173–97.
10. Насонов Е.Л. Применение ингибиторов фактора некроза опухоли при ревматоидном артрите: место этанерцепта. Научно–практическая ревматология, 2008, 5 (приложение), 1–20.
11. Wallis R.S., Broder M.S., Wong J.Y., et al., Granulomatous infections diseases associated with TNF antagonists. Clin.Infect., 2004, 38, 1261–1265..
12. C.Cientifico BIOBADASER. Spanish experience with a registry of adverse events in biological therapy. Ann.Rheum.Dis., 2002, 61, suppl.1, 388.
13. Wolfe F., Michaud K., Anderson J. et al. Tuberculosis infection in patients with rheumatoid arthritis and the effect of infliximab therapy. Arthr.Rheum., 2003, 48, suppl., 537–538.
14. Keane J., Gershon S., Wise R. Tuberculosis associated with infliximab, a tumor necrosis factor a–neutralizing agent. New Engl.J.Med., 2001, 345, 1098–1104.
15. Лукина Г.В., Сигидин Я.А., Насонов Е.Л. Применение инфликсимаба у больных ревматоидным артритом в клинической практике (по данным Российского регистра). Тер.архив, 2009, 8, 1–5.
16. Klareskog L., Moreland L.W., Cohen S.B. et al. The safety and efficacy of over seven years of continuous etanercept therapy in patients with rheumatoid arthritis in North America and Europe. Ann.Rheum.Dis., 2005, 64, suppl.III, 410.
17. G.E.A.R. Rheumatoid Arthritis study group. Portuguese society for rheumatology. Tuberculosis in patients treated with anti–TNF–alpha therapy. The Portuguese experience. Ann.Rheum.Dis., 2006, 65, suppl.II, 498
18. Seong S.–S., Choi C.–B., Woo J.–H. Incidence of TB in Korean patients with RA: Effects of RA itself and of TNF blockers. J.Rheumatol., 2007, 34, 706.
19. Cush J., Matteson E. (eds.). FDA Advisory Committee Rewiews Safety on TNFInhibitors. http:/www.rheumatology.org/research/hotline/09901tnf.html.
20. Lee J.–H., Slifman N.R., Gershon S.K. et al. Life–threatening histoplasmosis complicating immunotherapy with tumor necrosis factor a antagonists infliximab and etanercept. Arthr.Rheum., 2002, 46, 2565–2570.
21. Ruderman E.M., Markenson J.A. Granulomatous infections and tumor necrosis factor antagonists therapy. Ann.Rheum.Dis., 2003, 62, suppl.1, 172–173.
22. Tubach F., Salmon D., Ravaud P. et al. Risk of tuberculosis is higher with anti–tumor necrosis factor monoclonal antibody therapy than with soluble tumor necrosis factor receptor therapy. Arthr. Rheum., 2009, 60, 1884–1894.
23. Dixon W.G., Hyrich K.L., Watson K.D. et al. Drug–specific risk of tuberculosis in patients with rheumatoid arthritis treated with anti–TNF therapy. Results from the BSR biologics register (BSRBR). Ann.Rheum.Dis., 2008, 67, suppl.II, 178.
24. Mitoma H., Horiuchi T., Tsuhamoto H. et al. Mechanisms for cytotoxic effects of anti–tumor necrosos factor agents on transmembrane tumor necrosis factor ?–expressing cells: comparison among infliximab, etanercept and adalimumab. Arthr.Rheum., 2008, 58, 1248–1257.
25. Hamdi H., Mariette X., Godot V. et al. Inhibition of anti–tuberculosis T–lymphocyte function by tumor necrosis factor antagonists. Arthritis Res.Ther., 2006, 8, 114.
26. Saliu O.Y., Sofer C., Stein D.S. et al. Tumor–necrosis–factor blockers: differential effects on mycobacterial immunity. J.Infect.Dis., 2006, 194, 486–492.
27. Remicade (package insert). Malvern, PA, Centocor, Inc, 2006.
28. Perez J.L., Kupper H., Spencer–Green G.T. Impact of screening for latent TB prior to initiating anti–TNF therapy in North America and Europe. Ann.Rheum.Dis., 2005, 64, 86.
29. Kavanaugh A., Tutuncu Z., Sanchez T. The TNF inhibitors in clinical use. J.Musculoskel.Med., October 2005, suppl., 29–34.
30. Aggarwal R., Manadan A., Poliyedath A. et al. Study of etanercept in patients at high risk for mycobacterial tuberculosis infections. J.Rheumatol., 2009, 36, 914–917.
31. Gomez–Reino J.J., Cormona L., Descalzo M.A., Risk of tuberculosis in patients treated with tumor necrosis factor antagonists due to incomplete prevention of reactivation of latent infection., Arthr. Rheum., 2007, 57, 756–761.
32. Joven B.E., Almodovar R., Galindo M. Does anti–tumour necrosis factor a treatment modify the tuberculin PPD response? Ann.Rheum.Dis., 2006, 65, 699.












