За последние годы неоспоримо доказано, что изменить отдаленные исходы РА реально возможно только на самых первых этапах заболевания [3]. Проблема ранней стадии заболевания не ограничивается только РА. Для всех воспалительных ревматических болезней весьма типично наличие более или менее длительного начального периода, когда адекватная терапия имеет максимально выраженное влияние на их дальнейшее течение («окно возможности»). В то же время РА – самое частое из хронических воспалительных ревматических заболеваний. Поэтому ранняя стадия РА, который представляет собой большую общемедицинскую и социальную проблему [4], привлекает к себе наибольшее внимание исследователей во всем мире.
За последние годы на основании отечественных и зарубежных клинических наблюдений [2–5] определенно показано, что в течение первых 1–2 лет болезни при РА могут возникать необратимые структурные повреждения в суставах. При этом выделяют:
• «Очень ранний РА» – заболевание с длительностью симптоматики до 3 месяцев, поскольку в течение этого периода можно сделать вывод о стойкости артрита (этот период можно считать потенциально обратимым состоянием), и «ранний» РА с длительностью болезни до 2 лет, когда можно определить наличие или отсутствие типичного эрозивного процесса в суставах.
• Ранний РА (или «ранний установившийся РА») – первые 1–2 года болезни (когда можно определить первые признаки прогрессирования болезни).
• Недифференцированный артрит (НА) – воспалительное поражение суставов, не соответствующее (еще?) классификационным критериям РА.
Согласно схеме, предложенной Firestein G.S. [6], иммунопатологические процессы при развитии РА протекают в 3 этапа:
• Этап «врожденного иммунитета», когда активируются генетически обусловленные иммунные механизмы путем стимуляции дендритных клеток, макрофагов, фибробластов, тучных клеток.
• Этап «адаптивного иммунитета», во время которого происходит генерализация процесса с включением про– и антивоспалительных механизмов.
• Этап деструкции, когда провоспалительные стимулы побеждают, происходит активация остеокластов с резорбцией костной ткани и внедрение пролиферирующих синовиальных клеток в хрящ.
Этой схеме соответствует представление о наличии нескольких стадий в формировании клинической картины болезни, на каждой из которых генетические факторы должны сочетаться с воздействием гипотетических факторов внешней среды [7]. Такая схема объясняет возможность как типичного, так и атипичного (в виде НА) дебюта болезни, а также формирование клинической гетерогенности.
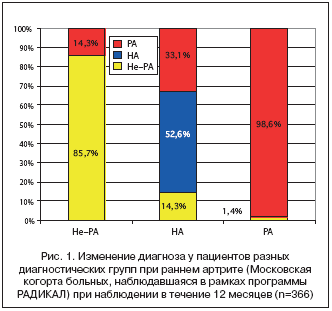
Наблюдения за большой когортой больных [8] в рамках Программы «Ранний Артрит: Диагностика, Исход, Критерии, Активное Лечение (РАДИКАЛ)» показало, что из 366 больных с воспалительным поражением суставов и давностью болезни до 1 года только у 57,9% сразу мог быть установлен диагноз РА, 36,3% была классифицированы, как имеющие НА, у 5,7% были выставлены другие диагнозы при первичном обследовании. Через 12 месяцев диагноз РА был установлен у 33,1% больных с НА (рис. 1), что соответствует данным зарубежных исследователей [9].
Таким образом, клинические наблюдения говорят о следующих особенностях раннего РА:
• болезнь только в 50–60% случаев дебютирует с типичной клинической картины;
• у 1/3 больных с картиной воспалительного поражения суставов наблюдается т.н. НА;
• у больных НА в течение 1 года наблюдения РА развивается примерно в 30% случаев.
Затруднения в диагностике объективного характера связаны с тем, что при РА отсутствуют патогномоничные симптомы. Это касается даже такого классического симптома, как артрит кистей. При ранней диагностике РА необходимо учитывать следующие особенности [10]:
1) артрит пястно–фаланговых и плюсно–фаланговых суставов может быть асимметричным;
2) рано выявляются поражения околосуставных тканей: теносиновиты сгибателей и разгибателей, амиотрофия межкостных мышц;
3) имеются характерные симптомы:
• положительный симптом сжатия кисти,
• сгибательная контрактура пальцев,
• невозможность сжатия кисти в кулак.
Важнейшей проблемой ранней диагностики РА с точки зрения организации здравоохранения является позднее обращение впервые заболевших за специализированной медицинской помощью. Поскольку время в данном случае является критичным фактором, определяющим в значительной степени исход лечения, для улучшения взаимодействия врачей первичного звена со специалистами–ревматологами Европейской лиги по борьбе с ревматизмом (EULAR) рекомендованы уже апробированные в нашей стране критерии клинического подозрения на РА, которые являются показаниями для консультации ревматолога [5]:
• Наличие 3 и более припухших суставов;
• ‑Вовлечение пястно– и плюснефаланговых суставов (положительные симптомы «сжатия»);
• Утренняя скованность ≥ 30 минут.
Мы рекомендуем на основании собственного опыта подозревать РА даже у больных с 1–2 припухшими суставами, поскольку начало болезни с моно– и олигоартрита – не редкость.
Согласно разработанному в ГУ Институт ревматологии РАМН алгоритму этапной ранней диагностики РА [8], при наличии критериев клинического подозрения больной должен быть направлен на следующий этап диагностики – обследование у ревматолога поликлиники, а при необходимости – на этап ревматологического отделения.
«Арсенал» современного ревматолога для ранней диагностики воспалительных заболеваний суставов достаточно широк:
• Классификационные критерии, для определения которых основное значение имеет тщательное клиническое исследование;
• Иммунологические тесты: ревматоидный фактор (РФ), исследование антицитруллиновых антител, в частности, антител к циклическому цитруллинированному пептиду (АЦЦП) и др.;
• Инструментальные методы: помимо традиционной рентгенографии, все шире используются магнитно–резонансная томография (МРТ), ультразвуковое исследование (УЗИ) суставов кистей;
• Могут иметь значение иммуногенетические исследования (типирование определенных человеческих лейкоцитарных антигенов – HLA);
• При некоторых вариантах дифференциальной диагностики, особенно в случае дебюта заболевания с олигоартрита крупных суставов, важнейшее значение может иметь артроскопия и биопсия синовиальной оболочки.
Среди новых иммунологических методов наибольшее значение имеет определение АЦЦП. Этот метод в настоящее время практически стал вторым стандартным иммунологическим тестом (первый – определение РФ) для диагностики РА.
Данный тест достаточно специфичен (75–90%) для РА, а чувствительность его на ранней стадии болезни достигает также 75% [11]. Особенно важно определение АЦЦП у серонегативных по РФ больных. Как показывают многочисленные литературные данные [12], АЦЦП, особенно 2–го поколения (АЦЦП–2) специфичнее для РА, чем РФ, а также может успешно использоваться для прогнозирования развития РА у больных НА. Кроме того, высокий титр АЦЦП ассоциирован с более тяжелым течением болезни (в частности, с более быстрым прогрессированием эрозивных изменений в суставах) [12], а также с устойчиво высокой активностью РА [13], поэтому этот тест обладает несомненным прогностическим значением.
Методики иммунологической диагностики РА находятся сейчас в стадии бурного развития, предложено множество новых тестов, каждый из которых имеет свои преимущества:
• Антицитруллиновые антитела:
– АЦЦП–2, АЦЦП–3,
– ‑А/т к мутированному цитруллинированному виментину (анти–МЦВ),
– А/т к цитруллинированному фибриногену,
– А/т к цитруллинированной α–энолазе,
– А/т к цитруллинированному коллагену II типа,
• А/т к RA33 – гетерогенному ядерному нуклеопротеину А2 (hnRNP–A2).
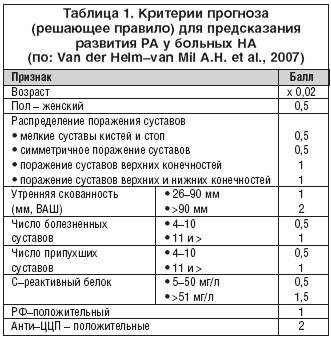
Предложен алгоритм иммунологической диагностики РА [14], основанный на повторном определении РФ, АЦЦП, анти–МЦВ, RА33 в динамике, что при правильной интерпретации должно помочь не только поставить нозологический диагноз, но и уточнить прогноз болезни (рис. 2).
Выявление ранних структурных изменений – одно из основных направлений диагностического поиска при раннем РА. Наибольший потенциал в этом отношении в настоящее время имеет МРТ суставов кисти. Эта современная методика позволяет:
• Объективизировать наличие синовита в сомнительных случаях;
• Провести дифференциальную диагностику с периартрикулярными поражениями;
• Выявить ранние эрозивные и преэрозивные изменения (отек костного мозга, повреждение хряща), патологию сухожилий.
МРТ значительно чувствительнее, чем стандартная рентгенография, при выявлении ранних признаков костно–хрящевой деструкции. Специальные исследования [15], посвященные сопоставлению выявления костных эрозий разными методами, показали, что рентгено–негативные эрозии, выявляемые с помощью МРТ и УЗИ, могут считаться истинными эрозиями.
Иммунологические и инструментальные показатели оказываются взаимосвязанными между собой. Так, нами было показано, что при наличии высоких уровней АЦЦП и С–реактивного белка отмечается высокая активность РА, высокий РФ и большое число эрозий по данным МРТ у больных ранним РА. Таким образом, данные иммунологических и инструментальных исследований могут помочь в определении тяжести состояния больного и, соответственно, в выборе терапии.
Особенно сложным бывает уточнение диагноза у пациентов с НА, который, по нашим наблюдениям [16], чаще всего встречается в следующих клинических вариантах:
• Олигоартрит крупных суставов (коленные, голеностопные, плечевые, тазобедренные);
• Асимметричный артрит суставов кисти;
• Серонегативный по РФ олигоартрит суставов кистей;
• Нестойкий полиартрит.
Нередко для верификации нозологической формы требуется многомесячное наблюдение и повторные обследования. Предложены специальные критерии (решающее правило), позволяющие предсказать трансформацию НА в «настоящий» РА (табл. 1) путем подсчета суммы баллов [17]. Эти критерии недавно были апробированы на 3 независимых когортах больных с НА [18]. При этом точность прогнозирования оказалась весьма высокой: точность предсказания низкого риска перехода в РА (≤6 баллов) составила 83–86%, высокого риска (≥8 баллов) – 93–100%.
В 2007 г. были опубликованы рекомендации EULAR по ведению больных ранним артритом [19]. Так же, как рекомендации по другим нозологиям (подагра, анкилозирующий спондилит), данные рекомендации вырабатывались большой группой экспертов согласно определенной процедуре с оценкой силы доказательности каждого пункта. В кратком изложении эти рекомендации представлены ниже.
1. Артрит характеризуется припухлостью сустава, сопровождающейся болью и скованностью. Пациент с артритом более чем одного сустава должен быть осмотрен ревматологом в идеале в течение 6 недель после появления симптоматики.
2. Клиническое исследование – главный метод выявления синовита. В сложных случаях полезно использование УЗИ, лазер–допплеровского исследования, МРТ.
3. Исключение других заболеваний (не–РА) требует тщательного опроса и клинического осмотра больного, а также проведения, как минимум, следующих тестов: развернутый общий анализ крови, общий анализ мочи, трансаминазы, антинуклеарные антитела.
4. У каждого пациента с ранним артритом, направленного к ревматологу, должны быть определены следующие факторы развития персистирующего эрозивного артрита:
• число припухших и болезненных суставов,
• СОЭ или СРБ,
• РФ и АЦЦП,
• эрозии на рентгенограммах.
5. Пациенты с риском развития персистирующего эрозивного артрита, даже если больной не отвечает классификационным критериям РА, должна быть как можно раньше назначена базисная терапия.
6. Важно информировать больного о болезни, лечении и исходе. Как дополнительное средство может быть проведена специальная образовательная программа.
7. Назначение нестероидных противовоспалительных препаратов (НПВП) должно быть рассмотрено при наличии симптомов артрита после оценки состояния ЖКТ, сердечно–сосудистой системы и почек.
8. Системное лечение глюкокортикоидами (ГК) уменьшает боль и припухлость и должно быть рассмотрено в качестве дополнительной (преимущественно временной) терапии как часть стратегии базисного лечения. Внутрисуставное введение ГК должно быть рассмотрено как средство купирования локальных симптомов воспаления.
9. Среди базисных противовоспалительных препаратов (БПВП) метотрексат рассматривается как основной («якорный») препарат и должен назначаться первым у пациентов с риском развития персистирующего заболевания.
10. Основная цель терапии – достижение ремиссии. Регулярный мониторинг активности болезни и побочных эффектов должен приводить к принятию решений по выбору и изменению терапии (БПВП и генно-инженерных биологических препаратов).
11. Нефармакологические методы, такие как лечебная физкультура, физиотерапия, могут использоваться как дополнение к лекарственной терапии.
12. Мониторинг активности болезни должен включать число припухших и болезненных суставов, оценку общего состояния больным и врачом, СОЭ и СРБ. Активность болезни должна оцениваться с интервалом в 1–3 месяца до развития ремиссии. Структурные повреждения должны оцениваться по рентгенограммам кистей и стоп каждые 6–12 месяцев в течение первых нескольких лет болезни. Оценка функции (например, HAQ) может быть добавлена к мониторингу активности и структурных повреждений.
Рекомендации EULAR представляют собой большой шаг вперед в отношении улучшения практической помощи больным ранним артритом. В качестве комментария хотелось бы обратить внимание на следующие основные моменты:
• Подчеркивается, что главное в диагностике – это клинический осмотр ревматолога;
• Подтверждено, что является обоснованным подозрение на РА при олигоартрите, локализация артрита специально не выделяется;
• АЦЦП рекомендованы для широкого применения наряду с РФ;
• Рекомендовано назначать терапию БПВП больным, не полностью соответствующим критериям РА 1987 г. при наличии факторов риска персистирующего эрозивного артрита;
• Подчеркивается, что основной базисный препарат – это метотрексат;
• Осторожность при назначении НПВП;
• Подтверждена важная роль ГК;
• Подчеркнуто, что залог успеха – раннее назначение и регулярный мониторинг базисной терапии.
В настоящее время хорошо известно, что первые несколько месяцев от начала заболевания – время наиболее быстрого прогрессирования структурных повреждений, когда формируется база для дальнейшего развития болезни. В связи с этим основной концепцией терапии раннего РА в настоящее время признается концепция «окна возможности» [20], когда активное лечение способно повлиять на дальнейшее течение заболевания.
Практические наблюдения позволили сформулировать новые цели лечения – ремиссия или, как минимум, стойко низкая активность болезни [21].
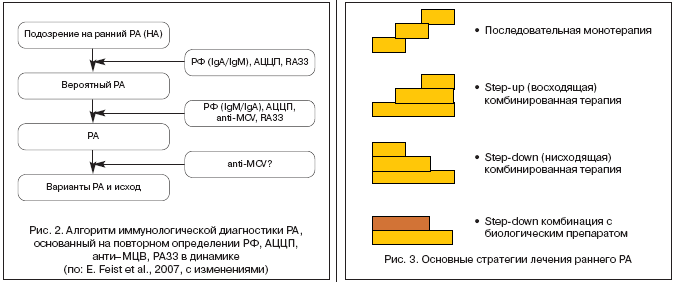
Основой терапии РА остаются БПВП – метотрексат, лефлуномид, сульфасалазин. В то же время монотерапия БПВП (+ НПВП в качестве симптоматического средства) все больше вытесняется схемами комбинированной терапии (рис. 3).
Наиболее часто БПВП комбинируются с ГК. Большой опыт лечения позволил выделить 2 основных направления применения ГК при раннем РА:
• Быстрое подавление воспалительной активности в период до развития эффекта БПВП (bridge–терапия);
• Достижение более высокой эффективности, индуцирование клинической ремиссии, в ряде случаев замедление деструкции суставов – при длительном применении низких доз (<10 мг/сут. преднизолона).
Несмотря на хорошие в целом результаты комбинированной терапии БПВП и ГК, сохраняется значительное число больных ранним РА (около 40%), у которых не достигается достаточный клинический ответ на терапию либо продолжается деструкция суставов. Для этих пациентов оптимальным является комбинация БПВП и генно-инженерных биологических препаратов (в первую очередь ингибиторов ФНО). В России активно применяются химерные моноклональные антитела к ФНО–α (инфликсимаб) и человеческие моноклональные антитела к ФНО–α (адалимумаб). Последние обладают более низкой иммуногенностью, что проявляется в значительно более низкой частоте появления антител к адалимумабу и, соответственно, в снижении частоты реакций гиперчувствительности.
Биологическим препаратам свойственны все черты, характерные для БПВП (подавление воспалительной активности, торможение деструкции суставов, возможное индуцирование ремиссии), но эффект, как правило, развивается намного быстрее (иногда сразу после инфузии) и значительно более выражен, в том числе в отношении торможения деструкции суставов.
Характерной особенностью терапии генно-инженерными биологическими препаратами является достижение клинической ремиссии. Результаты рандомизированных исследований BeSt [22–24], PREMIER [25], TEMPO [26] показывают, что частота стойкой ремиссии при лечении комбинацией метотрексата с каждым из ингибиторов ФНО–α (инфликсимабом, адалимумабом и этанерсептом) при наблюдении в течение 2–3 лет была сопоставима и составляла около 50%. Хороший клинический эффект при этом, как правило, сопровождался выраженным замедлением прогрессирования деструкции суставов (в отличие от обычных БПВП).
Накопленные за последние годы данные позволили Suresh E. и Lambert C.M. [27] постулировать следующее:
• Комбинированная терапия улучшает клинический ответ на лечение, замедляет рентгенологическое прогрессирование, улучшает исход в отношении функции суставов и снижает нетрудоспособность по сравнению с монотерапией;
• Стратегия «step–down» имеет преимущества перед стратегией «step–up», поскольку дает шанс быстрого и эффективного подавления воспаления;
• ГК и ингибиторы ФНО являются многообещающим компонентом комбинированной терапии при раннем РА, поскольку позволяют быстро добиться подавления воспалительной активности;
• Даже кратковременное применение агрессивной комбинированной терапии на ранней стадии РА дает значимое улучшение в отношении отдаленных результатов по сравнению с монотерапией;
• В настоящее время наиболее хорошо доказана эффективность комбинированной терапии с включением ГК и ингибиторов ФНО. Метотрексат при этом играет роль «якорного» («anchor») препарата по всех успешных комбинациях;
• Несмотря на ранее имевшее место мнение о большей токсичности комбинированных схем терапии, последние большие контролируемые исследования показали, что это не так.
К сожалению, внедрение в широкую практику ингибиторов ФНО не решает полностью вопрос лечения раннего РА. Как правило, для поддержания стойкого улучшения требуется проведение постоянного (многомесячного и многолетнего) поддерживающего лечения, поэтому говорить об излечении трудно. Это же касается и больных НА. Недавно опубликованное первое плацебо–контролируемое исследование биологического препарата у этих пациентов [28] на небольшой группе (17) больных показало, что короткий курс (4 инфузии) инфликсимаба не предотвращает развития РА у больных с НА.
В связи с высокой потребностью в новых генно-инженерных биологических препаратах в практику внедряются все новые молекулы, направленные на различные механизмы патологической активации иммунной системы (анти–В–клеточный препарат ритуксимаб, блокатор костимуляции абатасепт, ингибитор рецепторов интерлейкина–6 тоцилизумаб и др.).
В целом современные принципы ведения больных ранним РА можно суммировать следующим образом:
• Ранняя диагностика;
• Оценка прогноза – ключевой момент при выборе лечения;
– ‑Определение иммунологических маркеров (антицитруллиновые антитела),
– ‑Выявление ранних структурных изменений (МРТ, УЗИ);
• Все больные должны получать метотрексат (или другой БПВП), часто – в сочетании с ГК;
• Цель лечения – ремиссия или, как минимум, низкая активность болезни;
• При высокой активности болезни требуется раннее назначение генно-инженерных биологических препаратов (ингибиторы ФНО);
Литература
1. Сигидин Я.А., Лукина Г.В. Новые подходы к анализу патогенеза и патогенетической терапии ревматоидного артрита. //Научно–практическая ревматология, 2001, №5, с. 4–11
2. Каратеев Д.Е. Основные тенденции и вариабельность эволюции ревматоидного артрита: результаты многолетнего наблюдения. Научно–практическая ревматология, 2004, №1, с.8–14
3. Насонов Е.Л. Почему необходима ранняя диагностика и лечение ревматоидного артрита? //Русс. Мед. Журнал, 2002, т. 10, № 22, с. 1009–101
4. Насонов Е.Л. Ревматоидный артрит как общемедицинская проблема. //Тер. Архив, 2004, № 5, с. 5–7
5. Emery P., Breedveld F.C., Dougados M. et al. Early referral recommendation for newly diagnosed rheumatoid arthritis: evidence based development of a clinical guide //Ann. Rheum. Dis., 2002, Vol. 61, No. 4., p.290–297
6. Firestein GS. Evolving concepts of rheumatoid arthritis. // Nature, 2003, May 15; 423 (6937), p. 356–361
7. Dixon WG, Symmons DP. Does early rheumatoid arthritis exist? //Best Pract. Res. Clin. Rheumatol., 2005, v.19, No. 1, p. 37–53
8. Каратеев Д.Е., Лучихина Е.Л., Тюрина Л.Н. и соавт. Ранняя диагностика ревматоидного артрита в клинической практике на современном этапе (результаты наблюдений за московской когортой больных ранним артритом в рамках программы РАДИКАЛ). Тер. Архив, 2008, №5, с. 8–13
9. Van Aken J., van Dongen H., le Cessie S. et al. Comparison of long term outcome of patients with rheumatoid arthritis presenting with undifferentiated arthritis or with rheumatoid arthritis: an observational cohort study. Ann Rheum Dis 2006;65;20–25
10. Каратеев Д.Е. Ревматоидная кисть. //Consilium medicum, 2005, №2, с.83–87
11. Александрова Е.Н., Чемерис Н.А., Каратеев Д.Е. и соавт. Антитела к циклическому цитруллинированному пептиду при ревматоидном артрите. Тер. Архив, 2004, №12, с. 64–68
12. Avouac J., Gossec L ., Dougados M. Diagnostic and predictive value of anti–cyclic citrullinated protein antibodies in rheumatoid arthritis: a systematic literature review. Ann Rheum Dis 2006;65;845–851
13. Svard A., Kastbom A., Reckner–Olsson A., Skogh T. Presence and utility of IgA–class antibodies to cyclic citrullinated peptides in early rheumatoid arthritis: the Swedish TIRA project. Arthritis Research & Therapy 2008, 10:R75
14. Feist E., Burmester G.–R., Egerer K. Autoantikorperprofile bei der rheumatoiden Arthritis. Zeitschrift Fur Rheumatologie, 2007, 66(3): 212–218
15. Dohn U.M., Ejbjerg B.J., Hasselquist H. et al. Detection of bone erosions in rheumatoid arthritis wrist joints with magnetic resonance imaging, computed tomography and radiography. Arthritis Research & Therapy 2008, 10:R25
16. Каратеев Д.Е., Лучихина Е.Л. Ранняя диагностика ревматоидного артрита: проблемы и решения. Российские медицинские вести, 2007, №4, 24–27
17. Van der Helm–van Mil A.H., le Cessie S., van Dongen H. et al. A Prediction Rule for Disease Outcome in Patients With Recent–Onset Undifferentiated Arthritis. . Arthritis Rheum. 2007, 56(2): 433–440
18. Van der Helm–van Mil A.H., Detert J., le Cessie S. et al. Validation of a prediction rule for disease outcome in patients with recent–onset undifferentiated arthritis: moving toward individualized treatment decision–making. Arthritis Rheum. 2008, 58(8): 2241–2247
19. Combe B., Landewe R., Lukas C. et al. EULAR recommendations for the management of early arthritis: report of task force of the European Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). //Ann. Rheum. Dis., 2007, vol. 66, No. 1, p. 34–45
20. Лечение ревматоидного артрита. Клинические рекомендации. / Под ред. Е.Л. Насонова. – М., 2006.
21. Smolen J. et al., Therapeutic strategies in early rheumatoid arthritis //Best Practice & Research Clinical Rheumatology, 2005, Vol. 19, No. 1, pp. 163–177
22. Goekoop–Ruiterman Y.P.M., de Vries–Bouwstra J.K., Allaart C.F.et al. Clinical and Radiographic Outcomes of Four Different Treatment Strategies in Patients With Early Rheumatoid Arthritis (the BeSt Study)Arhtitis Rheum, 2005; 11: 3381–3390
23. Goekoop–Ruiterman Y.P.M., de Vries–Bouwstra J.K., Allaart C.F.et al. Comparison of Treatment Strategies in Early Rheumatoid Arthritis. A Randomized Trial. Ann Intern Med. 2007;146:406–415
24. Van der Kooij S.M., Goekoop–Ruiterman Y.P.M., de Vries–Bouwstra J.K et al. Clinical and radiological efficacy in fourth different treatment strategies in Patients With Early Rheumatoid Arthritis: 3–year follow–up of the BeSt Study. Ann Rheum Dis 2007;66(Suppl II):91
25. Breedveld F., Weisman M., Kavanaugh A. et al. A Multicenter, Randomized, Double–Blind Clinical Trial of Combination Therapy With Adalimumab Plus Methotrexate Versus Methotrexate Alone or Adalimumab Alone in Patients With Early, Aggressive Rheumatoid Arthritis Who Had Not Had Previous Methotrexate Treatment. Arthritis Rheum, 2006, 54: 26–37
26. Van der Heijde D, Klareskog L, Rodriguez–Valverde V. et al. Comparison of Etanercept and Methotrexate, Alone and Combined, in the Treatment of Rheumatoid Arthritis. Two–Year Clinical and Radiographic Results from the TEMPO Study, a Double–Blind, Randomized Trial. ArthritisRheum, 2006, 54: 1063–1074
27. Suresh E., Lambert C.M. Combination treatment strategies in early rheumatoid arthritis. Ann. Rheum. Dis., 2005; 64; 1252–1256
28. Saleem B., Mackie S., Quinn M. et al. Does the use of tumour necrosis factor antagonist therapy in poor prognosis, undifferentiated arthritis prevent progression to rheumatoid arthritis? Ann Rheum Dis 2008;67;1178–1180












