–Т —Н—В–Њ–є —Б–≤—П–Ј–Є –∞–Ї—В—Г–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–≤–µ–і–µ–љ–Є–µ —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ю–Р —Б —Г—З–µ—В–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б—Г—Б—В–∞–≤–Њ–≤, —Б—В–µ–њ–µ–љ–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П. –Ю—Б–Њ–±—Г—О –∞–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –љ–∞–ї–Є—З–Є–µ –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –£–Љ–µ—А–µ–љ–љ—Л–є —А–Є—Б–Ї, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–є –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В—М—О, –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —В–µ—А–∞–њ–Є–Є –Ю–Р –≤—Л–Ј—Л–≤–∞—О—В —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В (17,2%), –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П (55,2%), —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Ц–Ъ–Ґ (21,8%), –і–µ–њ—А–µ—Б—Б–Є—П, –Њ–ґ–Є—А–µ–љ–Є–µ; –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї – –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л–µ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –Є –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ, —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –њ–Њ—З–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М (—А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є OARSI, 2014), –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞ (12,9%), –±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П –∞—Б—В–Љ–∞ (9,6%), –Є–љ—Б—Г–ї—М—В –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ (4,5%). –≠—В–Є —Ж–Є—Д—А—Л —П–≤–ї—П—О—В—Б—П –љ–∞–≥–ї—П–і–љ—Л–Љ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ—А–Є –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є, —З—В–Њ –Њ–њ—А–µ–і–µ–ї—П–µ—В –Њ—Б–Њ–±—Л–µ —В—А–µ–±–Њ–≤–∞–љ–Є—П –Ї –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—З–Є—В–∞–µ—В—Б—П –Њ–±—Й–µ–њ—А–Є–Ј–љ–∞–љ–љ–Њ–є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ю–Р, –≤–Ї–ї—О—З–∞—О—Й–µ–є –Ї–∞–Ї –љ–µ—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –Ї–Њ—А—А–µ–Ї—Ж–Є–Є —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Н—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, —В–∞–Ї –Є –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
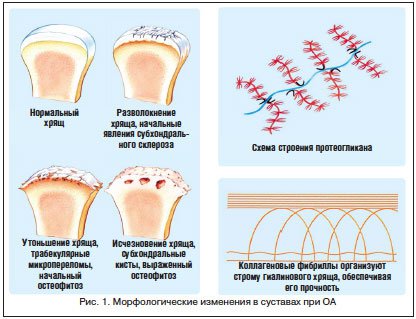
–Я–Њ—Б–Ї–Њ–ї—М–Ї—Г, –њ–Њ –Љ–љ–µ–љ–Є—О –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г–µ—В –±—Л—Б—В—А–µ–µ, —З–µ–Љ —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ —Е—А—П—Й–µ–≤–Њ–є —В–Ї–∞–љ–Є –Є —Б—Г–±—Е–Њ–љ–і—А–∞–ї—М–љ–Њ–є –Ї–Њ—Б—В–Є, —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–Љ –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ—Л–Љ –ї–µ—З–µ–љ–Є–µ–Љ —П–≤–ї—П–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Э–Я–Т–Я) –Є –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ–Њ–і–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М—Б—П –њ–Њ–±–Њ—З–љ—Л–Љ–Є —П–≤–ї–µ–љ–Є—П–Љ–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ –Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, —З—В–Њ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В –Є—Е —И–Є—А–Њ–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —Б—В–∞—А—И–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ–∞—Е. –Э–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ—Л–Љ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Э–Я–Т–Я —П–≤–ї—П–µ—В—Б—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –Ј–∞–і–µ—А–ґ–Ї—Г –≤–Њ–і—Л –Є —Б–Њ–ї–µ–є –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —Б–Є–љ—В–µ–Ј–∞ —А–µ–љ–∞–ї—М–љ–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є–љ–∞-1, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –њ—А–Є–≤–Њ–і—П—Й–Є–Љ –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –Я—А–Є –≤—Л–±–Њ—А–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤–∞–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –Э–Я–Т–Я –Є –≥—А—Г–њ–њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —В. –Ї. –Є–Ј–≤–µ—Б—В–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –Э–Я–Т–Я –љ–∞ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–Є–Р–Я–§), –∞ —В–∞–Ї–ґ–µ –±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–∞ –±—Г–і–µ—В –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—О –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, —З–µ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–∞, –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–∞ –Є –њ–Є—А–Њ–Ї—Б–Є–Ї–∞–Љ–∞. –°–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ —Б –і–Є—Г—А–µ—В–Є–Ї–∞–Љ–Є, β-–±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Є –Є–Р–Я–§ –њ—А–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–Љ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–Є —Б –±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤. –Т—Б–ї–µ–і—Б—В–≤–Є–µ –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ —Б—В–∞–љ–Њ–≤—П—В—Б—П –њ–Њ–љ—П—В–љ—Л–Љ–Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є —Н–Ї—Б–њ–µ—А—В–Њ–≤ OARSI –Њ–± –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Э–Я–Т–Я –њ—А–Є –Ю–Р –≤ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–µ –Є –љ–∞ –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –≤—А–µ–Љ–µ–љ–Є (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є 1–Р, —Б–Є–ї–∞ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є 93%).
–Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤ —Б–≤—П–Ј–Є —Б –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М—О –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ю–Р –љ–µ–ї—М–Ј—П –љ–µ–і–Њ–Њ—Ж–µ–љ–Є–≤–∞—В—М –Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Ј–∞–Љ–µ–і–ї–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Ї–Њ—В–Њ—А—Л–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В: —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–Њ–ї–Є, —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, –Ј–∞–Љ–µ–і–ї–µ–љ–Є–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є. –Т –і–Њ—Б—В—Г–њ–љ–Њ–є –љ–∞–Љ –љ–∞—Г—З–љ–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ –Є–Љ–µ—О—В—Б—П —Г–Ї–∞–Ј–∞–љ–Є—П –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–є —Б—В—А—Г–Ї—В—Г—А–љ–Њ-–Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В —Н—В–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Ї –њ—А–µ–њ–∞—А–∞—В–∞–Љ –њ–µ—А–≤–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –њ—А–Є–љ—П—В–Њ –Њ—В–љ–Њ—Б–Є—В—М –∞–ї—Д–ї—Г—В–Њ–њ, –≥–ї–Є–Ї–Њ–Ј–∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–∞–љ-–њ–µ–њ—В–Є–і–љ—Л–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б, –Ї–Њ –≤—В–Њ—А–Њ–Љ—Г –њ–Њ–Ї–Њ–ї–µ–љ–Є—О – –≥–ї—О–Ї–Њ–Ј–∞–Љ–Є–љ, –∞ —В–∞–Ї–ґ–µ —Е–Њ–љ–і—А–Њ–Є—В–Є–љ–∞ —Б—Г–ї—М—Д–∞—В (–•–°).
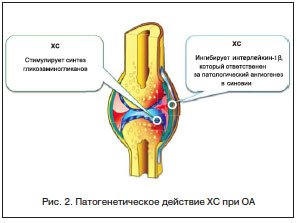
–Ґ—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–є –њ–Њ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ –•–° –≤–њ–µ—А–≤—Л–µ —Г–њ–Њ–Љ–Є–љ–∞–ї—Б—П –≤ 1891 –≥. [Oswald Schmiedeberg], –∞ –њ–µ—А–≤–∞—П –Њ–±–Ј–Њ—А–љ–∞—П —Б—В–∞—В—М—П, –њ–Њ—Б–≤—П—Й–µ–љ–љ–∞—П —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Є–Ј—Г—З–µ–љ–Є—П –•–° [Levene P.A., La Forge F.B.], –њ–Њ—П–≤–Є–ї–∞—Б—М –≤ 1913 –≥. –Т —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е 20 –ї–µ—В –•–° —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –≤ –ї–µ—З–µ–љ–Є–Є –Ю–Р, –Њ—В–ї–Є—З–∞—П—Б—М –≤—Л—Б–Њ–Ї–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є, –њ—А–Є—З–µ–Љ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ–і–љ–Њ–≥–Њ –Є–Ј –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ —Б –Љ–Є–љ–Є–Љ—Г–Љ–Њ–Љ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ґ–∞–Ї, –≤ —А—П–і–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –•–° –љ–µ –±—Л–ї–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є. –Т –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –•–°, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ –†–Њ—Б—Б–Є–Є, —Б–ї–µ–і—Г–µ—В –≤—Л–і–µ–ї–Є—В—М –љ–∞—Г—З–љ—Л–µ —В—А—Г–і—Л –Т.–Р. –Э–∞—Б–Њ–љ–Њ–≤–Њ–є, –і–Њ–Ї–∞–Ј–∞–≤—И–µ–є –≤—Л—Б–Њ–Ї—Г—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е —Д–Њ—А–Љ –•–°. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Д–Њ—А–Љ—Л –і–ї—П –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –•–° –љ–µ –њ–Њ—В–µ—А—П–ї–Є —Б–≤–Њ–µ–є –∞–Ї—В—Г–∞–ї—М–љ–Њ—Б—В–Є, –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Я—А–Є –њ—А–Є–µ–Љ–µ per os –•–° –±—Л—Б—В—А–Њ –∞–і—Б–Њ—А–±–Є—А—Г–µ—В—Б—П –Є–Ј –Ц–Ъ–Ґ, –∞ –µ–≥–Њ –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—В 10 –і–Њ 20%. –Я—А–Є —Н—В–Њ–Љ –≤ —Б–Є—Б—В–µ–Љ–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –њ–Њ–њ–∞–і–∞—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–Є–Ј–Ї–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ –і–µ—А–Є–≤–∞—В—Л, –Њ–±–ї–∞–і–∞—О—Й–Є–µ –Љ–µ–љ—М—И–µ–є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–∞—В–Є–≤–љ—Л–Љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є (—А–Є—Б. 2).
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е —Д–Њ—А–Љ–∞—Е —Б–њ–Њ—Б–Њ–±–љ–Њ –њ–Њ–≤—Л—И–∞—В—М –Є—Е –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М. –Я—А–Є –≤/–Љ –≤–≤–µ–і–µ–љ–Є–Є –•–° —Е–Њ—А–Њ—И–Њ –≤—Б–∞—Б—Л–≤–∞–µ—В—Б—П –Є —З–µ—А–µ–Ј 30 –Љ–Є–љ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е –≤ –Ї—А–Њ–≤–Є, –∞ —Б–њ—Г—Б—В—П 15 –Љ–Є–љ – –≤ —Б–Є–љ–Њ–≤–Є–∞–ї—М–љ–Њ–є –ґ–Є–і–Ї–Њ—Б—В–Є. –Я—А–µ–њ–∞—А–∞—В –љ–∞–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –≤ —Е—А—П—Й–µ–≤–Њ–є —В–Ї–∞–љ–Є, –њ—А–Є —Н—В–Њ–Љ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ —Б—Г—Б—В–∞–≤–љ–Њ–Љ —Е—А—П—Й–µ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —З–µ—А–µ–Ј 48 —З. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –•–° –≤ –Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е —Д–Њ—А–Љ–∞—Е –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ, –≤—Л—Б–Њ–Ї–Њ–±–µ–Ј–Њ–њ–∞—Б–љ–Њ –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Б –Ю–Р.
–Т –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –љ–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –•–Њ–љ–і—А–Њ–≥–∞—А–і–∞ (–Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ–∞—П —Д–Њ—А–Љ–∞ –•–°). –Т –Њ—В–Ї—А—Л—В–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 100 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–Љ—Г–ґ—З–Є–љ – 27, –ґ–µ–љ—Й–Є–љ – 73) —Б –≥–Њ–љ–∞—А—В—А–Њ–Ј–Њ–Љ (70%) –Є –Ї–Њ–Ї—Б–∞—А—В—А–Њ–Ј–Њ–Љ (30%), –љ–∞—Е–Њ–і–Є–≤—И–Є—Е—Б—П –љ–∞ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Њ—В–і–µ–ї–µ–љ–Є–Є –Э–£–Ч «–Ф–Њ—А–Њ–ґ–љ–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М–љ–Є—Ж–∞ –љ–∞ —Б—В–∞–љ—Ж–Є–Є «–Т–Њ—А–Њ–љ–µ–ґ-1» –Ю–Р–Ю «–†–Ц–Ф». –Ю–Р –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–ї—Б—П –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –Ї–Њ–ї–ї–µ–≥–Є–Є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Њ–≤ (American College of Rheumatology) 1987 –≥. [3, 5, 16, 20]. –Т—Б–µ –±–Њ–ї—М–љ—Л–µ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –Ї–Њ—В–Њ—А—Л—Е —Б–Њ—Б—В–∞–≤–ї—П–ї 51±2,78 –≥–Њ–і–∞, –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л. –Я–∞—Ж–Є–µ–љ—В—Л 1-–є (–Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є) –≥—А—Г–њ–њ—Л (n=50) –њ—А–Є–љ–Є–Љ–∞–ї–Є –њ—А–Є –±–Њ–ї—П—Е –≤ —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е –Є –Ї–Њ–ї–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–∞—Е –Э–Я–Т–Я, –њ–Њ–і–Њ–±—А–∞–љ–љ—Л–µ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ –≤ —Б—А–µ–і–љ–µ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е, –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –љ–∞–ї–Є—З–Є–µ–Љ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є. –С–Њ–ї—М–љ—Л–µ 2-–є –≥—А—Г–њ–њ—Л –њ–Њ–Љ–Є–Љ–Њ –Э–Я–Т–Я –њ–Њ–ї—Г—З–∞–ї–Є –•–Њ–љ–і—А–Њ–≥–∞—А–і –≤/–Љ –њ–Њ 100 –Љ–≥ —З–µ—А–µ–Ј –і–µ–љ—М, –і–Њ–Ј—Г —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є –і–Њ 200 –Љ–≥, –љ–∞—З–Є–љ–∞—П —Б 4-–є –Є–љ—К–µ–Ї—Ж–Є–Є. –Ъ—Г—А—Б –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї 25 –Є–љ—К–µ–Ї—Ж–Є–є.
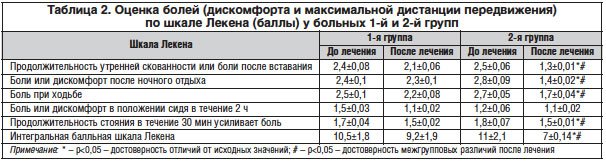
–£ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –±–Њ–ї—М –њ–Њ –≤–Є–Ј—Г–∞–ї—М–љ–Њ-–∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ (–Т–Р–®) –≤ –њ–Њ–Ї–Њ–µ –Є –њ—А–Є —Е–Њ–і—М–±–µ, –∞ —В–∞–Ї–ґ–µ –њ–Њ —И–Ї–∞–ї–µ –Ы–µ–Ї–µ–љ–∞ (–≤ –±–∞–ї–ї–∞—Е), –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М —Б—Г—Б—В–∞–≤–Њ–≤, –Њ—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –њ–Њ –Љ–љ–µ–љ–Є—О –±–Њ–ї—М–љ–Њ–≥–Њ –Є –≤—А–∞—З–∞, –∞ —В–∞–Ї–ґ–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —П–≤–ї–µ–љ–Є—П –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —В–µ—А–∞–њ–Є–Є –•–Њ–љ–і—А–Њ–≥–∞—А–і–Њ–Љ. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –і–Њ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є –Є –њ–Њ—Б–ї–µ –µ–µ –Њ–Ї–Њ–љ—З–∞–љ–Є—П.
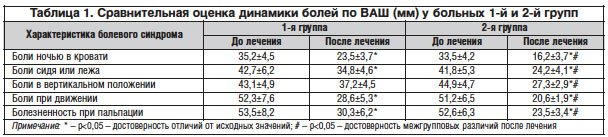
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ —Д–Њ–љ–µ –≤/–Љ –≤–≤–µ–і–µ–љ–Є—П –Є–љ—К–µ–Ї—Ж–Є–є –•–Њ–љ–і—А–Њ–≥–∞—А–і–∞ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –±–Њ–ї–µ–є –њ–Њ –Т–Р–® –Ї–∞–Ї –≤ –њ–Њ–Ї–Њ–µ, —В–∞–Ї –Є –њ—А–Є —Е–Њ–і—М–±–µ (—В–∞–±–ї. 1) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б 1-–є (–Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є) –≥—А—Г–њ–њ–Њ–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Є –≥–Њ–љ–∞—А—В—А–Њ–Ј–µ –Є –Ї–Њ–Ї—Б–∞—А—В—А–Њ–Ј–µ –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –±–Њ–ї–µ–є –њ–Њ –Т–Р–® –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —В–µ—А–∞–њ–Є–Є –•–Њ–љ–і—А–Њ–≥–∞—А–і–Њ–Љ, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –µ–≥–Њ —Е–Њ–љ–і—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ —Б—В—А—Г–Ї—В—Г—А—Г —Е—А—П—Й–∞.
–Я–Њ –і–∞–љ–љ—Л–Љ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–Љ –≤ —В–∞–±–ї–Є—Ж–µ 2, –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Б—В–∞—В–Є—З–µ—Б–Ї–Є—Е –Є –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–є, –∞ —В–∞–Ї–ґ–µ –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В–Є —Б—Г—Б—В–∞–≤–Њ–≤ –њ—А–Є –њ–∞–ї—М–њ–∞—Ж–Є–Є, —З–µ–Љ—Г —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–∞ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–∞—П —В–µ—А–∞–њ–Є—П, –≤–Ї–ї—О—З–∞–≤—И–∞—П –•–Њ–љ–і—А–Њ–≥–∞—А–і –≤ –Ї–∞—З–µ—Б—В–≤–µ –±–∞–Ј–Є—Б–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ю–Р –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ —Б –Э–Я–Т–Я.
–°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —В–µ—А–∞–њ–Є–Є 1-–є –Є 2-–є –≥—А—Г–њ–њ –њ–Њ–Ј–≤–Њ–ї–Є–ї –Њ—Ж–µ–љ–Є—В—М –і–Є–љ–∞–Љ–Є–Ї—Г –±–Њ–ї–µ–є —Г –±–Њ–ї—М–љ—Л—Е –Ю–Р –њ—А–Є —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—В–µ–њ–µ–љ—П—Е —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є —Б—Г—Б—В–∞–≤–Њ–≤.
–°–ї–µ–і—Г–µ—В —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е –Ю–Р 2-–є –≥—А—Г–њ–њ—Л –љ–∞ —Д–Њ–љ–µ –±–∞–Ј–Є—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –•–Њ–љ–і—А–Њ–≥–∞—А–і–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є—П —Б–Њ—Б—В–Њ—П–љ–Є—П –Є —А–∞—Б—И–Є—А–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Ї–Њ–ї–µ–љ–љ—Л—Е –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–ї–Њ—Б—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Њ–њ—В–Є–Љ–Є–Ј–Є—А–Њ–≤–∞–≤—И–µ–є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –Ґ–∞–Ї, —А–∞–Ј–≥–Є–±–∞–љ–Є–µ –≤ –Ї–Њ–ї–µ–љ–љ–Њ–Љ —Б—Г—Б—В–∞–≤–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2-–є –≥—А—Г–њ–њ—Л —Г–≤–µ–ї–Є—З–Є–ї–Њ—Б—М –љ–∞ 23,1±1,12–Њ (—А=0,023), –∞–Љ–њ–ї–Є—В—Г–і–∞ –і–≤–Є–ґ–µ–љ–Є–є –≤–Њ–Ј—А–Њ—Б–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 35,8±1,7–Њ (—А=0,018), —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є—П—Е —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —Б—Г—Б—В–∞–≤–Њ–≤.
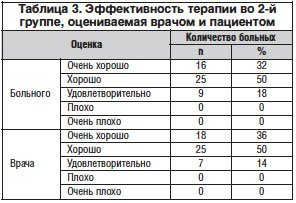
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –њ—А–Є–≤–Њ–і–Є–Љ –і–∞–љ–љ—Л–µ –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –•–Њ–љ–і—А–Њ–≥–∞—А–і–Њ–Љ –≤–Њ 2-–є –≥—А—Г–њ–њ–µ –љ–∞–±–ї—О–і–µ–љ–Є—П, –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ–Њ–є –≤—А–∞—З–Њ–Љ –Є –њ–∞—Ж–Є–µ–љ—В–Њ–Љ, –Ї–Њ—В–Њ—А—Л–µ –Њ—В—А–∞–ґ–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3.
–°–Њ–≥–ї–∞—Б–љ–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ, –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Г 8 (16%) —З–µ–ї–Њ–≤–µ–Ї –≤ 1-–є –≥—А—Г–њ–њ–µ, –∞ —Г 9 (18%) —З–µ–ї–Њ–≤–µ–Ї –≤–Њ 2-–є –≥—А—Г–њ–њ–µ –љ–∞–±–ї—О–і–µ–љ–Є—П –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є—Б—М –љ–µ –±–Њ–ї–µ–µ 2 —Б—Г—В, —В—А–µ–±–Њ–≤–∞–ї–Є –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Є–µ—В—Л –Є –љ–∞–Ј–љ–∞—З–µ–љ–Є—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я. 2 –±–Њ–ї—М–љ—Л–Љ —Б –≥–∞—Б—В—А–∞–ї–≥–Є–µ–є –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞ (–і—А–Њ—В–∞–≤–µ—А–Є–љ, –±–µ–љ—Ж–Є–Ї–ї–∞–љ), –њ—А–Є –≤–Ј–і—Г—В–Є–Є –ґ–Є–≤–Њ—В–∞ –≤ —В–µ—З–µ–љ–Є–µ 3 –і–љ–µ–є 1 –њ–∞—Ж–Є–µ–љ—В –њ—А–Є–љ–Є–Љ–∞–ї –і–Њ–Љ–њ–µ—А–Є–і–Њ–љ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ—Ж–µ–љ–Є–≤–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є, —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Њ–љ–∞ –±—Л–ї–∞ —Е–Њ—А–Њ—И–µ–є –Є –љ–µ —В—А–µ–±–Њ–≤–∞–ї–∞ –Њ—В–Љ–µ–љ—Л –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –љ–∞–±–ї—О–і–µ–љ–Є—П. –Т/–Љ –≤–≤–µ–і–µ–љ–Є–µ –•–Њ–љ–і—А–Њ–≥–∞—А–і–∞ –љ–µ –њ—А–µ–Ї—А–∞—В–Є–ї –љ–Є –Њ–і–Є–љ –±–Њ–ї—М–љ–Њ–є 2-–є –≥—А—Г–њ–њ—Л. –£ 1 –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –Ј–Њ–љ–µ –≤/–Љ –≤–≤–µ–і–µ–љ–Є—П –•–Њ–љ–і—А–Њ–≥–∞—А–і–∞ –љ–∞ –Ї–Њ–ґ–µ —П–≥–Њ–і–Є—Ж –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –µ–і–Є–љ–Є—З–љ—Л–µ –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є–µ –њ–µ—В–µ—Е–Є–Є.
–Ф–µ–ї–∞—П –≤—Л–≤–Њ–і—Л, —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є–Ј—Г—З–µ–љ–Є—П –љ–∞–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –•–Њ–љ–і—А–Њ–≥–∞—А–і–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –±–∞–Ј–Є—Б–љ–Њ–≥–Њ —Е–Њ–љ–і—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Г –±–Њ–ї—М–љ—Л—Е –≥–Њ–љ–∞—А—В—А–Њ–Ј–Њ–Љ –Є –Ї–Њ–Ї—Б–∞—А—В—А–Њ–Ј–Њ–Љ –≤—Л—П–≤–ї–µ–љ–∞ –µ–≥–Њ –≤—Л—А–∞–ґ–µ–љ–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–Љ–µ–љ—М—И–∞—В—М –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –≤ –њ–Њ–Ї–Њ–µ –Є –њ—А–Є —Е–Њ–і—М–±–µ, —А–∞—Б—И–Є—А—П—В—М —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –•–Њ–љ–і—А–Њ–≥–∞—А–і –Њ–±–ї–∞–і–∞–µ—В —Е–Њ—А–Њ—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –њ–Њ –Љ–љ–µ–љ–Є—О –≤—А–∞—З–µ–є –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –і–ї—П —И–Є—А–Њ–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л—Е –Є –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ-–њ–Њ–ї–Є–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Р–ї–µ–Ї—Б–µ–µ–≤–∞ –Ы.–Ш., –¶–≤–µ—В–Ї–Њ–≤–∞ –Х.–°. –Ю—Б—В–µ–Њ–∞—А—В—А–Њ–Ј: –Є–Ј –њ—А–Њ—И–ї–Њ–≥–Њ –≤ –±—Г–і—Г—Й–µ–µ // –Э–∞—Г—З–љ–Њ-–њ—А–∞–Ї—В–Є—З–µ—Б–Ї–∞—П —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П. 2009. вДЦ 2 (–њ—А–Є–ї–Њ–ґ–µ–љ–Є–µ). –°. 31–37.
2. –С–∞–і–Њ–Ї–Є–љ –Т.–Т. –Я—Г—В–Є –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є —В–µ—А–∞–њ–Є–Є –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞ // –†–Ь–Ц. 2006. –Ґ. 14. вДЦ 25. –°. 58–62.
3. –Т–µ—А—В–Ї–Є–љ –Р.–Ы., –Р–ї–µ–Ї—Б–µ–µ–≤–∞ –Ы.–Ш., –Э–∞—Г–Љ–Њ–≤ –Р.–Т. –Є –і—А. –Ю—Б—В–µ–Њ–∞—А—В—А–Њ–Ј –≤ –њ—А–∞–Ї—В–Є–Ї–µ –≤—А–∞—З–∞-—В–µ—А–∞–њ–µ–≤—В–∞ // –†–Ь–Ц. 2008. –Ґ. 16. вДЦ 7. –°. 478–480.
4. –У–Њ—А—П—З–µ–≤ –Ф.–Т. –Ь–µ—Б—В–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Е–Њ–љ–і—А–Њ–Є—В–Є–љ —Б—Г–ї—М—Д–∞—В–∞ –≤ –∞—А—Б–µ–љ–∞–ї–µ —Б—А–µ–і—Б—В–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞ // –†–Ь–Ц. 2008. –Ґ. 16. вДЦ 10. –°. 3–7.
5. –Ф—А–Њ–Ј–і–Њ–≤ –Т.–Э., –Ъ–Є–Љ –Т.–Р. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –Њ—Б—В–µ–Њ–∞—А—В—А–Є—В–∞. –Ь–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є. –Ь.: –Ь–Ш–Ъ, 2010. 23 —Б.
6. –Ъ–∞–Ј–Є–Љ–Є—А–Ї–Њ –Т.–Ъ. –Я–µ—А–≤–Є—З–љ—Л–є (–≤–Њ–Ј—А–∞—Б—В–Ј–∞–≤–Є—Б–Є–Љ—Л–є, –Є–љ–≤–Њ–ї—О—Ж–Є–Њ–љ–љ—Л–є) –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј / –Т.–Ъ. –Ъ–∞–Ј–Є–Љ–Є—А–Ї–Њ, –Т.–Э. –Ъ–Њ–≤–∞–ї–µ–љ–Ї–Њ, –Т.–Ш. –Ь–∞–ї—М—Ж–µ–≤. –Ъ.: –Ь–Ю–†–Ш–Ю–Э, 2006. 176 —Б.
7. –Ъ–∞—А–∞—В–µ–µ–≤ –Р.–Х. –Ы–µ—З–µ–љ–Є–µ –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є // –°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П. 2009. вДЦ 1. –°. 1–8.
8. –С—Г–Ї—Г–њ –Ъ. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ї–Њ—Б—В–µ–є, —Б—Г—Б—В–∞–≤–Њ–≤ –Є –Љ—Л—И—Ж / –њ–µ—А. —Б –∞–љ–≥–ї. –Ь.: –Ь–µ–і. –ї–Є—В., 2007. 320 —Б.
9. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є. –Ю—Б—В–µ–Њ–∞—А—В—А–Є—В. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –≤–µ–і–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –Њ—Б—В–µ–Њ–∞—А—В—А–Є—В–Њ–Љ –Ї–Њ–ї–µ–љ–љ—Л—Е –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ / –њ–Њ–і —А–µ–і. –Ю.–Ь. –Ы–µ—Б–љ—П–Ї. –Ь.: –У–≠–Ю–Ґ–Р–†-–Ь–µ–і–Є–∞, 2006. 176 —Б.
10. –Э–∞—Б–Њ–љ–Њ–≤–∞ –Т.–Р., –Р–ї–µ–Ї—Б–µ–µ–≤–∞ –Ы.–Ш., –Р—А—Е–∞–љ–≥–µ–ї—М—Б–Ї–∞—П –У.–°. –Є –і—А. –Ш—В–Њ–≥–Є –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –°—В—А—Г–Ї—В—Г–Љ –≤ –†–Њ—Б—Б–Є–Є. –Э–Њ–≤—Л–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –≤ –ї–µ—З–µ–љ–Є–Є –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞ –Є –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–∞. –Ь., 2006. –°. 5–7.
11. –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ. –†–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П / –њ–Њ–і —А–µ–і. –Х.–Ы. –Э–∞—Б–Њ–љ–Њ–≤–∞, –Т.–Р. –Э–∞—Б–Њ–љ–Њ–≤–Њ–є. –Ь.: –У–≠–Ю–Ґ–Р–†-–Ь–µ–і–Є–∞, 2008. –°. 573–588.
12. –†–∞—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ь., 2003. –Ґ. 3. –°. 143–149.
13. –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. –®–Ї–Њ–ї–∞ –Ј–і–Њ—А–Њ–≤—М—П. –Ю—Б—В–µ–Њ–∞—А—В—А–Є—В / –њ–Њ–і —А–µ–і. –Ю.–Ь. –Ы–µ—Б–љ—П–Ї. –Ь.: –У–≠–Ю–Ґ–Р–†-–Ь–µ–і–Є–∞, 2008. –°. 81–89.
14. –І–Є—З–∞—Б–Њ–≤–∞ –Э.–Т. –Ь–µ—Б—В–Њ –Љ–µ–і–ї–µ–љ–љ–Њ–і–µ–є—Б—В–≤—Г—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і–µ—Д–Њ—А–Љ–Є—А—Г—О—Й–µ–≥–Њ –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞ // Consislium medicum. 2005. –Ґ. 7. вДЦ 8. –°. 634–638.
15. –І–Є—З–∞—Б–Њ–≤–∞ –Э.–Т. –•–Њ–љ–і—А–Њ–Є—В–Є–љ —Б—Г–ї—М—Д–∞—В (–°—В—А—Г–Ї—В—Г–Љ) –≤ –ї–µ—З–µ–љ–Є–Є –Њ—Б—В–µ–Њ–∞—А—В—А–Њ–Ј–∞: –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М // –†–Ь–Ц. 2009. –Ґ. 17. вДЦ 3. –°. 3–7.
16. Bierma-Zeinstra S., Bohnen A., Ginai A. et al. Validity of American College of Rheumatology criteria for diagnosing hip osteoarthritis in primary care research // J. Rheumatol. 2003. Vol. 26. N 5. P. 1129–1133.
17. Health Care Guideline: Diagnosis and Treatment of Adult Degenerative Joint Disease (DJD) of the knee (Institute for Clinical System Improvement). May 2002. www.icsi.org.
18. Jordan J.M., Kington R.S., Lane L.E. et al. Osteoarthritis: New Insights. Pt I: The disease and its risk factors / Felson D.T., conference chair // Ann. Intern. Med. 2003. Vol. 133. P. 635–646.
19. Kawasaki T., Inoue K., Ushiyama T., Fukuda S. [Assessment of the American College of Rheumatology criteria for the classification and reporting of osteoarthritis of the knee] // Ryumachi. 2003. Vol. 38. N 1. P. 575–588.
20. Loeser R.F.Jr. Aging and the etiopathogenesis and treatment of osteoarthritis // Rheum. Dis. Clin. North Am. 2003. Vol. 26. N 3. P. 547–567.
21. McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. Glucosamine and chondroitin for treatment of osteoarthritis: a systematic quality assessment and meta-analysis // JAMA. 2003. Vol. 283. N 11. P. 1469–1475.












