–Ш–≠ —П–≤–ї—П–µ—В—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —А–µ–і–Ї–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ –і–∞–ґ–µ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–∞ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –µ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П – –±–Њ–ї–µ–Ј–љ—М –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Б —З–∞—Б—В–Њ—В–Њ–є 30 —Б–ї—Г—З–∞–µ–≤ –љ–∞ 1 –Љ–ї–љ –љ–∞—Б–µ–ї–µ–љ–Є—П. –Ч–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –љ–µ—Г–Ї–ї–Њ–љ–љ—Л–Љ —А–Њ—Б—В–Њ–Љ –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є –Љ–Њ–ї–Њ–і—Л—Е –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П —З–Є—Б–ї–∞ –і–µ—В–µ–є —Б –≤—А–Њ–ґ–і–µ–љ–љ—Л–Љ–Є –њ–Њ—А–Њ–Ї–∞–Љ–Є —Б–µ—А–і—Ж–∞ (–Т–Я–°), –Ї–∞–Ї –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е, —В–∞–Ї –Є –љ–µ –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ —Н—В–Њ–Љ—Г –њ–Њ–≤–Њ–і—Г, –∞ —В–∞–Ї–ґ–µ –≤ —Б–≤—П–Ј–Є —Б —И–Є—А–Њ–Ї–Є–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ–Љ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є –љ–∞—А–Ї–Њ–Љ–∞–љ–Є–Є.
–І–∞—Б—В–Њ—В–∞ –Ш–≠ —Г –і–µ—В–µ–є —Б –Т–Я–° –≤ 15–140 —А–∞–Ј –≤—Л—И–µ, —З–µ–Љ –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є, –Є –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –Њ—В 2 –і–Њ 18%, –њ–Њ –і–∞–љ–љ—Л–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е —Ж–µ–љ—В—А–Њ–≤. –Ч–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М –Ш–≠ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ —Г –ї–Є—Ж —Б –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –≤—А–Њ–ґ–і–µ–љ–љ—Л–Љ–Є —Б–µ—А–і–µ—З–љ—Л–Љ–Є –і–µ—Д–µ–Ї—В–∞–Љ–Є. –Ш–≠ –њ–Њ—З—В–Є –љ–µ–Є–Ј–±–µ–ґ–µ–љ —Г –і–µ—В–µ–є —Б –і–µ—Д–µ–Ї—В–Њ–Љ –Љ–µ–ґ–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ–µ—А–µ–≥–Њ—А–Њ–і–Ї–Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–Њ—А—В–∞–ї—М–љ–Њ–є —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є–µ–є. –Я—А–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Ш–≠ –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є –і–µ—В–µ–є —Б –Т–Я–° –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Њ—И–Є–±–Њ–Ї –љ–∞–Є–Љ–µ–љ—М—И–µ–µ, –і–∞–љ–љ—Л–є –≤–∞—А–Є–∞–љ—В –Є–Љ–µ–µ—В –љ–∞–Є–ї—Г—З—И–Є–є –њ—А–Њ–≥–љ–Њ–Ј –Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —Б–∞–Љ—Л–Љ–Є –љ–Є–Ј–Ї–Є–Љ–Є –њ–∞—А–∞–Љ–µ—В—А–∞–Љ–Є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є – –Њ—В 4 –і–Њ 10%. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Ї–ї–∞–њ–∞–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≥–Њ—А–∞–Ј–і–Њ –Љ–µ–і–ї–µ–љ–љ–µ–µ, —З–µ–Љ —Г –ї–Є—Ж —Б –њ–µ—А–≤–Є—З–љ—Л–Љ –Ш–≠.
–Ю—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—П—Б—М –љ–∞ –≤–Њ–њ—А–Њ—Б–∞—Е –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є –Є –і–µ—Д–Є–љ–Є—Ж–Є–є, —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б–Њ—Е—А–∞–љ–Є–ї–Њ—Б—М –≤—Л–і–µ–ї–µ–љ–Є–µ –Ш–≠ –ї–µ–≤—Л—Е –Є –њ—А–∞–≤—Л—Е –Њ—В–і–µ–ї–Њ–≤ —Б–µ—А–і—Ж–∞, –њ—А–Є—З–µ–Љ —Г –і–µ—В–µ–є —Б –Т–Я–° —Н—В–Њ—В –≤–Є–і –Ш–≠ –≤—Б—В—А–µ—З–∞–µ—В—Б—П —З–∞—Й–µ. –Т –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Є –Ј–∞—А—Г–±–µ–ґ–љ–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ —Д–Є–≥—Г—А–Є—А—Г–µ—В —В–µ—А–Љ–Є–љ «–∞–Ї—В–Є–≤–љ—Л–є –Ш–≠», –њ–Њ–і –Ї–Њ—В–Њ—А—Л–Љ –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞—О—В –±–Њ–ї–µ–Ј–љ—М —Б –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–µ–є –ї–Є—Е–Њ—А–∞–і–Ї–Њ–є –Є –њ–Њ–Ј–Є—В–Є–≤–љ–Њ–є –≥–µ–Љ–Њ–Ї—Г–ї—М—В—Г—А–Њ–є, –Є–ї–Є –Ш–≠ —Б –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П —Н–љ–і–Њ–Ї–∞—А–і–∞, –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ—Л–Љ–Є –≤–Њ –≤—А–µ–Љ—П —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞. –Р–Ї—В–Є–≤–љ–Њ—Б—В—М –Ш–≠ –њ—А–Є–Ј–љ–∞–µ—В—Б—П –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ–є, –µ—Б–ї–Є —В–∞–Ї–Њ–≤–∞—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –∞—Г—В–Њ–њ—Б–Є–Є –Є –њ–∞—В–Њ–≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –Я–Њ––њ—А–µ–ґ–љ–µ–Љ—Г –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –≤—Л–і–µ–ї–µ–љ–Є–µ —Б–ї–µ–і—Г—О—Й–Є—Е –≤–Є–і–Њ–≤ –Ш–≠: «—А–∞–љ–љ–Є–є» – —В–Њ—В –Ш–≠, –Ї–Њ—В–Њ—А—Л–є —А–∞–Ј–≤–Є–ї—Б—П –≤ —В–µ—З–µ–љ–Є–µ –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞ —Б–µ—А–і—Ж–µ, –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, «–њ–Њ–Ј–і–љ–Є–є –Ш–≠» – —В–Њ—В, –Ї–Њ—В–Њ—А—Л–є —А–∞–Ј–≤–Є–ї—Б—П —Б–њ—Г—Б—В—П –≥–Њ–і –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞ —Б–µ—А–і—Ж–µ.
–Т—Л–і–µ–ї—П—О—В –Ш–≠, —Б–≤—П–Ј–∞–љ–љ—Л–є —Б —Г—Б—В–∞–љ–Њ–≤–Ї–Њ–є –њ–Њ—Б—В–Њ—П–љ–љ–Њ–≥–Њ –њ–µ–є—Б–Љ–µ–Ї–µ—А–∞ –Є–ї–Є –Ї–∞—А–і–Є–Њ–≤–µ—А—В–µ—А–∞––і–µ—Д–Є–±—А–Є–ї–ї—П—В–Њ—А–∞, –љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л–є –Ш–≠, –љ–µ–љ–Њ–Ј–Њ–Ї–Њ–Љ–Є–∞–ї—М–љ—Л–є –Ш–≠, «–і–Њ–Љ–∞—И–љ–Є–є» –Ш–≠. –Э–∞–Є–±–Њ–ї—М—И–Є–µ –њ—А–Њ–±–ї–µ–Љ—Л –≤—Л–Ј—Л–≤–∞–µ—В —А–∞–Ј–≥—А–∞–љ–Є—З–µ–љ–Є–µ «—А–µ—Ж–Є–і–Є–≤–∞ –Ш–≠» –Є «—А–µ–Є–љ—Д–µ–Ї—Ж–Є–Є –Ш–≠». –Я–Њ–і —А–µ—Ж–Є–і–Є–≤–Њ–Љ –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞—О—В –њ–Њ–≤—В–Њ—А–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–≥–Њ —В–µ–Љ –ґ–µ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ, –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. –њ–Њ—Б–ї–µ –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ —Н–њ–Є–Ј–Њ–і–∞ –±–Њ–ї–µ–Ј–љ–Є. «–†–µ–Є–љ—Д–µ–Ї—Ж–Є—П – –љ–Њ–≤—Л–є –Ш–≠» – —Н—В–Њ –Ш–≠, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–є –і—А—Г–≥–Є–Љ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ, –Є–ї–Є –њ–Њ–≤—В–Њ—А—П—О—Й–Є–є—Б—П —Н–њ–Є–Ј–Њ–і –±–Њ–ї–µ–Ј–љ–Є, –≤—Л–Ј–≤–∞–љ–љ—Л–є —В–µ–Љ –ґ–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–Љ —Б–њ—Г—Б—В—П 6 –Љ–µ—Б. –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї—М–љ–Њ–≥–Њ —Н–њ–Є–Ј–Њ–і–∞.
–Ш–≠ –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ, –њ—А–Є –Ї–Њ—В–Њ—А—Л—Е –≤—Л–і–µ–ї–µ–љ–Є–µ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–≥–µ–љ—В–∞ —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ–µ–є—И–Є–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ –Ї—А–Є—В–µ—А–Є–µ–Љ. –Я–Њ –і–∞–љ–љ—Л–Љ –Ї—А—Г–њ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ –Ї–Њ—В–Њ—А–Њ–Љ —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є —Ж–µ–љ—В—А—Л —Б–Њ –≤—Б–µ—Е –Ї–Њ–љ—В–Є–љ–µ–љ—В–Њ–≤, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–Љ –Ш–≠ –Њ–Ї–∞–Ј–∞–ї—Б—П S. aureus, –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ—Л–є –≤ 31% —Б–ї—Г—З–∞–µ–≤, –њ—А–Є —Н—В–Њ–Љ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –≥–µ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є–µ —А–∞–Ј–ї–Є—З–Є—П. –Т –°–µ–≤–µ—А–љ–Њ–є –Р–Љ–µ—А–Є–Ї–µ —З–∞—Б—В–Њ—В–∞ –≤—Л–і–µ–ї–µ–љ–Є—П S. aureus —Б–Њ—Б—В–∞–≤–Є–ї–∞ 48%, –∞ –≤ –Ѓ–ґ–љ–Њ–є –Р–Љ–µ—А–Є–Ї–µ – 17%. –І–∞—Й–µ –≤—Б–µ–≥–Њ S. aureus –≤—Л–Ј—Л–≤–∞–ї —Н–љ–і–Њ–Ї–∞—А–і–Є—В —Г «–≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е» –љ–∞—А–Ї–Њ–Љ–∞–љ–Њ–≤ (68%). –Я–Њ—Б–ї–µ S. aureus –≤ –њ–Њ—А—П–і–Ї–µ —Г–±—Л–≤–∞–љ–Є—П —З–∞—Б—В–Њ—В—Л –≤—Л–і–µ–ї–µ–љ–Є—П —Б–ї–µ–і–Њ–≤–∞–ї–Є: —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є –≥—А—Г–њ–њ—Л viridans (17%), –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є (11%), Enterococcus spp. (10%), Streptococcus bovis (6%), –і—А—Г–≥–Є–µ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є (6%), –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –±–∞–Ї—В–µ—А–Є–Є –≥—А—Г–њ–њ—Л HACEK (Haemophilus spp., Actinobacillus actinomycetemocomitans, Cardiobacterium hominis, Eikenella corrodens, Kingella kingae – 2%), –≥—А–Є–±—Л (2%), –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –±–∞–Ї—В–µ—А–Є–є (1%). –Т 10% —Б–ї—Г—З–∞–µ–≤ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—М –љ–µ –±—Л–ї –Њ–±–љ–∞—А—Г–ґ–µ–љ. –Т 4% —Б–ї—Г—З–∞–µ–≤ –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є –≤–Є–і—Л –±–∞–Ї—В–µ—А–Є–є, –љ–∞ –Ї–∞–ґ–і—Л–є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М –Љ–µ–љ–µ–µ 1%, —Б—А–µ–і–Є –љ–Є—Е –±—Л–ї–Є Coxiella burnetii, Bartonella spp., Tropheryma whippelii –Є –і—А. –Т–∞–ґ–љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ —Г –і–µ—В–µ–є —А–Њ–ї—М —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –≤ —Н—В–Є–Њ–ї–Њ–≥–Є–Є –Ш–≠ –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –µ—Й–µ –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ–Њ–є. –Ґ–∞–Ї, –љ–∞ S. aureus –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М 57% —Б–ї—Г—З–∞–µ–≤, –∞ –љ–∞ –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–љ–µ–≥–∞—В–Є–≤–љ—Л–µ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є – 14%.
–°—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є (–≥—А—Г–њ–њ–∞ viridans –Є –і—А.). –С–∞–Ї—В–µ—А–Є–Є —Н—В–Њ–є –Њ–±—И–Є—А–љ–Њ–є –≥—А—Г–њ–њ—Л –≤—Е–Њ–і—П—В –≤ —Б–Њ—Б—В–∞–≤ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ–±–Є–Њ—В—Л –њ–Њ–ї–Њ—Б—В–Є —А—В–∞. –І–∞—Й–µ –≤—Б–µ–≥–Њ –Ш–≠ –≤—Л–Ј—Л–≤–∞—О—В –±–ї–Є–Ј–Ї–Њ—А–Њ–і—Б—В–≤–µ–љ–љ—Л–µ –≤–Є–і—Л, –Њ–±—К–µ–і–Є–љ–µ–љ–љ—Л–µ –≤ –≥—А—Г–њ–њ—Г viridans («–Ј–µ–ї–µ–љ—П—Й–Є–µ» – –њ–Њ —Е–∞—А–∞–Ї—В–µ—А—Г –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Ж–≤–µ—В–∞ –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е —Б—А–µ–і, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –Ї—А–Њ–≤—М), –∞ —В–∞–Ї–ґ–µ –±–ї–Є–Ј–Ї–Є–µ –Ї –љ–Є–Љ –±–∞–Ї—В–µ—А–Є–Є –≥—А—Г–њ–њ—Л S. bovis. –Т –њ—А–µ–і–µ–ї–∞—Е –≥—А—Г–њ–њ—Л viridans –≤—Л–і–µ–ї—П—О—В –њ–Њ–і–≥—А—Г–њ–њ—Л S. sanguinis, S. mitis, S. salivarius, S. mutans –Є S. anginosus. –Т –Ї–∞–ґ–і–Њ–є –Є–Ј –њ–Њ–і–≥—А—Г–њ–њ –≤—Л–і–µ–ї—П—О—В –Њ—В 3 –і–Њ 8 –≤–Є–і–Њ–≤. –Ъ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–∞–Љ –≥—А—Г–њ–њ—Л viridans —Б–ї–µ–і—Г–µ—В —В–∞–Ї–ґ–µ –Њ—В–љ–Њ—Б–Є—В—М S. pneumoniae.
–Т—Б–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –≤—Л—И–µ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є –Њ—В–ї–Є—З–∞—О—В—Б—П –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Є—А–Њ–і–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г –Є –і—А—Г–≥–Є–Љ β––ї–∞–Ї—В–∞–Љ–∞–Љ. –§–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Б–≤—П–Ј–∞–љ–Њ —Б –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–µ–є –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Б–≤—П–Ј—Л–≤–∞—О—Й–Є—Е –±–µ–ї–Ї–Њ–≤ (–Я–°–С), –њ—А–Є —Н—В–Њ–Љ –Њ—В–Љ–µ—З–∞—О—В –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ь–Я–Ъ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –Њ—В 0,03–0,125 (–µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–є —Г—А–Њ–≤–µ–љ—М —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є) –і–Њ 0,5–2,0 –Љ–Ї–≥/–Љ–ї –Є —А–µ–і–Ї–Њ –≤—Л—И–µ 2,0 –Љ–Ї–≥/–Љ–ї. –Э–µ–≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї β––ї–∞–Ї—В–∞–Љ–∞–Љ (0,25–2,0 –Љ–Ї–≥/–Љ–ї) –Љ–Њ–ґ–µ—В –±—Л—В—М –њ—А–µ–Њ–і–Њ–ї–µ–љ –њ—Г—В–µ–Љ –њ–Њ–≤—Л—И–µ–љ–Є—П –і–Њ–Ј—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤.
–Ю—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –і–ї—П –≤—Л–±–Њ—А–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј—Л β––ї–∞–Ї—В–∞–Љ–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –±–∞–Ї—В–µ—А–Є–є. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Є–Ј—Г—З–µ–љ–Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ, –≤ —А—П–і–µ —А–µ–≥–Є–Њ–љ–Њ–≤ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Г –њ—А–µ–≤—Л—И–∞–µ—В 10%. –Ъ—А–Њ–Љ–µ β––ї–∞–Ї—В–∞–Љ–Њ–≤, —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є –≥—А—Г–њ–њ—Л viridans —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –Ї —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ (–Њ—Б–Њ–±–µ–љ–љ–Њ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–Љ), —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ–∞–Љ, –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ, —Е–ї–Њ—А–∞–Љ—Д–µ–љ–Є–Ї–Њ–ї—Г, –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ—Г, –ї–Є–љ–µ–Ј–Њ–ї–Є–і—Г –Є –і–∞–њ—В–Њ–Љ–Є—Ж–Є–љ—Г. –Ъ —А–µ–і–Ї–Є–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ –Ш–≠ –Њ—В–љ–Њ—Б—П—В—Б—П β––≥–µ–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–µ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є: S. pyogenes, –∞ —В–∞–Ї–ґ–µ —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Є –≥—А—Г–њ–њ –Т, –° –Є G. –Я–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –±–∞–Ї—В–µ—А–Є–Є –≤—Л—Б–Њ–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –Ї β––ї–∞–Ї—В–∞–Љ–∞–Љ, –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–∞—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї—А–∞–є–љ–µ —А–µ–і–Ї–Њ –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Г —Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤ –≥—А—Г–њ–њ—Л –Т. –Х—Й–µ –±–Њ–ї–µ–µ —А–µ–і–Ї–Є–Љ–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ–Є –Ш–≠ –Љ–Њ–≥—Г—В –±—Л—В—М –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–і–∞–≤–љ–Њ –≤—Л–і–µ–ї–µ–љ–љ—Л–µ –Є–Ј —А–Њ–і–∞ Streptococcus –≤ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–µ —А–Њ–і—Л Abiotrophia spp. –Є Granulicatella spp., –Њ—В–ї–Є—З–∞—О—Й–Є–µ—Б—П –њ–Њ–љ–Є–ґ–µ–љ–љ–Њ–є –њ—А–Є—А–Њ–і–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї β––ї–∞–Ї—В–∞–Љ–∞–Љ.
–≠–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є. –Ъ —А–Њ–і—Г Enterococcus –Њ—В–љ–Њ—Б–Є—В—Б—П –±–Њ–ї–µ–µ 10 –≤–Є–і–Њ–≤, –Њ–і–љ–∞–Ї–Њ –Њ—Б–љ–Њ–≤–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –ї–Є—И—М 2 –Є–Ј –љ–Є—Е: Enterococcus faecalis –Є Enterococcus faecium, –њ—А–Є—З–µ–Љ –љ–∞ E. faecalis –њ—А–Є—Е–Њ–і–Є—В—Б—П –і–Њ 70–85% —Б–ї—Г—З–∞–µ–≤ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –Т–∞–ґ–љ–µ–є—И–Є–Љ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–Њ–Љ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Є—Е –љ–Є–Ј–Ї–∞—П –њ—А–Є—А–Њ–і–љ–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –Љ–љ–Њ–≥–Є—Е –≥—А—Г–њ–њ. –°–љ–Є–ґ–µ–љ–љ–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Ї β––ї–∞–Ї—В–∞–Љ–∞–Љ –Њ–±—К—П—Б–љ—П–µ—В—Б—П –љ–Є–Ј–Ї–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В—М—О –Ї —Н—В–Є–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –Я–°–С5. E. faecalis –њ—А–Њ—П–≤–ї—П–µ—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –њ—А–Є—А–Њ–і–љ—Л–Љ –Є –њ–Њ–ї—Г—Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ, –Њ–і–љ–∞–Ї–Њ –Ь–Я–Ъ —Н—В–Є—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤—Л—И–µ, —З–µ–Љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –і—А—Г–≥–Є—Е –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є. –£–Ї–∞–Ј–∞–љ–љ—Л–є —Д–∞–Ї—В –Њ–±—К—П—Б–љ—П–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П –і–Њ–Ј –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞ –Є –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. E. faecium –Є —А–µ–і–Ї–Є–µ –≤–Є–і—Л —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ —З–∞—Й–µ –≤—Б–µ–≥–Њ —Г—Б—В–Њ–є—З–Є–≤—Л. –Т—Б–µ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є —Г—Б—В–Њ–є—З–Є–≤—Л –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ. –Ш–Ј –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–Њ–≤ —В–Њ–ї—М–Ї–Њ –Є–Љ–Є–њ–µ–љ–µ–Љ –Њ–±–ї–∞–і–∞–µ—В –Ј–љ–∞—З–Є–Љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –њ—А–Є—З–µ–Љ —В–Њ–ї—М–Ї–Њ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є E. faecalis.
–Ш–Ј –і—А—Г–≥–Є—Е –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г–Љ–µ—А–µ–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –њ—А–Њ—П–≤–ї—П—О—В —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ—Л, —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ—Л, —Д–Њ—Б—Д–Њ–Љ–Є—Ж–Є–љ, –Њ–і–љ–∞–Ї–Њ –Њ—Б–љ–Њ–≤–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і–Њ–≤ (–≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞). –≠–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є —Г—Б—В–Њ–є—З–Є–≤—Л –Ї –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ, –Њ–і–љ–∞–Ї–Њ –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б β––ї–∞–Ї—В–∞–Љ–∞–Љ–Є –Њ–љ–Є –њ—А–Њ—П–≤–ї—П—О—В —Б–Є–љ–µ—А–≥–Є–Ј–Љ, –±–Њ–ї–µ–µ —В–Њ–≥–Њ – –µ—Й–µ –Є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М. –Я—А–Є—А–Њ–і–љ–Њ –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Ї –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ —Б–ї–µ–і—Г–µ—В –Њ—В–ї–Є—З–∞—В—М –Њ—В –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–≥–Њ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є. –Ы–µ—З–µ–љ–Є–µ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Њ—Б–ї–Њ–ґ–љ—П–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –љ–Є–Ј–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –њ—А–Є—А–Њ–і–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П, –љ–Њ –Є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є. –°—А–µ–і–Є E. faecium —И–Є—А–Њ–Ї–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–∞ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–∞—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–∞—П –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–µ–є –Я–°–С5, –њ—А–Є —Н—В–Њ–Љ E. faecalis, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —Б–Њ—Е—А–∞–љ—П—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М.
–Ф–ї—П E. faecalis –њ—А–Њ–±–ї–µ–Љ–Њ–є —П–≤–ї—П–µ—В—Б—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –Ї –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ, –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –Х–≤—А–Њ–њ—Л —Н—В–Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –і–Њ—Б—В–Є–≥–∞–µ—В 50%. –Ь–µ—Е–∞–љ–Є–Ј–Љ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –Ї –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –њ—А–Є–Њ–±—А–µ—В–µ–љ–Є–Є –±–∞–Ї—В–µ—А–Є—П–Љ–Є –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і––Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–Є—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤. –Т–∞–ґ–љ–Њ, —З—В–Њ –њ—А–Є —Н—В–Њ–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–µ —Г—В—А–∞—З–Є–≤–∞—О—В—Б—П —Б–Є–љ–µ—А–≥–Є–Ј–Љ —Б β––ї–∞–Ї—В–∞–Љ–∞–Љ–Є –Є –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М.
–°—А–µ–і–Є E. faecium –≥–ї–Њ–±–∞–ї—М–љ–Њ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –≤ –≥–Њ—Б–њ–Є—В–∞–ї—М–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ–Њ–ї—Г—З–Є–ї–∞ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і–∞–Љ, —Б—А–µ–і–Є E. faecalis —Н—В–Њ —П–≤–ї–µ–љ–Є–µ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —А–µ–і–Ї–Њ. –Т–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–—Г—Б—В–Њ–є—З–Є–≤—Л–µ —И—В–∞–Љ–Љ—Л E. faecium —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ—Л –Є –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є —Б—В–µ–њ–µ–љ—М –њ–Њ–≤—Л—И–µ–љ–Є—П –Ь–Я–Ъ –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–∞ –Є —В–µ–є–Ї–Њ–њ–ї–∞–љ–Є–љ–∞ –Љ–Њ–ґ–µ—В –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –≤ —И–Є—А–Њ–Ї–Є—Е –њ—А–µ–і–µ–ї–∞—Е. –Т–∞–ґ–љ–Њ, —З—В–Њ –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ–—Г—Б—В–Њ–є—З–Є–≤—Л–µ E. faecalis —З–∞—Б—В–Њ —Б–Њ—Е—А–∞–љ—П—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–∞–Љ, —З—В–Њ –Њ—Б—В–∞–≤–ї—П–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –і–ї—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј —Н—В–Є—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –®—В–∞–Љ–Љ—Л –ґ–µ E. faecium, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ —Г—Б—В–Њ–є—З–Є–≤—Л, —З—В–Њ —В—А–µ–±—Г–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї –ї–Є–љ–µ–Ј–Њ–ї–Є–і –Є –і–∞–њ—В–Њ–Љ–Є—Ж–Є–љ.
–°—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є. –Ю—Б–≤–µ—Й–µ–љ–Є–µ —А–Њ–ї–Є —Н—В–Є—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є —В—А–µ–±—Г–µ—В –Њ—Б–Њ–±–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П. –Т –њ—А–µ–і–µ–ї–∞—Е —А–Њ–і–∞ Staphylococcus –≤—Л–і–µ–ї—П—О—В –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ –±–∞–Ї—В–µ—А–Є–Є (S. aureus) –Є –≥—А—Г–њ–њ—Г –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е (Coagulase–Negative Staphylococcus – CoNS), –њ–Њ—Б–ї–µ–і–љ–Є–µ –љ–∞ –њ—А–∞–Ї—В–Є–Ї–µ —З–∞—Б—В–Њ –љ–µ –Є–і–µ–љ—В–Є—Д–Є—Ж–Є—А—Г—О—В –і–Њ –≤–Є–і–∞. –°—А–µ–і–Є –Ї–Њ–∞–≥—Г–ї–∞–Ј–Њ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л—Е —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ – –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є —Н–љ–і–Њ–Ї–∞—А–і–Є—В–∞ –і–Њ–Љ–Є–љ–Є—А—Г—О—В S. epidermidis, —В–∞–Ї–Є–µ –≤–Є–і—Л, –Ї–∞–Ї S. schleiferi, S. lugdunensis –Є S. haemolyticus –≤—Б—В—А–µ—З–∞—О—В—Б—П –≥–Њ—А–∞–Ј–і–Њ —А–µ–ґ–µ. CoNS –Љ–µ–љ–µ–µ –≤–Є—А—Г–ї–µ–љ—В–љ—Л, —З–µ–Љ S. aureus –Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –≤—Л–Ј—Л–≤–∞—О—В —Н–љ–і–Њ–Ї–∞—А–і–Є—В—Л –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ—Л—Е –Ї–ї–∞–њ–∞–љ–Њ–≤ –Є –њ—А–∞–≤–Њ—Б—В–Њ—А–Њ–љ–љ–Є–µ —Н–љ–і–Њ–Ї–∞—А–і–Є—В—Л —Г «–≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е» –љ–∞—А–Ї–Њ–Љ–∞–љ–Њ–≤. –Ш—Б–Ї–ї—О—З–µ–љ–Є–µ —Б–Њ—Б—В–∞–≤–ї—П–µ—В S. lugdunensis, –њ–Њ —Г—А–Њ–≤–љ—О –≤–Є—А—Г–ї–µ–љ—В–љ–Њ—Б—В–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л–є —Б S. aureus. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ—П–≤–ї—П—О—В—Б—П —Б–Њ–Њ–±—Й–µ–љ–Є—П –Њ —А–Њ–ї–Є CoNS –≤ —Н—В–Є–Њ–ї–Њ–≥–Є–Є —Н–љ–і–Њ–Ї–∞—А–і–Є—В–Њ–≤ –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л—Е –Ї–ї–∞–њ–∞–љ–Њ–≤.
–Я–Њ —Г—А–Њ–≤–љ—О –њ—А–Є—А–Њ–і–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–є —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є S. aureus –Є CoNS –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П. β––ї–∞–Ї—В–∞–Љ—Л –≤ —Ж–µ–ї–Њ–Љ –Њ—В–ї–Є—З–∞—О—В—Б—П –љ–∞–Є–±–Њ–ї—М—И–µ–є –∞–љ—В–Є—Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –љ–Њ –Љ–µ–ґ–і—Г –Њ—В–і–µ–ї—М–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—П–Љ–Є —Н—В–Њ–є –≥—А—Г–њ–њ—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є–Љ–µ—О—В—Б—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П. –Т —Б–≤—П–Ј–Є —Б —И–Є—А–Њ–Ї–Є–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ–Љ —Б—А–µ–і–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –њ–ї–∞–Ј–Љ–Є–і–љ—Л—Е β––ї–∞–Ї—В–∞–Љ–∞–Ј –њ—А–Є—А–Њ–і–љ—Л–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –Є –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –і–∞–≤–љ–Њ —Г—В—А–∞—В–Є–ї–Є —Б–≤–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –£—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤—Л–Љ β––ї–∞–Ї—В–∞–Љ–∞–Ј–∞–Љ –њ—А–Њ—П–≤–ї—П—О—В –Є–Ј–Њ–Ї—Б–∞–Ј–Њ–ї–Є–ї––њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, –Ј–∞—Й–Є—Й–µ–љ–љ—Л–µ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л, —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л –Є –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ—Л.
–Ш—Б—В–Њ—А–Є—З–µ—Б–Ї–Є –њ–µ—А–≤—Л–Љ –Є–Ј–Њ–Ї—Б–∞–Ј–Њ–ї–Є–ї––њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ–Њ–Љ –±—Л–ї –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ, —Г—В—А–∞—В–Є–≤—И–Є–є –Ј–љ–∞—З–µ–љ–Є–µ –Є–Ј––Ј–∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–Є–Ј–Ї–Њ–є —Б—В–∞–±–Є–ї—М–љ–Њ—Б—В–Є –Є –≤—Л—Б–Њ–Ї–Њ–є —В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є. –Т –†–Њ—Б—Б–Є–Є –Є–Ј —Н—В–Њ–є –≥—А—Г–њ–њ—Л –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ –Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ, –≤ –і—А—Г–≥–Є—Е —Б—В—А–∞–љ–∞—Е – –љ–∞—Д—Ж–Є–ї–ї–Є–љ, –Ї–ї–Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ –Є –∞–љ–∞–ї–Њ–≥–Є, —А–∞–Ј–ї–Є—З–∞—О—Й–Є–µ—Б—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –њ–Њ —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞–Љ. –°—А–µ–і–Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ –љ–∞–Є–±–Њ–ї—М—И–µ–є –∞–љ—В–Є—Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Њ–±–ї–∞–і–∞—О—В –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–Є I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П (—Ж–µ—Д–∞–Ј–Њ–ї–Є–љ), –∞ —В–∞–Ї–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, –Ї–∞–Ї —Ж–µ—Д—В–∞–Ј–Є–і–Є–Љ, –µ–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –ї–Є—И–µ–љ—Л. –Т–Њ–њ—А–Њ—Б –Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –Ј–љ–∞—З–µ–љ–Є–Є —А–∞–Ј–ї–Є—З–Є–є in vitro –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ–ґ–і—Г –Њ—В–і–µ–ї—М–љ—Л–Љ–Є β––ї–∞–Ї—В–∞–Љ–∞–Љ–Є –љ–µ —А–µ—И–µ–љ. –Я–Њ –і–∞–љ–љ—Л–Љ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ, —Ж–µ—Д—В—А–Є–∞–Ї—Б–Њ–љ, –∞ —В–∞–Ї–ґ–µ –Ј–∞—Й–Є—Й–µ–љ–љ—Л–µ –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л –њ—А–Њ—П–≤–ї—П–ї–Є –Љ–µ–љ—М—И—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–є –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–Є (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –≤—Л–Ј–≤–∞–љ–љ–Њ–є —Н–љ–і–Њ–Ї–∞—А–і–Є—В–Њ–Љ), —З–µ–Љ –Ї–ї–Њ–Ї—Б–∞—Ж–Є–ї–ї–Є–љ –Є —Ж–µ—Д–∞–Ј–Њ–ї–Є–љ.
–Ъ—А–Њ–Љ–µ β––ї–∞–Ї—В–∞–Љ–Њ–≤ —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є —В–∞–Ї–ґ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –Љ–љ–Њ–≥–Є—Е –і—А—Г–≥–Є—Е –≥—А—Г–њ–њ: –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ, –ї–Є–љ–Ї–Њ–Ј–∞–Љ–Є–і–∞–Љ, –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ, —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ–∞–Љ, –Ї–Њ–—В—А–Є–Љ–Њ–Ї—Б–∞–Ј–Њ–ї—Г, —Е–ї–Њ—А–∞–Љ—Д–µ–љ–Є–Ї–Њ–ї—Г, —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ, —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ—Г –Є –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і–∞–Љ.
–Х—Б–ї–Є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤, —Б–≤—П–Ј–∞–љ–љ—Г—О —Б –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є β––ї–∞–Ї—В–∞–Љ–∞–Ј, –ї–µ–≥–Ї–Њ –њ—А–µ–Њ–і–Њ–ї–µ–≤–∞—О—В –Љ–љ–Њ–≥–Є–µ β––ї–∞–Ї—В–∞–Љ–љ—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, —В–Њ –њ–Њ—П–≤–ї–µ–љ–Є–µ —Г —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Б–≤—П–Ј—Л–≤–∞—О—Й–µ–≥–Њ –±–µ–ї–Ї–∞ (–Я–°–С2–∞) —Б–Њ —Б–љ–Є–ґ–µ–љ–љ–Њ–є –∞—Д—Д–Є–љ–љ–Њ—Б—В—М—О –Ї β––ї–∞–Ї—В–∞–Љ–∞–Љ –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Ї–Њ –≤—Б–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ —Н—В–Њ–є –≥—А—Г–њ–њ—Л, –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –љ–Њ–≤—Л—Е —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–Њ–≤ (—Ж–µ—Д—В–Њ–±–Є–њ—А–Њ–ї–∞ –Є —Ж–µ—Д–∞—В–∞—А–Њ–ї–Є–љ–∞). –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г —Д–µ–љ–Њ—В–Є–њ–Є—З–µ—Б–Ї–Є–Љ –Љ–∞—А–Ї–µ—А–Њ–Љ –љ–∞–ї–Є—З–Є—П —Г –±–∞–Ї—В–µ—А–Є–є –Я–°–С2–∞ —П–≤–ї—П–µ—В—Б—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Ї –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—Г, —В–Њ –Є—Б—В–Њ—А–Є—З–µ—Б–Ї–Є –Ј–∞ —И—В–∞–Љ–Љ–∞–Љ–Є S. aureus, –Њ–±–ї–∞–і–∞—О—Й–Є–Љ–Є —Н—В–Є–Љ –±–µ–ї–Ї–Њ–Љ, –Ј–∞–Ї—А–µ–њ–Є–ї–Њ—Б—М –љ–∞–Ј–≤–∞–љ–Є–µ MRSA (Methicillin–Resistant Staphylococcus aureus). –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г–Ї–∞–Ј–∞–љ–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —И–Є—А–Њ–Ї–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ –Є —Б—А–µ–і–Є CoNS.
–Т —Б–Є–ї—Г —А—П–і–∞ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –љ–∞–ї–Є—З–Є–µ —Г —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤ –Я–°–С2–∞ –Њ—З–µ–љ—М —З–∞—Б—В–Њ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М—О –Ї –і—А—Г–≥–Є–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ, —З—В–Њ —А–µ–Ј–Ї–Њ —Б—Г–ґ–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Н—В–Є–Њ—В—А–Њ–њ–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Т —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е –ї–µ—В —Б—А–µ–і—Б—В–≤–Њ–Љ –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–є, –≤—Л–Ј—Л–≤–∞–µ–Љ—Л—Е –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–∞–Љ–Є, –±—Л–ї–Є –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і—Л (–≤ –†–Њ—Б—Б–Є–Є – –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ), –љ–Њ –≤ 1997 –≥. –±—Л–ї–Є –Њ–њ–Є—Б–∞–љ—Л –њ–µ—А–≤—Л–µ –Є–Ј–Њ–ї—П—В—Л —Б–Њ —Б–љ–Є–ґ–µ–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ—Г. –Ь–µ—Е–∞–љ–Є–Ј–Љ —Н—В–Њ–≥–Њ —П–≤–ї–µ–љ–Є—П –љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ, –Є–Ј––Ј–∞ –Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Є—Е —В—А—Г–і–љ–Њ—Б—В–µ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Є–Ј—Г—З–µ–љ–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –Є–Ј–Њ–ї—П—В–Њ–≤ —Б–Њ —Б–љ–Є–ґ–µ–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ —А—П–і–∞ –њ—А–Њ—Д–µ—Б—Б–Є–Њ–љ–∞–ї—М–љ—Л—Е —Б–Њ–Њ–±—Й–µ—Б—В–≤ –°–µ–≤–µ—А–љ–Њ–є –Р–Љ–µ—А–Є–Ї–Є, –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ –±—Г–і–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, –µ—Б–ї–Є –µ–≥–Њ –Ь–Я–Ъ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –љ–µ –њ—А–µ–≤—Л—И–∞–µ—В 1,0 –Љ–Ї–≥/–Љ–ї, –∞ –Ї–Њ–љ–µ—З–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є – –љ–µ –Љ–µ–љ–µ–µ 15–20 –Љ–Ї–≥/–Љ–ї. –Я—А–Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є—Е –Ј–љ–∞—З–µ–љ–Є—П—Е –Ь–Я–Ъ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –љ–Њ–≤—Л–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є –ї–Є–љ–µ–Ј–Њ–ї–Є–і –Є–ї–Є –і–∞–њ—В–Њ–Љ–Є—Ж–Є–љ.
–†–µ–і–Ї–Є–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–Є –Ш–≠ – –≥—А—Г–њ–њ–∞ HACEK (Haemophilus aphrophilus, Actinobacillus actinomycetemocomitans, Cardiobacterium hominis, Eikenella corrodens, Kingella kingae). –Я–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –±–∞–Ї—В–µ—А–Є–Є —П–≤–ї—П—О—В—Б—П –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Д–ї–Њ—А—Л –њ–Њ–ї–Њ—Б—В–Є —А—В–∞, –Њ–±–ї–∞–і–∞—О—В —Б–ї–Њ–ґ–љ—Л–Љ–Є –њ–Є—В–∞—В–µ–ї—М–љ—Л–Љ–Є –њ–Њ—В—А–µ–±–љ–Њ—Б—В—П–Љ–Є –Є —Б—Е–Њ–і–љ–Њ–є –≤—Л—Б–Њ–Ї–Њ–є –њ—А–Є—А–Њ–і–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї β––ї–∞–Ї—В–∞–Љ–∞–Љ, –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ, —Д—В–Њ—А—Е–Є–љ–Њ–ї–Њ–љ–∞–Љ, —Е–ї–Њ—А–∞–Љ—Д–µ–љ–Є–Ї–Њ–ї—Г, —В–µ—В—А–∞—Ж–Є–Ї–ї–Є–љ–∞–Љ, —А–Є—Д–∞–Љ–њ–Є—Ж–Є–љ—Г –Є –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ. –Э–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї–µ–µ —Г–Ј–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Њ—В–ї–Є—З–∞—О—В—Б—П –ї–Є—И—М E. corrodens, —Г—Б—В–Њ–є—З–Є–≤—Л–µ –Ї –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ/–ї–Є–љ–Ї–Њ–Ј–∞–Љ–Є–і–∞–Љ –Є —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ I –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є —Г–Љ–µ—А–µ–љ–љ–Њ —Г—Б—В–Њ–є—З–Є–≤—Л–µ –Ї –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і–∞–Љ. –Ш–Ј –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ β––ї–∞–Ї—В–∞–Љ–∞–Ј, –≥–Є–і—А–Њ–ї–Є–Ј—Г—О—Й–Є—Е –∞–Љ–Є–љ–Њ–њ–µ–љ–Є—Ж–Є–ї–ї–Є–љ—Л. –¶–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ—Л III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —Б–Њ—Е—А–∞–љ—П—О—В –њ–Њ–ї–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М.
–Ф—А—Г–≥–Є–µ –≥—А–∞–Љ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ –±–∞–Ї—В–µ—А–Є–Є. –Ш–≠ –Љ–Њ–≥—Г—В —В–∞–Ї–ґ–µ –≤—Л–Ј—Л–≤–∞—В—М –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–Є —Б–µ–Љ–µ–є—Б—В–≤–∞ Enterobacteriaceae, Pseudomonas aeruginosa, Acinetobacter spp., –∞ —В–∞–Ї–ґ–µ Neisseria spp. –Є Moraxella spp. –Я—А–Є—А–Њ–і–љ–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–∞—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –±–∞–Ї—В–µ—А–Є–є –≤–∞—А—М–Є—А—Г—О—В –≤ —И–Є—А–Њ–Ї–Є—Е –њ—А–µ–і–µ–ї–∞—Е. –І–∞—Й–µ –≤—Б–µ–≥–Њ –љ–∞–±–ї—О–і–∞—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ–∞–Љ III –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Є –Ї–∞—А–±–∞–њ–µ–љ–µ–Љ–∞–Љ.
–Т–Њ–Ј–±—Г–і–Є—В–µ–ї–Є «–Ї—Г–ї—М—В—Г—А–∞–ї—М–љ–Њ––љ–µ–≥–∞—В–Є–≤–љ—Л—Е» —Н–љ–і–Њ–Ї–∞—А–і–Є—В–Њ–≤. –Ю—В—Б—Г—В—Б—В–≤–Є–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ї—А–Њ–≤–Є –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ –Ї–∞–Ї —Б –Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ–≥—А–µ—И–љ–Њ—Б—В—П–Љ–Є (–њ–Њ–ї—Г—З–µ–љ–Є–µ –Љ–∞–ї–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ –Ї—А–Њ–≤–Є, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–∞—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є–љ–Ї—Г–±–∞—Ж–Є–Є –њ–Њ—Б–µ–≤–Њ–≤, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –љ–µ–∞–і–µ–Ї–≤–∞—В–љ—Л—Е –Є–ї–Є –љ–µ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е —Б—А–µ–і), —В–∞–Ї –Є —Б –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є (–њ–Њ–ї—Г—З–µ–љ–Є–µ –Љ–∞—В–µ—А–Є–∞–ї–∞ –љ–∞ —Д–Њ–љ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞–ї–Є—З–Є–µ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є, –љ–µ –Ї—Г–ї—М—В–Є–≤–Є—А—Г–µ–Љ—Л—Е –љ–∞ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е —Б—А–µ–і–∞—Е). –Ъ —В–∞–Ї–Є–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П–Љ –Њ—В–љ–Њ—Б—П—В—Б—П Coxiella burnetii, Bartonella spp., Tropheryma whipplei, Legionella spp., Chlamydia spp., Mycobacterium spp. –Ф–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П —Н—В–Є–Њ–ї–Њ–≥–Є–Є «–Ї—Г–ї—М—В—Г—А–∞–ї—М–љ–Њ––љ–µ–≥–∞—В–Є–≤–љ—Л—Е» —Н–љ–і–Њ–Ї–∞—А–і–Є—В–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —В–µ—Б—В—Л, –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л —В–∞–Ї–ґ–µ –Њ—В–Ї—А—Л–≤–∞—О—В—Б—П —Б –≤–љ–µ–і—А–µ–љ–Є–µ–Љ –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –Њ—Б–љ–Њ–≤–∞–љ–љ—Л—Е –љ–∞ –∞–Љ–њ–ї–Є—Д–Є–Ї–∞—Ж–Є–Є –≥–µ–љ–Њ–≤ 16S —А–†–Э–Ъ –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ —Б–µ–Ї–≤–µ–љ–Є—А–Њ–≤–∞–љ–Є–Є –∞–Љ–њ–ї–Є–Ї–Њ–љ–Њ–≤.
–Ф–ї—П –Њ—А–Є–µ–љ—В–Є—А–∞ –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—М –Ш–≠ –Є –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П —Н–Љ–њ–Є—А–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ (—В–∞–±–ї. 1).
–°–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П –Ї–Њ–љ—Ж–µ–њ—Ж–Є—П –Ш–≠ –Ї–∞–Ї –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ, —В–∞–Ї –Є –Ј–∞ —А—Г–±–µ–ґ–Њ–Љ –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞–µ—В –Њ–і–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤ —Б—В–Њ—А–Њ–љ—Г –Є—Е —Г—Б—Г–≥—Г–±–ї–µ–љ–Є—П –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±–µ–Ј –Ї–∞–Ї–Њ–є––ї–Є–±–Њ —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –Є —В–µ–Љ –±–Њ–ї–µ–µ —Б–∞–Љ–Њ–Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П. –Я–Њ—Н—В–Њ–Љ—Г –љ–Є –Њ –Ї–∞–Ї–Њ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ —В–µ—З–µ–љ–Є–Є –Ш–≠ (—В–∞–Ї–Њ–є –і–Є–∞–≥–љ–Њ–Ј –Љ–Њ–ґ–љ–Њ –≤—Б—В—А–µ—В–Є—В—М –≤ –†–§ –≤ –≤—Л–њ–Є—Б–Ї–∞—Е –Є–Ј —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Њ—В–і–µ–ї–µ–љ–Є–є) —А–µ—З–Є –±—Л—В—М –љ–µ –Љ–Њ–ґ–µ—В.
–°—В–∞–љ–і–∞—А—В–Њ–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ш–≠ –њ–Њ––њ—А–µ–ґ–љ–µ–Љ—Г —П–≤–ї—П—О—В—Б—П –Ї—А–Є—В–µ—А–Є–Є Duke, –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–µ Li et al. (2000). –Я—А–Є–Ј–љ–∞—О—В, —З—В–Њ –Ї–∞–Ї —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М, —В–∞–Ї –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М –Ї—А–Є—В–µ—А–Є–µ–≤ Duke –њ—А–Є–Љ–µ—А–љ–Њ —А–∞–≤–љ–∞ 80%, —З—В–Њ –Њ–љ–Є –≤–µ—Б—М–Љ–∞ –њ–Њ–ї–µ–Ј–љ—Л –і–ї—П –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є—П –Ш–≠, –љ–Њ –љ–µ –≤—Б–µ–≥–і–∞ –њ—А–Є–≥–Њ–і–љ—Л –і–ї—П –њ—А–Є–љ—П—В–Є—П –Ї–Њ–љ–Ї—А–µ—В–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–µ—И–µ–љ–Є–є.
–Т—Л—П–≤–ї—П–µ—В—Б—П –Ш–≠ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —Н—Е–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є–Є (–≠—Е–Њ––Ъ–У) –Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П –≤ –Ї—Г–ї—М—В—Г—А–∞—Е –Ї—А–Њ–≤–Є. –≠—В–Њ –і–≤–∞ «–±–Њ–ї—М—И–Є—Е» –Ї—А–Є—В–µ—А–Є—П –Ш–≠. –≠—Е–Њ––Ъ–У —П–≤–ї—П–µ—В—Б—П –Љ–µ—В–Њ–і–Њ–Љ –≤—Л–±–Њ—А–∞ –і–ї—П –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є—П —В–Є–њ–Є—З–љ–Њ–≥–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—Г–±—Б—В—А–∞—В–∞ –Ш–≠ – –≤–µ–≥–µ—В–∞—Ж–Є–є, –њ—А–Є—З–µ–Љ —З—А–µ—Б–њ–Є—Й–µ–≤–Њ–і–љ–∞—П –≠—Е–Њ––Ъ–У —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ. –Я–Њ––њ—А–µ–ґ–љ–µ–Љ—Г 3 –Ј–∞–±–Њ—А–∞ –Ї—А–Њ–≤–Є –љ–∞ –≥–µ–Љ–Њ–Ї—Г–ї—М—В—Г—А—Г –і–Њ–ї–ґ–љ—Л –±—Л—В—М –≤—Л–њ–Њ–ї–љ–µ–љ—Л –Є–Ј –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –≤–µ–љ –њ–Њ—Б–ї–µ –і–µ–Ј–Є–љ—Д–µ–Ї—Ж–Є–Є –Ї–Њ–ґ–Є –і–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤. –Я—А–Є —Н—В–Њ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –Љ–Њ–Љ–µ–љ—В –≤–Ј—П—В–Є—П –Ї—А–Њ–≤–Є –љ–µ –Є–Љ–µ–µ—В –Ј–љ–∞—З–µ–љ–Є—П.
–Т–Њ–њ—А–Њ—Б—Л –≥–Є–њ–µ—А–і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ш–≠ –≤ —Б–≤—П–Ј–Є —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –≠—Е–Њ––Ъ–У —Б–Њ—Е—А–∞–љ—П—О—В —Б–≤–Њ—О –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М. –С–Њ–ї—М—И–Є–µ –Ј–∞—В—А—Г–і–љ–µ–љ–Є—П –≤—Л–Ј—Л–≤–∞–µ—В —В—А–∞–Ї—В–Њ–≤–Ї–∞ –≤–µ–≥–µ—В–∞—Ж–Є–є –њ—А–Є —В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Њ–Љ –љ–µ–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–Љ —Н–љ–і–Њ–Ї–∞—А–і–Є—В–µ (–Ґ–Э–С–≠), –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М –≤—Л—П–≤–ї–µ–љ—Л —Г –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –Є–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–∞—А–і–Є–∞–ї–≥–Є—П–Љ–Є. –Э–Њ —Б–∞–Љ–Њ–µ —Б–ї–Њ–ґ–љ–Њ–µ – –Њ—В–≤–µ—А–≥–љ—Г—В—М –Ш–≠, –µ—Б–ї–Є –≤–µ–≥–µ—В–∞—Ж–Є–Є –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞—О—В —Г –ї–Є—Е–Њ—А–∞–і—П—Й–µ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ, –∞ –ї–Є—Е–Њ—А–∞–і–Ї–∞, –Ї–∞–Ї –њ–Њ—В–Њ–Љ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л—П—Б–љ–µ–љ–Њ, —Б–≤—П–Ј–∞–љ–∞ —Б –љ–∞–ї–Є—З–Є–µ–Љ –Њ–њ—Г—Е–Њ–ї–Є –Є–ї–Є –Є–љ–Њ–≥–Њ –Њ—З–∞–≥–∞ –Є–љ—Д–µ–Ї—Ж–Є–Є (–≥–∞–є–Љ–Њ—А–Є—В, –Є–љ—Д–µ–Ї—Ж–Є–Є –Љ–Њ—З–µ–≤—Л—Е –њ—Г—В–µ–є, –Њ–њ–Є—Б—В–Њ—А—Е–Њ–Ј –Є —В.–і.). –Ґ–Э–С–≠ –Љ–Њ–ґ–µ—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—В—М —В–µ—З–µ–љ–Є–µ —Б–Є—Б—В–µ–Љ–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (–њ—Б–µ–≤–і–Њ—В—Г–±–µ—А–Ї—Г–ї–µ–Ј, –±–Њ–ї–µ–Ј–љ—М –Ы–∞–є–Љ–∞, –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–є –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–Њ–Ј) –Є–ї–Є, –љ–∞–њ—А–Є–Љ–µ—А, —В–∞–Ї–Њ–µ —А–µ–і–Ї–Њ–µ —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ, –Ї–∞–Ї –±–Њ–ї–µ–Ј–љ—М –С–µ—Е—З–µ—В–∞. –Я—А–Є –Ґ–Э–С–≠ —В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–µ –љ–∞–ї–Њ–ґ–µ–љ–Є—П —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ –Ї–ї–∞–њ–∞–љ–∞—Е –ї–µ–≤–Њ–є –њ–Њ–ї–Њ–≤–Є–љ—Л —Б–µ—А–і—Ж–∞, –Њ–±—Л—З–љ–Њ –љ–∞ –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Љ–Є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞, –Њ–љ–Є –Љ–∞–ї–µ–љ—М–Ї–Є–µ (–љ–µ –±–Њ–ї–µ–µ 2–3–4 –Љ–Љ) –Є «—Б–Є–і—П—Й–Є–µ» –љ–∞ —И–Є—А–Њ–Ї–Њ–Љ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є. –£ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —З–∞—Б—В–Є —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ—Л –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–ї–Є –≥–µ–љ—Л —В—А–Њ–Љ–±–Њ—Д–Є–ї–Є–Є, –Є–љ–Њ–≥–і–∞ – –Є—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О.
–Ш–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є—П –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П – –љ–∞–Є–±–Њ–ї–µ–µ —Г—П–Ј–≤–Є–Љ–Њ–µ –Љ–µ—Б—В–Њ –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Ш–≠, –∞ –≤–µ–і—М —Н—В–Њ –Њ–і–Є–љ –Є–Ј –і–≤—Г—Е «–±–Њ–ї—М—И–Є—Е» –Ї—А–Є—В–µ—А–Є–µ–≤ Duke. –Ф–∞–љ–љ–∞—П –њ—А–Њ–±–ї–µ–Љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–∞ –љ–µ —В–Њ–ї—М–Ї–Њ —Б–Њ —Б–ї–∞–±—Л–Љ —А–∞–Ј–≤–Є—В–Є–µ–Љ –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–є –±–∞–Ј—Л, –љ–Њ –Є —Б –њ–Њ—П–≤–ї–µ–љ–Є–µ–Љ –љ–µ–Ї—Г–ї—М—В–Є–≤–Є—А—Г–µ–Љ—Л—Е –Љ–Є–Ї—А–Њ–±–Њ–≤. –Я–Њ—Н—В–Њ–Љ—Г —В–∞–Ї –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Љ–µ—В–Њ–і—Л –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–є – –њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–Њ–є —Ж–µ–њ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є. –Э–Њ–≤—Л–Љ —П–≤–ї—П–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–µ—В–Њ–і–Є–Ї–Є FISH – —Ж–Є—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ф–Э–Ъ––њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є –≤ —Е—А–Њ–Љ–Њ—Б–Њ–Љ–∞—Е.
–Ф–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Г—О –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –Ш–≠ —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –њ—А–Њ–≤–Њ–і—П—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б —Б–Є—Б—В–µ–Љ–љ—Л–Љ–Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї—А—Г–≥–∞.
–Я—А–Є –Њ—Б—В—А–Њ–є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –ї–Є—Е–Њ—А–∞–і–Ї–µ (–Ю–†–Ы), –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–µ—А–≤–Є—З–љ–Њ–≥–Њ –Ш–≠, –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞–µ—В—Б—П —Е—А–Њ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Б–≤—П–Ј—М —Б –Р–—Б—В—А–µ–њ—В–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–µ–є –≥–ї–Њ—В–Ї–Є (—З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –Љ–Є–Ї—А–Њ–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є), –њ–Њ–ї–Є–∞—А—В—А–Є—В –Є–Љ–µ–µ—В —Б–Є–Љ–Љ–µ—В—А–Є—З–љ—Л–є –Є –Љ–Є–≥—А–Є—А—Г—О—Й–Є–є —Е–∞—А–∞–Ї—В–µ—А, –Њ—В–Љ–µ—З–∞—О—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Љ–Є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ —Б–µ—А–і—Ж–∞ —Б –±–Њ–ї–µ–µ –Љ–µ–і–ї–µ–љ–љ—Л–Љ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –њ–Њ—А–Њ–Ї–∞, –≤—Л—Б–Њ–Ї–∞—П –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М –Є –±—Л—Б—В—А–Њ–µ –Њ–±—А–∞—В–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–∞ —Д–Њ–љ–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–С–Њ–ї–µ–µ —Б–ї–Њ–ґ–µ–љ –њ—А–Њ—Ж–µ—Б—Б –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –њ–Њ–≤—В–Њ—А–љ–Њ–є –∞—В–∞–Ї–Є –Ю–†–Ы –Є –≤—В–Њ—А–Є—З–љ–Њ–≥–Њ –Ш–≠ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Њ–±—А–µ—В–µ–љ–љ–Њ–≥–Њ –њ–Њ—А–Њ–Ї–∞ —Б–µ—А–і—Ж–∞. –Э–∞–ї–Є—З–Є–µ –≤ –±–ї–Є–ґ–∞–є—И–µ–Љ –∞–љ–∞–Љ–љ–µ–Ј–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є—Е –Љ–∞–љ–Є–њ—Г–ї—П—Ж–Є–є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –±–∞–Ї—В–µ—А–Є–µ–Љ–Є–µ–є (–≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Б—В–Њ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е), –Њ–Ј–љ–Њ–±—Л –і–∞–ґ–µ –њ—А–Є —Б—Г–±—Д–µ–±—А–Є–ї—М–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ —В–µ–ї–∞, –±—Л—Б—В—А–Њ–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –љ–Њ–≤–Њ–≥–Њ –њ–Њ—А–Њ–Ї–∞ —Б–µ—А–і—Ж–∞ (–Є–ї–Є —Г—Б—Г–≥—Г–±–ї–µ–љ–Є–µ —Г–ґ–µ –Є–Љ–µ—О—Й–µ–≥–Њ—Б—П) —Б –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ –Ї–ї–∞–њ–∞–љ–љ–Њ–є —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є–Є –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ –Ј–∞—Б—В–Њ–є–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –њ–Њ—П–≤–ї–µ–љ–Є–µ –њ–µ—В–µ—Е–Є–є –љ–∞ –Ї–Њ–ґ–µ –Є —Б–ї–Є–Ј–Є—Б—В—Л—Е, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ–ї–µ–Ј–µ–љ–Ї–Є, –≤—Л—Б–Њ–Ї–Є–µ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –њ–∞—А–∞–Љ–µ—В—А—Л –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н—Д—Д–µ–Ї—В–∞ –Њ—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є – –≤—Б–µ —Н—В–Њ –Ј–∞—Б—В–∞–≤–ї—П–µ—В –Ј–∞–њ–Њ–і–Њ–Ј—А–Є—В—М –љ–∞–ї–Є—З–Є–µ –≤—В–Њ—А–Є—З–љ–Њ–≥–Њ –Ш–≠ —Г –±–Њ–ї—М–љ–Њ–≥–Њ —А–µ–±–µ–љ–Ї–∞ –Є–ї–Є –њ–Њ–і—А–Њ—Б—В–Ї–∞ –µ—Й–µ –і–Њ –њ–Њ–ї—Г—З–µ–љ–Є—П –і–∞–љ–љ—Л—Е –≠—Е–Њ–Ъ–У –Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ –≥–µ–Љ–Њ–Ї—Г–ї—М—В—Г—А—Г.
–Ф–ї—П —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ —Б–Є—Б—В–µ–Љ–љ–Њ–є –Ї—А–∞—Б–љ–Њ–є –≤–Њ–ї—З–∞–љ–Ї–Є –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –ґ–µ–љ—Б–Ї–Є–є –њ–Њ–ї, —Г—Б–Є–ї–µ–љ–љ–Њ–µ –≤—Л–њ–∞–і–µ–љ–Є–µ –≤–Њ–ї–Њ—Б, —Н—А–Є—В–µ–Љ–∞ –љ–∞ —Й–µ–Ї–∞—Е –Є –љ–∞–і —Б–Ї—Г–ї–Њ–≤—Л–Љ–Є –і—Г–≥–∞–Љ–Є, —Д–Њ—В–Њ—Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є—П, —П–Ј–≤—Л –≤ –њ–Њ–ї–Њ—Б—В–Є —А—В–∞ –Є–ї–Є –љ–Њ—Б–∞. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–µ—А–і—Ж–∞ –њ—А–Є —Н—В–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є —П–≤–ї—П–µ—В—Б—П –њ–µ—А–Є–Ї–∞—А–і–Є—В; –Ї–ї–∞–њ–∞–љ–љ–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П – —Н–љ–і–Њ–Ї–∞—А–і–Є—В –Ы–Є–±–Љ–∞–љ–∞––°–∞–Ї—Б–∞ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–Ј–і–љ–µ–µ –Є –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Ї–∞—В–µ–≥–Њ—А–Є–Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–Ј–љ–Є. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –∞–љ—В–Є–љ—Г–Ї–ї–µ–∞—А–љ—Л–є —Д–∞–Ї—В–Њ—А –Є –∞–љ—В–Є—В–µ–ї–∞ –Ї –љ–∞—В–Є–≤–љ–Њ–є –Ф–Э–Ъ –Љ–Њ–≥—Г—В –≤—Л—П–≤–ї—П—В—М—Б—П –Є –њ—А–Є –Ш–≠, –Њ–і–љ–∞–Ї–Њ –њ–Њ–≤—В–Њ—А–љ–Њ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Є–µ –і–∞–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –≤—Л—Б–Њ–Ї–Є—Е —В–Є—В—А–∞—Е –±–Њ–ї–µ–µ —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –і–ї—П —Б–Є—Б—В–µ–Љ–љ–Њ–є –Ї—А–∞—Б–љ–Њ–є –≤–Њ–ї—З–∞–љ–Ї–Є.
–Т –њ—А–Њ—Ж–µ—Б—Б–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–Њ–ґ–µ—В –њ–Њ—В—А–µ–±–Њ–≤–∞—В—М—Б—П –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ш–≠ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б–µ—А–і—Ж–∞ –≤ —А–∞–Љ–Ї–∞—Е –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–Р–§–°), —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–≥–Њ—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –∞—А—В–µ—А–Є–∞–ї—М–љ—Л—Е –Є/–Є–ї–Є –≤–µ–љ–Њ–Ј–љ—Л—Е —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ —А–∞–Ј–ї–Є—З–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є, —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–њ–µ–љ–Є–µ–є –Є –і—А—Г–≥–Є–Љ–Є —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є, –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є, –Ї–Њ–ґ–љ—Л–Љ–Є, –њ–Њ—З–µ—З–љ—Л–Љ–Є –Є –≥–µ–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є, –∞ —В–∞–Ї–ґ–µ –љ–∞–ї–Є—З–Є–µ–Љ –≤–Њ–ї—З–∞–љ–Њ—З–љ–Њ–≥–Њ –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–∞, –∞–љ—В–Є—В–µ–ї –Ї —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–∞–Љ (–Р–§–Ы), –Ї–∞—А–і–Є–Њ–ї–Є–њ–Є–љ—Г –Є β–2 –≥–ї–Є–Ї–Њ–њ—А–Њ—В–µ–Є–љ—Г.
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–≥–Њ –Ї–Њ–љ—Б–µ–љ—Б—Г—Б–∞, –і–ї—П –Р–§–Ы––∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–ї–∞–њ–∞–љ–Њ–≤ —Б–µ—А–і—Ж–∞ —Е–∞—А–∞–Ї—В–µ—А–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є: –љ–∞–ї–Є—З–Є–µ –≤ –Ї—А–Њ–≤–Є –Р–§–Ы (–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Р–§–°) –њ–ї—О—Б –≠—Е–Њ–Ъ–У––њ—А–Є–Ј–љ–∞–Ї–Є –Ї–ї–∞–њ–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є/–Є–ї–Є —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є—П –Є/–Є–ї–Є —Б—В–µ–љ–Њ–Ј –Љ–Є—В—А–∞–ї—М–љ–Њ–≥–Њ –Є/–Є–ї–Є –∞–Њ—А—В–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ –Є–ї–Є –ї—О–±–Њ–µ –Є—Е —Б–Њ—З–µ—В–∞–љ–Є–µ. –Я–Њ–љ—П—В–Є–µ «–Ї–ї–∞–њ–∞–љ–љ–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П» –≤–Ї–ї—О—З–∞–µ—В —Г—В–Њ–ї—Й–µ–љ–Є–µ —Б—В–≤–Њ—А–Њ–Ї >3 –Љ–Љ, –ї–Њ–Ї–∞–ї—М–љ–Њ–µ —Г—В–Њ–ї—Й–µ–љ–Є–µ, –Ј–∞—Е–≤–∞—В—Л–≤–∞—О—Й–µ–µ –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Г—О –Є–ї–Є —Б—А–µ–і–љ—О—О —З–∞—Б—В—М —Б—В–≤–Њ—А–Ї–Є, —Г–Ј–µ–ї–Ї–Є –љ–µ–њ—А–∞–≤–Є–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л –љ–∞ –њ—А–µ–і—Б–µ—А–і–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Љ–Є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ –Є/–Є–ї–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –∞–Њ—А—В–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞. –Я—А–Є —Н—В–Њ–Љ –љ–∞–ї–Є—З–Є–µ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є–Є –Є/–Є–ї–Є —Б—В–µ–љ–Њ–Ј–∞ —Б–ї–µ–і—Г–µ—В –Њ—Ж–µ–љ–Є–≤–∞—В—М –њ—А–Є –і–Њ–њ–њ–ї–µ—А––≠—Е–Њ–Ъ–У, –Є–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є—О —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤—Л–њ–Њ–ї–љ—П—В—М —Б –њ—А–Є–≤–ї–µ—З–µ–љ–Є–µ–Љ –і–≤—Г—Е —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤ –њ–Њ –≠—Е–Њ–Ъ–У.
–Ф–ї—П —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є—П –Є –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –∞—А—В–µ—А–Є–Є—В–∞ –Ґ–∞–Ї–∞—П—Б—Г —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –њ—А–Є–Љ–µ–љ—П—О—В –Ї—А–Є—В–µ—А–Є–Є –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–є –∞–љ—В–Є—А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –ї–Є–≥–Є. –Ю—Б–љ–Њ–≤–љ–Њ–є –Ї—А–Є—В–µ—А–Є–є – —Н—В–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–Є –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є (Rg, –Ъ–Ґ, –Ь–†–Ґ) –∞–Њ—А—В—Л –Є –µ–µ –Ї—А—Г–њ–љ—Л—Е –≤–µ—В–≤–µ–є –≤ –≤–Є–і–µ –∞–љ–µ–≤—А–Є–Ј–Љ—Л/–і–Є–ї–∞—В–∞—Ж–Є–Є, —Б—Г–ґ–µ–љ–Є—П –њ—А–Њ—Б–≤–µ—В–∞, –Њ–Ї–Ї–ї—О–Ј–Є–Є –Є–ї–Є —Г—В–Њ–ї—Й–µ–љ–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є —Б—В–µ–љ–Ї–Є, –љ–µ —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б —Д–Є–±—А–Њ–Љ—Л—И–µ—З–љ–Њ–є –і–Є—Б–њ–ї–∞–Ј–Є–µ–є –Є–ї–Є –і—А—Г–≥–Є–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є (—Д–Њ–Ї–∞–ї—М–љ—Л–µ, —Б–µ–≥–Љ–µ–љ—В–∞—А–љ—Л–µ). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г—З–Є—В—Л–≤–∞—О—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є:
• –і–µ—Д–Є—Ж–Є—В –њ—Г–ї—М—Б–∞ –Є–ї–Є –њ–µ—А–µ–Љ–µ–ґ–∞—О—Й–Є–µ—Б—П –ї–Њ–Ї–∞–ї—М–љ—Л–µ –Љ—Л—И–µ—З–љ—Л–µ –±–Њ–ї–Є –њ—А–Є –і–≤–Є–ґ–µ–љ–Є–Є;
• —А–∞–Ј–љ–Є—Ж–∞ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Р–Ф >10 –Љ–Љ —А—В.—Б—В. –њ—А–Є –µ–≥–Њ –Є–Ј–Љ–µ—А–µ–љ–Є–Є –љ–∞ —А—Г–Ї–∞—Е –Є –љ–Њ–≥–∞—Е;
• –њ–∞–ї—М–њ–∞—В–Њ—А–љ–Њ–µ –і—А–Њ–ґ–∞–љ–Є–µ –Є–ї–Є —И—Г–Љ –њ—А–Є –∞—Г—Б–Ї—Г–ї—М—В–∞—Ж–Є–Є –љ–∞–і –Ї—А—Г–њ–љ—Л–Љ–Є –∞—А—В–µ—А–Є—П–Љ–Є;
• –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П: —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Є–ї–Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф –њ—А–µ–≤—Л—И–∞—О—В 95––є —Ж–µ–љ—В–Є–ї—М —И–Ї–∞–ї—Л —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –Р–Ф –і–ї—П –і–∞–љ–љ–Њ–≥–Њ —А–Њ—Б—В–∞;
• —Г—Б–Ї–Њ—А–µ–љ–Є–µ –°–Ю–≠ –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –°–†–С.
–Ф–Є–∞–≥–љ–Њ–Ј –∞—А—В–µ—А–Є–Є—В–∞ –Ґ–∞–Ї–∞—П—Б—Г –њ—А–∞–≤–Њ–Љ–Њ—З–µ–љ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б–Њ—З–µ—В–∞–љ–Є—П –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Њ–і–љ–Є–Љ –Є–Ј 5 –≤—Л—И–µ–њ–Њ–Є–Љ–µ–љ–Њ–≤–∞–љ–љ—Л—Е –Ї—А–Є—В–µ—А–Є–µ–≤.
–Ю–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –њ—А–Њ–±–ї–µ–Љ—Л –Љ–Њ–≥—Г—В –≤–Њ–Ј–љ–Є–Ї–љ—Г—В—М –њ—А–Є —А–∞–Ј–≥—А–∞–љ–Є—З–µ–љ–Є–Є –Ш–≠ —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –Ъ–∞–≤–∞—Б–∞–Ї–Є, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є–Љ —Б –≤–∞–ї—М–≤—Г–ї–Є—В–Њ–Љ –Є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Ї–ї–∞–њ–∞–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Ю—Б–љ–Њ–≤–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Б–Є–љ–і—А–Њ–Љ–∞ –Ъ–∞–≤–∞—Б–∞–Ї–Є —Б–ї–µ–і—Г—О—Й–Є–µ:
• —А–µ–Ј–Є—Б—В–µ–љ—В–љ–∞—П –Ї –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ –ї–Є—Е–Њ—А–∞–і–Ї–∞ –≤ —В–µ—З–µ–љ–Є–µ 5 –і–љ–µ–є –Є –±–Њ–ї–µ–µ;
• –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–є –Ї–Њ–љ—К—О–љ–Ї—В–Є–≤–Є—В;
• —В–Є–њ–Є—З–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≥—Г–± –Є –њ–Њ–ї–Њ—Б—В–Є —А—В–∞ (–≥–Є–њ–µ—А–µ–Љ–Є—П, –Њ—В–µ—З–љ–Њ—Б—В—М, —Б—Г—Е–Њ—Б—В—М –≥—Г–±, –Љ–∞–ї–Є–љ–Њ–≤—Л–є —П–Ј—Л–Ї, –і–Є—Д—Д—Г–Ј–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ —Б–ї–Є–Ј–Є—Б—В–Њ–є –њ–Њ–ї–Њ—Б—В–Є —А—В–∞ –Є –≥–ї–Њ—В–Ї–Є);
• –Њ—Б—В—А–Њ–µ –љ–µ–≥–љ–Њ–є–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –ї–Є–Љ—Д–Њ—Г–Ј–ї–Њ–≤ —И–µ–Є;
• –њ–Њ–ї–Є–Љ–Њ—А—Д–љ–∞—П —Б—Л–њ—М, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–∞ —В—Г–ї–Њ–≤–Є—Й–µ;
• –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Є—Б—В–µ–є –Є —Б—В–Њ–њ:
– —Н—А–Є—В–µ–Љ–∞ –ї–∞–і–Њ–љ–µ–є –Є –њ–Њ–і–Њ—И–≤;
– –≤ –Њ—Б—В—А–Њ–є —Б—В–∞–і–Є–Є – –Њ—В–µ—З–љ–Њ—Б—В—М –Ї–Є—Б—В–µ–є –Є —Б—В–Њ–њ;
– –≤ –њ–µ—А–Є–Њ–і —А–µ–Ї–Њ–љ–≤–∞–ї–µ—Б—Ж–µ–љ—Ж–Є–Є – —И–µ–ї—Г—И–µ–љ–Є–µ –Ї–Њ–ґ–Є –њ–∞–ї—М—Ж–µ–≤ –Ї–Є—Б—В–µ–є –Є —Б—В–Њ–њ.
–Ф–Є–∞–≥–љ–Њ–Ј —Б–Є–љ–і—А–Њ–Љ–∞ –Ъ–∞–≤–∞—Б–∞–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ –њ—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ 5 –Є–Ј 6 –≤—Л—И–µ—Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є–ї–Є —Б–Њ—З–µ—В–∞–љ–Є–Є 4 —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Б –∞–љ–µ–≤—А–Є–Ј–Љ–∞–Љ–Є –≤–µ–љ–µ—З–љ—Л—Е –∞—А—В–µ—А–Є–є (–њ–Њ –і–∞–љ–љ—Л–Љ –і–≤—Г—Е–Љ–µ—А–љ–Њ–є –≠—Е–Њ–Ъ–У –Є–ї–Є –Ї–Њ—А–Њ–љ–∞—А–Њ–≥—А–∞—Д–Є–Є).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –Ш–≠ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ –і–Њ–ї–ґ–µ–љ –±—Л—В—М –≤–Ї–ї—О—З–µ–љ –≤ –∞–ї–≥–Њ—А–Є—В–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–Є—Б–Ї–∞ –њ—А–Є –ї–Є—Е–Њ—А–∞–і–Ї–µ –љ–µ—П—Б–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ —Г –і–µ—В–µ–є –Є –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤.
–Ы–µ—З–µ–љ–Є–µ –Ш–≠. –°–µ–є—З–∞—Б –љ–Њ–≤—Л–Љ –≤ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є (–Р–С) —В–µ—А–∞–њ–Є–Є –Ш–≠ —П–≤–ї—П–µ—В—Б—П —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –µ–µ —Б—А–Њ–Ї–Њ–≤, –≤–≤–µ–і–µ–љ–Є–µ –Ї–Њ—А–Њ—В–Ї–Є—Е 2––љ–µ–і–µ–ї—М–љ—Л—Е –Ї—Г—А—Б–Њ–≤ –≤ —В–µ—А–∞–њ–Є—О —Б—В–∞–±–Є–ї—М–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–њ–Њ–і–≤–Є–ґ–љ—Л–Љ–Є –≤–µ–≥–µ—В–∞—Ж–Є—П–Љ–Є –Љ–∞–ї—Л—Е —А–∞–Ј–Љ–µ—А–Њ–≤, –∞ —В–∞–Ї–ґ–µ —А–∞—Б—И–Є—А–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –і–ї—П —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Ш–≠. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї—Г—А—Б–Њ–≤ –Р–С–—В–µ—А–∞–њ–Є–Є –њ—А–Є –Ш–≠ –љ–∞—В–Є–≤–љ—Л—Е –Ї–ї–∞–њ–∞–љ–Њ–≤ –Њ—Б—В–∞–µ—В—Б—П –њ—А–µ–ґ–љ–µ–є – 4–6 –љ–µ–і.
–Ъ–∞–Ї —Г–Ї–∞–Ј—Л–≤–∞–ї–Њ—Б—М –≤—Л—И–µ, –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ—А–Њ–±–ї–µ–Љ–љ—Л–Љ –≤–Њ–Ј–±—Г–і–Є—В–µ–ї–µ–Љ –Ш–≠ —П–≤–ї—П–µ—В—Б—П –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П S. aureus, –Ї–Њ—В–Њ—А—Л–є –њ—А–Њ—П–≤–ї—П–µ—В —В–µ–њ–µ—А—М —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М –љ–µ —В–Њ–ї—М–Ї–Њ –Ї –Љ–µ—В–Є—Ж–Є–ї–ї–Є–љ—Г, –љ–Њ –Є –Ї –≤–∞–љ–Ї–Њ–Љ–Є—Ж–Є–љ—Г – –њ—А–µ–њ–∞—А–∞—В—Г, –Ї–Њ—В–Њ—А—Л–є –і–Њ–≤–Њ–ї—М–љ–Њ –і–∞–≤–љ–Њ (–њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ–ї–Њ–≤–Є–љ—Г —Б—В–Њ–ї–µ—В–Є—П) –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –њ—А–Є –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є—П—Е.
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і–∞–Љ —П–≤–ї—П—О—В—Б—П —Г–ґ–µ –њ—А–Њ–≤–µ—А–µ–љ–љ—Л–є –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ –Ї–∞—А–і–Є–Њ—Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є—Е –Ї–ї–Є–љ–Є–Ї –†–§ –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –≤ –ї–µ—З–µ–љ–Є–Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Њ–≤–Њ–≥–Њ –Ш–≠ —Г –і–µ—В–µ–є –ї–Є–љ–µ–Ј–Њ–ї–Є–і, –∞ —В–∞–Ї–ґ–µ —Б–Њ–≤–µ—А—И–µ–љ–љ–Њ –љ–Њ–≤—Л–µ —В–∞–є–≥–µ—Ж–Є–Ї–ї–Є–љ –Є –і–∞–њ—В–Њ–Љ–Є—Ж–Є–љ. –Я–Њ—Б–ї–µ–і–љ–Є–є –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –љ–Њ–≤–Њ–Љ—Г –Ї–ї–∞—Б—Б—Г –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Б—А–µ–і—Б—В–≤, —Н—В–Њ –ї–Є–њ–Њ–њ–µ–њ—В–Є–і–љ—Л–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї, –њ—А–Њ—П–≤–ї—П—О—Й–Є–є —Б–≤–Њ—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤ –Є–љ—Д–µ–Ї—Ж–Є–є, –≤—Л–Ј–≤–∞–љ–љ—Л—Е –≥—А–∞–Љ–њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є —Д–ї–Њ—А–Њ–є, –Њ–љ –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –њ—А–Њ—В–Є–≤ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Њ–≤, –≤–Ї–ї—О—З–∞—П –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і–—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–µ —Н–љ—В–µ—А–Њ–Ї–Њ–Ї–Ї–Є, –∞ —В–∞–Ї–ґ–µ –Ї–Њ—А–Є–љ–µ–±–∞–Ї—В–µ—А–Є–Є –Є —Б—В–∞—Д–Є–ї–Њ–Ї–Њ–Ї–Ї–Є, –≤–Ї–ї—О—З–∞—П –Є—Е MRSA–—И—В–∞–Љ–Љ—Л. –Я–Њ–Ї–∞ —И—В–∞–Љ–Љ–Њ–≤, —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л—Е –Ї –і–∞–њ—В–Њ–Љ–Є—Ж–Є–љ—Г, –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ, —Г–і–Њ–±–µ–љ —А–µ–ґ–Є–Љ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П – 1 —А./—Б—Г—В. –≠—В–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –і–µ–ї–∞—О—В –µ–≥–Њ –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–Љ –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–Є —Б—В–∞–±–Є–ї—М–љ—Л—Е –∞–Љ–±—Г–ї–∞—В–Њ—А–љ—Л—Е –±–Њ–ї—М–љ—Л—Е.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –±–Њ–ї—М–љ–Њ–Љ—Г —Б –Ш–≠ –Є —Б–µ–њ—В–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П —И–Є—А–Њ–Ї–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ – —Ж–µ—Д–∞–ї–Њ—Б–њ–Њ—А–Є–љ + –∞–Љ–Є–љ–Њ–≥–ї–Є–Ї–Њ–Ј–Є–і –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –љ–∞–Ј–љ–∞—З–µ–љ–∞ –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ, —В.–µ. –≤ —В–µ—З–µ–љ–Є–µ 1 —З –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є. –Я—А–Є –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є –њ–∞—В–Њ–≥–µ–љ–∞ —В–µ—А–∞–њ–Є—П –Љ–Њ–ґ–µ—В –±—Л—В—М —Б—Г–ґ–µ–љ–∞ –і–Њ –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–є/—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є. –°–ї–µ–і—Г–µ—В –њ—А–Є–Ј–љ–∞—В—М, —З—В–Њ —А–Є—Б–Ї –њ–Њ—В–µ—А—П—В—М –±–Њ–ї—М–љ–Њ–≥–Њ –њ—А–Є –Ш–≠ —Б —Б–µ–њ—В–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ —В–∞–Ї –≤–µ–ї–Є–Ї, —З—В–Њ –≥–ї–Є–Ї–Њ–њ–µ–њ—В–Є–і—Л, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є —В–µ–є–Ї–Њ–њ–ї–∞–љ–Є–љ, —П–≤–ї—П–µ—В—Б—П –Њ–±—Л—З–љ–Њ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞. –Ю—Б—В—А—Л–є –Є –њ–Њ–і–Њ—Б—В—А—Л–є –Ш–≠ —Д–Є–≥—Г—А–Є—А—Г—О—В –њ–µ—А–≤—Л–Љ–Є –≤ —Б–њ–Є—Б–Ї–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–µ–њ–∞—А–∞—В –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Г –і–µ—В–µ–є –≤ –†–§.
–Я–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О –Ш–≠ –≤—Б–µ —А–∞—Б—И–Є—А—П—О—В—Б—П, –≤–µ–і—Г—Й–Є–Љ–Є —П–≤–ї—П—О—В—Б—П –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–∞—П –Ј–∞—Б—В–Њ–є–љ–∞—П —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П, —А–µ—Ж–Є–і–Є–≤ –Ш–≠ (–Њ—Б–Њ–±–µ–љ–љ–Њ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ—Л—Е –Ї–ї–∞–њ–∞–љ–Њ–≤), —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Ш–≠. –Т—Б–µ–≥–і–∞ –њ–Њ–ї–µ–Ј–љ–Њ –Є –Ї—А–∞–є–љ–µ –≤–∞–ґ–љ–Њ –≤–Ї–ї—О—З–∞—В—М –Ї–∞—А–і–Є–Њ—Е–Є—А—Г—А–≥–∞ –≤ –Ї–Њ–љ—Б–Є–ї–Є—Г–Љ, –µ—Б–ї–Є —А–µ—З—М –Є–і–µ—В –Њ –љ–∞—А–∞—Б—В–∞—О—Й–µ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–є –°–Э –Є–Ј––Ј–∞ –∞–Њ—А—В–∞–ї—М–љ–Њ–є, —А–µ–ґ–µ –Љ–Є—В—А–∞–ї—М–љ–Њ–є —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є–Є –Є–ї–Є –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є —Б–µ—А–і–µ—З–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ (–љ–∞—В–Є–≤–љ–Њ–≥–Њ –Є–ї–Є –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–≥–Њ) –≤–µ–≥–µ—В–∞—Ж–Є—П–Љ–Є.
–Т–Њ–њ—А–Њ—Б –≤—Б–µ–≥–і–∞ —А–µ—И–∞–µ—В—Б—П –≤ –њ–Њ–ї—М–Ј—Г —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Ш–≠, –µ—Б–ї–Є —А–µ—З—М –Є–і–µ—В –Њ –њ—А–Њ–±–ї–µ–Љ–љ—Л—Е/—В—А—Г–і–љ—Л—Е –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П—Е –±–Њ–ї–µ–Ј–љ–Є, –љ–∞–њ—А–Є–Љ–µ—А S. aureus, –њ–Њ—А–∞–ґ–∞—О—Й–µ–Љ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ—Л–є –Ї–ї–∞–њ–∞–љ –Є –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –≤–Њ–≤–ї–µ–Ї–∞—О—Й–µ–Љ –≤ –њ—А–Њ—Ж–µ—Б—Б –ї–µ–≤—Л–µ –Њ—В–і–µ–ї—Л —Б–µ—А–і—Ж–∞; –њ—А–Є –Ш–≠, –≤—Л–Ј–≤–∞–љ–љ–Њ–Љ –і—А—Г–≥–Є–Љ–Є –∞–≥—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–∞–Љ–Є (Brucella, Staphilococcus Lugdunesis, Achromobacter xylosoxidans, Ps. aeruginosa), –њ—А–Є –≥—А–Є–±–Ї–Њ–≤–Њ–Љ —Н–љ–і–Њ–Ї–∞—А–і–Є—В–µ, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –љ–∞–ї–Є—З–Є–Є —А–∞–Ј—А—Л–≤–∞ –∞–љ–µ–≤—А–Є–Ј–Љ—Л —Б–Є–љ—Г—Б–∞ –Т–∞–ї—М—Б–∞–ї—М–≤—Л –Є –њ—А–Є –њ–µ—А–Є–≤–∞–ї—М–≤—Г–ї—П—А–љ–Њ–Љ –∞–±—Б—Ж–µ—Б—Б–µ, –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞ –њ—А–Є —Н–љ–і–Њ–Ї–∞—А–і–Є—В–µ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ—Л—Е –Ї–ї–∞–њ–∞–љ–Њ–≤.
–Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е —А–∞–Ј–≤–Є—В–Є—П –Ш–≠ –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ (–њ—А–Њ—В–µ–Ј–љ—Л–є —Н–љ–і–Њ–Ї–∞—А–і–Є—В) –Њ–њ–µ—А–∞—Ж–Є—П –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –љ–µ–Љ–µ–і–ї–µ–љ–љ–Њ. –°—А–Њ—З–љ–Њ–µ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –њ–Њ–Ї–∞–Ј–∞–љ–Њ –±–Њ–ї—М–љ—Л–Љ, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–µ —Г–і–∞–µ—В—Б—П —Б–њ—А–∞–≤–Є—В—М—Б—П —Б –Ї–∞—А–і–Є–Њ–≥–µ–љ–љ—Л–Љ —И–Њ–Ї–Њ–Љ –Є–ї–Є –Њ—В–µ–Ї–Њ–Љ –ї–µ–≥–Ї–Є—Е. –Т–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —Н–Љ–±–Њ–ї–Є–Є –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Њ –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ —А–∞–љ—М—И–µ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ш–≠ –Њ—Б—В–∞–µ—В—Б—П –≤–∞–ґ–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л –≤ —Б–≤—П–Ј–Є —Б —А–∞—Б—В—Г—Й–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є –≤—Л—Б–Њ–Ї–Є–Љ–Є –њ–∞—А–∞–Љ–µ—В—А–∞–Љ–Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Є –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є. –Я–Њ—П–≤–ї—П—О—В—Б—П –≤—Б–µ –љ–Њ–≤—Л–µ –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —В–µ—А–∞–њ–Є–Є –Ш–≠, –Є –њ–µ–і–Є–∞—В—А—Л –і–Њ–ї–ґ–љ—Л –Ј–љ–∞—В—М –Њ —В–Њ–Љ, —З—В–Њ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ —Г–ґ–µ –љ–µ —П–≤–ї—П–µ—В—Б—П –њ–Њ—Б–ї–µ–і–љ–Є–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ. –Ю–≥—А–∞–љ–Є—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Є —Б—В—А–Њ–ґ–∞–є—И–∞—П –∞—Б–µ–њ—В–Є–Ї–∞ –њ—А–Є —Г—Б—В–∞–љ–Њ–≤–Ї–µ –Є –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–Є –Ї–∞—В–µ—В–µ—А–Њ–≤, –≤–љ–µ–і—А–µ–љ–Є–µ –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –љ–Њ–≤—Л—Е –Ї–∞—В–µ—В–µ—А–Њ–≤ (—Б –≥–Є–і—А–Њ—Д–Є–ї—М–љ–Њ–є –≤—Л—Б–Њ–Ї–Њ–њ–Њ–ї—П—А–Є–Ј–Њ–≤–∞–љ–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М—О) —Б–ї–µ–і—Г–µ—В –Њ—В–љ–µ—Б—В–Є –Ї –≤–∞–ґ–љ–µ–є—И–Є–Љ –Љ–µ—А–∞–Љ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–љ—Д–µ–Ї—Ж–Є–Є –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –Ш–≠.
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ –њ—А–µ–і–ї–∞–≥–∞–µ—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –њ—А–µ–Ј–µ–љ—В–∞—Ж–Є—П —Б–ї—Г—З–∞—П, –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—Й–µ–≥–Њ —Б–ї–Њ–ґ–љ–Њ—Б—В–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ш–≠ —Г –і–µ—В–µ–є.
–С–Њ–ї—М–љ–∞—П –Ь.–Ь., 16 –ї–µ—В, –љ–∞—Е–Њ–і–Є–ї–∞—Б—М –љ–∞ –ї–µ—З–µ–љ–Є–Є –≤ –і–µ—В—Б–Ї–Њ–є –Ї–ї–Є–љ–Є–Ї–µ –Э–Ш–Ш —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є (–Э–Ш–Ш–†) –†–Р–Ь–Э. –° 5––ї–µ—В–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –њ–Њ—Б–ї–µ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–Њ–є –Ю–†–Т–Ш —Г –љ–µ–µ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –і–ї–Є—В–µ–ї—М–љ–∞—П —Д–µ–±—А–Є–ї—М–љ–∞—П –ї–Є—Е–Њ—А–∞–і–Ї–∞, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–≤—И–∞—П—Б—П –Љ–Є–≥—А–Є—А—Г—О—Й–µ–є —А–Њ–Ј–µ–Њ–ї–µ–Ј–љ–Њ–є —Б—Л–њ—М—О, –њ—А–Є—Б–Њ–µ–і–Є–љ–Є–ї–Є—Б—М –њ–Њ–ї–Є–∞–і–µ–љ–Є—П, –≥–µ–њ–∞—В–Њ—Б–њ–ї–µ–љ–Њ–Љ–µ–≥–∞–ї–Є—П, –њ–Њ—П–≤–Є–ї–Є—Б—М –∞—А—В—А–∞–ї–≥–Є–Є. –Т –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –∞–љ–∞–ї–Є–Ј–∞—Е –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Г—Б–Ї–Њ—А–µ–љ–Є–µ –°–Ю–≠, –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–Ј. –І–µ—А–µ–Ј 1 –Љ–µ—Б. —А–∞–Ј–≤–Є–ї—Б—П —Б—В–Њ–є–Ї–Є–є —Б—Г—Б—В–∞–≤–љ–Њ–є —Б–Є–љ–і—А–Њ–Љ —Б –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —И–µ–є–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –ї—Г—З–µ–Ј–∞–њ—П—Б—В–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, –Љ–µ–ї–Ї–Є—Е —Б—Г—Б—В–∞–≤–Њ–≤ –Ї–Є—Б—В–µ–є, –Ї–Њ–ї–µ–љ–љ—Л—Е, –≥–Њ–ї–µ–љ–Њ—Б—В–Њ–њ–љ—Л—Е –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤. –Ф–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ —О–≤–µ–љ–Є–ї—М–љ—Л–є —А–µ–≤–Љ–∞—В–Њ–Є–і–љ—Л–є –∞—А—В—А–Є—В (–Ѓ–†–Р), –њ–Њ–ї–Є–∞—А—В—А–Є—В —Б —Б–Є—Б—В–µ–Љ–љ—Л–Љ –љ–∞—З–∞–ї–Њ–Љ. –Я—А–Њ–≤–µ–і–µ–љ–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–∞—П —В–µ—А–∞–њ–Є—П, –≤–Ї–ї—О—З–∞—О—Й–∞—П –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і—Л, –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –∞–Љ–Є–љ–Њ—Е–Є–љ–Њ–ї–Є–љ–Њ–≤—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Ј–∞—В–µ–Љ –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В. –Э–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ 4–5 –ї–µ—В –Њ—В–Љ–µ—З–∞–ї—Б—П –њ–µ—А–Є–Њ–і –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –Т 2004 –≥. –њ—А–Њ–Є–Ј–Њ—И–ї–Њ —А–µ–Ј–Ї–Њ–µ —Г—Е—Г–і—И–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П —Б –≤–Њ–Ј–Њ–±–љ–Њ–≤–ї–µ–љ–Є–µ–Љ —Д–µ–±—А–Є–ї–Є—В–µ—В–∞, –Љ–Є–≥—А–Є—А—Г—О—Й–µ–є —Б—Л–њ–Є, –Њ–±–Њ—Б—В—А–µ–љ–Є–µ–Љ —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–≠—В–Њ—В –њ–µ—А–Є–Њ–і –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї—Б—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–µ–є, –љ–µ–є—В—А–Њ—Д–Є–ї—М–љ—Л–Љ –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–Ј–Њ–Љ, —Г—Б–Ї–Њ—А–µ–љ–Є–µ–Љ –°–Ю–≠ –±–Њ–ї–µ–µ 55 –Љ–Љ/—З –Є –њ–∞–і–µ–љ–Є–µ–Љ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ –і–Њ 67 –≥/–ї. –У–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А –њ–Њ –Љ–µ—Б—В—Г –ґ–Є—В–µ–ї—М—Б—В–≤–∞, –≥–і–µ —З–µ—А–µ–Ј —Ж–µ–љ—В—А–∞–ї—М–љ—Л–є –≤–µ–љ–Њ–Ј–љ—Л–є –Ї–∞—В–µ—В–µ—А –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є—Б—М –њ–Њ–≤—В–Њ—А–љ—Л–µ –≥–µ–Љ–Њ—В—А–∞–љ—Б—Д—Г–Ј–Є–Є, –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–∞—П —В–µ—А–∞–њ–Є—П, –і–ї–Є—В–µ–ї—М–љ–∞—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П, –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Њ—Б—М –≤–≤–µ–і–µ–љ–Є–µ –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В–∞ –Є –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤. –Я–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —В–∞–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —З–µ—А–µ–Ј 2 –Љ–µ—Б. —Б–Њ—Б—В–Њ—П–љ–Є–µ –±–Њ–ї—М–љ–Њ–є —Г–і–∞–ї–Њ—Б—М —Б—В–∞–±–Є–ї–Є–Ј–Є—А–Њ–≤–∞—В—М. –Ґ–Њ—З–љ–∞—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П –і–Њ–Ї—Г–Љ–µ–љ—В–∞—Ж–Є—П, –Њ—В–љ–Њ—Б—П—Й–∞—П—Б—П –Ї —Н—В–Њ–Љ—Г –њ–µ—А–Є–Њ–і—Г –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Ї–Є, –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В. –І–µ—А–µ–Ј 1 –≥–Њ–і –њ–Њ—Б–ї–µ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є–µ –≤–љ–Њ–≤—М —А–µ–Ј–Ї–Њ —Г—Е—Г–і—И–Є–ї–Њ—Б—М, –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –ї–Є—Е–Њ—А–∞–і–Ї–∞, —Б—Л–њ—М, –Њ–±–Њ—Б—В—А–µ–љ–Є–µ —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –У–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–∞ –њ–Њ –Љ–µ—Б—В—Г –ґ–Є—В–µ–ї—М—Б—В–≤–∞, –≥–і–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –њ–Њ–≤—В–Њ—А–љ—Л–µ –Ї—Г—А—Б—Л –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –±—Л–ї–∞ —Г—Б–Є–ї–µ–љ–∞ —В–µ—А–∞–њ–Є—П –Ѓ–†–Р.
–Т–≤–Є–і—Г –Њ—В—Б—Г—В—Б—В–≤–Є—П —Н—Д—Д–µ–Ї—В–∞ –і–µ–≤–Њ—З–Ї–∞ –љ–∞–њ—А–∞–≤–ї–µ–љ–∞ –≤ –і–µ—В—Б–Ї–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є–µ –Э–Ш–Ш–† –†–Р–Ь–Э. –Я–∞—Ж–Є–µ–љ—В–Ї–∞ –њ–Њ—Б—В—Г–њ–Є–ї–∞ –≤ —В—П–ґ–µ–ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є: –ї–Є—Е–Њ—А–∞–і–Ї–∞ –і–Њ 40°–°, –њ—П—В–љ–Є—Б—В–Њ–—А–Њ–Ј–µ–Њ–ї–µ–Ј–љ–∞—П —Б—Л–њ—М, –њ–Њ–ї–Є–∞–і–µ–љ–Є—П, –≥–µ–њ–∞—В–Њ—Б–њ–ї–µ–љ–Њ–Љ–µ–≥–∞–ї–Є—П, –њ–Њ–ї–Є–∞—А—В—А–Є—В —Б —В–Њ—В–∞–ї—М–љ—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –≤—Б–µ—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ –Њ–њ–Њ—А–љ–Њ––і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞, –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ —Н–Ї—Б—Б—Г–і–∞—В–Є–≤–љ–Њ––њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ —Б—Г—Б—В–∞–≤–∞—Е, —А–µ–Ј–Ї–Є–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, –Є–Ј––Ј–∞ –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ–љ–∞ –±—Л–ї–∞ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Њ–±–µ–Ј–і–≤–Є–ґ–µ–љ–∞. –°–µ—А–і–µ—З–љ–∞—П –Њ–±–ї–∞—Б—В—М –±—Л–ї–∞ –≤–Є–Ј—Г–∞–ї—М–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–є, –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —А–∞—Б—И–Є—А–µ–љ–Є–µ –≥—А–∞–љ–Є—Ж —Б–µ—А–і—Ж–∞ –њ—А–Є –њ–µ—А–Ї—Г—Б—Б–Є–Є –≤–њ—А–∞–≤–Њ –і–Њ —Б—А–µ–і–Є–љ–љ–Њ–є –ї–Є–љ–Є–Є, –≤–ї–µ–≤–Њ – –љ–∞ 0,5–1 —Б–Љ; –њ–µ—А–≤—Л–є —В–Њ–љ –±—Л–ї –њ—А–Є–≥–ї—Г—И–µ–љ–љ—Л–Љ, –≤—В–Њ—А–Њ–є —В–Њ–љ –љ–∞–і –ї–µ–≥–Њ—З–љ–Њ–є –∞—А—В–µ—А–Є–µ–є – —Б–ї–µ–≥–Ї–∞ –∞–Ї—Ж–µ–љ—В–Є—А–Њ–≤–∞–љ; –≤ 3–4 –Љ–µ–ґ—А–µ–±–µ—А—М–µ –њ–Њ –ї–µ–≤–Њ–Љ—Г –Ї—А–∞—О –≥—А—Г–і–Є–љ—Л —Б –Є—А—А–∞–і–Є–∞—Ж–Є–µ–є –Ї –Њ—Б–љ–Њ–≤–∞–љ–Є—О –Љ–µ—З–µ–≤–Є–і–љ–Њ–≥–Њ –Њ—В—А–Њ—Б—В–Ї–∞ –≤—Л—Б–ї—Г—И–Є–≤–∞–ї—Б—П –ґ–µ—Б—В–Ї–Њ–і—Г—О—Й–Є–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Є–є —И—Г–Љ, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є–є—Б—П –љ–∞ –≤—Л—Б–Њ—В–µ –≤–і–Њ—Е–∞.
–Т –Њ–±—Й–µ–Љ –∞–љ–∞–ї–Є–Ј–µ –Ї—А–Њ–≤–Є: H–≤ – 79 –≥/–ї, —Н—А–Є—В—А–Њ—Ж–Є—В—Л – 3,3x1012/–ї, –ї–µ–є–Ї–Њ—Ж–Є—В—Л – 12,6x109/–ї, –њ–∞–ї–Њ—З–љ–Њ—П–і–µ—А–љ—Л–µ – 10, —Б–µ–≥–Љ–µ–љ—В–Њ—П–і–µ—А–љ—Л–µ – 82, —В—А–Њ–Љ–±–Њ—Ж–Є—В—Л – 403x109, –°–Ю–≠ – 120 –њ–Њ –Т–µ—Б—В–µ—А–≥—А–µ–љ—Г, –°–†–С – 4,0–3,1 –Љ–≥/% (–љ–Њ—А–Љ–∞ – –і–Њ 0,5), –Ї—А–Є–Њ–њ—А–µ—Ж–Є–њ–Є—В–Є–љ—Л – –Њ—В—А., –†–§ – –Њ—В—А., –Р–Э–§ – –Њ—В—А., –¶–Ш–Ъ – 360–266 –µ–і.–Њ–њ., –∞–љ—В–Є––Ф–Э–Ъ – 21 –µ–і., IgG – 22–22 –Љ–≥/–Љ–ї (–љ–Њ—А–Љ–∞ – 9,5±2,55), IgA – 2,79–1,98 –Љ–≥/–Љ–ї (–љ–Њ—А–Љ–∞ – 3,43±1,22), Ig–Ь – >2,0 –Љ–≥/–Љ–ї (–љ–Њ—А–Љ–∞ – 1,55±0,67), –Р–°–Ы––Ю – 200, –Р–Ъ–Ы – –Њ—В—А.
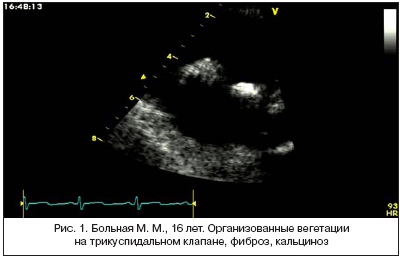
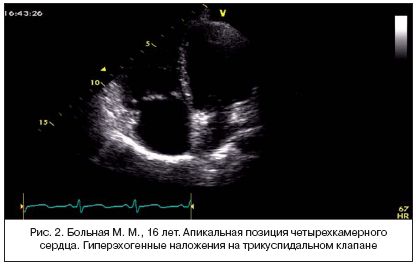
–Ф–∞–љ–љ—Л–µ –і–≤—Г—Е–Љ–µ—А–љ–Њ–є –≠—Е–Њ––Ъ–У (—А–Є—Б. 1–3): –њ–Њ—А–Њ–Ї —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ (–Ґ–Ъ): –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М IV —Б—В–µ–њ–µ–љ–Є –Є —Г–Љ–µ—А–µ–љ–љ—Л–є —Б—В–µ–љ–Њ–Ј. –Ь–∞—Б—Б–Є–≤–љ—Л–µ –≥–Є–њ–µ—А—Н—Е–Њ–≥–µ–љ–љ—Л–µ –љ–∞–ї–Њ–ґ–µ–љ–Є—П –љ–∞ —Б—В–≤–Њ—А–Ї–∞—Е –Ґ–Ъ (–Њ—А–≥–∞–љ–Є–Ј–Њ–≤–∞–љ–љ—Л–µ –≤–µ–≥–µ—В–∞—Ж–Є–Є). –Я—А–Є–Ј–љ–∞–Ї–Њ–≤ –љ–∞–ї–Є—З–Є—П —Б–≤–µ–ґ–Є—Е –≤–µ–≥–µ—В–∞—Ж–Є–є –љ–∞ –Ґ–Ъ –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ. –Ф–Є–ї–∞—В–∞—Ж–Є—П –њ—А–∞–≤–Њ–≥–Њ –њ—А–µ–і—Б–µ—А–і–Є—П. –Я—А–Њ–ї–∞–±–Є—А–Њ–≤–∞–љ–Є–µ –Љ–Є—В—А–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ (2,5 –Љ–Љ) —Б –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є —А–µ–≥—Г—А–≥–Є—В–∞—Ж–Є–µ–є. –°–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–∞—П —Д—Г–љ–Ї—Ж–Є—П –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–∞—П. –≠—Е–Њ––Ъ–У––њ—А–Є–Ј–љ–∞–Ї–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –ї–µ–≥–Њ—З–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є.
–Я–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–Њ—В–Є–≤–Њ—А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —Г–і–∞–ї–Њ—Б—М –і–Њ–±–Є—В—М—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Ї–Є: –љ–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–ї–∞—Б—М —В–µ–Љ–њ–µ—А–∞—В—Г—А–∞, —Б–Њ–Ї—А–∞—В–Є–ї–Є—Б—М —А–∞–Ј–Љ–µ—А—Л –њ–µ—З–µ–љ–Є –Є —Б–µ–ї–µ–Ј–µ–љ–Ї–Є, –Ї—Г–њ–Є—А–Њ–≤–∞–љ –∞–Ї—В–Є–≤–љ—Л–є —Б—Г—Б—В–∞–≤–љ–Њ–є —Б–Є–љ–і—А–Њ–Љ, —Г–ї—Г—З—И–Є–ї–Є—Б—М –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є (–њ–Њ–≤—Л—Б–Є–ї—Б—П –Э–≤, —Б–љ–Є–Ј–Є–ї–Є—Б—М –Њ—Б—В—А–Њ—Д–∞–Ј–Њ–≤—Л–µ –њ–∞—А–∞–Љ–µ—В—А—Л –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П – –°–Ю–≠, –°–†–С). –≠—Е–Њ––Ъ–У––Ї–∞—А—В–Є–љ–∞ –Ї–ї–∞–њ–∞–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –Њ—Б—В–∞–ї–∞—Б—М –±–µ–Ј –Є–Ј–Љ–µ–љ–µ–љ–Є–є.
–°–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М –і–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П –Ј–∞ –±–Њ–ї—М–љ–Њ–є, —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–≥–Њ, –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ—Б–ї—Г–ґ–Є–ї–Є –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П, –Ї —Б–Њ–ґ–∞–ї–µ–љ–Є—О, post factum, –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–Њ–≥–Њ –Ш–≠ —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –њ–Њ—А–Њ–Ї–∞ (–љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М IV —Б—В–µ–њ–µ–љ–Є) —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞. –С–Њ–ї—М–љ–∞—П –Ї–Њ–љ—Б—Г–ї—М—В–Є—А–Њ–≤–∞–љ–∞ –≤ –Э–¶ –°–°–• –Є–Љ. –С–∞–Ї—Г–ї–µ–≤–∞.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ: —Г –±–Њ–ї—М–љ–Њ–є —Б –Ѓ–†–Р –Њ—В–Љ–µ—З–∞–µ—В—Б—П —В–Њ—В–∞–ї—М–љ–∞—П —В—А–Є–Ї—Г—Б–њ–Є–і–∞–ї—М–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М. –Я–Њ –і–∞–љ–љ—Л–Љ –≠—Е–Њ––Ъ–У –њ—А–Є–Ј–љ–∞–Ї–Є –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–Њ–≥–Њ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Н–љ–і–Њ–Ї–∞—А–і–Є—В–∞ –Ґ–Ъ (–≤ —Е—А–Њ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–≤—П–Ј–Є —Б –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є). –≠—Е–Њ––Ї–∞—А—В–Є–љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –љ–µ–∞–Ї—В–Є–≤–љ–Њ–Љ—Г –њ—А–Њ—Ж–µ—Б—Б—Г, –≤–µ–≥–µ—В–∞—Ж–Є–Є —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ —Б —Г—З–∞—Б—В–Ї–∞–Љ–Є –Ї–∞–ї—М—Ж–Є–љ–Њ–Ј–∞. –Я–Њ–Ї–∞–Ј–∞–љ–Є–є –і–ї—П –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ—В.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н–њ–Є–Ј–Њ–і—Л –і–ї–Є—В–µ–ї—М–љ—Л—Е –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –Є –Є–Љ—Г–љ–љ–Њ—Б—Г–њ—А–µ—Б—Б–Є—П (–Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–∞—П –Ї–∞–Ї —Б–∞–Љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О, —В–∞–Ї –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М—О –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Б–Є—Б—В–µ–Љ–љ—Л—Е –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤ –Є —Ж–Є—В–Њ—Б—В–∞—В–Є–Ї–Њ–≤) –±—Л–ї–Є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–∞–Ј–≤–Є—В–Є—П –њ—А–∞–≤–Њ—Б–µ—А–і–µ—З–љ–Њ–≥–Њ –Ш–≠ —Г –і–∞–љ–љ–Њ–є –±–Њ–ї—М–љ–Њ–є. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –љ–∞–ї–Є—З–Є–µ –Ї–ї–∞–њ–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≤ –њ–µ—А–Є–Њ–і –Њ—З–µ—А–µ–і–љ–Њ–≥–Њ –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Ѓ–†–Р (–ї–µ—З–µ–љ–Є–µ –≤ –і–µ—В—Б–Ї–Њ–Љ –Њ—В–і–µ–ї–µ–љ–Є–Є –Э–Ш–Ш–† –†–Р–Ь–Э) —П–≤–Є–ї–Њ—Б—М –њ–Њ–≤–Њ–і–Њ–Љ –і–ї—П –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Ї—А—Г–≥ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А—Г–µ–Љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –Э–С–Ґ–≠ –≤ —А–∞–Љ–Ї–∞—Е –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Ф–∞–љ–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ –Є–ї–ї—О—Б—В—А–Є—А—Г–µ—В –њ—А–Є–Љ–µ—А —В—П–ґ–µ–ї–Њ–є –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В–Є –≤ –і–µ—В—Б–Ї–Њ–є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –Є —Б–ї—Г—З–∞–є –Њ—В—Б—А–Њ—З–µ–љ–љ–Њ–є (—Г–ґ–µ –љ–∞ —Н—В–∞–њ–µ —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–≤—И–µ–≥–Њ—Б—П –њ–Њ—А–Њ–Ї–∞) –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ш–≠.