Новейшие достижения в изучении патогенеза ОА наметили определенный прогресс в лечении заболевания. Терапия ОА, назначенная на ранних стадиях патологического процесса, должна быть направлена на решение следующих задач: уменьшение боли и воспаления, снижение частоты обострений и поражения новых суставов, замедление прогрессирования и предотвращение инвалидности, улучшение качества жизни больного [1,2,7].
Наиболее широкое применение в лечении ОА в последние годы нашли структурные аналоги хряща, к которым относятся хондроитинсульфат и глюкозамин. Принимая во внимание имеющиеся данные о том, что хондроитинсульфат и глюкозамин оказывают разнообразное фармакологическое воздействие на метаболизм хряща, относительно недавно появились исследования по сочетанному применению этих препаратов при ОА, показавшие перспективность такого их использования [1,2,6,16].
Целью проведенного исследования было оценить влияние длительной (3–летнее наблюдение) терапии Терафлексом (комбинация глюкозамина гидрохлорида и хондроитинсульфата) на симптомы и показатели качества жизни у больных на ранних стадиях гонартроза.
Материал и методы
Обследовано 244 амбулаторных пациента с достоверным диагнозом гонартроза (ГА), давших письменное согласие на участие в исследовании. Диагностика заболевания осуществлялась на основе критериев ГА Aмериканской коллегии ревматологов [12]. При отсутствии рентгенологических критериев диагноз устанавливался при сочетании клинических симптомов (боль механического характера, скованность в суставах <30 минут, ограничение функции) и выявленной при артросонографии неровности контура суставных поверхностей костей, образующих сустав. Рентгенологическая стадия ГА оценивалась по классификации Келлгрена–Лоуренса [14].
Критериями включения в исследование были: длительность симптомов ГА не менее 2, но не более 36 месяцев; 0, I, II рентгенологические стадии ГА; первичный ГА; отсутствие других заболеваний суставов. Критерии исключения: наличие тяжелой сопутствующей патологии, способной повлиять на результаты лабораторных исследований; применение препаратов симптоматического действия в течение 3 месяцев до момента включения в исследование (в том числе внутрисуставное введение глюкокортикостероидов).
Пациенты с ранними стадиями ГА (РГА) были разделены на основную и контрольную группы. В основную группу вошли 104 пациента с РГА, которым с момента включения в исследование была начата терапия Терафлексом (Т): 83 (79,7%) женщины и 21 (20,3%) мужчина (средний возраст 47,4±11,6 лет, средняя длительность ГА 11,5±6,7 месяцев). В соответствии с классификацией Келлгрена–Лоуренса 0 стадия ГА имела место у 22 (20,8%) больных, I – у 51 (49,4%), II – у 31 (29,8%) исследованного. Характеристика больных основной группы представлена в таблице 1. Т назначался по 1 капсуле 3 раза в сутки в течение 1 месяца, далее по 1 капсуле 2 раза в сутки в течение последующих 5 месяцев. Повторные курсы лечения Т в дозе 2 капсулы препарата в сутки в течение 2 месяцев повторяли с интервалом в 1 месяц. Общая длительность приема Т на момент окончания исследования составила 3 года. При усилении болей в суставах больным разрешался прием диклофенака в суточной дозе 100 мг.
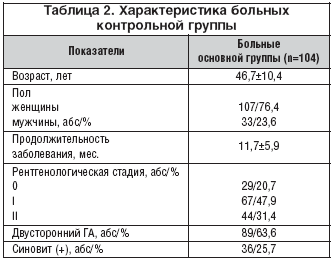
Контрольную группу составили 140 пациентов с РГА, 107 (76,4%) женщин и 33 (23,6%) мужчины (средний возраст 46,7±10,4 лет, средняя длительность ГА 11,7±5,9 месяцев). В соответствии с классификацией Келлгрена–Лоуренса 0 стадия ГА имела место у 29 (20,7%) больных, I – у 67 (47,9%), II – у 44 (31,4%) участников исследования. Характеристика больных контрольной группы представлена в таблице 2. Всем пациентам контрольной группы с момента включения в исследование был рекомендован прием 100 мг диклофенака в сутки в сочетании с различными видами физиолечения. При достижении положительного эффекта лечения диклофенак принимался лишь при усилении болей в суставах в суточной дозе 100 мг.
На момент включения в исследование основная и контрольная группы были сопоставимы по параметрам суставного синдрома.
Оценка выраженности болевого синдрома, функциональной активности суставов на момент включения в исследование, а также в контрольные сроки наблюдения проводилась определением:
• суммарного альго–функционального индекса Лекена (ФИЛ) для ГА в баллах [15];
• выраженности боли в суставах по визуально–аналоговой шкале (ВАШ) в мм;
• индексов WOMAC (Western Ontario and McMAster Universities Osteorthritis Index) боли, скованности, функции и суммарного глобального в мм по ВАШ [13].
Измерялась окружность коленных суставов для оценки выраженности местного воспаления в см. Потребность в НПВП определялась в мг в сутки диклофенака для оценки влияния терапии на течение заболевания.
Качество жизни (КЖ) больных оценивалось с использованием общего вопросника SF–36, который содержит 36 вопросов, 8 шкал. Шкала физического функционирования (ФФ) оценивает самообслуживание, ходьбу, переноску тяжестей, подъем по лестнице, выполнение наклонов, а также тяжелых физических нагрузок; ролевого физического функционирования (РФФ), роль физических проблем в ограничении жизнедеятельности; боль (Б) – интенсивность боли и ее влияние на способность заниматься нормальной деятельностью; общее здоровье (ОЗ) – состояние пациента на данный момент и перспективу лечения; жизнеспособность (Ж) – подразумевает оценку ощущения себя полным сил, энергии или, напротив, обессиленным; социальное функционирование (СФ) – удовлетворенность уровнем социальной активности; ролевое эмоциональное функционирование (РЭФ) подразумевает оценку степени, в которой эмоциональное состояние мешает выполнению работы или другой повседневной деятельности; психическое здоровье (ПЗ) – характеризует настроение, наличие депрессии, тревоги [4].
Опрос больных проводился при непосредственном контакте, без посторонней помощи ими заполнялась анкета с вопросами. Ответы на вопросы с помощью специальных алгоритмов выражались в баллах от 0 до 100 (более высокому уровню КЖ соответствовал более высокий балл шкалы вопросника).
Дополнительно к вышеперечисленным методам исследования выполнялись ЭКГ, ЭхоКГ, рентгенологическое исследование органов грудной клетки, УЗИ органов брюшной полости, общий анализ мочи, клинический анализ крови, определялись уровни фибриногена, билирубина, АСАТ, АЛАТ, креатинина, мочевой кислоты, холестерина, общего белка, глюкозы, калия крови для оценки влияния длительной терапии Т на функции жизненно важных органов и систем.
Результаты и обсуждение
При длительном приеме Т оказал положительное влияние на симптомы ГА. Уже через 6 месяцев ежедневного приема Т была отмечена положительная динамика всех клинических показателей. Так, выраженность боли по ВАШ в покое и при ходьбе снизилась по сравнению с исходными значениями с 31,44±7,12 и 52,82±12,48 мм до 20,89±7,44 и 30,65±12,42 мм соответственно (p<0,01). Достоверно отличались от исходных и значения ФИЛ (исходно 10,12±2,98 баллов), всех шкал индекса WOMAC (боли, скованности, функции, глобальный: исходно 172,48±47,54 мм, 48,91±12,75, 554,75±158,97, 785,65±160,51 мм), составив 5,20±2,42 баллов, 98,65±40,32 мм, 25,26±12,69, 376,86±131,34, 528,91±145,21 мм соответственно (р<0,01) через 6 месяцев непрерывного приема Т.
Далее в соответствии с протоколом исследования больные принимали Т повторными курсами по 2 месяца с интервалами 1 месяц. Положительная динамика всех клинических показателей сохранялась в течение всего срока наблюдения за больными основной группы.
Достоверность различий выраженности боли по ВАШ, ФИЛ, индекса WOMAC с исходными значениями сохранялась через 1, 2 и 3 года наблюдения. Так, ФИЛ составил 5,72±2,16 баллов, 6,08±2,75 баллов, 6,27±2,81 баллов через 1, 2 и 3 года лечения Т соответственно (р<0,05), а индекс WOMAC глобальный – 513,18±156,71 мм, 544,20±151,78 мм, 558,61±153,12 мм в вышеназванные сроки наблюдения соответственно (р<0,05). Данные о динамике клинических показателей больных основной группы, лечившихся Т, представлены в таблице 3.
На фоне лечения Т значительно снизилась потребность пациентов в НПВП, которая достоверно отличалась от исходной во все сроки наблюдения за больными. После 6 месяцев лечения 22% пациентов смогли полностью отказаться от приема НПВП, через 1 год – 26,4%, через 2 года – 27,5%, через 3 года 27,7% совсем не принимали НПВП.
В контрольной группе также наблюдалась положительная динамика всех клинических показателей через 6 месяцев, 1 и 2 года наблюдения. Однако уже через 2 года лечения достоверность различий с исходным значением сохранялась лишь для выраженности боли по ВАШ. Через 3 года наблюдения значения всех клинических показателей приблизились к исходным. Динамика клинических показателей больных контрольной группы представлена в таблице 4.
Достоверность различий в значениях клинических показателей в группе пациентов, лечившихся Т, и в контрольной отсутствовали через 6 месяцев и 1 год наблюдения. Однако через 2 и 3 года лечения все клинические показатели (за исключением выраженности боли по ВАШ в покое исследуемой группы) были достоверно ниже, чем в контрольной. При сравнении основной и контрольной групп выявлены достоверные различия выраженности боли по ВАШ при ходьбе через 3 года наблюдения (37,96±12,84 и 51,25±13,01 мм, р<0,05), ФИЛ – через 2 и 3 года (6,08±2,75 и 8,90±3,54 баллов через 2 года, 6,27±2,81 и 9,45±3,20 баллов через 3 года соответственно, р<0,05) (рис. 1) и индекса WOMAC глобального – через 2 и 3 года (544,20±151,78 и 658,24±172,30 мм через 2 года, 558,61±153,12 и 725,27±178,75 мм через 3 года соответственно, р<0,05).
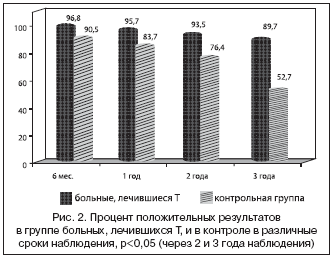
Положительные результаты лечения были достигнуты на фоне лечения Т через 6 месяцев наблюдения у 96,8 % пациентов, через 1 год – у 95,7%, через 2 года – у 93,5%, через 3 года – у 89,7% больных (в сравнении с контрольной группой различия достоверны через 2 и 3 года наблюдения, р<0,05). Эффективность терапии Т и в контрольной группе в различные сроки наблюдения представлена на рисунке 2.
На рисунке 3 представлен процент положительных результатов у больных, лечившихся Т, в зависимости от рентгенологической стадии ГА на момент начала терапии. Отмечено, что положительный эффект лечения Т наблюдался у всех больных, независимо от стадии ГА через 6 месяцев и 1 год терапии, однако более стойким он оказался у больных с 0 и I стадиями ГА и менее стойким – у пациентов со II рентгенологической стадией процесса на момент начала лечения. В группе больных со II стадией ГА отмечены более выраженное снижение процента положительных результатов и отрицательная динамика клинических показателей через 2 и 3 года наблюдения.
Таким образом, длительная терапия Т, назначенная на ранних стадиях ГА, оказала положительное влияние на симптомы заболевания, эффект терапии сохранялся во все сроки наблюдения. У пациентов с 0 и I рентгенологическими стадиями на момент начала терапии положительный эффект длительного лечения препаратом оказался более стойким по сравнению с пациентами со II стадией ГА.
Длительная терапия повторными курсами Т оказала положительное влияние на показатели КЖ всех шкал вопросника SF–36. Необходимо отметить, что наиболее высокие значения показателей КЖ были достигнуты через 1 и 2 года, а для ряда показателей – через 3 года терапии. Так, показатель ФФ вырос по сравнению с исходным значением на 35,3% через 1 год и на 35, 2% – через 3 года наблюдения (р<0,05), РФФ – на 27,4% через 1 год (р<0,05) и на 35% – через 3 года (р<0,01), Б – на 48,8 и 41, 4% (р<0,01), ОЗ – на 23,8% (р<0,05) и 4%, Ж – на 0,4 и 6,5%, СФ – на 36,3 и 39,1% (р<0,05), РЭФ – на 6,8 и 3,4%, ПЗ – на 14,5 и 12,1% через 1 год и 3 года наблюдения соответственно.
Несмотря на несомненный рост, статистической достоверности различий с исходными значениями в различные сроки наблюдения достигли не все показатели КЖ. Наибольший рост был отмечен для ФФ, РФФ, Б, в меньшей степени длительное лечение Т оказало влияние на самоощущение пациента в целом, его эмоциональную и психическую сферы, что, по–видимому, можно объяснить отсутствием у больного ощущения «полноты здоровья», связанное с необходимостью постоянного приема препаратов для его улучшения и поддержания.
При сравнительной оценке динамики показателей КЖ в основной и контрольной группах через 1 год наблюдения отмечен рост ФФ, РФФ, Б в обеих группах больных, однако более выраженный в основной группе (р<0,05 для РФФ и р<0,01 для Б). При росте значений ОЗ, СФ, ПЗ у пациентов, лечившихся Т, в контроле имела место отрицательная динамика вышеназванных показателей (р<0,01). Через 3 года наблюдения все показатели КЖ вопросника SF–36 (за исключением ОЗ, РЭФ и Ж) были достоверно выше у больных, лечившихся Т (р<0,01 для ФФ, РФФ, Б, СФ и р<0,05 для ПЗ), по сравнению с контролем. Динамика показателей КЖ в группе больных, лечившихся Т, и в контрольной через 1 и 3 года наблюдения представлена на рисунках 4 и 5.
Таким образом, длительная терапия Т, назначенная на ранних стадиях ГА, оказала положительное влияние на КЖ пациентов. Наиболее значимый рост по сравнению с исходными значениями показателей шкал вопросника SF–36 был отмечен через 1 и 2 года, а для ряда показателей – через 3 года лечения препаратом.
Необходимо отметить, что длительное лечение Т не оказало отрицательного влияния на функции жизненноважных органов и систем. Не было также отмечено побочных эффектов лечения препаратом, которые потребовали бы его отмены.
Таким образом, хотелось бы обратить внимание врачей–ревматологов, а также терапевтов, к которым преимущественно обращаются пациенты с недавно возникшей болью в коленных суставах, на необходимость раннего начала (в том числе на дорентгенологической стадии ГА) и длительного проведения патогенетической терапии заболевания, оказывающей положительное влияние на симптомы ГА, улучшающей КЖ пациентов.
Consilium Medicum Неврология и Ревматология, 2010, т. 12, №2: 136–140







Литература
1. Алексеева Л.И., Чичасова Н.В., Беневоленская Л.И. и др. Комбинированный препарат “Артра” при лечении остеоартроза // Тер. архив. – 2005. – № 11. – С. 69–75.
2. Алексеева Л.И. Терапия остеоартроза с позиций доказательной медицины // CONSILIUM MEDICUM экстравыпуск. – 2007. – № 8. – С. 14.
3. Алексеева Л.И. Современные подходы к лечению остеоартроза // РМЖ. – 2003. – № 4. – C. 85–88.
4. Амирджанова В.Н., Койлубаева Г.М. Методология оценки качества жизни в практике ревматолога // Научно–прктич. Ревматология. – 2003. – № 2. – C. 72–76.
5. Базоркина Д.И., Эрдес Ш. Социальная значимость ревматических заболеваний // Научно–практич. ревматология 2005. – № 6. – C. 79– 85.
6. Верткин А.Л., Талибов О.Б. Лечение остеоартроза: роль хондропротекторов // Леч. врач. – 2000. – № 9. – C. 40–43.
7. Насонова В.А. Фармакотерапия остеоартроза // Леч. врач. – 2004. – № 7. – C. 22–24.
8. Насонова В.А. Проблема остеоартроза в начале XXI века // CONSILIUM MEDICUM. – 2000. – том 2. – № 6. – C. 61–64.
9. Насонова В.А. Международное десятилетие болезней костей и суставов (2000–2010) – многодисциплинарная акция // Тер. архив. – 2001. – № 5. – C. 5–8.
10. Сизова Л.В. Оценка качества жизни в современной медицине // Научно–прктич. Ревматология. – 2003. – № 2. – C. 38–46.
11. Цурко В.В. Остеоартроз: гериартрическая проблема // РМЖ. – 2005. – том 13. – № 24. – C. 1627–1631.
12. Altman R., Asch E., Bloch D. et al. Development of criteria for the classification and reporting of osteoarthritis. Classification of the arthritis of the knee // Arthritis Rheum. – 1986. – № 29. – P. 1039–1049.
13. Bellamy N., Buchanan W.W., Goldsmith C.H. et al. Validation study of WOMAC: a health status instrument for measuring clinically important patient relevant outcomes to antirheumatic drug therapy in patients with osteoarthritis of the hip or knee // J. Rheumatol. – 1998. – № 15. – P. 1833–1840.
14. Kellgren J.H., Lawrence J.S. Radiographic assessment of osteoarthritis // Ann. Rheum. Dis. – 1957. – № 16. – P. 494–501.
15. Lequesne M., Samson M., Gerard P., Mery C. Pain–function indices for the follow–up of osteoarthritis of the hip and the knee // Rev. Rheum. Mal. Osteoartic. – 1990. – № 57(9pt2). – P. 32–36.
16. McAlindon T., LaValley M. Glucosamin and chondroitin for treatment of osteoarthritis: a systematic quality assessment and metaanalysis // JAMA. – 2000. – № 283. – P. 1469–1475.












