Неизвестность этиологических факторов и сложность патогенетических механизмов развития хронического воспаления синовиальной оболочки обусловливают необходимость наличия в арсенале клинициста противовоспалительных препаратов с доказанной эффективностью и хорошей переносимостью. Создание нового базисного противовоспалительного препарата (БПВП) лефлуномида (Арава) было весьма своевременным, так как к БПВП с хорошей длительной переносимостью относились только метотрексат и сульфасалазин. Причем последний препарат обладал ограниченной эффективностью при высокоактивных серопозитивных вариантах РА.
По химической структуре лефлуномид является низкомолекулярным синтетическим производным изоксазола, которое в желудочно–кишечном тракте и плазме быстро превращается в активный метаболит А77 1726 (малонитриламид). Активный метаболит А77 1726 имеет длительный период полураспада (15–18 дней) и хорошо связывается с белками плазмы – более чем на 99%. Основной механизм действия лефлуномида хорошо известен и неоднократно обсуждался в печати: ингибиция de novo синтеза пиримидиновых нуклеотидов в поздней (G1) фазе клеточного цикла, что наиболее выражено в активированных Т–лимфоцитах [4]. Снижение синтеза пиримидиновых нуклеотидов приводит к торможению пролиферации активированных Т–клеток в поздней фазе (G1) клеточного цикла [5] и к изменению Т– клеточного аутоиммунного ответа: подавляется синтез провоспалительных цитокинов (интерферона g и ФНО–a), уменьшается Т–зависимый синтез антител В–клетками [6]. Кроме того, влияние на активированные лимфоциты приводит к нарушению их взаимодействия с антиген–презентирующими клетками [7], есть данные об антипролиферативном влиянии активного метаболита лефлуномида на многие клетки (дендритные, эндотелиальные, макрофаги, фибробласты, остеокласты, В–лимфоциты) (рис. 1) [8], играющие важную роль в развитии воспаления и деструктивных процессов при РА. Было показано, что in vitro А77 1726 способен проявлять противовоспалительный эффект в культуре синовиальных макрофагов. При этом прогрессивное и достоверное уменьшение синовиальных макрофагов, позитивных по ФНО-a, IL–1b зависит от его дозы и длительности применения (рис. 2) [9].
К настоящему времени доказано во многих клинических испытаниях, проведенных как за рубежом, так и в нашей стране, что основные преимущества лефлуномида в лечении РА:
1. Быстрое развитие клинического эффекта – через 4 недели [10,11].
2. Выраженное подавление лабораторных параметров активности РА [11].
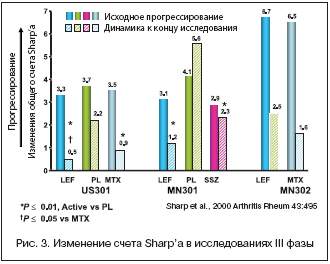
3. Подавление деструктивных процессов в суставах [11,12] (рис. 3).
4. Возможность применения лефлуномида с высокой эффективностью при раннем РА в качестве первого препарата [13,14].
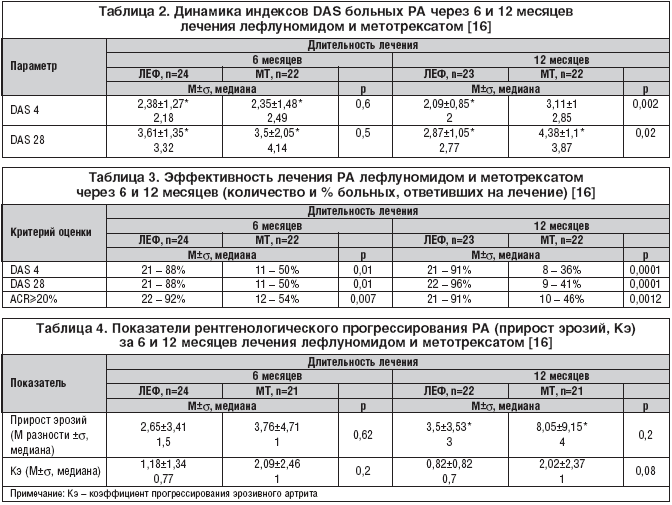
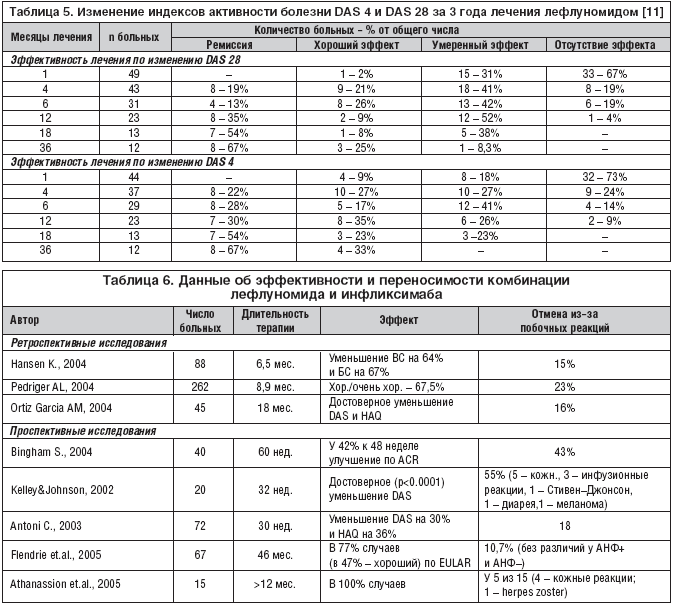
Клинико–лабораторный эффект лефлуномида, по нашим данным, развивается у 94% больных [15]. Параметры поражения суставов и СРБ с высокой степенью достоверности уменьшаются через 6 и еще в большей степени – через 12 месяцев лечения (p<0,001). При оценке выраженности уменьшения изучаемых параметров (табл. 1) мы получили очень высокий процент улучшения уже через 6 месяцев – от 60 до 71%.; через 12 месяцев лечения лефлуномидом выраженность положительного влияния на параметры поражения суставов возросла и составила от 64 до 96% улучшения по сравнению с исходным уровнем. Следует отметить, что эффект лефлуномида при РА не уступает, а подчас даже превышает эффект метотрексата, считающегося «золотым стандартом» среди БПВП, используемых в терапии РА (рис. 4, табл. 2,3) [16,17]. По нашим данным, лефлуномид не уступает метотрексату не только по влиянию на параметры активности, но в степени подавления прогрессирования деструктивного артрита (табл. 4). По данным зарубежных авторов, назначение лефлуномида в 4 раза уменьшает число вновь образованных эрозий [18]. В 12–месячном исследовании, проведенном в Северной Америке, было показано, что лефлуномид в большей степени замедляет прогрессирование эрозивного артрита, чем метотрексат [12].
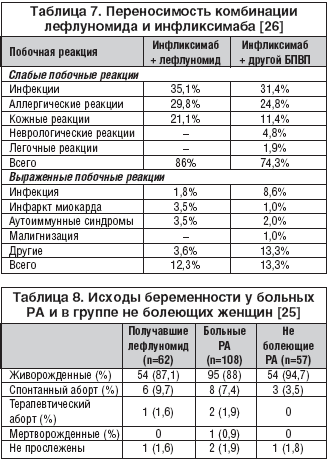
При лечении РА ценность противовоспалительного препарата определяется и возможностью длительного применения БПВП без уменьшения эффективности и сохранении переносимости. Опыт более чем 3–5–летнего применения лефлуномида свидетельствует, что препарат сохраняет свою эффективность в длительные сроки (табл. 5, рис. 5) [11,19].
За последние годы изучены комбинации лефлуномида с другими БПВП и биологическими агентами:
– метотрексатом;
– сульфасалазином;
– инфликсимабом;
– этанерцептом;
– адалимумабом.
Результаты исследования RELIEF продемонстрировали, что комбинация лефлуномида и сульфасалазина позволяет увеличить эффективность терапии РА без ухудшения переносимости лечения [20]. Получены данные о достоверно более выраженном эффекте комбинации лефлуномида (10–20 мг/сут.) и метотрексата (10–20 мг/неделю) по сравнению с монотерапией метотрексатом, также при удовлетворительной переносимости комбинации БПВП [21].
Особенный интерес представляет опыт использования лефлуномида в сочетании с биологическим и агентами, в первую очередь с ингибиторами ФНО–a. Уже сообщалось, что комбинация лефлуномида и инфликсимаба эффективна [22]. К настоящему времени отсутствуют проспективные рандомизированные исследования эффективности и переносимости этой комбинации. Имеется ряд открытых исследований, как проспективных, так и ретроспективных (табл. 6), которые свидетельствуют о выраженном эффекте применения инфликсимаба в комбинации с лефлуномидом. Ретроспективные исследования свидетельствуют и о ее приемлемой переносимости, тогда как в проспективных исследованиях данные о частоте побочных эффектов различны. Было высказано мнение [23], что увеличение числа аутоиммунных осложнений при комбинации лефлуномида и инфликсимаба (кожный васкулит, волчаночноподобный синдром, церебральный васкулит, синдром Стивена–Джонса) возникают у больных, имевших АНФ в сыворотке крови к началу терапии, или при его появлении на этапах лечения. Авторы зарегистрировали у своих больных наличие позитивности по АНФ к началу комбинированной терапии у 12% больных, а к концу – у 75% больных. Однако количество больных с позитивным АНФ на фоне лечения инфликсимабом увеличивается и при комбинации с метотрексатом. На сегодняшний день показано, что от присутствия АНФ не зависит ни эффективность, ни переносимость комбинации инфликсимаба с метотрексатом или лефлуномидом. Сравнение эффективности комбинации инфликсимаба с лефлуномидом или другими БПВП (рис. 6) показали их примерно равнозначность. Некоторое преимущество комбинации инфликсимаба именно с лефлуномидом заключается в длительности сохранения эффекта и даже увеличении больных с хорошим эффектом терапии через 18 и 24 месяца лечения. Переносимость комбинированного применения инфликсимаба с лефлуномидом или другими БПВП представлена в таблице 7. Видно, что комбинация инфликсимаба и лефлуномида имеет большее количество слабых побочных реакций за счет симптомов непереносимости со стороны кожи (кожные реакции являются самым частым симптомом непереносимости и монотерапии лефлуномидом). Выраженные побочные реакции при комбинации инфликсимаба с лефлуномидом встречаются не чаще, чем при комбинации с другими БПВП, а тяжелые инфекции встречались даже реже.
Таким образом, можно заключить, что комбинация лефлуномида с инфликсимабом является эффективной; профиль безопасности схож с применением лефлуномида в виде монотерапии; тем не менее частые кожные реакции могут приводить к отмене терапии.
Хорошая переносимость лефлуномида в сроки лечения до 2–3 лет отмечается как отечественными, так и зарубежными авторами [11,19]. Среди наших 50 больных лефлуномид был отменен из–за диареи в 1 случае и из–за кожного зуда у 6 больных, причем отмена препарата вследствие непереносимости потребовалась только у лиц старше 50 лет. У половины больных, получавших лефлуномид в первые месяцы лечения, отмечается повышенное выпадение волос, не требующее отмены лечения. Примерно у 10% больных при назначении лефлуномида может появиться артериальная гипертензия (или измениться течение существовавшей артериальной гипертензии), что требует мониторирования АД и коррекции антигипертензивной терапии. Развитие инфекционных заболеваний (ОРЗ, пневмония, панариций, обострение мочевой инфекции) требует перерыва в лечении лефлуномидом до купирования инфекции с дальнейшим продолжением лечения в обычной суточной дозе.
Основной целью терапии при РА является сохранение функциональной способности больного, предупреждение развитие инвалидности. Поэтому особый интерес представляет влияние терапии лефлуномидом на функциональное состояние больных, оцениваемое по стандартным тестам (HAQ, SF–36). На рисунке 7 продемонстрировано, что уже через 6 месяцев только у 10% больных средний балл индекса HAQ–DI составлял 1,6–2,1; а средний балл 0,5 (то есть практически полное отсутствие функциональной недостаточности) отмечалось у 54% больных [24]. При сравнении улучшения функции под влиянием лефлуномида и сульфасалазина в 2– летнем двойном слепом рандомизированном исследовании показано достоверное преимущество лефлуномида [24]. При оценке качества жизни больных РА по тесту SF–36 уже через 6 месяцев достигнуто достоверное улучшение по 5 из 8 доменов (данные ИР РАМН). При сравнении влияния на качество жизни лефлуномида и метотрексата за 1–2 года терапии было продемонстрировано преимущество лефлуномида с достоверным улучшением, достигающим нормы, по 3 из 8 доменов (телесная боль, жизнеспособность и ролевое эмоциональное функционирование) [17].
Внедрение в ревматологическую практику активных противовоспалительных препаратов (в том числе и лефлуномида, и биологических агентов), безусловно, значительно изменяет течение РА, улучшает качество жизни больных. Все чаще в последние годы женщины, больные РА, высказывают желание иметь ребенка. До настоящего времени при лечении женщины любым цитостатиком врач категорично возражал против зачатия. Вопрос о беременности ставился (и должен ставиться) при достижении ремиссии или сохранении длительно (1–2 года) минимальной активности ревматоидной болезни. Далее делается перерыв в лечении цитостатическим препаратом не менее 6–12 месяцев, а по рекомендации зарубежных авторов – 2 года, после чего женщина может забеременеть. Североамериканскими коллегами накоплен уникальный опыт регистра беременных женщин на фоне различных БПВП, в том числе и лефлуномида [25]. К январю 2007 года регистр составили 227 беременных, включая 62 женщин, получавших лефлуномид, 108 – другие БПВП, и 57 не болеющих РА женщин составили группу сравнения. Исходы беременности представлены в таблице 8. В группе больных РА женщин (табл. 9), получавших лефлуномид, у 4 из 54 живорожденных младенцев были большие структурные дефекты (7,4%), при приеме других БПВП большие структурные дефекты были у 6 из 95 живорожденных (6,3%), в группе сравнения, сопоставимых по основным параметрам, структурные дефекты были у 2 из 54 живорожденных. У больных РА чаще отмечались преждевременные роды, почти у половины больных, независимо от вида лечения, проводилось кесарево сечение. У женщин, получавших лефлуномид, достоверно чаще была преэклампсия. Таким образом, данное исследование позволило сделать следующие выводы:
1. Период гестации при приеме лефлуномида достоверно меньше (37 недель), чем у больных РА группы сравнения (38,1 неделя, р=0,02) и тем более чем у не болеющих РА женщин;
2. При приеме лефлуномида и других БПВП могут развиться у младенцев большие структурные дефекты (среди них микроцефалия). Причем дефекты новорожденных не совпадают с дефектами, полученными у экспериментальных животных [25].
3. Большие структурные дефекты новорожденных не однотипны.
Представляется, что беременность на фоне БПВП является весьма нежелательной, о чем следует настойчиво предупреждать болеющую РА женщину. Среди женщин, находившихся под нашим наблюдением в течение 3 десятилетий, более 20 родили здоровых детей при условии длительного перерыва между последним приемом БПВП и зачатием ребенка.








Литература
1. Pollard L., Choy EH., Scott DL. “ The consequences of rheumatoid arthritis: quality of life measures in the individual patient.” Clin. Exp. Rheum., 2005, 23: 543–552
2. Farragher TM., Lunt M., Bunn DK.et.al. “Early functional disability predicts both all–cause and cardiovascular mortality in people with inflammatory polyarthritis: results from the Norfolk Arthritis Register.” Ann.Rheum.Dis., 2007, 66:486–492
3. Е.Л. Насонов «Почему необходима ранняя диагностика и лечение ревматоидного артрита?» РМЖ, 2002, 10 (22): 1009–1014
4. Е.Л. Насонов, Н.В. Чичасова, К.А. Чижова «Перспективы применения лефлуномида в ревматологии» РМЖ, 2004, 12 (20): 1147–1151
5. Chervinski HM, Coln Rg, Cheung P, Webster DJ, Xu Y–Z, Caulfield JP, et al. The immunosuppressant Leflunomide ingibits lymphocyte proliferation by inhibiting pyrimidine biosynthesis. J Pharmacol Exp Ther 1995;275:1043–9.
6. Siemasko KF, Chong ASF, Williams JW, Bremer EG, Finnegan A. «Regulation of B cell function by the immunosuppressive agent leflunomide» Transplantation 1996;61:635–42.
7. Zeida M.et.al., “Disruption of the interaction of T cells with antigen–presenting cells by the active leflunomide metabolite teriflunomide: involvement of impaired integrin activation and immunologic synapse formation.” Arthr. Rheum., 2005,52(9),2730–39
8. Cutolo M. “Small molecules with high affinity for inflammation mediators: the case for leflunomide” Abstract book “Rheumatoid arthritis: optimizing management through education”, 17–18 March 2007, Vienna, Austria, P. 8–9
9. Cutolo M., Sulli A., Ghiorzo P. et.al “Anti–inflammatory effects of leflunomide on cultured synovial macrophages from patients with rheumatoid arthritis.” Ann. Rheum. Dis., 2003,62(4),297–302
10. Sciff MN, Strand V, Oed C, Loew–Fridirrich I. Leflunomide: efficacy and safety in clinical trials for the treatment of RA. Drugs today. 2000;36:383–394
11. Н.В. Чичасова, К.А. Чижова, Е.В. Иголкина и соавт. «Новый базисный препарат для лечения ревматоидного артрита – АРАВА (лефлуномид): опыт многомесячного применения» РМЖ, 2004, 12 (2): 124–128
12. Sharp J., Strand V., Leung H. et al. ”Treatment with leflunomide slows radiographic progression of rheumatoid arthritis” Arthritis Rheum, 2000, 43:495–505
13. D.E. Karateev, E.L. Luchikhina, E.L. Nasonov “High frequency of clinical remission in patients with early rheumatoid arthritis treated with leflunomide” Ann. Rheum. Dis., 2006, Suppl., EULAR 2006, FRI0179.
14. Scott L. “Comparing the benefits of DMARDs in early rheumatoid arthritis” Abstract book “Advancing arthritis therapy: addressing patient needs” 2006, Seville, Spain, P.8–9
15. Н.В. Чичасова, К.А.Бродецкая, Е.В. Иголкин, Г.Р.Имаметдинова, Е.Л.Насонов «Опыт длительного применения лефлуномида (препарат Арава) у больных активным ревматоидным артритом.» РМЖ, 2005, том 13, №8, 518–524
16. Н.В. Чичасова, Е.В. Иголкина, Г.Р. Имаметдинова «Лефлуномид в терапии ревматоидного артрита» Симпозиум «Базисная противовоспалительная терапия ревматических заболеваний», Москва 15–19 мая, 2006, 7 стр.
17. Strand V., Cohen S., Shiff M. et.al. “Treatment of active rheumatoid arthritis with leflunomide compared with placebo and methotrexate” Arch. Int. Med., 1999, 159: 2542–2550
18. van der Heijde D., Kalden JR., Scott D. et.al. “Long–term evaluation of radiologic disease progression in a subset of patients with rheumatoid arthritis treated with leflunomide beyond 2 years” Ann. Rheum. Dis., 2004, 63:737–739
19. Kalden JR, Schattenkirchen M., Sorensen H. Et.al. “Efficacy and safety of leflunomide in patients with active rheumatoid arthritis: a five–year follow–up” Arthr. Rheum., 2003, 48:1513–1520
20. Dougados M., Emery P., Lemmel EM. et.al. “When a DMARDs fails, should patients switch to sulfasalazine or add sulfasalazine to continuing leflunomide” Ann. Rheum. Dis., 2005, 64: 44–51
21. Kremer JM. “Methotrexate and Leflunomide: biochemical basis for combination therapy in the treatment of rheumatoid arthritis” Arthr. Rheum., 1999, 29: 14–26
22. Kalden JR., Antoni C., Alvaro–Gracia JM. et.al. “Use of combination of leflunomide with biological agents in treatment of rheumatoid arthritis” J. Rheum., 2005, 32: 1620–1631
23. Bingham et.al., Arthr. Rheum., 2004, 50: 4072–3
24. Strand V., Scott D., Emery P. Et.al. “Physical function and health related quality of life analysis of 2–year data from randomized, controlled studies of leflunomide, sulfasalazine, or methotrexate in patients with active rheumatoid arthritis” J. Rheum., 2005, 32: 590–601
25. Chambers C. ”Pregnancy outcomes in women inadvertently exposed to DMARDs: results of the OTIS medications in pregnancy project” Abstract book “Rheumatoid arthritis: optimizing management trough education” 17–18 March 2007, Vienna, Austria, P. 20–21
26. P. van Riel “Insights from Dutch DMARD and biologic registries” Abstract book “Rheumatoid arthritis: optimizing management trough education” 17-18 March 2007, Vienna, Austria, P. 16-17












