–°—А–µ–і–Є –њ—А–Є—З–Є–љ –Њ—Б—В—А—Л—Е –±–Њ–ї–µ–є –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л –≤—Л–і–µ–ї—П—О—В:
• –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О –Љ—Л—И–µ—З–љ–Њ–—Б–≤—П–Ј–Њ—З–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А —Б–њ–Є–љ—Л
• —Б–њ–Њ–љ–і–Є–ї–µ–Ј (—Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–Ј)
• –≥—А—Л–ґ—Г –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –і–Є—Б–Ї–∞
• —Б—В–µ–љ–Њ–Ј –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞
–Т –Ї–∞–ґ–і–Њ–Љ –Є–Ј —Н—В–Є—Е —Б–ї—Г—З–∞–µ–≤ –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –Є–Љ–µ–µ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —Б–≤–Њ–µ–Њ–±—А–∞–Ј–Є–µ, —А–∞–Ј–ї–Є—З–љ—Г—О –≤—А–µ–Љ–µ–љ–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –Є –њ—А–Њ–≥–љ–Њ–Ј.
–°—А–µ–і–Є —Д–∞–Ї—В–Њ—А–Њ–≤, –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—Й–Є—Е —А–∞–Ј–≤–Є—В–Є–µ –Њ—Б—В—А–Њ–є –ї—О–Љ–±–∞–ї–≥–Є–Є, –≤—Л–і–µ–ї—П—О—В —В—А–∞–≤–Љ—Г, –њ–Њ–і—К–µ–Љ –љ–µ–њ–Њ—Б–Є–ї—М–љ–Њ–≥–Њ –≥—А—Г–Ј–∞, –љ–µ–њ–Њ–і–≥–Њ—В–Њ–≤–ї–µ–љ–љ—Л–µ –і–≤–Є–ґ–µ–љ–Є—П, –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–µ–±—Л–≤–∞–љ–Є–µ –≤ –љ–µ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–Њ–Ј–µ, –њ–µ—А–µ–Њ—Е–ї–∞–ґ–і–µ–љ–Є–µ (—В–∞–±–ї. 1).
–У—А—Л–ґ–∞ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –і–Є—Б–Ї–∞ ( –Ь–Я–Ф) – –Њ—Б–љ–Њ–≤–љ–∞—П –њ—А–Є—З–Є–љ–∞ –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ–є –±–Њ–ї–Є —Г –ї–Є—Ж –Љ–Њ–ї–Њ–і–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ (30–50 –ї–µ—В). –Я–Њ–і –≥—А—Л–ґ–µ–є –Ь–Я–Ф –њ–Њ–љ–Є–Љ–∞—О—В –≤—Л–њ—П—З–Є–≤–∞–љ–Є–µ –њ—Г–ї—М–њ–Њ–Ј–љ–Њ–≥–Њ —П–і—А–∞ –Ь–Я–Ф —Б —А–∞–Ј—А—Л–≤–Њ–Љ –љ–∞—А—Г–ґ–љ—Л—Е —Б–ї–Њ–µ–≤ —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї—М—Ж–∞ –Ј–∞ –њ—А–µ–і–µ–ї—Л –ї–Є–љ–Є–Є, —Б–Њ–µ–і–Є–љ—П—О—Й–µ–є —В–µ–ї–∞ —Б–Њ—Б–µ–і–љ–Є—Е –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤ [2]. –° —Г—З–µ—В–Њ–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П –≥—А—Л–ґ–µ–≤–Њ–≥–Њ –≤—Л–њ—П—З–Є–≤–∞–љ–Є—П –≤—Л–і–µ–ї—П—О—В —Б–ї–µ–і—Г—О—Й–Є–µ –Є—Е –≤–Є–і—Л:
1. –Ф–Њ—А—Б–∞–ї—М–љ—Л–µ (–Љ–µ–і–Є–∞–љ–љ—Л–µ, –њ–∞—А–∞–Љ–µ–і–Є–∞–љ–љ—Л–µ, —Д–Њ—А–∞–Љ–Є–љ–∞–ї—М–љ—Л–µ), –њ—А–Њ–љ–Є–Ї–∞—О—Й–Є–µ –≤ —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –Ї–∞–љ–∞–ї –Є–ї–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л–µ –Њ—В–≤–µ—А—Б—В–Є—П –Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–µ—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Њ–є.
2. –Т–µ–љ—В—А–∞–ї—М–љ—Л–µ –Є –ї–∞—В–µ—А–∞–ї—М–љ—Л–µ, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є–µ –±–Њ–ї—М—И–µ–є —З–∞—Б—В—М—О –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ.
3. –У—А—Л–ґ–Є –®–Љ–Њ—А–ї—П – –Њ–±—А–∞–Ј—Г—О—В—Б—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ –≤–љ–µ–і—А–µ–љ–Є—П –њ—Г–ї—М–њ–Њ–Ј–љ–Њ–≥–Њ —П–і—А–∞ –Ь–Я–Ф –≤ –≥—Г–±—З–∞—В–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ —В–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Ї–∞ —Б —А–∞–Ј—А—Г—И–µ–љ–Є–µ–Љ –µ–≥–Њ –Ј–∞–Љ—Л–Ї–∞—В–µ–ї—М–љ–Њ–є –њ–ї–∞—Б—В–Є–љ—Л. –У—А—Л–ґ–Є –®–Љ–Њ—А–ї—П –Њ–±—Л—З–љ–Њ —П–≤–ї—П—О—В—Б—П —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –љ–∞—Е–Њ–і–Ї–Њ–є –Є –љ–µ –Є–Љ–µ—О—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П.
–Я—А–Є –і–Њ—А—Б–∞–ї—М–љ–Њ–Љ –≥—А—Л–ґ–µ–≤–Њ–Љ –≤—Л–њ—П—З–Є–≤–∞–љ–Є–Є –Ь–Я–Ф –±–Њ–ї—М –≤–љ–∞—З–∞–ї–µ –њ–Њ—П–≤–ї—П–µ—В—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П –±–Њ–ї–µ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –љ–∞—А—Г–ґ–љ—Л—Е —Б–ї–Њ–µ–≤ —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї—М—Ж–∞ –Є –Ј–∞–і–љ–µ–є –њ—А–Њ–і–Њ–ї—М–љ–Њ–є —Б–≤—П–Ј–Ї–Є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–≥–Њ—Б—П —Б–њ–∞–Ј–Љ–Њ–Љ —Б–µ–≥–Љ–µ–љ—В–∞—А–љ—Л—Е –Љ—Л—И—Ж (—А–µ—Д–ї–µ–Ї—В–Њ—А–љ–∞—П –ї—О–Љ–±–Њ–Є—И–Є–∞–ї–≥–Є—П). –°–Љ–µ—Й–∞—П—Б—М –≤ —Б—В–Њ—А–Њ–љ—Г –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –Є–ї–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П, –≥—А—Л–ґ–∞ –Ь–Я–Ф –Љ–Њ–ґ–µ—В –Ї–Њ–Љ–њ—А–Є–Љ–Є—А–Њ–≤–∞—В—М —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –Ї–Њ—А–µ—И–Њ–Ї, —З—В–Њ –≤–µ–і–µ—В –Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (—А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є). –Я—А–Њ—Ж–µ—Б—Б—Л –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Ї–Њ—А–µ—И–Ї–∞ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –љ–µ–≤—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –љ–∞ —Г—А–Њ–≤–љ–µ –Я–Ф–° [5].
–С–Њ–ї—М –њ—А–Є –≥—А—Л–ґ–µ –і–Є—Б–Ї–∞ —З–∞—Б—В–Њ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –њ—А–Є —А–µ–Ј–Ї–Њ–Љ –і–≤–Є–ґ–µ–љ–Є–Є, –љ–∞–Ї–ї–Њ–љ–µ, –њ–Њ–і—К–µ–Љ–µ —В—П–ґ–µ—Б—В–Є –Є–ї–Є –њ–∞–і–µ–љ–Є–Є. –С–Њ–ї—М —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є –і–≤–Є–ґ–µ–љ–Є–Є, –љ–∞—В—Г–ґ–Є–≤–∞–љ–Є–Є, –њ–Њ–і—К–µ–Љ–µ —В—П–ґ–µ—Б—В–Є, —Б–Є–і–µ–љ–Є–Є –≤ –≥–ї—Г–±–Њ–Ї–Њ–Љ –Ї—А–µ—Б–ї–µ, –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–µ–±—Л–≤–∞–љ–Є–Є –≤ –Њ–і–љ–Њ–є –њ–Њ–Ј–µ, –њ—А–Є –Ї–∞—И–ї–µ –Є —З–Є—Е–∞–љ—М–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ –µ—Б–ї–Є –±–Њ–ї—М–љ–Њ–є –ї–µ–ґ–Є—В –љ–∞ –Ј–і–Њ—А–Њ–≤–Њ–Љ –±–Њ–Ї—Г, —Б–Њ–≥–љ—Г–≤ –±–Њ–ї—М–љ—Г—О –љ–Њ–≥—Г –≤ –Ї–Њ–ї–µ–љ–љ–Њ–Љ –Є —В–∞–Ј–Њ–±–µ–і—А–µ–љ–љ–Њ–Љ —Б—Г—Б—В–∞–≤–µ.
–•–∞—А–∞–Ї—В–µ—А–љ—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –і–Њ—А—Б–∞–ї–≥–Є–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є –≥—А—Л–ґ–µ–є –Ь–Я–Ф, –Є –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –љ–∞ —Б—Е–µ–Љ–µ 1.
–°–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, —П–≤–ї—П—О—Й–Є—Е—Б—П –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –і–µ–Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Є –њ—А–Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –Њ—В—А–∞–ґ–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2 – «–њ—А–∞–≤–Є–ї–Њ –њ—П—В–Є» –Ь–∞–Ї–љ–∞–±–∞.
–Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О –≥—А—Л–ґ–Є –і–Є—Б–Ї–∞ –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П —Б–ї–µ–і—Г—О—Й–Є–Љ–Є —Г—Б–ї–Њ–≤–Є—П–Љ–Є [5]:
• –љ–∞–ї–Є—З–Є–µ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞;
• –≤—Л—П–≤–ї–µ–љ–Є–µ–Љ –њ—А–Є –Ь–†–Ґ –Ј–∞–і–љ–µ–є –≥—А—Л–ґ–Є –і–Є—Б–Ї–∞ –±–Њ–ї–µ–µ 5 –Љ–Љ;
• –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —Н—Д—Д–µ–Ї—В–∞ –Њ—В —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Э–∞ —Н—В–∞–њ–∞—Е –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Њ—Б—В—А–Њ–є –ї—О–Љ–±–∞–ї–≥–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–Љ–љ–Є—В—М –Њ –≤—В–Њ—А–Є—З–љ–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А–µ –±–Њ–ї–µ–є –≤ —Б–њ–Є–љ–µ. –Ъ–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ—Л–є –њ–µ—А–µ–ї–Њ–Љ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –њ—А–Є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–µ –Є–ї–Є –Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–µ (–Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ, –≥–µ–Љ–∞–љ–≥–Є–Њ–Љ—Л —В–µ–ї –њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤) –Љ–Њ–≥—Г—В —Б–ї—Г–ґ–Є—В—М –њ—А–Є—З–Є–љ–Њ–є –Њ—Б—В—А—Л—Е –±–Њ–ї–µ–є –≤ —Б–њ–Є–љ–µ. –Ю—Б—В–µ–Њ–њ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ—Л–є –њ–µ—А–µ–ї–Њ–Љ –Є–Љ–µ–µ—В —Е–∞—А–∞–Ї—В–µ—А–љ—Г—О –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Њ–Ї—А–∞—Б–Ї—Г: –±–Њ–ї—М –Љ–Њ–ґ–µ—В –Є—А—А–∞–і–Є–Є—А–Њ–≤–∞—В—М –≤ –≥—А—Г–і–љ—Г—О –Ї–ї–µ—В–Ї—Г, –±—А—О—И–љ—Г—О –њ–Њ–ї–Њ—Б—В—М –Є–ї–Є –±–µ–і—А–Њ —Б —А–µ–Ј–Ї–Є–Љ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–µ–Љ –і–≤–Є–ґ–µ–љ–Є–є. –С–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –і–ї–Є—В—Б—П 1–2 –љ–µ–і–µ–ї–Є, –Ј–∞—В–µ–Љ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Б—В–Є—Е–∞–µ—В. –Ю–±—Л—З–љ–Њ —Б—В—А–∞–і–∞—О—В –њ–Њ–Ј–≤–Њ–љ–Ї–Є, –Є—Б–њ—Л—В—Л–≤–∞—О—Й–Є–µ –љ–∞–Є–±–Њ–ї—М—И—Г—О –Њ—Б–µ–≤—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г (X–XII –≥—А—Г–і–љ—Л–µ –Є I–II –њ–Њ—П—Б–љ–Є—З–љ—Л–µ –њ–Њ–Ј–≤–Њ–љ–Ї–Є).
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ–Њ —В–Є–њ—Г –Њ—Б—В—А–Њ–є –ї—О–Љ–±–∞–ї–≥–Є–Є –Љ–Њ–≥—Г—В –њ—А–Њ—В–µ–Ї–∞—В—М —А–∞–Ј—А—Л–≤ –∞–љ–µ–≤—А–Є–Ј–Љ—Л –±—А—О—И–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –∞–Њ—А—В—Л, –і–Є–≤–µ—А—В–Є–Ї—Г–ї–Є—В—Л, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Љ–Њ—З–µ–њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤ (–∞–ї—М–≥–Њ–і–Є—Б–Љ–µ–љ–Њ—А—А–µ—П, –Љ–Њ—З–µ–Ї–∞–Љ–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М).
–Ю–і–љ–∞–Ї–Њ —Б–∞–Љ–Њ–є —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є –Њ—Б—В—А–Њ–є –ї—О–Љ–±–∞–ї–≥–Є–Є —Г –њ–Њ–ґ–Є–ї—Л—Е —П–≤–ї—П–µ—В—Б—П —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–Ј, –Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л–є –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ. –Я—А–Є –∞—А—В—А–Њ–Ј–µ —Д–∞—Б–µ—В–Њ—З–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤ –±–Њ–ї—М (–Њ–±—Л—З–љ–Њ –і–≤—Г—Е—Б—В–Њ—А–Њ–љ–љ—П—П) –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ—В—Б—П –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –і–Є—Б–Ї–Њ–≥–µ–љ–љ–Њ–є –њ–∞—А–∞–≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ, –∞ –љ–µ –њ–Њ —Б—А–µ–і–љ–µ–є –ї–Є–љ–Є–Є, —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ —Б—В–Њ—П–љ–Є–Є –Є–ї–Є —А–∞–Ј–≥–Є–±–∞–љ–Є–Є –Є —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –њ—А–Є —Е–Њ–і—М–±–µ –Є —Б–Є–і–µ–љ–Є–Є.
–Т–∞–ґ–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –±–Њ–ї–Є –њ—А–Є —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–Ј–µ —П–≤–ї—П–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ –љ–µ–≤—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Т –њ—А–Њ—Ж–µ—Б—Б–µ –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є —Б—Г—Б—В–∞–≤–љ–Њ–≥–Њ —Е—А—П—Й–∞ –≤ —Д–∞—Б–µ—В–Њ—З–љ—Л—Е —Б—Г—Б—В–∞–≤–∞—Е, –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –і–Є—Б–Ї–∞ –Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є –љ–Њ—Ж–Є—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ —Б—В—А—Г–Ї—В—Г—А–∞—Е –Я–Ф–° –≤–Њ–Ј–љ–Є–Ї–∞—О—В –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ –Є –Є–Љ–Љ—Г–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –Ј–∞–≤–µ—А—И–∞—О—В—Б—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–µ–є—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ «—Ж–Є—В–Њ–Ї–Є–љ–Њ–≤–Њ–≥–Њ –Ї–∞—Б–Ї–∞–і–∞».
–°—В—А–∞—В–µ–≥–Є—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї–µ–є –њ—А–Є –Њ—Б—В—А–Њ–є –ї—О–Љ–±–∞–ї–≥–Є–Є –≤–Ї–ї—О—З–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ – –Э–Я–Т–Я – –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е —Б—Г—В–Њ–Ї, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–µ–є—Б—В–≤–Є—П. –Я—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–µ –Є –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Э–Я–Т–Я —Б–≤—П–Ј–∞–љ–Њ —Б –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ–Љ –¶–Ю–У –Є —В–Њ—А–Љ–Њ–Ј—П—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ —Б–Є–љ—В–µ–Ј –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –Є —Н–є–Ї–Њ–Ј–∞–љ–Њ–Є–і–Њ–≤, —П–≤–ї—П—О—Й–Є—Е—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –Љ–µ–і–Є–∞—В–Њ—А–∞–Љ–Є, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є–Љ–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ, –і–Є–љ–∞–Љ–Є–Ї—Г –Є –Є—Б—Е–Њ–і—Л –±–Њ–ї–µ–≤—Л—Е –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ [3]. –Э–Њ–≤–µ–є—И–Є–µ –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В, —З—В–Њ –Э–Я–Т–Я –љ–µ —В–Њ–ї—М–Ї–Њ —Г–≥–љ–µ—В–∞—О—В —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ, –љ–Њ –Є –∞–Ї—В–Є–≤–љ–Њ –≤–ї–Є—П—О—В –љ–∞ —Б–Є–љ—В–µ–Ј –Я–У, —Б–≤—П–Ј–∞–љ–љ—Л–є —Б –Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є–µ–є –°–∞ –≤ –≥–ї–∞–і–Ї–Є—Е –Љ—Л—И—Ж–∞—Е. –Т–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–Љ –і–µ–є—Б—В–≤–Є–Є –Э–Я–Т–Я –Є–≥—А–∞–µ—В –Є—Е –≤–ї–Є—П–љ–Є–µ –љ–∞ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –Є –±–Є–Њ—Н—Д—Д–µ–Ї—В—Л –Ї–Є–љ–Є–љ–Њ–≤. –°–љ–Є–ґ–µ–љ–Є–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —В–Њ—А–Љ–Њ–ґ–µ–љ–Є—О –∞–Ї—В–Є–≤–∞—Ж–Є–Є —Д–Њ—Б—Д–Њ—А–Є–ї–∞–Ј—Л, —З—В–Њ –≤–µ–і–µ—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ – –њ—А–Њ—П–≤–ї–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–Њ–і—Г–Ї—В–Њ–≤ –µ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞. –Э–µ –Љ–µ–љ–µ–µ –≤–∞–ґ–љ–Њ–є —П–≤–ї—П–µ—В—Б—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Э–Я–Т–Я –±–ї–Њ–Ї–Є—А–Њ–≤–∞—В—М –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞ —Б —В–Ї–∞–љ–µ–≤—Л–Љ–Є —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –љ–∞—А—Г—И–µ–љ–љ–Њ–є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є, —Г–Љ–µ–љ—М—И–µ–љ–Є—О –њ–µ—А–µ—А–∞—Б—В—П–ґ–µ–љ–Є—П –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є—О –≤—Л—Е–Њ–і–∞ –ґ–Є–і–Ї–Њ–є —З–∞—Б—В–Є –њ–ї–∞–Ј–Љ—Л, –µ–µ –±–µ–ї–Ї–Њ–≤, –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –Є —Д–Њ—А–Љ–µ–љ–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤, —З—В–Њ –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ –≤–ї–Є—П–µ—В –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –і—А—Г–≥–Є—Е —Д–∞–Ј –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ [3]. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –Ї–∞–ї–ї–Є–Ї—А–µ–Є–љ––Ї–Є–љ–Є–љ–Њ–≤–∞—П —Б–Є—Б—В–µ–Љ–∞ –Є–≥—А–∞–µ—В –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –Њ—Б—В—А—Л—Е –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, —В–Њ –Є –љ–∞–Є–±–Њ–ї—М—И–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Э–Я–Т–Я –Њ—В–Љ–µ—З–∞–µ—В—Б—П –≤ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–Ю–і–љ–Є–Љ –Є–Ј —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Ъ–µ—В–Њ—А–Њ–ї (–Ї–µ—В–Њ—А–Њ–ї–∞–Ї) – –њ—А–Њ–Є–Ј–≤–Њ–і–љ–Њ–µ –∞—А–Є–ї—Г–Ї—Б—Г—Б–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –Є–љ–≥–Є–±–Є—В–Њ—А —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л. –Х–≥–Њ –Њ—Б–љ–Њ–≤–љ–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Ж–µ–љ–љ–Њ—Б—В—М —Б–≤—П–Ј–∞–љ–∞ —Б –Љ–Њ—Й–љ—Л–Љ –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞, –њ–Њ —Б—В–µ–њ–µ–љ–Є –Ї–Њ—В–Њ—А–Њ–≥–Њ –Њ–љ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –і—А—Г–≥–Є–µ –Э–Я–Т–Я. –Я—А–µ–њ–∞—А–∞—В –±—Л—Б—В—А–Њ –≤—Б–∞—Б—Л–≤–∞–µ—В—Б—П, –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О (80–100%). –Ъ–µ—В–Њ—А–Њ–ї–∞–Ї —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є –њ–ї–∞–Ј–Љ—Л –љ–∞ 90–99%, –њ–Њ–і–≤–µ—А–≥–∞–µ—В—Б—П –њ–µ—З–µ–љ–Њ—З–љ–Њ–Љ—Г –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ—Г, –≤—Л–≤–Њ–і–Є—В—Б—П –њ–Њ—З–Ї–∞–Љ–Є (90%) –Є –Ї–Є—И–µ—З–љ–Є–Ї–Њ–Љ (6%). –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ – 6–10 —З–∞—Б–Њ–≤. –Т—Л–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ –і–≤—Г—Е —Д–Њ—А–Љ–∞—Е: —В–∞–±–ї–µ—В–Ї–Є –і–ї—П –њ—А–Є–µ–Љ–∞ –≤–љ—Г—В—А—М –њ–Њ 10 –Љ–≥ –Є —А–∞—Б—В–≤–Њ—А –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –≤ –∞–Љ–њ—Г–ї–∞—Е – 30 –Љ–≥/1 –Љ–ї.
–Ф–ї—П –Є–Ј—Г—З–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–µ—В–Њ—А–Њ–ї —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≤ —Б–њ–Є–љ–µ –љ–∞ –Ї–∞—Д–µ–і—А–µ —Д–∞–Ї—Г–ї—М—В–µ—В—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Є–Љ. –∞–Ї–∞–і. –Р.–Ш. –Э–µ—Б—В–µ—А–Њ–≤–∞ –†–У–Ь–£ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Њ—В–Ї—А—Л—В–Њ–µ –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ. –¶–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–є –Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ –Ъ–µ—В–Њ—А–Њ–ї–∞ –њ—А–Є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л–Љ —Б —Г–Љ–µ—А–µ–љ–љ—Л–Љ –Є –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≤ —Б–њ–Є–љ–µ (–љ–µ –Љ–µ–љ–µ–µ 40 –Љ–Љ –њ–Њ –Т–Р–®).
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 30 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 30 –і–Њ 65 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 49,4 –ї–µ—В, –Љ—Г–ґ—З–Є–љ – 17, –ґ–µ–љ—Й–Є–љ – 13). –£ 7 –±–Њ–ї—М–љ—Л—Е –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–∞ –і–Њ—А—Б–Њ–њ–∞—В–Є—П, —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–Ј –њ–Њ—П—Б–љ–Є—З–љ–Њ––Ї—А–µ—Б—В—Ж–Њ–≤–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ (—Г 3 —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–Ј –Њ—Б–ї–Њ–ґ–љ–Є–ї—Б—П –ї—О–Љ–±–∞–ї–≥–Є–µ–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –≤ —Б—В–∞–і–Є–Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П, —Г 4 – –ї—О–Љ–±–∞–ї–≥–Є–µ–є –Њ—Б—В—А–Њ–≥–Њ —В–µ—З–µ–љ–Є—П), —Г 13 –±–Њ–ї—М–љ—Л—Е – –і–Њ—А—Б–Њ–њ–∞—В–Є—П, –ї—О–Љ–±–∞–ї–≥–Є—П –Њ—Б—В—А–Њ–≥–Њ —В–µ—З–µ–љ–Є—П, —Г 6 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –ї—О–Љ–±–Њ–Є—И–Є–∞–ї–≥–Є—П –±—Л–ї–∞ –≤—Л–Ј–≤–∞–љ–∞ –≥—А—Л–ґ–µ–є –Ь–Я–Ф –љ–∞ —Г—А–Њ–≤–љ–µ L4–L5, L5–S1, —Г 1––≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ – –ї—О–Љ–±–∞–ї–≥–Є—П –≤ —А–∞–Љ–Ї–∞—Е –∞–љ–Ї–Є–ї–Њ–Ј–Є—А—Г—О—Й–µ–≥–Њ —Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Є—В–∞, –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–µ–≥–Њ —Б–∞–Ї—А–Њ–Є–ї–µ–Є—В–∞ 2 —Б—В., 1 –±–Њ–ї—М–љ–∞—П —Б —В–Њ—А–∞–Ї–Њ–ї—О–Љ–±–∞–ї–≥–Є–µ–є –Њ—Б—В—А–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ–≥–Њ –њ–µ—А–µ–ї–Њ–Љ–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –љ–∞ —Д–Њ–љ–µ –њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ–Њ–≥–Њ –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–∞, 2 –њ–∞—Ж–Є–µ–љ—В–Ї–Є —Б —В–Њ—А–∞–Ї–Њ–ї—О–Љ–±–∞–ї–≥–Є–µ–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—З–µ–љ–Є—П –≤ —Б—В–∞–і–Є–Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П (–њ–Њ—Б—В–Љ–µ–љ–Њ–њ–∞—Г–Ј–∞–ї—М–љ—Л–є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј, –≤—В–Њ—А–Є—З–љ—Л–є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј –љ–∞ —Д–Њ–љ–µ —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–≥–Њ –∞—А—В—А–Є—В–∞). –Ф–Є–∞–≥–љ–Њ–Ј—Л –±—Л–ї–Є –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ—Л –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е, 6–—В–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Ь–†–Ґ– –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —Б —Ж–µ–ї—М—О –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—Л—П–≤–ї–µ–љ–љ—Л—Е –≥—А—Л–ґ –Ь–Я–Ф –љ–∞ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ —Г—А–Њ–≤–љ–µ.
–Ю–±—Й–∞—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–µ –њ—А–µ–≤—Л—И–∞–ї–∞ 5 –і–љ–µ–є. –Э–∞ –њ–µ—А–≤–Њ–Љ —Н—В–∞–њ–µ –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –Ъ–µ—В–Њ—А–Њ–ї –≤ –≤–Є–і–µ –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 60 –Љ–≥ (30 –Љ–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є) –≤ —В–µ—З–µ–љ–Є–µ 2 –і–љ–µ–є, –Ј–∞—В–µ–Љ –≤ —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ–µ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 20 –Љ–≥ (10 –Љ–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є). –Т–Њ –≤—А–µ–Љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Є–µ–Љ –і—А—Г–≥–Є—Е –Э–Я–Т–Я, –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤ –Є—Б–Ї–ї—О—З–∞–ї—Б—П.
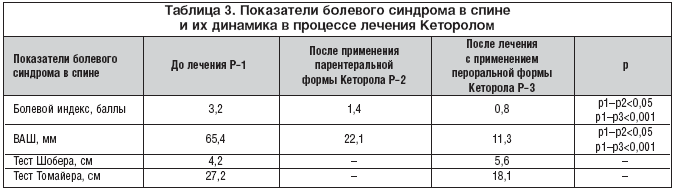
–Ю—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –≤–Є–Ј—Г–∞–ї—М–љ–Њ–є –∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї—Л (–Т–Р–®), –±–Њ–ї–µ–≤–Њ–≥–Њ –Є–љ–і–µ–Ї—Б–∞ (–±–∞–ї–ї—Л), —В–µ—Б—В–∞ –Ґ–Њ–Љ–∞–є–µ—А–∞ (—Б–Љ), —В–µ—Б—В–∞ –®–Њ–±–µ—А–∞ (—Б–Љ).
–Я–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –і–Њ –ї–µ—З–µ–љ–Є—П –њ–Њ –Т–Р–® —Б–Њ—Б—В–∞–≤–Є–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 65,4 –Љ–Љ. –Я–Њ—Б–ї–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–µ—А–≤–Њ–є –і–Њ–Ј—Л –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–µ—В–Њ—А–Њ–ї –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ –Т–Р–® –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–Ј–Є–ї–∞—Б—М (—А<0,05) –Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 22,1 –Љ–Љ, –њ–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П 5––і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –і–Њ—Б—В–Є–≥–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 11,3 –Љ–Љ. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –±–Њ–ї–µ–≤–Њ–≥–Њ –Є–љ–і–µ–Ї—Б–∞ –і–Њ –Є –≤–Њ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 3,2; 1,4; 0,8 –±–∞–ї–ї–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —В–µ—Б—В–∞ –Ґ–Њ–Љ–∞–є–µ—А–∞ –і–Њ –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–Є –≤ —Б—А–µ–і–љ–µ–Љ 27,2 —Б–Љ, –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П – 18,1 —Б–Љ, —В–µ—Б—В –®–Њ–±–µ—А–∞ – 4,2 –Є 5,6 —Б–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—В–∞–±–ї. 3).
–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж—Л 3, —Г –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–∞–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ—Б–ї–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ–є —Д–Њ—А–Љ—Л –Ъ–µ—В–Њ—А–Њ–ї–∞ (—А<0,05) –Є –њ–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –ї–µ—З–µ–љ–Є—П –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–µ—А–≤–Є—З–љ—Л–Љ–Є –і–∞–љ–љ—Л–Љ–Є (p<0,001). –Ю–±—К–µ–Љ –і–≤–Є–ґ–µ–љ–Є–є –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ъ–µ—В–Њ—А–Њ–ї–Њ–Љ —Г–≤–µ–ї–Є—З–Є–ї—Б—П, —З—В–Њ –Њ—В—А–∞–ґ–µ–љ–Њ –≤ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —В–µ—Б—В–∞ –Ґ–Њ–Љ–∞–є–µ—А–∞ (—Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –і–≤–Є–ґ–µ–љ–Є–є –љ–∞ 33% –Њ—В –Є—Б—Е–Њ–і–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є) –Є —В–µ—Б—В–∞ –®–Њ–±–µ—А–∞ (—Г–≤–µ–ї–Є—З–µ–љ–Є–µ –љ–∞ 25%).
–Т–∞–ґ–љ—Л–Љ —Н—В–∞–њ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–ї—П–µ—В—Б—П –Њ—Ж–µ–љ–Ї–∞ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Ъ–µ—В–Њ—А–Њ–ї–∞. –£ 83% –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —Е–Њ—А–Њ—И–∞—П –Є –Њ—В–ї–Є—З–љ–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ (—В–∞–±–ї. 4).
–£ 5 (16%) —З–µ–ї–Њ–≤–µ–Ї –≤—Л—П–≤–ї–µ–љ—Л –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л: 1 –њ–∞—Ж–Є–µ–љ—В – –≥–∞—Б—В—А–∞–ї–≥–Є—П –љ–∞ –њ–µ—А–≤–Њ–Љ –і–љ–µ –ї–µ—З–µ–љ–Є—П, 1 –њ–∞—Ж–Є–µ–љ—В – –≥–∞—Б—В—А–∞–ї–≥–Є—П –Є —З—Г–≤—Б—В–≤–Њ –њ–µ—А–µ–њ–Њ–ї–љ–µ–љ–Є—П –ґ–µ–ї—Г–і–Ї–∞ –љ–∞ —В—А–µ—В—М–µ–Љ –і–љ–µ –ї–µ—З–µ–љ–Є—П, —З—В–Њ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞; 1 –±–Њ–ї—М–љ–Њ–є – –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–∞—П—Б—П –њ–Њ–і—К–µ–Љ–Њ–Љ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П (–≤–Њ–Ј–љ–Є–Ї—И–µ–µ –њ–Њ–±–Њ—З–љ–Њ–µ —П–≤–ї–µ–љ–Є–µ –љ–µ —В—А–µ–±–Њ–≤–∞–ї–Њ –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Є –Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–∞–ї–Њ—Б—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ–Љ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤); —Г 1 –њ–∞—Ж–Є–µ–љ—В–∞ –≤–Њ–Ј–љ–Є–Ї–ї–Њ –ґ–ґ–µ–љ–Є–µ –≤ –Љ–µ—Б—В–µ –≤–≤–µ–і–µ–љ–Є—П –Є–љ—К–µ–Ї—Ж–Є–Є, —Г 1 –±–Њ–ї—М–љ–Њ–≥–Њ – —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М (–≤ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Б–ї—Г—З–∞—П—Е –Њ—В–Љ–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ —В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М).
–Т—Л–≤–Њ–і—Л
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ —Б–њ–Є–љ–µ –њ–Њ –Т–Р–® —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –Ї 3––Љ—Г –і–љ—О –ї–µ—З–µ–љ–Є—П –љ–∞ 66% –Є –љ–∞ 82% – –Ї –Њ–Ї–Њ–љ—З–∞–љ–Є—О –ї–µ—З–µ–љ–Є—П. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –±–Њ–ї–µ–≤–Њ–≥–Њ –Є–љ–і–µ–Ї—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М –≤ 2,3 —А–∞–Ј–∞, –њ–Њ—Б–ї–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л —Б–љ–Є–Ј–Є–ї–Є—Б—М –≤ 4 —А–∞–Ј–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ–Є. –Ґ–µ—Б—В—Л, –Њ—В—А–∞–ґ–∞—О—Й–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞.
–Я—А–Є –Њ—Ж–µ–љ–Ї–µ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Ъ–µ—В–Њ—А–Њ–ї–∞ —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–µ–љ–∞ –Њ—В–ї–Є—З–љ–∞—П –Є–ї–Є —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞. –£–Ї–∞–Ј–∞–љ–љ—Л–µ –≤—Л—И–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–µ –љ–Њ—Б–Є–ї–Є —Е–∞—А–∞–Ї—В–µ—А–∞ —Б–µ—А—М–µ–Ј–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є.
–Т –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–∞ –≤—Л—Б–Њ–Ї–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–µ—В–Њ—А–Њ–ї —Б —Е–Њ—А–Њ—И–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –µ–≥–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є —Г –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≤ —Б–њ–Є–љ–µ –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –њ–Њ —Б—Е–µ–Љ–µ: 2 –і–љ—П – 60 –Љ–≥/—Б—Г—В. – –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ; –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–µ 3 –і–љ—П – 20 –Љ–≥/—Б—Г—В. –њ–µ—А–Њ—А–∞–ї—М–љ–Њ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ъ–µ—В–Њ—А–Њ–ї –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Є –Љ–Њ–ґ–µ—В –±—Л—В—М —Б —Г—Б–њ–µ—Е–Њ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ –і–ї—П —А–∞–љ–љ–µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ—А–Є –і–Њ—А—Б–Њ–њ–∞—В–Є—П—Е, –і–Њ—А—Б–∞–ї–≥–Є—П—Е; –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –µ–≥–Њ –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —Б –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є.
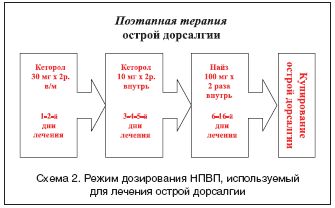
–° —Г—З–µ—В–Њ–Љ –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –љ–∞–Љ–Є –њ—А–Є–Љ–µ–љ–µ–љ–∞ —Б—Е–µ–Љ–∞ –њ–Њ—Н—В–∞–њ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А–Њ–є –і–Њ—А—Б–∞–ї–≥–Є–Є, —Б–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ—В–Њ—А–Њ–є –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 5 –і–љ–µ–є –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–∞—П –Є —В–∞–±–ї–µ—В–Є—А–Њ–≤–∞–љ–љ–∞—П —Д–Њ—А–Љ—Л –Ъ–µ—В–Њ—А–Њ–ї–∞, —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –њ–µ—А–µ—Е–Њ–і–Њ–Љ –љ–∞ –њ—А–Є–µ–Љ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є–љ–≥–Є–±–Є—В–Њ—А–∞ –¶–Ю–У–2 – –Э–∞–є–Ј–∞ –≤ –і–Њ–Ј–µ 200 –Љ–≥/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 10 –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е –і–љ–µ–є (—Б—Е–µ–Љ–∞ 2).
–£–Ї–∞–Ј–∞–љ–љ–∞—П —Б—Е–µ–Љ–∞ –ї–µ—З–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є, –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–є –Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Ї—Г–њ–Є—А–Њ–≤–∞—В—М —Б–Є–Љ–њ—В–Њ–Љ—Л –Њ—Б—В—А–Њ–є –і–Њ—А—Б–∞–ї–≥–Є–Є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е.




–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Т–∞—Б–Є–ї—М–µ–≤ –Р.–Ѓ., –Т–Є—В—М–Ї–Њ –Э.–Ъ. – –Ъ–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –Ь–2000 –≥
2. –Ы–µ–≤–Є–љ –Ю.–°. – –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –Consilium–medicum –2004–≥
3. –Э–∞—Б–Њ–љ–Њ–≤ –Х.–Ы. –Э–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Љ–µ–і–Є—Ж–Є–љ–µ) –Ь.,2000, 262
4. –£–ї—М—А–Є—Е –≠.–Т., –Ь—Г—И–Ї–Є–љ –Р.–Ѓ.– –Т–µ—А—В–µ–±—А–Њ–ї–Њ–≥–Є—П –≤ —В–µ—А–Љ–Є–љ–∞—Е, —Ж–Є—Д—А–∞—Е, —А–Є—Б—Г–љ–Ї–∞—Е – –°––Я—В–±.–2004 –≥.
5. Borenstein D. –≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—П, —Н—В–Є–Њ–ї–Њ–≥–Є—П, –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –њ–Њ—П—Б–љ–Є—З–љ–Њ–є –±–Њ–ї–Є. –Ь–µ–ґ–і.–Љ–µ–і.–ґ—Г—А–љ–∞–ї, 2000, вДЦ 35, —Б.36 –42












