Боль и ригидность наиболее присущи ревматоидному артриту (РА), анкилозирующему спондилиту (АС) и другим серонегативным спондилоартритам (ССА), а также дорсопатиям, включая миофасциальный синдром. У больных РА наблюдаются боли воспалительного типа, которые наиболее выражены в утренние часы, причем эти боли, как правило, сопровождаются утренней ригидностью. При этом заболевании интенсивность утренней скованности и ее продолжительность адекватно отображают активность воспалительного процесса и позволяют судить не только о выраженности лабораторной активности заболевания, но и об активности происходящих в тканях изменений. Выраженная ригидность, которая держится в течение многих месяцев и которая не уменьшается на фоне активной антивоспалительной терапии, является неблагоприятным прогностическим фактором и, как правило, ассоциируется с возможным прогрессированием структурных изменений в суставах. У больных РА причиной болей в суставах, как и ригидности, прежде всего является воспалительный процесс в синовиальной оболочке (синовит) и периартикулярных мягких тканях (теновагинит, теносиновит, бурсит).
Боль и ригидность имеют не меньшее значение и в полиморфной картине АС и других ССА. Известно, что боль воспалительного типа в позвоночнике (боль в ранние утренние часы на протяжении трех и более месяцев, не уменьшающаяся в покое и ослабевающая после двигательной нагрузки) входит в диагностические критерии АС. Динамика интенсивности боли является одним из показателей ответа на проводимую терапию и критерием ремиссии при этом заболевании (ASAS response criteria и ASAS remission criteria) [3]. Что же касается ригидности или скованности, то этот симптом, как и при РА, адекватно отображает активность воспалительного процесса при АС, причем в большей степени, чем такие лабораторные тесты, как СОЭ и уровень С–реактивного белка. Динамика выраженности и продолжительности утренней скованности позволяет судить об эффективности проводимой терапии. Для АС и других ССА это тем более важно, что при этой группе заболеваний наблюдается диссонанс клинических и лабораторных показателей активности заболевания и нередко выраженный воспалительный процесс может протекать с нормальными или субнормальными лабораторными показателями в течение длительного периода, а подчас и всего заболевания.
Ригидность (скованность) в дебюте АС преимущественно локализуется в поясничном отделе позвоночника и постепенно распространяется на вышележащие отделы осевого скелета. Она обычно более выражена в ранние утренние часы, но у некоторых больных с высокой активностью воспалительного процесса держится на протяжении всего дня. Интенсивность и длительность ригидности соответствует интенсивности болей в позвоночнике, подчеркивая их единый генез. Наличие воспалительного процесса в позвоночнике вызывает рефлекторное напряжение мышц спины, что, в свою очередь, приводит к изменению осанки и деформации позвоночника, при этом нивелируется физиологический лордоз в поясничном отделе позвоночника, подчеркивается кифоз в грудном и развивается гиперлордоз в шейном отделе. В далекозашедших случаях формируется характерная для больных АС поза «просителя» с положительным симптомом Форестье, высокими значениями теста Томайера и значительным нарушением функциональной способности позвоночника, причем ограничение подвижности и деформация позвоночника поддерживаются не только структурными изменениями в суставах и связках позвоночника, но и гипертонусом мышц спины.
Болевой синдром при АС обусловлен воспалительными изменениями в периферических, корневых, крестцово–подвздошных суставах и позвоночнике. Как известно, все структуры позвоночного столба, за исключением костной ткани, содержат нервные окончания и могут быть причиной появления боли [4]. Свободные нервные окончания, являющиеся болевыми рецепторами, имеются в капсулах межпозвонковых суставов, задней продольной и межостистой связках, периосте позвонков, сосудах паравертебральных мышц, фиброзном кольце межпозвоночных дисков. Боли при этом заболевании могут быть проявлением вертеброгенного корешкового синдрома (радикулопатия) или рефлекторных болевых синдромов. В основе радикулопатии лежит компрессия нервных корешков воспалительным отеком межпозвоночного канала или деформированным позвоночником. Возможны и другие причины развития дорсалгии, такие как спондилолистез, стеноз спинального канала, остеопороз, грыжи межпозвонковых дисков и реже – задние или передние остеофиты, вторичный артроз межпозвонковых (фасеточных) суставов, спондилез. Часто в основе болевого синдрома лежит несостоятельность структур, обеспечивающих вертикальное положение тела.
Все вышеописанные патологические процессы приводят к рефлекторным мышечно–тоническим синдромам, которые обусловлены раздражением рецепторов в ответ на изменения в дисках, связках и суставах позвоночника. Импульсы от рецепторов достигают двигательных нейронов спинного мозга, что приводит к повышению тонуса соответствующих мышц [5]. Спазмированные мышцы способствуют ограничению подвижности определенного сегмента позвоночника, а также становятся вторичным источником боли, который запускает порочный круг «боль – мышечный спазм – боль». Повторное возникновение таких изменений или их персистенция способствуют формированию миофасциального синдрома. Следует отметить, что в генезе развития контрактур и фиброза мышц также принимает участие гипертонус поперечно–полосатой мускулатуры. Некоторые авторы рассматривают повышение мышечного тонуса, как один из факторов риска этого заболевания и его неблагоприятного прогноза.
Боль и ригидность могут быть проявлением большой группы заболеваний, для которых характерны боли в нижней части спины (low back pain). Боль в нижней части спины определяется как боль, локализующаяся между XII парой ребер и ягодичными складками. Заболевания, сопровождающиеся болями в этой области, представляют собой чрезвычайно гетерогенную группу. Они объединены термином дорсопатии и включают в себя синдромы, сопровождающиеся болями в спине вертеброгенного и невертеброгенного генеза [5,6]. Среди вертеброгенных причин выделяют деформирующие дорсопатии, спондилопатии (спондилоартроз, анкилозирующий спондилоартрит), дорсалгии, нестабильность позвоночника с формированием спондилолистеза, а среди невертеброгенных – мышечно–фасциально–связочные боли, связанные с длительным перенапряжением мышц. При дегенеративных заболеваниях позвоночника основными патогенетическими факторами развития таких синдромов являются компрессионные механизмы и рефлекторные влияния с присоединением воспалительных нарушений, микроциркуляторных расстройств и их сочетаниями, а основными источниками ее болевой афферентации являются фиброзное кольцо, надкостница, связки позвоночника, межпозвонковые (фасеточные) суставы и мышцы. Особенность болевых синдромов в поясничном отделе позвоночника заключается в комбинации рефлекторных мышечно–тонических и миофасциальных синдромов с изменениями в эмоционально–личностной сфере [7].
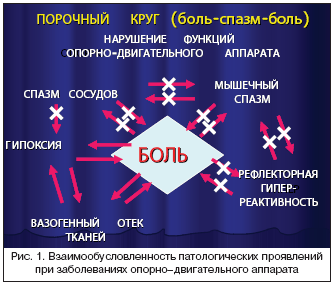
В формировании болевого синдрома в осевом скелете прослеживается определенная этапность развития. В самом начале имеет место повреждение фиброзного кольца, мышц, суставов и нервных стволов [4]. В ответ на это повреждение происходит выброс альгогенных соединений (например, гистамина, серотонина, простагландинов, брадикинина, субстанции Р), которые вызывают нарушение локальной микроциркуляции. Эти биологически активные вещества способствуют центральной и периферической сенситизации, т.е. повышению возбудимости ноцицепторов в фиброзном кольце диска, задней продольной связке, суставах позвоночника, корешках, ганглиях, паравертебральных мышцах и формированию вторичной гипералгезии поврежденной ткани. Наличие болей усиливает тонус мышц, приводит к спазму сосудов, гипоксии и вазоактивному отеку тканей, которые, в свою очередь, также вызывают боль, образуя порочный круг боль–спазм–боль (рис. 1). Весь каскад этих изменений способствует хронизации патологического процесса.
При многих ревматических заболеваниях формируется синдром спастичности, хотя и не в столь яркой форме, как это наблюдается в неврологической практике. Под спастичностью понимают двигательное расстройство, сопровождающееся повышением мышечного тонуса и обусловленное поражением кортико–спинального пути [7]. Синдром спастичности является проявлением заинтересованности верхних мотонейронов. К разнообразной симптоматике поражения этих мотонейронов, помимо ригидности мышц, относятся мышечная атрофия и развитие контрактур (табл. 1). Синдром спастичности способствует развитию остеопороза, повышает риск падений, делает неустойчивой походку, что еще более способствует остеопоротическим переломам костей.
Регуляция мышечного тонуса осуществляется под влиянием как центральной, так и периферической импульсации a–мотонейронов спинного мозга. Эти мотонейроны, расположенные в передних рогах спинного мозга, осуществляют иннервацию мышечных волокон [6]. В основе возникновения спастичности лежит нарушение тормозящих влияний супраспинальных отделов на спинальные двигательные и вставочные нейроны. Эти нарушения на спинальном уровне приводят к дисбалансу процессов возбуждения и торможения. В происхождении спастичности принимает участие не только дисфункция центральной и периферической нервной системы. Не меньшее значение в этом процессе имеет органическое и функциональное состояние поперечно–полосатой мускулатуры.
Для купирования повышенного мышечного тонуса или уменьшения его интенсивности чаще всего используются миорелаксанты. Их применение способствует не только существенному снижению гипертонуса, но и уменьшению выраженности болевого синдрома, предотвращению формирования контрактур, улучшению функциональной способности опорно–двигательного аппарата, облегчению возможности проведения широких реабилитационных мероприятий, сохранению трудоспособности пациента и его активности в повседневной жизни [8]. Миорелаксанты, уменьшая выраженность мышечного тонуса, приводят к увеличению амплитуды движений в позвоночнике и периферических суставах, что и делает их назначение целесообразным. К этой группе препаратов относятся тизанидин, толперизон, баклофен, диазепам, тетразепам и другие.
К основным требованиям, предъявляемым к миорелаксантам современной медицинской практикой, являются не только их высокая эффективность, но и селективность центрального миорелаксирующего действия, а также их безопасность. Идеальный миорелаксант должен снижать повышенную рефлекторную возбудимость без сопутствующего подавления тонической импульсации, а также иметь хорошую переносимость при длительном применении у больных пожилого возраста и детей, т.е. у тех контингентов, которые более других чувствительны к нежелательных эффектам лекарственных препаратов. Идеальный миорелаксант не должен оказывать отрицательного влияния на активность и трудоспособность пациента и хорошо сочетаться с другими лекарственными препаратами.
Толперизон является миорелаксантом центрального Н–холинолитического действия. Он оказывает избирательное угнетающее действие на каудальную часть ретикулярной формации ствола мозга и тем самым приводит к снижению миорелаксирующей активности. Этот препарат обладает мембраностабилизирующим действием. Он также блокирует спинномозговые моно– и полисинаптические рефлексы. Структура толперизона близка к структуре местных анестетиков, особенно лидокаина. Этим можно объяснить присущий ему анальгетический эффект. Кроме того, он обладает слабым спазмолитическим и сосудорасширяющим действием. Реализация лечебного эффекта этого препарата связана с редуцированием натриевого тока на мембране нервных волокон и клеток.
Баклофен также оказывает миорелаксирующее действие. Как и другие лекарственные препараты этой группы, баклофен обладает умеренной антиспастической и аналгезирующей активностью. Препарат является аналогом g–аминомасляной кислоты (ГАМК). Он связывается с пресинаптическими ГАМК–рецепторами, приводит к уменьшению выделения возбуждающих аминокислот (глутамата, аспартата) и подавляет моно– и полисинаптическую активность на спинальном уровне, что и вызывает снижение мышечного тонуса. Баклофен используется при лечении болезненных мышечных спазмов у пациентов с поражением структур спинного и головного мозга.
Особое место среди других миорелаксантов занимает производное имидазола – Сирдалуд (тизанидин) компании Novartis. Сирдалуд относится к миорелаксантам центрального действия и является специфическим агонистом α2–адренергических рецепторов. Основная мишень действия препарата – проводящие пути спинного мозга. Его терапевтический эффект связан с ингибицией высвобождения нейротрансмиттеров возбуждения из пресинаптических невральных окончаний [5]. Он снижает мышечный тонус за счет стимуляции моноаминергетических ядер ствола головного мозга, что, в свою очередь, приводит к торможению спинальных мотонейронов и, соответственно, к миорелаксации, купированию мышечно–тонических синдромов и спастичности. В то же время при его приеме не происходит уменьшения мышечной силы. Сирдалуд эффективен как при остром болезненном мышечном спазме, так и при хронической спастичности спинального и церебрального генеза. Он снижает сопротивление пассивным движениям, уменьшает выраженность спазма и клонических судорог, а также увеличивает силу произвольных сокращений скелетных мышц (табл. 2).
Помимо выраженного антиспастического действия, Сирдалуд обладает прямым аналгезирующим действием. Анальгетический эффект обусловлен не только непосредственным влиянием Сирдалуда на антиноцицептивную систему, но и опосредованным – за счет снижения патологически повышенного тонуса мышц. Он также усиливают аналгезирующее действие нестероидных противовоспалительных препаратов (НПВП). В известной степени его влияние на интенсивность боли усиливается его седативной активностью.
Сирдалуд быстро всасывается. Максимальная концентрация в плазме крови достигается примерно через 1 ч после приема препарата. Препарат быстро метаболизируется в печени. Период полувыведения Сирдалуда из системного кровотока в среднем составляет 2–4 ч. Препарат выделяется преимущественно почками (около 70% дозы) в виде метаболитов. Прием пищи не влияет на фармакокинетику тизанидина.
Основными показаниями для назначения Сирдалуда являются выраженная ригидность, болезненный мышечный спазм, миофасциальные синдромы и спастичность скелетных мышц [8–10]. При ревматических заболеваниях он применяется в небольших дозах. Начальная доза составляет 2 мг/сут. При выраженной утренней скованности целесообразно назначение дополнительно 2 мг на ночь. Для достижения максимального эффекта возможно увеличение дозы до 2–4 мг 3 раза в сутки. Лечебное действие Сирдалуда является дозозависимым, и при его назначении эффективность постепенно нарастает, достигая своего максимума уже в первые три дня от начала терапии. При остро возникших болевых синдромах препарат назначается на 5–7 дней. При наличии хронических болей, сопровождающихся спастичностью, длительность терапии Сирдалудом определяется индивидуально. При воспалительных заболеваниях суставов и позвоночника этот препарат обычно назначают одновременно с НПВП, а при миофасциальных синдромах с выраженным болевым синдромом его следует принимать в комбинации с анальгетиками.
Сирдалуд имеет солидную доказательную базу своей терапевтической активности. Многочисленными исследованиями установлено, что этот препарат снижает мышечный тонус, уменьшая лишь тонический его компонент. Это ведет к сохранению, а в ряде случаев и повышению мышечной силы, что выгодно отличает его от толперизона и баклофена, не обладающих этими свойствами. Благодаря такой особенности и отчетливому обезболивающему действию Сирдалуд повышает повседневную активность больных и улучшает качество их жизни.
Интересным представляется гастропротективное действие препарата, что связано с его адренергической активностью и спазмолитическим действием [11]. Такое свойство Сирдалуда имеет важное значение для ведения пациентов с хроническими заболеваниями суставов, которые принимают нестероидные НПВП на протяжении длительного периода, а некоторые из них – практически постоянно, а это, в свою очередь, нередко приводит к развитию эрозивного гастрита и язв желудка и/или 12–перстной кишки. Опубликованные экспериментальные данные дают основание считать, что Сирдалуд уменьшает частоту вызываемых НПВП желудочно–кишечных осложнений за счет уменьшения базальной и индуцированной секреции соляной кислоты, а также устранения дисбаланса гликопротеидов в слизистой оболочке желудка и желудочном секрете. Кроме того, этот препарат подавляет спонтанную моторику повздошной кишки и замедляет кишечный пассаж. Следует отметить, что антисекреторная активность Сирдалуда является характерным свойством всего класса агонистов α2–адренергических рецепторов.
Гастропротективная активность Сирдалуда доказана результатами многочисленных клинических исследований. Установлено, что Сирдалуд улучшает переносимость НПВП (в частности, диклофенака) и потенцирует их обезболивающее действие [12]. В многоцентровом двойном слепом плацебо–контролируемом исследовании с участием 405 больных с острыми локальными болевыми синдромами и клинически выраженными мышечными спазмами установлено, что комбинация Сирдалуд – диклофенак эффективнее комбинации плацебо – диклофенак. В течение 7 дней больные принимали Сирдалуд 4 мг/сут. и 50 мг диклофенака (основная группа) или плацебо и 50 мг диклофенака (контрольная группа). Частота желудочно–кишечных нежелательных явлений в основной группе составила 12%, в контрольной – 32%, а частота выявления скрытой крови – 5 и 11%, соответственно. Важно отметить, что при этом не потребовалось отмены лечения, и ни у одного больного не возникло серьезных нежелательных явлений [12].
Не только переносимость комбинации Сирдалуда с диклофенаком оказалась существенно лучше, чем плацебо с диклофенаком, но выше была и ее терапевтическая эффективность. По данным вышеприведенного исследования, очень хороший результат терапии отмечен у 40% больных контрольной группы и удовлетворительный – у 16%, а в группе сравнения – у 27 и 28% соответственно. Аналогичные данные были получены и в другой работе, где оценивались эффективность и переносимость комбинированной терапии диклофенака и Сирдалуда в 2–нед. контролируемом исследовании у больных с болями в нижней части спины [13]. В группе больных, которые получали комбинированную терапию, по сравнению с монотерапией диклофенаком наблюдалось более значимое уменьшение интенсивности боли и улучшение подвижности позвоночника. Показатели опросника Освестри, рекомендованные ВОЗ для оценки болей в спине, улучшились на 25%, а выраженность боли по визуальной аналоговой шкале (ВАШ) с 56 мм снизилась до 34. В этом же исследовании отмечена хорошая переносимость такой комбинации. По данным Berry H. et al., частота возникновения нежелательных явлений со стороны желудочно–кишечного тракта при применении комбинированной терапии ибупрофеном и Сирдалудом наблюдалась в 3 раза реже по сравнению с монотерапией ибупрофеном [14]. Складывается впечатление, что Сирдалуд является идеальным средством для сочетания с НПВП при лечении воспалительных и дегенеративных заболеваний суставов и позвоночника, т.к. обладает с ними синергизмом как в плане воздействия на болевой синдром, так и снижения гастроинтестинальной токсичности.
При наличии выраженного мышечного гипертонуса лечение миорелаксантами лучше комбинировать с приемом анальгетических средств. Такая комбинированная терапия имеет патогенетическое обоснование. Как известно, мышечное напряжение является защитной реакцией на боль, а боль, в свою очередь, является эмоциональным стрессом и ведет к повышению тонуса мышц, определяющих защитную реакцию. Мышечный спазм и боль, как уже указывалось выше, способствуют спазму сосудов, гипоксии и вазогенному отеку тканей. Купирование рефлекторного напряжения мышц приводит к улучшению кровоснабжения тканей, что способствует нормализации метаболических расстройств.
Сирдалуд обладает удовлетворительной переносимостью и высокой безопасностью, включая больных пожилого возраста. Как при краткосрочном, так и длительном применении малых доз препарата, которые обычно применяются в ревматологии, нежелательные явления возникают редко и купируются при отмене препарата [15]. Помимо сонливости, заторможенности и снижения концентрации внимания, могут наблюдаться головокружение, сухость во рту, повышенная утомляемость, тошнота, явления кишечной диспепсии. Возможно преходящее повышение активности печеночных трансаминаз, брадикардия, умеренное снижение артериального давления, тем более что препарат способен потенцировать гипотензивные препараты. Следует иметь в виду, что прекращение терапии Сирдалудом должно проходить постепенно, так как внезапная отмена может сопровождаться кратковременным повышением мышечного тонуса, что наблюдается и при быстрой отмене других миорелаксантов. Больным, у которых отмечают сонливость при приеме Сирдалуда, в начале лечения необходимо избегать всех видов деятельности, требующих повышенной концентрации внимания и быстроты реакции
Таким образом, симптом–модифицирующая терапия болевого синдрома и ригидности при воспалительных и дегенеративных заболеваниях суставов и позвоночника должна быть комплексной и направлена как на уменьшение интенсивности болей или полное их устранение, так и на ликвидацию ригидности. Исходя из этих позиций целесообразно проводить комбинированную терапию НПВП и миорелаксантами. Хотя симптом–модифицирующая терапия не замедляет темпы рентгенологического прогрессирования заболевания, назначение НПВП и миорелаксантов существенно улучшает качество жизни, предотвращает развитие атрофии мышц и сгибательных контрактур, а также способствует сохранению функциональной способности опорно–двигательного аппарата. Влияние Сирдалуда на различные патогенетические звенья заболевания и широкий профиль биологических эффектов позволяют использовать этот препарат как в качестве монотерапии, так и в комбинации с другими обезболивающими и антивоспалительными препаратами.


Литература
1. See S., Ginzburg R. Skeletal muscle relaxants. Pharmacotherapy 2008; 28: 207–213.
2. Coward D.M. Tizanidine: Neuropharmacology and mechanism of action. Neurology 1994; 44 (Suppl. 9): 6–11.
3. Dougados M., Dijrmans B., Khan M. et al. Сonventional treatments for ankylosing spondylitis. Ann Rheum Dis 2002; 61(Suppl. III): 40–50.
4. Алексеев В.В. Диагностика и лечение болей в спине. Соnsilium medicus 2002; 4 (2): 96–102.
5. Сhen D–F., Bianchetti M., Weisendanger M. Motor Disturbances. Ed. R.Benecke et al. London, 1987.
6. Шостак Н.А. Роль миорелаксантов при ревматических заболеваниях. РМЖ 2005; 13 (8): 557–559.
7. Korthlas–de Bos I, van Tulder M. Econonic evaluation and randomized trials in spinal disorders: principles and methods. Spine 2004; 29: 442–448.
8. Дамулин И.В. Синдром спастичности и основные направления его лечения. Журнал неврологии и психиатрии 2003; 12: 4–9.
9. Derry H, Hutchinson DR. A multicentral placebo–controlled study in general practice to evaluate the efficacy and safety of tizanidine acute low–back pain. J Intern Med Res 1988; 16: 75–82.
10. Malanga G, Reiter R, Garay E. Update on tizanidine for muscle spasticity and emerging indications. Expert Opinion 2008; 9: 2209 –2214.
11. Emre M. The gastroprotective effects of tizanidine: an overview. Curr Therapeutic Res 1998; 59 (1): 2–12.
12. Sirdalud Ternilin Asia–Pacific Study group. Efficacy and gastroprotective effects of tizanidine plus diclofenac versus placebo plus diclofenac in patients with painful muscle spasm. Curr Ther Res 1998; 59: 13–22.
13. Coward DM. Tizanidine: Neuropharmacology and mechanism of action. Neurology 1994; 44, 11 (Suppl. 9): 6–11.
14. Berry H, Hutchinson D.R. Tizanidine and ibuprofen in acute low–back pain: results of a double–blind multicentre study in general practice. J Int Med Res, 1988; 16: 83–91.
15. Парфенов В.А., Яхно Н.Н. Неврология в общемедицинской практике. М., 2001.












