ГКБ № 2, Владивосток
Заболевания предстательной железы являются самыми распространенными среди урологических страданий пациентов пожилого возраста, что вызвано развитием доброкачественной гиперплазии (ДГПЖ), рака предстательной железы, хронического простатита. Гистологические признаки ДГПЖ отмечаются у 50% мужчин в возрасте 60 лет и в 90% случаев к 80 годам. Смертность от ДГПЖ наступает главным образом от уремии, сепсиса и осложнений хирургических вмешательств [Л.М. Гориловский, 1999].
В России и США рак предстательной железы занимает второе место по уровню смертности после рака легких и второе по скорости прироста после меланомы кожи, общее 4–е место среди всех причин смерти мужчин [Б.П. Матвеев, 1999, Д.Ю. Пушкарь, 2002]. Среди онкоурологических заболеваний в России с 1992 г. по 1998 г. наиболее высокие темпы прироста отмечались для рака предстательной железы (43%), почки (36,6%) [Б.П. Матвеев с соавт., 2001].
Заболеваемость РПЖ в Российской Федерации в 2001 году составила 14,1 на 100000 мужского населения. В Приморском крае за последние десять лет заболеваемость РПЖ увеличилась с 5,4 до 12,4 на 100000 мужского населения (1992–2002 гг.). В 1992 г. по краю диагностировано 58 заболеваний простаты, а в 2002 г. число впервые взятых на учет составило 132 человека.
Многие авторы считают, что при локализованном РПЖ 88% больных могут прожить более 5 лет, но метастазирование снижает эту величину в 3 раза (до 29%). Однако при ранней диагностике и адекватной терапии прогноз бывает благоприятным [Coffey D.S., 1993, Epstein J.I., Carmichael V.J., 1993].
В связи с отсутствием патогномоничных симптомов ранних стадий рака простаты диагностика является одной из самых сложных проблем современной онкоурологии. Основная трудность: дифференциальная диагностика рака предстательной железы с доброкачественной гиперплазией, склерозом, туберкулезом, абсцессом простаты, простатитом – заболеваниями, сопровождающимися расстройствами мочеиспускания (учащенное, затрудненное, болезненное мочеиспускание вялой струей мочи, задержка начала мочеиспускания, чувство неполного опорожнения мочевого пузыря). Велик удельный вес сочетания рака простаты с доброкачественной гиперплазией предстательной железы (ДГПЖ) и хроническим простатитом, что снижает чувствительность, специфичность и точность таких известных методов обследования, как ПСА, пальцевое ректальное обследование простаты (ПРО), УЗИ и/или ТРУЗИ, биопсии простаты.
Для хронического простатита болевой синдром как клинический симптомокомплекс характерен для большинства пациентов (до 90%), нарушения мочеиспускания – до 36,6% случаев, при УЗИ выявляется неровность контуров, гетерогенность структуры предстательной железы, по данным пальцевого ректального обследования имеется пастозность, болезненность, часто неоднородность консистенции простаты различной степени выраженности.
Известно, что степень выраженности симптомов расстройства мочеиспускания может зависеть не столько от размеров гиперплазированной ткани, сколько от конфигурации узлов и направления их роста. При пролиферации ткани простаты в сторону прямой кишки симптомы нарушенного мочеиспускания могут долго не беспокоить больного. При росте узлового образования в просвет шейки мочевого пузыря, формировании «средней доли» и/или в просвет простатического отдела уретры заболевание очень скоро проявляется характерными симптомами нарушения акта мочеиспускания.
За последние несколько лет, с внедрением эндоскопической аппаратуры, ТУР, биопсии простаты, онкомаркера рака простаты – ПСА, качественно изменились диагностика и тактика лечения больных с заболеваниями простаты. Однако недооценка клинических симптомов, недообследование или неадекватная интерпретация результатов обследования иногда приводят к нерациональному, неоправданному хирургическому лечению, длительной реабилитации, обнаружению злокачественного заболевания при гистологическом исследовании после операции.
Нами проведен анализ обследования и хирургического лечения больных с раком предстательной железы, получавших лечение с 1990 по 2001 г. в 1 урологическом отделении ГКБ № 2 города Владивостока. Распределение больных с РПЖ по годам представлено в таблице 1.

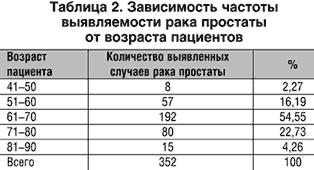
По возрастному составу среди больных раком предстательной железы преобладали лица старше 60 лет. Средний возраст заболевших мужчин составил 66,7 лет. Минимальное количество больных выявлено в возрасте от 40 до 50 лет, максимальное количество в возрасте от 60 до 70 лет, что составляет более половины всех больных. После 70 лет роста обращаемости и выявления заболевания мы не выявили (табл. 2). Причины данной возрастной зависимости требуют дальнейшего изучения.
Всем больным проводился тщательный сбор анамнеза, жалоб, пальцевое ректальное исследование простаты, УЗИ и/или ТРУЗИ. Оценку клинических симптомов проводили по Международной шкале простатических симптомов IPSS (0–35) согласно рекомендациям Консультативного комитета ВОЗ по ДГПЖ. У всех больных этот показатель был выше 22 баллов.
Подозрением на РПЖ считали симптомы расстройства мочеиспускания, пальпаторно–диффузное либо локальное уплотнение железы, ассиметрию долей, наличие бугристых, узловых, хрящевидных до деревянистой плотности образований. Диагностическими ультразвуковыми критериями подозрения на рак простаты считали наличие гипоэхогенных фокусов с неровными контурами в периферической части железы, неровность, нечеткость капсулы простаты, неоднородное расширение семенных пузырьков.
При необходимости дообследования, уточнения диагноза, стадии заболевания больным выполнялось рентгенологическое исследование ОГП, костей таза, позвоночника, компьютерная томография, уродинамические исследования. Пункционная биопсия простаты, как уточняющий этап диагностики, выполнена 12 больным.
Клиническими проявлениями в 87 (24,7%) случаях была острая задержка мочи (ОЗМ). Среди больных, которые мочились самостоятельно, у 260 (74%) наблюдалась поллакиурия; затрудненное, болезненное мочеиспускание вялой струей отмечали 105 (29,8%) пациентов; хроническая задержка мочи имелась у 109 (31%) пациентов; макрогематурию отмечали 14 человек (3,9%). Обострение хронического пиелонефрита подлежало лечению у 147 (42%) больных, из которых у 12 (3,6%) имелась ХПН 2–3 ст. Гидронефроз одно– или двухсторонний диагностирован в 27 (7,6%) случаях.
Стадия Т3–Т4 выявлена в 73,2 % случаев, хотя среди оперированных только у 6 (3,1%) человек рентгенологически или гистологически подтверждены метастазы в кости таза, позвоночник, легкие, яички.
Среди сопутствующей патологии наиболее часто имелись ИБС, атеросклеротический кардиосклероз, артериальная гипертензия, заболевания органов дыхания с дыхательной недостаточностью.
До 1998 года важная роль в ранней диагностике РПЖ отводилась пальцевому ректальному исследованию простаты (ПРИ), исследованию кислой фосфатазы крови. Однако повышенное содержание кислой фосфатазы, имеющееся в основном при метастазах в кости, для ранней диагностики заболевания непригодно. Ранняя диагностика с помощью ПРИ в значительной мере зависит от квалификации врача и позволяет установить правильный диагноз рака простаты в 30% случаев.
С внедрением и широким использованием онкомаркера РПЖ – простатического специфического антигена выявляемость злокачественных образований простаты увеличилась вдвое, с помощью ПСА можно оценивать течение заболевания и эффективность лечения. Среди больных, которым определялось ПСА, повышение уровня имелось в 87% случаев.
В отделении выполнялась ТУР простаты с последующей биопсией у 135 человек (38,3%), цистостомия с биопсией в 26 случаях (7,3%). Хирургическая кастрация, как этап МАБ, или в виде монотерапии, если другие методы были неприемлемы, выполнена 15 больным (4,2%). С предоперационным диагнозом ДГПЖ 30 больным (8,5%) выполнена одномоментная чреспузырная аденомэктомия или частичная простатэктомия с послеоперационным гистологическим заключением – рак простаты. У этой группы больных имелось сочетание трех компонентов: гиперплазия простаты (V > 60 см3), нарушение мочеиспускания и инфравезикулярная обструкция. При этом имелись отрицательные данные ПРИ и УЗИ (ТРУЗИ), незначительное или умеренное повышение ПСА (до 20 нг/мл).
Группе больных выполнялись операции – визуальная лазерная аблация простаты, лазерная уретротомия простатического отдела уретры, ревизия мочевого пузыря с дилатацией шейки мочевого пузыря, биопсией, цистостомией, наложение пункционных нефростом, контактная литотрипсия камней мочевого пузыря.
Послеоперационная смертность составила 2,7% (7 человек). Гистологически рак простаты подтвержден у 198 (74,4%) человек. Для дальнейшего специального лечения и наблюдения все больные направлялись к онкоурологу.
Заключение
1. До настоящего времени причинами распространенности РПЖ и запущенности больных чаще всего являются недообследование либо запоздалое обращение к врачам, скрытое течение болезни, низкая культура населения, несовершенство диспансеризации.
2. Поиск оптимального алгоритма, четких критериев ранней диагностики рака простаты остается актуальным. На современном этапе диагностика ранних стадий РПЖ основана на своевременной диагностике и правильной интерпретации узловых образований простаты, сопровождающихся симптомами расстройства мочеиспускания у мужчин старше 40 лет. Диагностика должна быть основана на последовательном применении ПСА, пальцевого ректального исследования простаты, УЗИ и/или ТРУЗИ. Недопустимо один метод заменять другим.
По–прежнему высока значимость пальпации простаты и ТРУЗИ при нормальном содержании ПСА или при уровне содержания, находящемся в пределах так называемой «серой зоны» (4–10 нг/мл).
3. Необходимо шире пользоваться уточняющим этапом диагностики – полифокальной биопсией простаты с последующим морфологическим исследованием биоптатов.
Биопсию предстательной железы необходимо выполнять при соответствующих показаниях. Биопсия должна быть доступной, при наличии современного оборудования и квалифицированных кадров.
4. Возраст является грозным фактором риска для возникновения РПЖ.
Более половины больных (54,5%), которые обратились за помощью и нуждались в диагностике, лечении и/или хирургическом пособии в рамках урологического отделения за 10 лет, были в возрасте 60 лет и старше.
5. Перспектива раннего выявления РПЖ, своевременного лечения и как результат – улучшение качества жизни пациентов и снижение смертности от рака простаты, совершенно очевидно, связаны с созданием эффективной системы диспансеризации лиц старшего возраста, формированием групп повышенного онкологического риска, внедрением элементов скрининга среди здорового населения, а также развертыванием целенаправленной санитарно–просветительной работы.












