Нейрогенные нарушения мочеиспускания являются типичным проявлением большинства неврологических заболеваний и наблюдаются у 10–90% больных в зависимости от характера и распространенности поражения нервной системы [1,3,7,10,15]. Эти расстройства носят функциональный характер и являются отражением процессов, происходящих в нервной системе (преимущественно в ее центральном отделе). Для каждого конкретного неврологического заболевания характерны индивидуальные симптомокомплексы и отличительные патогенетические механизмы, их формирующие [6]. Причины формирования стойких патологических рефлексов мочеиспускания заключаются в поражении центров мочеиспускания (ишемический инсульт, опухоли головного и спинного мозга), нарушении проведения нервных импульсов от рецепторов мочевого пузыря и уретры к корковым, подкорковым, стволовым или спинальным центрам мочеиспускания (рассеянный склероз, субкортикальная артериосклеротическая энцефалопатия), дегенеративных изменениях нервной системы и дисбалансе нейромедиаторов (болезнь Паркинсона, мультисистемная атрофия) [11,13,16].
Нейрогенные расстройства мочеиспускания могут быть первыми проявлениями заболевания (дисциркуляторная энцефалопатия) или присоединяться на поздних стадиях болезни (болезнь Паркинсона, болезнь Альцгеймера). В некоторых случаях симптомы нижних мочевых путей (СНМП) развиваются в первые сутки заболевания и постепенно регрессируют (ишемический инсульт, синдром Гийена–Барре), в других – указывают на обострение основного заболевания (рассеянный склероз ремиттирующего течения) [19].
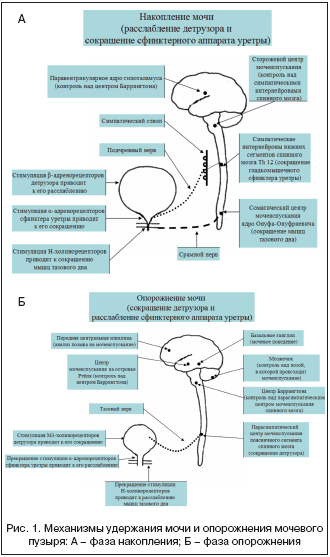
Прогноз дальнейшего развития дисфункций мочевого пузыря, как правило, зависит от течения основного неврологического заболевания и в большинстве случаев неблагоприятный. Исключением можно считать постинсультные нарушения мочеиспускания при возобновлении нормального его ритма в течение восстановительного периода, что обусловлено реорганизацией центров мочеиспускания, и синдром Гийена–Барре при успешной ремиелинизации периферических нервных волокон (рис. 1). Нарастание симптоматики мочепузырных дисфункций возможно даже при уменьшении неврологического дефицита на фоне лечения основного заболевания (например, неполная ремиссия рассеянного склероза).
Эти и некоторые другие особенности течения нейрогенных расстройств мочеиспускания могут вводить в заблуждение даже опытных клиницистов, приводя к неоправданным оперативным вмешательствам (гиперактивный мочевой пузырь при наличии бессимптомной доброкачественной гиперплазии простаты), лечению «простатита» у молодых пациентов, страдающих рассеянным склерозом, и т.д.
В этой связи необходимо отметить, что только раннее выявление симптомов нарушения мочеиспускания, а также их своевременная фармакологическая коррекция позволяют восстановить нарастающий дефицит функций нижних мочевых путей (НМП).
Диагностика нейрогенных
нарушений мочеиспускания
Диагностические мероприятия, связанные с ранним выявлением нейрогенных нарушений мочеиспускания, сводятся к следующим:
• определение симптомов нарушения мочеиспускания (качественная и количественная оценка);
• установление четкой связи урологических симптомов с неврологическим заболеванием (временные факторы, сравнение клинических проявлений с данными параклинических исследований);
• выявление причины нарушения НМП (демиелинизация, ишемия, нейродегенерация);
• определение формы нарушения мочеиспускания (уродинамические исследования);
• определение функциональных и нейромедиаторных особенностей расстройства мочеиспускания (соматосенсорные вызванные потенциалы, методы нейровизуализации и фармако–аналитические исследования).
Определение симптомов нарушения мочеиспускания (качественная и количественная оценка). Для оценки степени характера и степени выраженности симптомов используют специально разработанные шкалы IPSS, LISS, Medsen–Iversen, Боярского и другие [4,14]. Данные шкалы, выявляющие ирритативные и обструктивные СНМП, были разработаны для урологических больных и, несмотря на их информативность, не до конца отвечают требованиям диагностики нейрогенных нарушений мочеиспускания. В случае нейрогенных нарушений мочеиспускания целесообразнее разделять симптомы нарушения чувствительной и двигательной сферы мочевого пузыря и уретры, дизритмические и поведенческие симптомы, а также связанные с положением тела больного (например, в случае нарушения ходьбы или постельного режима, когда больной вынужден мочиться лежа). Ниже приводим список основных симптомов, выявляемых у неврологических больных.
Симптомы нижних мочевых путей:
Ритм мочеиспускания:
□ норма (5–8), □ поллакиурия до____раз,
□ ноктурия до____раз.
Симптомы нарушения чувствительности:
□ позыв на мочеиспускание сохранен,
□ интенсивность позыва на мочеиспускание снижена,
□ позыв на мочеиспускание отсутствует,
□ позыв на мочеиспускание носит императивный характер,
□ позыв на мочеиспускание сопровождается болью (от 1 до 10 баллов)_____,
□ позыв на мочеиспускание ощущается как давление внизу живота,
□ позыв на мочеиспускание ощущается как распирание внизу живота,
□ ощущение неполного опорожнения мочевого пузыря при наличии остаточной мочи,
□ ощущение неполного опорожнения мочевого пузыря при отсутствии остаточной мочи.
Симптомы нарушения сократительной активности детрузора:
□ удовлетворительная струя мочи,
□ вялая струя мочи,
□ императивное недержание мочи,
□ необходимость натуживания для инициации мочеиспускания,
□ необходимость натуживания для продолжения мочеиспускания,
□ необходимость натуживания для окончания мочеиспускания.
Симптомы нарушения сократительной активности гладкого сфинктера уретры:
□ невозможность самостоятельного мочеиспускания при наличии позыва на мочеиспускание,
□ прерывистое мочеиспускание, как правило, одинаковыми порциями,
□ отсроченное начало мочеиспускания.
Симптомы нарушения сократительной активности мышц тазового дна:
□ необходимость расслабления мышц тазового дна (промежности) для инициации мочеиспускания,
□ необходимость напряжения мышц тазового дна (промежности) для окончания мочеиспускания.
Поведенческие симптомы:
□ невозможность мочеиспускания в присутствии посторонних (в т.ч. медперсонала),
□ ограничение питьевого режима,
□ использование гигиенических средств (прокладок ______ шт./сут., памперсов),
□ контрольные мочеиспускания «на дорожку».
Симптомы НМП, связанные с положением тела больного (в пространстве):
□ невозможность точного попадания струи мочи в унитаз (для мужчин),
□ невозможность мочеиспускания в положении лежа,
□ невозможность мочеиспускания в положении стоя.
Установление четкой связи урологических симптомов с неврологическим заболеванием (временные факторы, сравнение клинических проявлений с данными параклинических исследований).
Для установления нейрогенной природы расстройства мочеиспускания необходимо несколько условий:
• наличие верифицированного неврологического заболевания;
• исключение психогенного расстройства мочеиспускания;
• соотношение во времени появления СНМП с двигательными, когнитивными, зрительными и др. неврологическими симптомами (табл. 1).
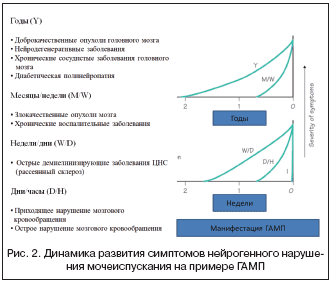
Анализ динамических показателей развития СНМП позволяет сопоставить их с основными неврологическими проявлениями болезни. Подобные сопоставления позволяют клиницисту выявить закономерность в развитии этих симптомов: например, постепенное развитие когнитивного дефицита и лобной апраксии ходьбы и переход поллакиурии в императивное недержание мочи при субкортикальной артериосклеротической энцефалопатии. Другим (обратным) примером может служить уменьшение проявлений гиперактивного мочевого пузыря (ГАМП) у больных, перенесших ишемический инсульт, в резидуальный период по сравнению с ранним восстановительным. На рисунке 2 графически изображены динамические показатели развития нейрогенных расстройств мочеиспускания при различных заболеваниях нервной системы на примере синдрома ГАМП.
Определение формы нарушения мочеиспускания. На следующем диагностическом этапе с помощью специальной уродинамической аппаратуры определяют форму нарушения мочеиспускания.
Сведения, полученные в ходе уродинамического исследования, помогают правильно оценить нарушения акта мочеиспускания, установить точный диагноз, определить показания и тактику лечения, обеспечив высокую степень успеха.
Уродинамические методы являются сложными с технической точки зрения и инвазивными с медицинской (опасность ятрогенного инфицирования НМП), поэтому вопрос о целесообразности их обязательного проведения дискутируется [2,5,8,9].
Урофлоуметрия – неинвазивный метод, позволяющий определить среднюю и максимальную скорость мочеиспускания (мл/сек.), степень инфравезикальной обструкции. Минусами метода является отсутствие информации о тонусе детрузора и уретры. Кроме того, для проведения исследования необходим объем мочеиспускания 200–300 мл, что невозможно у больных с ГАМП.
Цистометрия – малоинвазивный метод, позволяющий определить тонус детрузора в различные фазы наполнения мочевого пузыря по уродинамическому катетеру. Метод выявляет непроизвольные сокращения детрузора, но не позволяет оценить функциональное состояние уретры.
Профилометрия – метод, при использовании которого можно определить функциональное состояние замыкательного аппарата уретры в норме и при повышении абдоминального давления, достоверно диагностировать стрессовое недержание мочи и нестабильность уретры.
Комплексное уродинамическое исследование является наиболее информативным уродинамическим методом, позволяющим оценить сократительную активность детрузора (фаза наполнения – цистометрия, фаза опорожнения – «давление – поток») и сфинктерного аппарата уретры (урофлоуметрия + электромиография (ЭМГ) тазового дна).
При проведении комплексного исследования определяются 7 форм нарушения мочеиспускания:
1. Нейрогенная детрузорная гиперактивность (НДГ) характеризуется наличием непроизвольных сокращений детрузора, проявляющимся повышением детрузорного давления при цистометрии. Это моторная форма клинически характеризуется наличием ирритативной симптоматики, в том числе императивного недержания мочи. Наиболее часто НДГ встречается при поражении паравентрикулярных областей головного мозга и Варолиевого моста (инсульт, рассеянный склероз, болезнь Паркинсона).
2. Нейрогенная детрузорная гиперактивность в сочетании со сниженной сократительной способностью детрузора характеризуется наличием непроизвольных сокращений детрузора, сопровождающихся колебанием детрузорного давления более 5 см вод. ст., регистрируемых как в первой, так и во второй фазах наполнения в ходе цистометрии. Однако несмотря на выраженный позыв к акту мочеиспускания, в момент непроизвольного сокращения детрузора при мочеиспускании отмечалось снижение максимальной и средней скорости потока мочи за счет уменьшения сократительной способности детрузора. Клинически проявляется смешанной симптоматикой. Эта форма встречается при рассеянном склерозе и, по–видимому, связана с дискоординацией стволовых и подкорковых центров мочеиспускания.
3. Нарушение сократительной способности детрузора характеризуется отсутствием повышения внутрипузырного давления при наполнении мочевого пузыря и снижением или отсутствием позыва на мочеиспускание. При мочеиспускании отмечается повышение внутрипузырного давления, в основном за счет повышения абдоминального давления. У больных с данной формой наиболее часто встречалась остаточная моча, выявляемая при УЗИ. Клинически проявляется обструктивными симптомами. Наиболее часто этот вид расстройства мочеиспускания отмечается у больных с височной и стволовой локализацией инсульта и при поражении поясничных и крестцовых сегментов спинного мозга, реже – при полинейропатиях (синдром Гийена– Барре, сахарный диабет).
4. Детрузорно–сфинктерная диссинергия (ДСД) характеризуется наличием непроизвольных сокращений детрузора при цистометрии. Непроизвольные сокращения детрузора регистрируются во все фазы наполнения мочевого пузыря как повышение детрузорного давления выше 5 см вод. ст. и в ряде случаев приводят к непроизвольным утечкам мочи. В то же время мочеиспускание из–за непроизвольных сокращений мышц тазового дна, регистрируемых на ЭМГ, отличается прерывистым характером. Наряду с ирритативными симптомами у больных с ДСД отмечаются симптомы обструкции (ощущение неполного опорожнения мочевого пузыря после мочеиспускания, прерывистое мочеиспускание, отсроченное начало мочеиспускания). Эта форма наиболее часто встречается при рассеянном склерозе, спинальном инсульте и поперечном миелите при наличии очагов поражения спинного мозга на уровне шейных и грудных сегментов.
5. Нарушение произвольного расслабления поперечно–полосатого сфинктера уретры (псевдодиссинергия) характеризуется равномерным повышением внутрипузырного давления в ходе цистометрии и достаточной цистометрической емкостью. Во время мочеиспускания у этих больных не отмечается «угасания» ЭМГ – активности мышц тазового дна, что, по всей видимости, является причиной снижения максимальной скорости потока мочи. Клинически проявляется отсроченным началом мочеиспускания. Наиболее часто встречается при нарушении стволово–мозжечковых связей (рассеянный склероз, болезнь Паркинсона, дисциркуляторная энцефалопатия) [12].
6. Гиперактивный мочевой пузырь без детрузорной гиперактивности характеризуется отсутствием непроизвольных сокращений детрузора при цистометрии в сочетании с уменьшением цистометрической емкости. Эта гиперсенсорная форма клинически сходна с НДГ и встречается при поражении лобных центров или нарушении проводящих путей, идущих от лобной доли (рассеянный склероз, инсульт, дисциркуляторная энцефалопатия), реже – при поражении периферических нервов (сахарный диабет).
7. Стрессовое недержание мочи выявляется в ходе профилометрии и характеризуется наличием утечек мочи при кашле, что регистрируется недостаточным смыканием шейки мочевого пузыря и внутреннего сфинктера уретры. Данная форма характерна для нейродегенеративных и ишемических процессов, происходящих в стволе мозга (синдром Шай–Драйжера, вертебрально–базилярная недостаточность).
Заболевания нервной системы отличаются не только по клиническим признакам нарушения мочеиспускания, но и по уродинамическим показателям.
Определение функциональных
и нейромедиаторных особенностей расстройства мочеиспускания
Вызванные потенциалы. Вызванные потенциалы различных модальностей могут косвенно подтвердить нейрогенную причину расстройств мочеиспускания. Зоны головного мозга, соответствующие 3–му и 4–му пикам акустических стволовых вызванных потенциалов, пролегают в непосредственной близости от центра Баррингтона. Признаки ишемического и демиелинизирующего поражения ствола мозга (снижение амплитуды импульсов и удлинение межпикового интервала) могут в ряде случаев объяснить возникновение позыва на мочеиспускание, вызванное шумом падающей воды (болезнь Паркинсона, дисциркуляторная энцефалопатия).
Соматосенсорные вызванные потенциалы со срамного нерва позволяют объективно оценить различные параметры чувствительности половых органов, выявить ассиметрию в проведении импульсов (постинсультную), определить локализацию (периферическую, спинальную или центральную) и демиелинизирующий или ишемический характер поражения нервных проводников мочевых путей. Таким образом, метод ССВП при стимуляции n. pudendus вносит существенный вклад в объяснение механизмов формирования нарушения мочевой (и половой) функций при различных неврологических заболеваниях.
Методы нейровизуализации (КТ и МРТ). Как уже неоднократно отмечалось, ведущая роль в функционировании НМП как в физиологических, так и патологических условиях принадлежит различным структурам головного и спинного мозга. Одни из них выполняют роль, исключительно связанную с регуляцией мочеиспускания (ядро Баррингтона, сторожевой центр мочеиспускания, ядро Онуфа–Онуфровича), другие отвечают за различные процессы организма, не связанные напрямую с мочеиспусканием (паравентрикулярное ядро гипоталамуса, островок Рейля, зрительные бугры). Однако повреждение последних также часто сопровождается СНМП, различных по характеру и степени выраженности.
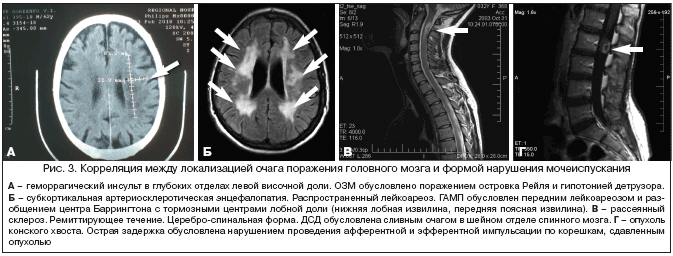
Оценку сохранности функционально значимых зон головного и спинного мозга осуществляют при проведении магнитно–резонансной томографии (МРТ), компьютерной томографии (КТ). Сравнение характера и степени выраженности СНМП у больных, перенесших ишемический инсульт, с локализацией патологического процесса позволяет предположить патогенетические механизмы симптомов, а также объяснить различия в динамическом развитии (или регрессе) этих проявлений в остром, восстановительном (раннем и позднем) и резидуальном периодах инсульта. Полученные результаты позволят сделать предположение о пластичности отдельных структур, регулирующих мочеиспускание, а следовательно, и прогнозировать течение «урологических» осложнений инсульта и некоторых других заболеваний ЦНС. В качестве примера приводим несколько томограмм с кратким описанием клинической картины (рис. 3).
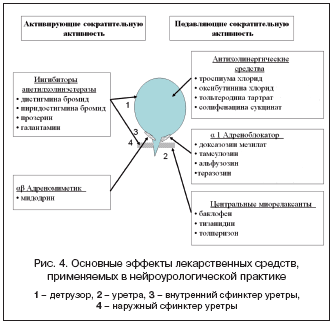
Фармакологический анализ. Определив форму нарушения мочеиспускания и установив связь с заболеванием нервной системы, т.е. установив диагноз «нейрогенный мочевой пузырь», клиницист назначает специфическое лечение. В практике нейроуролога используются лекарственные средства, влияющие преимущественно на холинергические, адренергические и, значительно реже, на другие нейромедиаторные системы. На рисунке 4 представлены основные точки приложения действия современных лекарств, применяемых для лечения нейрогенных расстройств мочеиспускания [17,18,20].
Анализ результатов лечения является заключительным диагностическим этапом. Например, применение специфического периферического конкурентного антагониста мускариновых рецепторов 2–го и 3–го подтипов троспиума хлорида уменьшает степень выраженности симптомов ГАМП при болезни Паркинсона, одновременно купируя сиалорею и спастический запор, что указывает на то, что ведущим механизмом этих трех, на первый взгляд, независимых симптомов болезни Паркинсона является парасимпатикотония, развивающаяся, как правило, к 5–7 году от начала заболевания.
Заключение
Нейрогенные расстройства мочеиспускания являются характерным и распространенным проявлением большинства заболеваний нервной системы. Использование уродинамических исследований позволяет выделить до 7 самостоятельных форм расстройств мочеиспускания, требующих индивидуального подхода к лечению. Диагностика нейрогенных нарушений мочеиспускания основывается на сравнении результатов клинических (вопросники и дневник мочеиспусканий) и параклинических (нейрофизиологических, уродинамических и нейровизуализационных) методов, а также на анализе результатов лечения, что позволяет на основании полученных данных оценить тяжесть неврологического заболевания и осуществить прогноз его дальнейшего развития.

Литература
1. Аль–Шукри С.Х., Кузьмин И.В. Гиперактивность детрузора и ургентное недержание мочи. Пособие для врачей. — СПб.:, 1999. — 48 с.
2. Борисов В.В. Лучевые и уродинамические методы функциональной диагностики в урологической практике: Дисс.. доктора мед. наук. – М., 1999.
3. Гусев Е.И., Демина Т.Л., Бойко А.Н. Рассеянный склероз. — М.: Нефть и газ, 1997. — 463 с.
4. Доброкачественная гиперплазия предстательной железы / Под редак. Лопаткина Н.А. — М., 1999. — 216 с.
5. Захматов Ю.М. Изменения уродинамики и их роль при экстра– и интравезикальных заболеваниях: Автореф. дис. …канд. мед. наук. — М., 1978. — 22 с.
6. Мазо Е.Б., Кривобородов Г.Г., Школьников М.Е. Нейрогенный гиперактивный мочевой пузырь / Трудный пациент. – 2004. – № 6. – С. 1–7.
7. Нейрогенные дисфункции мочевого пузыря. Под ред. Джавад–заде М.Д., Державина В.М. — М.: Медицина, 1989. — 384 с.
8. Осипов И.Б., Смирнова Л.П. Нейрогенный мочевой пузырь у детей. — СПб.: Питер, 2001. — 79 с.
9. Пушкарь Д.Ю. Гиперактивный мочевой пузырь у женщин. — М.: МЕДпресс–информ, 2003. — 159 с.
10. Рассеянный склероз. Избранные вопросы теории и практики / Под ред. Завалишина И.А., Головкина В.И. — М., 2000. — 625 с.
11. Савченко Н.Е., Мохорт В.А. Нейрогенные расстройства мочеиспускания. — Минск.: Беларусь, 1970. — 244 с.
12. Салов П.П. Тазовое дно и дисфункции тазовых органов. — Новосибирск, 1998. — 348 с.
13. Шварц П.Г. Нарушение акта мочеиспускания у больных рассеянным склерозом ремитирующего течения: Автореф. дис. …канд. мед. наук. — М., 2004. — 22 с.
14. Abrams P.H., Blaivas J.G., Stanton S.L., Anderson J.T. Standartization of terminology of lower urinary tract function // Neurourol. Urodyn. — 1988. — Vol. 7 — P. 403–428.
15. Araki I., Kuno S. Assessment of voiding dysfunction in Parkinson's disease by the international prostate symptom score // J. Neurol Neurosurg Psychiatry. — 2000. — Apr. — 68(4). — Р. 429–33.
16. Blok B.F.M, Willemsen A.T.M., Holstege G. A PET study on the brain control of micturition in humans // Brain — 1997. — Vol. 20 — P. 111–121.
17. Chapple C.R. Muscarinic receptor antagonists in the treatment of overactive bladder // Urology — 2000. — Vol. 55, № 5A — P. 33–46.
18. Florante J., Leuson J., Martin B.F., Sporer A. Baclofen in the treatment of detrusor–sphincter dyssynergia in spinal cord injury patients // J. Urol. — 1980. — Vol. 124, № 1 — P. 82–84.
19. Langhorne P. et al. Medical complication after stroke // Stroke. – 2000. – Vol. 31, № 6. – P. 1223–1229.
20. Nordling J. Alpha–blockers and urethral pressure in neurological patients // Urol. Int. — 1978. — Vol. 33 — P. 304–309.












