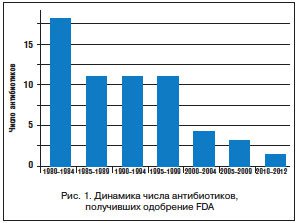
–І–Є—Б–ї–Њ –љ–Њ–≤—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –µ–ґ–µ–≥–Њ–і–љ–Њ –Њ–і–Њ–±—А—П–µ–Љ—Л—Е Food and Drug Administration (FDA) –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, –љ–µ—Г–Ї–ї–Њ–љ–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П (—А–Є—Б. 1) [14].
–Т –°–®–Р –µ–ґ–µ–≥–Њ–і–љ–Њ —А–µ–≥–Є—Б—В—А–Є—А—Г—О—В –і–Њ 2 –Љ–ї–љ —Б–ї—Г—З–∞–µ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –≤—Л–Ј–≤–∞–љ–љ—Л—Е –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л–Љ–Є –±–∞–Ї—В–µ—А–Є—П–Љ–Є. –°–≤—П–Ј–∞–љ–љ—Л–µ —Б —Н—В–Є–Љ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ —А–∞—Б—Е–Њ–і—Л —Б–Њ—Б—В–∞–≤–ї—П—О—В –Њ–Ї–Њ–ї–Њ 20 –Љ–ї—А–і –і–Њ–ї–ї–∞—А–Њ–≤. –Я–Њ –Њ—Ж–µ–љ–Ї–∞–Љ European Medicines Agency –Є European Centre for Disease Prevention and Control, 25 —В—Л—Б. —Б–Љ–µ—А—В–µ–є –≤ –Х–≤—А–Њ–њ–µ –µ–ґ–µ–≥–Њ–і–љ–Њ —П–≤–ї—П—О—В—Б—П –њ—А—П–Љ—Л–Љ —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –±–∞–Ї—В–µ—А–Є–є, –∞ –Њ–±—Й–Є–µ –Ј–∞—В—А–∞—В—Л –љ–∞ –ї–µ—З–µ–љ–Є–µ –і–Њ—Б—В–Є–≥–∞—О—В 1,5 –Љ–ї—А–і –µ–≤—А–Њ [21].
–Ю–і–љ–Є–Љ –Є–Ј –≤–µ–і—Г—Й–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –њ—А–Є–Ј–љ–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –љ–µ–Ї–Њ—В–Њ—А—Л—Е –±–∞–Ї—В–µ—А–Є–є —Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М –±–Є–Њ–њ–ї–µ–љ–Ї–Є. –Э–∞–њ—А–Є–Љ–µ—А, Escherichia coli – –Њ—Б–љ–Њ–≤–љ–Њ–є –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—М –Ш–Ь–Я –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е in vitro –≤ 63% —Б–ї—Г—З–∞–µ–≤ –і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М –±–Є–Њ–њ–ї–µ–љ–Ї–Є [20].
–С–Є–Њ–њ–ї–µ–љ–Ї–∞ – —Н—В–Њ –Њ—З–∞–≥ –Є–љ—Д–µ–Ї—Ж–Є–Є, —Б–Њ—Б—В–Њ—П—Й–Є–є –Є–Ј –Њ–і–љ–Њ–≥–Њ –≤–Є–і–∞ –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –Є–ї–Є —Б–Њ–Њ–±—Й–µ—Б—В–≤–∞ —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Є–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ—О—В —Б–≤–Њ—О —Б—В—А—Г–Ї—В—Г—А—Г, –њ—А–Є–љ—Ж–Є–њ—Л –ґ–Є–Ј–љ–µ–і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Є –ґ–Є–Ј–љ–µ–Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –Є —Б–Є—Б—В–µ–Љ—Л –Ј–∞—Й–Є—В—Л –Њ—В –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –Ј–∞—Й–Є—В—Л —Е–Њ–Ј—П–Є–љ–∞ –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Б—А–µ–і—Б—В–≤ [3]. –Т –≥–ї—Г–±–Њ–Ї–Є—Е —Б–ї–Њ—П—Е –±–Є–Њ–њ–ї–µ–љ–Њ–Ї –Љ–Є–Ї—А–Њ–±—Л –≤—Л–і–µ—А–ґ–Є–≤–∞—О—В –і–Њ–Ј—Л –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤ –і–µ—Б—П—В–Ї–Є –Є —Б–Њ—В–љ–Є —А–∞–Ј –њ—А–µ–≤—Л—И–∞—О—В —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є [16].
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Є–Љ–µ—О—Й–Є–µ—Б—П —Г—В–≤–µ—А–ґ–і–µ–љ–љ—Л–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –ї–µ—З–µ–љ–Є—О –Ш–Ь–Я, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –≤ —А–∞–Ј–љ—Л—Е —Б—В—А–∞–љ–∞—Е, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –љ–µ–њ—А–∞–≤–Є–ї—М–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Ї–∞–Ї –≤ –≥–Њ—Б–њ–Є—В–∞–ї—М–љ–Њ–є, —В–∞–Ї –Є –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є —Г—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–∞—Е–Њ–і–Є—В —Б–≤–Њ–µ –Њ—В—А–∞–ґ–µ–љ–Є–µ –≤ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –±–Њ–ї–µ–µ —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–Є –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–є –Ш–Э–Ь–Я, –ї–µ—З–µ–љ–Є–Є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Г—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П.
–Ъ –њ—А–Њ–±–ї–µ–Љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Л—Е —Б—А–µ–і—Б—В–≤ –њ—А–Є –Ш–Ь–Я –њ–Њ–і—Е–Њ–і—П—В –±–Њ–ї–µ–µ –≤–Ј–≤–µ—И–µ–љ–љ–Њ. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Є–ї–Њ—В–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П J. Bleidorn et al. (2010) –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ—А–Є –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–є –Ш–Ь–Я —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ–≤ –Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–∞ [15]. –Ґ–Њ –µ—Б—В—М –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Г–±—А–∞—В—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –і–∞–≤–∞—П –Њ—А–≥–∞–љ–Є–Ј–Љ—Г –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ —Б–њ—А–∞–≤–Є—В—М—Б—П —Б –Є–љ—Д–µ–Ї—Ж–Є–µ–є.
–Т –µ–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е (European Guidelines) –њ–Њ –ї–µ—З–µ–љ–Є—О –Є–љ—Д–µ–Ї—Ж–Є–є –≤ —Г—А–Њ–ї–Њ–≥–Є–Є (2014) –≤ –≥–ї–∞–≤–µ «–Р–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–є –Є–љ—Д–µ–Ї—Ж–Є–Є –љ–Є–ґ–љ–Є—Е –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є —Г –ґ–µ–љ—Й–Є–љ» –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Г—О –Є–ї–Є –њ–Њ—Б—В–Ї–Њ–Є—В–∞–ї—М–љ—Г—О –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ—Г—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г –і–ї—П –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є—Е –Ш–Ь–Я —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Є–Љ–µ–љ—П—В—М —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ —В–Њ–≥–Њ, –Ї–∞–Ї —Г—Б—В—А–∞–љ–µ–љ–Є–µ –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—А –љ–µ–∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є. –°–Ї—А–Є–љ–Є–љ–≥ –Є –ї–µ—З–µ–љ–Є–µ –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –±–∞–Ї—В–µ—А–Є—Г—А–Є–Є —В–µ–њ–µ—А—М —Б–ї–µ–і—Г–µ—В –њ—А–Є–Љ–µ–љ—П—В—М —В–Њ–ї—М–Ї–Њ —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–Љ –њ—А–µ–і—Б—В–Њ–Є—В –Є–љ–≤–∞–Ј–Є–≤–љ–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –љ–∞ –Љ–Њ—З–µ–њ–Њ–ї–Њ–≤—Л—Е –њ—Г—В—П—Е [18].
–Я–Њ –∞–љ–∞–ї–Њ–≥–Є–Є —Б European Guidelines –≤ —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е «–Р–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Є–љ—Д–µ–Ї—Ж–Є–є –њ–Њ—З–µ–Ї, –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є –Є –Љ—Г–ґ—Б–Ї–Є—Е –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤» –≤ —А–∞–Ј–і–µ–ї–µ «–Р–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є—Е –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є» —В–∞–Ї–ґ–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ—Л –њ—А–µ–њ–∞—А–∞—В—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–Ь–Я, –љ–µ —П–≤–ї—П—О—Й–Є–µ—Б—П –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є [3].
–§–Є—В–Њ–њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є –Љ–Њ–ґ–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –і–ї—П –ї–µ—З–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–є –Ш–Ь–Я, —П–≤–ї—П–µ—В—Б—П –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э («–С–Є–Њ–љ–Њ—А–Є–Ї–∞ –°–Х», –У–µ—А–Љ–∞–љ–Є—П). –≠—В–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Б –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –і–ї—П –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–Є—Е –Ш–Ь–Я (—Ж–Є—Б—В–Є—В, –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В—Л) –Є –Љ–Њ—З–µ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є. –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э —В–∞–Ї–ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –і–ї—П —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –љ–∞ –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В—П—Е. –Т —Б–Њ—Б—В–∞–≤ –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Е–Њ–і—П—В —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ —Н–Ї—Б—В—А–∞–Ї—В—Л –Ј–Њ–ї–Њ—В–Њ—В—Л—Б—П—З–љ–Є–Ї–∞, –ї—О–±–Є—Б—В–Њ–Ї–∞ –Є —А–Њ–Ј–Љ–∞—А–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–µ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є, —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–є, –∞–љ—В–Є–∞–і–≥–µ–Ј–Є–≤–љ—Л–є, –њ—А–Њ—В–Є–≤–Њ–Љ–Є–Ї—А–Њ–±–љ—Л–є –Є –Љ–Њ—З–µ–≥–Њ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В—Л.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—О –±–Њ–ї–µ–є –Є —А–µ–Ј–µ–є –њ—А–Є –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–Є, —Г–Љ–µ–љ—М—И–∞–µ—В —З–Є—Б–ї–Њ –њ–Њ–≤—В–Њ—А–љ—Л—Е –Њ–±–Њ—Б—В—А–µ–љ–Є–є, –њ–Њ–≤—Л—И–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є [2, 7, 9]. –Я—А–µ–њ–∞—А–∞—В —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –і–ї—П –Љ–µ—В–∞—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Љ–Њ—З–µ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Њ—В—Е–Њ–ґ–і–µ–љ–Є—О –Ї–Њ–љ–Ї—А–µ–Љ–µ–љ—В–Њ–≤ –Є –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –Є—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О [1, 2], –Ј–љ–∞—З–Є–Љ–Њ —Б–љ–Є–ґ–∞–µ—В –Є—А—А–Є—В–∞—В–Є–≤–љ—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ [4].
–° —Г—З—В–Њ–Љ –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ–Є–ї–Њ—В–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–µ –љ–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –њ—А–Є –Њ—Б—В—А–Њ–Љ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–Њ–Љ —Ж–Є—Б—В–Є—В–µ. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Њ—И–ї–Є 125 –ґ–µ–љ—Й–Є–љ, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э –≤ —В–µ—З–µ–љ–Є–µ 7 –і–љ–µ–є. –Т –ї—О–±–Њ–є –Љ–Њ–Љ–µ–љ—В –њ–Њ –ґ–µ–ї–∞–љ–Є—О –Ї–∞–ґ–і–∞—П –Є–Ј —Г—З–∞—Б—В–љ–Є—Ж –Љ–Њ–≥–ї–∞ –љ–∞—З–∞—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—О. –І–µ—А–µ–Ј 7 –і–љ–µ–є —В–µ—А–∞–њ–Є—О –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –њ—А–µ–Ї—А–∞—Й–∞–ї–Є. –Э–∞–±–ї—О–і–µ–љ–Є–µ –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–Ї–∞–Љ–Є –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –µ—Й–µ 30 —Б—Г—В. –Т—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–Њ–є –±–∞–ї–ї—М–љ–Њ–є —И–Ї–∞–ї–µ, —В–∞–Ї–ґ–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–±—Й–µ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –Љ–Њ—З–Є –Є –Ї—А–Њ–≤–Є.
–Я–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Њ–є —Б–ї—Г–ґ–Є–ї–∞ —З–∞—Б—В–Њ—В–∞ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –љ–∞ –њ—А–µ–њ–∞—А–∞—В –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 7-–і–љ–µ–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э. –Т—В–Њ—А–Є—З–љ—Л–Љ–Є –Ї–Њ–љ–µ—З–љ—Л–Љ–Є —В–Њ—З–Ї–∞–Љ–Є –±—Л–ї–Є –њ—А–Њ—Ж–µ–љ—В –њ–∞—Ж–Є–µ–љ—В–Њ–Ї, –Ї–Њ—В–Њ—А—Л–Љ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –ї–µ—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є –і–Њ 7-–≥–Њ –і–љ—П, –Є –і–Њ–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–Ї, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–∞ 7-–є –і–µ–љ—М –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є —Б–Є–Љ–њ—В–Њ–Љ—Л –Ш–Э–Ь–Я (–і–Є–Ј—Г—А–Є—П, –њ–Њ–ї–ї–∞–Ї–Є—Г—А–Є—П –Є –Є–Љ–њ–µ—А–∞—В–Є–≤–љ—Л–µ –њ–Њ–Ј—Л–≤—Л) —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –±–Њ–ї—М—И–µ–є, —З–µ–Љ —Б—А–µ–і–љ–µ–є —Б—В–µ–њ–µ–љ–Є (—В. –µ. –њ–∞—Ж–Є–µ–љ—В—Л, –Њ—В–≤–µ—В–Є–≤—И–Є–µ –љ–∞ –ї–µ—З–µ–љ–Є–µ).
–Э–Є —Г –Њ–і–љ–Њ–є –Є–Ј 125 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –љ–µ –±—Л–ї–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞. 97,6% –ґ–µ–љ—Й–Є–љ –љ–µ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М –ї–µ—З–µ–љ–Є–µ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–∞–Љ–Є –і–Њ 7-–≥–Њ –і–љ—П, –∞ –Њ–±—Й–∞—П –і–Њ–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–Ї, –Њ—В–≤–µ—В–Є–≤—И–Є—Е –љ–∞ –ї–µ—З–µ–љ–Є–µ, —Б–Њ—Б—В–∞–≤–Є–ї–∞ 71,2%. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –њ—А–Є –Њ—Б—В—А—Л—Е –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Ш–Э–Ь–Я. –Ю–і–љ–∞–Ї–Њ –і–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –і–∞–ї—М–љ–µ–є—И–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤–Ї–ї—О—З–∞—О—Й–Є–µ –≤—Л–±–Њ—А–Ї—Г –±–Њ–ї—М—И–µ–≥–Њ –Њ–±—К–µ–Љ–∞ [19].
–Ъ–∞–љ–µ—Д—А–Њ–љ® –Э —Г—Б–њ–µ—И–љ–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Ш–Ь–Я. –Т –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –Ы.–Р. –°–Є–љ—П–Ї–Њ–≤–Њ–є, —Г 91% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є–∞–≥–љ–Њ–Ј–∞–Љ–Є «–Њ—Б—В—А—Л–є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В» –Є «—Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є —Ж–Є—Б—В–Є—В» –љ–∞ —Д–Њ–љ–µ –Є–љ—Д–µ–Ї—Ж–Є–є, –њ–µ—А–µ–і–∞—О—Й–Є—Е—Б—П –њ–Њ–ї–Њ–≤—Л–Љ –њ—Г—В–µ–Љ, –њ–Њ—Б–ї–µ –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ —В–µ—З–µ–љ–Є–µ 1 –≥–Њ–і–∞ –њ—А–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э [10].
–Я–Њ–і —Н–≥–Є–і–Њ–є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –∞–Ї—Г—И–µ—А–Њ–≤-–≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Њ–≤ (–њ—А–µ–Ј–Є–і–µ–љ—В – –∞–Ї–∞–і–µ–Љ–Є–Ї –†–Р–Э, –њ—А–Њ—Д. –Т.–Э. –°–µ—А–Њ–≤) –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ «–Ю—Ж–µ–љ–Ї–∞ –Њ–њ—Л—В–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е». –Т —А–∞–±–Њ—В–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї—Г—О –і–Њ–Ї—Г–Љ–µ–љ—В–∞—Ж–Є—О 550 –±–µ—А–µ–Љ–µ–љ–љ—Л—Е, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е 480 –ґ–µ–љ—Й–Є–љ –љ–∞—А—П–і—Г —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є–µ–є –њ–Њ –њ–Њ–≤–Њ–і—Г —Ж–Є—Б—В–Є—В–∞, –Њ–±–Њ—Б—В—А–µ–љ–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ –Є–ї–Є –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ –ї–Є–±–Њ –≥–µ—Б—В–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Є–µ–ї–Њ–љ–µ—Д—А–Є—В–∞ –њ—А–Є–љ–Є–Љ–∞–ї–Є –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э. 70 –ґ–µ–љ—Й–Є–љ–∞–Љ –±—Л–ї–∞ –љ–∞–Ј–љ–∞—З–µ–љ–∞ —В–Њ–ї—М–Ї–Њ –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Њ—В–µ—А–∞–њ–Є—П (–≥—А—Г–њ–њ–∞ —Б—А–∞–≤–љ–µ–љ–Є—П). –†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ –і–Є–љ–∞–Љ–Є–Ї–∞ –і–Є–Ј—Г—А–Є—З–µ—Б–Ї–Є—Е —П–≤–ї–µ–љ–Є–є –њ—А–Є –Њ—Б—В—А–Њ–Љ —Ж–Є—Б—В–Є—В–µ –Є –Њ–±–Њ—Б—В—А–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Ж–Є—Б—В–Є—В–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ –ї—Г—З—И–µ –≤ –≥—А—Г–њ–њ–µ –ґ–µ–љ—Й–Є–љ, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э (—А–Є—Б. 2) [9].
–С–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ –Ї–∞–Ї –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е, —В–∞–Ї –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є. –†–µ–Ј—Г–ї—М—В–∞—В—Л –∞–љ–∞–ї–Є–Ј–∞ 19 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤ –Ї–Њ—В–Њ—А—Л–µ –≤–Њ—И–ї–Є 3327 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э, –≤ —В. —З. 2270 –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ, –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є –≤—Л—Б–Њ–Ї–Є–є –њ—А–Њ—Д–Є–ї—М –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ [6].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б —Г—З–µ—В–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–Є—П —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Г—А–Њ–њ–∞—В–Њ–≥–µ–љ–Њ–≤ –Ї –њ—А–Њ—В–Є–≤–Њ–Љ–Є–Ї—А–Њ–±–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –≤ –Љ–Є—А–Њ–≤–Њ–Љ –Љ–∞—Б—И—В–∞–±–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –њ–Њ–Є—Б–Ї –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–Њ–є –Є —Б–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є. –Ъ–∞–љ–µ—Д—А–Њ–љ® –Э, —А–∞—Б—В–Є—В–µ–ї—М–љ—Л–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Б –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –Љ–Њ–ґ–µ—В —Б —Г—Б–њ–µ—Е–Њ–Љ –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А—П–і–∞ –љ–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ—Л—Е –Ш–Ь–Я.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Р–ї—П–µ–≤ –Ѓ.–У. –Є —Б–Њ–∞–≤—В. –†–∞—Б—В–Є—В–µ–ї—М–љ—Л–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –Ъ–∞–љ–µ—Д—А–Њ–љ –Э –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –Љ–µ—В–∞—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Љ–Њ—З–µ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є // –£—А–Њ–ї–Њ–≥–Є—П. 2010. вДЦ 5. –°. 65–71.
2. –Р–ї—П–µ–≤ –Ѓ.–У., –Р–Љ–Њ—Б–Њ–≤ –Р.–Т. –Є —Б–Њ–∞–≤—В. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–∞–љ–µ—Д—А–Њ–љ –Э —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ —Ж–Є—Б—В–Є—В–Њ–Љ –Є –Љ–Њ—З–µ–Ї–∞–Љ–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О // –£—А–Њ–ї–Њ–≥–Є—П. 2005. вДЦ 4. –°. 29–33.
3. –Ы–Њ–њ–∞—В–Ї–Є–љ –Э.–Р., –Р–њ–Њ–ї–Є—Е–Є–љ –Ю.–Ш., –Я—Г—И–Ї–∞—А—М –Ф.–Ѓ. –Є –і—А. –†–Њ—Б—Б–Є–є—Б–Ї–Є–µ –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є «–Р–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Є–љ—Д–µ–Ї—Ж–Є–є –њ–Њ—З–µ–Ї, –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є –Є –Љ—Г–ґ—Б–Ї–Є—Е –њ–Њ–ї–Њ–≤—Л—Е –Њ—А–≥–∞–љ–Њ–≤». –Ь., 2014.
4. –Ь–∞—А—В–Њ–≤ –Р.–У., –Х—А–≥–∞–Ї–Њ–≤ –Ф.–Т. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–∞–љ–µ—Д—А–Њ–љ –Э –≤ —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ—Б–ї–µ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є // –≠—Д—Д–µ–Ї—В–Є–≤–љ–∞—П —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П. –£—А–Њ–ї–Њ–≥–Є—П –Є –љ–µ—Д—А–Њ–ї–Њ–≥–Є—П. 2012. вДЦ 4. –°. 16–23.
5. –Ь–Њ–Є—Б–µ–µ–≤ –°.–Т. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –њ–Њ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є —Б –њ–Њ–Ј–Є—Ж–Є–є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л // –Ш–љ—Д–µ–Ї—Ж–Є–Є –Є –∞–љ—В–Є–Љ–Є–Ї—А–Њ–±–љ–∞—П —В–µ—А–∞–њ–Є—П. 2003. вДЦ 5. –°. 3.
6. –Э–∞–±–µ—А –Ъ.–У., –Я–µ—А–µ–њ–∞–љ–Њ–≤–∞ –Ґ.–°. –Ю–±–Ј–Њ—А —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ъ–∞–љ–µ—Д—А–Њ–љ –Э –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Г—А–Њ–≥–µ–љ–Є—В–∞–ї—М–љ—Л—Е –Є –≥–µ—Б—В–∞—Ж–Є–Њ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є // –†–Ь–Ц. 2012. –°. 922–927.
7. –Я–µ—А–µ–њ–∞–љ–Њ–≤–∞ –Ґ.–°., –•–∞–Ј–∞–љ –Я.–Ы. –†–∞—Б—В–Є—В–µ–ї—М–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –Ъ–∞–љ–µ—Д—А–Њ–љ –Э –≤ –ї–µ—З–µ–љ–Є–Є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л—Е –њ—Г—В–µ–є // –Т—А–∞—З–µ–±–љ–Њ–µ —Б–Њ—Б–ї–Њ–≤–Є–µ. 2005. вДЦ 4–5. –°. 1–4.
8. –Я–µ—А–µ–њ–∞–љ–Њ–≤–∞ –Ґ.–°., –Ъ—Г–і—А—П–≤—Ж–µ–≤ –Ѓ.–Т., –•–∞–Ј–∞–љ –Я.–Ы. –Э–µ–Њ—Б–ї–Њ–ґ–љ–µ–љ–љ–∞—П –Є–љ—Д–µ–Ї—Ж–Є—П –Љ–Њ—З–µ–≤—Л—Е –њ—Г—В–µ–є // Consilium medicum. 2003. вДЦ 5. –°. 1.
9. –°–µ—А–Њ–≤ –Т.–Э., –С–∞—А–∞–љ–Њ–≤ –Ш.–Ш., –Ґ–Ї–∞—З–µ–љ–Ї–Њ –Ы.–Т., –Ъ—Г–Ї–∞—А—Б–Ї–∞—П –Ш.–Ш., –Я—А–Њ—В–Њ–њ–Њ–њ–Њ–≤–∞ –Э.–Т. –Ю—Ж–µ–љ–Ї–∞ –Њ–њ—Л—В–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —А–∞—Б—В–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е (–Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ) // –Р–Ї—Г—И–µ—А—Б—В–≤–Њ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є—П. 2013. вДЦ 9.
10. –°–Є–љ—П–Ї–Њ–≤–∞ –Ы.–Р., –Ъ–Њ—Б–Њ–≤–∞ –Ш.–Т. –Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л—Е –њ—Г—В–µ–є // –£—А–Њ–ї–Њ–≥–Є—П. 2009. вДЦ 2. –°. 22–25.
11. –ѓ–Ї–Њ–≤–ї–µ–≤ –°.–Т. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–љ—Д–µ–Ї—Ж–Є–є –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є // Consilium medicum. 2001. вДЦ 3. –°. 300–306.
12. –ѓ–Ї–Њ–≤–ї–µ–≤ –°.–Т., –Ф–≤–Њ—А–µ—Ж–Ї–Є–є –Ы.–Ш., –°—Г–≤–Њ—А–Њ–≤–∞ –Ь.–Я. –С–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Л–µ –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ: –≤—Л–±–Њ—А –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ // Consilium medicum. 2002. вДЦ 4. –°. 10–21.
13. –ѓ–Ї–Њ–≤–ї–µ–≤ –°.–Т., –Ф–µ—А–µ–≤—П–љ–Ї–Њ –Ш.–Ш. –Ш–љ—Д–µ–Ї—Ж–Є—П –Љ–Њ—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є: –£—З–µ–±–љ–Њ-–Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—Б–Њ–±–Є–µ –і–ї—П –≤—А–∞—З–µ–є. –Ь.: –Ь–µ–і–Є–∞ –Ь–µ–і–Є–Ї–∞, 2001.
14. Antibiotic resistance threats in the United States, 2013. U.S. Departament of Health and Human Services Centers for Disease Control and Prevention. P. 44.
15. Bleidorn J., Gagyor I., Kochen M.M., Wegscheider K., Hummers-Pradier E. Symptomatic treatment (ibuprofen) or antibiotics (ciprofloxacin) for uncomplicated urinary tract infection? – results of a randomized controlled pilot trial // BMC Med. 2010. Vol. 26 (8). –†. 30.
16. Donlan R.M., Costerton J.W. Biofilms: Survival mechanisms of clinically relevant microorganisms // Clin Microbiol Rev. 2002. Vol.15 (2). –†. 167–193.
17. European Antimicrobial Resistance Surveillance Network (EARS-Net).
18. Grabe M., Bjerklund-Johansen T.E., Botto H., Cek M., Naber K.G., Pickard R.S., Tenke P., Wagenlehner F., Wullt B. // Urological infections European Guidelines, 2014.
19. Naber K., Steindl H., Abramov-Sommariva D., Eskoetter H. Non-antibiotic herbal therapy of uncomplicated lover urinary tract infection in wamen – a pilot study. Planta Medica // J. Med. Plant Nat. Prod. Res. 2013. Vol. 79. P. 1079–1288.
20. Subramanian P., Shanmugam N., Sivaraman U., Kumar S., Selvaraj S. Antiobiotic resistance pattern of biofilm-forming uropathogens isolated from catheterised patients in Pondicherry, India // Australas Med J. 2012. Vol. 5 (7). –†. 344–348.
21. Uchil R.R., Kohli G.S., Katekhaye V.M., Swami O.C. Strategies to combat antimicrobial resistance // J Clin Diagn Res. 2014 Jul. Vol. 8 (7). ME01-4.












