Гиперактивный мочевой пузырь (ГМП) является широко распространенным заболеванием, оказывающим существенное влияние на качество жизни пациентов и сопровождающимся ощутимыми финансовыми затратами на лечение. Данное заболевание не является угрожающим жизни состоянием, однако часто приводит к дезадаптации и в тяжелых случаях – к инвалидизации пациентов [1,6]. Синдром не имеет явной причины, и диагноз устанавливают на основании указанных симптомов нарушения мочеиспускания при отсутствии других заболеваний, приводящих к этим симптомам. В основе ГМП лежит детрузорная гиперактивность, которая проявляется в виде внезапного повышения детрузорного давления амплитудой более 5 см вод. ст. Существуют две основные формы детрузорной гиперактивности: нейрогенная (НДГ), как следствие повреждения или заболеваний нервной системы, и идиопатическая (ИДГ), когда причину непроизвольных сокращений детрузора выявить не удается [4].
Трудности, с которыми сталкиваются врачи при лечении больных ГМП, связаны с отсутствием понятного механизма, объясняющего развитие симптомов ГМП. Выбор метода лечения больных ГМП и сегодня остается актуальной задачей урологии. Очевидно, что применяемый метод лечения должен быть основан на результатах комплексного обследования больного. Пока основным методом, позволяющим определить форму ГМП, является уродинамическое исследование [2,8].
К настоящему времени существует множество методик лечения ГМП. Наиболее распространенную в лечении ГМП медикаментозную терапию препаратами антихолинергического действия можно рассматривать только как симптоматическую, т. е. избавляющую больного лишь от клинических проявлений заболевания, но не устраняющую причину. В то же время значительным недостатком применения указанной группы препаратов являются выраженные побочные эффекты в виде сухости во рту, запоров, задержки мочеиспускания, нарушения зрения и когнитивной функции (функции распознавания) у пожилых больных. Кроме этого, у 20–30% больных ГМП холинолитики оказываются недостаточно эффективными, несмотря на применение высоких доз. В связи с этим практическую ценность приобретают эффективные альтернативные методы лечения, из которых все большее внимание уделяется электростимуляции и нейромодуляции. Принимая во внимание тот факт, что в последнее время большинство исследователей склоняются к нейрогенной теории развития ГМП, такой метод лечения, как нейромодуляция, может рассматриваться как патогенетический [13,15].
До настоящего времени нет точного объяснения терапевтического эффекта нейромодуляции при ГМП. Существуют два гипотетических механизма, объясняющих эффект нейромодуляции, изученных экспериментально на животных моделях. Так, во время работы по созданию электростимулятора мочевого пузыря у животных с параплегией была отмечена тесная взаимосвязь между функциональным состоянием мышц тазового дна и детрузора. В частности, при электростимуляции пудендального нерва прекращалось непроизвольное сокращение детрузора. Таким образом, было показано, что в регуляции функции нижних мочевых путей вегетативная и соматическая иннервации участвуют взаимосвязанно и влияют друг на друга. Первый механизм действия основан на исследованиях Tanagho E. и Schmidt R., которые показали, что нейромодуляция на уровне моторных проводящих путей приводит к тренировке и увеличению силы сокращения мышечных волокон тазового дна. Это восстанавливает нормальное произвольное сокращение мышц тазового дна и возвращает ингибиторное влияние поперечно–полосатых мышц на сократительную активность детрузора [16,18].
Второй механизм действия нейростимуляции основан на том, что эфферентная активность тазового нерва, ответственного за сокращение мочевого пузыря, контролируется афферентными импульсами других нервов, которые в свою очередь, с одной стороны, действуют через центральные структуры на подчревный нерв, а с другой – через интернейроны сакрального отдела спинного мозга непосредственно на тазовый нерв [12]. Нарушение центрального механизма подавления эфферентной активности тазового нерва может быть компенсировано стимуляцией миелинизированных афферентных А?–волокон при раздражении мышц тазового дна и электростимуляцией дорсального нерва полового члена или клиторного нерва, а также пудендального, тибиального и сакральных нервов [10]. В то же время известно, что в составе тибиального нерва идут волокна из II и III сакральных сегментов спинного мозга, которые в большей степени, чем другие ответственны за иннервацию мочевого пузыря и его сфинктеров. Поэтому, учитывая доступность этого нерва, тибиальная нейромодуляция (ТНМ) является наиболее оптимальной для лечения больных с детрузорной гиперактивностью. Согласно проведенным ранее исследованиям, эффективность нейромодуляции в лечении больных разных форм ГМП достигает 60%, при этом отмечено, что эффект от ее применения зависит от состояния (проводимости) по афферентным путям нервной системы [5,14]. Методом, позволяющим исследовать проводимость по афферентным путям нервной системы, является нейрофизиологическое исследование соматосенсорных вызванных потенциалов (ССВП) [3].
В урологической практике этот метод использовался для оценки афферентной проводимости по афферентным путям, участвующим в регуляции мочеиспускания. Он позволил проследить проведение афферентной волны возбуждения от стимулируемого периферического нерва до коры больших полушарий и выявить нарушения нервной проводимости у больных нейрогенными формами нарушений мочеиспускания и эректильной дисфункцией [9,11]. Проведенные исследования показывают отклонения от нормальных значений параметров ССВП у больных с нейрогенными расстройствами мочеиспускания.
В нашем исследовании мы применили нейрофизиологический метод регистрации ССВП при стимуляции тибиального нерва с целью прогноза эффективности ТНМ у больных ГМП.
Материалы и методы
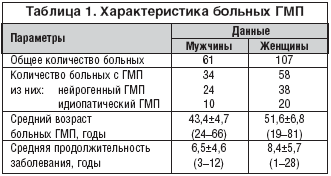
Обследовано 168 больных с симптомами нижних мочевых путей. В основу настоящего исследования положен анализ результатов обследования и лечения 92 больных – 34 мужчин и 58 женщин с синдромом ГМП. Средний возраст мужчин составил 43,4±4,7 (24–66) г., женщин 51,6±6,8 (19–81) г. Длительность заболевания составила от 1 года до 28 лет (7,6±3,6). В работе были выделены три этапа. На первом этапе проводили клиническое обследование больных ГМП. Жалобы больных и эффективность лечения оценивали по дневнику мочеиспускания, который заполняли в течение 72 часов. При выяснении анамнеза уточняли продолжительность заболевания, эффективность проводимой терапии. Критериями включения больных в исследование являлись:
– отсутствие инфекции мочевых путей;
– отсутствие урологических заболеваний, имеющих в клинической картине ГМП (доброкачественная гиперплазия простаты, простатит, рак простаты);
– отсутствие других заболеваний, имеющих в клинической картине ГМП (эндокринологические, гинекологические заболевания, стрессовое недержание мочи);
– наличие непроизвольных сокращений детрузора при проведении цистометрии.
Причиной ГМП являлись: у 46 больных – дегенеративно–дистрофический процесс позвоночника (остеохондроз), у 4 – травма позвоночника, у 12 – болезнь Паркинсона. Диагноз неврологического заболевания установлен на основании анамнестических данных, результатов неврологического осмотра и лучевых методов обследования (рентгенография, магниторезонансная томография позвоночника). При сборе анамнеза выясняли жалобы больного, длительность неврологического заболевания, предшествующее лечение, если таковое проводилось. Всем больным с остеохондрозом позвоночника, а также с травматическими повреждениями позвоночника ранее выполнялась рентгенография позвоночника в двух проекциях и магниторезонансная томография позвоночника. Необходимо отметить, что у 34 из 46 (73,7%) больных имели поражение на уровне пояснично–крестцового отдела позвоночника, 9 (19,7%) – на уровне грудного отдела, и 3 (6,6%) на уровне шейного отдела. При этом у 34 больных (73,7%) дегенеративно–дистрофический процесс позвоночного столба сопровождался образованием грыж межпозвоночных дисков.
У 30 больных не обнаружено каких–либо неврологических и других заболеваний, которые могли привести к появлению ГМП, поэтому у данной категории больных характер ГМП расценен как идиопатический. Характеристика больных ГМП, включенных в исследование представлена в таблице 1.
На втором этапе всем больным проводили комплексное уродинамическое исследование по стандартной методике ICS 2002 [7], а также нейрофизиологическое исследование ССВП при стимуляции тибиального нерва.
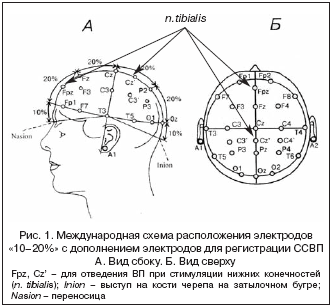
Для исследования ССВП использовали нейроусреднитель «Nicolet» CA–1000 (США). Во время исследования больные находились в тихом, хорошо проветриваемом помещении, лежа в удобном положении на спине. Регистрацию ССВП проводили с коркового уровня при стимуляции левого и правого тибиальных нервов. Накожный электрод фиксировали на внутренней части лодыжки таким образом, чтобы анод находился дистальнее катода. Интенсивность стимула подбирали вручную, таким образом, чтобы при стимуляции было видно рефлекторное движение большого пальца стопы. Для регистрации корковых ответов чашечковый электрод, обработанный электродной пастой, располагали на коже волосистой части головы в точке Сz’ – проекции соматосенсорной зоны коры головного мозга (международная система 10–20%, рис. 1). Индифферентный электрод размещали на лобной кости в точке Fpz. Электрод для заземления устанавливали на плече. Условия регистрации ССВП: полоса пропускания 5 Гц – 3 кГц, время регистрации 200 мс; число суммаций 500, при частоте 4 Гц и длительности 0,3 мс. Сопротивление накожных электродов было менее 10 кОм. Для того, чтобы результаты считались достоверными, получали три идентичных ответа при регистрации трех серий суммаций. С целью контроля работы аппаратуры записывали периферический ответ: для этого электроды располагали в области подколенной ямки (проекция тибиального нерва).
Уродинамическое исследование, включающее в себя ретроградную водную цистометрию умеренного наполнения (75 мл/мин.), исследование давление–поток, а также пластинчатую электромиографию наружного анального сфинктера, имеющего синергию со сфинктером уретры выполняли, используя уродинамическую установку Ellipse 4 фирмы Andromeda (Германия). Мы регистрировали: объем жидкости, вызывающий первый позыв к акту мочеиспускания (мл), максимальную цистометрическую емкость мочевого пузыря (мл), максимальную амплитуду непроизвольного сокращения детрузора (см вод.ст.), максимальную скорость мочеиспускания (мл/с), объем остаточной мочи (мл) и электромиографию наружного анального сфинктера.
Всем 92 больным ГМП первым этапом в лечении применяли ТНМ. Для стимуляции тибиального нерва использовали двухканальный электростимулятор зарубежного производства «Нейростим» (American Imex). Стимуляцию проводили в течение 12 недель с периодичностью 1 раз в неделю. Время одной процедуры 30 мин. Больных с улучшением симптомов учащенного мочеиспускания включали в так называемый заключительный протокол. Это означает, что в дальнейшем этим больным проводили одну процедуру в течение 2–3 недель.
Анализ эффективности лечения включал ведение дневника мочеиспускания и комплексное уродинамическое исследование. При анализе эффективности лечения, помимо объективных методов исследования, использовали специальную шкалу, аналогичную «шкале боли». Шкала представляет собой градуированный отрезок, одно из крайних значений которого соответствует максимальному проявлению нарушения акта мочеиспускания, а противоположное свидетельствует об их отсутствии. Больному предлагали отметить на таком отрезке степень выраженности симптомов нарушения акта мочеиспускания до и после того или иного вида лечения. Результаты лечения считали хорошим при исчезновении симптомов или их снижении на 50% от исходных данных.
Результаты
По результатам комплексного уродинамического исследования (КУДИ) больных разделили на 4 группы: первую группу составили больные с нейрогенной детрузорной гиперактивностью (НДГ), вторую – с идиопатической детрузорной гиперактивностью (ИДГ), третью – с детрузорно–сфинктерной диссинергией (ДСД). Четвертая группа больных представлена нейрогенной детрузорной гиперактивностью в сочетании со снижением активности детрузора.
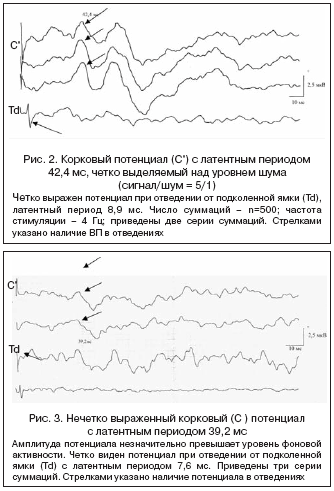
По результатам исследования ССВП мы также выделили 3 группы. Первую группу составили больные с наличием четко выраженного коркового потенциала – соотношение сигнал/шум = 5/1. Четко выраженный корковый потенциал показан на рисунке 2.
Вторую группу составили больные с наличием нечетко выраженного коркового потенциала. Амплитуда такого потенциала незначительно превышает уровень фоновой активности. Нечетко выраженный корковый потенциал показан на рисунке 3.
Третью группу составили больные, у которых мы не смогли зарегистрировать корковый потенциал в наших условиях регистрации (рис. 4).
При исследовании ССВП из 45 больных НДГ четко выраженный корковый потенциал выявлен у 20 больных (44,4%) – у 8 больных с болезнью Паркинсона и у 12 больных с вертеброгенными заболеваниями. Нечетко выраженный корковый потенциал наблюдали у 4 больных (8,9%) – у 1 больного с болезнью Паркинсона и у 3 больных с вертеброгенными заболеваниями. Мы не смогли зарегистрировать корковый потенциал у 21 больного НДГ (46,7%): у 3 с болезнью Паркинсона и у 18 больных с вертеброгенными заболеваниями. Из 12 больных, у которых мы наблюдали четко выраженный корковый потенциал, у 9 (75%) была 1–2 степень дегенеративно–дистрофического процесса позвоночника. Напротив, у всех 18 больных, у которых корковый потенциал мы не смогли зарегистрировать, была 3–4 степень дегенеративно–дистрофического процесса.
При исследовании ССВП у 7 больных ДСД четко выраженный корковый потенциал выявлен у 2 (28%) больных: у 1 с травмой позвоночника (после оперативного вмешательства) и у 1 – с 3–4 степенью дегенеративно–дистрофического процесса пояснично–крестцового отдела позвоночника. У 5 (72%) больных корковый потенциал отсутствовал: у 3 – травма позвоночника, у 2 – 3–4 стадия дегенеративно–дистрофического процесса пояснично–крестцового отдела позвоночника.
При исследовании ССВП у 10 больных НДГ в сочетании со снижением активности детрузора четко выраженный корковый потенциал наблюдался у 4 (40%) больных, нечетко выраженный у 1 (10%), отсутствовал у 5 (50%) больных. У всех 10 больных причиной нарушения функции детрузора служили вертеброгенные заболевания. Из 4 больных с наличием четко выраженного коркового потенциала у 2 была 1–2–я степень и у 2 – 3–4–я степень дегенеративно–дистрофического процесса пояснично–крестцового отдела позвоночника. У 1 больного с нечетко выраженным корковым потенциалом была 3–4 степень дегенеративно–дистрофического процесса пояснично–крестцового отдела позвоночника. У всех 5 больных с отсутствием коркового потенциала была 3–4 степень дегенеративно–дистрофического процесса пояснично–крестцового отдела позвоночника.
При исследовании ССВП у больных ИДГ четко выраженный корковый потенциал регистрировался у 17 больных (56,6%), нечетко выраженный – у 6 (20%), отсутствовал у 7 больных (23,4%).
ТНМ была эффективна у 21 (46,6%) из 45 больных НДГ. Положительный результат в виде снижения частоты мочеиспусканий по данным дневника мочеиспускания мы получили в виде снижения числа мочеиспусканий в среднем с 16,1 до 12,4 в сутки, количество ургентных позывов в среднем с 5,4 до 2,8 в сутки. Количество эпизодов ургентного недержания мочи снизилось в среднем с 6,5 до 3,2 в сутки. Клиническое улучшение сопровождалось статистически значимым увеличением цистометрической емкости по данным КУДИ в среднем с 167 до 204 мл, увеличением объема жидкости, вызывающей первый позыв к акту мочеиспускания в среднем с 76 до 92 мл. Динамика изменений клинических показателей и уродинамических параметров у больных НДГ показана на рисунке 5.
При применении ТНМ из 30 больных ИДГ положительный результат применения ТНМ мы получили у 22 больных (73%) в виде снижения числа мочеиспусканий в среднем с 11,7 до 8,7 в сутки, количества ургентных позывов в среднем с 2,3 до 1,6 в сутки. Число эпизодов ургентного недержания мочи снизилось в среднем с 2,9 до 1,7 в сутки. Клиническое улучшение сопровождалось статистически значимым увеличением цистометрической емкости по данным КУДИ в среднем с 231 до 272 мл, увеличением объема жидкости, вызывающей первый позыв к акту мочеиспускания в среднем со 104 до 157 мл, а также снижением амплитуды непроизвольных сокращений детрузора с 32 до 15 см. вод. ст. Динамика изменений клинических показателей и уродинамических параметров у больных ИДГ показана на рисунке 6.
Применение ТНМ было эффективно у 4 (40%) из 10 больных НДГ в сочетании со снижением активности детрузора. Число мочеиспусканий снизилось в среднем с 12,5 до 10,4 в сутки, количество ургентных позывов в среднем с 4,1 до 3,2 в сутки. Количество эпизодов ургентного недержания мочи снизилось в среднем с 1,7 до 0,4 в сутки. Клиническое улучшение сопровождалось увеличением цистометрической емкости по данным КУДИ в среднем с 112 до 165 мл, увеличением объема жидкости, вызывающей первый позыв к акту мочеиспускания, в среднем со 87 до 102 мл.
Динамика изменений клинических показателей и уродинамических параметров у больных НДГ в сочетании со снижением активности детрузора показана на рисунке 7.
ТНМ была эффективна только у 1 больного с ДСД (14,7%). После проведения 12 сеансов ТНМ у этого больного отметили снижение числа мочеиспусканий в среднем с 14 до 10 и числа ургентных позывов к акту мочеиспускания с 6 до 4 в сутки.
С целью выявления взаимосвязи между результатами исследования ССВП при стимуляции тибиального нерва и эффективностью ТНМ мы исследовали предиктивную чувствительность указанного нейрофизиологического метода у 92 больных ГМП.
Из 45 больных НДГ ТНМ была эффективна у 21 (46%). При сопоставлении данных исследования ССВП с результатами ТНМ оказалось, что ТНМ была эффективна у 18 (85,7%) больных с наличием четко выраженного коркового потенциала, у 1 (4,7%) больного с наличием нечетко выраженного коркового потенциала и только у 2 (9,6%) больных с отсутствием коркового потенциала. Из 24 (54%) больных, у которых ТНМ была не эффективна, четко выраженный потенциал регистрировали только у 2 (8,4%) больных, у 6 (25%) больных регистрировался нечетко выраженный корковый потенциал, у 16 (66,6%) больных корковый потенциал отсутствовал. Чувствительность метода исследования ССВП в прогнозе эффективности ТНМ составила 90%.
ТНМ была эффективна у 22 (73%) из 30 больных ИДГ. При сопоставлении результатов исследования ССВП при стимуляции тибиального нерва с результатами ТНМ оказалось, что тибиальная ТНМ была эффективна у 16 (72,7%) больных с наличием четко выраженного коркового потенциала, у 4 (18,2%) с наличием нечетко выраженного коркового потенциала и только у 2 (9,1%) больных с отсутствием коркового потенциала. Напротив, из 8 (27%) больных ТНМ оказалась неэффективной только у 1 (12,5%) больного с наличием четко выраженного коркового потенциала, у 2 (25%) с наличием нечетко выраженного коркового потенциала и у 5 (62,5%) больных с отсутствием потенциала. Чувствительность метода исследования ССВП в прогнозе эффективности ТНМ у больных ИДГ составила 94%.
ТНМ была эффективной у 4 (40%) из 10 больных НДГ в сочетании со снижением активности детрузора и только у 1 (14%) из 7 больных с ДСД. При сопоставлении результатов исследования ССВП с результатами ТНМ оказалось, что ТНМ была эффективна у 3 (75%) из 4 больных НДГ в сочетании со снижением активности детрузора и у 1 (50%) из 2 больных ДСД и наличием четко выраженного коркового потенциала. ТНМ была неэффективна у 6 (60%) больных НДГ в сочетании со снижением активности детрузора: у 1 (16,6%) с наличием четко выраженного коркового потенциала, у 1 (16,6%) с наличием нечетко выраженного коркового потенциала и у 4 (66,8%) больных с отсутствием коркового потенциала. Среди больных ДСД (n=6), у которых ТНМ была неэффективна, четко выраженный корковый потенциал регистрировали только у 1 (16,6%) больного, у 5 (83,4%) корковый потенциал отсутствовал. Чувствительность метода исследования ССВП в прогнозе эффективности ТНМ составила 66%.
Таким образом, из 48 больных ГМП, у которых ТНМ была эффективна, четко выраженный корковый потенциал регистрировался у 38 больных. Из этого следует, что эффективность ТНМ у больных ГМП с наличием четко выраженного коркового потенциала составляет 79%.
Обсуждение
Подводя итоги, можно отметить, что тибиальная нейромодуляция является эффективным патогенетическим средством лечения синдрома ГМП. По данным ряда авторов, эффективность применения ТНМ у больных ГМП достигает 60%. В доступной нам литературе мы не нашли объяснения причин, из–за которых у 40% больных ТНМ не влияет на симптомы ГМП. В то же время, оценка состояния афферентных путей нервной системы является перспективным, но недостаточно изученным направлением в диагностике нейрогенных форм нарушений мочеиспускания. В литературе мы встретили единичные работы, посвященные изучению вызванных потенциалов у больных с расстройствами мочеиспускания. Проведенные исследования показывают отклонения от нормальных значений параметров ССВП у больных с нейрогенными расстройствами мочеиспускания. Однако вопрос о взаимосвязи между результатами ССВП и эффективностью ТНМ у больных ГМП остается неизученным. Malaguti с соавт. в 2003 г. предположили, что нейрофизиологическое исследование ССВП может прогнозировать эффективность сакральной нейромодуляции. В работе участвовали 24 больных с симптомами нижних мочевых путей, которым проводили исследование ССВП при стимуляции пудендального и тибиального нервов. Лечение проводили стимуляцией S3 сакрального сплетения. При сопоставлении данных исследования вызванных потенциалов с результатами лечения, авторы отметили, что в группе больных с положительными результатами лечения отмечено статистически достоверное уменьшение латентного периода коркового потенциала при стимуляции тибиального и пудендального нерва. В группе больных с отрицательными результатами сакральной нейромодуляции отмечено уменьшение латентного периода коркового потенциала только при стимуляции пудендального нерва. Таким образом, проведенное исследование позволило авторам, во–первых – подтвердить предыдущие предположения о том, что сакральная нейромодуляция воздействует на супраспинальные центры мочеиспускания, во–вторых – предположить, что исследование вызванных потенциалов во время сакральной нейромодуляции позволяет прогнозировать ее эффект [14].
Мы также полагаем, что механизм действия ТНМ не ограничивается воздействием на сакральный центр мочеиспускания. Можно предположить, что в случае повреждения афферентных волокон, передающих сигналы от мочевого пузыря к корковым центрам мочеиспускания вследствие неврологических или вертеброгенных заболеваний, эффект ТНМ ограничивается воздействием на сакральные нервные центры. В результате этого, у таких больных с повреждением афферентных путей спинного мозга ТНМ может быть не эффективна. По этой причине мы применили нейрофизиологический метод исследования, позволяющий оценить состояние афферентных нервных путей нервной системы, которым является метод регистрации ССВП.
У всех 92 больных ГМП мы исследовали ССВП с коркового уровня при стимуляции тибиального нерва. Анализ результатов исследования показал, что у 76,6% больных с ГМП идиопатического характера регистрировался корковый потенциал. Среди больных с ГМП нейрогенного происхождения корковый потенциал регистрировался только у 50%. Выявлена зависимость результатов исследования ССВП от стадии дегенеративно–дистрофического процесса позвоночника у больных НДГ. Так, у 75% больных с наличием четко выраженного коркового потенциала была 1–2 стадия дегенеративно–дистрофического процесса (без образования грыж межпозвоночных дисков). Напротив, у всех больных с отсутствием коркового потенциала была 3–4 стадия (с наличием грыж межпозвоночных дисков).
Анализ результатов применения ТНМ показал, что ее эффективность у больных нейрогенной и идиопатической детрузорной гиперактивностью выше (46,6 и 73% соответственно), чем у больных со смешанными уродинамическими формами нарушений мочеиспускания – НДГ в сочетании со снижением активности детрузора и ДСД (40 и 14% соответственно).
При сопоставлении результатов исследования ССВП с результатами ТНМ, оказалось, что у больных ГМП с наличием четко выраженного коркового потенциала эффективность ТНМ выше, чем у больных с отсутствием коркового потенциала. Сопоставление результатов ССВП с результатами ТНМ показало высокую чувствительность метода в прогнозе эффективности ТНМ у больных нейрогенной и идиопатической детрузорной гиперактивностью (90 и 94% соответственно). Чувствительность метода у больных смешанными уродинамическими формами нарушений мочеиспускания составила 66%. В итоге из 48 больных ГМП, у которых ТНМ была эффективна, четко выраженный корковый потенциал регистрировался у 38 (79%) больных. Напротив, из 44 больных, у которых ТНМ была неэффективна, четко выраженный корковый потенциал регистрировали только у 5 (11,3%) больных. У всех 5 больных продолжительность заболевания составляла более 10 лет, что могло привести к формированию необратимых ультраструктурных изменений в детрузоре [17]. Из этого следует, что эффективность ТНМ у больных с четко выраженным корковым потенциалом составляет 79%.
У больных ГМП и наличием нечетко выраженного коркового потенциала чувствительность метода регистрации ССВП составила 35%. Следовательно, наличие нечетко выраженного коркового потенциала при регистрации ССВП не позволяет прогнозировать результат ТНМ.
Заключение
Таким образом, проведенное нами исследование позволяет предположить, что эффективность ТНМ зависит от состояния афферентных путей периферической и центральной нервной системы. Результаты исследования ССВП позволяют прогнозировать эффект от применения ТНМ у больных ГМП вследствие как нейрогенной, так и идиопатической детрузорной гиперактивности. Однако следует отметить недостатки метода ССВП. В нашем исследовании мы проводили регистрацию ССВП только с двух уровней – коркового и периферического для контроля работы аппаратуры. Это связано с техническими возможностями нейроусреднителя «Nicolet» CA–1000 – наличия двух каналов усреднения. Более современные нейроусреднители имеют 4 канала усреднения, что позволяет исследовать ССВП на уровне шейного и поясничного утолщений спинного мозга, что способствует более точному определению локализации нарушений нервной проводимости. Другим недостатком является то, что при всей точности метода, объективности его показателей, остается ряд нерешенных вопросов, связанных с его применением в клинической практике. Например, появление ложных негативных данных, когда в ответ на стимул потенциал отсутствует (иногда на всем протяжений соматосенсорного пути), в то время как при клиническом обследовании у больного не обнаруживается существенного неврологического дефицита. Так, в нашем исследовании положительный результат тибиальной нейромодуляции наблюдался у 5 из 48 (10,5%) больных с отсутствием коркового потенциала. Методы регистрации и анализа ССВП необходимо совершенствовать в отношении параметров стимуляции и проблем регистрации более поздних и длиннолатентных ответов.


Литература
1. Аль–Шукри С.Х., Кузьмин И.В. Гиперактивность детрузора и ургентное недержание мочи. Пособие для врачей. Санкт–Петербург.1999.
2. Аляев Ю.Г., Винаров А.З., Гаджиева З.К., Балан В.Е., Локшин К.Л., Спивак Л.Г. Гиперактивный мочевой пузырь // Врачебное сословие, №1–2/2004. Стр. 36–42.
3. Гнездицкий В. В. Опыт применения вызванных потенциалов в клинической практике. М.: АОЗТ «Антидор», 2001. – 480 с – стр. 223.
4. Мазо Е. Б., Кpивобоpодов Г. Г. Вpеменная сакpальная и тибиальная нейpомодуляция в лечении больных с гипеpактивным мочевым пузыpем. Вопросы нейрохирургии им. Н. Н. Бурденко №1 2002, стр 17–22.
5. Мазо Е.Б., Соколова А.А., Кривобородов Г.Г., Школьников М.Е., Моисеев П.П. Значение вызванных потенциалов в прогнозе тибиальной нейромодуляции у больных гиперактивным мочевым пузырем. Врачебное сословие, №7/2006. Стр. 33–37.
6. Трапезникова М.Ф., Дутов В.В., Бычкова Н.В. и др. Гиперактивный мочевой пузырь: Учебное пособие. М., 2004.
7. Abrams P, Cardozo L, Fall M et al. The standardisation of terminology of lower urinary tract function: Report from the standardisation sub–committee of the International Continence Society. // Neurourol Urodin–2002; vol.1, issue 2, p 167–178.
8. Abrams P., Wein A.J. Introduction: Overactive bladder and its treatsments. //Urology–2000– 55 (Suppl 5A),12.
9. Braun P.M., Baezner H., Seif C. at al. Altaration of Cortical Electrical Activity in Patients with Sacral Neuromodulator. //European Urology– 2002–41.
10. Gruenewald V, Jonas U. Neurostimulation for lower urinary tract voiding problems. //Curr Urol Rep, 2000 Oct;1(3):199–203.
11. Klausner A, Barta A. Pudendal nerve somatosensory evoked potentials in patients with voiding and/or erectile dysfunction: correlating test results with clinical findings. //J Urol–1996–156: 1425–1427.
12. Lindstrom S, Fall M, Carlsson CA, Erlandson BE //Urol Int 1984;39: 272–279.
13. Madersbacher H., Awad S., Fall M., Janknegt R.A., Stohrer M., Weisner B. Urge incontinence in the elderly–supraspinal reflex incontinence. //World J Urol–1998–16 (Suppl 1): P35–43.
14. Malaguti S., Spinelli M., Giardiello G., Lazzeri M., Van Den Hombergh U.. Neurophisiological evidence may predict the outcome of sacral neuromodulation. //The Journal of Urology–2003– vol. 170, 2323–2326.
15. McGrother C., Resnick M., Yalla S.V., Kirschner–Hermanns R., Broseta E., Muller C., Welz–Barth A., Fischer G.C., Mattelaer J., McGuire E.J. Epidemiology and etiology of urinary incontinence in the elderly. //World J Urol–1998– 16 (Suppl 1): S3–9.
16. Schmidt RA. Advances in genitourinary neurostimulation. // Neurosurgery. 1986 Dec;19(6):1041–4.
17. Suzanne M. Biers and Alison F. Brading. Nerve regeneration: might this be only solution for functional problems of urinary tract? //Current Opinion Urology–2004 – V.13: 495 – 500.
18. Tanagho EA. Sacral root stimulation. // Neurourol Urodyn. 1993;12(5):505.












