Изложенное показывает сложность проблемы антимикробной терапии УГИ. Различия в свойствах и особенностях биологии возбудителей делают практически невозможным создание антимикробного препарата, эффективного в отношении всех указанных выше микроорганизмов. Кроме того, успех терапии будет определяться не только антимикробной активностью соединения, но и особенностями его фармакокинетики (биодоступность при пероральном применении, степень метаболизма и экскреции почками, концентрация неизмененного препарата и его активных метаболитов в моче, степень проникновения в ткани гениталий и, что существенно для возбудителей с внутриклеточной локализацией, степень проникновения в клетки фагоцитарной системы).
Достаточно большое число разработанных антибактериальных препаратов различных классов экскретируются почками, обеспечивают высокую концентрацию в системе мочевыводящих путей и в моче и позволяют в монотерапии эффективно лечить острые несложненные процессы ИМВП и ряд ЗППП, конечно, при условии чувствительности возбудителя к соответствующему препарату.
Развитие лекарственной резистентности у клинических штаммов микроорганизмов к известными классам антимикробных веществ резко снижает эффективность терапии или делает ее безрезультатной.
Сложной проблемой является лечение тяжелых и хронических форм УГИ, с локализацией инфекции в тканях почки, гениталий, органов малого таза. При гнойных процессах в почках следует учитывать возможность возникновения бактериемии и уросепсиса. Существенные трудности могут быть связаны с терапией инфекций, вызванных хламидиями и микоплазмами, туберкулеза почек, микотической и вирусных инфекций, особенно при их сочетании с инфекцией, вызванной условно-патогенными бактериями, N. gonorrhoeae, H. ducreyi, анаэробными микроорганизмами.
Фторхинолоны (ФХ; введены в клиническую практику в начале 80-х годов) – большая группа антимикробных препаратов в пределах класса хинолонов, которые хорошо известны также (исходя из основной мишени действия в микробной клетке) под названием “ингибиторы ДНК-гиразы”. Введение фтора в положение 6 хинолонового цикла и других строго определенных дополнительных структур в молекулу хинолона (или аналога, например нафтиродона) позволило получить высокоэффективные антимикробные препараты. Общая характеристика ФХ подробно рассматривается в ряде монографий и обзоров, а широкая клиническая практика подтверждает их высокую клиническую эффективность. Различия между ФХ (6-фторхинолонами) и нефторированными препаратами класса хинолонов приведены в таблице 1; соответственно определяются преимущества именно ФХ.
По своим свойствам ФХ удовлетворяют большинству требований, предъявляемым к препаратам для лечения УГИ.
ФХ характеризуются широким антибактериальным спектром действия, однако он не включает всех возможных возбудителей УГИ; и это необходимо иметь в виду при применении ФХ для лечения УГИ.
ФХ характеризуются высокой бактерицидной активностью. Это обеспечивают в большинстве случаев высокий терапевтический эффект по клиническим и, что особенно важно, по бактериологическим показателям.
Фармакокинетические свойства ФХ (высокие сывороточные концентрации и хорошее проникновение в органы и ткани) определяют показания к применению препаратов практически при любой локализации инфекционного процесса. ФХ обеспечивают высокие концентрации препаратов в системе мочевыводящнх путей и в тканях гениталий (равные или превышающие сывороточные концентрации). Высокая биодоступность ФХ при применении внутрь позволяет в большинстве случаев получить терапевтический эффект только при перооральном применении, а достаточно медленное выведение из организма – применять препараты два или даже один раз в сутки, что крайне важно для амбулаторной практики. Хорошее проникновение ФХ в клетки фагоцитарной системы обеспечивает эффективность препаратов при инфекциях, вызванных возбудителями с внутриклеточной локализацией.
Основное преимущество ФХ и значение для клиники имеет их активность в отношении штаммов бактерий, резистентных к антибактериальным препаратам других фармакологических групп. Необходимо отметить, что нефторированные хинолоны (налидиксовая, оксолиновая, пипемидовая кислоты и некоторые другие препараты) эффективны в отношении ряда возбудителей бактериальных ИМВП и ЗППП и применяются до сих пор в урологической практике. Однако к этим препаратам достаточно быстро может развиваться лекарственная резистентность. Фторхинолоны, несмотря на перекрестный характер устойчивости в пределах класса хинолонов (общий механизм действия на микробную клетку), благодаря значительно более высокой бактерицидной активности в большинстве случаев преодолевают уровень этой устойчивости и оказывают эффект при инфекции, вызванной резистентными к нефторированным хинолонам штаммами.
К ФХ относительно медленно развивается лекарственная резистентность. За последнее время отмечают повышение частоты выделения резистентных к ФХ клинических штаммов бактерий, однако эта проблема при лечении УГИ пока не приобрела клинического значения. Вместе с тем, необходимо обратить внимание на возможность снижения активности ФХ в отношении P. aeruginosa и полирезистентньк штаммов стафилококков, особенно штаммов, устойчивых к оксациллину и метициллину.
В настоящее время в клинической практике в России и за рубежом наиболее широко применяются пять препаратов группы ФХ (монофторхинолоны) – норфлоксацин (НОР), пефлоксацин (ПФЛ), ципрофлоксацин (ЦФЛ), офлоксацин (ОФЛ) и ломефлоксацин (ЛФЛ). Обосновано рассмотреть антимикробные и фармакокинетические свойства именно этих препаратов с точки зрения применения при УГИ.
Все эти ФХ характеризуются высокой активностью в отношении N. gonorrhoeae и большинства Enterobacteriaceae, и в первую очередь в отношении Е. соli (основного возбудителя ИМВП), активны в отношении P. aeruginosa и S. aureus. ФХ сохраняют высокую активность в отношении штаммов бактерий, устойчивых к нефторированным хинолонам.
Некоторые ФХ достаточно высоко активны в отношении хламидий, микоплазм, проявляют активность в отношении микобактерий туберкулеза.
Наиболее высокую активность in vitro в отношении грамотрицательных бактерий проявляет ЦФЛ, в отношении грамположительных – ЦФЛ и ОФЛ. В отношении ряда штаммов активность всех пяти препаратов может быть сопоставима. Наиболее существенны различия в активности в отношении P. aerugmosa. В отношении хламидий и микоплазм наиболее активны ОФЛ и ЛФЛ, по действию на М. tuberculosis наиболее выраженной активностью характеризуются ОФЛ, ЦФЛ и ЛФЛ.
Необходимо отметить недостаточно высокую активность ФХ в отношении гарднерелл (факультативные анаэробы), что может быть существенно при лечения бактериальных вагинозов, и в отношении анаэробных бактерий, которые могут быть причиной инфекции при ГВЗ малого таза (в частности пельвиоперитонита) и случаях гнойной инфекции почек (абсцесс, карбункул почки, послеоперационный гнойный процесс).
ФХ неактивны в отношении возбудителя сифилиса, трихомонад, условно-патогенных и патогенных грибов и вирусов. Вместе с тем, ФХ хорошо совмещаются с химиотерапевтическими препаратами, применяющимися при этих заболеваниях, и, в случаях смешанных инфекций, могут быть применены в комбинированной терапии.
Наиболее важные с точки зрения УГИ параметры фармакокинетики рассматриваемых ФХ представлены в табл. 2.
ЦФЛ, ОФЛ, HOP, ПФЛ, ЛФЛ достаточно медленно выводятся из организма, поэтому назначаются два или даже один раз в сутки. Элиминация ОФЛ и ЛФЛ осуществляется преимущественно почечным путем, причем при минимальной трансформации в организме; элиминация ПФЛ – главным образом, внепочечными механизмами (за счет транформации в печени с образованием основного метаболита НОР (до 55%)), ЦФЛ и НОР элиминируют по смешанному типу – почечными и внепочечными механизмами. Все пять препаратов, независимо от пути элиминации при ненарушенной функции почек, обеспечивают в терапевтических дозах очень высокие концентрации в моче и в ткани почек; концентрация в тканях и жидкостях гениталий варьирует в зависимости от физико-химических свойств и липофильности препаратов. Наибольшие преимущества с точки зрения концентрации в тканях гениталий имеют ОФЛ и ЛФЛ; это обстоятельство для клинического эффекта наиболее существенно в случаях инфекционных процессов, вызванных возбудителями с внутриклеточной локализацией – хламидиями и микоплазмами, а также стафилококками. Подчеркивают хорошее проникновение всех ФХ в ткань простаты и в семенную жидкость, где концентрация препаратов соответствует или превышает их концентрацию в плазме крови, составляя 100–400% от концентрации в плазме. В простатической жидкости эта концентрация составляет 10–50% от концентрации в плазме при наиболее высоком уровне у ЛФЛ. При инфекции, вызванной энтеробактериями, в частности кишечной палочкой, все пять ФХ обеспечивают необходимый терапевтический уровень при ИПО, что подтверждает высокая эффективность НОР и других ФХ при бактериальных простатитах.
Различие в механизмах элиминации ФХ необходимо иметь в виду при нарушении выделительной функции почек. Как видно из табл. 2, выведение из организма ОФЛ и ЛФЛ в этом случае резко замедляется (увеличение показателей Т1/2 и фармококинетической кривой (AUC)), что требует снижения разовых доз препаратов или увеличения интервалов между приемами. Практически не изменяется процесс элиминации ПФЛ, и коррекция его доз может быть необходима только при тяжелом нарушении функции почек, это же относится к ЦФЛ и НОР, учитывая характерный для препаратов смешанный механизм элиминации. Коррекция доз ПФЛ необходима при нарушении функции печени.
Концентрация всех пяти ФХ в моче при применении рекомендуемых терапевтических доз и схемах лечения значительно превышает не только величины минимальной подавляющей концентрации (МПК) чувствительных к ФХ возбудителей, но и бактерицидные концентрации. Поэтому различие в степени активности in vitro между отдельными препаратами при лечении инфекций нижних мочевыводящих путей, вызванных условно-патогенными бактериями, не существенно.
Эффективность антимикробного препарата в инфицированном организме зависит от того, насколько его концентрация в сыворотке и очаге инфекции превышает величину МПК возбудителя, и как длительно сохраняется это превышение. Важным показателем, позволяющим прогнозировать эффективность, является отношение площади под AUC к величине МПК, которое варьирует в зависимости от чувствительности возбудителя к препарату. Чем выше данный индекс, тем выше антимикробный эффект in vitro.
1) свойствами самих препаратов – высокой бактерицидной активностью, достаточно длительным постантибиотическим эффектом (ПАЭ), что облегчает фагоцитарную активность в отношении клеток, не восстановивших способность к делению, и высокими концентрациями в жидкостях и тканях организма, в том числе в урогенитальном тракте;
2) величиной разовой дозы при условии строгого контроля за интервалами дозирования (обеспечивается необходимый уровень максимальной концентрации, оптимальная величина AUC и, при чувствительности возбудителя, высокие значения показателя AUC/МПК).
Показания к применению ФХ при эмпирической терапии бактериальных ИМВП (исходя из вероятных возбудителей) представлены в табл. 3.
При неосложненных ИМВП могут быть применены все ФХ, причем препараты высокоэффективны при применении только внутрь. Курс лечения варьирует от 3 до 5–7 дней.
При осложненных ИМВП и ненарушенном оттоке мочи показано применение ФХ в монотерапии, как правило, также только внутрь.
При тяжелых формах пиелонефрита, в случаях гнойной инфекции почек, т.е. при госпитальной ИМВП, особенно при инфекции, вызванной P. aerugnosa или полирезистентными штаммами других микроорганизмов, необходимо начинать терапию с внутривенного введения ФХ – ЦФЛ, ОФЛ или ПФЛ, при улучшении клинического состояния больного, с учетом бактериологических данных, переходить на применение ФХ внутрь, т.е. проводить ступенчатую терапию. При этом, если отсутствует пероральная лекарственная форма ФХ, который применялся внутривенно, для перорального применения может быть применен ЛФЛ или НОР. Те же схемы ступенчатой терапии могут быть рекомендованы в случаях развития бактериемии или уросепсиса.
Эффективность ФХ при ИМВП высокая, в том числе и при осложненных формах заболевания, при условии ненарушенного оттока мочи.
Все ФХ высокоэффективны при лечении острой неосложненной гонореи и мягкого шанкра в случаях моноинфекции в однократной дозе или при коротких курсах лечения: эффективность 90–100%.
При осложненной гонорее, хронических формах заболевания, смешанной гонорейно-хпамидийной инфекции необходимы более длительные курсы лечения ФХ (7–14 дней, иногда до 3–4 недель).
При хламидийной УГИ наиболее эффективен ОФЛ. Опыт отечественных клиницистов показывает высокий лечебный эффект ЛФЛ при урогенитальном хламидиозе.
При ГВЗ малого таза и послеродовых эндометритах, когда высока вероятность смешанной аэробно-анаэробной инфекции ФХ (ОФЛ,ЦФЛ И ЛФЛ) следует применять в комбинированной терапии с антианаэробными препаратами. Большинство наблюдений касается применения ФХ с нитроимидазолами (в частности с метронидазолом). Препараты этих классов химиотерапевтических веществ хорошо сочетаются.
При бактериальных вагинозах, учитывая полимикробный характер процесса, этиологическую роль анаэробных микроорганизмов и слабую активность ФХ в отношении анаэробов, обосновано применение антианаэробных препаратов или комбинированная терапия этими препаратами с ФХ. Имеются наблюдения по применению ЦФЛ, ОФЛ в монотерапии при бактериальных вагинозах, показывающие недостаточную эффективность ФХ.
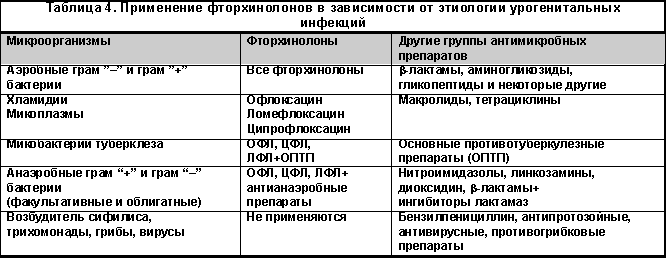
Анализируя возможность применения ФХ в терапии УГИ, следует подчеркнуть, что все препараты этой группы, в том числе рассматриваемые ЦФЛ, ОФЛ, ПФЛ, НОР, ЛФЛ эффективны при лечении инфекции, вызванной условно-патогенными аэробными бактериями (табл. 4). При сравнении с b-лактамами следует иметь в виду высокую активность ФХ при пероральном применении и более высокую степень проникновения ФХ в ткани гениталий, в частности, в ткань простаты. При сравнении с аминогликозидами преимущество ФХ несомненно с точки зрения существенно лучшей переносимости, а также эффективности при приеме внутрь. В случаях инфекции, вызванной полирезистентными штаммами стафилококков, в том числе устойчивыми к ФХ, и штаммами энтерококков фторхинопоны уступают в эффективности гликопептидам. При острых неосложненных инфекциях нижних мочевыводящих путей сопоставимыми по эффективности с фторхинолонами при бактериальной инфекции могут быть производные нитрофурана (нитрофурантоин). При осложненных ИМВП, в частности осложненных пиелонефритах, хронических процессах, вызванных резистентными возбудителями, преимущество будет на стороне ФХ.
При хламидийной и микоплазменной инфекциях могут быть применены с хорошим клиническим эффектом ОФЛ, ЛФЛ и ЦФЛ. Большинство клиницистов наиболее эффективным препаратом считают ОФЛ; это соответствует и международным рекомендациям.
На основании применения ФХ в комплексной терапии осложненных лекарственно-устойчивых форм туберкулеза легких и костного туберкулеза обосновано в комплексе с противотуберкулезными препаратами применить ФХ в случаях туберкулеза почек, хотя к настоящему времени клинический опыт при этой патологии очень невелик. В качестве препаратов второй линии при осложненных формах туберкулеза из ФХ наиболее целесообразны ОФЛ, ЦФЛ или ЛФЛ.
ФХ неэффективны и не должны применяться для лечения сифилиса, трихомонадной инфекции, микозов и вирусных инфекций урогенитального тракта.
Следует подчеркнуть в целом хорошую переносимость ФХ больными. Важным свойством препаратов является отсутствие нефро-, гепато- и ототоксического действия. Учитывая, что ФХ достаточно часто применяются в амбулаторной практике, в том числе и у больных, которым не показан постельный режим, необходимо предупреждать пациентов о возможном фототоксическом эффекте (развитие фотодерматоза) и запрещать во время терапии ФХ и еще в течение 2–3 дней после окончания приема препаратов пребывание на солнце или УФ-облучение.
ФХ относятся к группе важнейших высокоэффективных антимикробных препаратов, составляя серьезную альтернативу антибиотикам широкого спектра действия. Их применение строго по показаниям с учетом чувствительности возбудителя позволит надолго сохранить значение ФХ для химиотерапии инфекционных заболеваний. В амбулаторной практике при неосложненных ИМВП и бактериальных простатитах наиболее показано применение норфлоксацина. При осложненных пиелонефритах, тяжелых формах ИПО и ГВЗ малого таза для перорального применения показаны ципрофлоксацин, офлоксацин, ломефлоксацин. При госпитальной УГИ, когда необходима парентеральная терапия, применяют ципрофлоксацин или офлоксацин.
| Приложения к статье |

| Рисунок 1. Общая схема заболеваний урогенитального тракта в зависимости от локализации и возбудителя инфекции |
| Развитие лекарственной резистентности микроорганизмов делает терапию антибиотиками безрезультатной |

| Фторхинолоны высокоэффективны только при пероральном применении |

| Фторхинолоны высокоэффективны при лечении острой неосложненной гонореи и мягкого шанкра |









.gif)



