Подходы к рациональной терапии любого инфекционного заболевания, в том числе и инфекций мочевыводящих путей, – сложный и многоступенчатый процесс, который, как показывает клиническая практика, никогда не может быть решен окончательно. Это обусловлено тем, что прогресс фармакологии и других разделов биомедицинской науки предлагает врачу, с одной стороны, постоянно обновляющийся перечень препаратов для терапии инфекций, с другой – новые сведения об эффективности и безопасности уже существующих режимов терапии. Обновление такой информации особенно актуально для антимикробных препаратов в силу изменения их активности по отношению к возбудителям инфекций.
Несмотря на то, что в мире выполнено достаточно большое количество исследований по изучению резистентности разных форм ИМП к антимикробным препаратам (АП), использовать напрямую данные подобных исследований в России, а тем более в отдельных регионах России, нельзя. Такое ограничение обусловлено прежде всего значительными отличиями в чувствительности уропатогенов к АП в разных странах. Например, частота выделения уропатогенной кишечной палочки, резистентной к ко–тримоксазолу в Европе, между отдельными странами может отличаться в несколько раз. В связи с этим для рационального выбора антибактериальной терапии ИМП необходимо использовать локальные данные по устойчивости уропатогенов [6,7]. Москва представляет собой уникальный город Российской Федерации с целым рядом демографических, социальных и экономических особенностей, которые могут существенно повлиять на этиологическую структуру, и особенно на резистентность возбудителей ИМП. В связи с этим характеристика внебольничных ИМП в крупнейшем мегаполисе Российской Федерации представляет крайне важную научную и практическую задачу.
Прежде всего при планировании исследования мы принимали во внимание, что, по самым скромным подсчетам, в Москве проживает не менее 12 миллионов человек, поэтому для репрезентативной эпидемиологической характеристики амбулаторных ИМП был выбран дизайн многоцентрового исследования, позволяющего оценить состояние в нескольких географических точках города. В исследовании принимали участие 8 лечебно–профилактических учреждений г. Москвы. Клиническая часть настоящей работы выполнена на базе лечебных учреждений г. Москвы: муниципальное лечебно–профилактическое учреждение (МЛПУ) п–ка № 20 (Горлов Тупик, д. 4), МЛПУ п–ка № 37 (ул. Иерусалимская, д. 4), МЛПУ п–ка № 51 (Б. Татарский пер., д. 4), МЛПУ п–ка № 68 (ул. Б. Ордынка, д. 34), МЛПУ п–ка № 104 (ул. Воронцовская, д. 14/14), МЛПУ п–ка № 171 (1–й Зачатьевский пер., д. 1/15), МЛПУ п–ка № 42 (Шмитовский пр–д, д. 25).
Другой особенностью настоящего исследования была реализация принципа получения максимального количества клинической информации о пациенте, что позволяло охарактеризовать инфекцию, выявить факторы риска, возможную предшествующую антибактериальную терапию, исключить нозокомиальную природу инфекций, оценить проводимую антибактериальную терапию. В исследование включали пациентов с внебольничными ИМП в соответствии со следующими критериями: возраст старше 18 лет, наличие клиники ИМП, пациенты с амбулаторными ИМП, бактериологически подтвержденный диагноз ИМП (выделение возбудителя из мочи в диагностическом титре).
Реидентификация микроорганизмов и постановка чувствительности к антибиотикам выполнялась на базе бактериологической лаборатории (зав. – к.м.н. О.И. Кречикова) НИИ антимикробной химиотерапии ГОУВПО СГМА Росздрава. Идентификацию микроорганизмов до рода и вида проводили с помощью рутинных биохимических тестов. Исследование чувствительности проводилось количественным методом путем определения минимальной подавляющей концентрации (МПК) антибиотиков для каждого микроорганизма. Для определения МПК антибиотиков применялся метод разведения в агаре Мюллер–Хинтон (BBL, США) в соответствии с методикой NCCLS. Определение МПК и интерпретацию результатов проводили в соответствии с рекомендациями и критериями NCCLS, 2002. При характеристике микроорганизмов использовались общепринятые критерии – «чувствительные», «умеренно–резистентные» и «резистентные». Контроль качества определения чувствительности проводился параллельно с тестированием исследуемых возбудителей с помощью контрольных штаммов АТСС, рекомендованных NCCLS: E. coli ATCC 25922, E. coli ATCC 35218, P. aeruginosa ATCC 27853.
Всего в исследование было включено 170 пациентов, средний возраст которых составил 54,7±18,6 года. Основные нозологические формы, выявленные у амбулаторных пациентов с ИМП, распределились следующим образом: острый цистит или обострение хронического цистита – 49,1% случаев, хронический и острый пиелонефрит – 39,8% и 5,3% случаев соответственно. В 5,8% случаев диагноз уточнить было невозможно.
Частота выявления осложненных форм ИМП составила 37,6% и достоверно не отличалась от частоты выявления неосложненных форм ИМП – 38,8%. Пациенты с осложненными ИМП были в 1,82 раза старше, чем пациенты с неосложненными формами заболевания – 65,6±12,7 и 36,0±10,6 лет соответственно. Наиболее часто регистрировались мочекаменная болезнь и сахарный диабет – 48,5% и 24,2% случаев соответственно, реже выявлялись кисты почек – 7,6%, инфравезикальная обструкция – 6,1%, состояние после нефрэктомии – 3,0% и др.
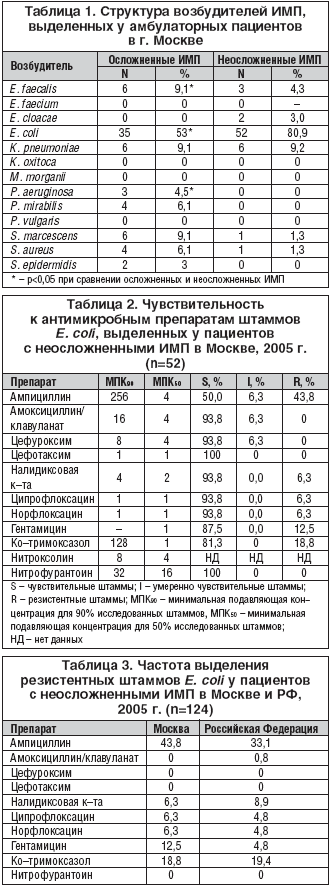
Установлено, что возбудителями как неосложненных, так и осложненных форм амбулаторных ИМП в г. Москве являются в основном представители семейства Enterobacteriaceae. Наиболее частым уропатогеном является E. coli, которая встречалась у 80,9% пациенток с неосложненными и 53% с осложненными ИМП. Другие микроорганизмы выявлялись значительно реже. Так, при неосложненных ИМП K. pneumoniae выделялась у 9,2%, E. faecalis у 4,3%, E. cloacae у 3,0%, S. marcescens у 1,3% и S. aureus у 1,3% пациентов (табл. 1). При осложненных ИМП K. pneumoniae выделялась в 9,1%, P. mirabilis – 6,1%, S. marcescens – 9,1%, E. faecalis – 9,1%, S. aureus – 6,1%, P. aeruginosa – 4,5%. При осложненных ИМП по сравнению с неосложненными формами достоверно реже выделялась E. coli (53% и 80,9%, p<0,05) и достоверно чаще P. aeruginosa (4,5% и 0%, p<0,05) и E. faecalis (9,1% и 4,2%, p<0,05). Таким образом, в структуре возбудителей при осложненных ИМП по сравнению с неосложненными формами, снижается доля E. coli и возрастает роль грам (+) кокков и синегнойной палочки.
В связи с тем, что E. coli является наиболее распространенным возбудителем как неосложненных, так и осложненных ИМП, определение чувствительности этого уропатогена представляет наибольший интерес, а полученные данные и являются основой для дальнейшего проведения эмпирической антимикробной терапии.
Данные по чувствительности E. coli, выделенной от пациентов с неосложненными ИМП в 2005 г. в г. Москве, представлены в таблице 2. Обращает на себя внимание высокая частота выделения резистентных штаммов E. сoli к ампициллину – 43,75%. Штаммов, устойчивых к амоксициллину/клавуланату, цефалоспоринам II (цефуроксим) и III (цефотаксим) поколений, нитрофурантоину обнаружено не было. Анализ резистентности E. coli к гентамицину выявил, что частота выделения устойчивых штаммов достаточно высока и составляет 12,5%. Уровень резистентности E. coli к ко–тримоксазолу составил 18,8%. Резистентность уропатогенных штаммов E. coli, выделенных от пациентов с неосложненными ИМП, к налидиксовой к–те и фторхинолонам (норфлоксацин и ципрофлоксацин) составила 6,3%.
Полученные в исследовании данные достаточно хорошо коррелируют с результатами исследования структуры возбудителей и их резистентности по России в целом (табл. 3) [8]. Также как и в других российских городах (Владивосток, Казань, Нижний Новгород, Санкт–Петербург, Смоленск, Челябинск), основным возбудителем внебольничных ИМП является E. coli. Выявлено только одно принципиальное отличие в частоте выделения резистентных уропатогенов в г. Москве от общероссийских данных, а именно – более высокий уровень резистентности E. coli к гентамицину (12,5%) по сравнению с общероссийским уровнем (4,8%). Характерно, что в 1998 г частота выделения уропатогенной E. coli к гентамицину в г. Москве была достоверно ниже и составляла 1,9%. Вероятно, такой прирост резистентности связан с особенностями применения антибиотиков в г. Москве, прежде всего в амбулаторных условиях [9].
Выводы
1. Первое место среди амбулаторных форм инфекций мочевых путей в г. Москве занимает цистит – 49,1%, второе – хронический пиелонефрит – 39,8%, третье – острый пиелонефрит – 5,3% всех случаев ИМП. Неосложненные и осложненные формы ИМП встречаются одинаково часто – 37,6% и 38,8% соответственно. Самыми частыми осложняющими факторами являются мочекаменная болезнь – 48,5% и сахарный диабет – 24,2%, реже встречаются кисты почек – 7,6%, инфравезикальная обструкция – 6,1% и др.
2. Основным возбудителем амбулаторных ИМП в г. Москве является E. coli – 72,5% всех случаев инфекции. E. coli достоверно реже (p<0,05) выделяется при осложненных ИМП (53%), чем при неосложненных формах (80,9%). При осложненных ИМП достоверно чаще (p<0,05), чем при неосложненных, выделяли P. aeruginosa – 4,5% и 0% и E.faecalis – 9,1% и 4,2%.
3. В г. Москве отмечается высокий уровень резистентности E. coli, выделенной у пациентов с неосложненными ИМП, к ко–тримоксазолу – 28,7% и ампициллину – 39,1%, низкий – к амоксициллину/клавуланату – 6,3%, фторхинолонам – 6,3%, цефуроксиму – 6,3%, нитрофурантоину – 0%, цефотаксиму – 0%, фосфомицину – 0%.
4. В силу повышения уровня резистентности E. coli к гентамицину за последние 7 лет с 1,9% до 12,5% не рекомендуется использовать этот препарат для эмпирической терапии ИМП. Для терапии внебольничных ИМП в стационарах г. Москвы гентамицин рационально назначать только после определения чувствительности к нему возбудителей ИМП.
Литература
1. National Institutes of Health. The National Kidney and Urologic Diseases Advisory Board 1990 Long–Range Plan. Window on the 21st Century. Bethesda: National Institutes of Health, publication number 90–583, 1990.
2. Mazzulli T. J. Resistance trends in urinary tract pathogens and impact on management. Urol 2002; 168 (4 Pt 2): 1720–2.
3. Romanenkova O., Rafalskiy V., Chemesov S. et al. Epidemiology of acute cystitis: the first Russian multicenter study. 5th European congress of chemotherapy and infections, 1–4 April 2006, Nice, France.
4. IMS antibiotic prescription data 1999. Plymouth Landing (PA): IMS Health, 1999
5. Сидоренко С.В., Иванов Д.В. Результаты изучения распространения антибиотикорезистентности среди возбудителей внебольничных инфекций мочевыводящих путей в Москве. Фаза I // Антибиотики и химиотерапия : ежемесячный научно–практический журнал.– 2005.– Том 50.– N 1.– С. 3–10.
6. Kahlmeter G. An International Survey of the Antimicrobial Susceptibility of pathogens from Uncomplicated Urinary Tract Infections: the ECO–SENS Project // J Antimicrob. Chemother.– 2003.– N. 51.– P. 69–76.
7. Karlowsky J.A., Kelly L.J., Thornsberry C., Jones M.E., Sahm D.F. Trends in antimicrobial resistance among urinary tract infection isolates of Escherichia coli from female outpatients in the United States // Antimicrob. Agents Chemother.– 2002.– N. 46.– P. 2540–5.
8. Рафальский В.В., Страчунский Л.С., Бабкин П.А., Валенская В.С., Габбасова Л.А., Дмитриева О.Б. и др. Резистентность возбудителей неосложненных инфекций мочевых путей в России // Урология.– 2006.– №5.– С. 34–37.
9. Рохликов И.М. Клинико–микробиологическая и фармакоэпидемиологическая характеристика внебольничных инфекций мочевыводящих путей в г. Москве // Автореф. дис. канд. мед. наук.– Смоленск, 2006.– 24 с.












