А.В. Говоров, А.В. Бормотин, профессор Д.Ю. Пушкарь
МГМСУ им. Н.А. СемашкоПрофессор И.И. Бабиченко
РУДН, МоскваДиагностика опухолей и опухолеподобных процессов предстательной железы является важной онкоурологической проблемой. Эти состояния, как правило, отражают изменения железистого компонента простаты. Секреторный эпителий желез вырабатывает простатспецифический антиген (ПСА), который обнаруживается в крови как у здоровых мужчин, так и при развитии патологических процессов. ПСА относится к семейству калликреиновых serine–протеаз и является химотрипсинподобной гликопротеазой [6]. Ген ПСА имеет участок с определенной гомологичной последовательностью для андрогенов, в связи с чем биосинтез ПСА–белков контролируется действием андрогенов через андроген–рецепторы эпителиальных клеток желез простаты [3,7]. Считают, что андрогены непосредственно регулируют транскрипцию гена ПСА [4,5]. Синтезируемый ПСА поступает непосредственно в кровяное русло, где находится в свободном и связанном состояниях.
Концентрация ПСА в крови является наиболее важным биомаркером патологических состояний в предстательной железе. Считается, что увеличение концентрации общего ПСА в крови более 4 нг/мл (а у пациентов моложе 60 лет более 3 нг/мл) является неблагоприятным фактором. Однако подобное увеличение концентрации нередко происходит и при заболеваниях неопухолевой природы. В связи с этим решение проблемы дифференциальной диагностики предопухолевых состояний и рака предстательной железы требует выработки специфических критериев для оценки ПСА, как опухолевого маркера [1,2,6]. В настоящее время в клинической практике широко используется определение концентраций свободного и общего ПСА в крови и их соотношение. Особенно это важно для ранней диагностики рака предстательной железы, выбора тактики лечения и последующего терапевтического контроля.
В настоящем исследовании была проведена корреляция между концентрацией ПСА сыворотки крови пациентов и иммуногистохимическими особенностями его локализации в опухолях и опухолеподобных процессах предстательной железы человека на разных стадиях онкогенеза.
Материалы и методы
Исследование проводилось у 92 больных мужчин в возрасте 61–86 лет с патологией опухолевой и псевдоопухолевой природы, поступивших для лечения в урологическое отделение Госпиталя ветеранов войн № 2. У 33 мужчин была выявлена доброкачественная гиперплазия предстательной железы (ДГПЖ), у 6 человек диагностирована простатическая интраэпителиальная неоплазия (ПИН) низкой степени, в 9 случаях выявлена простатическая интраэпителиальная неоплазия высокой степени. У 44 пациентов был диагностирован рак предстательной железы (РПЖ). До определения уровня ПСА пациенты никакого лечения не получали. Контрольную группу для исследования сывороточного ПСА составляли 8 мужчин без неопластической патологии. В качестве контроля при проведении иммуногистохимической реакции использован секционный материал предстательной железы, полученный от 5 мужчин среднего возраста.
Концентрация общего и свободного ПСА определялась в образцах сыворотки крови при помощи иммуноферментного анализа (Enzymun–Test PSA, « Boehringer Mannheim»). Определение концентраций фракций ПСА проводили на автоматическом иммуноферментном анализаторе ES 300 («Boehringer Mannheim»).
Гистологические образцы в 51 случае получали с помощью биопсии простаты, в 10 – после трансвезикальной простатэктомии, в 31 случае – посредством трансуретральной резекции простаты. Полученный материал фиксировали в 10% забуференном формалине, заливали в парафин. Срезы окрашивали гематоксилином и эозином. Выявление тканевого ПСА проводили с помощью авидин–биотинового метода, в котором биотинилированные вторичные антитела реагируют с соответствующими молекулами пероксидазно–коньюгированного стрептовидина. При постановке иммуногистохимической реакции использовали универсальный DAKO LSAB + Kit, пероксидазный (DAKO CORPORATION USA). В качестве первичных и вторичных иммунных сывороток использовали моноклональные мышиные сыворотки к ПСА в рабочем разведении. В качестве негативного контроля иммуногистохимической реакции использовали нормальную неимуннную мышиную сыворотку. При оценке иммуногистохимической реакции учитывали характер иммунопреципитата (отдельные коричневые зерна; зерна, сливающиеся в комочки), локализацию их в клеточных структурах, в секрете полости желез, количество окрашенных клеток в железе, количество прореагировавших желез. В зависимости от этого характер экспрессии оценивали по 3–балльной шкале на 300 клеток.
Для оценки гистологического материала использовали шкалу Глисона (1974) с определением градации гистологического типа опухоли. Таким образом у 8 человек выявлена аденокарцинома с суммарной оценкой по Глисону менее 4 баллов, у 23 человек суммарная оценка степени злокачественности составляла 5–7 баллов, у 13 человек суммарная оценка была 8–10 баллов.
Результаты исследования
При сравнительном исследовании ПСА в сыворотке крови исследуемых мужчин выявлено достоверное увеличение концентрации свободного и общего ПСА у больных ПИН высокой степени и раком простаты по сравнению с контрольной группой и доброкачественной гиперплазией предстательной железы (табл. 1).
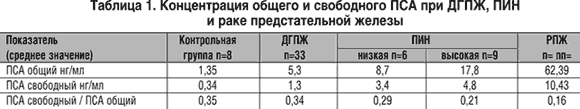
При анализе концентрации свободного ПСА в сыворотке крови отмечается повышение концентрации в группе больных раком простаты (среднее значение 10,43 нг/мл) по сравнению с контрольной группой (0,54 нг/мл) и ДГПЖ (1,3 нг/мл).
Полученные показатели концентраций свободного и общего ПСА могут свидетельствовать о нарушениях способности секреторных клеток к восприятию действия андрогенов и соответствующей продукции ПСА.
При анализе соотношения концентраций свободного и общего ПСА оказалось, что степень увеличения концентрации свободного ПСА в сыворотке больных РПЖ была ниже по отношению к контролю и ДГПЖ соответственно в 30,7 и 8,02 раза, что отражает различие в экспрессии связанных и свободных форм антигенов при злокачественных и доброкачественных процессах. Учитывая, что показатели концентрации общего ПСА в сыворотке крови при доброкачественном и злокачественном процессах иногда совпадают, становится очевидным, что определение соотношения свободного ПСА к общему играет важную роль в диагностике патологического процесса, так как отражает в целом состояние и численность клеточной популяции.
При анализе распределения значений ПСА с учетом гистологической градации в зависимости от степени дифференцирования опухоли установлена зависимость между концентрацией ПСА и степенью дифференцировки (табл. 2).
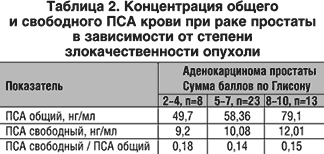
Необходимо также отметить, что при определении концентрации свободного и общего ПСА при аденокарциномах различной гистологической степени у некоторых больных были получены значения, которые не превышали 4 нг/мл, хотя имелись другие клинические признаки ракового процесса. Вероятно, у таких больных в клетках опухоли нарушаются процессы синтеза ПСА, и в этих случаях диагноз ставится по клиническим данным и результатам биопсии простаты.
Так, учитывая недостаточное количество данных о частоте и клинической значимости РПЖ при уровне ПСА от 1 до 4 нг/мл и об использовании соотношения свободный ПСА / общий ПСА для раннего выявления рака простаты, в клинике урологии МГМСУ было обследовано 158 мужчин с соотношением ПСАсвободный / ПСАобщий < 0,20. Всем пациентам была выполнена трансректальная мультифокальная биопсия простаты, по результатам которой диагностировано 17 случаев РПЖ (10,8%) (табл. 3). В одном из 17 случаев по результатам пальцевого ректального исследования определялся очаг уплотнения в ткани простаты.
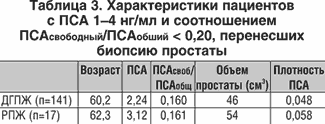
15 пациентам была выполнена радикальная позадилонная простатэктомия. У одного больного обнаружены метастазы в подвздошных лимфатических узлах. У 10 из оставшихся 14 мужчин (71%) показатель Глисона после операции соответствовал таковому после биопсии; у 4 пациентов диагностирована опухоль 7 баллов (3 + 4) по Глисону в образце простатэктомии.
Проведенное исследование показало, что у пациентов с уровнем ПСА от 1 до 4 нг/мл и соотношением ПСАсвободный/ПСАобший < 0,20 рак простаты выявляется в 11% случаев, причем большинство опухолей являются клинически значимыми.
Принимая во внимание полученные данные, а также учитывая наметившуюся во всем мире тенденцию к снижению порогового уровня ПСА, в клинике урологии МГМСУ было изучено влияние снижения порога «нормы» ПСА на выявляемость РПЖ.
В исследовании участвовала группа случайно отобранных мужчин, не предъявляющих урологических жалоб или имеющих минимально выраженную симптоматику, в возрасте от 50 до 76 лет, которые были разделены на две подгруппы. Всем исследуемым определялся уровень общего ПСА радиоиммунным методом. У первой группы пороговое значение показателя ПСА составляло 4 нг/мл, у второй – 3 нг/мл. При превышении пороговых значений выполнялось пальцевое ректальное исследование с последующей трансректальной мультифокальной биопсией простаты по принятой в клинике методике. По результатам исследования был сделан вывод, что уменьшение порогового значения «нормы» ПСА с 4 нг/мл до 3 нг/мл привело к увеличению выявляемого рака предстательной железы на 24%. При этом все опухоли, выявленные в данном исследовании, оказались клинически значимыми.
Таким образом, данные концентраций свободного и общего ПСА в сыворотке крови и их соотношение помогают определить характер патологического процесса в предстательной железе. Снижение порога «нормы» ПСА полезно у относительно молодых мужчин и позволяет рано диагностировать клинически значимые опухоли.
Для определения характера экспрессии ПСА в собственно ткани предстательной железы при разных состояниях было проведено иммуногистохимическое исследование биоптатов и операционного материала.
При иммуногистохимическом исследовании в ткани железы нормального строения в 97–99% желез в цитоплазме клеток секреторного эпителия имелись интенсивно окрашенные в желтый цвет, равномерно распределенные многочисленные гранулы иммунопреципитата. Имеющийся в отдельных железах секрет имел слабое желтоватое окрашивание.
При доброкачественной гиперплазии предстательной железы иммуногистохимически в цитоплазме секреторных эпителиальных клеток желез и протоков в 23 наблюдениях в 70 % желез отмечалась умеренная экспрессия ПСА в виде диффузно расположенных перинуклеарных мелких частиц светло–коричневого цвета, в отдельных кистозно расширенных просветах желез также слабому окрашиванию в желтый цвет подвергался секрет желез. В 8 наблюдениях (криброзная форма) во всех секреторных клетках отмечалась умеренная равномерная положительная реакция в виде коричневых зерен, расположенных по всей цитоплазме клеток. Базальные клетки ПСА не экспрессировали. При аденоматозно–кистозной форме (2 случая) со значительным расширением протоков желез ПСА в цитоплазме клеток эпителия отсутствовал, однако секрет и амилоидные тельца давали слабо положительное окрашивание.
При ПИН экспрессия антигенов ПСА была неоднородной в зависимости от степени ПИН. При ПИН высокой степени в 6 случаях в 70% клеток наблюдалось слабо выраженное накопление ПСА в виде коричневых крупных зерен преимущественно в апикальных областях клеток желез, в 3 случаях в 10% клеток имелось выраженное окрашивание также в апикальной области, в остальных 90% – слабовыраженное окрашивание в виде глыбчатого преципитата в цитоплазме клеток. При ПИН низкой степени наблюдалось некоторое увеличение процентного содержания прореагировавших клеток до 80% по сравнению с ДГПЖ и ПИН высокой степени в виде диффузно расположенных коричневых зерен продуктов реакции, в отдельных клетках расположенных базально.
При исследовании образцов предстательной железы с аденокарциномой разных гистологических типов была обнаружена вариабельность экспрессии ПСА. В опухолях с суммой баллов по Глисону 2–4 в 5 случаях отмечалась выраженная положительная реакция у половины всех рассматриваемых опухолевых клеток большей части желез: желто–коричневый преципитат располагался как в цитоплазме клеток, так и в апикальной ее части. В 3 случаях наблюдалось увеличение интенсивности окраски до темно–коричневого цвета с преимущественно внутриклеточной локализацией с экспрессией до 60% всех опухолевых клеток. Однако даже при одной и той же степени гистологического типа аденокарциномы также выявлена неоднородность распределения и положительного окрашивания опухолевых клеток.
По мере нарастания степени злокачественности при иммуногистохимическом исследовании опухолей с суммой баллов по Глисону 5–7 наблюдалось увеличение количества положительно окрашенных клеток с разной степенью выраженности от 1 до 3 баллов. В 13 случаях мелкие интенсивно окрашенные коричневые гранулы иммунопреципитата выявлялись в цитоплазме 80% опухолевых клеток, местами в отдельных железах сливаясь между собой. В 8 случаях в 70% опухолевых клеток имелось умеренно выраженное желто–коричневое окрашивание зерен преципитата, причем отдельные железы (в частности, криброзные структуры) не подвергались окрашиванию вовсе. В 2 случаях специфического окрашивания не наблюдалось.
При исследовании аденокарцином 8–10 баллов по Глисону выявлены неравномерность и разнообразие содержания продуктов реакции: в 6 случаях экспрессия наблюдалась в 60% опухолевых клеток, иммунопреципитат локализовался главным образом вблизи цитоплазматической мембраны или диффузно в виде отдельных или сливающихся темно–коричневых зерен. В 3 случаях имелось выраженное темно–коричневое окрашивание гранул в цитоплазме почти половины опухолевых клеток. В 2 случаях наблюдалось слабовыраженное окрашивание менее чем половины опухолевых клеток. В 2 случаях окрашивание было в единичных опухолевых клетках. Количество подвергшихся реакции клеток менялось даже в препаратах от одного и того же больного. Кроме этого, с учетом гетерогенности строения опухоли выявлены случаи неоднородного распределения иммунопреципитата в одном и том же случае рака.
Заключение
Таким образом, проведенное исследование подтвердило значимость определения ПСА в крови у мужчин различного возраста. Сывороточный ПСА является биомаркером анапластических состояний предстательной железы. При иммуногистохимическом определении ПСА в ткани простаты выявляется гетерогенность экспрессии ПСА при разных патологических процессах в железе. Выявлена тенденция к увеличению интенсивности окрашивания в зависимости от степени выраженности диспластических изменений. При сравнении полученных результатов с определением ПСА в сыворотке крови прослеживается корреляция этих показателей. Корреляционное увеличение концентрации сывороточного ПСА определяется увеличением либо интенсивности экспрессии ПСА в эпителиальных клетках желез простаты, либо их количества при невысокой интенсивности. Более выраженная и интенсивная (по сравнению с тканью железы нормального строения и доброкачественной гиперплазией) экспрессия наблюдается в аденокарциномах, преимущественно в низкодифференцированных. Однако при сопоставлении сывороточного и тканевого ПСА при доброкачественной гиперплазии предстательной железы имеется определенное несоответствие между уровнем выявленной экспрессии ПСА и концентрацией ПСА в крови. Несомненно, одну из главных ролей в продукции ПСА эпителиальными клетками и попаданием его в кровяное русло играет архитектоника процесса и степень выраженности ангиогенеза. Можно предположить, что по мере нарастания злокачественности процесса происходит активное поступление ПСА из эпителиальных клеток в кровь, что проявляется увеличением его концентрации в крови. При ДПГЖ мы не наблюдаем выраженной перестройки органа с увеличением ангиогенеза. При ПИН высокой степени уменьшение экспрессии ПСА в ткани железы и увеличение концентрации его в сыворотке крови связано, возможно, с тем, что происходит активное вымывание ПСА из секреторного эпителия желез. Наряду с этим отсутствие экспрессии ПСА в ткани при минимальных значениях ПСА в сыворотке крови дает основание предположить существование высокой степени атипии опухолевых клеток с нарушением их фенотипических свойств. Скорее всего, с учетом андрогенового влияния на синтез ПСА эпителиальными клетками, происходит утрата фенотипических особенностей секреторных клеток, т.е. опухолевые клетки перестают быть андрогено–резистентными, что является плохим прогностическим признаком.
Таким образом, полученные данные свидетельствуют, что значение сывороточного ПСА является выражением морфофункциональной сущности эпителиального компонента при разных состояниях предстательной железы. Содержание ПСА в ткани простаты коррелирует со значением ПСА в крови и отражает степень утраты тканевой дифференцировки.
1. Кушлинский Н.Е., Любимова Н.В., Гориловский Л.М. ПСА при раке и доброкачественной гиперплазиипредстательнойжелезы.//Бюл.эксперим.биологии и медицины, 1997.–x.124.– № 9– С. 327–330.
2. Gleason D.F., Mellinger G.T. et al. Prediction of prognosis for prostatic adenocarcinoma by combined histological grading and clinical staging //J.Urol.(Baltimore).–1974.–Vol. 111.–N.1.–P.58–64.
3. Sadar M.D. Androgen–independent induction of prostate–specific antigengene expression viacross–talk between the androgen receptor and protein kinase a signal transduction pathways // J Biol Chem .–1999.–Mar 19;– 274 (12): 7777–83.
4. Sadar M.D., Hussain M., Bruchowsky W. Prostate cancer: molecular bioliogy of early progression to androgen independence // Endocr Relat Cancer. 1, 1999.–Dec; 6(4):487–502.
5. Xue W., Irvine R.A.,Yu M.C. et al. Susceptibility to prostate cancer: interaction between genotypes al the androgen receptor and prostate specificantigen loci // Cancer Res 2000 Feb 15; 60(4):839–41.
6. Young F., Li X, Ellet J., et al. Regions of prostate specific antigen (PSA) promoter confer androgen –independent expression of PSA in prostate cancer cell // J Biol Chem 2000 Dec 29; 275(52): 40486–55.
7. Zhu W., Young C.Y. Androgen–dependent transcriptional regulation of the prostate specific antigen by thyroid hormons 3,5,3–l–triiodthyrosinine // J Androl 2001, Jan–Feb; 22(1): 136–41.












