Для лечения впервые выявленных больных туберкулезом повсеместно используется 1 стандартный режим химиотерапии, состоящий из комбинации основных противотуберкулезных препаратов (изониазид, рифампицин, пиразинамид и этамбутол или стрептомицин), который был закреплен Приказом МЗ РФ от 21 марта 2003 г. [3].
Согласно официальным статистическим данным эффективность лечения впервые выявленных больных туберкулезом в РФ 1 режимом химиотерапии на протяжении последних трех лет остается практически на одном уровне и не имеет тенденции к увеличению. За период с 2003 по 2006 г. прекращение выделения микобактерий туберкулеза (МБТ) у впервые выявленных больных не превышало 73,5%, а закрытие каверн в легких – 63%. При этом летальность больных с деструктивными процессами в легких составляет 14,4%, при этом частота ранних рецидивов – 31,5% [4,5]. Следует отметить, что пациенты с деструктивными процессами в 2006 г. составили 49% от всех впервые выявленных больных туберкулезом легких [5].
В значительной степени низкая эффективность химиотерапии впервые выявленных больных деструктивным туберкулезом легких связана с первичной лекарственной устойчивостью МБТ [6]. По классификации Всемирной Организации Здравоохранения (ВОЗ) выделяют: монорезистентность, устойчивость МБТ к 1 противотуберкулезному препарату, полирезистентность – к 2 и более препаратам (но не к сочетанию изониазида и рифампицина) и множественную лекарственную устойчивость (МЛУ), по крайней мере, к изониазиду и рифампицину [7]. Наиболее неблагоприятной в прогностическом плане является МЛУ. За последние 3 года уровень первичной МЛУ неуклонно нарастает и если она в 2004 г. составляла 8,1%, в 2005 г. – 9,5%, то в 2006 г. уже – 11,4% [5].
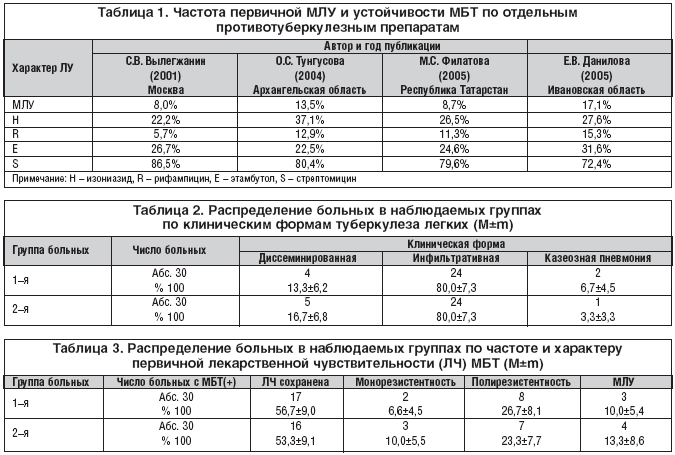
Следует отметить, что при этом первичная МЛУ не отражает лекарственную устойчивость МБТ к отдельным противотуберкулезным препаратам в популяции впервые выявленных больных. В таблице 1 представлены данные контролируемых клинических исследований по изучению первичной МЛУ и устойчивости МБТ у больных деструктивным туберкулезом легких к отдельным противотуберкулезным препаратам, используемым в 1 режиме химиотерапии [8–11].
Как видно из таблицы 1, в представленных регионах РФ МЛУ составляет от 8 до 17%. В различных регионах она представлена по–разному, но факт того, что устойчивость к изониазиду и этамбутолу колеблется от 20 до 30%, к рифампицину – от 6 до 15% и к стрептомицину – от 70 до 90%. Из чего следует, что впервые выявленные больные деструктивным туберкулезом легких являются группой высокого риска развития первичной лекарственной устойчивости, в том числе МЛУ МБТ.
Как указывают эксперты ВОЗ, в регионах, где первичная МЛУ составляет 10% и более, она может стать важной причиной неэффективности лечения и смерти больных, поэтому первоначальный режим химиотерапии должен включать не менее 3 противотуберкулезных препаратов, к которым, вероятно, сохранена чувствительность МБТ. К числу таких препаратов относятся фторхинолоны, аминогликозиды и протионамид [12].
Таким образом, сложившаяся эпидемическая ситуация в РФ и высокий уровень первичной лекарственной устойчивости МБТ ставит под сомнение эффективность 1 стандартного режима химиотерапии впервые выявленных больных деструктивным туберкулезом легких комбинацией изониазида, рифампицина, пиразинамида и этамбутола.
Тем же Приказом МЗ РФ №109 от 21 марта 2003 г. определен 2б режим химиотерапии для больных туберкулезом легких с высоким риском развития лекарственной устойчивости, являющийся приоритетным и обоснованным отечественными учеными [13]. 2б режим состоит из комбинации изониазида, рифампицина, пиразинамида, этамбутола, фторхинолона и канамицина (амикацина). Решающая роль в эффективности 2б режима химиотерапии принадлежит фторхинолонам, которые применяются для лечения туберкулеза с 90–х годов прошлого столетия. Такие препараты, как ципрофлоксацин, офлоксацин, левофлоксацин (Лефокцин и др.), моксифлоксацин и гатифлоксацин, обладают бактерицидным действием на МБТ. При этом у ципрофлоксацина и офлоксацина установлен синергидный и/или аддитивный эффект с рифампицином, изониазидом, пиразинамидом и этамбутолом [14].
С целью повышения эффективности химиотерапии впервые выявленных больных деструктивным туберкулезом легких с выделением МБТ было проведено контролируемое клиническое исследование эффективности 2б режима химиотерапии в сравнительном аспекте с 1 режимом. Под наблюдением находились 60 впервые выявленных больных деструктивным туберкулезом легких с выделением МБТ, установленным методом микроскопии и посева мокроты на питательные среды, в возрасте от 20 до 50 лет (мужчин 39, женщин – 21).
Больные рандомизированы на 2 группы. В 1–ю группу (основную) вошли 30 больных, которым назначался 2б режим химиотерапии. 2–ю группу (контрольную) составили также 30 больных, которые получали 1 режим химиотерапии.
В таблице 2 представлено распределение больных в наблюдаемых группах по клиническим формам туберкулеза легких.
Как видно из таблицы 2, у больных в наблюдаемых группах клинические формы туберкулеза легких были одинаковы. Распростра¬ненность специфических изменений в легких была также примерно одина¬кова. Преимущественной была распространенность специфического процесса в пределах 2 долей легкого (у больных 1–й группы в 53,3%, у 2–й – в 60% случаев). Двухсторонние процессы также встречались с одинаковой частотой у больных 1–й и 2–й группы, соответственно в 33,3 и 36,7% случаев.
Распределение больных в наблюдаемых группах по частоте и характеру первичной лекарственной устойчивости МБТ представлено в таблице 3.
Как видно из таблицы 3, у 43,3% больных 1–й группы и у 46,7% 2–й были выявлены штаммы МБТ, устойчивые к противотуберкулезным препаратам. При этом характер лекарственной устойчивости у больных обеих групп существенно не различался.
Таким образом, в наблюдаемых группах больные были практически идентичны по половым, возрастным и клиническим параметрам, что позво¬лило объективно оценить эффективность 2б и 1 стандартного режима химиотерапии при лечении впервые выявленных больных деструктивным туберкулезом легких с выделением МБТ.
В комбинации 2б режима химиотерапии в качестве фторхинолона был использован левофлоксацин, который зарегистрирован в РФ, как противотуберкулезный препарат с длительностью применения в течение трех месяцев [15]. Данный срок является оптимальным для лечения впервые выявленных больных туберкулезом легких в интенсивной фазе химиотерапии [3].
Сравнительный анализ динамики синдрома интоксикации, клиниче¬ских проявлений и нормализация клинического анализа крови у больных 1–й и 2–й группы показал более высокую эффективность 2б режима химиотерапии, чем использование 1 режима химиотерапии. Через 1 месяц лечения у больных 1–й группы интоксикацион¬ный синдром был полностью купирован в 90,0±5,5% (у 27 из 30 больных). В то время как у больных 2–й группы только у 56,7±9,0% (у 17 из 30) больных, что было соответственно в 1,6 раза меньше по сравнению с больными 1–й группы (р<0,05). К концу третьего месяца лечения синдром интоксикации исчез у всех больных 1–й группы, а у больных 2–й группы у 83,3±6,8% (у 25 из 30), т.е. у больных 2–й группы в 16,7±6,8% случаев (у 5 из 30 больных) синдром интоксикации сохранялся и после трех месяцев химиотерапии.
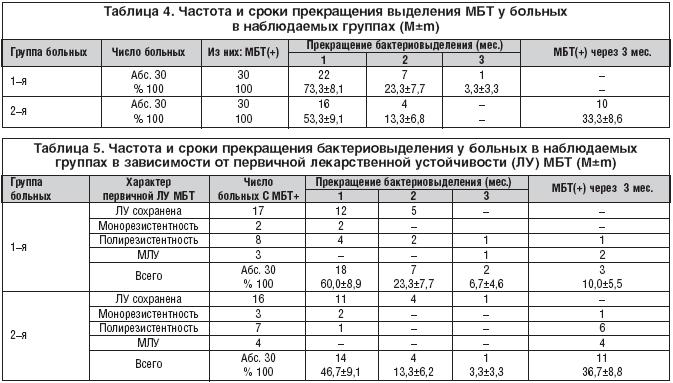
В таблице 4 представлена частота и сроки прекращения выделения МБТ по микроскопии мокроты методом Циля–Нельсена в наблю¬даемых группах.
Как видно из таблицы 4, у больных 1–й группы через 3 месяца лечения прекращение выделения МБТ произошло у всех 30 пациентов. В то время как у больных 2–й группы прекращение бактериовыделения удалось добиться у 66,6% (р<0,05). Необходимо отметить тот факт, что у 10 (33,3%) больных этой группы, продолжающих выделять МБТ, микробиологическими методами посева мокроты на питательные среды установлено формирование вторичной лекарственной устойчивости к большему числу противотуберкулезных препаратов, в том числе у 8 МЛУ.
Таким образом, у впервые выявленных больных деструктивным туберкулезом легких с бактериовыделением применение 2б режима химиотерапии позволяет добиться прекращения выделения МБТ в течение первых 2–3 месяцев практически у всех пациентов, в то время как использование 1 режима химиотерапии у этого контингента больных приводит к положительным результатам менее чем у 2/3 пациентов. 33,3% больных остаются эпидемиологическими опасными выделителями МБТ, переходят в категорию лекарственно–устойчивого туберкулеза, требующего длительного применения резервных противотуберкулезных препаратов и различных методов хирургического лечения.
Частота и сроки прекращения бактериовыделения по методу посева мокроты на питательные среды у больных в наблюдаемых группах в зависимости от первичной лекарственной устойчивости МБТ представлены в таблице 5.
Как следует из таблицы 5, при сохраненной лекарственной чувствительности МБТ прекращения бактериовыделения через 3 месяца лечения удалось добиться в 100% случаев, как у больных 1–й, так и 2–й группы. При монорезистентности эти показатели также существенно не отличались в наблюдаемых группах, соответственно: у 2 больных 1–й группы и у 2 из 3 пациентов 2–й (р>0,05). При полирезистентности МБТ этот показатель существенно различался. У больных 1–й группы с полирезистентностью прекращение выделения МБТ через 3 месяца химиотерапии наступило у 7 из 8 больных (87,5%), а у больных 2–й группы только у 1 из 7 (14,3%) пациентов (р<0,05). При МЛУ МБТ через 3 месяца лечения остались выделителями МБТ 2 из 3 больных 1–й группы и все 4 пациента 2–й.
Следовательно, применение 2б режима химиотерапии у больных впервые выявленным деструктивным туберкулезом легких с выделением МБТ позволяет преодолевать первичную полирезистентность и МЛУ МБТ и существенно повышать эффективность лечения данного контингента.
Побочные реакции на противотуберкулезные препараты у больных 1–й группы установлены у 6 из 30 (20,0±7,3%), а у больных 2–й – у 5 из 30 (16,6±6,8%) (р>0,05). Все побочные явления носили устранимый характер и купировались с применением патогенетических методов лечения. У 4 больных 1–й группы было транзиторное повышение аминотрансфераз и у 2 – аллергические реакции на канамицин. При применении левофлоксацина ни в одном случае не было выявлено неустранимых побочных реакций. У 4 больных 2–й группы было транзиторное повышение аминотрансфераз и у 1 – нейротоксический побочный эффект на прием изониазида. Применение гепатопротекторов и десенсибилизирующих лекарств позволило у больных обеих групп, купировать побочные реакции без отмены назначенной комбинации противотуберкулезных препаратов.
Таким образом, проведенное клиническое исследование эффективности и переносимости 2б режима химиотерапии при лечении больных впервые выявленным деструктивным туберкулезом легких с выделением МБТ показало его высокую эффективность по показателю прекращения выделения МБТ и низкую частоту побочных реакций в интенсивную фазу химиотерапии. Это позволяет рекомендовать его к более широкому применению, особенно в регионах с высоким уровнем первичной МЛУ МБТ.
Литература
1. Рабухин А.Е. Химиотерапия больных туберкулезом. – М. – 1970. – 400с.
2. Хоменко А.Г. Химиотерапия туберкулеза легких. – М. – 1980. – 279 с.
3. Приказ МЗ РФ от 21 марта 2003 года № 109. «О совершенствовании противотуберкулезных мероприятий в Российской федерации». Приложение №6 «Инструкция по химиотерапии туберкулеза». – С. 84–89». – М. – 2003. – 347 с.
4. Шилова М.В. Туберкулез в России в 2005 году. – Воронеж.. – 2006. – 126 с.
5. Ресурсы и деятельность противотуберкулезных учреждений. Основные эпидемиологические показатели за 2005–2006 годы (статистические показатели. – М: ЦНИИОКЗ. – 148 с.
6. Мишин В.Ю. К вопросу об оптимизации химиотерапии больных с впервые выявленным туберкулезом легких. // Клиническая микробиология и антимикробная химиотерапия. – 2002. – Том. 4. – № 1. – С. 4–14.
7. Лечение туберкулеза. Рекомендации для национальных программ. (Перевод с английского). – Всемирная Организация Здравоохранения – Женева. – 1998. – 77 с.
8. Вылегжанин С.В. Инволюция туберкулеза при контролируемой химиотерапии укороченной длительности у впервые выявленных больных туберкулезом легких. // Автореф. дис. … канд. мед. наук. – М. – 2001. – 46 с.
9. Данилова Е.В. Особенности клинического течения и эффективность лечения больных туберкулезом органов дыхания с первичной лекарственной устойчивостью возбудителя: Автореф. … дис. канд. мед. наук. – М. – 2005. – 24 с.
10. Тунгусова О.С. Молекулярно–генетические аспекты развития лекарственной устойчивости в условиях угрозы развития эпидемии туберкулеза в Архангельской области: Автореф. дис. … докт. мед наук. – Архангельск. – 2004. – 34 с.
11. Филатова М.С. Особенности течения и лечения лекарственно–устойчивого туберкулёза лёгких: Автореф. дис. … канд. мед наук. – М. – 2004. – 25 с.
12. Туберкулез выявление, лечение и мониторинг. Вопросы и ответы. Под редакцией Т.Фридена. (Перевод с английского). – Всемирная Организация Здравоохранения. – Женева. – 2004. – 387 с.
13. Мишин В.Ю., Борисов С.Е., Соколова Г.Б. и др. Разработка современных протоколов диагностики и лечения туберкулеза органов дыхания. // Consilium medicum. – 2001. – Том 3. – № 3. – С. 148–154.
14. Berning S. The role of fluorquinolones in tuberculosis today. // Drugs. – 2001. – V. 61. – № 1. – P. 9–18.
15. Справочник Видаль. Лекарственные препараты в России. – АстраФармСервис. – 2007. – С. 1037–1039.












