в терапии ХОБЛ
Тиотропия бромид относится к группе М–холинолитиков. Препарат отличается сверхдлительным (более 24 ч) бронхолитическим эффектом, благодаря которому тиотропий может назначаться 1 р./сут. На сегодняшний день тиотропия бромид является наиболее активным препаратом в ряду холинолитиков: по своей холинолитической активности тиотропиум в 12 раз превосходит атропин и на 20–30% более активен, чем ипратропиум и аклидиниум бромид [1].
Все М–холинолитики являются неселективными препаратами, т.е. они блокируют М–холинорецепторы всех подтипов. При этом блокада М1– и М3–рецепторов способствует расширению бронхов и обеспечивает лечебный эффект препаратов, а блокада M2–рецепторов является нежелательной, т.к. этот подвид холинорецепторов отвечает за торможение сигнала в синапсах. Тиотропия бромид отличает очень кратковременная блокада М2–рецепторов (Т½ связи с M2–рецепторами у тиотропия всего 3,6 ч), в то время как блокада M1 и M3–рецепторов продолжается больше 1 сут. [1].
У больных ХОБЛ основные патологические изменения происходят на уровне мелких периферических дыхательных путей, которые в большей степени повреждаются под воздействием табачного дыма и нейтрофильного воспаления. Причем эти изменения носят необратимый характер. Но наряду с этим больных ХОБЛ отличает повышенный тонус парасимпатической системы, что приводит к сужению крупных бронхов (общее сопротивление дыхательных путей определяется главным образом центральными бронхами, так как их суммарный просвет – около 2 см2 – значительно меньше общего просвета периферических бронхов) и повышению общего сопротивления дыхательных путей [2]. Воздействуя на холинорецепторы центральных бронхов, тиотропиум бромид устраняет влияние парасимпатической нервной системы, крупные бронхи расширяются, а общее сопротивление дыхательных путей – снижается. В итоге уменьшается остаточная емкость легких и увеличивается дыхательный объем. Как следствие, у больных уменьшается одышка, им легче выполнять физические нагрузки [3].
После ингаляции тиотропия бромида величина объема форсированного выдоха за первую секунду (ОФВ1) увеличивается на 150–180 мл (по сравнению с плацебо) или на 103 мл по сравнению с группой контроля, получавшей терапию β2–агонистами и ингаляционными ГКС [4]. Еще в большей степени тиотропиум бромид устраняет так называемую «воздушную ловушку», т.е. уменьшает объем воздуха, который остается в легких больного после максимального выдоха [5]. В результате препарат увеличивает дыхательный объем, уменьшает выраженность одышки, повышает переносимость физической нагрузки [6] и снижает связанную с нагрузкой концентрацию катехоламинов в крови [7].
Положительное влияние тиотропия не ограничивается функцией внешнего дыхания – он значимо (на 38–44%) уменьшает число обострений ХОБЛ [8,9] и на 12–16% – летальность от любых причин у больных ХОБЛ [4,10].
Важно подчеркнуть, что положительное действие тиотропия сохраняется длительное время (в настоящее время наиболее продолжительное исследование этого препарата продолжалось 4 года [4]), в то время как эффекты других бронхолитиков (β2–агонисты длительного действия, например, салметерол) могут заметно уменьшаться при постоянном приеме [11] из–за снижения числа и чувствительности β–адренорецепторов [12].
У больных ХОБЛ тиотропий может назначаться в виде монотерапии, что позволяет существенно (на 27%) снизить риск тяжелых обострений ХОБЛ по сравнению с монотерапией салметеролом (β2–агонист длительного действия) [13]. Результаты метаанализа исследований, в которых применение тиотропия сравнивались с терапией β2–агонистами длительного действия, показали, что тиотропий и β2–агонисты обеспечивают примерно одинаковый прирост величины ОФВ1, но при этом у больных, получавших тиотропий, риск обострений оказался на 14% ниже, а частота нежелательных явлений – на 12% меньше, чем при назначении β2–агонистов (в анализ были включены сравнительные исследования тиотропия с салметеролом, формотеролом и индакатеролом) [14].
При тяжелом течении ХОБЛ, когда требуется комбинация нескольких препаратов, тиотропий можно эффективно сочетать с препаратами других фармацевтических групп. В частности, тиотропий выступает как синергист β2–агонистов длительного действия [15], т.к. на фоне его приема увеличивается чувствительность β–адренорецепторов [16]. В ходе клинических исследований была доказана эффективность комбинации тиотропия с рофлумиластом [17] и комбинированными препаратами, в состав которых входят β2–агонисты и ингаляционные ГКС (будесонид/формотерол) [18].
Респимат® –
ингалятор нового поколения
Тиотропия бромид в виде нового ингаляционного устройства Респимат® (рис. 1) появился в продаже в нашей стране в 2012 году. Этот прибор объединяет в себе лучшие качества дозированного аэрозольного ингалятора (ДАИ): простоту, компактность, возможность быстро выполнить ингаляцию и положительные свойства небулайзера: ингалятор медленно (около 1,5 с) выделяет аэрозоль. Таким образом, в процессе ингаляции у больных не возникает проблем с координацией дыхания.
Частицы аэрозоля, генерируемые обычными ДАИ, имеют высокую начальную скорость – от 2 до 8 м/с [19]. Двигаясь с такой скоростью, частицы по инерции сталкиваются с задней стенкой глотки. В результате большая часть дозы (от 50 до 80%) осаждается в ротоглотке, проглатывается со слюной и абсорбируется в ЖКТ, вызывая нежелательные системные эффекты.
Во время ингаляции Респимат выделяет аэрозоль со скоростью около 1 м/с, которая в несколько раз меньше, чем скорость аэрозоля, создаваемого ДАИ. Двигаясь медленно, частицы аэрозоля избегают столкновения с задней стенкой глотки и языком, что снижает депозицию препарата в полости рта. Как следствие, существенно увеличивается количество действующего вещества, доставленное в дыхательные пути.
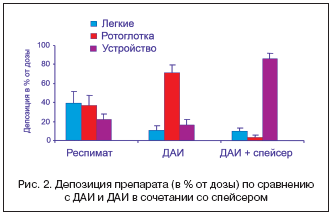
Важно отметить, что Респимат генерирует аэрозоль в течение 1,5 с, в то время как из ДАИ препарат выделяется в среднем всего за 0,2 с [19]. При ингаляции через ДАИ больные вынуждены координировать свой вдох так, чтобы активация ингалятора и начало вдоха идеально совпадали по времени: если пациент начинает вдыхать до активации ингалятора или, наоборот, выполняет вдох с опозданием, то количество препарата, доставленное в дыхательные пути, может уменьшиться в несколько раз [20]. Целому ряду больных трудно добиться хорошей координации между вдохом и активацией ингалятора, например, 18% больных активируют свой ДАИ во второй половине вдоха, а 5% – уже после завершения вдоха [21]. Респимат, обеспечивая выделение препарата на протяжении 1,5 с, существенно снижает последствия ошибок, связанных с недостаточной координацией вдоха больным. В результате Респимат способен в несколько раз по сравнению с ДАИ увеличить депозицию препарата в нижних дыхательных путях (рис. 2).
Для другого типа устройств доставки – порошковых ингаляторов также существуют особенности применения, зачастую лимитирующие их эффективность. Так, больные, использующие порошковые ингаляторы, должны вдыхать порошок достаточно быстро. В частности, минимальная скорость вдоха через Турбухалер, Мультидиск и ХандиХалер должна составлять 30 л/мин. [22]. Большинство больных ХОБЛ способны вдыхать препарат с такой скоростью [23]. Но если больной использует ингалятор капсульного типа, продолжительность вдоха должна составлять не менее 3 с: если вдох продолжается меньшее время, то порошок не успевает полностью покинуть капсулу. Сделать долгий вдох с высокой скоростью для больных ХОБЛ в целом проблематично, тем более что некоторые ингаляторы (Аэролайзер) требуют вдоха со скоростью более 60 л/мин. (объем вдоха продолжительностью 3 с со скоростью 60 л/мин. составляет 3 л). В результате при использовании порошковых ингаляторов часть дозы остается в капсуле, и больной должен каждый раз проверять капсулу и при необходимости совершать ингаляцию повторно.
При использовании порошковых ингаляторов от больного требуется более быстрый и продолжительный вдох, в то время как при применении Респимата нет никаких особых требований к дыхательному маневру, который осуществляет больной. Таким образом, Респимат значительно удобнее в использовании для больных ХОБЛ по сравнению с ДАИ и порошковыми ингаляторами.
Еще одним важным преимуществом нового ингалятора является то, что 55% дозы тиотропия бромида в Респимате выделяется в виде частиц оптимального аэродинамического диаметра, что гарантирует высокую степень легочной депозиции (табл. 1). Таким образом, Респимат на сегодняшний день – одно из наиболее совершенных средств доставки препаратов в дыхательные пути.
Кроме того, Респимат является универсальным средством доставки. В перспективе в виде Респимата будут выпускаться не только тиотропий, но и бронхолитики короткого действия, а также новый β2–агонист сверхдлительного (24 ч) действия – олодатерол.
Благодаря высокой степени легочной депозиции суточная доза тиотропия в Респимате составляет всего 5 мкг (2 ингаляции по 2,5 мкг), но при этом Спирива Респимат обеспечивает лечебный эффект, сопоставимый с назначением 18 мкг препарата через ХандиХалер [28].
Респимат с точки зрения пациента
Респимат прост в использовании. В исследовании 97,7% опрошенных пациентов заявили, что использовать Респимат «очень просто» или «просто» (рис. 3) [29]. На вопрос: «Как быстро Вы почувствовали уверенность при использовании Респимата?» большинство (76,6%) больных ответили, что почувствовали уверенность после первого или второго опыта использования этого ингалятора (рис. 4). Среди больных, применявших для лечения ХОБЛ как Респимат, так и ДАИ, 74% отдали предпочтение Респимату, 19% – ДАИ и 9% затруднились дать ответ [29].
Больные ХОБЛ, для которых предназначен Респимат, представляют серьезную проблему для врачей в плане обучения технике ингаляций из–за пожилого возраста и психологических проблем, связанных с воздействием заболевания на психические процессы (депрессия, негативное отношение к терапии). В частности, исследование, проведенное Brand P. с соавт. [30], показало, что дополнительное обучение технике ингаляции с помощью ДАИ практически не способно улучшить степень доставки препарата в дыхательные пути. Однако если больные применяют Респимат, то количество препарата, доставленного в легкие, в среднем существенно выше по сравнению с ДАИ, причем контроль со стороны врача и дополнительное обучение способны еще более повысить уровень легочной депозиции препарата (рис. 5).
Безопасность
Безопасность тиотропия бромида (ХандиХалер) была изучена и доказана в ходе 30 международных сравнительных исследований с участием более 30 тыс. пациентов. В частности, было показано, что тиотропия бромид хорошо переносится больными и не оказывает нежелательного воздействия на сердечно–сосудистую систему [31], а также не влияет на уродинамику у больных с доброкачественной гипертрофией предстательной железы [32].
Спирива Респимат (в отличие от ХандиХалера):
• содержит в качестве суточной дозы в 3,6 раза меньше действующего вещества;
• меньше задерживается в полости рта и, как следствие, меньшее количество тиотпропия может быть проглочено больным со слюной и впоследствии абсорбироваться в ЖКТ;
• концентрация препарата в крови после ингаляции через Респимат достаточно мала и существенно не отличается от концентрации, которая создается после ингаляции через ХандиХалер [33–35].
Таким образом, Спирива Респимат должен обеспечивать по крайней мере такую же высокую степень безопасности для больных, как и Спирива ХандиХалер. Действительно, по общему числу нежелательных явлений Спирива Респимат не отличается от плацебо [36] – за исключением жалоб на сухость во рту, которые в 2 раза чаще отмечались в группе тиотропия и закономерно объясняются холинолитическим действием препарата.
Однако обобщенный анализ 2 исследований тиотропия, проведенных Bateman E. с соавт. [37], показал, что число летальных исходов по любой причине, включая пациентов, не закончивших исследование, в группах, получавших тиотропий Респимат, было больше, чем в группе плацебо: 2,4% (тиотропий 5 мкг), 2,7% (тиотропий 10 мкг) и 1,6% (плацебо). При этом важно отметить, что разница в частоте летальных исходов по любой причине между группами терапии и плацебо не была статистически достоверна. К тому же увеличение риска летального исхода было зафиксировано далеко не во всех исследованиях Респимата и может быть связано с ошибками в организации исследований (в частности, включение в исследование больных, о которых было известно, что они страдают нарушениями сердечного ритма [38]).
Предполагаемое повышение риска летальных исходов, о которых сообщили Bateman E. и Singh S., не повлияло на позицию регуляторных инстанций, отвечающих за безопасность лекарственных средств более чем в 55 странах, – в том числе в странах Западной Европы и в России. Заявка на регистрацию SpirivaRespimat в США подана на рассмотрение FDA. Однако чтобы окончательно подтвердить безопасность Спиривы Респимат, было начато специальное исследование TIOSPIR с участием более 17 тыс. больных ХОБЛ. В этом исследовании больные были рандомизированы для приема Спиривы Респимат (5 мкг/сут.) и Спиривы ХандиХалер (18 мкг/сут.). Основным выводом TIOSPIR должно стать заключение о безопасности применения тиотропия, доставляемого через Респимат. Также в ходе исследования будет получена дополнительная информация об эффективности Спиривы Респимат в лечении ХОБЛ. Завершение исследования ожидается в 2013 г., однако уже в настоящее время можно предполагать, что никаких неожиданных результатов в ходе исследования получено не будет. Независимый комитет по контролю безопасности клинических испытаний в ходе последнего совещания в январе 2013 г. рекомендовал дальнейшее проведение исследования TIOSPIR согласно протоколу без внесения каких–либо изменений [39]. Все сказанное делает маловероятным наличие взаимосвязи между применением Спиривы Респимат и летальными исходами.
В этом плане можно вспомнить исследование INSPIRE [40], в котором терапия Спиривой ХандиХалер сравнивалась с терапией салметеролом/флутиказоном. Сравниваемые группы больных в этом исследовании не отличались как по числу обострений ХОБЛ, так и по показателям спирометрии. Кроме того, в группе салметерола/флутиказона случаи пневмонии отмечались в 2 раза чаще, чем в группе Спиривы. Но при этом число летальных исходов оказалось выше в группе Спиривы. Подобный результат оказался абсолютно неожиданным, т.к. существенно более крупное и более продолжительное исследование UPLIFT доказало способность тиотропия снижать летальность у больных ХОБЛ [4], в то время как достоверные данные о снижении летальности при терапии салметеролом/флутиказоном (аэрозоль) так и не были получены [41]. Анализ методологии исследования, проведенный крупнейшим специалистом в области респираторных исследований Samy Suissa [42], убедительно показал, что различия в смертности были обусловлены методологическими погрешностями в проведении исследования INSPIRE (отсутствие полной информации о выбывших из исследования больных, притом что исследование не завершили согласно протоколу более 1/3 пациентов).
Респимат: техническое устройство
В ингаляторе действующее вещество помещено в металлический картридж, рассчитанный на 60 доз. Препарат в картридже надежно защищен от воздействия внешней среды. Перед первым использованием картридж вставляется в ингалятор, далее для подготовки к работе надо 3 раза подряд после появления аэрозольного облачка активировать ингалятор вхолостую.
Респимат не содержит пропеллентов, т.е. жидких веществ, активное испарение которых создает в ДАИ давление, выталкивающее аэрозоль наружу. Отсутствие в Респимате пропеллента позволяет избежать ситуации, при которой пропеллент, поступая вместе с препаратом в дыхательные пути, быстро испаряется на слизистой бронхов, создавая эффект охлаждения, что может спровоцировать бронхоспазм у чувствительных больных [43].
Подача аэрозоля в Респимате осуществляется механически. Поворачивая до щелчка прозрачную гильзу, больной сжимает пружину, а при активации ингалятора пружина проталкивает очередную дозу препарата через так называемый юни–блок, в котором создается аэрозоль. Главная деталь ингалятора – юни–блок состоит из 2 функциональных частей: фильтра и сопла с 2 отверстиями. Пройдя через фильтр, раствор препарата покидает юни–блок через 2 отверстия диаметром 8 мкм, давление и соударение 2 потоков жидкости под определенным углом формирует аэрозоль, состоящий на 55% из частиц оптимального (от 1 до 5 мкм) диаметра.
Выводы
Респимат обладает целым рядом особенностей, выделяющих это устройство в ряду других ингаляторов. В частности, низкая скорость и продолжительное выделение аэрозоля создают оптимальные условия для доставки препарата в дыхательные пути, а 55% от дозы представлено частицами оптимального размера. Ингалятор обеспечивает минимальную степень депозиции в ротоглотке и содержит меньшее количество препарата по сравнению со Спиривой ХандиХалером. Эти свойства должны сделать терапию тиотропием еще более безопасной. Респимат отличает простая техника ингаляций. В результате больные с первых дней уверенно обращаются с ингалятором.
Положительные свойства Респимата позволяют оптимизировать терапию тиотропием и, в конечном итоге, улучшить качество оказания медицинской помощи больным ХОБЛ.

![Рис. 3. Мнение больных о простоте применения Респимата [29]](/data/articles/Image/t21/n7/379-3.gif)
![Рис. 4. Ответы больных на вопрос: «Как быстро Вы почувствовали уверенность при использовании Респимата?» [29]](/data/articles/Image/t21/n7/379-4.gif)
![Таблица 1. Доля частиц оптимального диаметра в % к дозе [24–27]](/data/articles/Image/t21/n7/379-5.gif)
![Рис. 5. Депозиция препарата в дыхательных путях до и после дополнительного обучения технике ингаляции: Респимат и ДАИ [32]](/data/articles/Image/t21/n7/379-6.gif)
Литература
1. Disse B et al. Life Sci 1993, 52: 537-44.
2. Gross NJ, Co E, Skorodin MS. Chest. 1989 Nov;96(5):984-7.
3. Buels KS, Fryer AD. Handb Exp Pharmacol. 2012;(208):317-41.
4. Tashkin DP et al. UPLIFT Study Investigators. N Engl J Med 2008;359:1543-54
5. Celli B, ZuWallack R, Wang S, Kesten S. Chest. 2003 Nov;124(5):1743-8.
6. O'Donnell DE et al. Eur Respir J. 2004 Jun;23(6):832-40.
7. Yoshimura K et al. Int J Chron Obstruct Pulmon Dis. 2012;7:109-17
8. Casaburi R et al. Eur Respir J 2002; 19:217-224
9. Vincken W et al. Eur Respir J 2002; 19:209-216
10. Celli В et al. CHEST 2010; 137(1): 20-30
11. Donohue JF et al. Chest. 2002 Jul;122(1):47-55
12. Vasudevan NT et al. Cell Cycle. 2011 Nov 1;10(21):3684-91
13. Vogelmeier C et al. N Engl J Med 2011;364:1093-103
14. Chong J, Karner C, Poole P. Cochrane Database Syst Rev. 2012 Sep 12;9:CD009157.
15. Van Noord JA, et al. Eur Respir J. 2005;26:214-222
16. Johnson M. Proc Am Thorac Soc. 2005;2(4):320-5
17. Fabbri LM et al. Lancet. 2009;374(9691):695-703
18. Aaron CD et al. Ann Intern Med. 2007;146:545-555.
19. Hochrainer D, Hцlz H, Kreher C, et al. J Aerosol Med, 2005; 18; 273–82.
20. Newman SP et al. Thorax 1991;46;712-716
21. Мelani AS et al. Respir Med 2011; 105: 930-938.
22. Laube BL et al. Eur Respir J 2011; 37: 1308-1331
23. Malmberg LP et al. Intern J of COPD 2010:5 257–26
24. De Backer W et al. J Aerosol Med and Pulmmon Drug Delivery 2010; Vol. 23 #3: 137–148
25. Rosenborg J et al. Eur Respir J 1999; 14:62s.
26. Criée CP et al. J Aerosol Med. 2006 Winter;19(4):466-72.
27. Ziegler, J., Wachtel H. (2001), Drug delivery to the Lungs XII, 54-57
28. van Noord et al. Respir Med 2009; 103: 22-29
29. Barczok M et al. Presented at VIII Deutsches Aerosol Therapie Seminar, Marburg, Germany. November 2003.
30. Brand P et al. International Journal of COPD 2008:3(4) 763–770
31. Rodrigo GJ et al. Pulmonary Pharmacology & Therapeutics 2012 ;25 : 40-47
32. Miyazaki et al. Pulmonary Pharmacology & Therapeutics 2008; 21: 879–883
33. van Noord J et al. Respir Med 2009;103:22–9.
34. Ichinose M et al. Respir Med 2010;104:228–36.
35. Tiotropium Respimat Pharmacokinetic Study in COPD http://www.clinicaltrials.gov/ ct2/show/NCT01222533?
36. Bateman E, et al. Respir Med 2010; 104: 1460-72
37. Bateman E et al. Int J Chron Obstruct Pulmon Dis. 2010 Aug 9;5:197-208.
38. Singh S et al. BMJ. 2011 Jun 14;342:d3215
39. Metzdorf N. Thorax Online First, published on February 12, 2013 as 10.1136/thoraxjnl-2013-203228
40. Wedzicha JA et al. Am J Respir Crit Care Med Vol 177. pp 19–26, 2008
41. Calverley PM et al. N Engl J Med 2007;356:775–789.
42. Suissa S. Am J Respir Crit Care Med. 2008 Nov 15;178(10):1090-1
43. Berger W. Curr Drug Deliv. 2009 Jan;6(1):38-49












