Именно АтД является самым частым из хронических заболеваний кожи вообще [3] и одним из первых проявлений аллергии у детей, дебютирует в раннем возрасте (в подавляющем большинстве случаев – до 1 года), характеризуется хроническим рецидивирующим течением, многообразием и тяжестью клинических проявлений, в связи с чем представляет собой серьезную проблему современной педиатрии [4]. Все больше данных свидетельствуют о том, что АтД оказывает негативное влияние на качество жизни пациентов и их семей, а также является причиной значительного экономического бремени как на семейном, так и на государственном уровне [5]. Более того, АтД почти у половины детей становится первым шагом на пути реализации атопического марша, характеризующегося последующим развитием симптомов респираторной аллергии в виде аллергического ринита и/или бронхиальной астмы [6].
Именно поэтому внимание специалистов в области аллергологии-иммунологии, дерматологии, педиатрии сегодня приковано к изучению механизмов формирования аллергической сенсибилизации при АтД и созданию новых эффективных стратегий лечения и профилактики этого заболевания. Ключевым звеном в этом поиске становятся новые данные о патофизиологии АтД и понимание роли дисфункции кожного барьера в формировании и поддержании хронического воспалительного процесса в коже [7], а также доказательства эффективности воздействия на эти механизмы с помощью современных увлажняющих и смягчающих косметических средств.
Целью настоящего обзора является систематизация накопленных к настоящему времени данных о значении дисфункции кожного барьера в патогенезе АтД и формировании аллергической сенсибилизации, о роли современных средств ухода за кожей в программах лечения заболевания, а также о новых перспективах их использования с целью первичной профилактики АтД и других аллергических болезней.
Дисфункция кожного барьера при АтД
Серьезный прогресс в понимании патогенеза АтД в последние годы связан в первую очередь с пересмотром роли барьерной функции кожи и ее нарушения у пациентов-атопиков. Безусловно, АтД является мультифакториальным заболеванием, в развитии которого имеют значение как генетические, так и средовые факторы [8]. Однако большинство проведенных в настоящее время исследований подтверждают, что именно дисфункция эпидермального барьера на фоне измененного иммунного ответа играет важнейшую роль как в развитии АтД [7], так и в последующем формировании чрескожной сенсибилизации и реализации атопического марша [9].В сложный патогенетический процесс вовлечены все виды кожного барьера: физический (роговой слой, десмосомы, плотные межклеточные контакты), биохимический (липиды, органические кислоты, лизосомы, антимикробные пептиды), иммунный (лимфоциты, нейтрофилы, моноциты, клетки Лангерганса). В результате нарушения их функций при АтД происходят, с одной стороны, увеличение трансэпидермальной потери влаги (TEWL – transepidermal water loss) и снижение способности связывания влаги кожей больного, а с другой стороны – усиление проницаемости кожного барьера для внешних неблагоприятных агентов (микробных и химических антигенов, токсинов, аллергенов) [10].
Основные события, приводящие к нарушению барьерной функции кожи, разворачиваются в самом поверхностном – роговом – слое (Stratum Corneum), дефекты функционирования которого обусловлены множеством врожденных и приобретенных механизмов [11]. Одним из наиболее хорошо изученных факторов, принимающих участие в этом процессе, является дефект гена филаггрина – структурного белка кожи, без которого не может осуществляться процесс дифференцировки клеток эпидермиса [12]. Филаггрин образуется из профилаггрина в зернистом слое эпидермиса и распадается на аминокислоты в верхней части рогового слоя, где продукты его метаболизма участвуют в поддержании оптимального значения pH кожи и обеспечивают необходимую влажность рогового слоя [13]. Показано, что носительство мутации гена филаггрина, приводящее к его отсутствию или недостаточной продукции, достоверно коррелирует с недостаточной увлажненностью кожи и высокой трансэпидермальной потерей влаги [14], что, в свою очередь, ассоциировано с риском пищевой сенсибилизации и более тяжелым течением АтД [15]. В то же время мутации гена филаггрина обнаруживаются у 3–55% пациентов с АтД и не являются единственным и/или обязательным условием для его формирования, вероятно, лишь способствуя развитию заболевания при наличии у индивидуума других генетических и эпигенетических предпосылок [16].
К таким предпосылкам относится изменение pH кожного покрова в сторону повышения, приводящее к увеличению его проницаемости [17], что связано с деградацией липид-процессируемых энзимов, необходимых для образования натурального увлажняющего фактора из молекул филаггрина [18]. Кроме того, повышение pH кожи у пациентов с АтД и мутациями гена филаггрина является одной из предпосылок, поддерживающих рост инфекционных агентов, в частности S. аureus [19]. Недавние исследования на мышиных моделях показали возможность частично предотвращать формирование дисфункции кожного барьера и подавлять иммунные нарушения при АтД за счет повышения кислотности рогового слоя [20], что может послужить основой для создания новых направлений лечения и профилактики этого заболевания.
Еще одним фактором, необходимым для обеспечения адекватного функционирования кожного барьера, являются плотные межклеточные контакты, которые играют основную роль в ограничении и регуляции парацеллюлярной диффузии и миграции клеток воспаления, а также в процессах пролиферации, поляризации и дифференцировки эпителиальных клеток [21]. Накоплено множество доказательств наличия у пациентов с АтД композиционного и функционального дефекта плотных контактов [22, 23], что способствует повышению проницаемости кожного барьера. Более того, в исследованиях на животных показано, что блокирование продукции клаудина – основного белка плотных контактов – приводит к нарушению формирования у мышей рогового слоя, значительному повышению трансэпидермальной потери влаги и гибели животных [24]. Наконец, было продемонстрировано снижение в очагах поражения кожи у пациентов с АтД активации Toll-подобных рецепторов (TLR2), необходимой как для обеспечения адекватного функционирования плотных контактов в кератиноцитах [25], так и для распознавания различных микробных антигенов и регуляции активности антимикробных пептидов, в частности бета-дефензина [26].
Антимикробные пептиды (AMPs), являясь важнейшим компонентом врожденной иммунной защиты кожи против различных инфекционных агентов и опухолевых антигенов, обладают также способностью влиять на воспалительный ответ и процессы регенерации и репарации в коже [27]. У пациентов с АтД описано снижение продукции AMPs и локальной бактерицидной активности [28, 29], что является главной причиной инфицирования и колонизации кожи больных бактериальными (S. aureus) и грибковыми агентами и одной из важнейших проблем лечения заболевания, поскольку именно стафилококковые суперантигены способны индуцировать гиперпродукцию IgE и поддерживать воспаление при АтД [30].
Значительную роль в нарушении защитных свойств кожного барьера играют и изменения в составе липидов рогового слоя, основными из которых являются церамиды, жирные кислоты и холестерол [31]. Показано селективное снижение уровня церамидов (в частности, церамида 1) у пациентов с АтД, что связано как с подавлением на фоне нейтральной pH активности энзимов, обеспечивающих процессинг липидов, так и с повышенной кислотной церамидазной активностью [32]. Дефект липидного барьера усугубляет подверженность больных АтД колонизации S. aureus, поскольку нарушенный метаболизм церамидов приводит к снижению уровня в роговом слое сфингозина, обладающего высокой антимикробной активностью [33].
Регуляция метаболизма липидов, а также процесса эпидермальной дифференцировки в значительной степени определяется активностью особых классов рецепторов, экспрессируемых клетками кожи, – рецепторов, активируемых протеиназами (PAR), и рецепторов, активируемых пероксисомными пролифераторами (PPARs). Они принимают участие в контроле процессов клеточной пролиферации и дифференцировки, проницаемости кожного барьера и регуляции воспалительного ответа в коже [34]. Доказано, что клетки кожи, вовлеченные в воспалительный процесс, экспрессируют более высокий уровень PAR-2, активация которого имеет важнейшее значение в развитии зуда при АтД [35]. Напротив, более низкая экспрессия PPARs, выявляемая в очагах поражения у пациентов с АтД, является одним из механизмов нарушения целостности эпидермального барьера и формирования аллергического воспаления [36]. Результаты современных исследований дают серьезные основания полагать, что использование антагонистов PAR-2 и активаторов PPARs, в т. ч. топических, может стать одним из новых направлений лечения АтД [37–39].
Немаловажное значение в поддержании воспалительного процесса в коже при АтД имеет и механическое повреждение кожного барьера. Зуд, являясь одной из важнейших проблем у взрослых и детей с АтД, часто сопровождается расчесыванием и последующим повреждением кожи с разрушением эпителиальных и эндотелиальных клеток [40], что способствует выбросу из них аларминов (ассоциированных с повреждением молекулярных частиц), к которым относятся гистамин, эозинофильный нейротоксин, интерлейкин-33 и др. [41]. Они, в свою очередь, активируют различные типы клеток, участвующих в развитии аллергического воспаления: мастоциты, резидуальные тканевые клетки, врожденные лимфоидные клетки 2 типа [42]. Именно поэтому поиск средств, эффективно подавляющих зуд, является одной из приоритетных задач в лечении пациентов с АтД.
Роль нарушения функции кожного барьера в формировании аллергической сенсибилизации
В течение длительного времени не вызывала сомнений идея о том, что кожа является эффективным барьером на пути проникновения извне различных антигенов и препятствует развитию патологического иммунного ответа, в т. ч. сенсибилизации к поверхностно воздействующим аллергенам [13]. Предполагалось, что белки с высоким молекулярным весом не абсорбируются через кожу. Однако в последующем выяснилось, что такие высокомолекулярные протеины могут захватываться дендритными клетками, что приводит к реализации иммунного ответа, в т. ч. патологического [43]. Так, анализ результатов проспективного когортного исследования почти 1500 дошкольников в Великобритании в 2003 г. обнаружил ассоциацию между наличием у детей аллергии на арахис и использованием в раннем возрасте средств для ухода за кожей, содержащих арахисовое масло [44]. В то же время было доказано, что кожа может способствовать формированию толерантности при эпикутанном контакте с аллергеном, что и было продемонстрировано у пациентов с пищевой и пыльцевой аллергией, а также на мышиных моделях [45, 46].Ответ на вопрос, в каких случаях воздействие антигена на кожу приводит к развитию сенсибилизации, а в каких – к толерантности, стал проясняться после доказательства индукции Th2-опосредованного иммунного ответа и экспрессии тимического стромального лимфопоэтина (TSLP) у пациентов с АтД на фоне механического повреждения кожи [47]. В последующем исследовании на моделях животных показали, что именно интактная (неповрежденная) кожа является обязательным фактором безопасности и эффективности эпикутанной иммунотерапии [48]. А в проспективных когортных исследованиях подтвердили, что атопический дерматит является достоверным фактором риска развития сенсибилизации к яйцу [49] и арахису [44], а экзема рук – к латексу [50].
Накопившиеся данные послужили основанием для появления и широкого распространения в научной среде гипотезы «двойной аллергенной экспозиции», согласно которой энтеральное поступление пищевых антигенов в организм приводит к формированию пищевой толерантности, а их накожная экспозиция при АтД – к пищевой сенсибилизации [51]. В настоящее время имеется достаточное количество подтверждений данной гипотезы, в т. ч. и доказанная ассоциация дефекта гена филаггрина с аллергией на арахис и развитием респираторных аллергических заболеваний, несмотря на отсутствие экспрессии филаггрина в кишечной стенке и бронхиальном эпителии [12, 52]. А опубликованный недавно систематический обзор 66 исследований, изучавших взаимосвязь между АтД и пищевой аллергией, показал, что АтД, действительно, часто предшествует развитию пищевой сенсибилизации [53].
Кроме того, имеются основания предполагать, что чрескожной пенетрации аллергенов, в т. ч. антигена клеща домашней пыли, способствуют механические повреждения кожи, изменение ее pH и состава плотных межклеточных контактов, воздействие протеазных антигенов, что увеличивает возможность реализации системного аллергического процесса и является одним из механизмов развития атопического марша [23]. Интересно, однако, что проспективное наблюдение за детьми с различными типами дерматозов в первые месяцы жизни (экзема, себорейный дерматит, интертриго и пеленочный дерматит) выявило более высокую частоту реализации АтД и свистящего дыхания в возрасте 2 лет именно в группе младенцев с экземой [54].
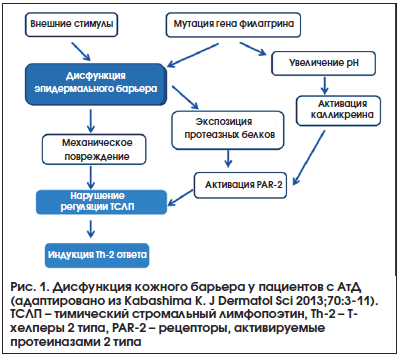
Таким образом, современные данные подтверждают, что нарушение функции эпидермального барьера на фоне измененного иммунного ответа не только играет важнейшую роль в патогенезе АтД (рис. 1), но и способствует формированию эпикутанной аллергической сенсибилизации и последующей реализации атопического марша [9]. А это, в свою очередь, дает возможность переосмыслить роль средств ухода за кожей в программах лечения пациентов с АтД, а также их использование для профилактики аллергических заболеваний.
Современные средства ухода за кожей в лечении АтД
Значительное улучшение понимания патофизиологии АтД в последние десятилетия внесло серьезные коррективы в подходы к ведению пациентов. Поскольку дисфункция кожного барьера в настоящее время рассматривается в качестве ключевого механизма патогенеза этого хронического заболевания, одним из важнейших направлений его лечения стало обязательное использование пациентами специальных средств ухода за кожей, что определяется всеми современными международными и отечественными согласительными документами как базовая терапия АтД [3, 55, 56]. Главными целями такого базового ухода являются увлажнение кожи и нормализация основных функций эпидермального барьера, в т. ч. снижение трансэпидермальной потери влаги, а также чрескожной пенетрации аллергенов и инфекционных агентов [57], что достигается путем использования топических смягчающих и увлажняющих средств.Интересно, что в настоящее время не существует официального консенсуса в отношении определения увлажняющих и смягчающих средств ухода за кожей [58], так же как нет доказательств преимуществ использования конкретных их классов при определенных фенотипах АтД [59]. Термин «увлажнители» (“moisturizers”) впервые был предложен в конце прошлого века американскими маркетологами, хотя желание нанести на сухую кожу смягчающие маслянистые вещества можно считать столь же старым, как само человечество [60]. В зависимости от механизма действия все увлажняющие и смягчающие косметические средства можно разделить на 4 основных класса [61]: эмоленты, хумектанты, окклюзивные вещества и восстановители белка. При этом у пациентов с АтД используются преимущественно продукты первых 3 классов (табл. 1).
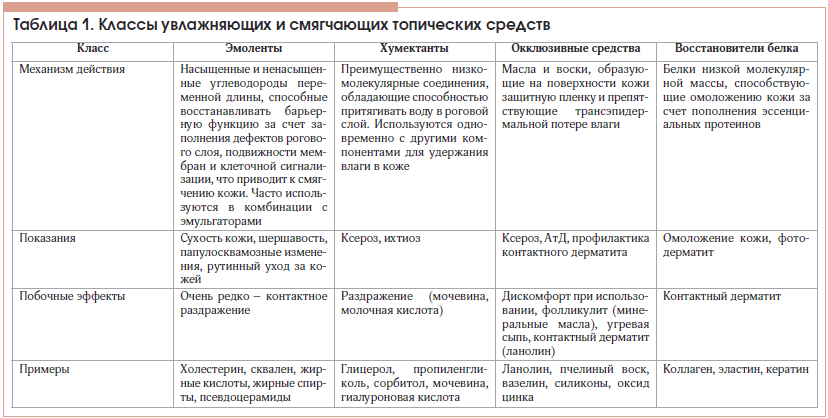
При обсуждении вопросов, связанных с базовой терапией АтД, все средства ухода за кожей часто объединяют термином «эмоленты». Это, действительно, один из самых необходимых для пациентов с АтД классов косметических средств, включающий компоненты (чаще всего липиды и масла), подобные натуральным липидам рогового слоя и себума, способные придавать коже мягкость и эластичность [62]. Холестерин, церамиды или псевдоцерамиды, длинноцепочечные насыщенные жирные кислоты (линолевая, линоленовая, олеиновая и др.) восстанавливают эпидермальный барьер, встраиваясь в естественную архитектуру липидного матрикса кожи [63]. Так, было показано, что использование крема на основе псевдоцерамидов у пациентов с АтД хотя и не влияло на тяжесть течения заболевания, однако значительно улучшало влажность кожи, а также снижало потребность пациентов в применении топических кортикостероидов [64]. Сквален, являясь одним из важных липидов, продуцируемых клетками кожи человека, и компонентом кожного сала, также широко используется в составе эмолентов, обладая дополнительной способностью защищать поверхность кожи от перекисного окисления липидов в результате воздействия ультрафиолетового и других источников ионизирующего излучения [61].
Хумектанты (собственно увлажняющие средства) – гигроскопические соединения, способные привлекать молекулы воды в эпидермис как из дермы, так и из окружающей среды при соответствующих условиях. Многие хумектанты обладают одновременно и качествами эмолентов [63]. Так, натуральный увлажняющий фактор, состоящий из смеси низкомолекулярных гигроскопических соединений (молочная кислота, пирролидон карбоновой кислоты, аминокислоты), является «важнейшим игроком на арене поддержания высокой влажности кожи» [63]. Наиболее часто используемыми ингредиентами из этой группы являются глицерин, мочевина, пропиленгликоль. Однако в связи с возможностью раздражающего действия средства, содержащие мочевину и пропиленгликоль, не рекомендуются для применения у детей раннего возраста [65, 66]. В двойном слепом плацебо-контролируемом исследовании был показан положительный эффект увлажняющего средства на основе глицерина на состояние кожи у пациентов с АтД, сопровождавшийся значительным повышением влажности рогового слоя [67].
Окклюзивные компоненты, среди которых наиболее часто используются вазелин, ланолин, минеральное масло и силиконы, представляют собой вещества, физически блокирующие трансэпидермальную потерю влаги за счет создания на поверхности кожи гидрофобного барьера. Показано, что вазелин обладает наиболее мощным влагосберегающим эффектом, в минимальной концентрации 5% снижая показатель TEWL более чем на 98% [68]. Тем не менее применение средств этой группы может быть несколько ограничено в связи с наличием запаха, ощущения жирности кожи после их использования и потенциальной аллергенности.
Современные средства ухода за кожей пациентов с АтД содержат, как правило, комплекс ингредиентов, обладающих различными механизмами действия, что значительно повышает их эффективность. Кроме того, в последние годы появляется все больше продуктов для ухода, содержащих в своем составе дополнительные компоненты, к которым относятся различные растительные субстанции (алоэ, аллантоин, бисаболол, экстракты овса, ячменя, масло ши и др.), витамины (Д-пантенол, ниацинамид, альфа-токоферол и пр.), соли магния и цинка, а также лизаты бактерий и пребиотики [61, 69]. Помимо дополнительного смягчающего, увлажняющего и антиоксидантного действия такие ингредиенты способны оказывать противовоспалительный, противозудный и антимикробный эффект. Так, в клинических исследованиях подтверждены более высокая эффективность у пациентов с АтД средств ухода за кожей, содержащих масло ши, по сравнению с обычным эмолентом на основе церамидов [70], а также значительное улучшение кожной гидратации при использовании увлажняющих средств с аргановым маслом [71].
Одним из таких примеров является новая разработка российской компании «Аванта» (Краснодар) – линия специализированных косметических средств atopic® для детей с АтД, которые в качестве основного ингредиента содержат патентованную формулу на основе масла ши, арганового масла и воска ячменного зерна (торговая марка Stimu-Tex® AS, Pentapharm, Швейцария). Открытое несравнительное наблюдение пациентов с АтД, получавших в качестве средств ухода за кожей atopic®, подтвердило клиническую эффективность продуктов серии [72]. Показано, что они достоверно улучшают состояние кожи у детей с АтД, не оказывают раздражающего и сенсибилизирующего действия. При регулярном использовании Крем для ежедневного ухода atopic® улучшает показатель увлажненности кожи и снижает значение показателя трансэпидермальной потери влаги. Применение Крема успокаивающего atopic® приводило к значительному снижению индекса SCORAD за 14 дней применения, при этом резко уменьшались субъективные симптомы, такие как зуд и нарушения сна у детей.
Результаты других исследований продемонстрировали, что пребиотик Биолин в составе эмолентов способствует повышению влажности кожи, увеличивает продукцию кожного сала и снижает TEWL [73], а эмолент на основе термальной воды с входящим в состав крема экстрактом Aquaphilus dolomiae обладает положительным действием на состав кожной микрофлоры [74]. Наконец, доказано, что некоторые дополнительные компоненты увлажняющих средств (флавоноиды, агонисты PPARs) способны подавлять продукцию провоспалительных цитокинов и оказывать значительный клинический эффект в отношении не только признаков воспаления и сухости кожи, но и интенсивности зуда [75–77].
Завершая обсуждение роли современных средств ухода за кожей в программах лечения пациентов с АтД, можно выделить их основные эффекты, к которым относятся:
• Увлажняющее и смягчающее действие – гидратация, обеспечивающая повышение содержания влаги в роговом слое, и восстановление липидного матрикса кожи [60, 63, 68].
• Противовоспалительное действие: некоторые ингредиенты современных увлажняющих средств подавляют выработку провоспалительных цитокинов путем блокирования активности циклооксигеназы, оказывая таким образом успокаивающее действие на воспаленную кожу [65, 75, 78].
• Противозудное действие: многие из эмолентов способны подавлять зуд за счет торможения продукции цитокинов. Кроме того, использование увлажняющих средств на водной основе сопровождается испарением воды с поверхности кожи, что приводит к развитию охлаждающего эффекта [61, 75, 77].
• Антимикробное действие: подавляют активность микроорганизмов на поверхности кожи, что имеет большое значение в поддержании контроля за бактериальной и грибковой контаминацией у пациентов с АтД [80, 81].
• Репаративное действие: гиалуроновая кислота и некоторые другие компоненты могут оказывать положительный эффект на процесс заживления ран, расчесов и трещин кожи [61, 63].
В совокупности все перечисленные эффекты приводят к улучшению клинического течения АтД: уменьшению частоты обострений и их выраженности [59, 63, 82, 83], снижению потребности в ТКС [64, 84, 85], положительно влияют на микробиоту кожи больных, что способствует снижению риска вторичного инфицирования [79, 80, 86], а также улучшают качество жизни пациентов и их семей [59, 87].
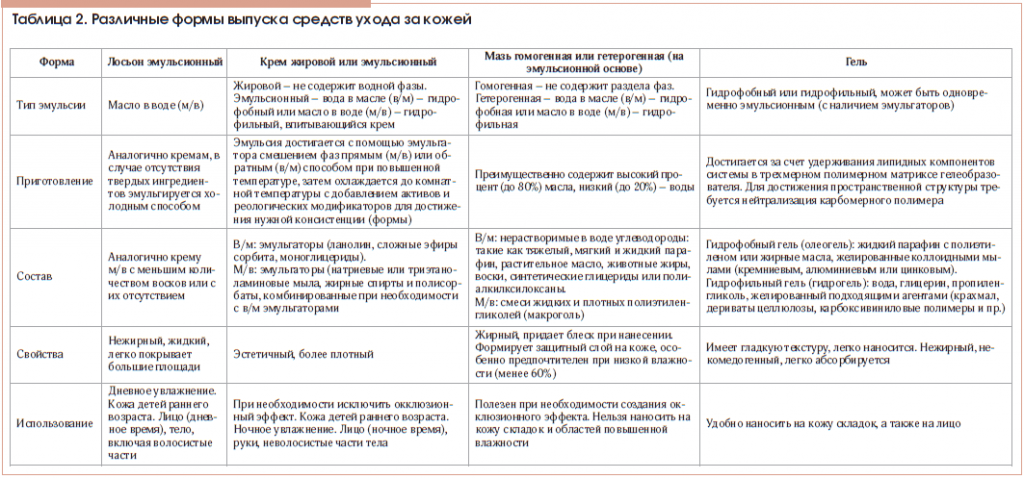
Как видим, необходимость использования средств ухода за кожей у взрослых и детей с АтД не вызывает сомнений, однако пациентам зачастую непросто сделать конкретный выбор. В первую очередь это связано с тем, что до настоящего времени масштабные сравнительные исследования эффективности различных классов и типов топических увлажняющих и смягчающих средств в мире не проводились [58, 79]. Поэтому существующие согласительные документы и клинические рекомендации по лечению АтД предлагают осуществлять такой выбор пациенту совместно с лечащим врачом, индивидуально, в зависимости от формы и тяжести заболевания, его стадии (обострение или ремиссия), сезонных и климатических условий, специфического статуса больного и даже его финансовых возможностей [3, 55, 56, 65, 89]. Немаловажную роль в этом выборе играет форма выпуска средства ухода за кожей (табл. 2). При этом необходимо принимать во внимание, что жидкие формы (лосьоны и эмульсии) и гели рекомендуются для использования в острый период заболевания, при процессах, сопровождающихся мокнутием, а также в кожных складках и волосистых частях тела. Легкие кремы с высоким содержанием воды применяются преимущественно у детей раннего возраста, а также у пациентов с сухой кожей в области лица, особенно в летний период. Наконец, мази (особенно жирная мазь, не содержащая в своем составе воды) обладают наиболее выраженным окклюзионным эффектом, что обеспечивает их высокую эффективность у пациентов с более тяжелым течением заболевания, выраженным ксерозом, преимущественно в холодное время года, но делает неприемлемым их нанесение на участки мокнутия и кожные складки [55, 59, 65, 88].
Важно помнить, что использование эмолентов, составляющее основу базовой терапии АтД, должно проводиться в соответствии с определенными правилами ухода за кожей, представленными на рисунке 2. Результаты многочисленных исследований показали, что клиническая эффективность такого базового ухода в значительной мере зависит от продолжительности применения топических средств, кратности их нанесения и количества используемого продукта [63, 67, 90, 91]. Кроме того, продемонстрировано значительное улучшение течения АтД и удовлетворенности пациентов результатами его лечения после проведения образовательных мероприятий, организованных с участием специально подготовленного персонала [92, 93]. Наконец, в некоторых исследованиях была подтверждена и экономическая эффективность рационального ухода за кожей [94, 95]. Следовательно, обучение больных и поддержание высокого уровня комплаентности пациента (или родителей больного ребенка) являются основой достижения контроля над таким хроническим заболеванием кожи, как АтД, и должны стать приоритетными направлениями в программах его лечения.

Перспективы использования специальных средств ухода за кожей с целью первичной профилактики АтД
В связи с углублением знаний о роли нарушения защитных функций кожи в патогенезе АтД и последующем развитии атопического марша место средств ухода за кожей, способных восстанавливать эпидермальный барьер, в стратегиях ведения пациентов с АтД было серьезно переоценено [96]. Стало очевидным, что длительное регулярное применение эмолентов больными в качестве базового ухода фактически является основной мерой вторичной профилактики заболевания, способствующей снижению частоты и тяжести обострений, риска развития инфекционных осложнений и, вероятно, возможности формирования аллергической сенсибилизации и реализации симптомов респираторной аллергии [97]. Более того, результаты недавних исследований создали серьезные предпосылки для появления новых подходов к решению проблемы первичной профилактики АтД, что еще до недавнего времени не представлялось реальным [98].Идея новой концепции заключается в использовании специальных средств ухода за кожей младенцев с самого раннего возраста, до появления симптомов АтД, с целью повышения функциональных свойств эпидермального барьера. Начиная с 2010 г. было проведено несколько пилотных исследований, продемонстрировавших, что раннее начало применения эмолентов в виде кремов или масляных ванн у здоровых малышей приводит к значительному улучшению состояния их кожи, повышению ее увлажненности и с большой долей вероятности уменьшает частоту развития у них АтД [99–101]. Причем подобный исход был отмечен у детей как из группы риска по развитию аллергических заболеваний, так и без отягощенного семейного анамнеза. Такие обнадеживающие результаты, безусловно, послужили основанием для организации более серьезных проектов в данной области, и к настоящему времени уже опубликованы первые итоги двух подобных исследований.
Так, в международном рандомизированном контролируемом исследовании, проведенном в США и Великобритании, определялась кумулятивная частота АтД в 6 мес. у 124 детей из группы высокого риска по развитию аллергических заболеваний, часть которых получала уход за кожей с применением эмолентов с первого месяца жизни [102]. Было показано, что ежедневное использование специальных увлажняющих средств у детей раннего возраста снижает частоту развития АтД на 50% по сравнению с детьми, не получавшими специального ухода за кожей (ОР 0,50; 95% ДИ, 0,28–0,9; р=0,017).
Другое аналогичное исследование было проведено в Японии и также изучало эффективность ежедневного использования специальных средств ухода за кожей в виде эмульсии с точки зрения профилактики АтД [103]. 116 новорожденных из группы высокого риска по развитию аллергии наблюдались до 32 нед. Помимо общего клинического обследования у детей проводились изучение состояния эпидермального барьера (TEWL, влажность рогового слоя и pH кожи), а также исследование аллергической сенсибилизации. В результате наблюдения оказалось, что у детей, получавших эмоленты, риск развития АтД снижался на 32% по сравнению с контрольной группой (р=0,012). Кроме того, была показана более высокая частота реализации АтД и сенсибилизации к овомукоиду у детей с исходно повышенными показателями TEWL (p<0,05). Интересно, что достоверное снижение частоты развития АтД на фоне использования эмолентов подтвердилось только у детей с исходно высокой трансэпидермальной потерей влаги [104], что дает возможность рассматривать этот показатель в качестве не только предиктора реализации АтД, но и возможного предиктора эффективности профилактического применения увлажняющих средств.
Таким образом, имеющиеся на сегодняшний день данные дают серьезные основания полагать, что применение специальных средств ухода за кожей здоровых малышей с самого раннего возраста является эффективным и безопасным способом решения проблемы первичной профилактики АтД, что уже находит свое отражение и в рекомендациях профессиональных сообществ [105].












