–Т–≤–µ–і–µ–љ–Є–µ
–Я–Њ—А–∞–ґ–µ–љ–Є–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —А–∞–љ–љ–Є—Е –Є —И–Є—А–Њ–Ї–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ (–°–Ф). –≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є (–Ф–Я–Э) –љ–µ —В–∞–Ї —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і—А—Г–≥–Є–Љ–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–Љ–Є –≤ —А–¶ 5–Ј—Г–ї—М—В–∞—В–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, –Њ–і–љ–∞–Ї–Њ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –љ–∞ –і–Њ–ї—О –Ф–Я–Э –њ—А–Є—Е–Њ–і–Є—В—Б—П –Њ–Ї–Њ–ї–Њ 75% –њ–Њ—А–∞–ґ–µ–љ–Є–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ—А–Є –°–Ф [1, 2]. –Я–Њ –і–∞–љ–љ—Л–Љ –Љ–Є—А–Њ–≤–Њ–є –ї–Є—В–µ—А–∞—В—Г—А—Л, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ф–Я–Э —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ –Њ—З–µ–љ—М —И–Є—А–Њ–Ї–Њ–Љ –і–Є–∞–њ–∞–Ј–Њ–љ–µ (5вАУ100%) [3]. –°—В–Њ–ї—М –±–Њ–ї—М—И–Њ–є —А–∞–Ј–±—А–Њ—Б –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —З–µ—В–Ї–Њ–≥–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –њ–Њ–љ—П—В–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є, –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–µ–Љ –µ–µ –њ—А–Њ—П–≤–ї–µ–љ–Є–є, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –Є –Ї—А–Є—В–µ—А–Є–µ–≤ –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і–Є–∞–≥–љ–Њ–Ј–∞, –∞ —В–∞–Ї–ґ–µ —А–∞–Ј–ї–Є—З–Є—П–Љ–Є –Љ–µ–ґ–і—Г e8—Б—Б–ї–µ–і—Г–µ–Љ—Л–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Ж–Є—Д—А—Л —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Ф–Я–Э –±—Г–і—Г—В –≤–∞—А—М–Є—А–Њ–≤–∞—В—М –µ—Й–µ –±–Њ–ї—М—И–µ –њ—А–Є —Г—З–µ—В–µ —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Л –Ф–Я–Э [4]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –†–Њ—Б—Б–Є–Є –љ–µ—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Њ–±–Њ–±—Й–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –Њ —А–∞–љ–љ–µ–є (—Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є/–±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є) —Б—В–∞–і–Є–Є –Ф–Я–Э, —В–∞–Ї –Ї–∞–Ї –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –µ–µ –љ–µ–є—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –≤—Л—П–≤–ї–µ–љ–Є—П –Ф–Я–Э –љ–∞ —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –і–Њ–ї–ґ–љ—Л –±—Л—В—М –њ—А–Њ—Б—В—Л–Љ–Є –≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є, –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–Њ–і–Є–Љ—Л–Љ–Є –њ—А–Є –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є, –њ—А–µ–і–Њ—Б—В–∞–≤–ї—П—О—Й–Є–Љ–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Г—О –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—О –Њ —Б–Њ—Б—В–Њ—П–љ–Є–Є —В–Њ–љ–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ. –Ч–∞ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –љ–∞–Є–±–Њ–ї–µ–µ –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ–Є –Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ–Є –Ј–∞—П–≤–ї–µ–љ–љ—Л–Љ —В—А–µ–±–Њ–≤–∞–љ–Є—П–Љ –Љ–µ—В–Њ–і–∞–Љ–Є —А–∞–љ–љ–µ–≥–Њ –≤—Л—П–≤–ї–µ–љ–Є—П –њ–∞—В–Њ–ї–Њ –≥–Є–Є —В–Њ–љ–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ —Б—В–∞–ї–Є –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П –±–Є–Њ–њ—Б–Є—П –Ї–Њ–ґ–Є –≥–Њ–ї–µ–љ–Є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –Є–Љ–Љ—Г–љ–Њ–≥–Є—Б—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –Є–љ—В—А–∞—Н–њ–Є–і–µ—А–Љ–∞–ї—М–љ—Л—Е –љ–µ—А–≤–Њ–≤ –Є –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П –Љ–µ—В–Њ–і–Є–Ї–∞ вАФ –ї–∞–Ј–µ—А–љ–∞—П –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–∞—П –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П —А–Њ–≥–Њ–≤–Є—Ж—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—Г—А—А–Њ–≥–∞—В–љ–Њ–≥–Њ –Љ–∞—А–Ї–µ—А–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є [5, 6]. –°—Г—В—М –і–∞–љ–љ—Л—Е –Љ–µ—В–Њ–і–Є–Ї –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ –Љ–µ–ї–Ї–Є—Е –љ–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ —Б –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ –і–Є–љ–∞–Љ–Є—З–µ—Б–¶ a–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –≤—Л—П–≤–ї–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є. –Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П –Є –њ—А–µ–і–Є–Ї—В–Є–≤–љ–∞—П —Ж–µ–љ–љ–Њ—Б—В—М –Њ–±–Њ–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–∞.
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –ї–µ—З–µ–љ–Є—О –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є —Б–Њ—Б—А–µ–і–Њ—В–Њ—З–µ–љ—Л –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–∞ —Г–ї—Г—З—И–µ–љ–Є–Є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П, –Є–Ј–Љ–µ–љ–µ–љ–Є–Є –Њ–±—А–∞–Ј–∞ –ґ–Є–Ј–љ–Є (–≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞), –≤–ї–Є—П–љ–Є–Є –љ–∞ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л–µ –Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г–µ–Љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –Є, –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є, –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є [7]. –У–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є–є –Ї–Њ–љ—В—А–Њ–ї—М –њ–Њ–і—А–∞–Ј—Г–Љ–µ–≤–∞–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ —А–µ–≥—Г–ї—П—А–љ–Њ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ (Hb1Ac), –љ–Њ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї. –Я–Њ –њ–Њ—Б–ї–µ–і–љ–Є–Љ —Б–≤–µ–і–µ–љ–Є—П–Љ, –і–∞–љ–љ—Л–є –Љ–∞—А–Ї–µ—А –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–є, –±–Њ–ї–µ–µ —В–Њ—З–љ—Л–є –њ—А–µ–і–Є–Ї—В–Њ—А –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –љ–µ–є—А–Њ–њ–∞—В–Є–Є [8, 9].
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ—Ж–µ–љ–Ї–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Њ–±—А–∞—В–Є–Љ–Њ—Б—В–Є –љ–∞—А—Г—И–µ–љ–Є–є, –≤—Л—П–≤–ї–µ–љ–љ—Л—Е –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–љ–∞—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ–Є –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э –љ–∞ —Д–Њ–љ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ (–≤ —В–µ—З–µ–љ–Є–µ 5 –Љ–µ—Б.) —Г–ї—Г—З—И–µ–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Ф–Є–Ј–∞–є–љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ–і–љ–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Њ–і–љ–Њ–≤—Л–±–Њ—А–Њ—З–љ–Њ–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ (—Б–ї—Г—З–∞–є–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ.
–Ь–µ—Б—В–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –§–У–Р–Ю–£ –Т–Ю –Я–µ—А–≤—Л–є –Ь–У–Ь–£ –Є–Љ. –Ш.–Ь. –°–µ—З–µ–љ–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є (–°–µ—З–µ–љ–Њ–≤—Б–Ї–Є–є –£–љ–Є–≤–µ—А—Б–Є—В–µ—В).
–Ш–Ј—Г—З–∞–µ–Љ–∞—П –њ–Њ–њ—Г–ї—П—Ж–Є—П: –Є–Ј—Г—З–∞–ї–∞—Б—М –Њ–і–љ–∞ –њ–Њ–њ—Г–ї—П—Ж–Є—П вАФ –њ–∞—Ж–Є–µ–љ—В—Л —Б –°–Ф 2 —В–Є–њ–∞ –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ф–Я–Э.
–Ъ—А–Є—В–µ—А–Є–Є –≤–Ї–ї—О—З–µ–љ–Є—П: –Љ—Г–ґ—З–Є–љ—Л –Є –ґ–µ–љ—Й–Є–љ—Л –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 40 –і–Њ 75 –ї–µ—В, –љ–∞–ї–Є—З–Є–µ –°–Ф 2 —В–Є–њ–∞, –љ–∞–ї–Є—З–Є–µ —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–Є –Ф–Я–Э (–њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–є –њ—А–Є –њ–Њ–Љ–Њ—Й–Є —Н–ї–µ–Ї—В—А–Њ–љ–µ–є—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є–Є, –≠–Э–Ь–У).
–Ъ—А–Є—В–µ—А–Є–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П: –°–Ф 1 —В–Є–њ–∞, –≤–Њ–Ј—А–∞—Б—В –Љ–Њ–ї–Њ–ґ–µ 40 –ї–µ—В –Є —Б—В–∞—А—И–µ 75 –ї–µ—В, –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є—П –і—А—Г–≥–Њ–є (–љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є) —Н—В–Є–Њ–ї–Њ–≥–Є–Є, –њ–∞—В–Њ–ї–Њ–≥–Є—П —А–Њ–≥–Њ–≤–Є—Ж—Л.
–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–ї—Г—З–∞–ї–Є –∞–і–µ–Ї–≤–∞—В–љ—Г—О —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й—Г—О –Є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О –Є –±—Л–ї–Є –Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ—Л –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ –≥–ї–Є–Ї–µ–Љ–Є–Є –Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П.
–°–њ–Њ—Б–Њ–± —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –≤—Л–±–Њ—А–Ї–Є –Є–Ј –Є–Ј—Г—З–∞–µ–Љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є. –Т—Л–±–Њ—А–Ї–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–ї–∞—Б—М –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ—Л–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –і–∞–љ–љ—Л—Е —Д–Є–Ј–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤–Ї–ї—О—З–∞–≤—И–µ–≥–Њ —Б–±–Њ—А –∞–љ–∞–Љ–љ–µ–Ј–∞ –Є –ґ–∞–ї–Њ–±, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ј–∞–і–∞–љ–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є, –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Є–і–Њ–≤ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є–љ–Є–Љ–∞–ї–Є —Г—З–∞—Б—В–Є–µ –њ–∞—Ж–Є–µ–љ—В—Л —Б –°–Ф 2 —В–Є–њ–∞ –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э (n=40), –і–Њ—Б—В–Є–≥—И–Є–µ –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л—Е —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –≥–ї–Є–Ї–µ–Љ–Є–Є (HbA1c вЙ§6,5%).
–Ю–њ–Є—Б–∞–љ–Є–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞. –Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –∞–љ—В—А–Њ–њ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Є–Ј–Љ–µ—А–µ–љ–Є–µ —А–Њ—Б—В–∞, –Љ–∞—Б—Б—Л —В–µ–ї–∞, —А–∞—Б—З–µ—В –Ш–Ь–Ґ.
–Т—Л–њ–Њ–ї–љ—П–ї—Б—П –Ј–∞–±–Њ—А –≤–µ–љ–Њ–Ј–љ–Њ–є –Ї—А–Њ–≤–Є –љ–∞—В–Њ—Й–∞–Ї –і–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞, –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Є –і—А—Г–≥–Є—Е –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї—А–Њ–≤–Є.
–Э–µ–є—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М –≠–Э–Ь–У.
–Ф–ї—П –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П —В–Њ–љ–Ї–Є—Е –љ–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–∞—П –±–Є–Њ–њ—Б–Є—П –Ї–Њ–ґ–Є –Є –ї–∞–Ј–µ—А–љ–∞—П –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–∞—П –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є—П —А–Њ–≥–Њ–≤–Є—Ж—Л.
–Ь–µ—В–Њ–і—Л. –§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ (–і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е) –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–Њ—Б—М –Љ–µ—В–Њ–і–Њ–Љ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–є –≠–Э–Ь–У –љ–∞ –њ—А–Є–±–Њ—А–µ Viking IV P Nicolet Biomedical (–°–®–Р). –Ф–ї—П —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є—П –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е –љ–µ—А–≤–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –Љ–∞–ї–Њ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ (n. peroneus) –Є –±–Њ–ї—М—И–µ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ (n. tibialis) –љ–µ—А–≤–Њ–≤ —Б –∞–љ–∞–ї–Є–Ј–Њ–Љ –∞–Љ–њ–ї–Є—В—Г–і—Л –Ь-–Њ—В–≤–µ—В–∞, —Б–Ї–Њ—А–Њ—Б—В–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є—П (–°–†–Т) –Є —А–µ–Ј–Є–і—Г–∞–ї—М–љ–Њ–є –ї–∞—В–µ–љ—В–љ–Њ—Б—В–Є. –Ф–ї—П –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–µ–љ—Б–Њ—А–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М –∞–љ—В–Є–і—А–Њ–Љ–љ–∞—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ –Є–Ї—А–Њ–љ–Њ–ґ–љ–Њ–≥–Њ –љ–µ—А–≤–∞ (n. suralis) —Б –∞–љ–∞–ї–Є–Ј–Њ–Љ –∞–Љ–њ–ї–Є—В—Г–і—Л S-–Њ—В–≤–µ—В–∞ –Є –°–†–Т.
–Я–µ—А—Д–Њ—А–∞—Ж–Є–Њ–љ–љ–∞—П (–Є–љ–≤–∞–Ј–Є–≤–љ–∞—П) –±–Є–Њ–њ—Б–Є—П –Ї–Њ–ґ–Є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞ ¬Ђ–і–µ—А–Љ–Њ-–њ–∞–љ—З¬ї –љ–∞ –±–Њ–Ї–Њ–≤–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –≥–Њ–ї–µ–љ–Є, –њ–Њ–і –Љ–µ—Б—В–љ–Њ–є –∞–љ–µ—Б—В–µ–Ј–Є–µ–є 1% –ї–Є–і–Њ–Ї–∞–Є–љ–Њ–Љ (–≥–ї—Г–±–Є–љ–∞ –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 3 –Љ–Љ, –љ–∞–ї–Њ–ґ–µ–љ–Є–µ —И–≤–Њ–≤ –љ–µ —В—А–µ–±–Њ–≤–∞–ї–Њ—Б—М). –Я–Њ–ї—Г—З–µ–љ–љ—Л–є –Њ–±—А–∞–Ј–µ—Ж –≤–Ї–ї—О—З–∞–ї –≤ —Б–µ–±—П —Н–њ–Є–і–µ—А–Љ–Є—Б –Є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–µ —Б–ї–Њ–Є —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –і–µ—А–Љ—Л (—Б–Њ—Б–Њ—З–Ї–Њ–≤—Л–є –Є —Б–µ—В—З–∞—В—Л–є).
B —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–∞–љ–љ–∞—П –њ—А–Њ—Ж–µ–і—Г—А–∞ –≤—Л–њ–Њ–ї–љ—П–ї–∞—Б—М –і–≤–∞–ґ–і—Л: –Є—Б—Е–Њ–і–љ–Њ –Є —З–µ—А–µ–Ј 5 –Љ–µ—Б. –љ–∞ —Д–Њ–љ–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Є —Г–і–µ—А–ґ–∞–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ –њ—А–µ–і–µ–ї–∞—Е —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є.
–Я–Њ—Б–ї–µ–і—Г—О—Й–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Є —Б–Њ—Б—Г–і–Њ–≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞ –≤ –Ї–Њ–ґ–љ—Л—Е –±–Є–Њ–њ—В–∞—В–∞—Е –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Њ—Б—М –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е –Є–Љ–Љ—Г–љ–Њ–≥–Є—Б—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї.
–Т –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є–љ—В—А–∞—Н–њ–Є–і–µ—А–Љ–∞–ї—М–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Є –Є–љ—В—А–∞–і–µ—А–Љ–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –≤–Њ—И–ї–Њ 40 –±–Є–Њ–њ—В–∞—В–Њ–≤ –Ї–Њ–ґ–Є –Њ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э.
–Т –Ї–∞—З–µ—Б—В–≤–µ –Љ–∞—А–Ї–µ—А–∞ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –±—Л–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –∞–љ—В–Є—В–µ–ї–∞ –Ї –љ–µ–є—А–Њ–њ–µ–њ—В–Є–і—Г PGP 9.5, –Ї–Њ—В–Њ—А—Л–є —И–Є—А–Њ–Ї–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ –Є —П–≤–ї—П–µ—В—Б—П –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–Љ –њ–∞–љ–∞–Ї—Б–Њ–љ–∞–ї—М–љ—Л–Љ –Љ–∞—А–Ї–µ—А–Њ–Љ [10]. –Ь–∞—А–Ї–µ—А–Њ–Љ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ –Ї–Њ–ґ–Є –±—Л–ї –≤—Л–±—А–∞–љ CD34 [11]. –Я—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Љ–Њ—А—Д–Њ–Љ–µ—В—А–Є—П –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–Ј–Њ–≤ –±–Є–Њ–њ—В–∞—В–Њ–≤ –Ї–Њ–ґ–Є —Б –Њ—Ж–µ–љ–Ї–Њ–є —Б—А–µ–і–љ–µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –љ–µ—А–≤–љ—Л—Е –Њ–Ї–Њ–љ—З–∞–љ–Є–є, –Њ–Ї—А–∞—И–µ–љ–љ—Л—Е PGP 9.5, –Є —Б–Њ—Б—Г–і–Њ–≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞, –Њ–Ї—А–∞—И–µ–љ–љ—Л—Е CD34, –≤ –њ—П—В–Є –њ–Њ–ї—П—Е –Ј—А–µ–љ–Є—П –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є √Ч200 –љ–∞ –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–µ AXIOImagerA2 CarlZeissc —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є –Љ–Њ—А—Д–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л.
–Ш–Љ–Љ—Г–љ–Њ–≥–Є—Б—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤—Л–њ–Њ–ї–љ—П–ї–Њ—Б—М –њ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –Љ–µ—В–Њ–і–Є–Ї–µ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –њ–Њ–ї—Г–Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Њ–є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —А–µ–∞–Ї—Ж–Є–є: PGP 9.5 –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ —Б—А–µ–і–љ–µ–Љ—Г –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –Њ–Ї—А–∞—И–µ–љ–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –Њ–Ї–Њ–љ—З–∞–љ–Є–є –≤ –Ї–Њ–ґ–µ –≤ 5 –њ–Њ–ї—П—Е –Ј—А–µ–љ–Є—П –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є √Ч200 –Є √Ч400. –Ь–∞—А–Ї–µ—А PGP 9.5 –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї—Б—П –≤ –≤–Є–і–µ –Ї–Њ—А–Є—З–љ–µ–≤–Њ–≥–Њ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ. –Ю—Ж–µ–љ–Ї–∞ –Є–Љ–Љ—Г–љ–Њ–≥–Є—Б—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є CD34 –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–∞—Б—М –њ—Г—В–µ–Љ –њ–Њ–і—Б—З–µ—В–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –Њ–Ї—А–∞—И–µ–љ–љ—Л—Е —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –≤ –Ї–∞–њ–Є–ї–ї—П—А–∞—Е –Ї–Њ–ґ–Є, –∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ вАФ –њ–Њ —Б—А–µ–і–љ–µ–Љ—Г —З–Є—Б–ї—Г –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ –Њ–Ї—А–∞—И–µ–љ–љ—Л—Е –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ –≤ 5 –њ–Њ–ї—П—Е –Ј—А–µ–љ–Є—П –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є √Ч400. –Ь–∞—А–Ї–µ—А CD34 –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –≤ –≤–Є–і–µ –Ї–Њ—А–Є—З–љ–µ–≤–Њ–≥–Њ –Њ–Ї—А–∞—И–Є–≤–∞–љ–Є—П —Н–љ–і–Њ—В–µ–ї–Є—П —Б–Њ—Б—Г–і–Њ–≤.
–Ф–ї—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї–∞–Ј–µ—А–љ–Њ–є –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є–Є —А–Њ–≥–Њ–≤–Є—Ж—Л –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –≥–µ–є–і–µ–ї—М–±–µ—А–≥—Б–Ї–Є–є —В–Њ–Љ–Њ–≥—А–∞—Д (HRT III) —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —А–Њ–≥–Њ–≤–Є—З–љ–Њ–≥–Њ –Љ–Њ–і—Г–ї—П RostockCornea (RC; HeidelbergEngineering, Heidelberg, Germany).
–Р–љ–∞–ї–Є–Ј –Є –Є–љ—В–µ—А–њ—А–µ—В–∞—Ж–Є—П –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ—Л—Е —Б–љ–Є–Љ–Ї–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О –Њ—А–Є–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ –∞–ї–≥–Њ—А–Є—В–Љ–∞, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–Њ–≥–Њ –≤ –§–У–С–Э–£ ¬Ђ–Э–Ш–Ш–У–С¬ї (–њ–∞—В–µ–љ—В –љ–∞ –Є–Ј–Њ–±—А–µ—В–µ–љ–Є–µ вДЦ 2014145271) [12].
–Э–Њ–≤—Л–є –њ–Њ–і—Е–Њ–і –Ї –Љ–Њ—А—Д–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–Љ—Г –∞–љ–∞–ї–Є–Ј—Г –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ —А–Њ–≥–Њ–≤–Є—Ж—Л (–Э–Т–†) –Њ—Б–љ–Њ–≤–∞–љ –љ–∞ –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–Љ –Њ–њ–Є—Б–∞–љ–Є–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Э–Т–† –Є –∞–ї–≥–Њ—А–Є—В–Љ–µ –≤—Л—З–Є—Б–ї–µ–љ–Є—П –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–Њ–≤ –∞–љ–Є–Ј–Њ—В—А–Њ–њ–Є–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є (—Г–њ–Њ—А—П–і–Њ—З–µ–љ–љ–Њ—Б—В–Є) –Э–Т–† –Є —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ—Б—В–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Э–Т–†. –Ф–ї—П –і–∞–ї—М–љ–µ–є—И–µ–є –Њ–±—А–∞–±–Њ—В–Ї–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Њ—Б—М –∞–≤—В–Њ—А—Б–Ї–Њ–µ –њ—А–Њ–≥—А–∞–Љ–Љ–љ–Њ–µ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ Liner 1.2 S. –Ф–∞–љ–љ—Л–є –Љ–µ—В–Њ–і –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —А—П–і–∞ —Б–Є—Б—В–µ–Љ–љ—Л—Е –љ–µ–є—А–Њ–њ–∞—В–Є–є (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –Ф–Я–Э), –∞ —В–∞–Ї–ґ–µ –Ї–∞–Ї –Ї—А–Є—В–µ—А–Є–є –ї–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є–љ–љ–µ—А–≤–∞—Ж–Є–Є —А–Њ–≥–Њ–≤–Є—Ж—Л [13].
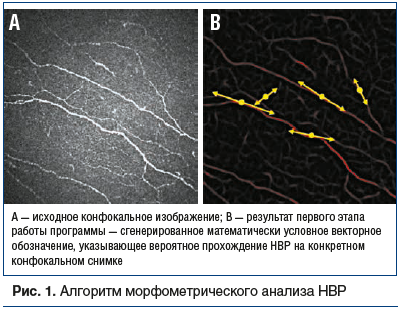
–Э–∞ –њ–µ—А–≤–Њ–Љ —Н—В–∞–њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –∞–≤—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–µ —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є–µ –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ—Л—Е —Ж–Є—Д—А–Њ–≤—Л—Е —Б–љ–Є–Љ–Ї–Њ–≤ —А–Њ–≥–Њ–≤–Є—Ж—Л –Є –Ї–∞—А—В–Є—А–Њ–≤–∞–љ–Є–µ –Э–Т–†: –њ—А–Њ–≥—А–∞–Љ–Љ–∞ –∞–≤—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –Є–љ—В–µ—А–њ—А–µ—В–Є—А—Г–µ—В –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –Є –≥–µ–љ–µ—А–Є—А—Г–µ—В –Ї–∞—А—В—Г –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є—П –Э–Т–† –љ–∞ —Г—З–∞—Б—В–Ї–µ, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–Љ —Н—В–Њ–Љ—Г –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—О. –Т—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–≤—В–Њ–Љ–∞—В–Є–Ј–Є—А–Њ –≤–∞–љ–љ–Њ–≥–Њ —А–∞—Б–њ–Њ–Ј–љ–∞–≤–∞–љ–Є—П –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –Њ—Б–љ–Њ–≤–∞–љ–∞ –љ–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Њ—А–Є–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ –∞–≤—В–Њ—А—Б–Ї–Њ–≥–Њ –∞–ї–≥–Њ—А–Є—В–Љ–∞. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Б –њ–Њ–Љ–Њ—Й—М—О –љ–Њ–≤–Њ–є –њ—А–µ–і–ї–∞–≥–∞–µ–Љ–Њ–є –Љ–µ—В–Њ–і–Є–Ї–Є —Г—З–∞—Б—В–Ї–Є –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –љ–∞—Е–Њ–і—П—Й–Є–µ—Б—П –≤–љ–µ —Д–Њ–Ї—Г—Б–∞, –∞ —В–∞–Ї–ґ–µ –≤ –Њ–±–ї–∞—Б—В—П—Е –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є, –≤—Л–і–µ–ї—П—О—В—Б—П –ї—Г—З—И–µ, —З–µ–Љ –њ—А–Є –≤–Є–Ј—Г–∞–ї—М–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ.
–Э–µ—А–≤–љ–Њ–µ –≤–Њ–ї–Њ–Ї–љ–Њ —А–Њ–≥–Њ–≤–Є—Ж—Л –љ–∞ –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–Њ–Љ —Б–љ–Є–Љ–Ї–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Б–≤–µ—В–ї—Г—О –њ–Њ–ї–Њ—Б—Г –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є —И–Є—А–Є–љ—Л –Є –Є–Ј–≤–Є—В–Њ—Б—В–Є –љ–∞ –±–Њ–ї–µ–µ —В–µ–Љ–љ–Њ–Љ —Д–Њ–љ–µ. –Ъ–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П –∞–≤—В–Њ—А—Б–Ї–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–∞ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Ј–∞–і–∞–љ–љ–Њ–є –Љ–∞—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ—Г–ї—Л –∞–≤—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є –≥–µ–љ–µ—А–Є—А—Г–µ—В –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ—Г—О —В—А–∞–µ–Ї—В–Њ—А–Є—О –њ—А–Њ —Е–Њ–ґ–і–µ–љ–Є—П –љ–µ—А–≤–љ–Њ–≥–Њ –≤–Њ–ї–Њ–Ї–љ–∞ –љ–∞ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–Љ –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–Њ–Љ —Б–љ–Є–Љ–Ї–µ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є ¬Ђ–Є–і–µ–∞–ї—М–љ—Л–є¬ї —Г—З–∞—Б—В–Њ–Ї –љ–µ—А–≤–∞). –Ч–∞—В–µ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —А–∞–Ј–ї–Є—З–љ—Л—Е —Г—З–∞—Б—В–Ї–Њ–≤ –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Б–љ–Є–Љ–Ї–∞ –Є –Њ—Ж–µ–љ–Ї–∞ –Є—Е —Б—А–Њ–і—Б—В–≤–∞ —Б –Ј–∞—А–∞–љ–µ–µ –Љ–∞—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є —Б–≥–µ–љ–µ—А–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–≤–µ—В–ї–Њ–є –њ–Њ–ї–Њ—Б–Њ–є –≤ —З–µ—А–љ–Њ–Љ –Ї–≤–∞–і—А–∞—В–љ–Њ–Љ –њ–Њ–ї–µ. –Я—А–Є —Н—В–Њ–Љ –љ–µ—А–≤–љ–Њ–µ –≤–Њ–ї–Њ–Ї–љ–Њ, –њ—А–Њ—Е–Њ–і—П—Й–µ–µ —З–µ—А–µ–Ј –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О —В–Њ—З–Ї—Г, –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Њ –њ–Њ–і –ї—О–±—Л–Љ —Г–≥–ї–Њ–Љ, –њ–Њ—Н—В–Њ–Љ—Г –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–є —Г—З–∞—Б—В–Њ–Ї –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б—А–∞–≤–љ–Є—В—М —Б —Б–µ—А–Є–µ–є ¬Ђ–Є–і–µ–∞–ї—М–љ—Л—Е¬ї –Љ–Њ–і–µ–ї—М–љ—Л—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–є, –Ї–∞–ґ–і–Њ–µ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –њ–Њ–≤–µ—А–љ—Г—В–Њ –љ–∞ –љ–µ–Ї–Њ—В–Њ—А—Л–є —Г–≥–Њ–ї ќ± –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –≤ –њ—А–µ–і–µ–ї–∞—Е 180¬∞ (—А–Є—Б. 1) [12].
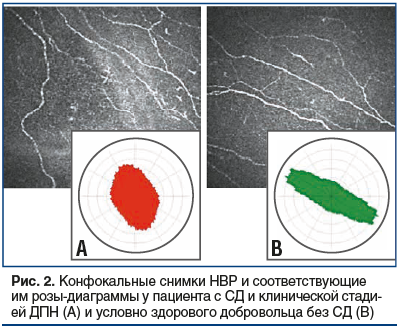
–Э–∞ —Б–ї–µ–і—Г—О—Й–µ–Љ —Н—В–∞–њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ —Б—В–µ–њ–µ–љ–Є –Є–Ј–≤–Є—В–Њ—Б—В–Є –Э–Т–† —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–Њ–≤ –∞–љ–Є–Ј–Њ—В—А–Њ–њ–Є–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є (—Г–њ–Њ—А—П–і–Њ—З–µ–љ–љ–Њ—Б—В–Є) –Э–Т–† –Є —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ—Б—В–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Э–Т–†. –Ф–ї—П –љ–∞–≥–ї—П–і–љ–Њ–є –і–µ–Љ–Њ–љ—Б—В—А–∞—Ж–Є–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П –Є —Б—В—А—Г–Ї—В—Г—А—Л –Э–Т–† –±—Л–ї–Њ –Є—Б ef–Њ–ї—М–Ј–Њ–≤–∞–љ–Њ —Б—Е–µ–Љ–∞—В–Є—З–љ–Њ–µ –Є—Е –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ –≤ –≤–Є–і–µ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–є —А–Њ–Ј—Л-–і–Є–∞–≥—А–∞–Љ–Љ—Л. –†–Њ–Ј–∞-–і–Є–∞–≥—А–∞–Љ–Љ–∞ –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Э–Т–† –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –Њ–±—Й—Г—О —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М –≤—Б–µ—Е –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–є –Э–Т–† –љ–∞ –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–Љ –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–Њ–Љ —Б–љ–Є–Љ–Ї–µ; –њ—А–Є —Н—В–Њ–Љ —З–µ–Љ –±–Њ–ї–µ–µ —А–∞–Ј–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–є —Е–Њ–і –Є —Б—В—А—Г–Ї—В—Г—А–∞ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ (–Ї–∞–Ї –±—Л–≤–∞–µ—В, –љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є), —В–µ–Љ –±–Њ–ї–µ–µ –Њ–Ї—А—Г–≥–ї—Г—О —Д–Њ—А–Љ—Г –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —А–Њ–Ј–∞-–і–Є–∞–≥—А–∞–Љ–Љ–∞. –Э–∞ —А–Є—Б—Г–љ–Ї–µ 2 –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ—Л —В–Є–њ–Є—З–љ—Л–µ –≤–∞—А–Є–∞–љ—В—Л —А–Њ–Ј—Л-–і–Є–∞–≥—А–∞–Љ–Љ—Л –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Э–Т–† —Г –њ–∞—Ж–Є–µ–љ—В–∞ —Б –°–Ф 2 —В–Є–њ–∞ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є (—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є) —Б—В–∞–і–Є–µ–є –Ф–Я–Э, –∞ —В–∞–Ї–ґ–µ —Г—Б–ї–Њ–≤–љ–Њ –Ј–і–Њ—А–Њ–≤–Њ–≥–Њ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞ –±–µ–Ј –°–Ф. –Т —Б–ї—Г—З–∞–µ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —В–Њ–љ–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ —А–Њ–Ј–∞-–і–Є–∞–≥—А–∞–Љ–Љ–∞ –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —Е–∞—А–∞–Ї—В–µ—А–љ–Њ–µ –Є–Ј–Њ–Љ–µ—В—А–Є—З–љ–Њ–µ —Б—В—А–Њ–µ–љ–Є–µ, –±–Њ–ї–µ–µ –њ—А–Є–±–ї–Є–ґ–µ–љ–љ–Њ–µ –њ–Њ —Б–≤–Њ–µ–є —Д–Њ—А–Љ–µ –Ї –Ї—А—Г–≥—Г. –Ґ–∞–Ї—Г—О —Д–Њ—А–Љ—Г —А–Њ–Ј—Л-–і–Є–∞–≥—А–∞–Љ–Љ—Л –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М —А–∞–Ј–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–Љ –Є –±–Њ–ї–µ–µ –Є–Ј–≤–Є—В—Л–Љ —Е–Њ–і–Њ–Љ –Э–Т–†. –Т –љ–Њ—А–Љ–µ —Д–Њ—А–Љ–∞ —А–Њ–Ј—Л-–і–Є–∞–≥—А–∞–Љ–Љ—Л —Б—Е–Њ–ґ–∞ —Б —Г–і–ї–Є–љ–µ–љ–љ—Л–Љ –Њ–≤–∞–ї–Њ–Љ, –≤—Л—В—П–љ—Г—В—Л–Љ –≤ —В—Г –Є–ї–Є –Є–љ—Г—О —Б—В–Њ—А–Њ–љ—Г, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –Њ–і–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–≥–Њ —Е–Њ–і–∞ –Э–Т–† [12].
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј. –Ь–Є–љ–Є–Љ–∞–ї—М–љ–Њ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–∞–±–ї—О–і–µ–љ–Є–є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –њ–Њ —Д–Њ—А–Љ—Г–ї–∞–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —В–∞–±–ї–Є—Ж –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П —А–∞–Ј–Љ–µ—А–∞ –≤—Л–±–Њ—А–Ї–Є –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П 80% –Љ–Њ—Й–љ–Њ—Б—В–Є (ќ±=0,05, –і–≤—Г—Б—В–Њ—А–Њ–љ–љ—П—П).

–Т—Б–µ –і–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –Ї–∞–Ї —Б—А–µ–і–љ–µ–µ ¬± —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ –і–ї—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ –Є –Ї–∞–Ї –Љ–µ–і–Є–∞–љ–∞ –Є 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї –і–ї—П –њ–µ—А–µ–Љ–µ–љ–љ—Л—Е —Б —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ, –Њ—В–ї–Є—З–љ—Л–Љ –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ. –Ъ–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –њ–µ—А–µ–Љ–µ–љ–љ—Л–µ –њ—А–Є–≤–µ–і–µ–љ—Л –≤ –∞–±—Б–Њ–ї—О—В–љ—Л—Е –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л—Е (%) –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П—Е. –†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Њ—В–ї–Є—З–∞–ї–Є—Б—М –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ, –њ–Њ—Н—В–Њ–Љ—Г –і–ї—П —Б—А–∞–≤–љ–µ–љ–Є—П –Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≥—А—Г–њ–њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –љ–µ–њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–є –Ї—А–Є—В–µ—А–Є–є –Т–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞, –і–ї—П —Б—А–∞–≤–љ–µ–љ–Є—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≥—А—Г–њ–њ вАФ –Ї—А–Є—В–µ—А–Є–є –Ь–∞–љ–љ–∞ вАФ –£–Є—В–љ–Є.
–≠—В–Є—З–µ—Б–Ї–∞—П —Н–Ї—Б–њ–µ—А—В–Є–Ј–∞. –Я—А–Њ–≤–µ–і–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ –Њ–і–Њ–±—А–µ–љ–Њ –Ь–µ–ґ–≤—Г–Ј–Њ–≤—Б–Ї–Є–Љ –Ї–Њ–Љ–Є—В–µ—В–Њ–Љ –њ–Њ —Н—В–Є–Ї–µ (–њ—А–Њ—В–Њ–Ї–Њ–ї вДЦ 10-11 –Њ—В 17.11.2011). –Т—Б–µ —Г—З–∞—Б—В–љ–Є–Ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–і–њ–Є—Б–∞–ї–Є ¬Ђ–Ш–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ—Л–є –ї–Є—Б—В–Њ–Ї –њ–∞—Ж–Є–µ–љ—В–∞¬ї.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є–љ—П–ї–Є —Г—З–∞—Б—В–Є–µ 40 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–є (–њ—А–Є –њ–Њ–Љ–Њ—Й–Є –≠–Э–Ь–У) —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э, –љ–∞—Е–Њ–і–Є–≤—И–Є–µ—Б—П –≤ —Ж–µ–ї–µ–≤–Њ–Љ –і–Є–∞–њ–∞–Ј–Њ–љ–µ –≥–ї–Є–Ї–µ–Љ–Є–Є (HbA1cвЙ§6,5%) –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Є –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П (5 –Љ–µ—Б.).
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –љ–∞–ї–Є—З–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, –њ–Њ –њ–Њ–≤–Њ–і—Г –Ї–Њ—В–Њ—А–Њ–є –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б–ї–µ–і—Г—О—Й–µ–µ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ: –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ –Є–ї–Є —Б–∞—А—В–∞–љ—Л (87%), ќ≤-–±–ї–Њ–Ї–∞—В–Њ—А—Л (50%), –і–Є—Г—А–µ—В–Є–Ї–Є (60%), –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ (24%). –Т —Б–≤—П–Ј–Є —Б –љ–∞–ї–Є—З–Є–µ–Љ –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–Є –њ–Њ—З—В–Є –њ–Њ–ї–Њ–≤–Є–љ–∞ (48%) –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О —Б—В–∞—В–Є–љ–∞–Љ–Є. –•–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ.
–Т—Л–±—Л–≤—И–Є—Е –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ј–∞ –≤–µ—Б—М –њ–µ—А –Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ –±—Л–ї–Њ.
–Э–∞ —Д–Њ–љ–µ —Г–ї—Г—З—И–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –Є –Є—Е —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 5 –Љ–µ—Б. –њ–Њ –і–∞–љ–љ—Л–Љ –≠–Э–Ь–У –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –∞–Љ–њ–ї–Є—В—Г–і—Л S-–Њ—В–≤–µ—В–∞ –Є–Ї—А–Њ–љ–Њ–ґ–љ–Њ–≥–Њ –љ–µ—А–≤–∞ (—А=0,010).
–І–µ—А–µ–Ј 5 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ —Б–љ–Є–ґ–µ–љ–Є—П –Є —Г–і–µ—А–ґ–∞–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ –њ—А–µ–і–µ–ї–∞—Е —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–µ–љ–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є–Є –Ї–Њ–ґ–љ–Њ–≥–Њ –ї–Њ—Б–Ї—Г—В–∞, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≥–Є–њ–µ—А–Ї–µ—А–∞—В–Њ–Ј–∞ —Н–њ–Є–і–µ—А–Љ–Є—Б–∞ (p=0,025) (—А–Є—Б. 3)

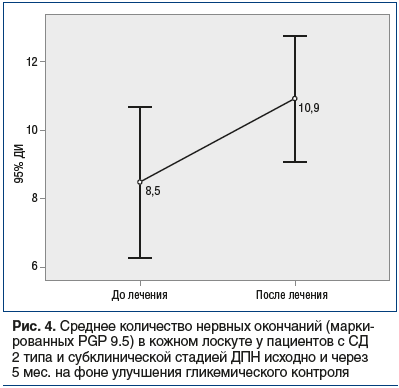
–Т —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –і–µ—А–Љ–µ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤ 1,5 —А–∞–Ј–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —В–Њ–љ–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –њ—А–Њ—П–≤–ї—П—О—Й–µ–µ—Б—П –≤ –≤–Є–і–µ —Г—Б–Є–ї–µ–љ–Є—П —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є –Љ–∞—А–Ї–µ—А–∞ PGP 9.5 (p=0,004) (—А–Є—Б. 4).
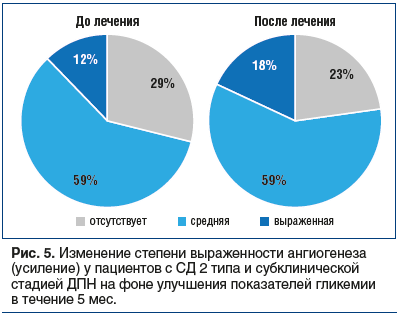
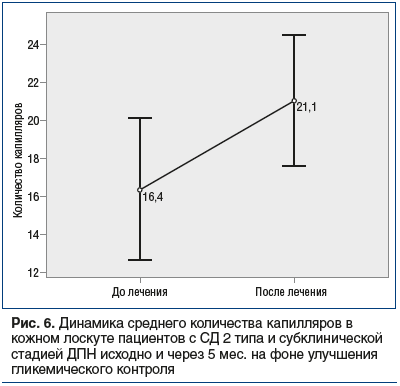
–Ґ–∞–Ї–ґ–µ –≤ —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ –і–µ—А–Љ–µ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Љ–∞—А–Ї–µ—А–∞ CD34 (p=0,007) вАФ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П —Г–ї—Г—З—И–µ–љ–Є—П –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Є —Г—Б–Є–ї–µ–љ–Є—П –∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј–∞ (pвЙ§0,049) (—А–Є—Б. 5, 6).
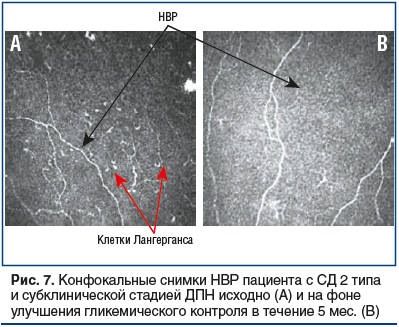
–Т –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э –љ–∞ —Д–Њ–љ–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Є –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–і–µ—А–ґ–∞–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П HbA1c, –њ—А–Є–±–ї–Є–ґ–µ–љ–љ–Њ–≥–Њ –Ї –љ–Њ—А–Љ–µ (HbA1cвЙ§6,5%), –Њ—В–Љ–µ—З–µ–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Є–Ј–≤–Є—В–Њ—Б—В–Є —В–Њ–љ–Ї–Є—Е –Э–Т–† (pвЙ§0,05) –Є –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –Ї–ї–µ—В–Њ–Ї –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ (–Ї–ї–µ—В–Њ–Ї –Ы–∞–љ–≥–µ—А–≥–∞–љ—Б–∞) (—А–Є—Б. 7).
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–Њ–≤ –∞–љ–Є–Ј–Њ—В—А–Њ–њ–Є–Є –Є —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ—Б—В–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Э–Т–† (—А–Њ–Ј–∞-–і–Є–∞–≥—А–∞–Љ–Љ–∞ –њ—А–Є–Њ–±—А–µ–ї–∞ –±–Њ–ї–µ–µ –≤—Л—В—П–љ—Г—В—Г—О —Д–Њ—А–Љ—Г, –њ—А–Є–±–ї–Є–ґ–µ–љ–љ—Г—О –Ї –љ–Њ—А–Љ–µ) (—А–Є—Б. 8).

–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–і–љ–Є–Љ –Є–Ј —Б–∞–Љ—Л—Е –∞–Ї—В—Г–∞–ї—М–љ—Л—Е –Њ—Б—В–∞–µ—В—Б—П –≤–Њ–њ—А–Њ—Б –Њ –≤–ї–Є—П–љ–Є–Є —Г–ї—Г—З—И–µ–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –Ф–Я–Э. –Ф–∞–љ–љ—Л–µ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б —Г—З–∞—Б—В–Є–µ–Љ –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 1 —В–Є–њ–∞ –љ–∞–≥–ї—П–і–љ–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞–њ—А—П–Љ—Г—О —Б–≤—П–Ј–∞–љ —Б–Њ –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є HbA1c [14, 15]. –І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –Є–Ј—Г—З–µ–љ–Є–µ –°–Ф 2 —В–Є–њ–∞, —В–Њ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –Њ—З–µ–љ—М –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ. –Ф–Њ–ї–≥–Њ–µ –≤—А–µ–Љ—П –њ–Њ–ї–∞–≥–∞–ї–Є, —З—В–Њ –ґ–µ—Б—В–Ї–Є–є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Є–є –Ї–Њ–љ—В—А–Њ–ї—М —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ф–Я–Э —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –Њ–і–љ–∞–Ї–Њ –≤ —А—П–і–µ —А–∞–±–Њ—В –Ј–∞—А—Г–±–µ–ґ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –љ–∞ —Г–Ї–∞–Ј–∞–љ–љ—Л–µ —А–Є—Б–Ї–Є –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ [16]. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞–≥–ї—П–і–љ–Њ –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г—О—В, —З—В–Њ –љ–µ–є—А–Њ–њ–∞—В–Є—П, –≤—Л—П–≤–ї—П–µ–Љ–∞—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—А–µ–і–Є–∞–±–µ—В–Њ–Љ (–љ–∞ —Б—В–∞–і–Є–Є –љ–∞—А—Г—И–µ–љ–Є—П —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Ї –≥–ї—О–Ї–Њ–Ј–µ), –њ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ —Б—Е–Њ–ґ–∞ —Б –љ–µ–є—А–Њ–њ–∞—В–Є–µ–є, –і–Є–∞–≥–љ–Њ—Б—В–Є—А—Г–µ–Љ–Њ–є –њ—А–Є –°–Ф [17вАУ19].
–Т –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–Є –њ—А–Є—Ж–µ–ї—М–љ–Њ –Є–Ј—Г—З–µ–љ—Л –њ–∞—Ж–Є–µ–љ—В—Л —Б –љ–µ–±–Њ–ї—М—И–Њ–є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –°–Ф (–Њ—В –љ–µ–і–∞–≤–љ–Њ –≤—Л—П–≤–ї–µ–љ–љ–Њ–≥–Њ –і–Њ 5-–ї–µ—В–љ–µ–≥–Њ) –Є –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э, —З—В–Њ–±—Л –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ —А–∞–љ–Њ –њ–Њ–њ—Л—В–∞—В—М—Б—П –≤—Л—П–≤–Є—В—М –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–љ–∞—Е –Є –Њ—Ж–µ–љ–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Њ–±—А–∞—В–Є–Љ–Њ—Б—В–Є –≤—Л—П–≤–ї–µ–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–∞ —Д–Њ–љ–µ —Б—В–Њ–є–Ї–Њ–є –і–ї–Є—В–µ–ї—М–љ–Њ–є –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П.
–Э–∞ —Д–Њ–љ–µ —Г–ї—Г—З—И–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –Є –Є—Е —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 5 –Љ–µ—Б. –њ–Њ –і–∞–љ–љ—Л–Љ –≠–Э–Ь–У –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –∞–Љ–њ–ї–Є—В—Г–і—Л S-–Њ—В–≤–µ—В–∞ –Є–Ї—А–Њ–љ–Њ–ґ–љ–Њ–≥–Њ –љ–µ—А–≤–∞. –Ф–∞–љ–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В –Њ—В—А–∞–ґ–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –∞–Ї—Б–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В–∞ –њ–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ–Љ—Г –љ–µ—А–≤–љ–Њ–Љ—Г –≤–Њ–ї–Њ–Ї–љ—Г, –∞ –Ј–љ–∞—З–Є—В, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Њ–±—А–∞—В–Є–Љ–Њ—Б—В–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ (—А–µ–Є–љ–љ–µ—А–≤–∞—Ж–Є—О). –°—Е–Њ–ґ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–µ–љ—Л –≤ —П–њ–Њ–љ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ–Њ–Ї–∞–Ј–∞–≤—И–µ–Љ, —З—В–Њ –≤—Б–µ —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л —Г–ї—Г—З—И–∞–ї–Є—Б—М –њ—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –Є —Г–і–µ—А–ґ–∞–љ–Є–Є –љ–Њ—А–Љ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ (—Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ HbA1cвЙ§6,5%) [20]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і –Њ —В–Њ–Љ, —З—В–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–Њ-–њ—А–µ–ґ–љ–µ–Љ—Г —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ–Є —Г—Б–ї–Њ–≤–Є—П–Љ–Є –і–ї—П —Б–Њ—Е—А–∞–љ–µ–љ–Є—П —Б—В—А—Г–Ї—В—Г—А—Л –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ.
–Т—Л—П–≤–ї–µ–љ–љ–Њ–µ –≤ –і–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–ї–Њ—В–љ–Њ—Б—В–Є –Є–љ—В—А–∞—Н–њ–Є–і–µ—А–Љ–∞–ї—М–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ (–Я–Ш–Э–Т) –њ—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ —Г–і–µ—А–ґ–∞–љ–Є–Є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞—И–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –≤ –Њ–±–Ј–Њ—А–µ –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Њ–≤ (–Р–Р–°–Х) –і–∞–љ–љ—Л—Е –Њ –Ф–Я–Э, –≥–і–µ —Н–Ї—Б–њ–µ—А—В–љ–Њ–є –Ї–Њ–Љ–Є—Б—Б–Є–µ–є –±—Л–ї —Б–і–µ–ї–∞–љ –≤—Л–≤–Њ–і –Њ —В–Њ–Љ, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Я–Ш–Э–Т —П–≤–ї—П–µ—В—Б—П —А–∞–љ–љ–Є–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –њ—А–µ–і–Є–∞–±–µ—В–∞ –Є –°–Ф. –Ю–і–љ–∞–Ї–Њ –њ—А–Є —Н—В–Њ–Љ –њ–Њ–і—З–µ—А–Ї–љ—Г—В–Њ, —З—В–Њ —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—П –Є–љ—В—А–∞—Н–њ–Є–і–µ—А–Љ–∞–ї—М–љ—Л—Е –љ–µ—А–≤–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–∞ –ї–Є—И—М –њ—А–Є —Б—В–Њ–є–Ї–Њ–є –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ (–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ —Б –њ–µ—А–≤—Л—Е –і–љ–µ–є –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–Є –і–Є–∞–≥–љ–Њ–Ј–∞ –°–Ф) –Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞: –Њ—В–Ї–∞–Ј–µ –Њ—В –Ї—Г—А–µ–љ–Є—П –Є —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –∞–ї–Ї–Њ–≥–Њ–ї—П, —Б–љ–Є–ґ–µ–љ–Є–Є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є —Б–Њ–±–ї—О–і–µ–љ–Є–Є —А–µ–ґ–Є–Љ–∞ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–Є [21].
–Я—А–Є –Њ—Ж–µ–љ–Ї–µ –≤–ї–Є—П–љ–Є—П —Б—В—А–Њ–≥–Њ–≥–Њ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –њ–ї–Њ—В–љ–Њ—Б—В–Є –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –≤ —А–Њ–≥–Њ–≤–Є—Ж–µ –њ–Њ –і–∞–љ–љ—Л–Љ –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є–Є —А–Њ–≥–Њ–≤–Є—Ж—Л –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –Є —Г–і–µ—А–ґ–∞–љ–Є–µ —Ж–µ–ї–µ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є –≥–ї–Є–Ї–µ–Љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 5 –Љ–µ—Б. (HbA1cвЙ§6,5вАУ6,3%) –њ—А–Є–≤–Њ–і–Є—В –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Є–Ј–≤–Є—В–Њ—Б—В–Є –Э–Т–† (pвЙ§0,05), –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є—О –Ї–ї–µ—В–Њ–Ї –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ (–Ї–ї–µ—В–Њ–Ї –Ы–∞–љ–≥–µ—А–≥–∞–љ—Б–∞) –Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –Є–Ј–Љ–µ–љ–µ–љ–Є—О –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–Њ–≤ –∞–љ–Є–Ј–Њ—В—А–Њ–њ–Є–Є –Є —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ—Б—В–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є –Э–Т–†. –Ю–і–љ–∞–Ї–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–¶ 5 –і–∞–љ–љ—Л–µ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –љ–µ —Г –≤—Б–µ—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —З—В–Њ –Љ–Њ–ґ–µ—В –≥–Њ–≤–Њ—А–Є—В—М –ї–Є–±–Њ –Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Г–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –Њ—В—А–µ–Ј–Ї–∞ –і–ї—П –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –ї–Є–±–Њ –Њ —В–Њ–Љ, —З—В–Њ —В–Њ–ї—М–Ї–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї—А–Њ–≤–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є. –Я–Њ—Е–Њ–ґ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Yorek et al. [22], –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤–ї–Є—П–љ–Є–µ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ —В–Њ–љ–Ї–Є—Е –љ–¶ 5—А–≤–Њ–≤ —А–Њ–≥–Њ–≤–Є—Ж—Л –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї—Г—О –љ–µ–є—А–Њ–њ–∞—В–Є—О –љ–∞ –Љ–Њ–і–µ–ї–Є —Б—В—А–µ–њ—В–Њ–Ј–Њ—В–Њ—Ж–Є–љ-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ —Г –Љ—Л—И–µ–є.
–Ф–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –Є–ї–Є –Њ–њ—А–Њ–≤–µ—А–ґ–µ–љ–Є—П –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –і–∞–ї—М–љ–µ–є—И–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б —Г—З–∞—Б—В–Є–µ–Љ –±–Њ–ї—М—И–µ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –≤ –Њ—З–µ—А–µ–і–љ–Њ–є —А–∞–Ј –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –Љ–љ–µ–љ–Є–µ –Њ —В–Њ–Љ, —З—В–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї—Г –Ф–Я–Э –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –љ–∞ —Б–∞–Љ—Л—Е —А–∞–љ–љ–Є—Е —Н—В–∞–њ–∞—Е —А–∞–Ј–≤–Є—В–Є—П –°–Ф –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –љ–µ —В–Њ–ї—М–Ї–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ, –љ–Њ –Є –љ–µ–є—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—В–Њ–і–Њ–≤ –њ—Г–љ–Ї—Ж–Є–Њ–љ–љ–Њ–є –±–Є–Њ–њ—Б–Є–Є –Ї–Њ–ґ–Є –Є/–Є–ї–Є –Ї–Њ–љ—Д–Њ–Ї–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Б–Ї–Њ–њ–Є–Є —А–Њ–≥–Њ–≤–Є—Ж—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ—Б–љ–Њ–≤–љ—Л—Е –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї –і–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –Ф–Я–Э –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Њ–і–љ–∞–Ї–Њ –Њ–±–∞ –Љ–µ—В–Њ–і–∞ –Є–Љ–µ—О—В —А–Ц f–і –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–є –і–ї—П –њ–Њ–≤—Б–µ–Љ–µ—Б—В–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Т –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є –Љ–Њ—А—Д–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П —В–Њ–љ–Ї–Є—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –ї–Є—И—М –≤ –љ–∞—Г—З–љ—Л—Е —Ж–µ–ї—П—Е –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є.
–Ь–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ –њ—А–Є–±–ї–Є–ґ–µ–љ–Є–µ –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –Ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Ј–љ–∞—З–µ–љ–Є—П–Љ –≥–ї—О–Ї–Њ–Ј—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Б—В–∞–і–Є–µ–є –Ф–Я–Э —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –Њ–±—А–∞—В–Є–Љ–Њ—Б—В–Є –љ–∞—А—Г—И–µ–љ–Є–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ—А–Є —А–∞–љ–љ–µ–Љ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–µ.












