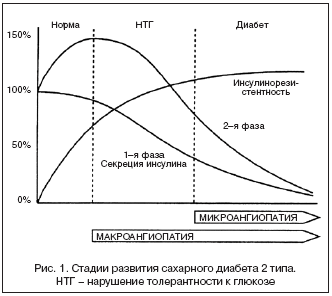
Согласно современным представлениям основу патогенеза сахарного диабета 2 типа составляют два фундаментальных патофизиологических дефекта:
• сниженная чувствительность периферических тканей к инсулину – инсулинорезистентность (ИР);
• нарушенная функция ?–клеток поджелудочной железы.
К моменту возникновения сахарного диабета 2 типа (СД 2) у большинства пациентов уже присутствуют оба эти фактора [21].
В начале у генетически предрасположенных лиц (задолго до появления симптомов СД 2, по крайней мере, не менее чем за 10 лет) развивается ИР (рис. 1). На этом этапе наблюдается снижение поступления глюкозы в инсулинозависимые ткани (жировая, мышечная) и повышается продукция глюкозы печенью.
Но адекватная способность ?–клеток компенсировать гипергликемию повышенной секрецией инсулина способствует сохранению гомеостаза глюкозы. Дальнейшее сохранение или нарастание ИР и прогрессирование нарушения секреции инсулина приводят к нарушенной толерантности (НТГ) к глюкозе или СД 2. При хронической персистирующей гипергликемии (глюкозотоксичность) значительно снижается способность оставшихся ?–клеток отвечать адекватной секрецией инсулина на острую стимуляцию глюкозой. Отсутствие ответа ?–клеток на поступающую глюкозу сопровождается нарушением первой и второй фаз секреции инсулина.
Глюкозотоксичность, как состояние длительной гипергликемии, является одной из причин вторичной инсулинорезистентности, способствуя десенситизации ?–клеток, что проявляется ухудшением их секреторной активности. В свою очередь, некоторые аминокислоты, в частности, глутамин, значительно влияют на действие инсулина, модулируя поглощение глюкозы. В этих случаях наблюдаемая десенситизация является следствием образования продуктов обмена – гексозаминов (гексозаминовый шунт).
Гипергликемия и гиперинсулинемия, бесспорно, могут рассматриваться, как независимые факторы риска сердечно–сосудистых заболеваний. Неслучайно Американская кардиологическая ассоциация причислила СД 2 к сердечно–сосудистым заболеваниям [10].
Фоновая и постпрандиальная гипергликемия запускают ряд патологических механизмов, которые участвуют в развитии осложнений. В результате хронической гипергликемии происходит интенсивное образование свободных радикалов, которые могут связываться с молекулами липидов и приводить к раннему развитию атеросклероза.
При СД 2 типа нарушение обмена глюкозы сочетается с изменениями постпрандиального уровня различных липидов, в том числе и триглицеридов.
Дислипидемия – наиболее неблагоприятный прогностический фактор. Ее характерные признаки при СД 2: гипертриглицеридемия, снижение уровня ЛПВП и пограничные уровни липопротеидов низкой плотности (ЛПНП) со сдвигом их состава в сторону высокоатерогенных мелких плотных ЛПНП [17]. Такие же признаки встречаются при синдромах, протекающих с ИР (метаболический синдром) [30].
Нарушение липидного обмена с повышением высвобождения свободных жирных кислот (СЖК) из жировых абдоминальных депо и их избыточное накопление в островках поджелудочной железы приводят к снижению функциональной активности ?–клеток (липотоксичность), наблюдаемому при СД 2. В свою очередь, абдоминальное ожирение связано с повышенным содержанием в системе воротной вены СЖК, препятствующих адекватной работе печени в очищении крови от инсулина. Все это приводит к увеличению синтеза липопротеидов и как следствие – ведет к развитию инсулинорезистентности, т.е. к СД 2 и атеросклерозу, а также повышению АД.
Риск ИБС у пациентов с СД 2 при гипертриглицеридемии возрастает в 2 раза, при снижении уровня ЛПВП – в 4 раза, а при преобладании мелких плотных ЛПНП – в 6 раз [8].
Анализ данных UKPDS показал, что повышение уровня гликогемоглобина только на 1% повышает риск смертности, связанный с диабетом, на 21%, инфаркта миокарда на 14%, болезней периферических сосудов на 43%, микрососудистых осложнений на 37%, экстракции катаракты на 19%, что требует более жесткого контроля компенсации углеводного обмена [35].
В соответствии с рекомендациями European Diabetes Policy Group (1998–1999) приняты более жесткие критерии компенсации углеводного (табл. 1) и липидного обменов (табл. 2).
Учитывая патогенетические процессы, лежащие в основе сахарного диабета, тактика лечения должна быть направлена как на уменьшение инсулинорезистентности, так и на улучшение функции ?–клеток.
Исследование UKPDS убедительно продемонстрировало естественное прогрессирующее течение СД 2 (функция ?–клеток ухудшается со скоростью 5% в год). Эти данные диктуют необходимость постоянного усиления сахароснижающей терапии с целью сохранения гликемического контроля, в связи с чем возникает потребность в комбинированной терапии.
Наиболее выраженный сахароснижающий эффект продемонстрирован при применении комбинации препаратов сульфонилмочевины и бигуанидов (табл. 3) [16,19,26].
В настоящее время пациентам с СД 2 одновременно с мероприятиями по изменению образа жизни назначается метформин. При отсутствии противопоказаний метформин является препаратом первой линии фармакотерапии СД 2.
В 1956–1957 гг. для клинического применения были предложены препараты фенформин и буформин (группа бигуанидов). Но при дальнейшем анализе опубликованных данных из–за способности увеличивать частоту развития лактатацидоза были запрещены в клинической практике [4]. В настоящее время из группы бигуанидов применяется метформин.
Интерес к метформину значительно возрос после публикации результатов UKPDS в 1998 г. Научные результаты убедительно продемонстрировали, что прием препарата приводил к снижению риска сосудистых осложнений СД на 32 %, смертности, связанной с СД, на 42 %, общей смертности на 36%, инфаркта миокарда на 39%, инсульта на 41 %. В последующем другими научными исследованиями было подтверждено кардиопротективное действие метформина. Антигипергликемическое действие метформина обусловлено несколькими механизмами:
• усиление утилизации глюкозы путем анаэробного гликолиза;
• уменьшение продукции глюкозы печенью;
• уменьшение всасывания глюкозы в желудочно– кишечном тракте;
• увеличение потребления глюкозы мышечной и жировой тканями;
• усиление действия инсулина;
• увеличение числа рецепторов инсулина на клеточной мембране;
• увеличение числа мест транспорта глюкозы в тканях, чувствительных к инсулину.
Гиперинсулинемия, являющаяся при ИР компенсаторной реакцией, играет важную роль в развитии сердечно–сосудистых осложнений и ассоциируется с артериальной гипертензией, атерогенной дислипидемией, абдоминальным ожирением, повышенной агрегацией тромбоцитов и угнетенной фибринолитической активностью. При применении метформина у пациентов СД 2 наблюдается снижение ИР [36,37]. Препарат также благоприятно действует на метаболизм липидов. Под влиянием метформина на 10–30 % снижается окисление свободных жирных кислот [36,11], уровень триглицеридов [25,16,18]. Лечение метформином снижает уровень общего холестерина и ЛПНП [16,31,32], в то время как уровень ЛПВП не меняется [31,32]. Метформин снижает свободнорадикальное окисление и уменьшает степень окисления липидов путем снижения уровня глюкозы в крови [33].
Многочисленные научные исследования показали, что метформин оказывает положительное влияние на систему гемостаза: его действие на систему свертывания связано с уменьшением уровней ингибитора тканевого активатора плазминогена–1 [27] и фактора Виллебранда [13], угнетением агрегации тромбоцитов [24]. Сегодня метформин по праву можно назвать препаратом антиатерогенного действия (рис. 2).
Метформин снижает не только риск сердечно–сосудистых осложнений, но и может, согласно результатам исследования DPP, предотвращать или отсрочить развитие СД 2 типа у лиц в доклиническом периоде этого заболевания [14].
Перечисленные положительные эффекты метформина можно подразделить на: 1) прямые – улучшение фибринолиза, гемореологических показателей, снижение скорости развития атеросклероза, неоваскуляризации и тромбообразования, гликирования белков и окислительного стресса и 2) непрямые – снижение гликемии, инсулинемии и инсулиновой резистентности.
Наиболее грозное потенциальное осложнение терапии бигуанидами – молочнокислый ацидоз (лактатацидоз). Однако анализ данных литературы по метформину, ассоциированный с лактатацидозом, показывает минимальную вероятность развития этого состояния на фоне приема препарата.
Риск развития лактатацидоза увеличивается у пациентов, имеющих еще до назначения метформина гипоксический фон. Среди этих состояний можно выделить выраженную декомпенсацию СД 2, диабетический кетоацидоз, почечную или печеночную недостаточность, злоупотребление алкоголем, а также тяжелые сердечно–сосудистые заболевания и заболевания легких, анемии фолиево–, В12– и железодефицитные. Перечисленные состояния являются абсолютным противопоказанием к применению бигуанидов.
Подбор дозы метформина следует проводить постепенно (в течение 1–2 месяцев). Начальная доза составляет 500 мг вечером. Такая же доза рекомендуется для комбинированной с глимепиридом терапиии. Через 5–7 дней при отсутствии побочного действия со стороны желудочно–кишечного тракта, доза увеличивается до 850–1000 мг. Терапевтические дозы составляют 1–2 г/сут. 1–2 раза в день. Максимальная терапевтическая доза составляет 2,5 г/сут., оптимальным препаратом для подбора дозировки и поддерживающей терапии может являться Багомет 500, производства «Лабораториос Баго». Принимается «Багомет» во время или сразу после еды.
В настоящее время успешно применяется пролонгированная форма метформина – Багомет 850 мг, разработанная компанией «Лабораториос Баго». Препарат содержит 850 мг метформина в специальной форме «гидрофильная матрица», что обеспечивает замедленное, близкое к физиологическому уровню, высвобождение активного вещества. Это приводит к отсутствию резких изменений концентрации препарата в кишечнике и значительному снижению нежелательных побочных эффектов со стороны ЖКТ.
Первым показанием для назначения препаратов сульфонилмочевины является невозможность достижения адекватного гликемического контроля СД 2 типа на фоне предпринятых мер по изменению образа жизни вместе с максимально переносимыми дозами метформина. Уровень гликированного гемоглобина при этом будет либо соответствовать 7%, либо превысит этот уровень.
Производные сульфонилмочевины (ПСМ) начали применять в клинике с середины 50–х годов прошлого века. Еще в 1970 году в исследовании UGDP было отмечено повышение смертности от инфаркта миокарда при лечении ПСМ 1– го поколения [34]. Сегодня в мире для лечения СД 2 применяются препараты сульфонилмочевины второй и третьей генерации.
Производные сульфонилмочевины представлены следующими препаратами:
• глибенкламид
• глипизид
• гликлазид
• гликвидон
• глимепирид
Механизм действия ПСМ основан на взаимодействии со специфическими белками–рецепторами (SUR1) АТФ–зависимых К+–каналов на поверхности ?–клеток. Далее происходит закрытие этих каналов и деполяризация мембраны. Открытие вслед за этим кальциевых каналов обеспечивает поступление кальция внутрь ?–клетки и стимуляцию секреции инсулина путем экзоцитоза из секреторных гранул. Однако похожие рецепторы имеются и в других тканях, в частности, в клетках миокарда, некоторых нейронах мозга. В мышце сердца АТФ–зависимые калиевые каналы играют ключевую роль в процессе ишемического прекондиционирования, т.е. подготовке миокарда к повторным эпизодам ишемии [29]. Это эндогенный защитный механизм, повышающий устойчивость клеток миокарда к повторным эпизодам ишемического повреждения.
Нарушение этого механизма может, например, способствовать распространению зоны некроза при инфаркте миокарда.
Взаимодействие «неселективных» производных сульфонилмочевины (ПСМ) с рецепторами кардиомиоцитов нивелирует их благоприятный эффект, связанный со снижением гипергликемии.
Учитывая, что пациенты с СД 2 типа имеют повышенный риск развития ИБС, инсульта, желательно было бы использовать лекарственные средства, оказывающие селективное действие по отношению к ?–клеткам.
Учитывая вышеизложенное, оптимальный сахароснижающий препарат у больных СД 2 должен соответствовать ряду требований:
• лекарственный препарат должен обладать высоким сродством с рецепторами СМ ?–клеток, а также свободно и обратимо взаимодействовать с ними, что позволяет получить эффективный результат при более низких дозах препарата;
• препарат не должен вызывать гиперинсулинемию натощак, но должен повышать секрецию инсулина после еды, а также улучшать чувствительность к инсулину на уровне тканей и печени;
• препарат не должен вызывать прибавки массы тела в случаях его длительного применения;
• препарат должен обеспечивать низкий риск развития гипогликемий (что особенно важно у пациентов пожилого возраста);
• должно отсутствовать взаимодействие сахароснижающего препарата с сердечно–сосудистыми К+ АТФ–зависимыми каналами.
Одним из таких препаратов является глимепирид, который относится к третьей генерации ПСМ. Главным механизмом действия глимепирида является усиление секреции и высвобождения инсулина в ?–клетках поджелудочной железы. Глимепирид характеризуется 100% биодоступностью, всасывание не зависит от приема пищи. Глимепирид с высокой замещающей скоростью соединяется и отсоединяется от субъединицы белка ?–клетки, имеющей молекулярную массу 65 кДа/SURX, которая ассоциируется с АТФ–зависимыми калиевыми каналами, но отличается от обычного места связывания других препаратов сульфонилмочевины (белок с молекулярной массой 140 кДа/SUR1). Связывание глимепирида с соответствующим белком происходит в 2–3 раза быстрее, а диссоциация в 8–10 раз выше по сравнению с другими препаратами из класса ПСМ (в частности, глибенкламида). Этот процесс приводит не только к ускоренной секреции инсулина, но и к быстрому снижению его уровня без увеличения количества. Терапевтическая доза глимепирида, составляющая 1–4 мг в сутки, является наименьшей среди всех ПССП. Пролонгированное действие (24 ч) позволяет назначать его в режиме приема – 1 раз в сутки, что имеет ряд преимуществ, положительно влияет на комплайнс и, несомненно, является удобным и безопасным как для работающих пациентов молодого возраста, так и для больных пожилого и преклонного возраста. Эти свойства глимепирида обеспечивают более низкую вероятность гипогликемических состояний. Препарат полностью метаболизируется в печени и имеет двойной путь выведения: почками – 60%, желчью – 40%, что делает возможным его применение при умеренной почечной недостаточности.
Глимепирид, обладая слабым сродством к АТФ–зависимым калиевым каналам кардиомиоцитов, оказывает незначительное действие на кардиоваскулярную систему в отличие от глибенкламида [28]. В клиническом исследовании у больных коронарным атеросклерозом, которым проводилась ангиопластика коронарных артерий, глимепирид, как и плацебо, не влиял на ишемическое прекондиционирование миокарда, в то время как глибенкламид подавлял его [22]. Таким образом, было доказано, что глимепирид не нарушает адаптацию миокарда к условиям ишемии, что особенно важно для пациентов, страдающих ишемической болезнью сердца.
Считается, что в некоторой степени сахароснижающий эффект глимепирида обусловлен его внепанкреатическим действием [23]. Так, в нормальных клетках глимепирид увеличивает количество иммунореактивного GLUT–4 в плазматической мембране в 3–3,5 раза. В клетках, резистентных к действию инсулина, транслокация GLUT–4 снижена примерно вдвое. Под воздействием глимепирида в описанных клетках было зафиксировано лишь незначительное снижение транслокации транспортеров глюкозы по сравнению с нормальными клетками. По–видимому, глимепирид вызывает перераспределение GLUT–4 из микросом низкой плотности к плазматической мембране адипоцитов, что и опосредует стимулирующий эффект в отношении транспорта глюкозы [12]. Процесс распространения GLUT–4 между микросомами низкой плотности и плазматической мембраной, как считают, регулируется скоростью фосфорилирования. Так, глимепирид, как и инсулин, тормозит фосфорилирование GLUT–4 примерно на 25–35%.
Глимепирид оказывает антиатерогенный эффект вследствие торможения процесса агрегации тромбоцитов, одного из наиболее важных этапов патогенеза атеросклероза (АС). Этот процесс инициируется тромбином, который связывается со специфическим рецептором на мембране тромбоцита. Данное взаимодействие индуцирует процесс фосфорилирования внутриклеточных белков и увеличивает содержание Са2+ внутри клетки, что, в свою очередь, ведет к активации фосфолипазы А2. Активированная фосфолипаза А2 стимулирует высвобождение арахидоновой кислоты, которая под влиянием циклооксигеназы и 12–липооксигеназы конвертируется в тромбоксан А2 и лейкотриены. Тромбоксан А2 и АДФ инициирует процесс агрегации тромбоцитов. Наличие антиагрегатного эффекта у глимепирида позволяет предположить, что его прием способен замедлять темпы прогрессирования АС [23].
Глимепирид, производимый фармацевтической компанией «Лабораториос Баго» (Аргентина) под названием «Глемаз», разработан по новой технологии «Флексидоза». Данная технология производства обеспечивает гомогенность формы активного вещества, содержащегося в таблетке. Каждая таблетка «Глемаза» содержит 4 мг глимепирида. Насечки, нанесенные на таблетку, разделяют ее на четыре равные части, содержащие эквивалентные количества действующего вещества в каждой части (1 мг). Благодаря этому упрощается и облегчается процесс титрования необходимой для пациента дозы препарата. Лечение начинают с дозы, соответствующей 1 мг (1/4 часть таблетки) перед или во время завтрака, независимо от того переводится ли пациент с лечения другими пероральными сахароснижающими препаратами, в частности сульфанилмочевины, или назначается впервые. Рекомендуемая максимальная суточная доза – 6 мг. Увеличение дозы препарата на 1–2 мг (1/4–1/2 части таблетки) проводится с интервалом в неделю соответственно значениям гликемии.
Глимепирид является единственным препаратом сульфонилмочевины, способным снижать массу тела, что делает его препаратом выбора для лечения больных с СД и ожирением [9].
Противопоказанием к применению ПСМ являются: СД 1 типа, кетоацидоз, тяжелая почечная и печеночная недостаточность, беременность и лактация, индивидуальная непереносимость.
Как и другие ПСМ, глимепирид может назначаться больным СД 2 как в виде монотерапии, так и в сочетании с инсулином и инсулиновыми «сенситизаторами». Показано, что комбинация глимепирида и метформина, позволяет добиться более успешного контроля гликемии на фоне более низких доз препаратов по сравнению с монотерапией метформином или глимепиридом [15]. Комбинированная терапия позволяет воздействовать на оба нарушенных звена в патогенезе СД 2 – инсулинорезистентность и секрецию инсулина, контролировать гликемию после еды и натощак, а также массу тела и основные параметры метаболизма. Следует заметить, что в случае назначения указанной комбинации глимепирид принимается утром, а метформин – в вечерние часы. В последние годы в практическую медицину активно внедряется метод длительного мониторирования глюкозы (CGMS), который позволяет идентифицировать периоды скрытых гипогликемий и постпрандиальных гипергликемий. Этот метод обеспечивает информацию о направлении, величине, продолжительности, частоте и причинах изменений уровня глюкозы крови, позволяя, таким образом, более адекватно осуществлять контроль за течением и лечением пациентов сахарным диабетом.
Таким образом, лечение СД 2 типа должно предполагать адекватный контроль гликемии и устранение факторов риска сердечно–сосудистых заболеваний. При оценке результатов сахароснижающей терапии необходимо учитывать не только уровень глюкозы натощак, но и постпрандиальную гипергликемию, которая является самостоятельным фактором риска сердечно–сосудистых осложнений. Для улучшения результатов лечения СД 2 типа перспективно применение «селективных» препаратов сульфонилмочевины и бигуанидов (метформина), уменьшающих инсулинорезистентность.