–Ф–∞–љ–љ—Л–є –≤–Њ–њ—А–Њ—Б –±—Л–ї —А–∞—Б—Б–Љ–Њ—В—А–µ–љ –љ–∞ –Ј–∞—Б–µ–і–∞–љ–Є–Є –Ъ–Њ–љ—Б—Г–ї—М—В–∞—В–Є–≤–љ–Њ–≥–Њ –Ї–Њ–Љ–Є—В–µ—В–∞ –њ–Њ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –і–ї—П –ї–µ—З–µ–љ–Є—П —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Р–і–Љ–Є–љ–Є—Б—В—А–∞—Ж–Є–Є –њ–Њ –њ–Є—Й–µ–≤—Л–Љ –њ—А–Њ–і—Г–Ї—В–∞–Љ –Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ —Б—А–µ–і—Б—В–≤–∞–Љ (Food and Drug Administration – FDA) –°–®–Р –≤ –Є—О–ї–µ 2008 –≥. [3]. –°–Њ–≥–ї–∞—Б–љ–Њ –Љ–љ–µ–љ–Є—О —Н–Ї—Б–њ–µ—А—В–Њ–≤ –і–ї—П —Г—Б–њ–µ—И–љ–Њ–є —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –љ–Њ–≤—Л—Е –Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —Г–ґ–µ –њ—А–Є–Љ–µ–љ—П—О—Й–Є—Е—Б—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –і–∞–љ–љ—Л–µ –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –і–Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –Є—Е –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, —А–∞–≤–љ–Њ –Ї–∞–Ї –Є –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Г–Љ–µ–љ—М—И–∞—В—М —А–Є—Б–Ї –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞.
–Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —Г–±–µ–і–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Љ–∞–Ї—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –ї—О–±–Њ–≥–Њ –Є–Ј –Є–Љ–µ—О—Й–Є—Е—Б—П –љ–∞ —А—Л–љ–Ї–µ —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤–Ї–ї—О—З–∞—П –Є–љ—Б—Г–ї–Є–љ [3].
–≠–Ї—Б–µ–љ–∞—В–Є–і (–С–∞–µ—В–∞®, –≠–ї–Є –Ы–Є–ї–ї–Є —Н–љ–і –Ъ–Њ–Љ–њ–∞–љ–Є) —П–≤–ї—П–µ—В—Б—П –њ–µ—А–≤—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –Њ—В–љ–Њ—Б—П—Й–Є–Љ—Б—П –Ї —Б–Њ–≤–µ—А—И–µ–љ–љ–Њ –љ–Њ–≤–Њ–Љ—Г –Ї–ї–∞—Б—Б—Г –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –°–Ф 2 —В–Є–њ–∞ – –Љ–Є–Љ–µ—В–Є–Ї–Њ–≤ –Є–љ–Ї—А–µ—В–Є–љ–∞. –Ф–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ—Б–љ–Њ–≤–∞–љ–Њ –љ–∞ –Ј–∞–Љ–µ—Й–µ–љ–Є–Є –љ–∞—А—Г—И–µ–љ–љ—Л—Е –њ—А–Є –°–Ф 2 —В–Є–њ–∞ —Н—Д—Д–µ–Ї—В–Њ–≤ –≥–Њ—А–Љ–Њ–љ–∞––Є–љ–Ї—А–µ—В–Є–љ–∞ –У–Я–Я–1 (–≥–ї—О–Ї–∞–≥–Њ–љ–Њ–њ–Њ–і–Њ–±–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞–1). –Ф–∞–љ–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ —В–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–Њ–љ—В—А–Њ–ї—П –≥–ї–Є–Ї–µ–Љ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –≠–Ї—Б–µ–љ–∞—В–Є–і –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є —Б –љ–Њ—П–±—А—П 2006 –≥. –Є —А–∞–Ј—А–µ—И–µ–љ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –≤ –Ї–∞—З–µ—Б—В–≤–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ —Б –љ–µ—Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ, –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ–Є —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л, —В–Є–∞–Ј–Њ–ї–Є–і–Є–љ–і–Є–Њ–љ–∞–Љ–Є, –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –Є –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л –Є–ї–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ –Є —В–Є–∞–Ј–Њ–ї–Є–і–Є–љ–і–Є–Њ–љ–∞ [4].
–Я–Њ–Љ–Є–Љ–Њ –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –њ–∞—А–∞–Љ–µ—В—А—Л —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –њ—А–Є –°–Ф 2 —В–Є–њ–∞, —Б—А–∞–≤–љ–Є–Љ–Њ–≥–Њ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є [5], –і–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Б–њ–Њ—Б–Њ–±–µ–љ —В–∞–Ї–ґ–µ –Њ–Ї–∞–Ј—Л–≤–∞—В—М –љ–µ–њ—А—П–Љ—Л–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є –љ–∞ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є. –Э–Є–ґ–µ –Љ—Л —А–∞—Б—Б–Љ–Њ—В—А–Є–Љ –Є–Љ–µ—О—Й–Є–µ—Б—П –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –і–∞–љ–љ—Л–µ –Њ –≤–ї–Є—П–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –Љ–∞—Б—Б—Г —В–µ–ї–∞, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є, –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Є –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–µ–љ–љ—Л–µ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е.
–Т–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞
–љ–∞ –Љ–∞—Б—Б—Г —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Њ–ґ–Є—А–µ–љ–Є–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–µ, —Б–≤—П–Ј–∞–љ–Њ —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Є –°–Ф 2 —В–Є–њ–∞. –Ш–Ј–±—Л—В–Њ—З–љ–∞—П –Љ–∞—Б—Б–∞ —В–µ–ї–∞ –Є–ї–Є –Њ–ґ–Є—А–µ–љ–Є–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г 85–90% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞. –Я–Њ—Н—В–Њ–Љ—Г –Њ–і–љ–Є–Љ –Є–Ј –±–µ–Ј—Г—Б–ї–Њ–≤–љ—Л—Е –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ —П–≤–ї—П–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –≤–µ—Б–∞ –Ј–∞ —Б—З–µ—В –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Њ–±—А–∞–Ј–∞ –ґ–Є–Ј–љ–Є –Є —Е–∞—А–∞–Ї—В–µ—А–∞ –њ–Є—В–∞–љ–Є—П, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –і–∞–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ–±–Є—В—М—Б—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є –Љ–µ–љ–µ–µ —З–µ–Љ —Г 30% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤–њ–µ—А–≤—Л–µ –≤—Л—П–≤–ї–µ–љ–љ—Л–Љ –°–Ф 2 —В–Є–њ–∞ [6]. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–µ—А–Њ—А–∞–ї—М–љ—Л—Е —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞) –Є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л–Љ –°–Ф 2 —В–Є–њ–∞ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–Њ–љ—В—А–Њ–ї—П –≥–ї–Є–Ї–µ–Љ–Є–Є, –Њ–і–љ–∞–Ї–Њ –≤–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–Є–≤–Њ–і–Є—В –Ї –і–∞–ї—М–љ–µ–є—И–µ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–≠–Ї—Б–µ–љ–∞—В–Є–і –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–є –њ–µ–њ—В–Є–і, –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ–∞—П –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–≥–Њ –љ–∞ 53% –Є–і–µ–љ—В–Є—З–љ–∞ —В–∞–Ї–Њ–≤–Њ–є —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Њ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ – –Є–љ–Ї—А–µ—В–Є–љ–∞ –У–Я–Я–1, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Н–Ї—Б–µ–љ–∞—В–Є–і—Г –≤—Л—Б—В—Г–њ–∞—В—М –≤ —А–Њ–ї–Є –Љ–Њ—Й–љ–Њ–≥–Њ –∞–≥–Њ–љ–Є—Б—В–∞ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї –У–Я–Я–1 —Г —З–µ–ї–Њ–≤–µ–Ї–∞. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е –Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –У–Я–Я–1 —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ—Л—Е —А–µ–≥—Г–ї—П—В–Њ—А–Њ–≤ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–Њ—В—А–µ–±–ї—П–µ–Љ–Њ–є –њ–Є—Й–Є, —Г—Б–Є–ї–Є–≤–∞–µ—В —З—Г–≤—Б—В–≤–Њ –љ–∞—Б—Л—Й–µ–љ–Є—П –Є —Г–Љ–µ–љ—М—И–∞–µ—В –Њ—Й—Г—Й–µ–љ–Є–µ –≥–Њ–ї–Њ–і–∞ [7]. –Р–љ–∞–ї–Њ–≥–Є—З–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —А–µ—Ж–µ–њ—В–Њ—А—Л –Ї –У–Я–Я–1, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л–µ –≤ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –≤–≤–µ–і–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ [8], —З—В–Њ –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –Є—В–Њ–≥–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Ґ–∞–Ї, –≤–≤–µ–і–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –Ј–і–Њ—А–Њ–≤—Л–Љ –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–∞–Љ –≤—Л–Ј—Л–≤–∞–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ–Њ—В—А–µ–±–ї—П–µ–Љ–Њ–є –њ–Є—Й–Є (–љ–∞ 19% –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –њ–Њ—В—А–µ–±–ї—П–µ–Љ—Л—Е –Ї–∞–ї–Њ—А–Є–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≤–≤–µ–і–µ–љ–Є–µ–Љ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞, p=0,012) [9].
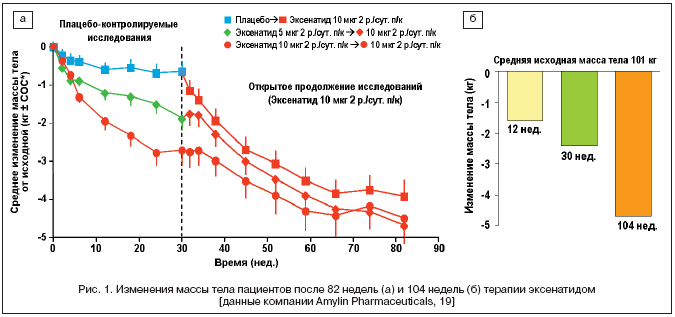
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞–і–Є–і–∞ –њ—Г—В–µ–Љ –њ–Њ–і–Ї–Њ–ґ–љ—Л—Е (–њ/–Ї) –Є–љ—К–µ–Ї—Ж–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞ –Є–ї–Є –Њ–ґ–Є—А–µ–љ–Є–µ–Љ —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–Љ—Г –Є —Б—В–Њ–є–Ї–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Т–Њ –≤—Б–µ—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–Љ—Г —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А–Њ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–ґ–µ –њ–Њ—Б–ї–µ 2–4 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П [10–18] —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є–Ј–±—Л—В–Њ—З–љ–Њ–є –Љ–∞—Б—Б–Њ–є —В–µ–ї–∞. –Ю—В–Љ–µ—З–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В —Б–Њ—Е—А–∞–љ—П–ї—Б—П –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 2––ї–µ—В–љ–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –ї–µ—З–µ–љ–Є—П –≤ —А–∞–Љ–Ї–∞—Е –Њ—В–Ї—А—Л—В—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [19], —П–≤–ї—П–≤—И–Є—Е—Б—П –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є–µ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є III —Д–∞–Ј—Л [11–13] (—А–Є—Б. 1 –∞, –±).
–Т–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –Љ–∞—Б—Б—Г —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —П–≤–ї—П–µ—В—Б—П –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ. –Ґ–∞–Ї, –њ–Њ—Б–ї–µ 30 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Н–Ї—Б–µ–љ–∞—В–Є–і –≤ –і–Њ–Ј–µ 5 –Љ–Ї–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є, –Љ–∞—Б—Б–∞ —В–µ–ї–∞ —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М –љ–∞ 1,6 –Ї–≥ (—Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–µ—А–∞–њ–Є—О –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ –Є–ї–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л – –Я–°–Ь) –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ 10 –Љ–Ї–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є – –љ–∞ 1,6–2,8 –Ї–≥ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ–Њ–є. –Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –≤ –і–Њ–Ј–µ 5 –Љ–Ї–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ –і–Њ–њ–Њ–ї–љ–µ–љ–Є—П –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Я–°–Ь –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —В–Њ–ї—М–Ї–Њ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–0,9 –Ї–≥) [12]. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ–ї–∞—Ж–µ–±–Њ, –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Ј–∞ –≤—А–µ–Љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (–0,3 – –0,9 –Ї–≥ –Њ—В –Є—Б—Е–Њ–і–љ–Њ–є) [11–14].
–Я—А–Є –і–Њ–±–∞–≤–ї–µ–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –Ї —В–µ—А–∞–њ–Є–Є —В–Є–∞–Ј–Њ–ї–Є–і–Є–љ–і–Є–Њ–љ–∞–Љ–Є —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [15]. –Т –≥—А—Г–њ–њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–ї–∞—Ж–µ–±–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Ј–∞ –≤—А–µ–Љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Г–ґ–µ –њ–Њ—Б–ї–µ 4 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П, –∞ –Ї –Љ–Њ–Љ–µ–љ—В—Г –Ј–∞–≤–µ—А—И–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (16 –љ–µ–і–µ–ї—М) —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є —Б–Њ—Б—В–∞–≤–Є–ї–Є –1,51 –Ї–≥ (95%––є –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї – –Ф–Ш –Њ—В –2,15 –і–Њ –0,88 –Ї–≥, —А<0,001) [15].
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ–і–Њ–ї–ґ–Є–ї–Є —В–µ—А–∞–њ–Є—О —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –њ–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П —Г—З–∞—Б—В–Є—П –≤ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е III —Д–∞–Ј—Л [11–13], —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ —З–µ—А–µ–Ј 82 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П –і–Њ—Б—В–Є–≥–ї–Њ –5,2, –4,0 –Є –4,1% –≤ –≥—А—Г–њ–њ–∞—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й—Г—О —В–µ—А–∞–њ–Є—О –Љ–µ—В—Д–Њ—А–Љ–Є–љ–Њ–Љ, –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є —Б—Г–ї—М—Д–Њ–љ–Є–ї–Љ–Њ—З–µ–≤–Є–љ—Л (–Я–°–Ь) –Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–µ–є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞ —Б –Я–°–Ь —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [20]. –£ –ї–Є—Ж, –њ–Њ–ї–љ–Њ—Б—В—М—О –Ј–∞–≤–µ—А—И–Є–≤—И–Є—Е 2––ї–µ—В–љ–Є–є –њ–µ—А–Є–Њ–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —В–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –≤ –і–Њ–Ј–µ 10 –Љ–Ї–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ –і–Њ–±–Є—В—М—Б—П —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ –љ–∞ 1,6 –Ї–≥, 2,4 –Ї–≥ –Є 4,7 –Ї–≥ —З–µ—А–µ–Ј 12, 30 –Є 104 –љ–µ–і–µ–ї–Є –ї–µ—З–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ (—А–Є—Б. 1 –±) [19]. –°–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Г 81% –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Н–Ї—Б–µ–љ–∞—В–Є–і –≤ —В–µ—З–µ–љ–Є–µ 2 –ї–µ—В, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –≤ –њ—А–Њ—В–Њ–Ї–Њ–ї–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є –Њ—Б–Њ–±—Л–µ —В—А–µ–±–Њ–≤–∞–љ–Є—П –њ–Њ —Б–Њ–±–ї—О–і–µ–љ–Є—О –і–Є–µ—В—Л –Є –њ—А–Њ–≥—А–∞–Љ–Љ—Л —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —Г–њ—А–∞–ґ–љ–µ–љ–Є–є [19]. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (n=217), –Ї–Њ—В–Њ—А—Л–µ –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –њ—А–Є–µ–Љ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 3 –Є –±–Њ–ї–µ–µ –ї–µ—В, –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –і–∞–ї—М–љ–µ–є—И–µ–µ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞, –і–Њ—Б—В–Є–≥—И–µ–µ – 5,3±0,4 –Ї–≥ —З–µ—А–µ–Ј 3 –≥–Њ–і–∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ (–њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ–Њ–є, p<0,0001) [21], –њ—А–Є—З–µ–Љ –≥—А–∞—Д–Є–Ї –і–Є–љ–∞–Љ–Є–Ї–Є —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Ј–∞ —Г–Ї–∞–Ј–∞–љ–љ—Л–є –њ–µ—А–Є–Њ–і –љ–µ –Є–Љ–µ–ї –≤–Є–і–Є–Љ–Њ–≥–Њ –њ–ї–∞—В–Њ.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –і–∞–љ–љ—Л—Е, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –Ї 82––є –љ–µ–і–µ–ї–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Б—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –±—Л–ї–∞ –њ—А—П–Љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–∞ –Є—Б—Е–Њ–і–љ–Њ–Љ—Г –Ј–љ–∞—З–µ–љ–Є—О –Ш–Ь–Ґ –њ–∞—Ж–Є–µ–љ—В–∞: —Б—В–µ–њ–µ–љ—М —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ –ї–Є–љ–µ–є–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞–ї–∞ –Њ—В –2,9 –і–Њ –5,5% —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б—Е–Њ–і–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Ш–Ь–Ґ –Њ—В <25 –і–Њ >40 –Ї–≥/–Љ2 [20].
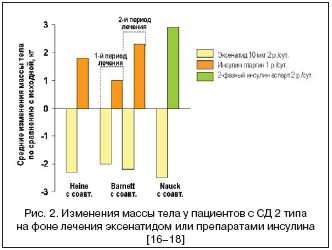
–Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ –Њ—З–µ–≤–Є–і–љ—Л –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Є–љ—Б—Г–ї–Є–љ–∞ [16–18]. –Т —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —В–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –≤ –і–Њ–Ј–µ 10 –Љ–Ї–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є –њ—А–Є–≤–Њ–і–Є–ї–∞ –Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –Љ–∞—Б—Б—Л —В–µ–ї–∞, –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є—П (–Є–љ—Б—Г–ї–Є–љ–Њ–Љ –≥–ї–∞—А–≥–Є–љ–Њ–Љ –Є–ї–Є –і–≤—Г—Е—Д–∞–Ј–љ—Л–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –∞—Б–њ–∞—А—В) –≤—Л–Ј—Л–≤–∞–ї–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—А–Є—Б. 2). –†–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є (p<0,001) –Є –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Г–ґ–µ –њ–Њ—Б–ї–µ 2 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П, –і–Њ—Б—В–Є–≥–∞—П –Ї –Ї–Њ–љ—Ж—Г –ї–µ—З–µ–љ–Є—П (26, 16 –Є 52–—П –љ–µ–і–µ–ї–Є) 4,1 –Ї–≥ [16], 3,0–4,5 –Ї–≥ [18] –Є 5,4 –Ї–≥ [17].
–Т –љ–µ–±–Њ–ї—М—И–Њ–Љ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–Њ –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–Њ –≤–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞, –Ї–Њ—В–Њ—А—Л–є –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–µ—А–Њ—А–∞–ї—М–љ—Л–Љ–Є —Б–∞—Е–∞—А–Њ—Б–љ–Є–ґ–∞—О—Й–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є (–Я–°–Я) –Є –Є–љ—Б—Г–ї–Є–љ–Њ–Љ, –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –Њ–ґ–Є—А–µ–љ–Є–µ–Љ. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –Ј–∞ –њ–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П (–≤ —Б—А–µ–і–љ–µ–Љ 26 –љ–µ–і–µ–ї—М) –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —А–µ–≥—Г–ї—П—А–љ–Њ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Н–Ї—Б–µ–љ–∞—В–Є–і –≤ –і–Њ–Ј–µ 5 –Љ–Ї–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є (n=38), –Љ–∞—Б—Б–∞ —В–µ–ї–∞ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –љ–∞ 6,46±0,8 –Ї–≥, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–µ–Ї—А–∞—В–Є–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –њ–Њ —А–∞–Ј–ї–Є—З–љ—Л–Љ –њ—А–Є—З–Є–љ–∞–Љ (n=14), –Љ–∞—Б—Б–∞ —В–µ–ї–∞ —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М –љ–∞ 2,4±0,6 –Ї–≥ (p<0,001) [22].
–£–Љ–µ–љ—М—И–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –љ–µ —Б–≤—П–Ј–∞–љ–Њ —Б –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ —В–Њ—И–љ–Њ—В—Л –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Є–Љ–µ–ї–Њ –Љ–µ—Б—В–Њ –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ –Њ—В–Љ–µ—З–∞–≤—И–Є—Е –і–∞–љ–љ–Њ–є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є. –Ґ–∞–Ї, —З–µ—А–µ–Ј 16 –љ–µ–і–µ–ї—М —В–µ—А–∞–њ–Є–Є –Љ–∞—Б—Б–∞ —В–µ–ї–∞ —Б–љ–Є–Ј–Є–ї–∞—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ –1,95±0,43 –Ї–≥ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є—Б–њ—Л—В—Л–≤–∞–≤—И–Є—Е —В–Њ—И–љ–Њ—В—Г, –Є –љ–∞ –1,25±0,35 –Ї–≥ —Г –±–Њ–ї—М–љ—Л—Е, –љ–µ –Њ—В–Љ–µ—З–∞–≤—И–Є—Е —В–Њ—И–љ–Њ—В—Л –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ [15]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —З–∞—Б—В–Њ—В–∞ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —В–Њ—И–љ–Њ—В—Л –±—Л–ї–Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–Љ–Є –≤ –њ–µ—А–≤—Л–µ 8 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П, –∞ –Ј–∞—В–µ–Љ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Г–Љ–µ–љ—М—И–∞–ї–Є—Б—М –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –љ–Њ—Б–Є–ї–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–є —Е–∞—А–∞–Ї—В–µ—А –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –ї–µ—З–µ–љ–Є—П [11–21].
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (–†–Ъ–Ш) —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ [23] –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є, —З—В–Њ —Н–Ї—Б–µ–љ–∞—В–Є–і –≤—Л–Ј—Л–≤–∞–µ—В –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –Ї–Њ—В–Њ—А–Њ–µ –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –1,44 –Ї–≥ (95% –Ф–Ш –Њ—В –2,13 –і–Њ –0,75 –Ї–≥) –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ –Є –4,76 –Ї–≥ (95% –Ф–Ш –Њ—В –6,03 –і–Њ –3,49 –Ї–≥) –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–µ–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ї–Њ–≥–Є—З–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –Ј–∞ —Б—З–µ—В –≤–ї–Є—П–љ–Є—П –љ–∞ –Љ–∞—Б—Б—Г —В–µ–ї–∞ —В–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —Б–љ–Є–ґ–µ–љ–Є—О –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞, –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Г–Љ–µ–љ—М—И–µ–љ–Є—П —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —Б–Њ–±—Л—В–Є–є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –Ґ–∞–Ї, –љ–∞–њ—А–Є–Љ–µ—А, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –≤–µ—Б–∞ –±—Л–ї–Є —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ—Л –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Є –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –Ї—А–Њ–≤–Є (—Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є – –Ы–Я–Т–Я) [20]. –Т —Ж–µ–ї–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Њ–±—Й–µ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –љ–∞ 25%, —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –і–Є–∞–±–µ—В–Њ–Љ, –љ–∞ 28% [24].
–Т–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –≤ 2,5–3 —А–∞–Ј–∞ –≤—Л—И–µ, —З–µ–Љ —Б—А–µ–і–Є –љ–∞—Б–µ–ї–µ–љ–Є—П –≤ —Ж–µ–ї–Њ–Љ, –њ—А–Є —Н—В–Њ–Љ –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є —Б–Љ–µ—А—В–Є —П–≤–ї—П—О—В—Б—П —Б–Њ—Б—В–Њ—П–љ–Є—П, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е, —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤. –Т —Ж–µ–ї–Њ–Љ –Њ—В –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ, —Г–Љ–Є—А–∞–µ—В –±–Њ–ї—М—И–µ –±–Њ–ї—М–љ—Л—Е –°–Ф, —З–µ–Љ –Њ—В –≤—Б–µ—Е –і—А—Г–≥–Є—Е –њ—А–Є—З–Є–љ, –≤–Љ–µ—Б—В–µ –≤–Ј—П—В—Л—Е [25]. –£—З–Є—В—Л–≤–∞—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П, –Ї–Њ—В–Њ—А–∞—П —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Є –Њ—Б—В—А–Њ–є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є, –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –Њ—Б–Њ–±—Л–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Г–ї—Г—З—И–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–Њ—В–Є–≤–Њ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–Т –Ї—А–∞—В–Ї–Њ—Б—А–Њ—З–љ—Л—Е (4–30 –љ–µ–і–µ–ї—М) –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є [11,12,15,26]. –Р–љ–∞–ї–Њ–≥–Є—З–љ–Њ –≤ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –і–≤—Г—Е—Д–∞–Ј–љ—Л–Љ –Є–љ—Б—Г–ї–Є–љ–Њ–Љ –∞—Б–њ–∞—А—В —В–∞–Ї–ґ–µ –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 52 –љ–µ–і–µ–ї—М [17].
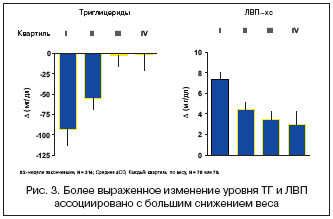
–Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ (82 –Є 182 –љ–µ–і–µ–ї–Є) –ї–µ—З–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ [20,21] –≤ —А–∞–Љ–Ї–∞—Е –Њ—В–Ї—А—Л—В—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є, –Ј–∞–Ї–ї—О—З–∞—О—Й–µ–µ—Б—П –≤ —Б–љ–Є–ґ–µ–љ–Є–Є —Г—А–Њ–≤–љ–µ–є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤, –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –љ–Є–Ј–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є (–Ы–Я–Э–Я) –Є –њ–Њ–≤—Л—И–µ–љ–Є–Є —Г—А–Њ–≤–љ—П –Ы–Я–Т–Я. –Ґ–∞–Ї, –њ–Њ –Ј–∞–≤–µ—А—И–µ–љ–Є–Є 82 –љ–µ–і–µ–ї—М —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Њ—Б—В–∞–≤–Є–ї–Є – 38,6 –Љ–≥/–і–ї; – 2,4 –Љ–≥/–і–ї; – 1,6 –Љ–≥/–і–ї –Є + 4,6 –Љ–≥/–і–ї (–Њ—В –Є—Б—Е–Њ–і–љ—Л—Е 243,1 –Љ–≥/–і–ї; 188,2 –Љ–≥/–і–ї; 116,7 –Љ–≥/–і–ї –Є 38,6 –Љ–≥/–і–ї) —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –њ—А–Є—З–µ–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ы–Я–Т–Я –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є [20]. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 3,5 –ї–µ—В (n=151), —Г—А–Њ–≤–µ–љ—М —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Б–љ–Є–Ј–Є–ї—Б—П –љ–∞ 12% (p=0,0003), –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ – –љ–∞ 5% (p=0,0007), –Ы–Я–Э–Я – –љ–∞ 6% (p<0,0001), –∞ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Ы–Я–Т–Я —Г–≤–µ–ї–Є—З–Є–ї–Њ—Б—М –љ–∞ 24% (p<0,0001) (—А–Є—Б. 3) [21].
–С–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –±—Л–ї–Є –Њ—В–Љ–µ—З–µ–љ—Л –≤ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –Њ–ґ–Є—А–µ–љ–Є–µ–Љ [22]. –Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ, –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ (–љ–∞ 8,5±3,3%, p=0,03) –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –љ–∞ 26±7,6%, —А=0,01) –Њ—В –Є—Б—Е–Њ–і–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є [22].
–Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –±—Л–ї–Є –Њ—В–Љ–µ—З–µ–љ—Л –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–∞–Є–±–Њ–ї—М—И–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Ґ–∞–Ї, —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞, —Г –Ї–Њ—В–Њ—А—Л—Е –Љ–∞—Б—Б–∞ —В–µ–ї–∞ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 11,9 –Ї–≥ –њ–Њ—Б–ї–µ 82 –љ–µ–і–µ–ї—М —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ; —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Б–Њ—Б—В–∞–≤–Є–ї–Є – 93 –Љ–≥/–і–ї, –∞ —Г—А–Њ–≤–љ—П –Ы–Я–Т–Я + 7,3 –Љ–≥/–і–ї [20]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–µ —В–Њ–ї—М–Ї–Њ –њ—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є –≤–µ—Б–∞, –љ–Њ —В–∞–Ї–ґ–µ –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –њ–Њ—В–µ—А–Є –Љ–∞—Б—Б—Л —В–µ–ї–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –і–∞–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П (—Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П HbA1c) —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ –Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П –і–∞–ґ–µ –њ—А–Є –љ–µ–±–Њ–ї—М—И–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є HbA1c (–љ–∞ 0,7–0,8% –Њ—В –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П) [20].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ–±–Є—В—М—Б—П —Г–ї—Г—З—И–µ–љ–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –Ї—А–Њ–≤–Є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –Я—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –Є —Б—В–∞—В–Є–љ–Њ–≤ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є —Б—В–∞—В–Є–љ–∞–Љ–Є, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –і–Њ–±—А–Њ–≤–Њ–ї—М—Ж–µ–≤ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–ї–Њ—Й–∞–і–Є –њ–Њ–і —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –Ї—А–Є–≤–Њ–є – –Я–§–Ъ0– 0–∞ –Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є – Cmax –ї–Њ–≤–∞—Б—В–∞—В–Є–љ–∞ –≤ –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –љ–∞ 40 –Є –љ–∞ 28% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –∞ —В–∞–Ї–ґ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤—А–µ–Љ–µ–љ–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є—П Cmax –≤ –њ–ї–∞–Ј–Љ–µ – Tmax –љ–∞ 4 —З–∞—Б–∞ –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ [27]. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ, –њ–Њ–ї—Г—З–∞—О—Й–Є–Љ —Б—В–∞—В–Є–љ—Л, –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Њ–Ј—Л –њ–Њ—Б–ї–µ–і–љ–Є—Е –љ–µ —В—А–µ–±—Г–µ—В—Б—П.
–Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –µ—Й–µ –љ–µ –њ–Њ–ї—Г—З–µ–љ—Л –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–∞ —В–Њ–≥–Њ, —З—В–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –ї–Є–њ–Є–і–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –Ї—А–Њ–≤–Є –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –њ—А–Є–≤–Њ–і—П—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞. –Ф–ї—П –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є—П –њ–Њ–і–Њ–±–љ–Њ–≥–Њ –Ј–∞–Ї–ї—О—З–µ–љ–Є—П —В—А–µ–±—Г–µ—В—Б—П –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Є —И–Є—А–Њ–Ї–Њ–Љ–∞—Б—И—В–∞–±–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, –љ–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ—Л–µ –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –ї–Є–њ–Є–і–љ—Л–є –њ—А–Њ—Д–Є–ї—М –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –≤–µ—Б—М–Љ–∞ –Љ–љ–Њ–≥–Њ–Њ–±–µ—Й–∞—О—Й–Є–Љ–Є.
–Т–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П
–Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П —П–≤–ї—П–µ—В—Б—П –µ—Й–µ –Њ–і–љ–Є–Љ —Б–µ—А—М–µ–Ј–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Љ–Є–Ї—А–Њ– –Є –Љ–∞–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Є –°–Ф 2 —В–Є–њ–∞, —З—В–Њ –≤ –Є—В–Њ–≥–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ –≤ 2,5 —А–∞–Ј–∞ (95% –Ф–Ш –Њ—В 1,6 –і–Њ 3,8 —А–∞–Ј) [28]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є UKPDS –±—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –љ–∞ –Ї–∞–ґ–і—Л–µ 10 –Љ–Љ —А—В. —Б—В. –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–Љ–µ–љ—М—И–Є—В—М —А–Є—Б–Ї –ї—О–±—Л—Е –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ 12% (95% –Ф–Ш –Њ—В 10 –і–Њ 14%, —А<0,0001); —А–Є—Б–Ї —Б–Љ–µ—А—В–љ–Њ—Б—В–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –і–Є–∞–±–µ—В–Њ–Љ, –љ–∞ 15% (95% –Ф–Ш –Њ—В 12 –і–Њ 18%, —А<0,0001), –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ – –љ–∞ 11% (95% –Ф–Ш –Њ—В 7 –і–Њ 14%, —А<0,0001), –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є – –љ–∞ 13% (95% –Ф–Ш –Њ—В 10 –і–Њ 16%, —А<0,0001) [29].
–Т –і–ї–Є—В–µ–ї—М–љ—Л—Е (52–182 –љ–µ–і–µ–ї–Є) –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П [17,19–21]. –Ґ–∞–Ї, –≤ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –Є –і–≤—Г—Е—Д–∞–Ј–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –∞—Б–њ–∞—А—В –≤ —В–µ—З–µ–љ–Є–µ 52 –љ–µ–і–µ–ї—М [17] –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ – 5±15 –Љ–Љ —А—В.—Б—В., p<0,001) –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ – 2±10 –Љ–Љ —А—В.—Б—В., p=0,03) –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В–µ—А–∞–њ–Є—О —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ 2–—Д–∞–Ј–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –∞—Б–њ–∞—А—В –љ–µ –≤—Л–Ј—Л–≤–∞–ї–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П.
–Я—А–Є —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –Њ–ґ–Є—А–µ–љ–Є–µ–Љ —В–∞–Ї–ґ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –љ–∞ 9,2±3,3 –Љ–Љ —А—В.—Б—В. (—А=0,02) [22].
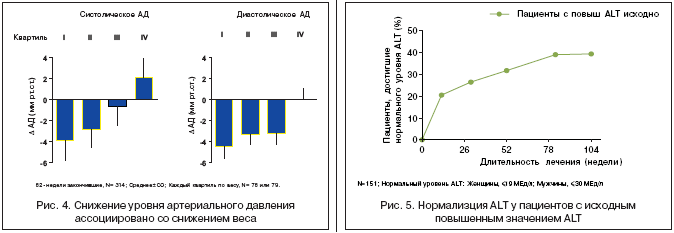
–Ґ–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 82 –љ–µ–і–µ–ї—М –≤ —А–∞–Љ–Ї–∞—Е –Њ—В–Ї—А—Л—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П —Г—З–∞—Б—В–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е III —Д–∞–Ј—Л –њ—А–Є–≤–µ–ї–∞ –Ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –љ–∞ 2,7 –Љ–Љ —А—В.—Б—В. [20]. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В–∞–Ї–ґ–µ –Є–Љ–µ–ї–Є —В–µ–љ–і–µ–љ—Ж–Є—О –Ї —Б–љ–Є–ґ–µ–љ–Є—О (–1,3 –Љ–Љ —А—В.—Б—В.), –Њ–і–љ–∞–Ї–Њ —Г–Ї–∞–Ј–∞–љ–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–µ –і–Њ—Б—В–Є–≥–ї–Є —Г—А–Њ–≤–љ—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є [20]. –Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ —Б –љ–∞–Є–±–Њ–ї—М—И–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ–∞—Б—Б—Л —В–µ–ї–∞ (–11,9 –Ї–≥ –њ–Њ—Б–ї–µ 82 –љ–µ–і–µ–ї—М –ї–µ—З–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ). –Т —Г–Ї–∞–Ј–∞–љ–љ–Њ–є –њ–Њ–і–≥—А—Г–њ–њ–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М –љ–∞ 3,9 –Љ–Љ —А—В.—Б—В., –∞ –і–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ – –љ–∞ 4,4 –Љ–Љ —А—В.—Б—В. [20]. –Т—Л—П–≤–ї–µ–љ–љ—Л–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —Б–Њ—Е—А–∞–љ—П–ї–Є—Б—М –Є –њ–Њ—Б–ї–µ 104 [19] –Є 182 [21] –љ–µ–і–µ–ї—М —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ. –°—А–µ–і–љ–µ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Њ—В –Є—Б—Е–Њ–і–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–Є–ї–Њ –Ї 104––є –љ–µ–і–µ–ї–µ –ї–µ—З–µ–љ–Є—П – 2,6±0,9 –Љ–Љ —А—В.—Б—В. (95% –Ф–Ш –Њ—В – 4,3 –і–Њ – 0,9 –Љ–Љ —А—В.—Б—В., —А=0,003), –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ – 1,9±0,5 –Љ–Љ —А—В.—Б—В. (95% –Ф–Ш –Њ—В – 3,0 –і–Њ – 0,9 –Љ–Љ —А—В.—Б—В., —А<0,001) (—А–Є—Б. 4) [19].
–Т–Њ–Ј–Љ–Њ–ґ–љ–Њ, —З—В–Њ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–±–Њ–ї—М—И–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П, –Њ—В–Љ–µ—З–µ–љ–љ–Њ–µ –≤ –і–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, —Б–≤—П–Ј–∞–љ–Њ —Б —В–µ–Љ, —З—В–Њ –Є—Б—Е–Њ–і–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –±—Л–ї–Є –≤ –њ—А–µ–і–µ–ї–∞—Е –љ–Њ—А–Љ–∞–ї—М–љ—Л—Е –Ј–љ–∞—З–µ–љ–Є–є (–Є—Б—Е–Њ–і–љ—Л–є —Б—А–µ–і–љ–Є–є —Г—А–Њ–≤–µ–љ—М ~ 130/80 –Љ–Љ —А—В.—Б—В.) [19,20]. –Т–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є —В—А–µ–±—Г–µ—В –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П.
–Т–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ–µ—З–µ–љ–Њ—З–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤
–Т–µ—Б—М–Љ–∞ –Є–љ—В–µ—А–µ—Б–љ—Л –і–∞–љ–љ—Л–µ –Њ –≤–ї–Є—П–љ–Є–Є –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј (–∞–ї–∞–љ–Є–љ –∞–Љ–Є–љ–Њ—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л – –Р–Ы–Ґ –Є –∞—Б–њ–∞—А—В–∞—В –∞–Љ–Є–љ–Њ—В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л – –Р–°–Ґ), —П–≤–ї—П—О—Й–Є—Е—Б—П –Љ–∞—А–Ї–µ—А–∞–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є [19,21]. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –°–Ф 2 —В–Є–њ–∞ –Є –Њ–ґ–Є—А–µ–љ–Є–µ —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–≥–Њ –ґ–Є—А–Њ–≤–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є – –Э–Р–Ц–Ч–Я (nonalcoholic fatty liver disease – NAFLD) –Є –µ–≥–Њ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –≤–∞—А–Є–∞–љ—В–∞ – –љ–µ–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–≥–Њ —Б—В–µ–∞—В–Њ–≥–µ–њ–∞—В–Є—В–∞ – –Э–Р–°–У (nonalcoholic steatohepatitis – NASH), –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –Њ—В–Љ–µ—З–∞—О—В—Б—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ, –љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є–µ –Є —А—Г–±—Ж–Њ–≤—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —В–Ї–∞–љ–Є –њ–µ—З–µ–љ–Є, –њ—А–Є–≤–Њ–і—П—Й–Є–µ –Ї –љ–∞—А—Г—И–µ–љ–Є—О –µ–µ —Д—Г–љ–Ї—Ж–Є–Є [30]. –Ь–∞—А–Ї–µ—А–Њ–Љ –Э–Р–Ц–Ч–Я —П–≤–ї—П–µ—В—Б—П –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –Р–Ы–Ґ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є, —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В –њ–Њ–≤—Л—И–∞—В—М—Б—П —Г—А–Њ–≤–µ–љ—М –Р–°–Ґ –Є —Й–µ–ї–Њ—З–љ–Њ–є —Д–Њ—Б—Д–∞—В–∞–Ј—Л. –Я—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Э–Р–Ц–Ч–Я –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —А–∞–Ј–≤–Є—В–Є—О —Ж–Є—А—А–Њ–Ј–∞ –њ–µ—З–µ–љ–Є –Є –µ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є – –њ–Њ—А—В–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –љ–∞–ї–Є—З–Є–µ –Э–Р–°–У —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Н—Д—Д–µ–Ї—В–∞ –Є–љ—Б—Г–ї–Є–љ–∞, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–≥–Њ –љ–∞ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –ї–Є–њ–Њ–ї–Є–Ј–∞. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н—В–Њ–≥–Њ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –њ–Њ–≤—Л—И–∞—О—В—Б—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Б–≤–Њ–±–Њ–і–љ—Л—Е –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В (–°–Ц–Ъ), —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –і–∞–ї—М–љ–µ–є—И–µ–Љ—Г –љ–∞—А—Г—И–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Є b––Ї–ї–µ—В–Њ–Ї –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л –Є —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є [31].
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –і–ї—П –ї–µ—З–µ–љ–Є—П –Э–Р–Ц–Ч–Я. –Э–µ–Ї–Њ—В–Њ—А–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Љ–µ—В—Д–Њ—А–Љ–Є–љ–∞, —В–Є–∞–Ј–Њ–ї–Є–і–Є–љ–і–Є–Њ–љ–Њ–≤ –Є —А—П–і–∞ –і—А—Г–≥–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—О –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—О –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Э–Р–Ц–Ч–Я —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞. –£—З–Є—В—Л–≤–∞—П –≤–ї–Є—П–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–∞ –Љ–∞—Б—Б—Г —В–µ–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞, –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–∞—А–Ї–µ—А–Њ–≤ –Э–Р–Ц–Ч–Я – –Р–°–Ґ –Є –Р–Ы–Ґ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ (—А–Є—Б. 5).
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (132/283 – 47%) —Б –Є—Б—Е–Њ–і–љ–Њ –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Р–Ы–Ґ –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –µ–µ —Г—А–Њ–≤–љ—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –ї–µ—З–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Г –±–Њ–ї—М–љ—Л—Е (151/283 – 53%) —Б –Є—Б—Е–Њ–і–љ–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ–Є –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є –Р–Ы–Ґ –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П (–11 –Х–Ф/–ї –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ; —А<0,05) –Є —Г 59/151 (39%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–∞ –Њ—В–Љ–µ—З–µ–љ–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —Г—А–Њ–≤–љ—П –Р–Ы–Ґ –Ї 104––є –љ–µ–і–µ–ї–µ –ї–µ—З–µ–љ–Є—П [19]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ —В–∞–Ї–ґ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Р–°–Ґ.
–Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р–Ы–Ґ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ —Б –љ–∞–Є–±–Њ–ї—М—И–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–Њ—Б–ї–µ 104 –љ–µ–і–µ–ї—М —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ. –Р–љ–∞–ї–Њ–≥–Є—З–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б—Е–Њ–і–љ–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ–Є –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є –Р–Ы–Ґ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞, —З–µ–Љ —Г –ї–Є—Ж —Б –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –Є—Б—Е–Њ–і–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Р–Ы–Ґ (—А=0,04) [19]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Р–Ы–Ґ –љ–µ –Ј–∞–≤–Є—Б–µ–ї–Є –Њ—В –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П HbA1c –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ.
–Я—А–Њ–і–Њ–ї–ґ–µ–љ–Є–µ —В–µ—А–∞–њ–Є–Є —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 3 –Є –±–Њ–ї–µ–µ –ї–µ—В —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (n=116) —Б –Є—Б—Е–Њ–і–љ–Њ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Р–Ы–Ґ –њ—А–Є–≤–µ–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О –µ–µ —Г—А–Њ–≤–љ—П –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 10,4±1,5 –Х–Ф/–ї (p<0,0001), —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–ї–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П —Г 41% –±–Њ–ї—М–љ—Л—Е [21]. –Я—А–Є —Н—В–Њ–Љ, –Ї–∞–Ї –Є —А–∞–љ–µ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б—Е–Њ–і–љ–Њ –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ–Є –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є –Р–Ы–Ґ, –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–∞—Б—Б—Л —В–µ–ї–∞, —З–µ–Љ –≤ –њ–Њ–і–≥—А—Г–њ–њ–µ —Б –Є—Б—Е–Њ–і–љ–Њ –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–∞–љ–љ–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ (–6,1±0,6 –Ї–≥ –Є –4,4±0,5 –Ї–≥ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, p=0,03) [21]. –Ґ–∞–Ї–ґ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –љ–∞ —Д–Њ–љ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ (–≤ —В–µ—З–µ–љ–Є–µ 156–182 –љ–µ–і–µ–ї—М) —Б–Њ—Е—А–∞–љ—П–ї–Њ—Б—М —Б—В–Њ–є–Ї–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Р–°–Ґ [21].
–Ю–±–љ–∞—А—Г–ґ–µ–љ–љ–Њ–µ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —Г—А–Њ–≤–µ–љ—М –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –Љ–∞—А–Ї–µ—А–Њ–≤ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є –љ–∞–Є–±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –њ–Њ–і –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ–Љ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞. –Ф–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є—Е —Г–ї—Г—З—И–µ–љ–Є–µ –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –њ–µ—З–µ–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Э–Р–Ц–Ч–Я –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ, –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–µ—В. –Ю–і–љ–∞–Ї–Њ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Г –ґ–Є–≤–Њ—В–љ—Л—Е –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –љ–µ —В–Њ–ї—М–Ї–Њ —Б–љ–Є–ґ–∞—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–Ы–Ґ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є, –љ–Њ –Є —Г–Љ–µ–љ—М—И–∞—В—М –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Э–Р–Ц–Ч–Я [32]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –≤ –њ–µ—З–µ–љ–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –Љ––†–Э–Ъ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —А–µ–≥—Г–ї—П—В–Њ—А–Њ–≤ –ї–Є–њ–Њ–≥–µ–љ–µ–Ј–∞ –Є –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О –Љ––†–Э–Ъ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –∞–Ї—В–Є–≤–Є—А—Г–µ–Љ—Л—Е –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Њ—А–Њ–Љ –њ–µ—А–Њ–Ї—Б–Є—Б–Њ–Љ, –Ї–Њ—В–Њ—А—Л–µ —П–≤–ї—П—О—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –°–Ц–Ъ [32]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Љ–µ–µ—В—Б—П –Њ–њ–Є—Б–∞–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–ї—Г—З–∞—П, –Ї–Њ–≥–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–∞ —Б –°–Ф 2 —В–Є–њ–∞ –Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л–Љ –Э–Р–Ц–Ч–Я —В–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 44 –љ–µ–і–µ–ї—М –њ—А–Є–≤–µ–ї–∞ –Ї –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ—Г (–љ–∞ 73%) —Г–Љ–µ–љ—М—И–µ–љ–Є—О –ґ–Є—А–Њ–≤–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є —Б–љ–Є–ґ–µ–љ–Є—О –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Р–Ы–Ґ [33].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–Љ–µ—О—Й–Є–µ—Б—П –і–∞–љ–љ—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ —Н–Ї—Б–µ–љ–∞—В–Є–і —Б–њ–Њ—Б–Њ–±–µ–љ –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ (–њ—Г—В–µ–Љ —Б–љ–Є–ґ–µ–љ–Є—П –Љ–∞—Б—Б—Л —В–µ–ї–∞) –Є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ (–Ј–∞ —Б—З–µ—В –≤–ї–Є—П–љ–Є—П –љ–∞ –ґ–Є—А–Њ–≤–Њ–є –Њ–±–Љ–µ–љ) —Г–Љ–µ–љ—М—И–∞—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Э–Р–Ц–Ч–Я —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞. –Ф–∞–ї—М–љ–µ–є—И–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞ –Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ—Л–Љ –Э–Р–Ц–Ч–Я –њ–Њ–Ј–≤–Њ–ї—П—В –ї—Г—З—И–µ –њ–Њ–љ—П—В—М –Ј–љ–∞—З–µ–љ–Є–µ –Ї–∞–ґ–і–Њ–≥–Њ –Є–Ј —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–µ—З–µ–љ–Є.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є, –љ–Њ –Є –љ–∞ –≤—Б–µ –Њ—Б—В–∞–ї—М–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –Є–Љ–µ—О—В –Љ–µ—Б—В–Њ —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞ (–Є–Ј–±—Л—В–Њ—З–љ–∞—П –Љ–∞—Б—Б–∞ —В–µ–ї–∞, –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—П, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –ї–µ—З–µ–љ–Є–µ —Н–Ї—Б–µ–љ–∞—В–Є–і–Њ–Љ –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —Г–Љ–µ–љ—М—И–µ–љ–Є—О –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Э–Р–Ц–Ч–Я —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2 —В–Є–њ–∞. –Ф–∞–ї—М–љ–µ–є—И–Є–µ –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –њ–Њ–Ј–≤–Њ–ї—П—В –Њ—Ж–µ–љ–Є—В—М –Ј–љ–∞—З–µ–љ–Є–µ –≤—Л—П–≤–ї–µ–љ–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤ —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –і–ї—П –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е –°–Ф 2 —В–Є–њ–∞.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Hsueh W.A., Low R.E. Cardiovascular risk continuum: implications of insulin resistance and diabetes. Am. J. Med. 1998; 105: 4S–14S.
2. Nichols G.A., et al. Am. J. Med. 2008; 121: 519–524.
3. Richwine L. UPDATE 2–US advisers urge higher bar for new diabetic drugs. Thomson Reuters.
2 July 2008. Available at: http://www.reuters.com/articlePrint?articleId=USN0241429420080702.
4. –С–∞–µ—В–∞ (—Н–Ї—Б–µ–љ–∞—В–Є–і). –Ґ–Є–њ–Њ–≤–∞—П –Ї–ї–Є–љ–Є–Ї–Њ–—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Б—В–∞—В—М—П. http://www.regmed.ru.
5. –Р–Љ–µ—В–Њ–≤ –Р.–°. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Н–Ї—Б–µ–љ–∞—В–Є–і–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤—Л –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞. –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В. 2008; ????
6. Taylor S.I., Accili D. Mutations in the genes encoding the insulin receptor and insulin receptor substrate–1. In: LeRoith D., Taylor S.I., Olefsky J.M., eds. Diabetes mellitus: a fundamental and clinical text. Philadelphia: Lippincott Williams & Wilkins. 2000: 681–691.
7. Zander M., Madsbad S., Madsen J.L., Holst J.J. Effect of 6–week course of glucagon–like peptide 1 on glycaemic control, insulin sensitivity, and beta–cell function in type 2 diabetes: a parallel–group study. Lancet. 2002; 359: 824–830.
8. Flint A., Raben A., Astrup A., Holst J.J. Glucagon–like peptide–1 promotes satiety and suppresses energy intake in humans. J Clin Invest 1998; 101: 515–20.
9. Edwards C.M., Stanley S.A., Davis R., et al. Exendin–4 reduces fasting and postprandial glucose and decreases energy intake in healthy volunteers. Am. J. Physiol. Endocrinol. Metab. 2001; 281 (1): E155–161.
10. Poon T., Nelson P., Shen L., et al. Exenatide improves glycemic control and reduces body weight in subjects with type 2 diabetes: a dose–ranging study. Diabetes Technol. Ther. 2005; (3): 467–477.
11. DeFronzo R.A., Ratner R.E., Han J., et al. Effects of exenatide (exendin–4) on glycemic control and weight over 30 weeks in metformin–treated patients with type 2 diabetes. Diabetes Care. 2005; 28: 1092–1100.
12. Buse J.B., Henry R.R., Han J., et al. Effects of exenatide (exendin–4) on glycemic control over 30 weeks in sulfonylurea–treated patients with type 2 diabetes. Diabetes Care. 2004; 27: 2628–2635.
13. Kendall D.M., Riddle M.C., Rosenstock J., et al. Effects of exenatide (exendin–4) on glycemic control over 30 weeks in patients with type 2 diabetes treated with metformin and a sulfonylurea. Diabetes Care. 2005; 28: 1083–1091.
14. Nelson P., Poon T., Guan X., et al. The incretin mimetic exenatide as a monotherapy in patients with type 2 diabetes. Diabetes Technol. Ther. 2007; 9 (4): 317–326.
15. Zinman B., Hoogwerf B.J., Garcia S.D., et al. The effect of adding exenatide to a thiazolidinedione in suboptimally controlled type 2 diabetes: a randomized trial. Ann. Intern. Med. 2007; 146 (7): 477–485.
16. Heine R.J., Van Gaal L.F., Johns D., et al. Exenatide versus insulin glargine in patients with suboptimally controlled type 2 diabetes: a randomized trial. Ann. Intern. Med. 2005; 143 (8): 559–569.
17. Nauck M.A., Duran S., Kim D., et al. A comparison of twice–daily exenatide and biphasic insulin aspart in patients with type 2 diabetes who were suboptimally controlled with sulfonylurea and metformin: a non–inferiority study. Diabetologia. 2007; 50 (2): 259–267.
18. Barnett A.H., Burger J., Johns D., et al. Tolerability and efficacy of exenatide and titrated insulin glargine in adult patients with type 2 diabetes previously uncontrolled with metformin or a sulfonylurea: a multinational, randomized, open–label, two–period, crossover noninferiority trial. Clin. Ther. 2007; 29 (11): 2333–2348.
19. Buse J.B., Klonoff D.C., Nielsen L.L., et al. Metabolic effects of two years of exenatide treatment on diabetes, obesity, and hepatic biomarkers in patients with type 2 diabetes: An interim analysis of data from the open–label, uncontrolled extension of three double–blind, placebo–controlled trials. Clin. Ther. 2007; 29 (1): 139–153.
20. Blonde L., Klein E.J., Han J., et al. Interim analysis of the effects of exenatide treatment on A1C, weight and cardiovascular risk factors over 82 weeks in 314 overweight patients with type 2 diabetes. Diabetes Obes. Metab. 2006; 8 (4): 436–447.
21. Klonoff D.C., Buse J.B., Nielsen L.L., et al. Exenatide effects on diabetes, obesity, cardiovascular risk factors and hepatic biomarkers in patients with type 2 diabetes treated for at least 3 years. Curr. Med. Res. Opin. 2008; 24 (1): 275–286.
22. Viswanathan P., Chaudhuri A., Bhatia R., et al. Exenatide therapy in obese patients with type 2 diabetes mellitus treated with insulin. Endocr. Pract. 2007; 13 (5): 444–450.
23. Amori R.E., Lau J., Pittas A.G. Efficacy and safety of incretin therapy in type 2 diabetes: systematic review and meta–analysis. JAMA. 2007; 298 (2): 194–206.
24. Williamson D.F., Thompson T.J., Thun M., et al. Intentional weight loss and mortality among overweight individuals with diabetes. Diabetes Care. 2000; 23: 1499–1504.
25. –Ф–Њ–±–Њ—А–і–ґ–≥–Є–љ–Є–і–Ј–µ –Ы.–Ь., –У—А–∞—Ж–Є–∞–љ—Б–Ї–Є–є –Э.–Р. –†–Њ–ї—М —Б—В–∞—В–Є–љ–Њ–≤ –≤ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є–Є. –°–∞—Е. –і–Є–∞–±–µ—В. 2001; 2: 41–47.
26. Fineman M.S., Bicsak T.A., Shen L.Z., et al. Effect on glycemic control of exenatide (synthetic exendin–4) additive to existing metformin and/or sulfonylurea treatment in patients with type 2 diabetes. Diabetes Care. 2003; 26 (8): 2370–2377.
27. Kothare P.A., Linnebjerg H., Skrivanek Z., et al. Exenatide effects on statin pharmacokinetics and lipid response. Int. J. Clin. Pharmacol. Ther. 2007; 45 (2): 114–120.
28. Rewers M., Swenson C., Shetterly S., et al. Mortality in persons with type 2 diabetes: the Saint Luis Valley diabetes study 1984–98. 59th Annual Scientific Sessions of ADA, San Diego, CA, 1999. Abstract 0069.
29. Adler A.I., Stratton I.M., Neil H.A.W., et al. Association of systolic blood pressure with macrovascular and microvascular complications of type 2 diabetes (UKPDS 36): prospective observational study. BMJ. 2000; 321: 412–419.
30. American Gastroenterological Association. American Gastroenterological Association medical position statement: Nonalcoholic fatty liver disease. Gastroenterology. 2002; 123: 1702–1704.
31. Raz I., Eldor R., Cernea S., Shafrir E. Diabetes: Insulin resistance and derangements in lipid metabolism. Cure through intervention in fat transport and storage. Diabetes Metab. Res. Rev. 2005; 21: 3–14.
32. Ding X., Saxena N.K., Lin S., et al. Exendin–4, a glucagon–like protein–1 (GLP–1) receptor agonist, reverses hepatic steatosis in ob/ob mice. Hepatology. 2006; 43 (1): 173–181.
33. Tushuizen M.E., Bunck M.C., Pouwels P.J., et al. Incretin mimetics as a novel therapeutic option for hepatic steatosis. Liver Int. 2006; 26: 1015–1017.












